ISSN eissn Psichologija
|
|
|
- Nerijus Kalvėnas
- prieš 3 metus
- Peržiūrų:
Transkriptas
1 ISSN eissn Psichologija 124
2 KLINIKINĖS BIOCHEMIJOS ir LABORATORINĖS DIAGNOSTIKOS PAGRINDAI
3 2
4 Zita Aušrelė Kučinskienė KLINIKINĖS BIOCHEMIJOS ir LABORATORINĖS DIAGNOSTIKOS PAGRINDAI 2008
5 UDK 577(075.8) Ku46 Apsvarstė ir rekomendavo spausdinti Vilniaus universiteto Medicinos fakulteto taryba 2007 m. balandžio 17 d.; protokolas Nr. 8 Recenzavo: prof. HP dr. Janina Didžiapetrienė (Vilniaus universiteto Onkologijos institutas) doc. dr. Arvydas Kaminskas (Vilniaus universitetas) prof. HP dr. Vaidotas Urbananvičius (Vilniaus universitetas) Vadovėlis išleistas vykdant Vilniaus universiteto projektą, įgyvendinamą pagal BPD 2.5 priemonę SFMIS Nr. BPD2004-ESF /0006 Molekulinės medicinos magistrantūros ir podiplominių studijų tobulinimo bei dėstytojų kvalifikacijos kėlimo programa. Vadovėlis skiriamas medicinos, biomedicinos studijų programų studentams, laboratorinės medicinos ir kitų rezidentūros programų rezidentams, taip pat medicinos biologijos specialybės magistrantams, doktorantų studijoms, besitobulinantiems gydytojams. ISBN Zita Aušrelė Kučinskienė, 2008 Vilniaus universitetas, 2008 Vilniaus universiteto leidykla,
6 Turinys Įvadas 9 Klinikinės biochemijos laboratorija ir jos struktūra 11 Tiriamosios medžiagos ėmimas, ruošimas ir analizė 13 Tyrimų rezultatų įvairovė, jos biologiniai veiksniai, rezultatų interpretavimas 18 Vandens apykaita, jos reguliavimas, sutrikimai ir laboratorinė diagnostika 21 Natrio, kalio ir chloridų apykaita, jos reguliavimas, sutrikimai ir laboratorinė diagnostika 28 Rūgščių ir šarmų pusiausvyra, jos palaikymas, sutrikimai ir jų laboratorinė diagnostika 44 Nebaltyminės azotinės medžiagos, jų apykaitos rodiklių svarba ligų diagnostikai 66 Inkstų funkcija, jos tyrimas ir sutrikimų laboratorinė diagnostika 80 Žmogaus kraujo plazmos baltymai, jų tyrimas, klinikinis rezultatų interpretavimas 94 Fermentų klinikinė biochemija ir interpretavimas 132 Miokardo infarktas ir jo laboratorinė diagnostika 159 Gliukozės apykaita, cukrinis diabetas ir jo laboratorinė diagnostika 168 Bilirubino apykaita, jos laboratoriniai rodikliai ir kitimas sergant gelta 185 5
7 Kepenys ir jų pažeidimo laboratorinė diagnostika 201 Kalcio ir fosforo apykaita, jos sutrikimai ir laboratorinė diagnostika 210 Kaulinio audinio medžiagų apykaita, ligos ir laboratorinė diagnostika 221 Magnio, geležies ir vario apykaita, jos sutrikimų laboratorinė diagnostika 235 Lipoproteinai, jų sudėtis, apykaita ir sutrikimų laboratorinė diagnostika 246 Laisvaradikalė oksidacija, antioksidacinė gynyba ir ligos 282 Kraujo plazmos krešėjimo ir fibrinolizės sistema, jos sutrikimų laboratorinė diagnostika 290 Širdies ir kraujagyslių ligų laboratorinė diagnostika 307 Hormonų klinikinė biochemija ir jų nustatymo reikšmė 318 Molekuliniai navikų žymenys ir jų naudojimas ligų diagnostikai 374 Naujagimių, vaikų ir senyvų žmonių klinikinės biochemijos ypatybės 399 Literatūra 403 Dalykinė rodyklė 404 6
8 Sutrumpinimai ir paaiškinimai SUTRUMPINIMAI IR PAAIŠKINIMAI ADF adenozindifosfatas AIDS įgyto imuniteto deficito sindromas AKTH adrenokortikotropinis hormonas ALT alaninaminotransferazė AMF adenozinmonofosfatas AST aspartataminotransferazė ATF adenozintrifosfatas Bi bilirubinas Ch cholesterolis ChL cheminės liuminescencijos tyrimas CRB C reaktyvusis baltymas Da daltonas DHCC dihidroksicholekalciferolis DIK diseminuota intravazalinė koaguliacija DNR deoksiribonukleorūgštis DTL didelio tankio lipoproteinai EDTA etilendiamintetraacto rūgštis ERCP endoskopinė retrogradinė cholangiopankreatografija FAD flavinadenindinukleotidas GDH glutamatdehidrogenazė GFG glomerulų filtracijos greitis GGT g glutamiltransferazė GMF guanozinmonofosfatas GTF guanozintrifosfatas Hb hemoglobinas HLP hiperlipoproteinemija HMG-KoA-reduktazės inhibitoriai hidroksimetilglutarilkofermento A reduktazės inhibitoriai Hp haptoglobinas IL interleukinas Ig imunoglobulinas irnr informacinė ribonukleorūgštis KK kreatinkinazė LDH laktatdehidrogenazė LMTL labai mažo tankio lipoproteinai MTL mažo tankio lipoproteinai NAD nikotinamidadenindinukleotidas NADF nikotinamidadenindinukleotido fosfatas RF rūgščioji fosfotazė RNR ribonukleorūgštis SAA serumo amiloidas A TG triacilgliceroliai UDF uridindifosfatas UFB ūminės fazės baltymas ŽIV žmogaus imunodeficito virusas padidėjimas reikšmingas padidėjimas sumažėjimas V ar V reiškia vaisto poveikį ar būklę, kuri gali turėti įtakos analitės koncentracijai in vivo Ch ar Ch cheminė interferencija, t. y. įvairių veiksnių poveikis cheminei reakcijai [ ] medžiagos koncentracija nurodoma laužtiniuose skliaustuose 7
9 8
10 ĮVADAS Klinikinė biochemija (klinikinė chemija) tai laboratorinės medicinos dalis, kurioje ligos yra nustatomos bei tyrinėjamos cheminiais ir biocheminiais metodais. Klinikiniai biocheminiai tyrimai sudaro apie trečdalį ir daugiau visų ligoninės laboratorinių tyrimų. Biocheminių tyrimų rezultatai yra svarbūs: diagnozuojant slaptą ligą; numatant negrįžtamus pažeidimus; ankstyvajai ligos diagnozei atsiradus pirmiesiems jos požymiams ar simptomams; diferencijuojant ligas; nustatant ligos etapą ir aktyvumą; ligos pasikartojimą; įvertinant gydymo efektyvumą ir ligos prognozę; siekiant išvengti ligų; genetiškai konsultuojant šeimas. Taip pat biocheminiai tyrimai yra reikšmingi moksliniams ligų etiopatogenezės, klinikiniams naujų vaistų tyrimams. Diagnozuojant ligą pagal tyrimų normos reikšmes, būtina žinoti, kad rekomenduojamos (referentinės) sveikų asmenų tyrimų rezultatų normos ribų reikšmės yra tik nuoroda, o ne griežta riba, skirianti normalią būseną nuo patologinės. Neretai sveikų asmenų tyrimų rodiklių reikšmės susikloja su sergančiųjų. Laboratorinių tyrimų rezultatų įvairavimas priklauso ne tik nuo laboratorinės įrangos, naudojamo metodo, bet ir nuo preanalizinių veiksnių, pavyzdžiui, ligonio padėties ir būklės (gulima ar sėdima, pavalgęs ar badavęs), paros meto, amžiaus, lyties, klimato, maisto, vartojamų vaistų poveikio ir kt. Todėl klinicistui būtina vadovautis tyrimo rezultatų normos reikšmėmis, patvirtintomis konkrečioje laboratorijoje. Klaidingai interpretavus laboratorinių tyrimų rezultatus vadovaujantis kitoje laboratorijoje nustatytomis normos reikšmėmis, taip pat per daug pasikliaujant ribine reikšme, bus klaidingai diagnozuojama, paskiriamas netinkamas gydymas, vadinasi, bus pakenkta ligoniui, sulaukta ir ekonominių nuostolių. Būtina rekomenduojamų reikšmių naudojimo sąlyga užtikrinti standartizuotą tiriamosios medžiagos (kraujo, šlapimo, kt.) ėmimą. 9
11 10
12 KLINIKINĖS BIOCHEMIJOS LABORATORIJA IR JOS STRUKTŪRA Klinikinė biochemija kaip atskira medicinos specialybė atsirado XIX amžiuje, pirmiausia Vokietijoje, Prancūzijoje, Jungtinėje Karalystėje. Pirmą kartą klinikinės chemijos laboratorijos terminą pasiūlė Johanas Jozefas Šereris (Scherer) ir tokia laboratorija buvo įsteigta Viurcburge (Vokietija). Biocheminiai tyrimai atliekami beveik visose ligoninėse, nors ir skirtingu mastu. Daugumoje klinikinės biochemijos laboratorijų atliekami būtinieji tyrimai, t. y. įprastiniai tyrimai, dažniausiai reikalingi daugumai ligonių. Gydytojai neretai pageidauja specialiai sugrupuotų tyrimų, kurie gali būti žymimi sutartiniais ženklais. Klinikinės biochemijos laboratorijos struktūroje gali būti įvairių specialius tyrimus atliekančių padalinių. Dideli laboratoriniai skyriai gali vykdyti patvirtinančių (referentinių) centrų, kuriuose atliekami reti specialūs tyrimai, funkcijas. Šalyje gali būti viena ar dvi laboratorijos, kuriose daromi labai reti tyrimai. Visose klinikinės biochemijos laboratorijose turi būti galimybė skubos tvarka atlikti užsakomuosius tyrimus. Skubus tyrimas yra toks, kurį atlikus gydytojas dažniausiai nedelsdamas imasi veiksmų ar keičia ligonio tyrimo ir gydymo taktiką. Tokių tyrimų paprastai yra nedaug, juos galima atlikti per trumpą laiką, o atsakymus persiųsti kompiuteriniais tinklais tiesiai užsakiusiam tyrimus gydytojui. Didelėse ligoninėse kai kurie biocheminiai tyrimai yra atliekami arti jų poreikio vietos: operacinių, kuriose daromos sudėtingos transplantacijos operacijos, intensyviosios slaugos palatų ar, pavyzdžiui, gliukozės tyrimai šeimos klinikoje. Laboratorijos kompiuterizavimas leidžia tyrimo rezultatą perduoti tiesiai jį užsakiusiam gydytojui. Brūkšninis kodavimas ir automatizavimas padeda atlikti tyrimus greičiau ir kokybiškiau. Tyrimų įvairovė priklauso nuo laboratorijos paskirties (ligoninės laboratorija ar bendrosios praktikos gydytojo kabinete atliekami tyrimai): nuo paprasčiausių, pavyzdžiui, gliukozės ar hemoglobino koncentracijos nustatymo, iki sudėtingiausių, DNR analize pagrsįtų tyrimų, lipoproteinų fenotipavimo ir kt. Dažniausiai tiriama automatiniais analizatoriais. Dauguma tyrimų gali būti atliekami naudojant paruoštus komercinius reagentų rinkinius. Visa tai lemia tyrimo kainą. Laboratorijos atlieka ir dinaminius pacientų tyrimus, kuriems naudojamas biocheminis stimuliavimas, pavyzdžiui, gliukozės tolerancijos mėginys cukrinio diabeto diagnostikai. 11
13 Šioje knygoje aprašomi dažniausiai atliekami tyrimai, jų patobiochemija, interpretavimas, o ne atlikimo technika. Svarbi daugelio klinikinių skyrių, ypač klinikinių ir universitetų ligoninių, darbo sritis yra moksliniai tyrimai, naujų diagnostikos ir gydymo metodų ieškojimai. Tokie sudėtingi tyrimai priklauso nuo šių ligoninių laboratorijos ir jos techninių galimybių, taip pat personalo profesinės kompetencijos. Laboratorijos personalą sudaro gydytojai, medicinos biologai ir klinikos laborantai (technologai), kuriems būtinos pagrindinės klinikinių tyrimų žinios, šių tyrimų atlikimo ir interpretavimo įgūdžiai. Api b e n d r i n i m a s Laboratorinio tyrimo rezultatas yra dalis visos individo ištyrimo schemos. Vieniems asmenims laboratorinio tyrimo rezultatas gali visai neturėti reikšmės ligos diagnozei ar gydymui, kitiems lemti ligos diagnozę, skiriamą gydymą, priežiūrą. Laboratoriniai tyrimai naudojami ligos diagnozei, gydymui, ligonių atrankai, ligos prognozei ir profilaktikai. Visose ligoninėse yra sudaromi atliekamų tyrimų sąrašai: atliekamų skubos tvarka, kasdien atliekamų, o kai kuriose gydymo įstaigose ir specialiųjų tyrimų. Laboratorijos personalas teikia informaciją ir konsultuoja gydytoją dėl tyrimo būdo parinkimo, interpretuoja tyrimo rezultatą. 12
14 TIRIAMOSIOS MEDŽIAGOS ĖMIMAS, RUOŠIMAS IR ANALIZĖ Kiekvienas paskirtas tyrimas turi duoti atsakymą į gydytojo keliamus klausimus apie ligonio sveikatą. Norint atlikti tyrimą, būtina tinkamai paimti medžiagą užsakytam tyrimui ir pateikti kitą būtiną informaciją apie ligonį, įtariamą ligą. Dauguma biocheminių tyrimų atliekama tiriant kraują, plazmą ar serumą ir šlapimą. Asmens parengimas tyrimui 1. Pacientas turi būti nevalgęs 8 12 valandų. 2. Pageidaujama, kad būtų nevartojęs vaistų, veikiančių tiriamas analites (pvz., geležies preparatų 2 savaites prieš tiriant geležies apykaitos rodiklius; gliukozės apykaitą veikiančių vaistų 3 dienas prieš atliekant gliukozės tolerancijos mėginį ir kt.). 3. Kol nepaimtas ėminys, pacientui negalima daryti kitų diagnostinių bei fizioterapinių procedūrų (rentgenologinio, veloergometrinio tyrimo, funkcinių kvėpavimo mėginių ir kt.). 4. Prieš tyrimus negalima rūkyti, vartoti alkoholio, kaitintis saulėje, reikia vengti streso. Imant kraują iš venos, timpa žasto srityje suveržiama tol, kol įduriama adata. Kraują galima imti ne ilgiau kaip 2 min. Planinis kraujo ėminys daromas 7 9 val. ryto, ligoniui gulint ar sėdint. Kartotinai imant kraujo, tiriamojo kūno padėtis turi būti ta pati. Jei kraujas iš venos imamas į tuščią mėgintuvėlį (be priedų) ir leidžiama kraujui sukrešėti (laikoma ~30 min. kambario temperatūroje), po to centrifuguojama gaunamas kraujo serumas. Jei tyrimui reikalinga plazma, tai kraujas imamas į mėgintuvėlį su stabdančia krešėjimą medžiaga (antikoaguliantu), pvz., heparinu, ir paskui centrifuguojama. Imant kraują labai svarbu tiksliai pripildyti mėgintuvėlį, kad būtų reikiamas antikoagulianto ir kraujo santykis. Paėmus kraujo į vakuuminę sistemą, ji tuoj pat turi būti identifikuojama. Jei kraujo imama į mėgintuvėlį su priedais, mėgintuvėlį reikia 5 6 kartus pavartyti, kad priedai gerai susimaišytų su krauju. Ėminys tai tiriamosios visumos dalies, paimtos tirti arba bandyti, apibendrinamasis pavadinimas; mėginys tai ėminys ar jo dalis, paruošta iš karto tinkamai tirti. 13
15 Keletas pastabų, kurios žinotinos imant kraują tyrimams 1. Ėminių seka: biocheminiams tyrimams, kraujo krešėjimo tyrimams, hematologiniams tyrimams ir kt. Krešėjimui tirti kraujo rekomenduojama imti į du vakuuminius mėgintuvėlius: pirmas be antikoaguliantų, antras su nartrio citratu. Mikrobiologiniam pasėliui kraujo imama kitu dūriu į sterilų buteliuką su terpe. 2. Kraujo negalima imti: aukščiau infuzijos vietos, iš rankos, į kurią perpilta kraujo, iš hematomos, iš patinusios vietos. 3. Po riebalų emulsijos infuzijos kraujo tyrimams galima imti tik praėjus 8 valandoms. 4. Suleidus elektrolitų, angliavandenių, aminorūgščių ir baltymų tirpalų, kraujo tyrimams galima imti tik po 1 valandos. Vakuuminiai mėgintuvėliai pagal paskirtį ir juose eantį priedą yra identifikuojami ir ženklinami pagal kamštelių spalvas (1 lentelė). 1 lentelė. Vakuuminių mėgintuvėlių spalviniai kodai Mėgintuvėlis Tuščias, be priedų naudojamas serumui gauti Su geliu Pritaikymas Klinikinė biochemija, alergologija Klinikinė biochemija, alergologija Kamštelio spalva Europos standartas JAV standartas Balta Raudona Ruda Ruda Su ličio heparinatu Plazmos klinikinė biochemija Oranžinė Žalia Su K 3 -EDTA Su natrio fluoridu (glikolizės inhibitorius) Hematologiniai ir kai kurie klinikinės biochemijos tyrimai (pvz., glikozilinto hemoglobino) Raudona Violetinė Gliukozės tyrimai Geltona Pilka Su trinatrio citratu (1:10) Krešėjimo tyrimai Žalia Mėlyna Su trinatrio citratu (1:5) Eritrocitų nusėdimo greitis Violetinė Juoda Vidinė sienelė padengta krešėjimą skatinančiomis silicio dalelėmis Skubiems kraujo serumo tyrimams. Kraujas jame sukreša per 30 min., todėl pristatytas į laboratoriją tuoj pat centrifuguojamas Geltona 14
16 Tiriamosios medžiagos ėmimas, ruošimas ir analizė Įvairių kraujo plazmos ir serumo sudedamųjų dalių kiekio skirtumus lemia fiziologinės ir techninės priežastys: krešant kraujui šiek tiek sueikvojama gliukozės, fibrinogenas virsta fibrinu, naudojami trombocitai, dėl to jų skaičius mažėja; krešėjimo metu iš ląstelių išsiskiria medžiagų, pavyzdžiui, kalio, laktatdehidrogenazės, fosfatų, amoniako, laktato; esantis plazmoje antikoaguliantas gali iškreipti kai kurias reakcijas. Kraujo plazmos tyrimo pranašumai prieš serumo tyrimą: sutaupoma laiko nereikia laukti, kol susidarys krešulys, o centrifugavimo laiką galima sutrumpinti didinant apsukų skaičių; didesnė išeiga plazmos gaunama apie 15 20% daugiau negu serumo; centrifuguotas serumas dar gali krešėti, o naudojant plazmą to išvengiama; plazmos tyrimo rezultatai geriau atspindi būklę in vivo negu serumo; maža hemolizės ir trombocitolizės rizika. Nepatogumai, su kuriais susiduriama tiriant kraujo plazmą: pakinta baltymų elektroforezė, nes fibrinogenas γ globulinų zonoje gali dengti ar būti panašus į M gradientą; antikoaguliantai, kaip patvarius kompleksus sudarančios ir fermentus slopinančios medžiagos, gali sutrikdyti kai kurias reakcijas. Laboratorijose tiriami ir kiti organizmo skysčiai: šlapimas ir prakaitas, smegenų, pilvo ir krūtinės ertmės skysčiai. Šlapimo surinkimo induose gali būti bakterijų augimą slopinančių medžiagų ar rūgšties, kuri stabilizuoja kai kuriuos metabolitus. Tokie indai turi būti pakankamos talpos, kad į juos būtų galima surinkti paros šlapimą. Pavienės šlapimo porcijos tyrimams renkamos į mažus universalius indus. Pacientams primintina, kad prieš renkant šlapimą būtina švariai apsiplauti išorinius lyties organus. Paros šlapimo ėminį sudaro visos porcijos, surinktos per 24 valandas. Šį ėminį galima pradėti rinkti bet kuriuo paros metu, pacientui pasišlapinus ir pažymėjus laiką. Tačiau dažniausiai rekomenduojama rinkti taip: ryte, pavyzdžiui, 8 val., pacientas turi ištuštinti šlapimo pūslę; tas šlapimas išpilamas ir jo kiekis neskaičiuojamas; po to šlapimas renkamas visą dieną ir naktį į vieną indą; kitos dienos ryte 8 val. šlapimo pūslė vėl ištuštinama, ir gautas kiekis supilamas į tą patį indą tai ir yra 24 valandų šlapimas. Jis stabilizuojamas kiekvienam tyrimui reikiamu būdu. Įtariant pavojingą infekciją, mėgintuvėlį su tokia tiriamąja medžiaga pažymėti specialiu lipduku su užrašu Pavojinga. Laboratorijos personalui daugiausiai rūpesčių kelia B hepatito, žmogaus imunodeficito viruso (ŽIV) infekcijos. Tačiau būtina žinoti, kad su bet kuria tiriamąja medžiaga medicinos personalas turi elgtis kaip su galima pavojinga. 15
17 Klaidos, susijusios su medžiagos ėmimu. Galimos šio pobūdžio klaidos gali turėti įtakos tyrimo atlikimui, kartu jo rezultatui. Kraujo ėmimo technika. Jei kraujas sunkiai bėga į mėgintuvėlį ir ranka yra masažuojama, gali įvykti hemolizė; dėl to iš ląstelių atsipalaiduoja kalio ir kitų sudėtinių dalių, jų koncentracija gali klaidinti būti didesnė už tikrą. Pailgėjusi kraujo stazė užspaudus timpa paviršinę veną imant kraujo. Plazmos vanduo difunduoja į intersticinę erdvę, dėl to paimtame kraujo serume ar plazmoje sumažėjus vandens kiekiui klaidingai padidės baltymų ar su baltymais susijungusių plazmos komponentų koncentracija, pavyzdžiui, kalcio, tiroksino. Nepakankamas tiriamosios medžiagos kiekis. Kiekvienam tyrimui reikalingas tam tikras medžiagos kiekis. Jei jos yra per mažai, laboratorija negalės atlikti visų užsakytų tyrimų. Klaidos, susijusios su medžiagos rinkimo laiku. Dažniausiai šio pobūdžio klaidų šaltinis yra netinkamai surinktas paros (24 val.) šlapimas. Nepritaikytas tiriamosios medžiagos rinkimui indas. Kai kuriems tyrimams kraujo turi būti imama į mėgintuvėlius su priedais, pvz., su antikoaguliantu. Paėmus kraujo ne į tą mėgintuvėlį, griežtai draudžiama jo turinį perpilti į kitą mėgintuvėlį. Pavyzdžiui, jei kraujo buvo paimta į mėgintuvėlį su etilendiamintetraacto rūgštimi (EDTA), tai jame bus sumažėjusi kalcio koncentracija. Netinkama medžiagos paėmimo vieta. Imamas kraujas turi tekėti į mėgintuvėlį srove žemyn. Negalima imti kraujo gliukozės tyrimui iš tos pačios rankos, į kurią buvo sušvirkšta (ar sulašinta) gliukozės tirpalo. Netinkamas tiriamosios medžiagos laikymas. Jei mėgintuvėlis su paimtu krauju iki tyrimo laikomas per naktį, tai bus nustatytos per didelės kalio, fosfatų ir laktatdehidrogenazės (jos daugiausiai esti eritrocituose) koncentracijos, nes iš ląstelių šios medžiagos patenka į plazmą (serumą). Kaip dažnai atlikti tyrimus. Dauguma biocheminių tyrimų yra kartojami tam tikrais laiko tarpais. Tyrimų dažnumas priklauso nuo to, kaip greit galimi akivaizdūs tam tikrų tiriamosios medžiagos sudedamųjų dalių pokyčiai. Pernelyg dažnai kartoti tyrimus nerekomenduojama, jeigu jie neturi įtakos ligos diagnozavimui ar gydymui. Tyrimų atlikimas. Užsakymo lapelis ir tiriamoji medžiaga laboratorijoje yra sutikrinami pagal identifikacijos numerį ar brūkšninį kodą. Be tiriamosios medžiagos analizės, yra atliekami kokybei užtikrinti būtini tyrimai. Gauti rezultatai įvertinami kokybės užtikrinimo schema ir išrašomas atsakymas. Dauguma biocheminių analičių tiriamos kraujo serume, kuris gaunamas kaip viršnuosėdinis skystis centrifuguojant sukrešėjusį mėgintuvėlyje kraują. Kitoms analitėms tirti reikalinga kraujo plazma tai viršnuosėdinis skystis, kuris gaunamas įdėjus stabdančių kraujo krešėjimą medžiagų (antikoaguliantų). 16
18 Tiriamosios medžiagos ėmimas, ruošimas ir analizė Kraujo ėmimo ir iki pristatant į laboratoriją padarytos klaidos gali turėti įtakos tyrimo rezultatui. Tyrimo rezultatų interpretavimas. Tyrimo rezultatas nėra tik popieriuje parašytas skaičius. Pirmiausia, tam skaičiui gauti reikia tam tikrų pastangų, piniginių sąnaudų ir kokybę užtikrinančios sistemos. Tik tada minėtasis skaičius bei jo interpretavimas galės lemti teisingos diagnozės formuluotę ar skiriamo gydymo pagrįstumą. Biocheminių tyrimų rezultatų išraiška. Dauguma biocheminių tyrimų rezultatų yra kiekybiniai, kai tyrimo metu yra išmatuojama analitės koncentracija tam tikroje ėminio (kraujo plazmos, serumo, šlapimo ar kitos tiriamosios medžiagos) dalyje. Tyrimo rezultatas paprastai išreiškiamas moliniais vienetais. Bet kurios medžiagos molis visada turi molekulių. Nurodydami, koks analitės kiekis yra molyje, nurodome ir medžiagos molekulių skaičių jame. Moliniai vienetai gali būti paversti moline mase: vienas molis yra medžiagos molekulinė masė gramais. Tyrimo rezultatai pateikiami kaip koncentracija, t. y. molių skaičius litre medžiagos (mol/l). Analitės koncentracija organizme yra santykis medžiagos kiekio, ištirpinto žinomame tūrio kiekyje. Koncentracijos pokyčiai galimi dėl kelių priežasčių: analitės kiekis gali padidėti ar sumažėti; skysčio kiekis, kuriame analitė yra ištirpinta, gali kisti panašiai. Fermentų tyrimo rezultatas paprastai išreiškiamas ne moliais, o aktyvumo vienetais. Kai kurių hormonų matavimai išreiškiami vienetais, palyginti su žinomo biologinio aktyvumo standartine referentine medžiaga. Didelių molekulių, pvz., baltymų, tyrimų rezultatai pateikiami gramais ar miligramais litre ar decilitre. Kraujo dujų tyrimo rezultatai (pco 2, po 2 ) išreiškiami mmhg ar kilopaskaliais (kpa) vienetais, kuriais matuojamas slėgis. Laboratorinių tyrimų metodai. Laboratorijose naudojama įranga įvairuoja nuo paprasčiausios, naudojamos prie ligonio lovos, iki sudėtingų analizatorių, kuriuose suderinti įvairūs analizės metodai ir kurie dažniausiai naudojami centralizuotose laboratorijose. Įvairioms medžiagoms išskirti, jų sudėčiai, struktūrai nustatyti bei koncentracijai organizmo skysčiuose matuoti taikoma fotometrija, spektrofotometrija, liepsnos fotometrija, fluorescencija, liuminescencija, osmometrija, taip pat elektroferozė, chromatografija, masių spektrometrija bei įvairūs šių būdų deriniai, pavyzdžiui, imunocheminiai analizės metodai. 17
19 TYRIMŲ REZULTATŲ ĮVAIROVĖ, jos BIOLOGINIAI VEIKSNIAI, REZULTATŲ INTERPRETAVIMAS Biocheminių tyrimų rezultatai įvairuoja dėl dviejų priežasčių analizinės ir biologinės įvairovės. Laboratorinė analizinė įvairovė Tyrimo rezultatą apibūdina: tyrimo duomenų tikslumas ir glaudumas; tyrimo jautrumo slenkstis ir specifiškumas; matavimo neapibrėžtis; tyrimo metodo tiesiškumas; gautųjų verčių svyravimo ribos. Tikslumas (angl. accuracy) gautosios vertės artumas tikrajai vertei. Glaudumas (angl. precision) nepriklausomų tyrimo rezultatų artumas. Jautrio slenkstis (angl. sensitivity) mažiausia išmatuojama analitės koncentracija. Specifiškumas nusako tyrimo galimybę atskirti analitę nuo pašalinių medžiagų. Neapibrėžtis (angl. uncertainty) parametras, susijęs su matavimo rezultatu ir apibūdinantis matuojamojo dydžio verčių dispersiją. Metodo tiesiškumas (angl. linearity) apibrėžia tyrimo metodo galimybę gauti duomenis, proporcingus analitės koncentracijai. Re k o m e n d u o j a m o s (re f e re n t i n ė s) re i k š m ė s Analizinė duomenų įvairovė paprastai yra mažesnė negu biologinė. Tyrimų rezultatai yra lyginami su rekomenduojamomis reikšmėmis, esant normaliai (sveikai) būklei. Šios reikšmės pasirenkamos sutarimu ir apima 95 proc. reikšmių, kurios nustatomos tiriant sveikus savanorius. Kitų tirtosios populiacijos 5 proc. tyrimo rezultatai nepateks į rekomenduojamas ribas. Realiame gyvenime (praktikoje) nėra griežtų ribų, kurios skirtų sveikų ir sergančių individų populiacijas. Tačiau kuo reikšmė yra toliau nuo rekomenduojamųjų, tuo didesnė tikimybė, kad tas rezultatas rodo ligą. Sveikųjų ir sergančiųjų tyrimo reikšmės neretai susikloja. Kai asmeniui tyrimu nustatyta reikšmė patenka už rekomenduojamų ribų, tačiau ligos požymių nėra, sakoma, kad rezultatas yra klaidingai teigiamas. Kai asmuo serga, o tyrimo rezultatas normalus, sakoma, kad rezultatas yra klaidingai neigiamas. Šioje knygoje 18
20 Tyrimų rezultatų įvairovė... vadovaujamasi Vilniaus universiteto ligoninės Santariškių klinikų Laboratorinės diagnostikos centre patvirtintomis rekomenduojamomis (normos) reikšmėmis. Tyrimų rezultatus veikiantys biologiniai veiksniai Tyrimų rezultatai priklauso nuo įvairių veiksnių, kurie įvertinami interpretuojant rezultatą. Fiziologiniai veiksniai: lytis; kai kurios analitės, pavyzdžiui, kreatinino koncentracija kraujo serume, vyrų ir moterų skiriasi; amžius; naujagimių, vaikų, suaugusiųjų ir pagyvenusių žmonių rekomenduojamos reikšmės neretai skiriasi; mitybos pobūdis; tiriamoji medžiaga, paimta pavalgius ar badaujant, dažniausiai yra netinkama tirti; tiriamosios medžiagos paėmimo laikas tai cirkadinio (paros) ritmo poveikis; daugumos analičių tyrimo rezultatai įvairiu paros metu svyruoja; stresas; jis gali iškreipti tyrimo rezultatą; paciento padėtis; skysčių persiskirstymas gulint ar stovint gali turėti įtakos tyrimo rezultatui (pvz., keičiant gulimą padėtį į stovimą plazmos tūris gali sumažėti iki 12%); fizinis aktyvumas; įtampos ar intensyvių fizinių pratimų metu iš ląstelių išsiskiria kai kurie fermentai; anamnezė; infekcija ir (ar) audinių pažaida gali turėti įtakos tyrimo rezultatui, nepriklausomai nuo ligos eigos; nėštumas; jo metu keičiasi kai kurių analičių rekomenduojamos ribos; mėnesinių ciklas; jo metu kai kurių hormonų kiekis gali svyruoti ir tai atsispindėti tyrimuose; vaistai; jie specifiškai veikia kai kurių analičių kraujo plazmoje koncentracijas. Ki t i veiksniai Įrašytą atsakymo lape (formoje) tyrimų rezultatą taip pat reikia įvertinti. Buvo aptarti analiziniai ir biologiniai veiksniai, galintys turėti įtakos rezultatui. Kiti veiksniai tiesiogiai priklauso nuo paciento. Gydytojas įvertina rezultatą matydamas pacientą. Laboratorijos specialistas vertina tik matavimo rezultatą. Gydytojas, gavęs tyrimo duomenis, juos gali aptarti su laboratorijos specialistais šiais aspektais: ar tyrimo rezultatas atitinka duomenis, gautus surinkus anamnezę ar objektyviai tiriant ligonį; jei rezultatas ne toks, kokio tikėtasi, tai kaip paaiškinti tokį neatitikimą; kaip tyrimo rezultatas gali pakeisti gydytojo suformuluotą diagnozę ar numatomą ligonio tyrimą ir gydymą; kokie tolesni veiksmai. 19
21 Kokybės užtikrinimas Laboratorijos užduotis yra nuolat vertinti, ar naudojamas tyrimo metodas yra reikiamo tikslumo, ar patikimas. Laboratorijos darbuotojai tyrimo kokybei vertinti naudoja kontrolinius mėginius, kad įsitikintų, ar metodas yra pakankamo tikslumo. Vidaus kokybės kontrolei naudojamos medžiagos analizuojamos kasdien ar kiekvieną kartą, kai atliekamas tyrimas. Analičių reikšmės yra žinomos. Išorės kokybei vertinti laboratorijoms yra išdalijama vienoda tiriamoji medžiaga, kad būtų galima palyginti gautus rezultatus. Šio vadovėlio įvadą baigsime Kelvino žodžiais, parašytais dar 1889 metais: Jeigu galima išmatuoti tai, apie ką galvojama, ir išreikšti skaičiais, vadinasi, šis tas yra žinoma. Api b e n d r i n i m a s Klinikinė biochemija kartu su kitomis laboratorinės diagnostikos sritimis (laboratorine hematologija, klinikine mikrobiologija, virusologija, klinikine imunologija ir citologija) sudaro laboratorinės medicinos visumą. Nenormalus tyrimo rezultatas ne visada rodo ligą, o normalus tyrimo rezultatas kad ligos nėra. Laboratorinio tyrimo poreikis yra tarsi klausimas apie paciento sveikatą, o tyrimo rezultatas atsakymas į tą klausimą. Laboratorinio tyrimo užsakymo lapas turi būti tvarkingai užpildytas, o indas su tiriamąja medžiaga pažymėtas, kad tyrimo rezultatas greitai pasiektų gydytoją. Tyrimo rezultatams įtakos turi analiziniai ir biologiniai veiksniai. Rekomenduojamos (normos) reikšmės, kurios nurodomos kartu su tyrimo rezultatu, gali tik padėti statistiškai įvertinti rezultatą, ar jis yra normalus, ar nenormalus. Rekomenduojamos reikšmės gali skirtis priklausomai nuo individo lyties, amžiaus. Tyrimo rezultato kitimas yra tiek pat svarbus, kiek ir absoliučioji jo reikšmė. Jei laboratorinio tyrimo rezultatas neatitinka kitų tiriamojo asmens duomenų, tą rezultatą reikia aptarti su laboratorijos specialistais. 20
22 VANDENS APYKAITA, JOS REGULIAVIMAS, SUTRIKIMAI IR LABORATORINĖ DIAGNOSTIKA Gyvajame pasaulyje labai svarbios yra organinės medžiagos baltymai, nukleorūgštys, riebalai, angliavandeniai. Be jų, gyvybiškai būtinas ir vanduo, ir neorganinės medžiagos: makroelementai, iš jų ir elektrolitai, mikroelementai. Va n d u o Vanduo susieja organizmo vidinę terpę su išorine aplinka, taip pat jis reikalingas ląstelių, organizmo dalių sąveikai. Be to, vanduo yra organinių ir neorganinių medžiagų tirpiklis. Vanduo sudaro 60 65% žmogaus kūno masės. Taigi 70 kg sveriančio žmogaus organizme yra apie 42 l vandens. Du trečdalius šio kiekio sudaro ląstelėse esantis (ląstelinis) skystis jo yra apie 28 l, o neląstelinis vandens tūris sudaro apie 14 litrų. Neląste linis dar skirstomas į intersticinį (audinių, arba tarpląstelinį, skystį apie 10,5 l), kuriame yra mažai baltymų, ir kraujagyslių skystį kraujo plazmą (3,5 l), kurioje yra didelė baltymų koncentracija. Visą organizmo vandenį galima suskirstyti į dvi frakcijas: laisvasis vanduo, kuris dalyvauja apykaitoje, sujungtasis vanduo, kuris sudaro koloidines sistemas su organinių medžiagų molekulėmis. Pavyzdžiui, žinoma, kad 1 g glikogeno ir baltymų sulaiko apie 1,5 ar 3 ml vandens. Organizme esantis vanduo atsinaujina per 4 savaites. Per parą suvartojame apie 2300 ml vandens: apie 1300 ml jo išgeriame, 1000 ml gauname su maisto produktais. Apie 300 ml susidaro endogeninio vandens galutinio katabolinių procesų produkto. Tiek pat jo ir išsiskiria iš organizmo: 1500 ml šlapimo, 600 ml prakaito pavidalu, 200 ml su išmatomis, 300 ml iškvepiame. Vandens netekimas per odą, su prakaitu ir iškvepiamu oru dar vadinamas nepastebimu vandens netekimu; jo kiekis svyruoja nuo 500 ml iki 850 ml per dieną. Skaičiuojant organizmo vandens apykaitą, reikia atsižvelgti į kūno temperatūrą: jai didėjant, daugiau vandens netenkama per odą ir plaučius su iškvepiamu oru. Sergant skysčių galima netekti viduriuojant, gausiai vemiant, per fistules. Karščiuojantis organizmas gali išprakaituoti apie 1 litrą ir daugiau skysčio. Padažnėjus kvėpavimui ar naudojant respiratorių, su iškvepiamu oru netenkama gerokai daugiau vandens. 21
23 ! Selektyvusis ląstelinio ar neląstelinio skysčio netekimas sukelia įvairių simptomų. Pavyzdžiui, dėl ląstelinio skysčio netekties sutrinka ląstelių funkcija, prasideda letargija, apsiblausia sąmonė ir ištinka koma. Netenkant neląstelinio skysčio, sutrinka kraujotaka, inkstų veikla, ištinka šokas. Tačiau šie požymiai išryškėja ne iš karto, nes vanduo pasiskirsto ląstelių viduje ir už jų ribų. Žinotina, kad organizmo skysčių tūris negali būti išmatuotas klinikinės biochemijos laboratorijoje. Paprastai tai įvertinama remiantis klinikiniais požymiais. Terminas dehidratacija reiškia, kad organizmas yra netekęs skysčių. Hiperhidratacija išsivysto, kai organizme kaupiasi skysčiai. Sutrikusios vandens apytakos klinikiniai požymiai pateikiami 2 lentelėje. 2 lentelė. Sutrikusios vandens apykaitos klinikiniai požymiai Pulsas Kraujospūdis Odos elastingumas Akių obuoliai Gleivinės Šlapimo kiekis Sąmonė Požymis Dehidratacija Hiperhidratacija Dažnas Sumažėjęs Sumažėjęs Minkšti Sausos Sumažėjęs Sutrikusi Normalus Normalus ar padidėjęs Padidėjęs Normalūs Normalios Gali būti normalus Sutrikusi Prisimintina, kad su amžiumi odos elastingumas mažėja, o intensyviai kvėpuojant pro burną, jos gleivinė sausėja. El e k t r o l i t a i Elektrolitai tai organizme tirpalus sudarančios medžiagos, kurios tirpdamos suskyla į teigiamai ar neigiamai įelektrintas daleles jonus. Natris (Na + ) yra svarbiausias neląstelinės terpės katijonas, kalis (K + ) svarbiausias ląstelinis katijonas. Svarbiausi ląsteliniai anijonai yra baltymų ir fosfatų, o tarp ląstelių vyrauja chloridų (Cl - ) ir rūgščiojo karbonato (HCO - 3 ) anijonai (rūgštieji karbonatai tai tie patys bikarbonatai). Elektrolitų nustatymas kraujo serume paprastai apima natrio, kalio, chloridų, rūgščiojo karbonato jonų koncentracijas. Natrio jonų koncentracija yra didžiausia ir lemia bendrą plazmos osmoliališkumą. Nors kalio jonų koncentracija neląsteliniame skystyje yra nedidelė, palyginti su jo koncentracija ląstelių viduje, koncentracijos svyravimas plazmoje yra labai svarbus rodiklis ir gali būti pavojingas gyvybei. Apie natrio, kalio ir chloridų apykaitą organizme skaitykite kitame skyriuje. Elektrolitų pasiskirstymas tarp ląstelinio ir neląstelinio skysčio. Ląstelėse esantis natris sudaro mažiau kaip 1/10 jo kiekio, esančio tarp ląstelių, o ląstelėse kalio yra 30 kartų daugiau negu terpėje tarp jų. Skaičiuojant absoliučiaisiais skaičiais, apie 95% natrio, dalyvaujančio medžiagų apykaitoje, yra tarpląstelinėje terpėje, o 22
24 Vandens apykaita, jos reguliavimas,... tokia pat dalis kalio ląstelėse. Tokiems natrio ir kalio koncentracijos skirtumams palaikyti būtina siurbimo energija (ATF). Elektrolitų pasiskirstymas tarp kraujo plazmos ir intersticinio skysčio. Kraujagyslių endotelis, skirtingai nuo ląstelių membranų, pralaidus tik nedaugeliui jonų, todėl plazmoje, bet ne intersticiniame skystyje yra didelė baltymų koncentracija, o elektrolitų koncentracija kiek didesnė intersticiniame skystyje. Elektrolitų koncentracijos skirtumas yra toks mažas, kad jo galima nepaisyti ir manyti, kad elektrolitų koncentracija plazmoje rodo jo koncentraciją tarpląstelinėje terpėje. Ko n c e n t r a c i j a, o s m o s a s ir os m o s i n i s sl ė g i s Koncentracija tai dviejų kintamųjų ištirpintos medžiagos (pvz., natrio) kiekio ir tirpiklio (vandens) kiekio santykis. Koncentracija gali kisti dėl abiejų kintamųjų pokyčių. Organizmo skysčiai tarp įvairių jo dalių yra skiriami puslaidės membranos, kurią lengvai įveikia vanduo. Vandens judėjimas pro membraną, laidžią tik vandeniui, priklausys nuo ištirpusių medžiagų abipus membranos koncentracijos skirtumo. Kuo didesnės dalelės ar kuo didesnė jų molekulinė masė, tuo mažiau jų yra tūrio vienete ir tuo mažesnis jų sukurtas osmosinis efektas. Taigi osmosas yra vandens judėjimas pro puslaidžią membraną dėl slėgio skirtumo abipus membranos. Vertinant vandens pasiskirstymą organizme, reikia turėti omenyje tris veiksnius: 1) dalelių skaičių tūrio vienete, 2) koncentracijos gradientą, susidarantį tarp abiejų membranos pusių, 3) santykį tarp dalelių dydžio ir membranos laidumo. Molekulių koncentraciją galima išreikšti jų molių (ar milimolių) kiekiu viename litre tirpalo tirpalo moliškumu, arba molių (ar milimolių) kiekiu 1 kg tirpiklio moliališkumu. Todėl ir osmosinį slėgį galima išreikšti osmoliškumo dydžiu molių skaičiumi viename litre tirpalo, arba osmoliališkumo dydžiu ištirpusios medžiagos kiekiu moliais (ar milimoliais) kilogramui tirpiklio (paprastai tai vanduo). Nors medžiagų koncentracija įvairiuose organizmo skysčiuose svyruoja, bendras ištirpusių dalelių skaičius osmoliališkumas nekinta. Osmosinis slėgis abipus ląstelės membranos turi būti vienodas, ir vanduo juda (pasiskirsto) taip, kad išliktų vienodas osmoliališkumas, net jei dėl šio vandens judėjimo ląstelės susitrauktų ar išburktų. Ląstelinio skysčio osmoliališkumas visada yra lygus neląstelinio skysčio osmoliališkumui. Tirpalo osmoliališkumas priklauso tik nuo dalelių skaičiaus tirpale, o jų dydis ar krūvis jam įtakos neturi. Osmoliališkumo išraiška yra tikslesnė, nes tirpalo koncentracija, išreikšta per svorį, nepriklauso nuo temperatūros, o išreikšta per tūrį įvairuoja pagal temperatūrą. Kadangi fiziologinių skysčių osmoliališkumas yra palyginti mažas, tai paprastai patogiau naudotis miliosmoliališkumo vienetu. Žmogaus kraujo 23
25 serumo (ir visų kitų organizmo skysčių, išskyrus šlapimą) osmolališkumas yra apie 285 mmol/kg (3 lentelė). 3 lentelė. Kraujo plazmos komponentų įnašas į jos osmoliališkumą Komponentas Osmoliališkumas (mmol/kg) Natris ir anijonai 270 (92% bendro osmoliališkumo) Kalis ir anijonai 7 Kalcis (jonizuotasis) ir anijona 3 Magnis ir anijonai ~ 1 Šlapalas 5 Gliukozė 5 Baltymai ~ 1 Iš viso ~ 292 Serumo ar plazmos osmoliališkumą mėginyje galima išmatuoti tiesiogiai (pvz., osmometrijos metodu pagal užšalimo taško sumažėjimą) arba apskaičiuoti, jei žinomos svarbiausių ištirpusių medžiagų koncentracijos: Serumo osmoliališkumas (mmol/kg) = 2 serumo [natrio] (mmol/l). Ši formulė taikytina tik tuo atveju, kai šlapalo ir gliukozės koncentracija yra rekomenduojamos normos sveiko žmogaus jos sudaro tik nedidelę plazmos osmoliališkumo dalį. Tačiau, esant hiperuremijai ar hipergligemijai, šlapalo ar gliukozės koncentracijos, padidėjusios apie 15 kartų, tampa svarbiais osmoliališkumo veiksniais. Tada skaičiuojant osmoliališkumą reikia pridėti vienos ar abiejų šių medžiagų koncentracijas (mmol/l). Natrio koncentracijos padidėjimas plazmoje sukelia ląstelių dehidrataciją, o sumažėjimas hiperhidrataciją. Kartais išmatuotasis ir apskaičiuotasis osmoliališkumas akivaizdžiai skiriasi. Taip susidaro osmolialinis plyšys. Vandens apykaitos reguliavimas Žmogaus organizme esantis vanduo ir elektrolitai yra nuolatinio tekėjimo (kaitos) būklės: mes geriame, valgome, išskiriame šlapimą, prakaituojame. Tačiau vykstant visiems šiems procesams organizmo būklė išlieka pastovi. Vis dėlto, jei staigiai netektume kad ir nedidelio vandens kiekio iš kraujagyslėse esančio jo tūrio, tai būtų pavojinga gyvybei. Į skysčių kiekio pokyčius žmogaus organizmas reaguoja jautriai, todėl veikia nemažai svarbių homeostazę reguliuojančių mechanizmų, apsaugančių nuo pavojingų pokyčių arba juos minimizuojančių. Elektrolitų koncentracijos pokyčiai taip pat yra labai nedideli. Netekus skysčių ar neduodant jų gerti, mirštama jau po kelių dienų: dėl bendro organizme esančio skysčio kiekio sumažėjimo išsivysto apykaitos nepakankamumas. 24
26 Vandens apykaita, jos reguliavimas,... Jei neužtikrinamas pastovus kraujo plazmos tūris, sutrinka kraujo apytaka, dėl to greitai apmiršta audiniai, nes negauna pakankamai deguonies ir kitų maisto medžiagų, taip pat nešalinami galutiniai medžiagų apykaitos produktai. Suvartojamo vandens kiekis yra įvairus ir priklauso nuo įpročių. Kai kurie žmonės vandens geria nedaug mažiau negu pusę litro per dieną, o kiti jo gali išgerti iki 5 l. Troškulys yra veiksnys, lemiantis išgeriamų skysčių kiekį. Netenkamo vandens kiekis taip pat yra nepastovus dydis ir dažniausiai nustatomas pagal išskiriamo šlapimo kiekį. Inkstai greitai pašalina vandens perteklių, ir šlapimo kiekis gali pasikeisti per labai trumpą laiką. Tačiau, kai reikia sulaikyti vandenį organizme, žmogus nesugeba pristabdyti šlapimo išsiskyrimo. Sveikame organizme bendras vandens kiekis yra gana pastovus, nepaisant didelio išgerto vandens kiekio svyravimo. Vandens šalinimą per inkstus jautriai reguliuoja antidiurezinis hormonas. Antidiurezinis hormonas. Pogumburio (hypothalamus) srityje esančios specializuotos ląstelės jautriai reaguoja į ląstelinio ir neląstelinio osmoliališkumo skirtumą. Pagal tai jos reguliuoja antidiurezinio hormono sekreciją iš užpakalinės hipofizės dalies. Didėjant osmosiniam slėgiui dirginami osmoreceptoriai (dėl to jaučiamas troškulys) ir padažnėję impulsai į specializuotas ląsteles suaktyvina jose antidiurezinio hormono sekreciją. Šis hormonas skatina vandens reabsorbciją distaliniuose inkstų kanalėliuose. Biocheminis šio proceso mechanizmas susijęs su fermento hialuronidazės suaktyvėjimu dėl antidiurezinio hormono poveikio. Hialuronidazė hidrolizina hialurono rūgštį ir padidina kanalėlių pralaidumą, t. y. jų sienelėse atveria poras. Dėl osmosinio gradiento (tarp hiperosmosinio tarpląstelinio skysčio ir hipoosmosinio šlapimo) vanduo pasyviai grįžta į organizmą. Taip būna ir nustojus gerti skatinama endogeninė antidiurezinio hormono sekrecija, dėl to šlapimo tėkmė kanalėliuose sumažėja iki 0,5 ml/min., ir tokiu būdu vanduo sulaikomas organizme. Jeigu per valandą išgeriama apie 2 l vandens, šlapimo tėkmės greitis gali padidėti iki 15 ml/ min., nes nebeišskiriama antidiurezinio hormono. Be reabsorbcijos inkstų kanalėliuose, antidiurezinis hormonas: stipriai sutraukia kraujagysles (vazokonstriktorius), aktyvina glikogenolizės fermentus kepenyse, didina adrenokortikotropinio hormono sekreciją iš priekinės hipofizės dalies ir tokiu būdu skatina kortizolio gamybą, didina VIII krešėjimo faktoriaus koncentraciją plazmoje. Antidiurezinio hormono sekreciją skatina nemažai veiksnių: stresas, skausmas, kai kurie vaistai (barbitūratai, analgetikai), o šio hormono sekreciją slopina alkoholis. Taigi reguliuojant vandens išskyrimą ir sulaikymą (reabsorbciją), organizme palaikoma normali elektrolitų koncentracija. Tūrio reguliavimas. Vanduo neląstelinėje terpėje yra sulaikomas tik dėl osmosinio jonų efekto (veikimo). Kadangi daugiausia natrio ir su juo susijusių jonų, pavyz- 25
27 džiui, chloridų, yra neląstelinėje terpėje, tai natrio kiekis neląsteliniame skystyje yra jo tūrį lemiantis veiksnys. Aldosteronas ir antidiurezinis hormonas palaiko normalų neląstelinio skysčio tūrį ir koncentraciją. Pavyzdžiui, dėl virškinamojo trakto infekcijos ligonis vemia ir viduriuoja. Jei jis negertų, jo organizmas greitai netektų vandens, su juo ir natrio. Sumažėjus neląstelinio skysčio tūriui, padidėja aldosterono sekrecija, dėl to skatinama natrio kalio siurblio veikla, daugiau natrio ir vandens bus sugrąžinta į kraujotaką (apie aldosteroną detaliau skyriuje Natrio, kalio ir chloridų apykaita, jos reguliavimas, sutrikimai ir laboratorinė diagnostika ). Pradėjus ligoniui gerti, suvartotas natris (druska) bus sulaikomas. Padidėjus natrio kiekiui, padidės neląstelinio skysčio osmoliališkumas, tai padidins antidiurezinio hormono sekreciją, dėl to bus sulaikomas vanduo. Tokia aldosterono ir antidiurezinio hormono sąveika truks tol, kol sunormalės neląstelinio skysčio tūris ir sudėtis. Api b e n d r i n i m a s Nors biocheminis tyrimas yra svarbus vertinant ligonio būklę ir jį gydant, nustačius skysčių ir elektrolitų pusiausvyros sutrikimą, negalima pamiršti pildyti skysčių pusiausvyros lentelę. Skysčių suvartojimo ir išsiskyrimo per dieną žymėjimas gali suteikti vertingos informacijos apie paciento organizmo skysčių būklę. Organizmo skysčių tūris klinikinės biochemijos laboratorijoje nematuojamas. Šis dydis įvertinamas kliniškai renkant anamnezę ir objektyviu tyrimu. Organizme skysčiai yra pasiskirstę dviejose erdvėse: ląstelinėje ir neląstelinėje. Ląstelinė erdvė yra dvigubai didesnė už neląstelinę. Dėl vandens susilaikymo organizme padaugėja ir ląstelinio, ir neląstelinio skysčio. Vanduo iš organizmo pasišalina su šlapimu, išmatomis ir kaip nepastebimas vanduo per odą ir plaučius. Dėl vandens netekimo (dehidratacijos) sumažėja ir ląstelinio, ir neląstelinio skysčių. Serumo osmoliališkumas gali būti išmatuotas tiesiogiai ar apskaičiuotas pagal natrio, šlapalo ir gliukozės koncentracijas serume. Antidiurezinis hormonas reguliuoja vandens netekimą per inkstus ir tokiu būdu lemia organizmo skysčių osmoliališkumo pokyčius. Laboratorinis tyrimas Osmoliališkumo tyrimas Tiriamoji medžiaga. Serumas. Rekomenduojama reikšmė mosm/kg. Diagnostinė vertė. Netekus vandens, hiperosmosinė neketoninė diabetinė koma, diabetinė ketoacidozė, hipernatreminė intoksikacija etanoliu, inkstinis diabetas, hiperkalcemija, smegenų pažeidimas, dažnai maitinant pro vamzdelį. 26
28 Vandens apykaita, jos reguliavimas,... Antinksčių žievės nepakankamumas, hipofizės panhipofunkcija, apsinuodijimas vandeniu, pooperacinės būklės (naudojant pakaitinį gydymą ypač dideliais kiekiais skysčių), sutrikusios antidiurezinio hormono sekrecijos sindromas. Papildoma informacija V: glicerolis, insulinas (didelės dozės), gliukokortikoidai, manitolis, šlapalas. Ch: gliukozė, šlapalas. V: ciklofosfamidas, karbamazepinas, tiazidai. 27
29 NATRIO, KALIO IR CHLORIDŲ APYKAITA, JOS REGULIAVIMAS, SUTRIKIMAI IR LABORATORINĖ DIAGNOSTIKA Na t r i s Natrio pasiskirstymas organizme. Natris yra svarbiausias neląstelinis katijonas. Žmogaus, sveriančio 70 kg, organizme yra apie 3700 mmol natrio, ir apie 75% šio kiekio nuolat keičiasi. Ketvirtadalis organizme esančio natrio įeina į audinių, pavyzdžiui, kaulo, sudėtį ir jo apykaitos greitis yra labai lėtas. Didžiausia pasikeičiančio natrio dalis yra neląsteliniame skystyje: plazmoje ir intersticiniame skystyje palaikoma natrio koncentracija yra apie 140 mmol/l ( mmol/l). Eritrocituose jo yra 172 mmol/l. Natrio suvartojama įvairiai nuo mažiau kaip 100 mmol (~2 3 g) iki daugiau kaip 300 mmol per dieną (~7 g). Sveikame organizme bendras natrio kiekis nesikeičia, net jei jo suvartojama mažiau kaip 5 mmol per dieną ar jei šis kiekis didesnis negu 750 mmol per dieną. Kadangi vidutiniškai per parą natrio reikia 4 5 g, tai natrio chlorido (NaCl) turime suvartoti g per parą. Taip pat įvairuoja ir netenkamo iš organizmo natrio kiekis. Su šlapimu pašalinamo natrio kiekis beveik atitinka jo suvartojimą ( mmol per parą). Daugiausia natrio netenkama per inkstus. Nedaug jo pasišalina su prakaitu (apie 5 mmol per dieną), išmatomis (5 mmol per dieną). Tai svarbu žinoti klinikoje, ypač pediatrinėje praktikoje, nes kūdikių viduriavimas gali baigtis mirtimi dėl natrio ir vandens netekimo. Natrio koncentracija yra svarbi: palaikant osmosinį slėgį, rūgščių ir šarmų pusiausvyrą (padaugėjus natrio ir sumažėjus kalio, terpės reakcija pakrypsta į šarminę), raumenų susitraukimui. Natrio apykaitos reguliavimas. Natrio išskyrimą per inkstus reguliuoja du hormonai: aldosteronas ir prieširdžių natriurezinis peptidas. Aldosteronas slopina natrio ekskreciją per inkstus didindamas jo reabsorbciją inkstų kanalėliuose, keisdamas į kalio ir vandenilio jonus. Pagrindinis aldosterono sekrecijos stimulas yra neląstelinio skysčio tūris. Tūrio receptoriai yra išsidėstę stam- 28
30 Natrio, kalio ir chloridų apykaita... biose kraujagyslėse ir specializuotose inkstų jukstaglomerulinio aparato ląstelėse. Jie reaguoja į kraujospūdžio sumažėjimą. Kai, pavyzdžiui, kylančiosios kraujagyslės (vas afferens) sienelė nepakankamai ištempiama (taip būna, kai į glomerulus nepakankamai priteka kraujo), yra dirginami jukstaglomeruliniame aparate išsidėstę tūrio receptoriai. Tuomet juose intensyviai gaminasi reninas tai pirmoji grandinės reakcija, kuri skatina aldosterono sekreciją antinksčiuose. Inkstų fermentas reninas alfa-2-globulinų frakcijai priklausantį baltymą angiotenzinogeną paverčia dekapeptidu angiotenzinu I. Iš jo, veikiant angiotenziną konvertuojančiam fermentui (AKF), kuris atskelia dipeptidą, susidaro oktapeptidas angiotenzinas II: Reninas AKF Angiotenzinogenas Angiotenzinas I Angiotenzinas II Angiotenzinazė Neaktyvi medžiaga Pastarasis skatina aldosterono sekreciją, taip pat tiesiogiai sutraukia kraujagyslių sienelę ir yra viena stipriausių kraujospūdį didinančių medžiagų. Išsiskyręs aldosteronas suaktyvina Krebso ciklo fermentą sukcinatdehidrogenazę, ir tuomet daugiau gaminama energijos (ATF). Pastaroji skatina natrio kalio siurblio veiklą, daugiau natrio ir vandens bus sugrąžinta į kraujotaką. Taigi svarbiausias veiksnys, skatinantis renino sekreciją, yra kraujotakos inkstuose sulėtėjimas. Aldosteronas taip pat stimuliuoja natrio sulaikymą prakaito liaukose ir storosios žarnos gleivinės ląstelėse (sveikame organizme šis poveikis būna silpnas). Prieširdžių natriurezinis peptidas. Tai polipeptidinis hormonas, kurį sekretuoja širdies dešiniojo prieširdžio kardiocitai. Dėl jo poveikio didėja natrio ekskrecija su šlapimu. Šis hormonas silpnai veikia neląstelinio skysčio bei natrio kiekio reguliaciją. Detaliau apie natriurezinius peptidus skyriuje Širdies ir kraujagyslių ligų laboratorinė diagnostika. Api b e n d r i n i m a s Natrio jonai yra svarbiausi neląstelinio skysčio katijonai. Natrio iš organizmo galima netekti ilgai ir gausiai vemiant, viduriuojant, pro fistules. Aldosteronas reguliuoja natrio netekimą per inkstus ir palaiko natrio kiekį neląsteliniame skystyje. Natrio kiekio pokyčiai neląsteliniame skystyje lemia šio skysčio pakitimus dėl antidiurezinio hormono ir aldosterono poveikio. 29
31 Natrio apykaitos sutrikimai ir jų diagnostika Hipernatremija Hipernatremija tai natrio koncentracijos padidėjimas kraujo serume virš rekomenduojamo dydžio 148 mmol/l. Esant šiai būklei vystosi organizmo hiperhidratacijos sindromas. Hipernatremijos priežastys ir požymiai. Hipernatremija gali išsivystyti: kai organizmas negauna vandens; netekus daug vandens, o kartu ir natrio; per daug suvartojus natrio; kai organizmas neišskiria natrio, pavyzdžiui, esant inkstų veiklos nepakankamumui. Vertinant natrio koncentraciją kraujo serume būtina išsiaiškinti veiksnius, kurie galėjo sukelti elektrolitų apykaitos sutrikimus, t. y. ar yra duomenų, rodančių, kad ligonis neteko skysčių, ar buvo gydytas, pavyzdžiui, skiriant skysčius ir gavo jų nepakankamai, ar buvo gydomas natrio druskomis. Tai žinant galima vertinti, ar hipernatremija yra susijusi su sumažėjusiu, normaliu ar net padidėjusiu neląstelinio skysčio kiekiu. Vandens organizme gali sumažėti jo mažai geriant ar per daug netekus. Ilgą laiką mažai geriant vandens ar daugiau netenkant nepastebimo vandens, gali sumažėti neląstelinio ir ląstelinio skysčio tūris. Kai patenkančio vandens kiekis neatitinka nepastebimos vandens netekties, išsivysto hipernatremija. Tai viena dažniausių hipernatremijos priežasčių, būdinga sergantiems senyvo amžiaus asmenims, kurie negauna pakankamai skysčių ar jų negeria. Netekus vandens hipernatremija gali išsivystyti ir sutrikus vandens homeostazės reguliavimo mechanizmams. Antidiurezinio hormono sekrecija sutrinka sergant necukriniu diabetu (diabetes insipidus), kai inkstų kanalėliai nesulaiko vandens ir dėl to vystosi hipernatremija. Sergant nefrogenine necukrinio diabeto forma antidiurezinis hormonas gali neturėti poveikio, nes inkstų kanalėlių ląstelės į jį nereaguoja. Tais atvejais, kai iš neląstelinio skysčio prarandama ir vandens, ir natrio, hipernatremija išsivystys tik tuomet, kai daugiau bus netenkama vandens negu natrio. Osmosinė diurezė, kuri būdinga sergantiesiems cukriniu diabetu, sukelia vandens ir natrio stoką, ir mažėjant neląstelinio skysčio tūriui išryškės hipernatremija. Kai netenkama skysčių vemiant, viduriuojant ar pro fistules dažniau prasideda hiponatremija, o ne hipernatremija. Šiais atvejais netenkama natrio chlorido, kurio vietą užima vanduo ir vystosi hiponatremija. Hipernatremiją gali sukelti padidėjęs natrio kiekis neląsteliniame skystyje. Koreguojant acidozę vartojamas natrio rūgštusis karbonatas. Jei tokiame tirpale natrio koncentracija bus didesnė už fiziologinę, tai jį vartojant greitai pasireikš hipernatremija. Todėl natrį reikia vartoti atsargiai ir tik jei būtina. 30
32 Natrio, kalio ir chloridų apykaita... Esant pirminiam hiperaldosteronizmui, kai perteklingai sekretuojamas aldosteronas, inkstų kanalėliuose sulaikomas natris taip būna esant Kono sindromui. Panašius pokyčius sukelia ir Kušingo sindromas, kai per daug gaminama kortizolio, nes kortizoliui būdingas silpnas mineralokortikoidinis aktyvumas. Hipernatremijos diferencinei diagnostikai svarbu nustatyti šlapimo osmoliališkumą ir natrio koncentraciją jame. Hipernatremija dėl per didelio natrio vartojimo ir vandens netekimo dažniausiai yra lengvai diferencijuojama remiantis anamneze. Hipernatremijos priežastys yra apibendrintos 1 paveiksle. 1. Na + koncentracija normali, sumažėjęs H 2 O kiekis (dažniausia priežastis) dėl vandens netekimo per inkstus (necukrinis diabetas) dėl sumažėjusio H 2 O vartojimo 2. Sumažėjusi Na + koncentracija, labai sumažėjęs H 2 O kiekis Šlapimas labai koncentruotas, jo tūris mažas dėl osmosinės diurezės (cukrinis diabetas) dėl padidėjusio prakaitavimo ar viduriavimo (ypač vaikams) Šlapimas gali būti nekoncentruotas, jo tūris normalus ar padidėjęs 3. Padidėjusi Na + koncentracija, H 2 O kiekis normalus Kono sindromas, Kušingo sindromas padidėjęs natrio (druskos) vartojimas 1 pav. Hipernatremijos priežastys Netekus skysčių, išryškėja dehidratacijos požymiai. Vienas jų sumažėjęs odos elastingumas; šis požymis nepatikimas senyvo amžiaus asmenims, kurių odos elastingumas yra sumažėjęs dėl amžiaus, jauniems tai dehidratacijos, susijusios su skysčių netekimu iš neląstelinės terpės, požymis. Dėl druskų pertekliaus išryškėja skysčių perkrovos požymiai: padidėjęs veninis spaudimas ir plaučių edema. Didelis kraujo plazmos osmoliališkumas gali būti ir nesusijęs su hipernatremija. Taip būna padidėjus šlapalo kiekiui sergant inkstų ligomis, esant hiperglikemijai sergant cukriniu diabetu, daug suvartojus, pvz., etanolio. Didelis nustatytojo ir apskaičiuotojo osmoliališkumo neatitikimas yra vadinamas osmolialiniu plyšiu. Taip gali būti, kai į organizmą patenka osmoliališkumą veikiančių medžiagų etanolio ar panašių. Osmolialinio plyšio apskaičiavimas gali būti kliniškai svarbus tiriant komos būsenos pacientus. 31
33 Natrio koncentracijos sumažėjimas gali turėti didelį poveikį osmoliališkumui, nes natris yra vienintelis jonas, kurio daug yra neląsteliniame skystyje. Esant hiponatremijai dažniausiai kraujo plazmos osmoliališkumas yra sumažėjęs. Osmoliališkumo sutrikimai gali būti susiję su tūrio pokyčiais, o pastarieji su vandens judėjimu į ląsteles ar iš jų. Ryškų skysčių persiskirstymą gali sukelti gliukozės koncentracijos pokyčiai: gliukozė negali laisvai patekti į ląsteles, ir didėjanti jos koncentracija neląsteliniame skystyje verčia vandenį skirtis iš ląstelių, o tai lemia ląstelinę dehidrataciją. Šlapalas ir etanolis laisvai praeina ląstelių membraną ir skysčių persiskirstymo nesukelia, kol jų koncentracijos kinta lėtai. Api b e n d r i n i m a s Neretai hipernatremija išsivysto nejaučiant troškulio. Pavyzdžiui, komos būsenos pacientai negali bendrauti ir pasakyti apie savo poreikius, todėl nepastebimai per plaučius, odą prarandama vandens, kurio atsargas organizme reikia nuolat papildyti. Hipernatremija gali vystytis dėl organizmo negebėjimo sulaikyti vandenį, kai yra sutrikusi antidiurezinio hormono sekrecija ar veikimas. Hipernatremija gali išsivystyti ir dėl natrio, ir dėl vandens netekimo, kaip diabetinei ketoacidozei būdingos osmosinės diurezės padarinys. Hipernatremija gali išsivystyti dėl per didelio natrio kiekio patekimo į organizmą, pvz., intraveninės infuzijos, retai dėl pirminio hiperaldosteronizmo (Kono sindromo). Didelis plazmos osmoliališkumas būdingas esant nemažai gliukozės, šlapalo ar etanolio, o ne natrio koncentracijai. Hiponatremija Palyginti su hipernatremija, hiponatremija yra kur kas dažnesnė ir paprastai yra kompensuota. Hiponatremija išsivysto smarkiai sumažėjus natrio koncentracijai kraujo serume, t. y. kai natrio yra mažiau negu rekomenduojama apatinė riba 134 mmol/l. Hiponatremijos priežastys ir požymiai. Hiponatremija gali išsivystyti dėl: vandens sulaikymo organizme, t. y. kai žmogaus organizme vandens yra sulaikoma daugiau negu normaliai ir jis praskiedžia neląstelinės terpės medžiagas; natrio praradimo, kai natrio jonų šalinimas viršija vandens šalinimą. Taip būna, kai natrio turinčių organizmo skysčių netenkama vemiant ar pro fistules ir juos kompensuojant paprasčiausiu vandeniu. Hiponatremija dėl vandens sulaikymo apibūdinta 4 lentelėje. Klinikinėje praktikoje hiponatremija dėl vandens pertekliaus, nesumažėjus bendrojo natrio kiekiui organizme, yra dažnas reiškinys. Tolesnis šio hiponatremijos tipo vertinimas ir gydymas priklauso nuo to, ar yra edema, ar jos nėra. Edema yra skysčių susikaupimas intersticinėje terpėje. Ją galima nustatyti pagal pirštų įspaudus kojose stovint ar kryžmens srityje gulintiems ligoniams. 32
34 Natrio, kalio ir chloridų apykaita... 4 lentelė. Hiponatremijos priežastys 1. Vandens susilaikymas (dažniausia priežastis): hiponatremija su edema: kai per daug geriama vandens, pvz., į veną sušvirkštus netinkamą druskos kiekį, kai per daug šalinama vandens, pvz., sergant nefroziniu sindromu; hiponatremija be edemos: kai per daug geriama vandens, kai per daug šalinama vandens, pvz., sergant inkstų nepakankamumu. 2. Vandens ir natrio susilaikymas, pvz., esant Kono sindromui, hiperaldosteronizmui. 3. Natrio stoka dėl to sumažėja neląstelinio skysčio tūris: per daug netekus natrio per inkstus, virškinamąjį traktą, odą, per mažai vartojant natrio (labai retai). Esant hiponatremijai be edemos, natrio kiekis organizme yra normalus, tačiau kraujyje sumažėjęs (hiponatremija); kraujospūdis, glomerulų filtracijos greitis yra normalūs, taip pat normali ir šlapalo bei kreatinino koncentracija kraujo serume. Šlapimo tėkmės greitis paprastai yra mažesnis negu 1,5 l per dieną. Šis sindromas išryškėja dėl įvairių būklių: infekcijos (pneumonijos), piktybinių procesų (žarnų ar plaučių vėžio), traumos (po operacijų pilvo srityje), vartojant vaistų (tiazidinių diuretikų). Šių būklių metu yra stimuliuojama antidiurezinio hormono sekrecija (neosmosinė), t. y. ligoniams išsivystys hiponatremija, jei jie per daug gers vandens įvairių skysčių pavidalu ar jeigu jiems į veną bus sušvirkščiama per daug tirpalų, pavyzdžiui, gliukozės. Sveikame organizme antidiurezinio hormono sekrecija reguliuojama keičiantis natrio koncentracijai neląsteliniame skystyje: nedidelis šio hormono kiekis skatina vandens reabsorbciją inkstų kanalėliuose ir kartu šlapimo išsiskyrimą. Neosmosinis stimulas, pavyzdžiui, skausmas, hipotenzija, pykinimas, vėmimas, gali labai padidinti antidiurezinio hormono sekreciją ir dėl to vanduo bus sulaikomas. Retai dėl greito vandens kaupimosi organizme gali išsivystyti neurologiniai simptomai traukuliai ar net koma. Hiponatremija su edema. Pagrindiniai edemos požymiai yra širdies veiklos nepakankamumas ir hipoalbuminemija. Šioms būklėms yra būdingas sumažėjęs efektyvusis kraujo tūris: esant nepakankamumui širdis nepajėgia palaikyti pakankamos kraujo ir neląstelinio skysčio cirkuliacijos, o esant hipoalbuminemijai sumažėjęs albuminų kiekis mažina plazmos onkotinį slėgį; tai sutrikdo normalią medžiagų ir skysčių apykaitą, dėl to kraujo ir tarpląstelinio skysčio cirkuliacija yra nepakankama. Pacientams, kuriems nustatyta generalizuotoji edema, būdingas bendro vandens ir natrio kiekio organizme perteklius. Ši būklė išsivysto dėl to, kad kaip atsakas į sumažėjusį efektyvųjį kraujo tūrį yra sekretuojamas aldosteronas, dėl to sulaikoma natrio ir padidėja neląstelinio skysčio tūris. Smarkiai sumažėjęs kraujo tūris yra vie- 33
35 Padidėjusi aldosterono sekrecija Sumažėjęs kraujo tūris dėl širdies veiklos nepakankamumo ar hipoalbuminemijos Padidėjusi antidiurezinio hormono sekrecija Natrio sulaikymas Vandens sulaikymas Hiponatremija 2 pav. Hiponatremijos vystymasis esant edemai nas neosmosinių dirgiklių sekretuoti antidiurezinį hormoną, kuris sulaiko vandenį organizme. Paprastai sulaikoma daugiau vandens negu natrio, dėl to neląstelinėje terpėje išsivysto hiponatremija (2 pav.). Hiponatremija dėl natrio netekimo. Nors dažniausia hiponatremijos priežastis yra vandens susilaikymas organizme, ji gali išsivystyti ir netekus natrio. Paprastai toks natrio netekimas yra patologinis ir gali būti susijęs su jo šalinimu per virškinamąjį traktą ar su šlapimu. Natrio per virškinamąjį traktą netenkama užsitęsus vėmimui (pvz., esant skrandžio prievarčio stenozei), viduriuojant, pro fistules. Su šlapimu natrio netenkama stokojant aldosterono (pvz., dėl antinksčių žievės veiklos nepakankamumo sergant Adisono liga), vartojant vaistų, kurie yra aldosterono veikimo antagonistai. Hiponatremija gali išsivystyti ir tada, kai natrio turinčio skysčio stoka yra kompensuojama tik geriamu ar į veną leidžiamu vandeniu. Iš pradžių natrio netenkama su vandeniu, todėl natrio koncentracija serume išlieka normali. Kai tokia būklė tęsiasi, neląstelinio skysčio ir kraujo kiekio sumažėjimas skatina antidiurezinio hormono sekreciją, padidėjusi antidiurezinio hormono sekrecija vandens sulaikymą, ir taip vystosi hiponatremija. Hiponatremija dėl per mažo natrio vartojimo yra labai reta būklė (žr. 4 lentelę). Natrio stokos diagnozė paprastai remiasi ligos anamneze. Iš visų klinikinių neląstelinio skysčio stokos požymių svarbiausi yra hipotenzija ir tachikardija. Jei šie požymiai yra nustatomi gulint, galima įtarti gyvybei pavojingą natrio stoką ir būtina kuo greičiau pradėti gydyti. Kai natrio stokos stadijos ankstyvos, vienintelis požymis gali būti ortostatinė hipotenzija. Kiti būdingi klinikiniai neląstelinio skysčio stokos požymiai yra šie: sausos gleivinės, minkšti akių obuoliai, sumažėjęs odos elastingumas, prislopinta sąmonė, sumažėjęs šlapimo kiekis ir, kaip minėjome, sumažėjęs kraujospūdis stovint, padažnėjęs pulsas. Taigi, hiponatremija paprastai atsiranda asmenims, kurie neteko natrio turinčių skysčių ir kurių neląstelinio skysčio tūris sumažėjo. Kai kada netenkant natrio gali 34
36 Natrio, kalio ir chloridų apykaita... išsivystyti ir hipernatremija. Taip pat įmanoma, kad pacientų, kuriems yra gyvybei pavojinga natrio stoka, natrio koncentracija kraujo serume gali būti normali. Taigi gydytojas visada turi atkreipti dėmesį į ligonio ligos istoriją, simptomus ir požymius, o ne tik į biocheminio tyrimo rezultatus. Žinotina, kad padidėjęs baltymų ar lipoproteinų kiekis užima didesnę plazmos tūrio dalį negu normaliai, o vanduo sudaro mažesniąją. Kai kurie analiziniai prietaisai natrio kiekį nustato nedideliame tūryje ir natrio koncentraciją bandinyje įvertina kaip normalią, o iš tiesų ji būna sumažėjusi. Tai pseudohiponatremija, kuri gali būti aptikta matuojant serumo osmoliališkumą jis bus normalus. Api b e n d r i n i m a s Edema nėra vien antrinio hiperaldosteronizmo padarinys. Pavyzdžiui, esant uždegimui ar sutrikus veninio kraujo grįžimui, atsiranda veiksnių, kurie padidina neląstelinio skysčio tūrį. Hiponatremija, kai susilaiko vanduo: hiponatremija dėl vandens susilaikymo yra dažnas reiškinys klinikinėje praktikoje; daugeliui pacientų neosmosinis antidiurezinio hormono reguliavimas būna stipresnis negu osmosinio reguliavimo mechanizmai ir dėl to sulaikomas vanduo tai yra nespecifinis ligos požymis; asmenų, kuriems nustatyta hiponatremija be edemos, kraujyje yra normali šlapalo, kreatinino koncentracija, šių asmenų kraujospūdis normalus, tačiau būdingas vandens perteklius organizme; asmenims, kuriems nustatyta hiponatremija su edema, būdingas ir vandens, ir natrio jonų perteklius. Jie gydomi diuretikais ir ribojant skysčių vartojimą. Hiponatremija gali išsivystyti asmenims, kurie netenka skysčių per virškinamąjį traktą ar su šlapimu; dėl to kartu netenkama ir natrio. Taip pat maža natrio koncentracija serume nustatoma, kai susilaiko vanduo; šį procesą skatina padidėjusi antidiurezinio hormono sekrecija. Išsivysčius hiponatremijai dėl natrio netekimo, išryškėja skysčių stokos požymiai, pvz., hipotenzija; edema nebūdinga. Laboratoriniai tyrimai Natris (Na) Tiriamoji medžiaga. Serumas. Rekomenduojama reikšmė mmol/l. Tiriamoji medžiaga. Smegenų skystis. Rekomenduojama reikšmė mmol/l. Diagnostinė vertė. Būklės, kai netenkama daugiau vandens negu druskų per odą (gausus prakaitavimas), plaučius (ilgai giliai kvėpuojant), virškinamąjį traktą (gausus vėmimas ar viduriavimas), inkstus (poliurija sergant inkstiniu diabetu, esant diabetinei acidozei); padidėjęs natrio sulaikymas inkstuose sergant hiperaldosteronizmu, Kušingo (Cushing) sindromu; nepa- 35
37 kankamas vandens vartojimas, nes nėra troškulio (pvz., koma, pogumburio ligos); dehidratacija; druskų perteklius gydant. Per mažas natrio suvartojimas; natrio netekimas vemiant, viduriuojant, gausiai prakaituojant ir pakankamai vartojant vandens, o per mažai druskų; piktnaudžiavimas diuretikais (dažna klinikinė priežastis) ar nefropatija netenkant druskų (policistiniai inkstai, lėtinis pielonefritas, inkstų kanalėlių acidozė); osmosinė diurezė; metabolinė acidozė (dėl padidėjusio katijonų šalinimo); pirminis ir antrinis antinksčių žievės nepakankamumas; įgimta antinksčių hiperplazija esant 21-hidroksilazės stokai (dažnai), kitos antinksčių hiperplazijos formos kartu netenkant druskų; praskiedimo hiponatremija, susijusi su edema, ascitu (pvz., lėtinis širdies veiklos nepakankamumas, cukrinis diabetas, kepenų cirozė, kepenų nepakankamumas, nefrozinis sindromas, intersticinis nefritas, nepakankama mityba ar intoksikacija skysčiais); hipotirozė; hiperosmoliališkumas; nepakankamos antidiurezinio hormono sekrecijos sindromas, kuris gali būti susijęs su plaučių, kasos vėžiu, plaučių infekcija, centrinės nervų sistemos ligomis; ūminė intermituojanti porfirija; pscihogeninė polidipsija; dirbtinė protarpinė, esant ypač ryškiai hipertriacilglicerolemijai ar hipoproteinemijai; hiperglikemija. Perteklinė antidiurezinio hormono gamyba. Papildoma informacija. Jei natrio <120 mmol/l, jaučiamas silpnumas; <110 mmol/l ištinka bulbarinis ar pseudobulbarinis paralyžius, mmol/l pasireiškia sunkūs neurologiniai simptomai, o jei koncentracija >155 mmol/l, sutrinka širdies ir kraujagyslių bei inkstų veikla. V: anaboliniai steroidai, androgenai, AKTH, estrogenai, fenilbutazonas, karbenicilinas, klonidas, gliukokortikoidai, laktuliozė, metildopa, geriamieji kontraceptikai, natrio bikarbonatas, rezerpinas, saldymedžio ekstraktas. V: aminoglikozidai, amonio chloridas, angiotenziną konvertuojančio fermento inhibitoriai, kaptoprilis, chlorpropamidas, cholestiraminas, ciklofosfamidas, diuretikai (chlortalidonas, etakrino rūgštis, furozemidas, manitolis, spironolaktonas, šlapalas, tiazidai, triamterenas), fenotiazinai, gliukozė (hipertoninis tirpalas), haloperidolis, heparinas, indometacinas, karbamazepinas, klofibratas, litis, nesteroidiniai vaistai nuo uždegimo, oksitocinas, tolbutamidas, tricikliai antidepresantai (amitriptilinas), vazopresinas, vinblastinas, vinkristinas Tiriamoji medžiaga. Paros šlapimas. Rekomenduojama reikšmė mmol/24 val. Diagnostinė vertė. Padidėjęs natrio vartojimas, pomenstruacinė diurezė (fiziologinė), antinksčių veiklos nepakankamumas (pirminis ir antrinis), nefritas netenkant druskų, inkstų kanalėlių intersticinė liga, inkstų kanalėlių acidozė, gydymas diuretikais, Barterio sindromas, antidiurezinio hormono nepakankamos sekrecijos sindromas, bet kuri alkalozės forma ir kitos būklės, kai skiriasi šarminis šlapimas. Mažas natrio vartojimas, premenstruacinis natrio ir vandens sulaikymas (fiziologinis), natrio netekimas pakankamai vartojant vandens, val. po operacijos (streso sindromo diurezė), antinksčių žievės hiperfunkcija, sumažėjęs inkstų glomerulų filtracijos greitis (įgimta širdies liga), ūminė oligurija ir prereninė azotemija, viduriavimas, gausus prakaitavimas. Papildoma informacija. Inkstų slenkstis natriui yra mmol/l. Natrio šalinimas per naktį sudaro 1/5 dienos maksimumo, ir tai rodo didelį natrio šalinimo įvairavimą per parą. Natrio šalinimui su šlapimu didelės įtakos turi maisto sudėtis ir vandens apykaita. Natrio koncentracija <15 mmol/l susidaro esant prereninei acidozei, o dar didesnes jo reikšmes lemia ūminė kanalėlių nekrozė. V: diuretikai, dopaminas, heparinas, kofeinas, kalcitoninas, kaptoprilis, karboksianhidrazės inhibitoriai, litis, progesteronas (didelės dozės), sulfatai, tetraciklinas, vinkristinas. V: adrenalinas, gliukokortikoidai, propranololis. 36
38 Natrio, kalio ir chloridų apykaita... Ka l i s Kalio pasiskirstymas organizme. Kalis yra svarbiausias ląstelių katijonas. 70 kg sveriančio žmogaus organizme yra apie 130 g (3600 mmol) kalio. Kalio jonų koncentracija kraujo plazmoje yra 4,5 mmol/l (3,8 5,3 mmol/l), o eritrocituose yra apie 20 kartų didesnė iki 115 mmol/l. Naujagimių kraujo plazmoje kalio jonų koncentracija yra apie 0,5 mmol/l mažesnė negu suaugusiųjų. Ypač daug kalio yra raumenyse, todėl, sergant širdies ligomis ar dėl įvairių ligų nykstant raumenims, mažėja ir kalio jonų koncentracija. Per parą kalio reikia 2 4 g. Didžioji kalio dalis iš organizmo pašalinama per inkstus ( mmol per parą). Kuo daugiau kalio suvartojama, tuo daugiau jo šalinama su šlapimu. Kalio šalinimas per inkstus pirmiausia priklauso nuo filtracijos glomeruluose. Svarbiausias veiksnys, reguliuojantis kalio ekskreciją su šlapimu, yra kalio koncentracija kraujo plazmoje. Dalis kalio pasišalina su išmatomis ( 5 mmol per dieną). Esant patologijai, šalinimas per virškinamąjį traktą vemiant, viduriuojant, pro fistules gali labai padidėti. Per odą su prakaitu pasišalina tik nedidelis kalio kiekis. Kraujo serume esantį kalio kiekį lemia šie veiksniai: bendrasis kalio kiekis organizme (pakitus bendrajam kalio kiekiui mmol, jo koncentracija serume pasikeičia 1 mmol/l); kraujo plazmos ph (ph pasikeitimas 0,1 dalimi atitinka kalio jonų koncentracijos pokytį 0,6 mmol/l); reguliavimo mechanizmai. Nedidelė bendrojo kalio dalis (2%), kuri yra neląstelinėje terpėje, yra tolygiai pasiskirsčiusi tarp intersticinės terpės ir kraujo plazmos. Kalio koncentracijos plazmoje svyravimai dėl vandens netekimo ar susilaikymo yra nedideli, o veiksniai, kurie sukelia staigų, kad ir nedidelį, ląstelinio kalio kiekio svyravimą, gali būti didelių neląstelinio kalio kiekio pokyčių ir koncentracijos svyravimų priežastis. Kalio patekimą į ląsteles skatina insulinas. Ypač svarbus yra kalio ir vandenilio jonų tarpusavio ryšys. Acidozės metu didėjant vandenilio jonų koncentracijai, kalio jonai iš ląstelės šalinami, o metabolinės alkalozės metu sulaikomi. Šie vandenilio jonų koncentracijos pokyčiai sukelia reikšmingus kalio koncentracijos plazmoje pokyčius. Kalio koncentracija kraujo plazmoje (serume) neatspindi jo kiekio organizme. Tačiau esant organizme normaliai rūgščių ir šarmų pusiausvyrai, hipokalemija rodo ir bendrojo kalio stoką. Taip pat kalis yra svarbus ląstelių membranos ramybės potencialui. Kalio koncentracijos pokyčiai plazmoje rodo, kad sudirgintos nervų ar raumenų ląstelės skirtingai reaguoja į stimulą. Ypač tai pasakytina apie širdį, kurią daugiausia sudaro raumuo ir nervai: padidėjusi ar sumažėjusi kalio koncentracija plazmoje gali būti pavojinga gyvybei. 37
39 Taigi kalio koncentracija plazmoje yra svarbi šiais atžvilgiais: angliavandenių ir baltymų apykaitai, ląstelių membranos poliarizacijos, depoliarizacijos ir repoliarizacijos procesams, nervų ir raumenų jaudrumui, nervinio impulso perdavimui (svarbus sintetinant organizmui acetilcholiną, cholinesterazės skaldymui), pasižymi depresiniu (vagotropiniu) veikimu (ryški hipokalemija širdį sustabdo per sistolę, o hiperkalemija per diastolę). Kalio apykaitos sutrikimai ir jų diagnostika Sutrikusią kalio apykaitą gali rodyti širdies aritmija, ligos, gydomos diuretikais, hipertenzija. Hiperkalemija (kalio koncentracija kraujo serume padidėja virš rekomenduojamo dydžio 5,3 mmol/l) yra sunkiausia būklė, kurią sukelia sutrikusi elektrolitų pusiausvyra. Hiperkalemiją rodo nusilpę raumenys (griaučių, širdies), parastezijos. Kalio koncentracija, viršijanti 7,0 mmol/l, yra pavojinga gyvybei gali sustoti širdis (skilvelių virpėjimas ar asistolija). Šią būklę galima aptikti iš elektrokardiogramos matyti platus QRS kompleksas, aukštas T dantelis. Tačiau hiperkalemijos požymiai elektrokardiogramoje gali paslėpti kitą būklę miokardo infarktą. Taigi sutrikus širdies darbui svarbu nustatyti kalio koncentraciją serume. Hiperkalemijos priežastys: 1) inkstų nepakankamumas, kai inkstai nesugeba pašalinti kalio pertekliaus esant susilpnėjusiai glomerulų filtracijai; 2) per didelis patekusio į organizmą kalio kiekis (retai, pvz., į veną sušvirkštus antibiotikų); 3) pakitus kalio pernašai per membraną: esant acidozei, nes tada kalio kiekis persiskirsto tarp ląstelinio ir neląstelinio skysčių; netenkant kalio iš pažeistų ląstelių, pvz., esant traumai, navikui; 4) esant mineralkortikoidų stokai, kuri gali išsivystyti, pvz., sergant Adisono liga. Su širdies ir kraujagyslių ligomis susijęs kalio kiekio kraujo plazmoje didėjimas nustatomas, kai daugiau kalio patenka iš ląstelių, pavyzdžiui, įvykus miokardo infarktui, kai sumažėja jo šalinimas per inkstus, pavyzdžiui, esant šokui, audinių išemijai, taip pat po sunkių fizinių pratimų (ypač vartojant β adrenoblokatorių). Padidėjęs kalio kiekis kaip artefaktas nustatomas įvykus hemolizei kraujo ėmimo metu ar uždelsus centrifuguoti paimtą į mėgintuvėlį kraują. Hipokalemija. Ji išsivysto, kai kalio koncentracija tampa <3,8 mmol/l, ypač jei kalio sumažėja staiga. Elektrokardiogramoje būdinga ST segmento depresija, pailgėjusi T banga. Jei hipokalemija vystosi lėtai, simptomai gali ir neišryškėti. 38
40 Natrio, kalio ir chloridų apykaita... Hipokalemijos priežastys: 1) nepakankamas kalio vartojimas (labai retai); 2) kalio netekimas: per virškinamąjį traktą, pavyzdžiui, vemiant, viduriuojant; per inkstus, pavyzdžiui, sergant inkstų ligomis, vartojant vaistus (tiazidinius diuretikus ir gliukokortikoidus); 3) pakitus kalio pernašai per ląstelių membraną, pavyzdžiui, esant alkalozei, nes kalis iš tarpląstelinio skysčio patenka ląsteles. Svarbiausi hipokalemijos požymiai yra susiję su nervų ir raumenų pažeidimu, kai jaučiamas nuovargis, silpnumas, susilpnėja refleksai; būdinga širdies aritmija (skilvelių virpėjimas), gali būti pažeisti inkstai (retai) ir dėl to vystytis poliurija. Api b e n d r i n i m a s Kalio jonai yra svarbiausi ląstelinio skysčio katijonai. Net ir nedidelis kalio kiekis neląsteliniame skystyje yra svarbus palaikant raumenų ir nervų ląstelių membranų potencialą. Kalio koncentracijos serume pokyčiai gali atspindėti bendrojo kalio kiekio organizme sumažėjimą ar padidėjimą, taip pat kalio judėjimą į ląsteles ir iš jų. Hiperkalemija yra pavojinga gyvybei būklė gali ištikti staigi mirtis. Didelis kalio kiekis serume yra susijęs su susilpnėjusia inkstų funkcija. Hipokalemija paprastai yra susijusi su kalio netekimu per virškinimąjį traktą ar per inkstus. Gydymas tiazidiniais diuretikais dažnai sukelia kalio stoką, kuri gali būti nepaaiškinamos metabolinės alkalozės priežastis. Laboratoriniai tyrimai Kalis (K) Tiriamoji medžiaga. Serumas. Rekomenduojama reikšmė. 3,8 5,3 mmo/l. Tiriamoji medžiaga. Smegenų skystis. Rekomenduojama reikšmė. 2,5 3,2 mmol/l. Diagnostinė vertė. Padidėjęs kalio patekimas į organizmą: greita kalio infuzija. Kalio persiskirstymas organizme (neląstelinis skystis gauna K iš ląstelių): masyvi hemolizė, didelis audinių pažeidimas, ūminis badas (pvz., nervinė anoreksija), hiperkinezinis aktyvumas (pvz., epilepsijos priepuolis), piktybinė hiperpireksija po anestezijos, hiperkaleminis periodinis paralyžius (priepuoliai atsiranda praėjus min. po fizinių pratimų), acidozė, dehidratacija. Sumažėjęs kalis šalinimas per insktus: bet kuri ūminio inkstų nepakankamumo su oligurija, anurija ar acidoze priežastis; lėtinių inkstų ligų galutinės stadijos esant oligurijai; Adisono liga; renino angiotenzino aldosterono sistemos hipofunkcija; pseudohipoaldosteronizmas; druskų netekimas (kitos priežastys); po sunkių fizinių pratimų (ypač vartojant β adrenoblokatorių); šokas, išplitusi hemolizė, audinių išemija. 39
41 Sumažėjęs kalio vartojimas: ilgalaikis badavimas, neląstelinio K koncentracijos sumažėjimas vartojant mažai K turinčius skysčius (pvz., po operacijos ligonis negali vartoti daug K turinčio maisto). Kalio netekimas iš organizmo: su žarnų sekretu: besitęsiantis vėmimas, viduriavimas, žarnų fistulės; su šlapimu: inkstų kanalėlių acidozė, inkstų kanalėlių nepakankamumas, Fankonio sindromas, pirminis ir antrinis aldosteronizmas, Kušingo sindromas, Barterio sindromas, osmosinė diurezė (pvz., dėl hiperglikemijos), alkalozė, diabetinė ketoacidozė gliukoneogenezės metu, vartojant AKTH, kortizono ar testosterono; su prakaitu: cistinė fibrozė. Kalio persiskirstymas organizme (patekimas į ląsteles): gydymas gliukoze ir insulinu, šeiminis periodinis paralyžius, K netekimas iš tarpląstelinės erdvės (į ląsteles ir šlapimą esant alkalozei; į ląsteles, šlapimą ir žarnų spindį esant prievarčio stenozei ir alkalozei). Įvairios priežastys: hipotermija, netekimas iš žaizdų ar nudegimų, megaloblastinės anemijos gydymas B 12 vitaminu ir folio rūgštimi, kasos ląstelių navikas, gaminantis vazoaktyvų žarnų polipeptidą, bulimija. Papildoma informacija. Klaidingai padidėjęs K kiekis serume galimas dėl šių priežasčių: rankos mankštinimas užspaudus timpa (gali padidėti 10 20%); paimto kraujo hemolizė ar per vėlai plazma (serumas) atskirta nuo eritrocitų (0,5% eritrocitų hemolizė padidina K kiekį 0,5 mmol/l); K atsipalaidavimas iš trombocitų krešant kraujui (ruošiant serumą); lėtinė limfoleukemija, esant labai dideliam leukocitų skaičiui; jei kraujas paliekamas kambario temperatūroje; trombocitozė, leukemija. Per parą K kiekis serume įvairuoja: mažiausia koncentracija apie 22 val; didžiausia 8 val. ryte. Negaudami pakankamai K, suaugusieji su šlapimu šalina mmol/l K per dieną, ir tai vyksta dar 4 dienas, kol šalinamo K kiekis krinta. NaCl vartojimas mažai K turintiems pacientams skatina tolesnę K netektį su šlapimu. Sergant metaboline alkaloze, kai inkstų funkcija gera, plazmos K koncentracija mažėja; dėl metabolinės alkalozės, kai inkstų funkcija bloga, K skiriasi mažai, bet plazmoje K kiekis yra normalus ar net padidėja. Klinikiniai hipokalemijos simptomai (nuovargis, silpnumas, susilpnėję refleksai, skilvelių virpėjimas) išsivysto K koncentracijai kritus < 2,0 mmol/l, ypač jei K sumažėja staiga. Hiperkalemiją rodo raumenų (griaučių ir širdies) dirglumas. Elektrokardiogramoje matyti aukštas T dantelis. K koncentracijos padidėjimas > 7,0 mmol/l yra pavojingas gyvybei. V: adrenalinas (pradinis poveikis), β adrenoblokatoriai (retai), aminokaprono rūgštis, angiotenziną konvertuojančio fermento inhibitoriai, argininas, ciklosporinas, digoksinas (toksiškumas), druskos pakaitalai, fenforminas (laktinė acidozė), heparinas, histaminas, izoniazidas, litis, manitolis, meticilinas, nesteroidiniai vaistai nuo uždegimo, penicilinas (K druska), priešnavikiniai vaistai (ciklofosfamidas, vinkristinas), spironolaktonas, tetraciklinas, triamterenas. V: β adrenerginiai agonistai (salbutamolis), aminoglikozidai, p aminosalicilatas, aminosalicilo rūgštis (retai), amfotericinas, cholestiraminas, ciankobalaminas, diuretikai (etakrino rūgštis, furozemidas, tiazidai), EDTA, fenolftaleinas, gliukozė, insulinas, karbenicilinas, gliukokortikooidai, kortikotropinas, levadopa, natrio bikarbonatas, natrio chloridas, G penicilinas (Na druska), B polimiksinas, salicilatai, teofilinas Tiriamoji medžiaga. Paros šlapimas. Rekomenduojama reikšmė mmol/24 val. Diagnostinė vertė. Badavimo pradžia (vėliau K kiekis krinta), Kušingo sindromas, pirminis ir antrinis aldosteronizmas, inkstų ligos (inkstų kanalėlių sindromai, sveikimas po ūminės kanalėlių nekrozės, metabolinė acidozė, metabolinė alkalozė), gydant AKTH, hidrokortizonu, kortizonu. 40
42 Natrio, kalio ir chloridų apykaita... Lėtinės K stokos būklės; Adisono liga; inkstų ligos, ypač sumažėjus šlapimo tėkmei (sunki glomerulonefrito forma, pielonefritas, nefrosklerozė). Papildoma informacija. Šlapimo K koncentracija <20 mmol/l yra susijusi su ne inkstų sukeltomis ligomis, o jei K koncentracija >20 mmol/l galimos inkstų ligos. V: amfotericinas, deoksikortikosteronas, gentamicinas, kalcitoninas, karbenicilinas, gliukokortikoidai, kortikotropinas, levadopa, penicilinas, sulfatai, diuretikai. V: alaninas (badaujant nutukusiems), adrenalinas, anestetikai, augimo hormonas, indometacinas, klopamidas. Chl o r i d a i Chloridų pasiskirstymas organizme. Chloridų jonai (Cl - ) yra svarbiausi neląsteliniai anijonai ir sudaro didžiausią kraujo plazmos visų neorganinių anijonų koncentraciją, t. y. apie 154 mmol/l. Kraujo plazmos chloridų koncentracija dažniausiai kinta kartu su natrio jonų koncentracija. Todėl chloridai yra svarbūs palaikant organizme vandens pasiskirstymą, osmosinį slėgį, anijonų ir katijonų pusiausvyrą. Sveikų asmenų chloridų koncentracija kraujo serume yra mmol/l, smegenų skystyje mmol/l; jo kiekis paros (24 val.) šlapime mmol. Su maistu patekę chloridų jonai yra absorbuojami virškinamajame trakte. Jų išsiskyrimas su šlapimu priklauso nuo kiekio, kuris patenka su maistu; trūkstant chloridų maiste, jo smarkiai sumažėja ir šlapime. Chloridai iš organizmo šalinami su šlapimu (90%), prakaitu, išmatomis. Chloridų jonai filtruojami inkstų glomeruluose ir po to pasyviai reabsorbuojami proksimaliniuose kanalėliuose kartu su natrio jonais, o Henlės kilpos kylančioje dalyje aktyvią chloridų, taip pat natrio reabsorbsorbciją lemia vadinamasis chloro siurblys. Pastarasis procesas skatina Na + reabsorbciją. Kilpiniai diuretikai, pavyzdžiui, furozemidas, slopina šio siurblio veiklą. Organizme didžiausia chloridų dalis yra jonizuotosios būklės NaCl, KCl, CaCl 2, MgCl 2 druskose. Chloridų atsargų yra odoje, joje susikaupia iki 30 60% organizmo chloridų. Chloridų apykaitos sutrikimai Hipochloremija išsivysto netekus chloridų jonų sergant nefritu (pavyzdžiui, lėtiniu pielonefritu). Nors chloridų stokojama, sutrinka jų reabsorbcija inkstų kanalėliuose. Chloridų galima netekti ir per virškinamąjį traktą, t. y. vemiant, viduriuojant. Hipochloremija gali atsirasti dirbant sunkų fizinį darbą, gausiai prakaituojant (esant aukštai aplinkos temperatūrai) bei karščiuojant, sumažėjus chloridų maiste. Hipochloremija išsivysto tais metabolinės acidozės atvejais, kai padidėja organinių rūgščių susidarymas ir sutrinka jų šalinimas. Taip būna, pavyzdžiui, dėl diabetinės ketoacidozės, inkstų nepakankamumo, be to, po įvairių operacijų (jei pooperacinę acidozę sukelia didėjantis CO 2 kiekis plazmoje ir daugiau chloridų jonų pereina į eritrocitus), kai chloridų jonų kraujyje sumažėja dėl jų susilaikymo audiniuose, sergant inkstų diabetu. 41
43 Hiperchloremija išryškėja sumažėjus chloridų išsiskyrimui iš organizmo (ūminis inkstų nepakankamumas, metabolinė acidozė užsitęsus viduriavimui); vartojant daug chloridų; ji gali būti smarkaus inkstų kanalėlių pažeidimo požymis (šlapimtakių užsikimšimas, glomerulonefritas); taip pat gali būti sergant alkaloze, kai kraujyje sumažėja CO 2 (kai chloridai iš eritrocitų pereina į plazmą); sumažėjus HCO 3 koncentracijai, gali atsirasti ir hipernatremija. Laboratoriniai tyrimai Chloridai (Cl) Tiriamoji medžiaga. Serumas. Rekomenduojama reikšmė mmol/l. Diagnostinė vertė. Dehidratacija, inkstų kanalėlių acidozė, ūminis inkstų veiklos nepakankamumas, inkstinis diabetas, metabolinė acidozė dėl besitęsiančio viduriavimo ir NaHCO 3 netekimo, apsinuodijimas salicilatais, respiracinė alkalozė, kai kurie pirminės hiperparatirozės atvejai, su galvos trauma susijusi pogumburio srities stimuliacija ar pažeidimas, antinksčių žievės hiperfunkcija. Per didelis prakaitavimas, bet kurios priežasties sukeltas užsitęsęs vėmimas, skrandžio turinio siurbimas, nefritas, susijęs su druskų netekimu, Adisono ligos krizė, metabolinė acidozė, susijusi su organinių anijonų kiekio padidėjimu, aldosteronizmas, kalio išeikvojimas, susijęs su alkaloze, respiracine acidoze, druskų netekimu dėl galvos traumos, intoksikacija vandeniu ir kitomis priežastimis, kai didėja neląstelinio skysčio tūris; ūminė protarpinė porfirija, sutrikusios antidiurezinio hormono sekrecijos sindromas. Papildoma informacija. Išskyrus ūminius atvejus, chloridai tiriami pacientui nevalgius. Pavalgius chloridų jonų kiekis šiek tiek sumažėja. Priežastys, kurios sukelia hipernatremiją, sukelia ir hiperchloremiją. Apsinuodijus bromidais, bromidų jonai (Br ) pakeičia chloridų jonus (Cl ). V: androgenai, cholestiraminas, estrogenai, fenilbutazonas, guanetidinas, metildopa, oksifenbutazonas, tiazidai (ilgo veikimo), triamterenas (nefrotoksinis poveikis). Ch: bromidai, jodidai. V: bikarbonatai, diuretikai (pvz., furozemidas, manitolis, tiazidai, triamterenas), kortikotropinas, teofilinas, vidurius laisvinantys vaistai (ilgalaikis vartojimas) Tiriamoji medžiaga. Paros šlapimas. Rekomenduojama reikšmė mmol/24 val. Diagnostinė vertė. Per didelis druskos vartojimas, pomenopauzinė diurezė (fiziologinė), gausi diurezė dėl kitų priežasčių (pvz., nefritas gausiai išsiskiriant druskoms, nes chloridai išskiriami su katijonais), kalio išeikvojimas, antinksčių veiklos nepakankamumas, kanalėlių intersticinė liga, Barterio sindromas. Sumažėjęs druskos vartojimas, premenstruacinis druskų ir vandens susilaikymas (fiziologinis), gausus ekstrareninis chloridų netekimas (pvz., vėmimas, žarnų fistulė, stiprus viduriavimas, gausus prakaitavimas ir nepakankamas NaCl vartojimas), antinksčių žievės hiperfunkcija, pooperacinis chloridų susilaikymas, bet kurios kitos druskų susilaikymo priežastys (pvz., edemos formavimasis, smegenų pažeidimas). Papildoma informacija. Normaliai chloridų išsiskyrimas su šlapimu atitinka jų suvartojimą su maistu. V: digitalis, diuretikai, izosorbidas. Ch: bromidai, jodidai. V: epinefrinas, gliukokortikoidai
44 Natrio, kalio ir chloridų apykaita... Tiriamoji medžiaga. Smegenų skystis. Rekomenduojama reikšmė mmol/l. Diagnostinė vertė. Bet kuri būklė, kai daugėja chloridų kraujo plazmoje. Bet kuri būklė, kai mažėja chloridų kraujo plazmoje; tuberkuliozinis meningitas, kitų tipų bakterinis meningitas (tyrimas atspindi sisteminę hipochloremiją, ligai nėra specifinis) Tiriamoji medžiaga. Prakaitas. Rekomenduojama reikšmė mmol/l. Diagnostinė vertė. Cistinė fibrozė (98% pacientų), negydytas antinksčių funkcijos nepakankamumas, šeiminė hipoparatirozė, šeiminė ektoderminė displazija su kurtumu, nefrogeninis necukrinis diabetas, hipotirozė, fukozidozė, gliukozės-6-fosfatdehidrogenazės stoka, mukopolisacharidozės, šeiminė cholestazė, alkoholinis pankreatitas, kai kurios kitos inkstų ligos. Dauguma šių būklių yra retos ir kliniškai skiriasi nuo cistinės fibrozės. Papildoma informacija. Chloridų prakaite tyrimas yra vienas patikimiausių diagnostinių cistinės fibrozės tyrimų. Tyrimas teigiamas 3 5 savaičių sergantiems kūdikiams. Jis gali būti teigiamas sveikiems asmenims, kai išeikvojamos druskos, pvz., esant labai karštiems orams. Būtina papildomai tirti elektrolitus. Su amžiumi chloridų kiekis prakaite padidėja 10 mmol/l. Odos pažeidimai ar bėrimai gali būti padidėjusio chloridų kiekio prakaite priežastis. 43
45 RŪGŠČIŲ IR ŠARMŲ PUSIAUSVYRA, JOS PALAIKYMAS, SUTRIKIMAI IR JŲ LABORATORINĖ DIAGNOSTIKA Audinių kvė p a v i m a s, r ū g š č i ų ir ša r m ų pu s i a u s v y r o s fiziologija Žmogaus organizmo funkcionavimas priklauso nuo audinių kvėpavimo intensyvumo mitochondrijose, kurio metu gaminama energija ATF pavidalu. Kad vyktų šis procesas, į ląsteles reikia atnešti deguones (O 2 ) ir iš jų pašalinti anglies dioksidą (CO 2 ). Šias funkcijas atlieka kraujas. Kraujas tai dalis organizmo vidinės terpės, kurios sudėtis yra gana pastovi. Be pasigaminusios angliarūgštės (H 2 CO 3 ), jame yra ir kitų rūgštinės reakcijos produktų: pieno, sieros, fosforo, β oksisviesto rūgščių ir kitų. Per parą iš viso susidaro apie mmol (vidutiniškai 60 mmol/l) protonų vandenilio jonų (H + ). Jei visą šį kiekį praskiestume už ląstelių ribų esančiu skysčiu (apie 14 litrų), tai vandenilio jonų koncentracija būtų 4 mmol/l, arba kartų didesnė negu susidaranti normaliai. Taip neatsitinka, nes susidarę protonai yra greitai pašalinami su šlapimu. Valgant daug baltymų turtintį maistą, išsiskiria rūgštesnis šlapimas. Be rūgščiosios reakcijos produktų, kurie yra protonų (H + ) tiekėjai, yra ir bazinių, t. y. šarminės reakcijos, jonų (HCO 3 ), kurie yra protonų akceptoriai. Pastarieji susidaro vykstant augalinių maisto komponentų apykaitai. Rūgščių ir šarmų pusiausvyra, arba organizmo skysčių reakcija, yra apibūdinama vandenilio jonų koncentracija ([H + ]) ir priklauso nuo rūgščių ir bazių koncentracijos. Taigi rūgščių ir šarmų pusiausvyros, t. y. vandenilio ir hidroksilo jonų (H + ir OH ) pusiausvyros, biologinėse terpėse fiziologijos esmė ta, kad ląstelėse vykstant medžiagų apykaitai gaminasi daug rūgštinės reakcijos vandenilio jonų, bet vis dėlto jų koncentracija ląstelėse turi būti maža, t. y. neviršyti tam tikrų ribų, nes kitaip ląstelė žus. Kad to neatsitiktų, organizmas efektyviai šalina H + tolygiai jų susidarymui; buferinės sistemos medžiagos sujungia H + ir taip palaikoma fiziologinė laisvųjų H + koncentracija. Pavyzdžiui, vykstant medžiagų apykaitai gliukozė skyla iki CO 2 ir susidaro: C 6 H 12 O 6 + 6O 2 6CO 2 + 6H 2 O CO 2 +H 2 O H 2 CO 3 H + + HCO 3 Karboanhidrazė Šalinamas 44
46 Rūgščių ir šarmų pusiausvyra... CO 2 gaminasi ląstelėse, praeina jų membraną ir pagaliau yra iškvepiamas, bet kiekviename etape reaguoja su vandeniu (H 2 O) (3 pav.). Ląstelinis skystis: ląstelių produktas Tarpląstelinis skystis Kraujas Alveolinis oras CO 2 + H 2 O H 2 CO 3 H + + HCO 3 CO 2 + H 2 O H 2 CO 3 H + + HCO 3 CO 2 + H 2 O H 2 CO 3 H + + HCO 3 CO 2 3 pav. Vandenilio jonų ir angliarūgštės apykaita ir šalinimas ph apibūdinimas Vanduo, kuris yra įprastas tirpiklis, labai blogai disocijuoja į vandenilio (H + ) ir hidroksilo (OH - ) jonus. Nedisocijuoto vandens koncentracija yra labai didelė, palyginti su jo disocijuotais jonais, ir gali būti laikoma konstanta (K). Tokią lygtį galima užrašyti taip: [H + ] [OH ] [H 2 O ] = K Kadangi nedisocijuoto vandens koncentracija yra didelė ir lieka beveik nepakitusi, todėl lygtį galima parašyti ir taip: K H2 O = [H+ ] [OH ], čia K H2 O yra joninis vandens produktas. Jo reikšmė yra labai maža: 25 C temperatūroje ji lygi 0, , arba 1/ , arba Taigi K H2 O = [H+ ] [OH ] = Distiliuotame vandenyje vandenilio jonų koncentracija yra lygi hidroksilo jonų koncentracijai. Kadangi [H + ] = [OH ], tai po pakeitimo lygtis bus [H + ] [H + ] = [H + ] 2 = Ištraukus šaknį, [H + ] = 10 7 Kitaip tariant, vandenilio jonų koncentracija vandenyje yra lygi 0, , arba g/l. Toks išraiškos būdas yra sudėtingas ir sunkiai išmatuojamas metais S. P. L. Sorensenas pasiūlė vandenilio jonų koncentraciją skysčiuose išreikšti neigia- 45
47 mu vandenilio jonų koncentracijos logaritmu ir vadinti vandenilio jonų jėga ph (angl. p power). Taigi ph = lg 10 [H + ]. Distiliuoto vandens ph yra 7,0. Kai ph yra lygi 7,0, tirpalo reakcija yra neutrali, ir tai atitinka vandenilio jonų koncentraciją 100 nmol/l. Visi tirpalai, kai ph reikšmės didesnės už 7,0, yra šarminės reakcijos, o mažesnės už 7,0 rūgštinės. Kai ph yra 7,4, vandenilio jonų koncentracija yra lygi 40 nmol/l. Esant reikšmėms, didesnėms už 120 nmol/l ar mažesnėms už 20 nmol/l, gyvybė nebegalima žmogus miršta. Vandenilio ir hidroksilo jonų koncentracijos santykis priklauso nuo medžiagų apykaitos intensyvumo, bet kraujo ph norma svyruoja nuo 7,35 iki 7,45, optimali ph reikšmė 7,4. Ribinės ph reikšmės yra 6,9 ir 7,7. Didesni nuokrypiai sukelia įvairius apykaitos sutrikimus, o kraujo ph < 6,8 ir >8,0 yra nesuderinama su gyvybe. Kitų skysčių ph skiriasi nuo kraujo, taip pat skiriasi arterinio ir veninio kraujo ph: ląstelinio skysčio ph yra 6,8 7,0, o tarpląstelinio 7,4; arterinio kraujo ph yra 7,4, veninio 7,35, eritrocitų ph yra 7,19±0,02. Vandenilio jonų koncentracija yra labai svarbi konstanta, kuri lemia apykaitos procesų visavertiškumą. Ją palaiko efektyviosios vandenilio jonų koncentracijos pastovumą garantuojančios sistemos. Šios sistemos turi šalinti vandenilio jonų perteklių arba juos sulaikyti. Rūgščių ir šarmų pusiausvyrą palaiko: buferinės sistemos, kurios greitai išlygina pusiausvyrą; fiziologinės organizmo sistemos: tai rūgščių ir šarmų pusiausvyros palaikymas veikiant plaučiams, inkstams, kepenims, prakaito liaukoms. Or g a n i z m o r ū g š č i ų ir ša r m ų pu s i a u s v y r o s palaikymo mechanizmai Buferinės sistemos Buferiniai tirpalai suriša patekusias rūgštinės ar šarminės reakcijos medžiagas ir tokiu būdu neleidžia kisti ph. Vandenilio jonai iš organizmo nėra pašalinami, buferiniai tirpalai tik sugeria vandenilio jonų perteklių, panašiai kaip kempinė sugeria vandenį. Toks protonų sugėrimas tai tik laikinas vandenilio jonų perteklinio kiekio sumažinimas organizme. Galiausiai jie yra pašalinami per inkstus. Buferinę sistemą sudaro silpnos rūgštys su jų pačių druskomis. Silpnų rūgščių anijonai, kaip karbonato (HCO 3 ), fosfato (HPO 4 2 ), taip pat baltymai, ypač hemoglobinas, suriša protonus (H + ) ir pasigamina silpnos, blogai disocijuojančiosios rūgštys. Taigi svarbiausios buferinės sistemos yra rūgščiųjų karbonatų, fosfatinė, baltyminė, hemoglobino. Rūgščiųjų karbonatų buferinė sistema:. Ją sudaro angliarūgštė (H 2 CO 3 ) ir natrio rūgštusis karbonatas (NaHCO 3 ) kraujo plazmoje ar kalio rūgštu- 46
48 Rūgščių ir šarmų pusiausvyra... sis karbonatas (KHCO 3 ) ląstelėse. Abi šios medžiagos turi tą patį rūgščiojo karbonato joną HCO 3. Daugiau šių jonų atsipalaiduoja disocijuojant NaHCO 3. Ši buferinė sistema unikali tuo, kad angliarūgštė gali disocijuoti į vandenį ir anglies dioksidą, kuris yra iškvepiamas. Reakcijos pavyzdys: HCl + NaHCO 3 NaCl + H 2 CO 3 H 2 CO 3 Karboanhidrazė Iškvepiamas CO 2 + H 2 O Vandenilio jonų sąveika su rūgščiaisiais karbonatais, kurių koncentracija neląsteliniame skystyje yra didelė 24 mmol/l, yra greita: ji trunka per 30 sekundžių ir jos daliai tenka ape 10% viso buferinio kraujo imlumo. Bet angliarūgštės skilimas į anglies dioksidą ir vandenį yra palyginti lėtas procesas. Šią reakciją katalizuoja fermentas karboanhidrazė jos daugiausia yra eritrocituose ir inkstuose. Fosfatinė buferinė sistema. Ją sudaro natrio dihidrofosfatas ir natrio hidrofosfatas:. Reakcijų pavyzdžiai: OH 2 + H 2 PO 4 HPO 4 + H 2 O; H HPO 4 H 2 PO 4. Fosfatinei buferinei sistemai tenka apie 1% bendrojo kraujo buferinio imlumo. Baltyminė buferinė sistema. Baltymai, kaip amfoteriniai junginiai, turintys amino ir karboksilo grupių, gali reaguoti ir kaip šarmai, ir kaip rūgštys. Hemoglobino buferinė sistema. Ją sudaro oksihemoglobinas ir hemoglobinas:. Hemoglobinas (Hb) 70 kartų geriau suriša vandenilio jonus negu oksihemoglobinas (HbO 2 ). Nuo hemoglobino buferinės sistemos 80% priklauso ph pastovumas. Ląstelėse (eritrocituose) svarbesnė yra hemoglobino buferinė sistema, o antroje vietoje pagal svarbą yra rūgščiųjų karbonatų buferinė sistema. Kraujo plazmoje atvirkščiai: svarbesnė yra rūgščiųjų karbonatų sistema, o baltyminė buferinė sistema mažiau reikšminga. Rū g š č i ų ir ša r m ų pu s i a u s v y r o s pa l a i k y m a s buferinėmis sistemomis Rūgščiųjų karbonatų buferinė sistema yra viena stipriausiai palaikančių rūgščių ir šarmų pusiausvyrą organizmo sistemų. Ši pusiausvyra sutrinka dėl anglies dioksido (CO 2 ) pertekliaus ar nepakankamo jo šalinimo per plaučius. 47
49 Anglies dioksido koncentracija tirpale yra proporcinga jo daliniam slėgiui. Normaliai dalinis CO 2 slėgis (pco 2 ) yra 40 mmhg ir atitinka 1,2 mmol/l ištirpusio CO 2. Per parą susidaro mmol CO 2, kurio apie 0,1% ištirpsta, ir susidaro angliarūgštė H 2 CO 3. Jai disocijuojant atsiranda H + perteklius. Kai CO 2 išskiriamas per plaučius, šie jonai nesikaupia. Vertinant rūgščių ir šarmų pusiausvyros būklę pagal rūgščiųjų karbonatų sistemos komponentus, prisimintina rūgščiojo karbonato su angliarūgšte pusiausvyra: H 2 O + CO 2 H 2 CO 3 H + + HCO 3 Taigi [H + ] + [HCO 3 ] [H 2 CO 3 ] ir tada [H + ] = ; čia K angliarūgštės disociacijos konstanta. Angliarūgštės komponentas yra susijęs su ištirpusiu anglies dioksidu. Ištirpęs CO 2 kiekis yra proporcingas daliniam CO 2 slėgiui. Taigi [CO 2 ] tirpale = spco 2 ; čia s yra dujų tirpumas vandenyje, p dalinis slėgis. [H 2 CO 3 ] formulėje gali būti pakeistas pco 2. Taigi vertinant rūgščių ir šarmų pusiausvyros sutrikimus galima remtis tuo, kad [H + ] yra proporcinga. Kitaip tariant, vandenilio jonų koncentracija kraujyje svyruoja keičiantis rūgščiojo karbonato koncentracijai ir pco 2. Kai ph 7,4, santykis ; vadinasi, HCO 3 koncentracija 20 kartų viršija CO 2 koncentraciją plazmoje. Iš tikrųjų H 2 CO 3 koncentracija plazmoje yra 1,2 mmol/l, o HCO 3 24 mmol/l. Šios sistemos buferinio veikimo mechanizmas remiasi tuo, kad išsiskyrus į kraują dideliam rūgščiųjų produktų kiekiui, vandenilio jonai rišasi su rūgščiojo karbonato anijonais, susidaro silpnai disocijuojanti angliarūgštė. Pastaroji skyla į CO 2 + H 2 O; CO 2 šalinamas per plaučius ir reakcija pasistūmėja į kairę pusę: CO 2 + H 2 O = H 2 CO 3 = H + + HCO 3. Todėl sumažėja H + ir HCO 3 jonų koncentracija. Kompensacijos atveju turi gerai dirbti plaučiai. Jei kraujyje padaugėja hidroksilo jonų, tai jie jungiasi su silpna angliarūgšte: susidaro H 2 O ir rūgščiojo karbonato anijonai. Taip nenukrypstama į rūgštinę ar šarminę pusę. Apibendrinant reikia pabrėžti, kad jei visos kitos organizmo terpės sudedamosios dalys išlieka pastovios: tokį pat poveikį turės vandenilio jonų pagausinimas, rūgščiųjų karbonatų pašalinimas ar pco 2 didėjimas visais atvejais [H + ] didės; 48
50 Rūgščių ir šarmų pusiausvyra... šalinant vandenilio jonus, gausinant rūgščiųjų karbonatų ir sumažinus pco 2, [H + ] mažės. [H + ] kraujyje yra 40 nmol/l ir ją palaiko plaučių bei inkstų veikla. Panašus veikimo mechanizmas būdingas ir kitai fosfatinei buferinei sistemai. Rūgštusis komponentas čia yra natrio dihidrofosfatas (NaH 2 PO 4 ), o šarminis natrio hidrofosfatas (Na 2 HPO 4 ). Kai kraujo ph yra 7,4, šių fosfatų (NaH 2 PO 4 : Na 2 HPO 4 ) molinių koncentracijų santykis yra 4: 1. Bendras jų jonas yra HPO 2 4. Fosfatinė buferinė sistema yra susijusi su karbonatine, nes turi bendrą rodiklį vandenilio jonų koncentraciją. Kraujyje fosfatų yra mažiau negu karbonatų, todėl fosfatinės buferinės sistemos imlumas (talpa) mažesnis negu rūgščiosios karbonatinės buferinės sistemos. Buferinėms sistemoms priklauso ir baltymai. Pati stipriausia kraujyje hemoglobino buferinė sistema. Kraujo baltymai turi ir rūgštinių, ir šarminių radikalų, todėl ši sistema veikia priklausomai nuo terpės ph. Esant ph nukrypimui į šarminę pusę, baltymas veiks kaip rūgštis, susidarant druskai. Didėjant ph daugėja druskų formos baltymų, o mažėjant ph daugiau baltymų yra rūgščių formos. Hemoglobino dalyvavimas vandenilio jonų koncentracijos reguliavimo mechanizme susijęs su jo funkcija pernešti deguonį (O 2 ) ir anglies dioksidą (CO 2 ). Hemoglobino grupių disociacijos konstanta keičiasi pagal jo įsotinimą O 2. Deguonies įsotintas hemoglobinas tampa stipresne rūgštimi, ir tada daugiau vandenilio jonų pereis į tirpalą. Atidavęs deguonį hemoglobinas tampa silpnesne rūgštimi, padidėja galimybė surišti vandenilio jonus. Didžiojo kraujo apytakos rato periferiniuose kapiliaruose hemoglobinas atiduoda O 2 į audinius. Tuo metu į eritrocitus patenka medžiagų apykaitos produktas CO 2. Veikiant karboanhidrazei, CO 2 jungiasi su H 2 O ir susidaro H 2 CO 3. Jai disocijuojant, perteklinis H + jungiasi su hemoglobinu, o besikaupiantys HCO 3 jonai iš eritrocitų pereina į plazmą. Kaip pakaitalas šiems jonams, į eritrocitus patenka chloridų anijonai, kuriems eritrocito membrana santykinai pralaidi, o natrio jonai lieka plazmoje. Tada kraujo plazmoje padidėja natrio rūgščiojo karbonato koncentracija. Taigi, rūgščiųjų karbonatų buferinė sistema glaudžiai susijusi su hemoglobino. Kiekviena buferinė sistema turi savo išteklius. Patekusios į plaučių kapiliarus kraujo buferinės sistemos atsiskiria nuo rūgštinių ekvivalentų išsiskiriant CO 2. Čia svarbu ir hemoglobino virtimas oksihemoglobinu. Oksihemoglobinas, tapęs stipresne rūgštimi, išstumia H 2 CO 3 iš kraujo rūgščiųjų karbonatų. CO 2 iškvepiamas su oru. Per parą su oru įkvepiama apie 600 litrų O 2 ir išsiskiria apie 480 litrų CO 2. Apibendrinant reikia pabrėžti, kad jei visos kitos organizmo terpės sudedamosios dalys išlieka pastovios, tai vandenilio jonų perteklius, rūgščiųjų karbonatų šalinimas ar pco 2 didėjimas sukels tokius pačius padarinius, t. y. [H + ] didės; 49
51 vandenilio jonų šalinimas, rūgščiųjų karbonatų perteklius ar pco 2 mažėjimas visi šie veiksniai mažins [H + ]. Visi buferinių tirpalų sujungti vandenilio jonai turi būti iš organizmo pašalinti per inkstus ir tokiu būdu papildytas šių tirpalų (rūgščiųjų karbonatų) kiekis. Rū g š č i ų ir ša r m ų pu s i a u s v y r o s pa l a i k y m a s fiziologinėmis organizmo sistemomis Plaučių funkcija. Be buferinės sistemos, kitą rūgščių ir šarmų pusiausvyros palaikymo mechanizmų grupę sudaro organų plaučių, inkstų, prakaito liaukų, kepenų veikla. Nors plaučiai yra svarbūs rūgščių ir šarmų pusiausvyrai palaikyti, tam reikia daugiau laiko negu kraujo buferinėms sistemoms: kad išsilygintų vandenilio jonų koncentracija, reikia 1 3 min. plaučių darbo, o rūgščiųjų karbonatų buferinė sistema tai atlieka per 30 sekundžių. Vis dėlto kvėpavimo mechanizmo svarba yra ta, kad didindami išskiriamos į aplinką angliarūgštės (H 2 CO 3 ) kiekį, plaučiai greitai kompensuoja polinkį į acidozę. Sveiko žmogaus organizme arterinio kraujo pco 2 palaikomas mmhg (4,66 5,99 kpa) lygio. Ventiliaciją reguliuoja kvėpavimo centras, kuris yra labai jautrus ph ir pco 2 pokyčiams. pco 2 padidėjimas ir ph nuokrypis į rūgščiąją pusę didina plaučių ventiliaciją ir skatina H 2 CO 3 šalinimą. Dėl to buferinė rūgščiųjų karbonatų sistema ir vandenilio jonų koncentracija sunormalėja. Esant kvėpavimo organų funkcijos sutrikimams (plaučių edema, pneumonija ir kt.), blogėja plaučių ventiliacija, taip pat dujų difuzija ir susidaręs CO 2 negali būti pašalintas per plaučius. Kraujyje susidaro daug H 2 CO 3 ir terpė rūgštėja. Ši acidozė yra respiracinė, nes susijusi su per dideliu H 2 CO 3 susikaupimu. Tokia respiracinė acidozė kompensuojama per inkstus išskiriant perteklinį vandenilio ir chloro jonų kiekį, taip pat sulaikant (didėja reabsorbcija) HCO 3 jonus (NaHCO 3 forma). Sergant kai kuriomis ligomis, kai yra dirginamas kvėpavimo centras (pvz., galvos trauma, kraujo išsiliejimas į smegenis, kepenų koma, intoksikacija salicilatais ir kt.), vystosi hiperventiliacija. Ilgalaikis perteklinis CO 2 išskyrimas padidina H + išskyrimą ir surišimą, šių jonų koncentracija mažėja ir ph pasistūmėja į šarminę pusę. Tai respiracinė alkalozė. Būklė, kai per daug susikaupia nelakiųjų rūgščių ar bazių, vadinama metaboline acidoze ar alkaloze. Inkstų veikla yra labai svarbi reguliuojant ir palaikant pastovią vandenilio jonų koncentraciją. Šiame reguliavimo mechanizme inkstai veikia lėčiau negu plaučiai. Kad atsitaisytų sutrikęs buferinių sistemų komponentų santykis, reikia, kad inkstai dirbtų valandų. Inkstai yra svarbiausia sistema, reguliuojanti H + išsiskyrimą ir palaikanti bazių kiekį: per parą inkstai išskiria 8 34 mmol vandenilio jonų titruojamų rūgščių (H 2 SO 4 ir H 3 PO 4 ) pavidalu, mmol vandenilio jonų NH
52 Rūgščių ir šarmų pusiausvyra... pavidalu ir tik nedidelį kiekį pačių vandenilio jonų pavidalu. Inkstai negali išskirti rūgštesnio negu ph = 4 šlapimo. Be to, inkstai išskiria ir HCO 3. Svarbiausias mechanizmas, palaikantis vandenilio jonų koncentraciją dalyvaujant inkstų kanalėlių ląstelėms, yra natrio jonų reabsorbcija ir vandenilio jonų sekrecija. Šis procesas vyksta keliais etapais. Pirmasis tai natrio jonų reabsorbcija natrio dihidrofosfatui NaH 2 PO 4 virstant natrio hidrofosfatu Na 2 HPO 4. Inkstų filtratas turi daug druskų, taip pat fosfatų. Tačiau Na 2 HPO 4 mažėja, kai pirminis šlapimas teka kanalėliais. Todėl kraujyje NaH 2 PO 4 santykis su Na 2 HPO 4 yra 1 : 4, o glomerulų filtrate atvirkščiai 9 : 1; distaliniuose inkstų kanalėliuose esančiame šlapime šis santykis jau yra 50 : 1. Tai įvyksta dėl pasirenkamosios natrio jonų reabsorbcijos. Kaip pakaitalą į kanalėlio spindį inkstai išskiria vandenilio jonų. Taigi didelė Na 2 HPO 4 dalis virsta NaH 2 PO 4 ir fosfatai išsiskiria su šlapimu. Kanalėlio ląstelėse iš H 2 CO 3 susidaro rūgštusis karbonatas (HCO 3 ), dėl to kraujyje padidėja rūgščiųjų karbonatų koncentracija. Kitas biocheminis procesas, dėl kurio organizme sulaikomi natrio jonai ir pašalinamas vandenilio jonų perteklius esant acidemijai, yra rūgščiųjų karbonatų virtimas angliarūgšte kanalėlių spindyje. Kanalėlių ląstelėse, katalizuojant karboanhidrazei, vyksta reakcija H 2 O + CO 2 H 2 CO 3. Vandenilio jonai, susidarę disocijuojant H 2 CO 3, išsiskiria į kanalėlio spindį ir ten jungiasi su rūgščiojo karbonato anijonais, o ekvivalentiškas šiam kiekiui natrio jonų kiekis grįžta į kanalėlių ląsteles. Spindyje susidariusi H 2 CO 3 lengvai skyla į CO 2 + H 2 O ir pasišalina iš organizmo. Dar vienas natrio jonų sulaikymo organizme būdas tai amoniako susidarymas inkstuose ir jo panaudojimas neutralizacijai ir rūgščių ekvivalentų šalinimui su šlapimu. Amoniako šaltinis yra aminorūgšties glutamino (Gln) deamininimas į glutamo rūgštį (Glu): Inkstų glutaminazė Gln Glu H 2 O NH 3 H + NH 4 + Susidaręs amoniakas lengvai patenka į kanalėlių spindį, kur jungiasi su vandenilio jonais ir virsta lėtai pro membranas prasiskverbiančiu amonio jonu NH 4 +. (Esant acidozei, amonio druskų šalinama apie 10 kartų daugiau.) Pastarasis nepraeina kanalėlio ląstelių sienelės ir nesugrįžta į organizmą. Taigi, kad vyktų efektyvi amonio jonų ekskrecija, būtina ne tik glutaminazės, bet ir karboanhidrazės skaidomoji veikla, kuriai katalizuojant susidaro angliarūgštė. 51
53 Apibendrinant reikia pasakyti, kad vandenilio jonų koncentracijos šlapime santykis su jų koncentracija kraujyje gali siekti 800 : 1 toks didelis yra inkstų pajėgumas šalinti šiuos jonus iš organizmo. Procesas dar sustiprėja, kai šie jonai organizme pradeda kauptis. Vandenilio jonų, kurie keičiami į natrio jonus, sekrecijos greitis priklauso nuo H 2 CO 3 koncentracijos tarpląsteliniame skystyje. Taigi inkstų kanalėlių sistemoje vienu metu veikia vandens ir druskų bei rūgščių ir šarmų pusiausvyros palaikymo mechanizmai. Tai vieno proceso dvi pusės: natrio jonų sulaikymas organizme skatina vandenilio jonų koncentracijos padidėjimą kraujyje; pastarųjų koncentracijos sumažėjimas kraujyje gali apriboti natrio jonų reabsorbciją inkstuose. Dažniausiai šlapimo ph svyruoja nuo 5,5 iki 7,5 (gyvybei grėsmingos ph<5,5 4,5 ir ph >7,5 8,5). Kepenų vaidmenį palaikant pastovią rūgščių ir šarmų pusiausvyrą organizme galima apibūdinti taip: 1. Kepenys yra gausiai aprūpinamos krauju ir yra atitekančio iš žarnyno kraujo kelyje. Jose iki galutinių medžiagų apykaitos produktų (H 2 O ir CO 2 ) yra oksiduojamos įvairios medžiagos, pvz., organinės rūgštys. 2. Kepenų ląstelėse iš smegenų, raumenų amoniako yra sintetinamas šlapalas CO(NH 2 ) 2. Šlapalas, jau neutrali medžiaga, patenka į bendrąją kraujo apytaką ir išskiriamas su šlapimu. 3. Kepenims būdinga išskiriamoji funkcija, todėl susikaupę pertekliniai rūgštiniai ar šarminiai apykaitos produktai gali būti su tulžimi išskiriami į virškinamąjį traktą. Prakaito liaukos taip pat dalyvauja rūgščių ir šarmų pusiausvyros palaikymo procese, nes prakaito ph kinta pagal kraujo ph. Taigi, kraujui rūgštėjant, skirsis ir rūgštesnės reakcijos prakaitas. Virškinamojo trakto svarbą rūgščių ir šarmų pusiausvyros reguliavimui rodo jau tai, kad dažnai vemiant ir netenkant daug skrandžio turinio, kartu su juo pasišalina vandenilio, chloridų ir kalio jonai. Dėl to vystosi metabolinė alkalozė. Rūgščių ir šarmų pusiausvyros palaikymo svarba Jau vien tai, kaip organizme gali išlikti pastovus skysčių ph, rodo, kad šis rodiklis yra labai svarbus. Nuo organizmo skysčių ph priklauso baltymų koloidinė būklė: terpei rūgštėjant koloidiniai tirpalai darosi ne tokie pastovūs ir gali iškristi nuosėdomis; hemoglobino gebėjimas pernešti O 2 : kraujui rūgštėjant jis mažėja; ląstelių membranų ir kraujo kapiliarų pralaidumas: terpei rūgštėjant jis didėja; fermentų aktyvumas: kadangi kiekvienam fermentui būdingas optimalus veikimo ph, tai, pakitus terpės rūgštingumui, pakinta fermentų katalizuojamų reakcijų intensyvumas, kartu sutrinka procesų pusiausvyra, būdinga sveikam organizmui. 52
54 Rūgščių ir šarmų pusiausvyra... Vaizdą apie kraujo buferinių sistemų pajėgumą galima susidaryti iš šių faktų: norint tiek pat pašarminti kraują ir distiliuotą vandenį, į kraują reikia įdėti kartų daugiau šarmų negu į tokį pat kiekį distiliuoto vandens. Dar sunkiau kraują parūgštinti: į jį reikia įdėti apie 327 kartus daugiau rūgščių negu į tokį pat kiekį distiliuoto vandens. Vadinasi, parūgštėjimo kraujas sugeba sėkmingiau išvengti negu pašarmėjimo. Taigi rūgščių perteklius organizme susidaro dažniau, negu per didelis šarminių medžiagų kiekis. Rūgščių ir šarmų pusiausvyros tyrimas Rūgščių ir šarmų pusiausvyros sutrikimams nustatyti gali būti tiriamas arterinis, veninis ar iš kapiliarų paimtas kraujas. Veninio kraujo tyrimai ne tokie stabilūs kaip arterinio. Kapiliarinio kraujo tyrimas artimesnis arterinio kraujo tyrimui. Kad veninio kraujo tyrimo rezultatai būtų kuo artimesni arterinio kraujo tyrimo rezultatams, paciento ranka prieš venos punkciją turi būti šildoma 20 minučių 45 C temperatūroje. Imant veninį kraują stazė (užveržimas timpa) turi būti kuo trumpesnė. Imant kapiliarinį kraują, oda turi būti šilta ir prie kraujo neprieiti oras. Ilgai laikomų ėminių ph mažėja, o pco 2 didėja. Kapiliarinis kraujas imamas į 50 µl stiklinius kapiliarus su heparinu iš lašo, neleidžiant jam pasklisti ant odos. Hemolizavęs ėminys netiriamas (gramas hemoglobino šimte mililitrų plazmos ph sumažina šimtąja dalimi). Tačiau informatyviausias yra vandenilio jonų koncentracijos ir pco 2 matavimas tiesiogiai arteriniame kraujyje. Rūgščių ir šarmų pusiausvyra yra apibūdinama keliais dydžiais (5 lentelė). Integralus rodiklis yra kraujo ph. Gaunami kiti dydžiai: dalinis CO 2 slėgis pco 2, tikrųjų rūgščiųjų karbonatų (bikarbonatų, angl. actual bicarbonate, AB) koncentracija, standartinių rūgščiųjų karbonatų (angl. standard bicarbonate, SB) koncentracija, visų bazinės reakcijos medžiagų suma kraujyje (angl. buffer base, BB), santykinė bazių stoka ar perteklius (angl. base excess, BE). Rūgčių ir šarmų pusiausvyros sutrikimams nustatyti dažniausiai naudojami analizatoriai, elektrodais tiesiogiai matuojantys ph ir pco 2, po to Sigaardo ir Anderseno nomograma apskaičiuojami ir išvestiniai dydžiai. Pagrindiniai laboratoriniai rūgščių ir šarmų pusiausvyros sutrikimo rodikliai yra trys: ph, pco 2 ir BE. Atsižvelgiant į ph dydį, skiriamos trys būklės: normali, kai ph = 7,4, acidozė, kai ph < 7,4, ir alkalozė, kai ph > 7,4. ph poslinkiai < 6,8 ir > 8,0 yra pavojingi gyvybei. Acidozės ar alkalozės mechanizmą metabolinį ar respiracinį rodo pco 2 ir BE pokyčiai. 53
55 5 lentelė. Svarbiausi rūgščių ir šarmų pusiausvyros rodikliai Rodiklis Pagrindinė charakteristika Normos ribos ph Tirpalo reakcija 7,35 7,45 Vidutinis dydis 7,4 pco 2 Dalinis CO 2 slėgis. Esant normaliam CO 2 kiekiui arteriniame kraujyje, pco 2 = 40 mmhg ir atitinka 1,2 mmol/l ištirpusio CO 2. pco 2 nuokrypis į dešinę (>40 mmhg) rodo jo susikaupimą kraujyje (respiracinė acidozė); nuokrypis į kairę (<40 mmhg) nepakankamą CO 2 kiekį kraujyje (respiracinė alkalozė). Vyrų mmhg Moterų mmhg 4,66 5,99 kpa 40 mmhg 5,32 kpa po 2 Dalinis deguonies slėgis mmhg AB Tikrieji kraujo rūgštieji karbonatai: HCO 3 - koncentracija tikrajame (paimtame iš konkretaus ligonio esamomis aplinkos sąlygomis) kraujyje mmol/l 24,5 mmol/l SB Standartiniai rūgštieji karbonatai tie patys rūgštieji karbonatai (HCO 3 ) paimtame ligonio kraujyje, bet laikomame standartinėmis sąlygomis, t. y. dirbtinėje terpėje, kurioje pco 2 = 40 mmhg, o oksihemoglobino kiekis HbO 2 = 100%, esant 37 C temperatūrai. 21,8 26,9 mmol/l 24 mmol/l! BB BE Visų buferinių kraujo sistemų bazių suma, t. y. rūgščiųjų karbonatų, fosfatinės, baltymų ir hemoglobino sistemų šarminiai komponentai Bazių stoka ar perteklius: tai buferinių kraujo bazių kiekio pokytis, palyginti su normalia konkrečiam ligoniui NBB. NBB ta pati visų buferinių sistemų bazinių komponentų suma paimtame ligonio kraujyje, bet dirbtinėmis standartinėmis sąlygomis (ph = 7,38; pco 2 = = 40 mmhg, 37 C). Šią priklausomybę galima išreikšti formule BE = BB NBB. Taigi BE rodo, kiek mmol/l NaHCO 3 reikia suleisti į organizmą (arba santykinai iš jo pašalinti), kad ph taptų 7,38, esant 37 C temperatūrai. Teigiama BE reikšmė rodo, kad yra bazių perteklius (ar rūgščių stoka), neigiama kad yra bazių stoka (arba rūgščių perteklius). kpa = mmhg 0,133; mmhg = kpa 7,502. Rūgščių ir šarmų pusiausvyros sutrikimai mmol/l 50 mmol/l Rūgščių ir šarmų pusiausvyra sutrinka, kai organizmo kompensaciniai mechanizmai nesugeba palaikyti pastovios vandenilio jonų koncentracijos. Galimos dvi priešingos būklės: acidozė ir alkalozė. Acidozė ir alkalozė yra klinikiniai terminai, apibūdinantys pirminį rūgščių ar šarmų pusiausvyros sutrikimą. Acidozė rodo vandenilio jonų koncentracijos padidėjimą virš normos tada kraujo ph mažėja. Kai ph < 6,8, ištinka mirtis. Mažėjant vandenilio jonų koncen- 54
56 Rūgščių ir šarmų pusiausvyra... tracijai, vystosi alkalozė kraujo ph didėja. Viršutinė su gyvybe suderinama ph riba yra 8. Klinikoje tokių reikšmių nenustatoma. Acidozė ir alkalozė gali išsivystyti dėl įvairių veiksnių, kurie sutrikdo rūgščių ir šarmų pusiausvyrą: CO 2 išskyrimo iš organizmo sutrikimas, suintensyvėjusi rūgščiųjų produktų gamyba audiniuose ir sutrikęs bazių išskyrimas su šlapimu bei kitais biologiniais skysčiais, šalinimo organų ligos. Priklausomai nuo mechanizmo, gali būti metabolinė ir respiracinė acidozė ar alkalozė. Metabolinės kilmės rūgščių ir šarmų pusiausvyros sutrikimai yra tiesiogiai susiję su rūgščiųjų karbonatų koncentracijos pokyčiais, o su kvėpavimu susiję rūgščių ir šarmų pusiausvyros sutrikimai tiesiogiai veikia pco 2. Apibendrintai galima sakyti, kad pirminiai rūgščių ir šarmų pusiausvyros sutrikimai gali būti tokie: metabolinė acidozė pirminis sutrikimas dėl rūgščiųjų karbonatų koncentracijos sumažėjimo; metabolinė alkalozė pirminis sutrikimas dėl rūgščiųjų karbonatų koncentracijos padidėjimo; respiracinė acidozė pirminis sutrikimas, susijęs su pco 2 padidėjimu; respiracinė alkalozė pirminis sutrikimas, susijęs su pco 2 sumažėjimu. Kompensacija. Acidozė ar alkalozė nebūtinai išryškėja kraujo ph pokyčiais tai priklauso nuo kompensacinių, pirmiausia inkstų ir plaučių, galimybių. Evoliucijos būdu išsivystė nemažai fiziologinių mechanizmų, kuriais organizmas stengiasi normalizuoti [H + ]. Jei ph pakinta dėl plaučių disfunkcijos, padidėja vandenilio jonų ekskrecija su šlapimu. Tai pirminio kvėpavimo sutrikimo kompensavimas inkstų veikla (lėtas procesas). Metabolinius sutrikimus iš dalies kompensuoja plaučių veikla tai pirminio metabolinio sutrikimo kompensavimas. Šis kompensavimas yra greitas ir efektyvus. Jei kompensacija veiksminga, [H + ] grįžta į normą, nors pco 2 ir [HCO 3 ] dar gali būti labai pakitę. Sakoma, kad rūgščių ir šarmų pusiausvyros sutrikimas yra visiškai kompensuotas. Dažnai kompensacija būna dalinė, ir tada [H + ] nepasiekia rekomenduojamų normos ribų. Rūgščių ir šarmų pusiausvyros sutrikimų kompensacija tai antrinis procesas, šalinantis pirminį sutrikimą ir keičiantis tą sistemą, kuri iš pradžių nebuvo pažeista. Priešingai nei kompensacija, korekcija tai normalizavimas dažniausiai terapinėmis priemonėmis tų komponentų, kurie iš pradžių buvo pakitę. Skiriami trys kompensavimo laipsniai: nekompensuotos būklės, kai neaptinkama kompensacijos požymių; iš dalies kompensuotos būklės, kai į pirminį sutrikimą kaip atsakas atsiranda kompensacinių pokyčių, bet kraujo ph dar nesunormalėjęs; visiškai kompensuotos būklės, kai kraujo ph sunormalėjęs (nors pco 2 ir [HCO 3 ] yra smarkiai pakitę). 55
57 Praktikoje dažniausiai susiduriama su iš dalies kompensuotomis būklėmis. Galimi ir mišrieji sutrikimai, kai juos sukelia dvi nepriklausomos priežastys. Pavyzdžiui, sergant cukriniu diabetu ir metaboline acidoze, dėl smegenų kraujotakos sutrikimo padažnėja kvėpavimas ir išsivysto respiracinė alkalozė. Tuomet tik iš klinikinio vaizdo galima atskirti kompensacinius pokyčius nuo prisidėjusios kitos ligos ar komplikacijos. Pagal eigą skiriamos ūminės būklės, kai reaguoja tik buferinės sistemos, ir stabilizuotosios, kai įsijungia ir kompensaciniai mechanizmai. Dėl kompensacinių mechanizmų inertiškumo plaučiai ir inkstai dar mėgina išlyginti rūgščių ir šarmų pusiausvyros sutrikimą, nors pirminė priežastis jau pašalinta gydant. Tada atsiranda priešingų pirminiams nukrypimų tai hiperkorekcija. Api b e n d r i n i m a s Rūgščių ir šarmų pusiausvyros būklė yra vertinama matuojant [H+ ], [HCO 3 ] ir pco 2, t. y. rūgščiųjų karbonatų sistemos komponentus kraujo plazmoje. Vandenilio jonų pagausinimas, rūgščiųjų karbonatų šalinimas ir pco 2 didėjimas turi tą patį poveikį, kaip ir [H + ] didėjimas. Vandenilio jonų šalinimas, rūgščiųjų karbonatų kiekio didėjimas ir pco 2 mažėjimas sukelia [H + ] mažėjimą. Pirmines piežastis, susijusias su vandenilio jonų gamyba ar šalinimu, atspindi [HCO 3 ]; tai metaboliniai rūgščių ir šarmų pusiausvyros sutrikimai. Pirmines priežastis, susijusias su CO 2 ekskrecija, rodo pco 2 ; tai respiraciniai rūgščių ir šarmų pusiausvyros sutrikimai. Organizme funkcionuoja fiziologinės [H+ ] normalizavimo sistemos. Tai kompensacijos procesas. Išmatuotoji vandenilio jonų koncentracija, esant sutrikusiai rūgščių ir šarmų pusiausvyrai, atspindi pusiausvyrą tarp pirminio sutrikimo ir kompensacijos laipsnio. Rū g š č i ų ir ša r m ų pu s i a u s v y r o s sutrikimai ir jų laboratorinė diagnostika Metabolinė acidozė Metabolinė acidozė išsivysto, kai dėl teigiamo vandenilio jonų balanso organizme besikaupiančių nelakiųjų (organinių ir neorganinių) rūgščių yra daugiau negu bazių. Priežastys: 1) neląsteliniame skystyje kaupiasi stiprios rūgštis: egzogeninės kilmės: druskos ar acto rūgštis, pavyzdžiui, apsinuodijus amonio chloridu (NH 4 Cl); 56
58 Rūgščių ir šarmų pusiausvyra... endogeninės kilmės: ketorūgštys, kai nevisiškai oksiduojami riebalai, pavyzdžiui, sergant cukriniu diabetu, badaujant, sergant paveldimomis medžiagų apykaitos ligomis; pieno rūgštis, kai nevisiškai oksiduojami angliavandeniai, pavyzdžiui, esant hipoksijai ar anoksijai dėl karščiavimo, širdies kraujagyslių sistemos nepakankamumui, po narkozės; fosforo ar sieros rūgštys, esant uremijai. 2) ląsteliniame skystyje sumažėja rūgščiųjų karbonatų: kai daugiau jų išsiskiria per inkstus, pavyzdžiui, esant inkstų kanalėlių acidozei, virškinamojo trakto negalavimams viduriuojant ar esant fistulių (kasos ir žarnų sultyse yra daug rūgščiųjų karbonatų), vartojant šlapimo išsiskyrimą skatinančius vaistus, kurie yra karboanhidrazės inhibitoriai (diakarbas). Klinika. Metabolinės acidozės pradžioje, kai ph < 7,3, būdingas dažnas ir gilus kvėpavimas (Kusmaulio tipo), nes padidėjusi vandenilio jonų koncentracija stimuliuoja kvėpavimo centrą. Taip pat būdingi simpatinės nervų sistemos dirginimo reiškiniai: dažnas širdies plakimas, padidėjęs arterinis kraujospūdis. Kai ph < 7,25, sukeliamas mažojo kraujo apytakos rato kraujagyslių spazmas vystosi plaučių hipertenzija. ph nukritus mažiau kaip 7,2, pradeda spazmuoti inkstų glomerulų arteriolės, blogėti inotropinė širdies funkcija, dėl to mažėja minutinis širdies tūris, kraujospūdis, sutrinka širdies ritmas. Kai ph < 7,1, sutrikdoma smegenų kraujotaka, dėl to trinka sąmonė, vystosi koma. Metabolinei acidozei būdingas padidėjęs (dėl padidėjusio membranų pralaidumo) leukocitų skaičius (leukocitozė), kraujo plazmoje daugėja kalio jonų, šlapimo reakcija būna rūgšti (ph < 5,0). Laboratorinė diagnostika. Svarbiausi rodikliai, būdingi metabolinei acidozei, yra šie: kraujo ph < 7,4; BE < 3,0 mmol/l; pco 2 sumažėjęs ar normalus. Kompensacija vyksta per plaučius ir per inkstus. Nelakiųjų rūgščių perteklių dėl metabolinės acidozės organizmas bando kompensuoti mažindamas CO 2 kiekį (hipokapnija), t. y. vystosi respiracinė alkalozė. Kad dėl respiracinio mechanizmo ūminė būklė būtų kompensuojama ir stabilizuotųsi, reikia valandų, per kurias kvėpavimo centro jautrumas anglies dioksidui didėja, nusistovi naujas, jau žemesnio lygio, pco 2. Ūminiu metabolinės acidozės tarpsniu kraujo ph labai sumažėja, vėliau, stiprėjant kompensavimo mechanizmui, sunormalėja, o pco 2 kiekio kaita būna atvirkščia krinta tol, kol išsivysto maksimalaus kompensavimo stadija. Jei būklė dekompensuotoji, pradeda staigiai mažėti kraujo ph. Korekcija. Gydymas priklauso nuo šios acidozės priežasties. Būtina papildyti sumažėjusias rūgščiųjų karbonatų atsargas, mažinti hiperkalemiją. Dažniausiai vartojamas natrio rūgštusis karbonatas, rečiau natrio laktatas. Visos šios medžiagos yra vandenilio jonų akceptoriai ir su juo sudaro greitai iš organizmo išsiskiriančius junginius. 57
59 Metabolinė alkalozė Metabolinė alkalozė išsivysto dėl neigiamo vandenilio jonų balanso susidarius bazių pertekliui, lyginant su nelakiosiomis rūgštimis. Priežastys: 1) rūgščiųjų karbonato (HCO 3 ) susikaupimas neląsteliniame skystyje dėl: padidėjusio jų patekimo į organizmą: išgėrus ar sušvirkštus į veną natrio rūgščiojo karbonato, laktato ar acetato; susidarius organinių rūgščių (pieno, citrinų) pertekliui: dėl patekusio maisto komponentų ar metabolinių procesų produktų oksidacijos; 2) neląsteliniame skystyje vandenilio jonų sumažėja netenkant daug druskos rūgšties vemiant, pvz., nėštumo metu; 3) padidėjus vandenilio jonų išsiskyrimui per inkstus, pvz., esant kalio stokai: vartojant diuretikus, perdozavus steroidinių vaistų, dėl hiperkorticizmo ar netenkant kalio per virškinamąjį traktą. Klinika. Pagrindinis simptomas yra padidėjęs nervų ir raumenų jaudrumas dėl sumažėjusio jonizuotojo kalcio (Ca 2+ ) kiekio kraujyje: padidėja skersaruožių raumenų tonusas, atsiranda parastezijos, sustiprėja refleksai, gali būti riešo ir pėdos spazmas, būdinga hipoventiliacija. Kraujo plazmoje sumažėja kalio, natrio, jonizuotojo kalcio, chloridų kiekis. Šlapimo ph > 6,0. Laboratorinė diagnostika. Kraujo ph > 7,4; BE 3,1 mmol/l, pco 2 padidėjęs ar normalus. Kompensavimas vyksta per plaučius ir inkstus. Ūminė būklė trunka val., paskui stabilizuojasi ir kvėpavimo centro jautrumas angliarūgštei sumažėja; dėl to nusistovi aukštesnio lygio pco 2. Taigi metabolinė alkalozė iš dalies kompensuojama respiracine acidoze. Organizmo gebėjimas priešintis metabolinei alkalozei daug silpnesnis negu acidozei. Respiracinė kompensacija yra nereguliari, jos gali iš viso nebūti. Korekcija yra sunki. Šios alkalozės yra lengviau išvengti negu ją gydyti. Parenkant gydymą iš pradžių reikia apskaičiuoti, kiek organizmas stokoja neląstelinio skysčio, kalio, chloridų, ir koreguoti jų stoką. Api b e n d r i n i m a s Esant metabolinei acidozei, vandenilio jonų koncentracija ([H+ ]) kraujyje yra padidėjusi ar normali, bet rūgščiojo karbonato jonų koncentracija ([HCO 3 ]) visada yra sumažėjusi. Dažniausios metabolinės acidozės priežastys yra inkstų ligos, diabetinė ketoacidozė, pieno rūgšties acidozė. Dėl metabolinės alkalozės [H+ ] yra sumažėjusi, o [HCO 3 ] visada yra padidėjusi. Respiracinei kompensacijai yra būdingas padidėjęs pco 2. Dažniausia metabolinės alkalozės priežastis yra užsitesęs vėmimas. 58
60 Rūgščių ir šarmų pusiausvyra... Respiracinė acidozė Respiracinė acidozė išsivysto esant teigiamam vandenilio jonų balansui dėl nepakankamos plaučių ventiliacijos ir nesugebėjimo išskirti visą susidariusią angliarūgštę. Priežastis nepakankama plaučių ventiliacija, kurios priežastys šios: kvėpuojamojo centro depresija, sukelta, pvz., barbitūratų, opiatų ar apsinuodijus etanoliu, kitais nuodais; kvėpavimo takų obstrukcija dėl sekreto ar svetimkūnio; sumažėjęs plaučių kvėpuojamojo paviršiaus plotas sergant pneumonija, plaučių fibroze, esant pneumotoraksui ar hemotoraksui, navikui, plaučių edemai, krūtinės ląstos traumai; sutrikusi difuzija plaučių alveolėse, pvz., esant hialininėms membranoms; nusilpę kvėpavimo raumenys, pvz., esant bulbariniam paralyžiui, hipokalemijai; hipoventiliacija po operacijos, krūtinės ląstos traumos; susidariusios plaučių arterinės-veninės jungtys. Klinika. Iš pradžių ligonis esti neramus, gausiai prakaituoja, padidėja arterinis kraujospūdis. Vėliau temsta ir visiškai išnyksta sąmonė. Ligonis vis gausiau prakaituoja, atsiranda cianozė, sumažėja arterinis kraujospūdis. Išnykus sąmonei, pavyzdžiui, dėl hiperkapninės komos, kuri ištinka, kai pco 2 > mmhg (13,3 26,6 kpa), retėja kvėpavimas, ryškėja cianozė, sutrinka kraujotaka. Nutrūkus kvėpavimui, ligonis gali mirti. Kaip ir sergant metaboline acidoze, būdinga leukocitozė, kurios metu galima hiperkalemija. Šlapimo reakcija rūgšti. Respiracinė acidozė gali būti ūminė ir lėtinė. Ūminė išsivysto per kelias minutes ar valandas. Lėtinė būklė, kuri dažniausiai išsivysto esant lėtinei plautinei širdžiai, gali būti sergant lėtiniu bronchitu, plaučių emfizema. Laboratorinė diagnostika. Kraujo ph <7,4 (esant lėtinei respiracinei acidozei, gali būti ir normalus), pco 2 > 45 mmhg (5,99 kpa), BE yra normalus ar padidėjęs. Pagrindinė kompensacija vyksta per inkstus, kai iš organizmo su šlapimu šalinama daugiau laisvųjų vandenilio jonų ar surištųjų su amoniaku ir į organizmą sugrąžinama rūgščiųjų karbonatų jonų (jie reabsorbuojami NaHCO 3 pavidalu). Respiracinės acidozės pradžia dažnai yra staigi, todėl galimos visos kompensavimo fazės. Buferinis mechanizmas reaguoja greičiausiai, ir tam reikia minučių, per kurias labai padidėja kraujo pco 2. Anglies dioksidas yra neutralizuojamas baltyminių buferinių sisemų, o susidarę rūgščiojo karbonato jonai iš dalies patenka už ląstelių ribų. Rūgščiųjų karbonatų persiskirstymas tarp kraujo ir tarpląstelinės erdvės lemia tai, kad bazių perteklius tam tikru respiracinės acidozės kompensavimo etapu tampa neigiamas. 59
61 Inkstų funkcijos persitvarkymui reikia laiko, todėl inkstų kompensaciniai mechanizmai ima veikti po 6 18 valandų, o visu pajėgumu po 5 7 parų. Tada inkstai gali maksimaliai šalinti vandenilio jonus, o atitinkamai kraujyje ir tarpląstelinėje erdvėje kaupsis rūgščiojo karbonato jonai. Todėl pastovios respiracinės acidozės fazėje bazių perteklius tampa teigiamas. Korekcija. Svarbiausia yra pašalinti priežastį, sutrikdžiusią kvėpavimą, ir gerinti alveolinę ventiliaciją, t. y. kvėpavimo takų praeinamumą, gydyti plaučių ligas, pvz., plaučių uždegimą. Kartu atliekama intubacija arba tracheostomija ir daroma dirbtinė plaučių ventiliacija. Ji indikuotina, kai pco 2 > 60 mmhg. Kai lėtinės respiracinės acidozės sąlygomis greitai koreguojamas pco 2, organizme lieka šarmų perteklius (metabolinė alkalozė), kuris pašalinamas lėtai. Respiracinė alkalozė Respiracinė alkalozė išsivysto dėl neigiamo vandenilio jonų balanso, kai plaučių ventiliacija būna neadekvačiai didelė, palyginti su angliarūgštės gamyba. Priežastis padidėjusi plaučių ventiliacija. Ji išsivysto: tiesiogiai dirginant kvėpavimo centrą: susijaudinus, sergant organinėmis smegenų ligomis, apsinuodijus salicilatais, dėl amoniako, progesterono poveikio; refleksiškai dirginant periferinius chemoreceptorius (pvz., esant hipoksemijai) ar intratorakalinius receptorius (pvz., sergant plaučių liga); netinkamai atliekant dirbtinę plaučių ventiliaciją. Kaip ir sergant respiracine acidoze, plaučių ventiliacijos pokyčiai pirmiausia paveikia angliarūgštės kiekį kraujyje. Esant ūminei fazei, per kelias minutes pco 2 kraujyje sumažėja, ph padidėja. Tada ima veikti buferinis mechanizmas dalis rūgščiojo karbonato dėl reakcijos su baltymine buferine sistema virsta H 2 CO 3. Skirtingai nuo respiracinės acidozės, alkalozės metu nėra rūgščiojo karbonato jonų persiskirstymo tarp kraujo ir tarpląstelinės erdvės. Todėl ūminei būklei nebūdingas bazių pertekliaus. Sumažėjus pco 2 iki 20 mmhg ir mažiau, spazmuojamos kraujagyslės, ypač centrinių kraujagyslių baseino, todėl silpnėja smegenų kraujotaka. Klinika. Pagrindinis požymis yra gilus ir dažnas alsavimas. Dėl galvos smegenų kraujagyslių spazmų ligoniui gali svaigti galva, sutrikti sąmonė, atsirasti parestezijos, o sumažėjus jonizuotojo kalcio (Ca 2+ ) kiekiui kraujyje tetanija. Dažniausiai kartu sumažėja ir kalio kiekis, o dėl to gali sutrikti širdies ritmas. Šlapimo ph 6,0. Laboratorinė diagnostika. Kraujo ph >7,4; pco 2 < 35 mmhg (4,66 kpa), BE sumažėjęs ar normalus. Pagrindinė kompensacija vyksta per inkstus. Inkstų kompensacinis mechanizmas pradeda veiki po valandų, o visu pajėgumu per kelias dienas. Tada inkstai išskiria šarminį šlapimą, kuriame gausu rūgščiųjų karbonatų. Pastovios alkolozės fazėje, kai kompensavimas maksimalus, ph sunormalėja, bazių pertekliaus nebūna. 60
62 Rūgščių ir šarmų pusiausvyra... Korekcija. Kvėpavimo centras slopinamas vaistais: barbitūratais, opiatais. Mažinama kūno temperatūra antiseptikais ar šaldant, koreguojamas dirbtinės plaučių ventiliacijos režimas. Ligoniui galima duoti pakvėpuoti karbogeno (O 2 95% + CO 2 5%). Jei ištinka traukuliai, į veną švirkščiama kalcio chlorido (CaCl 2, 10% 10,0 ml). Mišriosios būklės Dažnai ligoniui nustatomas daugiau negu vienas rūgščių ir šarmų pusiausvyros sutrikimas, pvz., metabolinė ir respiracinė acidozė sergant lėtiniu bronchitu ar išsivysčius inkstų funkcijos nepakankamumui. Tokiam pacientui padidėja [H + ], o pco 2 ir [HCO 3 ] yra sumažėjęs. Jei dvi būklės viena kitai yra antagonistinės pagal poveikį vandenilio jonų koncentracijai, tai viena jų gali panašėti į atsaką, būdingą kompensaciniam poveikiui. Pavyzdžiui, perdozavus salicilatų, pacientui, sergančiam metaboline acidoze, prisidės respiracinės alkalozės požymiai. Iš pirmo žvilgsnio ši respiracinė alkalozė gali atrodyti kaip kompensacinis atsakas. Įtarus mišrųjį rūgščių ir šarmų pusiausvyros sutrikimą, būtina atidžiai įvertinti klinikinį ligos vaizdą. Api b e n d r i n i m a s Esant respiracinei acidozei, kraujo vandenilio jonų koncentracija dažniausiai yra didelė, bet gali būti ir normali, o pco 2 visada yra padidėjęs. Jei būklė kompensuota, rūgščiojo karbonato jonų koncentracija yra padidėjusi. Ūminė respiracinė acidozė yra būklė, kurią būtina neatidėliotinai gydyti, pirmiausia šalinti ligos priežastį. Inkstų kompensacinis mechanizmas yra lėtas. Respiracinė alkalozė yra reta būklė ir gali išsivystyti dėl mechaninės hiperventiliacijos ar esant isteriniam kvėpavimui. Mišriųjų rūgščių ir šarmų apykaitos sutrikimų interpretacija gali būti sudėtinga, nes vienas iš sutrikimų gali priminti kompensacijos požymius. Todėl diagnozei labai svarbus klinikinis ištyrimas. Laboratoriniai tyrimai bendrasis Anglies dioksidas (CO 2 ) Tiriamoji medžiaga. Arterinis, veninis, kapiliarinis kraujas, plazma (heparinas). Rekomenduojama reikšmė (mmol/l): Arterinio kraujo Veninio kraujo Plazmos (veninio kraujo) Plazmos (kapiliarinio kraujo): naujagimių 13 22, kūdikių ir vaikų 20 28, suaugusiųjų Diagnostinė vertė. Respiracinė acidozė (ypač kompensuotoji) dėl blogos dujų apykaitos (plaučių emfizema, pneumonija, širdies nepakankamumas, cistinė fibrozė) ar kvėpavimo centro 61
63 slopinimo; kvėpavimo organų liga; metabolinė alkalozė, pvz., po gausaus vėmimo esant prievarčio stenozei, gausiai patekus į organizmą šarmų, esant hipokalemijai. Kompensuota respiracinė alkalozė, metabolinė acidozė sergant cukriniu diabetu, esant inkstų kamuolėlių ar kanalėlių funkcijos nepakankamumui, inkstų kanalėlių acidozei ar netenkant šarmų per virškinamąjį traktą; persodinus šlapimtakius į storąją žarną; esant hipotenzijai, dehidratacijai, blogam audinių aprūpinimui krauju. Papildoma informacija. Arterinio ir veninio kraujo sudėtis įvairuoja pagal audinių ar organų, iš kurių imama kraujo, metabolinį aktyvumą. Todėl rekomenduotina tirti arterinį kraują. V: aldosteronas, rūgštieji karbonatai, diuretikai (pvz., etakrino rūgštis, furozemidas, tiazidai), karbenicilinas, gliukokortikoidai. V: amonio chloridas, meticilinas, nitrofurantoinas, tetraciklinas, triamterenas; acidozė vartojant metanolį, paraldehidą; laktinė acidozė vartojant fenforminą, fruktozę. dalinis Anglies dioksido slėgis (pco 2 ) Tiriamoji medžiaga. Arterinis kraujas (heparinizuotas švirkštas). Rekomenduojama reikšmė. Vyrų mmhg, moterų mmhg (visos reikšmės jūros lygyje, dideliame aukštyje yra mažesnės). Veninio kraujo reikšmės 6 7 mmhg didesnės negu arterinio kraujo pco 2 Diagnostinė vertė. Respiracinė acidozė (hiperkapnija): padidėjęs pco 2 įkvepiamame ore (pvz., įkvepiant iškvėptą orą), sumažėjusi alveolių ventiliacija dėl plaučių ir bronchų ligų, svetimkūniai kvėpavimo takuose, alerginė gerklų edema, astminė būklė, lėtinis bronchitas, plaučių tuberkuliozė ar emfizema, lėtinė obstrukcinė plaučių liga, kvėpavimo centro pažeidimas (smegenų navikas, kvėpavimo centro depresija vartojant opiatus, barbitūratus), kvėpavimo nervų ir raumenų pažeidimas (poliomielitas, intoksikacija kurarės nuodais, žymus elektrolitų apykaitos sutrikimas, ūminė protarpinė porfirija, sunki hipotirozė), miopatija, širdies ligos, metabolinė alkalozė esant kompensacinei hipoventiliacijai; pco 2 > 80 mmhg sukelia narkozę. Respiracinė alkalozė (hipokapnija): padidėjusi alveolių ventiliacija dėl dirbtinės ventiliacijos ar kvėpavimo centro skatinimo; pastarąjį poveikį turi hipoksija, salicilatai, susijaudinimo būklė, hipertermija, galvos trauma, pažeidžianti kvėpavimo centrą. Papildoma informacija. Kvėpavimo sutrikimai pirmiausia išryškėja pco 2 pokyčiais, o metabolinius sutrikimus atspindi pakitęs HCO 3. Kraujyje, paimtame pacientui sėdint ar stovint, pco 2 reikšmės yra kiek mažesnės (2 4 mmhg) negu gulint. Skirtumas tarp arterinio ir veninio kraujo pco 2 svyruoja pagal kūno (odos) temperatūrą, stazės trukmę, raumenų aktyvumą. Klaidingų rezultatų priežastis gali būti kraujo laikymas ore ir rūgščiųjų produktų susidarymas vykstant medžiagų apykaitai eritrocituose ir leukocituose. Glikolizė ir oksidacinė apykaita didina pco 2 5 mmhg/val. 37 C temperatūroje ir 0,5 mmhg/val. 2 4 C. pco 2 reikšmės, išmatuotos 37 C temperatūroje, turi būti koreguojamos pagal tikrąją kūno temperatūrą (naudojantis nomograma), nes pco 2 didėja kylant temperatūrai. V: diazepamas, narkotiniai analgetikai. Bazių stoka ar perteklius (BE) Tiriamoji medžiaga. Arterinis kraujas (heparinizuotas švirkštas). Rekomenduojama reikšmė (mmol/l): naujagimių 10 ( 2), kūdikių 7 ( 1) mmol/l, vaikų 4 (+2), suaugusiųjų 2 (+3). Diagnostinė vertė. Metabolinė alkalozė, ūminė respiracinė alkalozė. Metabolinė acidozė, ūminė respiracinė acidozė. 62
64 Rūgščių ir šarmų pusiausvyra... Svarbu nustatyti gydant rūgščių ir šarmų pusiausvyros sutrikimus. Papildoma informacija. Šis rodiklis rodo bazių koncentraciją kraujyje titruojant stipria rūgštimi iki ph 7,4 esant pco 2 40 mmhg 37 C. Bazių perteklius ir buferinių bazių kiekis gali būti apskaičiuotas pagal nomogramą ar išmatuojamas tiesiogiai dujų analizatoriumi. V: diuretikai (pvz., chlortalidonas, etakrino rūgštis, tiazidas), karbenicilinas. V: metoksifluranas. Deguonies dalinis slėgis (po 2 ) Tiriamoji medžiaga. Arterinis kraujas. Rekomenduojama reikšmė mmhg. Diagnostinė vertė. Kvėpavimas deguonies papildytu oru, fiziniai pratimai, smegenų angiomos. Hipoksemija dideliame aukštyje, susilpnėjęs širdies darbas, buvimas anglies monoksido prisotintoje aplinkoje, anestezija, skendimas. Sumažėjusi alveolių dujų apykaita: naujagimių kvėpavimo sutrikimo sindromas, plaučių adenomatozė, limfmazgių karcinomatozė, sarkoidozė, beriliozė, antrinė plaučių hemosiderozė esant mitralinei stenozei; sumažėjęs alveolių kapiliarų membraninis paviršius (pvz., po rezekcijos ar plaučių suspaudimo). Ventiliacijos (perfuzijos) netolygumas: bronchitas, astma, emfizema, bronchektazijos, atelektazė, pneumokoniozė, granulomos, navikai, plaučių infarktas, pneumonija, mukoviscidozė, kvėpavimo takų obstrukcija (pvz., svetimkūniais), krupas, sekreto susilaikymas, šokas. Alveolinė hipoventiliacija Periferinės kilmės: uždusimas, skendimas, griaučių deformacijos (pvz., kifoskoliozė, plokščia krūtinė po traumos), nervų ir raumenų būklė, bloginanti kvėpavimą (pvz., diafragmos nervo paralyžius, traukuliai, ūminis poliomielitas). Centrinės kilmės: kvėpavimo centro slopinimas vaistais (pvz., barbitūratais ar morfinu), po galvos traumos, insulto. Širdies nuosruvis iš dešinės į kairę: intrapulmoninis veninis ir arterinis nuosruvis, įgimta širdies liga. Kartu gali veikti keletas iš aprašytų mechanizmų. Reikšmės < 40 mmhg rodo ryškią hipoksemiją; reikšmės < 20 mmhg dažniausiai yra nesuderinamos su gyvybe. Papildoma informacija. 55 mmhg yra kritinė riba, žemiau kurios staigiai krinta deguonies kiekis. Gydant grynu deguonimi arterinio kraujo po 2 gali padidėti iki 640 mmhg nelygu, koks yra kraujo nuosruvio laipsnis plaučiuose. po 2 reikšmės, išmatuotos 37 C temperatūroje, turi būti koreguotos pagal paciento temperatūrą. V: vaistai, sukeliantys kvėpavimo slopinimą, pvz., barbitūratai, diazepamas, heroinas. ph Tiriamoji medžiaga. Aterinis kraujas (heparinas). Imant kraują nemasažuoti ir nejudinti rankos. Rekomenduojama reikšmė. 7,35 7,45. Diagnostinė vertė. Metabolinė alkalozė (rūgščiųjų karbonatų perteklius). Per didelis šarmų patekimas į organizmą. Skrandžio HCl netekimas ar skrandžio turinio aspiracija. Kalio atsargų išeikvojimas: per virškinamąjį traktą (pvz., lėtinis viduriavimas), per mažas kalio vartojimas (pvz., nervinė anoreksija, leidžiant į organizmą tirpalus, kuriuose trūksta kalio), padidėjusi diurezė, antinksčių steroidų perteklius (pvz., pirminis aldosteronizmas, Kušingo liga) ar ilgalaikis vartojimas; glikogeno kaupimasis, taip pat lėtinė alkalozė, nefropatija netenkant daug kalio. 63
65 Respiracinė alkalozė (sumažėja ištirpusio CO 2 ): isterija; kvėpavimo centro stimuliacija padidėjus intrakranijiniam spaudimui ar pažeidus smegenų kamieną, kai plaučių funkcija normali; kvėpavimo centro stimuliacija esant hipoksijai ir normaliai alveolinei CO 2 difuzijai; karščiavimas, apsinuodijimas salicilatais, per stipri ventiliacija. Metabolinė acidozė (rūgščiųjų karbonatų stoka). Per didelis rūgščių susidarymas: ketozė (pvz., cukrinis diabetas, badavimas, hipertirozė, per didelis riebalų ir per mažas angliavandenių kiekis maiste; po traumos); ląstelių hipoksija (laktinė acidozė). Sumažėjusi H + ekskrecija: inkstų nepakankamumas (prereninis, reninis, postreninis), inkstų kanalėlių acidozė, Fankonio sindomas, įgyta (vaistai, hiperkalcemija), paveldima (cistinozė, Vilsono liga), Adisono liga. Per gausus rūgščių vartojimas: pvz., jonkaitinės dervos, salicilatai, amonio chloridas. Per didelis šarminių organizmo skysčių netekimas: su žarnų turiniu (pvz., viduriavimas, fistulė) su tulžimi (tulžis ir kasos turinys), per inkstus (karboanhidrazės inhibitoriai), antrinis procesas dėl kitų metabolinių sutrikimų (kalio perteklius). Respiracinė acidozė: ūminė dėl sumažėjusios alveolinės ventiliacijos (pvz., emfizema, pneumonija, plaučių edema, bronchokonstrikcija, kvėpavimo centrą slopinantys vaistai); širdies nepakankamumas, lėtinė (daugėjant rūgščiųjų karbonatų) obstrukcinė ar restrikcinė plaučių liga. Papildoma informacija. Suderinamos su gyvybe ph ribos yra 6,8 7,8. Arterinio ir veninio kraujo ph skirtumas yra 0,01 0,03. Jis didesnis esant širdies nepakankamumui, ištikus šokui. Kapiliarinis kraujas yra tinkamas tyrimui vietoj arterinio kraujo. Bet kai susilpnėja širdies darbas, kai sistolinis kraujospūdis <95 mmhg ar kai yra vazokonstrikcija, kapiliarinio kraujo tyrimo rezultatai nepatikimi. Svarbu, kad ėminys neturėtų sąlyčio su oru. Ką tik paimto kraujo ph mažėja 0,04 0,08 ph vnt./val. 37 C temperatūroje ir 0,03 ph vnt./val. 25 C, bet tik 0,008 ph vnt./val. 4 C temperatūroje. Pokyčiai didesni sergant leukemija. Jei tiriama plazma, kraują reikia pašildyti iki 37 C prieš atskiriant centrifugavimo būdu eritrocitus nuo plazmos. ph mažėja didėjant kūno temperatūrai, ir atvirkščiai. V: acetatai, antacidai, aspirinas (pradinė respiracinė alkalozė), citratai, diuretikai (etakrino rūgštis, furozemidas, tiazidai), glutamo rūgštis, fenilbutazonas, karbenicilinas, laktatai, saldymedžio ekstraktas, triamcinolonas, vidurius paleidžiantys vaistai (ilgalaikis vartojimas). V: acetazolamidas, acetonas, aminobenzenkarboksirūgštis, aminosalicilo rūgštis, amonio chloridas, argininas, aspirinas (vėlyvasis poveikis), cholestiraminas, ciklosporinas, etanolis, eteris, etilenglikolis (apsinuodijimas), fluoridai (apsinuodijimas), izoniazidas (didelės dozės), fenforminas, kalcio chloridas, kaptoprilis, metanolis, paraldehidas, spironolaktonas, tetraciklinas Tiriamoji medžiaga. Šlapimas. Tiriama reagentų juotelėmis. Rekomenduojama reikšmė. 6,3 7,3. Diagnostinė vertė. Kai maiste gausu vaisių, daržovių, ypač citrusinių; metabolinė alkalozė be kalio netekimo; užsitęsęs vėmimas ar skrandžio turinio siurbimas; šlapimo takų infekcija šlapalą skaidančiais organizmais (pvz., Proteus, Pseudomonas); pavalgius; inkstų kanalėlių acidozė; Fankonio sindromas (padidėjęs HCO 3 netekimas), gydymas šarminiais vaistais. Maiste gausu mėsos baltymų, spanguolių, metabolinė acidozė (pvz., cukrinis diabetas), metabolinė alkalozė netenkant kalio, respiracinė acidozė, badavimas, stiprus viduriavimas. Papildoma informacija. Šlapimui stovint ph kyla dėl amoniako susidarymo veikiant mikroorganizmams. Šlapime esant gliukozės, ph mažėja, nes mikroorganizmai metabolizuoja gliukozę; taigi nerekomenduojama matuoti pastovėjusio šlapimo ph. Bakterinė infekcija gali pakeisti ph į abi puses priklausomai nuo bakterinės veiklos produktų. Nuolat rūgštinis šlapimas gali rodyti polinkį susidaryti šlapimo rūgšties akmenims. ph reikšmės mažiausios po nakties (nevalgius), didžiausios pavalgius. Pastovi ph 7 8 reikšmė rodo šlapimo takų infekciją. 64
66 Rūgščių ir šarmų pusiausvyra... V: aldosteronas, amfotericinas B, adrenalinas, fenacetinas, kalio citratas, natrio rūgštusis karbonatas. Ch: nitrofurantoinas, riboflavinas. V: amonio chloridas, askorbo rūgštis, kortikotropinas, metioninas Tiriamoji medžiaga. Serozinių ertmių skystis (pleuros, perikardo, ascitinis). Rekomenduojama reikšmė. 6,8 7,6. Transudatas 7,4 7,5. Eksudatas 7,35 7,45. Tiriamoji medžiaga. Smegenų skystis. Rekomenduojama reikšmė. 7,35 7,40. Rūgštieji karbonatai (bikarbonatai HCO 3 ) Tiriamoji medžiaga. Kraujas (arterinis, veninis ar kapiliarinis). Rekomenduojama reikšmė (mmol/l): arterinio kraujo 21 28, veninio kraujo 23 29, kapiliarinio kraujo 21,8 26,9. Diagnostinė vertė. Kompensacinė respiracinė acidozė, metabolinė alkalozė. Metabolinė acidozė, kompensacinė respiracinė alkalozė. Papildoma informacija. Rūgščiuosius karbonatus galima nustatyti tiesiogiai titravimo būdu (retai atliekamu). Dažniausiai apskaičiuojama Hendersono ir Haselbacho lygtimi ar iš nomogramos (pastaroji taip pat remiasi minėta lygtimi): HCO 3 = bendrasis CO 2 H 2 CO 3. Į šią frakciją dažniausiai įskaičiuojamas ir nedidelis kiekis CO 3 bei karbamo rūgšties junginiai. HCO 3 yra didžiausia frakcija, nuo kurios priklauso bendrasis CO 2 kiekis. Todėl šie rodikliai dažniausiai kinta ta pačia kryptimi. Standartinis rūgštusis karbonatas tai kraujo rūgščiųjų karbonatų koncentracija, išmatuota, kai temperatūra 38 C, pco 2 40 mmhg ir kai visas kraujo hemoglobinas yra oksigenuotas. Jo reikšmė 21,8 26,9 mmol/l. V: morfinas, barbitūratai (jei būna respiracinė depresija), gliukokortikoidai (ilgalaikis vartojimas), diuretikai (pvz., tiazidai, chlortalidonas, etakrino rūgštis, furozemidas), vidurius paleidžiančių vaistų perteklinis vartojimas. V: amonio chloridas, cholestiraminas, ciklosporinas, apsinuodijimas etilenglikoliu, metanoliu, fenforminu, salicilatais (vėlyvasis toksiškumas). 65
67 NEBALTYMINĖS AZOTINĖS MEDŽIAGOS, JŲ APYKAITOS RODIKLIŲ SVARBA LIGŲ DIAGNOSTIKAI Vertinant baltymų apykaitą klinikoje, svarbią reikšmę turi tarpinių baltymų apykaitos rodiklių ir azotinių medžiagų kiekis kraujyje ir šlapime. Tai šlapalas, šlapimo rūgštis, kreatininas, kreatinas, indikanas. Nebaltyminės azotinės medžiagos ir jų komponentai Nebaltyminių azotinių medžiagų azotas tai azotas medžiagų, kurių lieka nusodinus kraujo plazmos baltymus. Į jų sudėtį įeina ir kai kurie polipeptidai, tačiau dauguma nebaltyminių azotinių medžiagų yra galutiniai baltymų skilimo produktai, kurie iš organizmo turi būti pašalinti. Jų kiekis priklauso nuo taikomo baltymų nusodinimo (deproteinizacijos) metodo. Dažniausiai baltymai yra nusodinami trichloracto ar fosfovolframo rūgštimis. Mažesnis šių medžiagų kiekis susidaro nusodinant baltymus fosfovolframo rūgštimi (dėl jos poveikio nusėda daugelis polipeptidų). Sveiko asmens kraujo plazmos nebaltyminių azotinių medžiagų azotą sudaro šių medžiagų azotas (procentais): Šlapalo 50 Aminorūgščių 25 Ergotioneino 8 Šlapimo rūgšties 4 Kreatino 5 Kreatinino 2,5 Amoniako, indikano 0,5 Kitų medžiagų (polipeptidų, biogeninių aminų, vitaminų) 5. 7,5 Maždaug pusę visų nebaltyminių azotinių medžiagų azoto sudaro šlapalo azotas. Šlapalo nustatymo metodas yra tikslus ir paprastas. Todėl nebaltyminių azotinių medžiagų kiekį geriausiai atspindi šlapalo tyrimas. (Seniau nebaltyminių azotinių medžiagų koncentracijai nustatyti buvo taikomas liekamojo azoto tyrimas. Šiuo metu jis neatliekamas.) 66
68 Nebaltyminės azotinės medžiagos... Dauguma mažos molekulinės masės azotinių medžiagų pasiskirsčiusi vienodai tarp plazmos ir eritrocitų. Amo n i a k a s Amoniakas susidaro kepenyse, inkstuose, žarnyne ir kituose audiniuose. Vartų venos sistemoje jo yra 8 kartus daugiau negu kitoje kraujotakos sistemos dalyje. Organizme amoniakas yra dviejų pavidalų: NH 3, kuris sudaro 4%, NH 4 +, kuris sudaro 96% ir yra tik šlapime. Amoniakas lengvai pereina ląstelių membraną ir organizmo reakcijai krypstant į šarminę pusę jo difuzija didėja. Daugiausiai amoniako į kepenis atneša glutaminas. Jo kraujyje randama apie 10 mg/dl. Streso sąlygomis glutamino koncentracija padidėja 6 8 kartus. Taigi glutaminas yra amoniako pernašos forma. Be to, amoniako į kepenis atneša alaninas, kurio didesni kiekiai susidaro raumenyse (alanino-gliukozės cikle). Amoniaką organizmas daro nekenksmingą keliais būdais: 1) amoniakas jungiasi su α ketoglutaro rūgštimi susidaro glutamo rūgštis, 2) amoniakas jungiasi su glutamo rūgštimi susidaro glutaminas, 3) amoniaką išskiria inkstai amonio chlorido pavidalu, o natrio ir kalio jonai organizme išsaugomi (į jį sugrąžinami) prisijungus protonui; 4) sintetinant šlapalą. Sveikų asmenų kraujo serume rekomenduojama amoniako koncentracija 11,6 µmol/l. Amoniako koncentracija padidėja: jaunuoliams lytinio brendimo metu; klimakteriniu tarpsniu; susijaudinus amoniako gaminasi smegenyse; jose yra daugiau glutamo rūgšties, kuriai dalyvaujant amoniako šalinimo procese susidaro glutaminas (gydymui yra naudojama glutamo rūgštis); sergant kepenų ligomis, ypač ciroze ir su ja susijusia portine hipertenzija; besivystančią kepenų cirozę galima nustatyti pagal amoniako koncentraciją kraujyje jo būna labai daug (kaip tik dėl to šiai ligai būdingas galvos skausmas). Dėl kepenų cirozės susidarant kraujagyslių kolateralėms, kraujyje daugėja amoniako, nes jis iš vartų venos sistemos patenka tiesiai į didįjį kraujo apytakos ratą; daug amoniako kraujyje randama po saulės smūgio (gali padėti gydymas glutamo rūgštimi); amoniako padaugėja vaikams, sergantiems distrofija, nes neretai jiems dėl fermentų stokos sutrinka šlapalo sintezė. Taigi amoniako koncentracijos nustatymas kraujyje yra svarbus diagnostinis rodiklis. 67
69 Šl a p a l a s Šlapalas (urea) (NH 2 CO NH 2 ) sintetinamas tik kepenyse ornitino-šlapalo cikle iš amoniako ir asparto rūgšties azoto bei CO 2. Vienas šio ciklo produktų argininas. Jis susiskaido į šlapalą ir ornitiną. Šlapalas lengvai pereina ląstelių membraną, jo koncentracija eritrocituose siekia 80% jo koncentracijos plazmoje (nes laisvasis vanduo eritrocituose sudaro 80% eritrocitų tūrio). Galimybės sintetinti šlapalą kepenyse labai didelės; jo mažiau susidaro stipriai pažeidus kepenis ar esant įgimtai šlapalo sintezės fermentų stokai. Sveikų asmenų kraujo plazmoje šlapalo koncentracija yra 2,5 6,4 mmol/l. Šlapalas išskiriamas per inkstus filtracijos būdu per parą su šlapimu pasišalina g šlapalo. Inkstų kanalėliuose dalis šlapalo sugrįžta į organizmą yra pasyviai reabsorbuojamas. Kitais būdais šlapalo išsiskiria nedaug suminis jo kiekis išmatose ir prakaite retai viršija 10% bendro išskiriamo kiekio. Esant inkstų funkcijos nepakankamumui, daugiau šlapalo gali pradėti skirtis su seilėmis, per virškinimo liaukas. Didesnį šlapalo kiekį kraujyje suskaldo fermentas ureazė ir šiame procese susidaręs amoniakas vartų vena patenka į kepenis, kuriose vėl paverčiamas šlapalu. Sveiki inkstai šlapalo gali išskirti kelis kartus daugiau, negu jo sintetinama kepenyse. Tačiau jo kiekis kraujyje retai nukrinta žemiau konkrečiam žmogui būdingo dydžio. Esant intensyviai šlapalo filtracijai per inkstus, dalis šlapalo, kaip minėta, reabsorbuojama ir taip organizme išsaugomos guanidino grupės. Nors pasitaiko ligonių, kuriems šlapalo sintezė sutrikusi ir dėl to kraujyje šlapalo kiekis esti labai mažas. Dėl reabsorbcijos inkstų kanalėliuose į organizmą sugrįžta apie 30% šlapalo taigi šlapalo klirensas yra nepastovus dydis, bet visada lygus ar mažesnis už kreatinino klirensą (šlapalo klirensas 75 ml/min.). Šlapalo klirensas, kaip ir šios medžiagos kiekio plazmoje sumažėjimas, didesnės diagnostinės vertės neturi. Ir atvirkščiai, šlapalo kraujyje gali padaugėti jau esant nedideliam inkstų veiklos pažeidimui, kai sutrinka inkstų kraujotaka ar suintensyvėja jo sintezė. Ir tai įvyksta daug anksčiau ir greičiau, negu padidėja kitų azotinių medžiagų, pavyzdžiui, kreatinino, kiekis. Pats šlapalas yra netoksiškas. Jis net vartojamas kaip vaistas osmosinis diuretikas, sukeliantis dehidrataciją, todėl juo gydoma smegenų edema. Kr e a t i n i n a s Kreatininas susidaro iš makroerginio junginio kreatinfosfato (KF), kuris kaupiamas raumenyse. Kreatinfosfato susidarymas: pirmajame jo sintezės etape iš glicino ir arginino susidaro vienas iš produktų guanidinoacto rūgštis; paskui kepenyse jis yra metilinamas (metilo grupių donoras S adenozilmetioninas) ir virsta metilguanidinoacto rūgštimi kreatinu. Pastarasis patekęs į raumenis fosforilinamas taip 68
70 Nebaltyminės azotinės medžiagos... susidaro kreatinfosfatas. Intensyviai dirbant raumenims iš jo susidaro ATF ir kreatinas (raumenų) (ramybėje susidaręs kreatinas dalyvauja grįžtamojoje reakcijoje); tik nedidelė jo dalis netenka vandens ir virsta kreatininu: KF Kreatinas Kreatininas ADF ATF H 2 O Kreatininas susidaro ir kitoje spontaniškoje (be fermento) reakcijoje defosforilinantis ir dehidratuojantis kreatinfosfatui. Kreatinino kiekis yra proporcingas raumenų masei; jo susidarymas priklauso ir nuo amžiaus bei lyties. Todėl kreatinino daugiau išsiskiria asmenims, kurių raumenys stiprūs, nors kiekybinės priklausomybės ir ryšio su fiziniu krūviu nėra. Sergant raumenų ligomis, pvz., progresuojančia raumenų distrofija, polimiozitu ar sutraiškymo sindromu, jo kiekis padidėja. Rečiau kreatinino koncentracija gali padidėti po sunkaus fizinio darbo (endogeninis kreatininas). Suvalgius daug virtos (bet ne keptos) mėsos, padidėja kreatinino reabsorbcija iš virškinamojo trakto (egzogeninis kreatininas). Kreatinino kiekis kraujyje gana pastovus, jo kiekio sumažėjimas diagnostinės reikšmės neturi. Kreatinino eritrocituose yra tiek pat, kiek ir plazmoje, tačiau galimas neteisingas tyrimo rezultatas, jei tirpale yra hemoglobino (matyt, kad kreatino eritrocituose yra daugiau negu plazmoje ir tai gali trukdyti reakcijai). Taigi būtina tirti nehemolizuotą kraujo plazmą ar serumą. Kraujo serume kreatinino koncentracija yra gana pastovi ir nedidelė: vyrų ( μmol/l) ji yra didesnė negu moterų (53 88 μmol/l). Jo labai padaugėja sutrikus didžiosios dalies nefronų veiklai tai informatyvus inkstų funkcijos nepakankamumo rodiklis. Konkretaus asmens endogeninio kreatinino paros ekskrecija yra gana pastovi per parą jo šalinama 1 2 g. Sveikuose inkstuose jis nei sekretuojamas, nei reabsorbuojamas išsiskiria tik filtracijos būdu. (Dalis jo sekretuojama esant sunkiai patologijai; taip pat sekretuojamas ir egzogeninis kreatininas.) Todėl iš endogeninio kreatinino kiekio šlapime įvertinama paros šlapimo rinkimo kokybė. Jo klirensas atspindi glomerulų filtraciją. (Apie kreatinino klirensą detaliau skyriuje Inkstų funkcija, jos tyrimas ir sutrikimų laboratorinė diagnostika ). Daugelio medžiagų kiekis šlapime išreiškiamas santykiu su 1 g kreatinino. Todėl galima tirti ne visą paros šlapimą, o jo porciją. Kreatinino klirenso normali reikšmė yra ml/min. Kreatinino ekskrecija su amžiumi mažėja apie 6,5 ml/min. per dešimtmetį. Hi p e r a z o t e m i j a Hiperazotemija tai būklė, kai kraujyje padidėja nebaltyminių azotinių medžiagų galutinių apykaitos produktų; svarbiausios jų šlapalas ir kreatininas. Todėl ši 69
71 būklė yra tapatinama su uremija (uraemia) apsinuodijimu medžiagų apykaitos produktais, sutrikus jų šalinimui su šlapimu (gr. uron šlapimas, haima kraujas). Taigi uremija šlapimas (jo sudedamosios dalys) kraujyje. Šios būklės sunkumą lemia ne tiek paties šlapalo ar kreatinino, o kitų medžiagų kaupimasis kraujyje, pavyzdžiui, kalio, toksinių guanidino darinių (guanidinogintaro rūgšties, metilguanidino, guanidinoacto rūgšties, guanidinopropiono rūgšties). Pastarųjų medžiagų susidaro sutrikus normaliam šlapalo susidarymui iš arginino. Tuomet dalis arginino guanidino grupių neverčiamos šlapalu, o sujungiamos su tam tikromis medžiagomis taip susidaro minėtųjų kenksmingų produktų. Kai kurie jų turi dar ir specifinį poveikį, pavyzdžiui, guanidinogintaro rūgštis slopina trečiojo trombocitų faktoriaus aktyvaciją, trombocitų agregaciją ir sukelia eritrocitų hemolizę. Hiperazotemijos (uremijos) priežastys. Skiriamos trys grupės priežasčių, lemiančių nebaltyminių azotinių medžiagų kiekio kraujyje padidėjimą: tai prereninės, reninės ir postreninės priežastys. Prereninės (ikiinkstinės) nebaltyminių azotinių medžiagų kiekio kraujyje padidėjimo priežastys yra susijusios su kraujotakos nepakankamumu ir dėl to sutrikusia filtracija inkstų glomeruluose ar padidėjusia sinteze. Taip atsitinka, kai sumažėja kraujo prietaka į inkstus esant širdies nepakankamumui, šokui, ūminei dehidratacijai, netekus kraujo, arteriniam kraujospūdžiui nukritus žemiau kaip 60 mmhg (toks kraujospūdis būtinas glomerulų filtrato susidarymui); sustiprėja baltymų katabolizmas nudegus, karščiuojant, kraujuojant į minkštuosius audinius, esant trauminei uremijai (angl. crush syndrome) ar hemolizei kūno ertmėse. Kita reninių (inkstinių) priežasčių grupė yra susijusi su ligomis ar būklėmis, dėl kurių laikinai ar visiškai nefunkcionuoja glomerulai: ūminis inkstų nepakankamumas sergant glomerulonefritu, esant piktybinei hipertenzijai, vartojant vaistus ar apsinuodijus metalais, kurie pažeidžia inkstus, įvykus inkstų žievinio sluoksnio nekrozei; lėtinės inkstų ligos, pavyzdžiui, glomerulonefritas, pielonefritas, inkstų kanalėlių ligos ar inkstų pažeidimai sergant cukriniu diabetu, ateroskleroze, kolagenozėmis. Postreninės (poinkstinės) nebaltyminių azotinių medžiagų koncentracijos kraujyje padidėjimo priežastys yra susijusios su šlapimo nuotakos sutrikimu dėl šlapimo takų užsikimšimo, sukelto akmens, naviko ar hipertrofavusios prostatos; šlapimtakių destrukcijos sergant akmenlige, vėžiu, uždegimu, po chirurginių traumų. Reta uremijos forma, kurią lemia hemodinamikos sutrikimai ir kuri vystosi dėl NaCl stokos organizme, yra žinoma kaip chloroprivinė uremija. 70
72 Nebaltyminės azotinės medžiagos... Šlapalo koncentracijos kraujyje padidėjimas suintensyvėjus audinių irimui (dėl traumos, karščiavimo) ar valgant daug baltymų turintį maistą, esant sveikiems inkstams, nėra labai ryškus, bet jei tęsiantis šioms būklėms pažeidžiami inkstai šlapalo gali labai padaugėti. Nors ir šlapalo, ir kreatinino kiekis rodo inkstų būklę, šių rodiklių interpretacija skiriasi; todėl inkstų veiklai įvertinti rekomenduojama tirti abi šias medžiagas. Nors kreatinino kiekis kraujo serume nedidelis, palyginti su kitais nebaltyminių azotinių medžiagų komponentais, jis nustatomas dažnai. Esant nedideliems inkstų funkciniams pakitimams, šlapalo kiekis kraujyje pradeda didėti, o kreatinino kiekis ilgai išlieka normalus. Jo koncentracija išauga tik tada, kai visiškai išsenka funkciniai inkstų rezervai. Nuolatos padidėjusi kreatinino koncentracija kraujyje rodo sutrikusią inkstų filtro funkciją. Kreatinino koncentracija kraujyje labai padidėja nefunkcionuojant didelei nefronų daliai kreatinino koncentracijos padvigubėjimas kraujyje atitinka jo filtracijos, kartu ir endogeninio kreatinino klirenso sumažėjimą 50%. Šlapalo klirensas įvairuoja ir yra neinformatyvus, o iš kreatinino klirenso galima įvertinti glomerulų filtraciją ir diagnostiškai jis yra svarbus. Kai inkstai pažeisti, anksčiausiai pradeda didėti šlapimo rūgšties (nes jos išskyrimo per inkstus mechanizmas yra sudėtingas žr. kitame skyriuje) ir šlapalo, o vėliausiai, bet stabiliai didėja kreatinino koncentracija kraujyje. Sergant inkstų ligomis, kreatinino koncentracija dažniausiai yra didelė. Paprastai visos uremijos reninės priežastys yra susijusios su padidėjusiu kreatinino kiekiu. Padidėjęs šlapalo kiekis pacientams, kurių kreatinino kiekis normalus, dažniau rodo ne su inkstų pažeidimu susijusias uremijos priežastis. Esant labai dideliam inkstų pažeidimui, šlapalo kiekis dažniausiai kyla, o kreatinino stabilizuojasi. Kai kraujyje kreatinino labai daug, dalis jo išskiriama per virškinamąjį traktą. Atliekant dializę šlapalas šalinamas greičiau negu kreatininas. Api b e n d r i n i m a s Diagnostinę reikšmę turi šios nebaltyminės azotinės medžiagos: šlapalas, šlapimo rūgštis, kreatininas. Šlapalas išskiriamas per inkstus filtracijos būdu, o inkstų kanalėliuose dalis jo yra pasyviai reabsorbuojama. Labai maža šlapalo koncentracija kraujyje gali būti esant ypač sunkiems kepenų pažeidimams ar įgimtai šlapalo sintezės fermentų stokai. Esant inkstų nepakankamumui, daugiau šlapalo gali pradėti skirtis su seilėmis, per virškinimo liaukas. Šlapalo kiekis kraujyje gali padidėti jau esant nedideliam inkstų veiklos pažeidimui, kai sutrinka inkstų kraujotaka ar padidėja jo sintezė, ir tai įvyksta daug anksčiau, negu padaugėja kitų azotinių medžiagų, pvz., kreatinino. 71
73 Šlapalas pats savaime yra netoksiškas. Jis net vartojamas kaip vaistas osmosinis diuretikas, sukeliantis dehidrataciją, todėl juo gydoma smegenų edema. Kasdien apie 1 2% kreatinfosfato virsta kreatininu per kreatino susidarymo stadiją tai galutinis jo apykaitos produktas. Konkretaus asmens endogeninio kreatinino paros ekskrecija yra gana pastovi: sveikuose inkstuose jis nei sekretuojamas, nei reabsorbuojamas, išsiskiria tik filtracijos būdu. Pasigaminusio endogeninio kreatinino kiekis yra proporcingas raumenų masei, todėl jo susidarymas priklauso nuo amžiaus ir lyties. Kreatinino ekskrecija su amžiumi mažėja apie 6,5 ml/min. per dešimtmetį. Hiperazotemija (uremija) tai būklė, kai kraujyje padidėja nebaltyminių azotinių medžiagų, svarbiausios jų šlapalas ir kreatininas. Uremija tai apsinuodijimas medžiagų apykaitos produktais, sutrikus jų šalinimui su šlapimu. Dažniausiai šią būklę sukelia šlapalo ir kreatinino koncentracijų padidėjimas kraujyje. Prereninės uremijos priežastys yra susijusios su kraujotakos nepakankamumu ir dėl to sutrikusia šlapalo filtracija inkstų glomeruluose ar padidėjusiu azotinių medžiagų susidarymu. Inkstinę uremiją lemia ligos, dėl kurių laikinai ar visiškai neveikia glomerulai. Postreninės uremijos priežastys yra susijusios su šlapimo nutekėjimo sutrikimu. Dažniausiai uremijos reninės priežastys yra susijusios su padidėjusiu kreatinino kiekiu. Padidėjęs šlapalo kiekis pacientams, kurių kreatinino kiekis normalus, dažniau rodo ne su inkstų pažeidimu susijusias uremijos priežastis. Amoniakas Tiriamoji medžiaga. Plazma (EDTA ar heparinas). Imant kraują nemasažuoti ir nejudinti rankos. Kraują tuoj pat šaldyti ir tirti, nes stovinčiame plazmos koncentracija greitai didėja. Netirti esant hemolizei. Rekomenduojama reikšmė µmol/l. Diagnostinė vertė. Žaibinis kepenų funkcijos nepakankamumas, kepenų cirozė, kraujavimas iš virškinamojo trakto, portosisteminis nuosruvis, inkstų ligos, lyties ir šlapimo organų sistemos infekcija (esant stazei). Šlapalo ciklo apykaitos sutrikimai: didėja badaujant, valgant daug baltymų turtinčio maisto. Papildoma informacija. Amoniako koncentracijos padidėjimas yra svarbus hepatinės encefalopatijos patogenezei. V: amonio druskos, asparaginazė, barbitūratai, diuretikai (pvz., chlortalidonas, furozemidas, tiazidai), etanolis, narkotiniai analgetikai, parenterinis maitinimas, valproatai. Ch: amoniakas atmosferoje, fluoridai, oksalatai, naudojami kaip antikoaguliantai. V: kanamicinas, Lactobacillus acidophilus, laktuliozė, levadopa, neomicinas, rūkymas. Kreatininas Laboratoriniai tyrimai Tiriamoji medžiaga. Serumas. Greit atskirti serumą nuo krešulio, kad nesigamintų amoniakas. 72
74 Nebaltyminės azotinės medžiagos... Rekomenduojama reikšmė (µmol/l): vyrų , moterų 53 88, vaikų 1 5 metų 27 44, vaikų 5 10 metų Diagnostinė vertė. Inkstų funkcijos sutrikimas (ūminis ir lėtinis) dėl bet kurios priežasties (kraujotakos sumažėjimas, inkstų ligos, postreninė kliūtis šlapimui nutekėti); aktyvusis akromegalijos ir gigantizmo tarpsnis; hipertirozė; kai vartojama daug mėsos. Silpnumas (pvz., dėl senyvo amžiaus, sumažėjus raumenų masei), nėštumas (ypač I ir III trimestrai). Papildoma informacija. Kreatininas nėra jautrus rodiklis pradinėse inkstų ligų stadijose. Serumo kreatinino kiekiui maistas turi mažiau įtakos negu šlapalo koncentracijai. Su kiekvienu glomerulų filtracijos greičio sumažėjimu 50% kreatinino koncentracija padvigubėja. Dėl lėtinių inkstų ligų kreatinino kiekis yra jautresnis glomerulų veiklos rodiklis negu kreatinino klirensas, kuris gali būti nenatūraliai (dirbtinai) aukštesnis negu tikroji reikšmė. V: nefrotoksiniai vaistai Tiriamoji medžiaga. Paros šlapimas. Stabilus laikomas šaldytuve. Rekomenduojama reikšmė (mmol/24 val.): vyrų 8,8 17,7, moterų 7,1 15,9. Diagnostinė vertė. Fiziniai pratimai, akromegalija, gigantizmas, cukrinis diabetas, infekcijos, hipotirozė, kai vartojama daug mėsos. Hipertirozė, anemija, paralyžius, raumenų distrofija, ligos, dėl kurių mažėja raumenų masė (pvz., neurogeninė atrofija, polimiozitas); uždegiminės raumenų ligos, metabolinės ligos, pažeidžiančios raumenis, toli pažengusios inkstų ligos, leukemija, vegetariškas maistas. Kreatinino kiekis yra sumažėjęs šlapime, ištekančiame iš stenozės pažeisto inksto. Papildoma informacija. Kadangi konkretaus žmogaus kreatinino ekskrecija yra santykinai pastovi (jei mityba nesikeičia), kreatinino kiekis 24 val. šlapime yra naudojamas patikrinti, ar tinkamai surinktas paros šlapimas. V: gliukokortikoidai. Ch: askorbo rūgštis, fruktozė, levadopa. V: anaboliniai steroidai, androgenai, tiazidai. Šlapalas Tiriamoji medžiaga. Serumas. Rekomenduojama reikšmė. 2,5 6,4 mmol/l. Diagnostinė vertė. Sutrikusi inkstų veikla: 1) sumažėjusi kraujotaka inkstuose, esant širdies nepakankamumui; netekus druskų ir vandens gausiai vemiant, viduriuojant, šlapinantis ar prakaituojant; šokas, kartu suintensyvėjęs baltymų katabolizmas, pvz., kraujuojant iš virškinamojo trakto, dėl ūminio infarkto ar nudegimų; 2) ūminė ar lėtinė inkstų liga; 3) postreninė kliūtis šlapimui nutekėti; 4) daug baltymų turintis maistas. Mažai baltymų ir daug angliavandenių turintis maistas, padidėjęs baltymų sunaudojimas sintezei, paskutiniai nėštumo mėnesiai, kūdikystės tarpsnis, akromegalija, tik intraveninė mityba, sunkus kepenų pažeidimas, apsinuodijimas, sutrikusi absorbcija Tiriamoji medžiaga. Paros šlapimas. Rekomenduojama reikšmė mmol/24 val. Diagnostinė vertė. Baltymų gausus maistas, hipertirozė, po operacijų. Normalus kūdikių ir vaikų augimas, nėštumas, mažai baltymų ir daug angliavandenių turintis maistas, sveikimo laikotarpis, kepenų ligos, apsinuodijimas, inkstų pažeidimas ir nepakankamumas. Papildoma informacija. Šlapalo kiekis didėja su amžiumi ir baltymų kiekiu maiste. V: gliukokortikoidai, nefrotoksiniai vaistai, tetraciklinas, tiroksino perteklius. V: augimo hormonas. 73
75 Šl a p i m o r ū g š t i s ir jo s nu s t a t y m o sv a r b a ligų diagnostikai Nukleorūgštis sudaro dviejų rūšių nukleotidai: pirimidinas ir purinas. Šlapimo rūgštis yra galutinis purinų nukleotidų adenino ir guanino skaidymosi produktas. Šlapimo rūgšties susidarymas ir išsiskyrimas. Šlapimo rūgštis susidaro trimis būdais: kai purinų nukleotidų bazės nepanaudojamos kartotinei nukleotidų sintezei; vykstant organizmo DNR, RNR, kitų purinų turinčių molekulių, kaip ATF, GTF, FAD +, NAD +, katabolizmui; katabolizuojantis organizme su maistu gautiems nukleoproteinams, į kurių sudėtį įeina purinų nukleotidų. Esant fiziologinei vandenilio jonų koncentracijai (ph 7,4) ir 38 C temperatūrai, šlapimo rūgštis kraujo plazmoje daugiausia yra jonizuotosios formos kaip natrio uratas. Dalis šlapimo rūgšties yra adsorbuota albuminų ir specialaus pernašos baltymo, priklausančio α globulinų frakcijai, todėl jos bendras kiekis gali viršyti tirpumo slenkstį. Šlapimo rūgšties eritrocituose yra daugiau negu kraujo plazmoje. Padidėjusi šlapimo rūgšties koncentracija kraujyje vadinama hiperurikemija. Šlapimo rūgštis blogai tirpsta kraujo plazmoje (jos tirpumo slenkstis yra 6,5 mg/ 100 ml = 390 μmol/l), sinoviniame skystyje, šlapime ir iškrinta nuosėdomis. Susidarę kristalai natrio uratai kaupiasi sąnariuose ir šlapimo takuose, sukelia podagrą ir šlapimo takų akmenligę. Šlapimo rūgšties vyrų plazmoje yra 17 19% daugiau negu moterų. Pastarųjų šlapimo rūgšties kiekis didėja su amžiumi. Uratai iš organizmo šalinami keliais būdais: Per inkstus. Taip pasišalina didžiausias uratų kiekis apie 80%. Šlapimo rūgštis glomeruluose yra filtruojama. Paskui proksimalinėje inkstų kanalėlių dalyje apie 99% filtruotos šlapimo rūgšties yra reabsorbuojama. Distaliniuose kanalėliuose ji yra sekretuojama ir didelė jos dalis vėl reabsorbuojama. Todėl šlapimo rūgšties koncentracijos padidėjimo kraujyje priežastis gali būti nepakankama jos sekrecija, padidėjusi reabsorbcija dėl kol kas neaiškių priežasčių, matyt, genetinių. Galiausiai su šlapimu pašalinama apie 10% glomeruluose filtruoto šlapimo rūgšties kiekio. Per virškinamąjį traktą. Nedidelis šlapimo rūgšties kiekis pašalinamas per žarnyną (apie 20%), kur ją suskaido bakterijos. Šis procesas vadinamas urikolize. Rekomenduojama šlapimo rūgšties koncentracija vyrams yra μmol/l, moterims μmol/l. Hiperurikemija dažniausiai išsivysto dėl nepakankamo šlapimo rūgšties išskyrimo per inkstus, rečiau dėl hiperprodukcijos (6 lentelė). Šlapimo rūgšties apykaitos ypatybės labai susijusios su genotipu: paveldimumas svarbus daugeliui ligonių, sergančių hiperurikemija. 74
76 Nebaltyminės azotinės medžiagos... 6 lentelė. Hiperurikemijos priežastys Pirminė hiperurikemija: hipoksantinguaninfosforiboziltransferazės stoka (Lešo Naijano sindromas) gliukozės-6-fosfatazės stoka (I tipo glikogeno kaupimo liga) Padidėjęs susidarymas Antrinė hiperurikemija: per didelis nukleoproteinų vartojimas suintensyvėjusi nukleorūgščių apykaita suintensyvėjęs ATF skilimas Sumažėjęs išsiskyrimas Pirminė hiperurikemija: idiopatinė Antrinė hiperurikemija: inkstų nepakankamumas padidėjęs pieno rūgšties ar ketoninių medžiagų kiekis, tiazidiniai diuretikai, mažos aspirino dozės, mažinančios sekreciją kanalėliuose padidėjusi reabsorbcija inkstų kanalėliuose Skiriama pirminė hiperurikemija, kai šlapimo rūgšties susikaupimas kraujyje nėra kurių nors ligų padarinys. Dauguma pirminių priežasčių (apie 90%) yra susijusios su nepakankamu šlapimo rūgšties šalinimu iš organizmo, esant įgimtai fermento stokai, kitos (apie 10%) su padidėjusiu susidarymu iš purino bazių pertekliaus, kai nukleotidų sintezei jos nepanaudojamos. Antrinę hiperurikemiją gali sukelti: padidėjęs purinų susidarymas sergant kraujo ligomis, kai organizme susidaro ir suyra daug branduolį turinčių ląstelių, pavyzdžiui, sergant leukemija, eritremija, psoriaze, ar yrant audiniams, kai badaujama, gydoma citoliziniais vaistais; inkstų funkcijos sutrikimas, kai sumažėja ekskrecija, pvz., dėl alkoholizmo, vartojant tiazidinius diuretikus, esant acidozei dėl cukrinio diabeto ar badaujant. Hiperurikemiją gali sukelti ir maistas, kuriame yra nukleoproteinų (kepenys, ikrai, jaunų gyvulių mėsa ir kt.), gėrimai, turintys purino darinių: kofeino (kava), teobromino (arbata), švinas juo apsinuodijus susergama pneumonija. Skirstymas į pirminę ir antrinę hiperurikemiją yra sąlyginis, nes daug mažos molekulinės masės medžiagų gali laikinai slopinti šlapimo rūgšties išskyrimą per inkstus; jos kiekis kraujyje padidėja dėl metabolinės acidozės (dažniau diabetinės etiologijos), nėščiųjų toksikozės, alkoholizmo, nors inkstai ir nepažeisti. Kitos indikacijos tirti šlapimo rūgšties koncentraciją yra antsvoris, hipertonija, sutrikęs angliavandenių toleravimas, inkstų ligos, ypač akmenligė, ankstyvoji aterosklerozė, suriebėjusių kepenų liga (riebalinė kepenų infiltracija) ir polinkis ja sirgti. Esant IV tipo hiperlipoproteinemijai, hiperurikemija nustatoma iki 40% atvejų. Priešinga būklė hiperurikemijai yra hipourikemija. Jos priežastys: sumažėjęs šlapimo rūgšties susidarymas, pavyzdžiui, išsivysčius ksantinurijai, kai dėl fermento ksantinoksidazės stokos galutinis purinų skilimo produktas yra ne šlapimo rūgštis, o ksantinas; 75
77 padidėjęs šlapimo rūgšties išskyrimas per inkstus, pvz., esant viso kanalėlio pažeidimui. Esant tam tikroms įgimtoms purinų nukleotidų skilimo fermentopatijoms, kraujyje bus nustatoma sumažėjusi šlapimo rūgšties koncentracija; pavyzdžiui, trūkstant adenozindeaminazės, kuri deaminina adenoziną ir jį verčia inozinu (hipoksantinriboze), gali išsivystyti sunkios imuninio deficito būklės; kito fermento purinnukleozidfosforilazės, kuri skaldo purino nukleozidus susidarant hipoksantinui ir ribozės-1- fosfatui, stoka yra susijusi su ne tokia sunkia būkle dėl T limfocitų stokos. Hipourikemija gali išsivystyti ir vartojant kai kuriuos vaistus, kaip antai dideles salicilatų dozes. Po d a g r a Podagrą aprašė Hipokratas dar penktame amžiuje prieš mūsų erą. Podagra tai klinikinis sindromas, kuriam būdinga hiperurikemija ir besikartojantis ūminis artritas. Nors visiems asmenims, kuriems išsivysto podagra, tam tikrame ligos vystymosi etape buvo nustatyta hiperurikemija, tik nedidelei jų daliai, turinčiai hiperurikemiją, išsivysto podagra. To reiškinio priežastis nežinoma. Ūminę podagrą pasunkina audiniuose besikaupiantys natrio urato kristalai, kurie sukelia uždegimą. Lėtinėms būklėms būdingi susiformavę mazgeliai uratinės granulomos (tophi urici) audiniuose tai šlapimo rūgšties kristalų ir jų sukelto uždegimo padarinys (šlapimo rūgšties kristalai yra fagocituojami makrofagų ir susidaro daugiabranduolės milžiniškos ląstelės). 40% negydomų ligonių išsivysto inkstų akmenligė. Podagrą pasunkina alkoholio vartojimas dėl kelių priežasčių. Etanolis skatina ATF skilimą ir kartu šlapimo rūgšties susidarymą. Taip pat etanolis skatina organinių rūgščių kaupimąsi, kurios konkuruoja su šlapimo rūgštimi šalinant jas inkstų kanalėliais. Todėl tokios būklės kaip intoksikacija alkoholiu, diabetinė ketoacidozė ir badavimas didina pieno rūgšties, β hidroksisviesto ir acetoacto rūgščių kiekį, skatina hiperurikemiją. Ypač daug šlapimo rūgšties esti kraujyje, kai podagra susijusi su inkstų funkcijos nepakankamumu (susiraukšlėjęs inkstas). Hiperurikemija gydoma vaistais, veikiančiais pasirinktinai sekreciją ir (ar) reabsorbciją įvairiose nefrono dalyse. Laboratoriškai nėra sunku diferencijuoti hiperurikemiją dėl šlapimo rūgšties padidėjusio susidarymo ir nepakankamo jos išsiskyrimo: pirmuoju atveju paros ekskrecija padidėjusi, antruoju ne. Ūminės podagros simptomus sušvelnina vaistai nuo uždegimo, pvz., indometacinas, tačiau jie neveikia šlapimo rūgšties koncentracijos kraujyje. Mažos aspirino dozės nerekomenduojamos, nes jis slopina šlapimo rūgšties išsiskyrimą su šlapimu. Tokie pacientai profilaktiškai turi vartoti vaistų, skatinančių uratų šalinimą per inkstus. Rekomenduojama mažai nukleoproteinų ir purinų turinti dieta, reikėtų vengti kavos, arbatos, nevartoti alkoholio taip sumažinama uratų koncentracija kraujyje. 76
78 Nebaltyminės azotinės medžiagos... Uratų koncentraciją veiksmingai mažina alopurinolis. Tai specifinis fermento ksantinoksidazės, kuri katalizuoja hipoksantino oksidaciją į ksantiną ir iš jos į šlapimo rūgštį, inhibitorius. Šlapimo rūgštį iš audinių efektyviausiai šalina litis, nes ličio uratas gerai tirpsta vandenyje. Be podagros, šlapimo rūgšties nustatymas yra svarbus asmenims, turintiems ir kitų širdies ir kraujagyslių ligų (aterosklerozės) rizikos veiksnių: hiperlipidemiją, ypač hipertriacilglicerolemiją, padidėjusį kraujospūdį, cukrinį diabetą. Kraujospūdžio didėjimo priežastis dažniausiai yra dėl inkstų pažeidimo besivystanti nefropatija. Lešo Naijano sindromas Žinoma keletas genetinių šlapimo rūgšties apykaitos sutrikimų. Gerai ištirtas su lytimi susijusio fermento hipoksantinguaninfosforiboziltransferazės gaminimosi sutrikimas. Už šio fermento sintezę atsakingas genas yra X chromosomoje taigi serga tik berniukai, o moterys yra patologinio geno nešiotojos. Naudojant hipoksantiną (adenino nukleotidų skilimo produktą) ir guaniną kartotinei purino nukleotidų sintezei, dalyvauja fermentas hipoksantinguaninfosforiboziltransferazė, sujungianti šias bazes su fosforibozildifosforo rūgštimi taip susidaro inozinmonofosfatas (IMF) bei guanozinmonofosfatas (GMF). Sutrikus šiai sintezei lieka nepanaudotų purino bazių, iš kurių pasigamina daugiau šlapimo rūgšties. Nukleotidų sintezė reguliuojama grįžtamuoju ryšiu (susidaręs didesnis AMF kiekis skatina GMF ir IMF sintezę, ir atvirkščiai). Kliniškai šio fermento stoka išryškėja nuo besimptomės hiperurikemijos, šeiminės podagros formos iki labai sunkaus Lešo Naijano (Lesch Nyhan) sindromo. Dėl pastarojo jau ankstyvoje vaikystėje sutrinka psichika, pažeidžiami sąnariai. Eritrocituose labai padidėja nepanaudotų purinų (hipoksantino ir guanino) bei AMF (kaip ir fosforibozildifosfato), dėl to paspartėja šlapimo rūgšties darinių šalinimas su šlapimu. Iš laboratorinių tyrimų informatyviausias yra šlapimo rūgšties koncentracijos santykis su kreatinino kiekiu šlapime. Normaliai jis lygus 0,21 0,59 g šlapimo rūgšties 1 g kreatinino. Esant fermento stokai, jis viršija 1. Kitas tyrimas tai fermento aktyvumo nustatymas eritrocituose. Ligonių, sergančių podagra, hipoksantinguaninfosforiboziltransferazės aktyvumas sudaro mažiau negu 20% normalaus, o adeninfosforiboziltransferazės aktyvumas išlieka normalus (sintetinasi adenozinmonofosfatas). Patologinio geno nešiotoją galima nustatyti tiriant fermento aktyvumą plaukų svogūnėliuose. Api b e n d r i n i m a s Šlapimo rūgšties daugiausia susidaro yrant endogeninės ir egzogeninės kilmės nukleoproteinams, į kurių sudėtį įeina purinų. 77
79 Hiperurikemija yra podagros rizikos veiksnys, ji išsivysto kaupiantis natrio urato kristalams audiniuose. Hiperurikemijos dėl suintensyvėjusio šlapimo rūgšties susidarymo priežastys: purinų perteklius maiste (jų esti mėsos, ikrų, galvijų liežuvio nukleoproteinuose), policitemija, navikų, ypač leukemijos, limfomos, gydymas citoliziniais vaistais, mieloidinė metaplazija, psoriazė, pjautuvinė anemija. Hiperurikemijos dėl sumažėjusios šlapimo rūgšties ekskrecijos priežastys: alkoholizmas, vartojant tiazidinius diuretikus, mažas aspirino dozes (<2 g per dieną), pieno rūgšties (laktinė) acidozė, ketoacidozė, ypač diabetinė ar badavimo, inkstų veiklos nepakankamumas. Hipourikemijos dėl padidėjusios šlapimo rūgšties ekskrecijos priežastys: didelės aspirino dozės (>4 g per dieną), adrenokortikotropinis hormonas (AKTH) ir gliukokortikoidai, kumarino grupės antikoaguliantai, estrogenai. Hipourikemijos dėl sumažėjusio šlapimo rūgšties susidarymo priežastys: alopurinolis. Ūminio podagrinio artrito diagnozė gali būti nustatyta tiriant sinovinį skystį, paimtą iš uždegimo pažeisto sąnario. Poliarizuotojoje šviesoje tiriant daugiabranduolius leukocitus bus randama natrio urato kristalų. Laboratoriniai tyrimai Šlapimo rūgštis Tiriamoji medžiaga. Serumas. Rekomenduojama reikšmė. Vyrų µmol/l, moterų µmol/l. Diagnostinė vertė. Podagra, inkstų nepakankamumas, dauginė mieloma, policitemija, limfoma, kiti išplitę navikai, nėštumo toksikozė, psoriazė, I tipo glikogenozė, Lešo Naijano sindromas, Dauno sindromas, inkstų policistozė, lėtinio apsinuodijimo švinu nefropatija. Kartu su hiperlipidemija, esant nutukimui, hipertenzijai, arterosklerozei, cukriniam diabetui, vartojant alkoholį, sergant hipotiroze, akromegalija, sarkoidoze, kepenų ligomis, po audinių destrukcijos (padidėja nukleoproteinų irimas), esant greitai nukleoproteinų apykaitai (pvz., mieloidinė leukemija, B 12 vitamino stoka, apsinuodijimas strichninu), gydant leukemiją citotoksiniais vaistais (gali labai padaugėti). Vilsono liga, Fankonio sindromas, kai kurios piktybinės ligos (Hodžkino liga, dauginė mieloma, bronchogeninis vėžys), ksantinurija, antidiurezinio hormono nepakankama sekrecija, adenozindeaminazės, purinų ir nukleozidfosforilazės stoka, mažai purinų turintis maistas Tiriamoji medžiaga. Paros šlapimas. Šarminio šlapimo palaikymui įdėti NaOH. 78
80 Nebaltyminės azotinės medžiagos... Rekomenduojama reikšmė. 1,5 4,5 mmol/24 val. Diagnostinė vertė. Leukemija, podagra, Lešo Naijano sindromas, Vilsono liga, cistinozė, virusinis hepatitas, tikroji policitemija. Ksantinurija, folio rūgšties stoka, apsinuodijimas švinu. Papildoma informacija. Purinų gausus maistas (kepenys, inkstai) ir fizinis aktyvumas didina šlapimo rūgšties kiekį šlapime. V: β adrenoblokatoriai, ciklosporinas, diuretikai (chlortalidonas, etakrino rūgštis), furozemidas, tiazidai, triamterenas), etanolis, etambutolis, fruktozė (į veną), gliukokortikoidai (ūminė leukemija), nikotino rūgštis (didelės dozės), noradrenalinas, kai kurie priešnavikiniai vaistai, salicilatai (mažos dozės), teofilinas (į veną). V: alopurinolis, azatioprinas, fenofibratas, furozemidas (į veną), klofibratas, kontrastinės medžiagos, salicilatai (didelės dozės). Kiti nebaltyminių azotinių medžiagų komponentai Be minėtųjų, į nebaltyminių azotinių medžiagų sudėtį įeina ir kitų medžiagų, kurių nustatymas didelės diagnostinės reikšmės neturi. Veikiant žarnyno bakterijų fermentams iš aminorūgšties triptofano susidaro indoksilas, šis kepenyse rezorbuojamas, sujungiamas su aktyvia H 2 SO 4, kalio jonais ir virsta indikanu, išskiriamu per inkstus. Normalus jo kiekis šlapime yra μmol per parą (10 20 mg per parą). Jo padaugėja užkietėjus viduriams; tada šlapimas tampa rudas. Indikano kiekis kraujyje padidėja dėl inkstų nepakankamumo. Sveikų asmenų kraujyje jo yra 1 3,2 μmol/l. Padidėjimas iki 4,7 μmol/l būdingas sergant žarnyno ligomis, o didesni kiekiai inkstų patologijai. Nebaltyminėms azotinėms medžiagoms taip pat priklauso nemažai tų, kurios turi guanidino grupę NH NH C NH 2, o jos šaltinis yra aminorūgštis argininas. Šią grupę turi kreatinas, kurio galutinis skaidymo produktas yra jau minėtasis kreatininas. Kreatino koncentracija kraujyje įvairuoja ir jo nustatymo klinikinė vertė yra nedidelė. Kreatinas inkstų glomeruluose yra filtruojamas ir proksimaliniuose inkstų kanalėliuose beveik visas reabsorbuojamas. Taigi šlapime kreatino yra labai nedaug ir jo nustatymas diagnostikai nereikšmingas. Nebaltyminių azotinių medžiagų komponentas yra ir kraujyje esantys polipeptidai, kurių kiekis priklauso nuo baltymų nusodinimo metodo. Eritrocituose jų yra daugiau negu plazmoje ir padaugėja valgant baltymingą maistą. Nemažai hormonų taip pat yra polipeptidai. Bendro polipeptidų kiekio nustatymas kraujyje diagnostinės reikšmės neturi. 79
81 INKSTŲ FUNKCIJA, JOS TYRIMAS IR SUTRIKIMŲ LABORATORINĖ DIAGNOSTIKA Inkstų funkcija Nors inkstas sveria tik apie 150 g, per inkstus prateka apie 25% viso į širdį patenkančio kraujo: 80% šio kiekio pasiskirsto inkstų žievėje ir 20% šerdyje. Taigi inkstai yra labai gerai krauju aprūpintas organas. Inkstų glomerulai filtruoja apie 20% per inkstus pratekančio kraujo plazmos tūrio, t. y. kas dieną per juos prateka apie 180 litrų vandens ir daugiau kaip 99% jo, t. y. 179 l, grįžta į organizmą vykstant efektyviai vandens reabsorbcijai inkstų kanalėliuose. Inkstų funkcinis vienetas yra nefronas. Jų kiekviename inkste arti milijono. Inkstai reguliuoja neląstelinio skysčio tūrį ir elektrolitų sudėtį kompensuodami vandens ir elektrolitų suvartojimo per dieną svyravimą. Inkstuose susidaro šlapimas, su kuriuo iš organizmo išskiriamos neutralizuotos medžiagos ir galutiniai medžiagų apykaitos produktai. Be to, juose sintetinamos kai kurios aktyviosios medžiagos, turinčios hormono savybių: eritropoetinas inkstų peptidinis hormonas, kuris skatina hemoglobino sintezę kaulų čiulpuose; 1,25-dihidroksicholekalciferolis, kuris reguliuoja kalcio ir fosfatų apykaitą organizme ir veikia žarnyną, kaulus, kitus organus; reninas hidrolazė, gaminama jukstaglomerulinėse ląstelėse; ji angiotenzinogeną verčia angiotenzinu I; angiotenziną konvertuojantis fermentas (AKF) angiotenziną I verčia angiotenzinu II; pastarasis skatina aldosterono sintezę ir yra viena stipriausių kraujo spaudimą didinančių medžiagų (detaliau skyriuje Natrio, kalio ir chloridų apykaita, jos reguliavimas, sutrikimai ir laboratorinė diagnostika ). Be to, procesus inkstuose veikia nemažai kitose endokrininėse liaukose gaminamų hormonų: užpakalinės hipofizės dalies sekretuojamas antidiurezinis hormonas skatina vandens reabsorbciją; antinksčių žievės sekretuojamas aldosteronas veikia natrio ir vandens reabsorbciją; pastarojo sekrecija priklauso nuo angiotenzino II; prieskydinių liaukų sekretuojamas paratiroidinis hormonas skatina kalcio reabsorbciją inkstų kanalėliuose ir fosfatų ekskreciją. 80
82 Inkstų funkcija, jos tyrimas... Endokrininės inkstų funkcijos išlieka nepažeistos iki galutinių inkstų nepakankamumo stadijų. Svarbiausiosios inkstų funkcijos yra šios: vandens, elektrolitų, rūgščių ir šarmų pusiausvyros palaikymas; baltymų, aminorūgščių ir nukleorūgščių apykaitos produktų ekskrecija (svarbiausios yra šlapalas, kreatininas, šlapimo rūgštis), aktyviųjų medžiagų, turinčių hormonų savybių, sintezė. Šlapimo susidarymas Šlapimas susidaro inkstuose vykstant kraujo filtracijai glomeruluose, susidariusio filtrato kai kurių medžiagų reabsorbcijai ir (ar) jų sekrecijai inkstų kanalėliuose. Pirminis šlapimas praktiškai yra identiškas kraujo plazmai be baltymų. Jame yra gliukozės, aminorūgščių, nedidelės molekulinės masės baltymų, fosfatų ir kitų medžiagų. Kanalėliuose prasideda reabsorbcijos procesas ir į organizmą grįžta tos medžiagos, kurių netekimas būtų nepageidaujamas organizmui: gliukozė, smulkiadispersiai baltymai, rūgštieji karbonatai, vanduo ir kitos. Be to, kai kurios medžiagos ne tik filtruojamos, bet inkstų kanalėlių ląstelių netgi aktyviai sekretuojamos. Tokiu būdu skiriasi vandenilio, kalio jonai, egzogeninis kreatininas, rūgštys, šarmai, hipuro rūgštis, kai kurie vaistai (pvz., penicilinas), dažai (pvz., kontrastinės medžiagos). Šlapimo rinkimas ir tyrimas Apie inkstų funkciją sprendžiama vertinant glomerulų ir kanalėlių funkcijas, atliekant šlapimo tyrimą. Viena didžiausių tyrimų klaidų, matuojant bet kurio metabolito ekskreciją su šlapimu ar nustatant kreatinino klirensą, yra susijusi su paros šlapimo surinkimu. Visada būtina išaiškinti ligoniui, kaip tinkamai surinkti paros šlapimą, ir įsitikinti, kad tai atlikta teisingai (detaliau skyriuje Tiriamosios medžiagos ėmimas, ruošimas ir analizė ). Paciento šlapimo tyrimas neturi apsiriboti vien biocheminių rodiklių nustatymu (ph, osmoliališkumo, baltymo, šlapalo, kreatinino, gliukozės). Dar įvertinama jo spalva, išmatuojamas tūris, mikroskopuojamos nuosėdos (ląstelės, cilindrai, kristalai, bakterijos). Inkstų glomerulų funkcijos tyrimas Glomerulų filtratas yra plazmos ultrafiltratas ir jo sudėtis yra tokia pat, kaip ir plazmos be didžiosios dalies baltymų. Plazma filtruojama glomeruluose apie 140 ml/min. greičiu. Normalus glomerulų filtracijos greitis (GFG) priklauso nuo normalios kraujo tėkmės inkstuose ir kraujo spaudimo. GFG tiesiogiai priklauso nuo kūno masės (vyrų yra didesnis negu moterų) ir amžiaus (su amžiumi mažėja). Jei GFG mažėja dėl inkstų aprūpinimo krauju sutrikimo ar dėl nefronų destrukcijos sergant inkstų ligomis, tai kraujyje sulaikomi galutiniai medžiagų apykaitos 81
83 produktai. Dėl lėtinių ligų pasiekiama nauja stabili būklė, kai nusistovi padidėjusios šlapalo ir kreatinino koncentracijos kraujo serume. Progresuojant inkstų ligoms, šlapalo ir kreatinino koncentracijos vėl laipsniškai didėja. Klirensas. Svarbus rodiklis glomerulų filtracijos greitis. Kaip jis matuojamas? Tam reikia aptarti klirenso terminą, ir kaip pavyzdys gali būti panaudota bet kuri plazmos sudėtinė medžiaga, kurios yra ir šlapime. Išskiriamą tam tikros medžiagos kiekį galima apskaičiuoti nustačius jos koncentraciją šlapime (Š, mmol/l) ir padauginus šį dydį iš surinkto per laiko vienetą šlapimo tūrio (V, litrai/24 val.). Taigi ekskretuotos su šlapimu medžiagos kiekis bus lygus Š V. Plazmos tūris, kuriame būtų toks medžiagos kiekis, gaunamas dalijant ekskretuotos medžiagos kiekį (Š V) iš tos medžiagos koncentracijos kraujo plazmoje (P): Plazmos tūris =. Taigi terminas klirensas apibūdina medžiagos pašalinimą iš kraujo inkstuose ir apibrėžiamas kaip ekvivalentiškas kraujo plazmos tūris (ml), kuris inkstuose visiškai apsivalo nuo tos medžiagos per laiko vienetą (min.) (išreiškiamas ml/min.). Maksimalus greitis, per kurį plazma apsivalo nuo tam tikros medžiagos, yra lygus GFG. Jį galima apskaičiuoti pagal klirensą medžiagos, kurios koncentracija kraujo plazmoje yra identiška jos koncentracijai glomerulų filtrate ir kuri nėra nei reabsorbuojama, nei sekretuojama tai glomerulų filtracijos greičio matas. Šiam tikslui galima naudoti kreatininą (endogeninį) ar inuliną (tai augalinis angliavandenis, kurio molekulinė masė yra 5100 daltonų). Pastarųjų sušvirkščiama ir po to matuojamas GFG. Inulino klirensas yra filtracijos vienetas, nes ši medžiaga nei reabsorbuojama, nei sekretuojama, o tik filtruojama. Tačiau praktikoje tam dažniausiai naudojamas endogeninis kreatininas, kuris jau yra kraujyje kaip raumenų kreatinfosfato apykaitos produktas ir atitinka beveik visus pirmiau išvardytus reikalavimus. Jei medžiaga visa filtruojama ir paskui reabsorbuojama, tai jos klirensas bus mažesnis už inulino (pvz., gliukozės klirensas yra lygus 0). O medžiaga, kurios klirensas viršija inulino klirensą, yra dar ir sekretuojama (pvz., egzogeninio kreatinino, amonio, vandenilio, kalio jonai). Klirensas yra proporcingas glomerulų skaičiui ir dydžiui, o šie inkstų parenchimos masei. Todėl paprastai klirensas yra standartizuojamas dauginant iš faktoriaus : tai vidutinis normalus kūno plotas (1,73 m 2 ), padalytas iš individo kūno ploto. Kreatinino klirensas. GFG gali būti apskaičiuotas pagal kreatinino kiekį, esantį 24 val. (paros) šlapime, ir jo koncentraciją plazmoje per šį laiko tarpą (kraujas imamas šlapimo rinkimo pradžioje ir pabaigoje). Plazmos apsivalymas nuo kreatinino (klirensas) tiesiogiai atspindi GFG, jeigu: 82
84 Inkstų funkcija, jos tyrimas...! 1) tiksliai surinktas paros šlapimas; 2) šlapime nėra ketoninių medžiagų ar didelės proteinurijos, kuri gali paveikti kreatinino tyrimo rezultatą. GFG yra apskaičiuojamas formule GFG = ; čia: Š kreatinino koncentracija šlapime, P kreatinino koncentracija kraujo plazmoje ar serume, V per 24 val. surinkto šlapimo tūris; šis dydis yra dalijamas iš dydžio: (24 60=1440 min.), nes GFG dažniausiai išreiškiamas ml/min. Matavimo vienetai turi būti tie patys. Kreatinino koncentracija šlapime išreiškiama mmol/l, serume µmol/l; taigi apskaičiuojant pirmąjį dydį reikia dauginti, o antrąjį dalyti iš Kraujo serumo kreatininas ir šlapalas. Kreatinino ir šlapalo koncentracijos kraujo serume yra naudojamos kaip patogus, nors ir nejautrus glomerulų funkcijos vertinimo metodas. Glomerulų filtracijos greitis sumažėja beveik perpus, kol yra ryškesnis kreatinino kiekio serume padidėjimas. Taigi normalus serumo kreatininas ne visada reiškia, kad viskas yra gerai. Rekomenduojamos ribos įvairuoja pagal amžių ir kūno masę. Vertinant kreatinino klirensą svarbu prisiminti, kad glomerulų filtracijos greitis mažėja su amžiumi, todėl kreatinino klirensas gali sumažėti beveik perpus, o kraujyje jo koncentracija labiau ir nepadidėti. Taip yra dėl to, kad su amžiumi dėl raumenų atrofijos mažėja kreatinfosfato susidarymas. Sumažėjus apie 50 70% glomerulų filtro plotui, kreatinino klirensas gerokai sumažėja. Serumo šlapalo koncentracija, atspindinti glomerulų filtraciją, yra nelabai vertingas diagnozei dydis. Šlapalo koncentracijai serume nemažos įtakos turi su maistu vartojamų baltymų kiekis. Šlapalas yra reabsorbuojamas inkstų kanalėliuose. Ši reabsorbcija didėja esant nedideliam šlapimo tekėjimo greičiui. Dažniausiai vertinant inkstų ligas nustatoma tiek kreatinino, tiek šlapalo koncentracija. Cistatinas C tai proteazių inhibitorius, kurio koncentracija kraujyje yra gana pastovi. Dėl savo mažos molekulinės masės jis inkstų glomeruluose yra laisvai filtruojamas, ir buvo siūloma jį naudoti kaip alternatyvų glomerulų filtracijos greičio rodiklį. Nurodomi šie cistatino C nustatymo pranašumai prieš kreatininą: jo dydis nepriklauso nuo amžiaus ir lyties, jam neturi poveikio raumenų masė ar kiti išoriniai veiksniai. Tačiau šis rodiklis susijęs su kai kuriomis problemomis, pavyzdžiui, nustatyta, kad nedidelis cistatino C kiekis yra reabsorbuojamas proksimaliniuose inkstų kanalėliuose, taigi ir šio rodiklio taikymas turi spragų. Vadinasi, cistatinas C gali būti naudojamas kaip alternatyvus glomerulų filtracijos greitį atspindintis ir papildomos informacijos suteikiantis rodiklis. Rekomenduojama kraujo serumo cistatino C koncentracija yra 0,53 0,95 mg/l. 83
85 Gl o m e r u l ų filtracijos su m a ž ė j i m o pr i e ž a s t y s ir laboratorinė diagnostika Skiriamos šios glomerulų filtracijos sumažėjimo priežastys: prereninės, kai sutrikęs (sumažėjęs) inkstų aprūpinimas krauju dėl širdies nepakankamumo, hipotonijos, ištikusio šoko, netekus vandens; reninės, kai susiaurėjusios inkstų kraujagyslės dėl organinių inkstų kraujagyslių ligų, ar sumažėjęs glomerulų tinklo plotas; postreninės dėl padidėjusio kapsulinio spaudimo susiformavus cilindrams, esant akmenims, spaudžiant navikams. Sergant daugeliu inkstų ligų, išsivysto proteinurija, tačiau ji galima ir sveikiems asmenims ar yra nesusijusi su inkstų ligomis. Nustačius proteinuriją, ligonis turi būti tiriamas toliau ieškant priežasties. Proteinurija ir jos rūšys. Sveikų asmenų inkstų glomerulų membrana nepraleidžia baltymų. Tačiau nedidelės molekulinės masės baltymai (jų molekulinė masė yra mažesnė negu daltonų) filtro barjerą praeina, o didesnės molekulinės masės baltymai yra sulaikomi. Vidutinio dydžio baltymų, pvz., albuminų, filtracijos greitis priklauso nuo jų krūvio: kuo didesnis neigiamas baltymo krūvis, tuo sunkiau jie įveikia ląstelių membraną. Dėl šios selektyviosios filtracijos baltymų sudėtis šlapime skiriasi nuo jų sudėties plazmoje. Dauguma šlapimo baltymų yra nedidelės molekulinės masės, nedaug yra vidutinio dydžio baltymų (priklausomai nuo jų krūvio) ir visai nėra didelės molekulinės masės baltymų. Procesas, kai pakinta šių baltymų proporcijos ir šlapime daugėja vidutinio dydžio baltymų molekulių, vadinamas selektyviąja proteinurija, o didelės molekulinės masės baltymų molekulių atsiradimas šlapime neselektyviąja proteinurija. Didelė dalis baltymų, kurie patenka į glomerulų filtratą, yra reabsorbuojami proksimaliniuose inkstų kanalėliuose ir jų ląstelėse suskaidomi. Galutiniame šlapime yra mažiau negu 1% filtruotų baltymų, be to, kanalėliuose yra ir nereabsorbuotų baltymų bei apatinių šlapimo takų baltymų. Todėl visada būtina nustatyti baltymų kiekį 24 valandas rinktame šlapime. Albuminai 24 valandas rinktame šlapime sudaro apie 10 15% (2 20 mg/l, arba mažiau negu 25 mg/24 val.). Fiziologinės proteinurijos viršutinė riba yra apie 100 mg/l (<0,1 g/l). Dėl tokio mažo baltymo kiekio rekomenduojama nustatyti baltymų kiekį 24 valandas rinktame šlapime. Rytinis šlapimas yra labiau koncentruotas, todėl rekomenduojama tirti kitą po rytinio šlapimo porciją. Esant pažeistai glomerulų membranai, šlapime randama daug baltymų jų kiekis paros šlapime viršija 250 mg. Ortostatinė proteinurija (proteinurija stovint) yra gana dažna paaugliams. Šiuo atveju proteinurija yra gerybinė (laikina, atsiranda ilgai stovint). Jos priežastis yra inkstų venose padidėjęs hidrostatinis slėgis. 84
86 Inkstų funkcija, jos tyrimas... Juostelėmis galima nustatyti proteinuriją, kuri viršija mg/l. Norint aptikti mažesnes baltymų koncentracijas, būtina taikyti jautresnius baltymų nustatymo šlapime metodus. Nedidelio laipsnio albuminurijoms (juostelėmis nenustatomoms) apibūdinti pasiūlytas lingvistiškai nelabai tikslus terminas mikroalbuminurija. Jis reiškia nedidelę albuminų ekskreciją su šlapimu apie mg/l ( mg/ 24 val.; normaliai neturi viršyti 30 mg/l.) Nustačius mikroalbuminuriją galima anksti įvertinti diabetinę ar hipertenzinę nefropatiją, kai gydant dar įmanoma sustabdyti ligos progresavimą ir neleisti vystytis inkstų nepakankamumui. Pagal išskiriamo baltymo kiekį proteinurija gali būti: silpna, kai baltymo kiekis yra mažesnis negu 0,2 g/l, nuosaiki, kai proteinurija yra 0,2 1,0 g/l, vidutinė, kai baltymo kiekis yra 1,0 3,0 g/l, ryški, kai proteinurija yra didesnė negu 3,0 g/l. Skiriamos šios proteinurijos rūšys: 1) prereninė (ikiinkstinė) proteinurija. Esant šiai retai proteinurijai, su šlapimu skiriasi mažos molekulinės masės baltymai, kurių būna padaugėję kraujo plazmoje. Šių baltymų pasirodo šlapime, kai viršijamos jų reabsorbavimo galimybės. Tai Bens-Džonso proteinurija, hemoglobinurija, mioglobinurija. Šios rūšies proteinurija dažniausiai nustatoma esant širdies nepakankamumui, po miokardo infarkto, insulto, galvos smegenų traumos, operacijų, karščiuojant. Pagydžius pagrindinę ligą, proteinurija išnyksta; 2) glomerulinė (inkstinė) proteinurija yra dažniausia ir diagnostikai svarbiausia. Ji nustatoma, kai su šlapimu skiriasi vidutinės molekulinės masės baltymai (pvz., albuminai) dėl pirminės (pvz., glomerulonefritas) ar antrinės (pvz., cukrinis diabetas, hipertenzija) glomerulonefropatijos. Netinkamai gydant cukrinį diabetą, po 2 5 metų glomerulų pamatinė membrana sustorėja, pakinta jos pralaidumas. Albuminurija šiuo atveju yra tinkamas diagnostinis žymuo; 3) inkstų kanalėlių (tubulinė) proteinurija yra apibūdinama padidėjusiu mažos molekulinės masės baltymų (pvz., β 2 mikroglobulino, α 1 mikroglobulino) šalinimu dėl sumažėjusio reabsorbavimo kanalėliuose, esant normaliai glomerulinei jų filtracijai. Ši proteinurija būdinga ūminiam ir lėtiniam kanalėlių pažeidimui dėl endogeninių (pvz., eant hepatoreniniam sindromui) ar egzogeninių (pvz., švinas, kadmis, nefrotoksiniai antimikrobiniai ir antineoplaziniai vaistai) toksiškų organizmui (pažeidžiančių kanalėlius) medžiagų poveikio, taip pat dėl lėtinės intersticinės nefropatijos (pvz., per ilgai didelėmis dozėmis vartojant analgetikus). Galima skirti dar vieną kanalėlių proteinurijos rūšį sekrecinę proteinuriją, pvz., Tamo Horsfolo (Tamm Horsfall) proteinurija, kai kanalėlių ląstelės sekretuoja specifinį šlapimo takams baltymą uromukoproteiną. 85
87 4) mišrioji inkstų glomerulinė ir kanalėlių (tubuloglomerulinė) proteinurija nustatoma sergant ir pirminėmis, ir antrinėmis inkstų ligoms, kai kanalėliams tenka per didelis krūvis ir jie neatlaiko glomerulinės proteinurijos (>3 g/l) ar kai pažeisti ir glomerulai, ir inkstų intersticiumas. 5) postreninė (poinkstinė) proteinurija išsivysto, kai su šlapimu skiriasi visi kraujo plazmoje esantys baltymai (pvz., kraujuojant iš apatinių šlapimo takų). Kanalėlių (tubulinė) proteinurija aptariama tekste toliau. Api b e n d r i n i m a s Glomerulų filtracijos greitis, kaip ir širdies plakimo ar kvėpavimo dažnis, per dieną keičiasi. Glomerulų funkcijos vertinimas: kraujo plazmos filtravimo per inkstų glomerulų membranas pajėgumas gali būti įvertinamas matuojant endogeninio kreatinino klirensą, kuris atspindi filtracijos greitį glomeruluose; netinkamas šlapimo surinkimas lemia klaidas nustatant metabolitų išsiskyrimą su šlapimu per laiko vienetą; klirensas apibūdina medžiagos pašalinimą iš kraujo inkstuose ir apibrėžiamas kaip ekvivalentiškas kraujo plazmos tūris (ml), kuris inkstuose visiškai apsivalo nuo tos medžiagos per laiko vienetą (min.) ir išreiškiamas ml/min.; klirensas yra proporcingas glomerulų skaičiui ir dydžiui, o jie proporcingi ir inkstų parenchimos masei; serumo kreatinino koncentracija jautrus inkstų funkcijos rodiklis. Kreatinino koncentracija gali ir nepadidėti, o glomerulų filtracijos greitis gali sumažėti daugiau negu 50%, palyginti su norma. Jei serumo kreatinino koncentracija didėja, tai koncentracijos pokyčiai atspindi GFG pakitimus; kreatinino klirensas labai sumažėja, kai dėl ligos nefunkcionuoja apie 50 70% glomerulų filtro ploto; dėl savo mažos molekulinės masės cistatinas C inkstų glomeruluose gerai filtruojasi, todėl naudotinas kaip alternatyvus glomerulų filtracijos greičio rodiklis; didesniąją dalį šlapimo sudaro nedidelės molekulinės masės baltymai, mažesniąją vidutinio dydžio baltymų molekulės (priklausomai nuo jų krūvio) ir visai jame nėra didelės molekulinės masės baltymų; vidutinės molekulinės masės baltymų kiekio didėjimas šlapime vadinamas selektyviąja proteinurija, o didelės molekulinės masės baltymų atsiradimas šlapime neselektyviąja proteinurija; mikroalbuminurija reiškia nedidelę albuminų ekskreciją su šlapimu apie mg/l ( mg/24 val.); didelis baltymo kiekis šlapime rodo glomerulų pažeidimą. 86
88 Inkstų funkcija, jos tyrimas... Laboratoriniai tyrimai Kreatinino klirensas (endogeninio kreatinino klirensas) Tiriamoji medžiaga. Serumas, šlapimas. Rinkti tiksliais laiko intervalais (4, 12 ar 24 val.). Laikyti šaltai. Rekomenduojama reikšmė. Glomerulų filtracija ml/min., reabsorbcoja 97 99%. Su kiekvienu dešimtmečiu reikšmės mažėja 6,5 ml/min. (kūno paviršiaus plotas 1,73 m 2 ). Diagnostinė vertė. Didelis širdies minutinis tūris, nėštumas, nudegimai, apsinuodijimas anglies monoksidu, didelis baltymų kiekis maiste, hiperkatabolinės būklės, anemija. Sumažėjusi kraujotaka inkstuose: šokas, hemoragija, dehidratacija, įgimtas širdies nepakankamumas, glomerulonefritas, nefrozinis sindromas, pielonefritas, amiloidozė, ūminė kanalėlių disfunkcija, intersticinis nefritas, papilinė nekrozė, postreninė kliūtis šlapimui nutekėti; taip pat mažėja sergant maliarija, mieloma, esant antinksčių žievės hipofunkcijai, cistinozei, hepatolentikulinei degeneracijai, D vitaminui atspariam rachitui, sergant lėtine obstrukcine plaučių liga, kepenų nepakankamumu, eklampsija ir preeklampsija. Papildoma informacija. Prieš tyrimą pacientas turi pakankamai gerti skysčių, kad šlapimo tėkmė būtų >2 ml/min. Rezultatą koreguoti pagal tiriamojo kūno paviršiaus plotą. Tyrimo metu reikia vengti energingų fizinių pratimų, nerekomenduojama arbata, kava ir vaistai. Prieš tyrimą nutraukti gydymą AKTH, kortizonu, tiroksinu. Esant labai stipriam inkstų pažeidimui, serumo kreatinino kiekio matavimas geriau atspindi (ir yra indikuojamas) glomerulų filtracijos greitį negu kreatinino klirensas, kuris yra nenatūraliai (dirbtinai) didesnis negu tikroji klirenso reikšmė. Kreatinino klirensas nėra patikimas matuojant glomerulų filtracijos greitį, jei yra proteinurija ir toli pažengęs inkstų nepakankamumas. Inulino klirensas yra tinkamiausias tiriant glomerulų filtracijos greitį, bet nėra standartinio rutininio metodo. Tiriant šlapalo klirensą galima išmatuoti bendrą inkstų funkciją, bet ne glomerulų filtracijos greitį. Šiam tyrimui didelės įtakos daro šlapimo tėkmės greitis. V: aminorūgštys, furozemidas. V: nefrotoksiniai vaistai, praeinantis kanapių ir heroino poveikis, tiazidai. Mikroalbuminas Tiriamoji medžiaga. Šlapimas. Rekomenduojama reikšmė. Iki 30 mg/l. Diagnostinė vertė. Galutinėse inkstų pažeidimo stadijose, sergant cukriniu diabetu (ypač I tipo), hipertenzija. Pacientams, kuriems yra didelė mikroalbuminurijos išsivystymo tikimybė, dažniausiai serga jauname amžiuje prasidėjusiu cukriniu diabetu, jiems nustatoma retinopatija, padidėjęs kraujospūdis, šeiminė hipertenzija, padidėjęs glikozilinto hemoglobino kiekis. Papildoma informacija. Mikroalbuminas nerodo skirtingų albumino rūšių, bet tik labai mažą šalinamo albumino kiekį. Anksti aptikta mikroalbuminurija gali padėti nustatyti besivystančią nefropatiją. Mažinant kraujospūdį ir gerinant gliukozės koncentracijos kraujyje kontrolę, galima sustabdyti nefropatijos progresavimą. Reninas Tiriamoji medžiaga. Plazma (EDTA). Rekomenduojama reikšmė. Ramybėje 0,5 1,9 mg/l, po krūvio 1,9 6,0 mg/l. Diagnostinė vertė. Kartu esant antriniam aldosteronizmui: Hipertenzinės būklės: piktybinė ar labai sunki hipertenzija, vienos pusės inksto liga su piktybine ar sunkia hipertenzija, inkstų parenchimos ligos, reniną sekretuojantys navikai, geriamųjų kontraceptikų sukelta hipertenzija, feochromacitoma. Normotenzinės būklės (su edema): kepenų cirozė, hepatitas, nefrozė, įgimta širdies liga. 87
89 Hipokaleminės normotenzinės būklės: jukstaglomerulinių ląstelių hiperplazija (Barterio sindromas), kitos neoplazijos, kurių metu netenkama Na + ar K +. Alimentiniai sutrikimai netenkant elektrolitų. Be antrinio aldosteronizmo: Antinksčių žievės nepakankamumas, kalio išeikvojimas (alimentinis). Su antinksčių žievės liga: Hipertenzinės būklės: pirminis aldosteronizmas dėl antinksčių adenomos, pseudopirminis ar idiopatinis aldosteronizmas (dažniausiai abipusė antinksčių žievės hiperplazija), gliukokortikoidais užslopinamas aldosteronizmas, antinksčių vėžys, gaminantis mineralkortikoidų perteklių, antinksčių fermentų stoka, pasireiškianti kitų mineralkortikoidų padidėjusia sekrecija. Be antinksčių žievės ligos: Hipertenzinės būklės: pirminė hipertenzija esant mažam renino kiekiui; kai kuriems pacientams sergantiems parenchiminėmis inkstų ligomis; pseudohiperaldosteronizmas (Liddle sindromas), mineralkortikoidų vartojimas. Normotenzinės būklės: parenchiminės inkstų ligos, autonominės nervų sistemos sutrikimai esant kūno padėties hipotenzijai, vaistų sukelta adrenerginė blokada, hiperkalemija. Papildoma informacija. Renino kiekis priklauso nuo metodo, Na + ar K + kiekio, vandens apykaitos būklės, kūno padėties. Pvz., mažai druskos turinti dieta, vertikali kūno padėtis ir diuretikai didina renino kiekį. Su amžiumi ir vyrų, ir moterų renino aktyvumas mažėja, bet moterų yra kiek mažesnis. Moterų renino koncentracija yra maža folikulinės fazės metu, prieš pat ovuliaciją kyla ir kiekis išlieka didelis geltonkūnio fazėje. Nėščiųjų renino kiekis yra padidėjęs. Tyrimas naudingas vertinant gydymą mineralkortikoidais. V: chlorpropamidas, enalaprilis, estrogenai, hidralazinas, kaptoprilis, lizinoprilis, nifedipinas, (jauniems), nitroprusidas, oraliniai kontraceptikai, kalį išsaugantys diuretikai (spironolaktonas, triamterenas), tiazidiniai diuretikai. V: β adrenoblokatoriai, angiotenzinas (į veną), aspirinas, deoksikortikosteronas, indometacinas, kalio preparatai, metildopa, rezerpinas, saldymedžio ekstraktas. Detaliau apie su šlapimu išskiriamus baltymus rašoma skyriuje Žmogaus kraujo plazmos baltymai, jų tyrimas, klinikinis rezultatų interpretavimas. Inkstų kanalėlių funkcijos tyrimas Inkstų nefronų glomeruluose vyksta efektyvus kraujo plazmos filtravimas, dėl kurio organizmas apsivalo nuo galutinių apykaitos produktų ir jam toksiškų medžiagų. Kad iš organizmo nepasišalintų tokios svarbios medžiagos, kaip vanduo, natris, gliukozė ir aminorūgštys, turi efektyviai vykti reabsorbcija kanalėliuose. Palyginti su GFG (jį nustačius, vertinama glomerulų funkcija), kanalėlių funkcijai įvertinti tokio kiekybinio tyrimo nėra. Kai kurie kanalėlių funkcijos sutrikimai gali būti paveldimi, neretai jų pažaida yra antrinė, sukelta kitų priežasčių: apsinuodijimo sunkiaisiais metalais, nefrotoksinių vaistų ar amiloidozės. Viena labiausiai pažeidžiamų kanalėlių funkcijų šlapimo koncentravimo funkcija. Jei kanalėliai dirba gerai ir jei yra išskiriamas antidiurezinis hormonas, vanduo bus reabsorbuojamas. Tai galima įvertinti nustačius šlapimo osmoliališkumą ir jį palyginus su kraujo plazmos osmoliališkumu. Sveikam vidutinišką skysčių kiekį var- 88
90 Inkstų funkcija, jos tyrimas... tojančiam žmogui šlapimo ir plazmos osmoliališkumo santykis yra 1,0 3,0. Taigi šlapimas yra labiau koncentruotas negu plazma. Mažesnis už 1,0 (ar jam lygus) šlapimo ir plazmos osmoliališkumo santykis rodo, kad inkstų kanalėliuose nereabsorbuojamas vanduo ir vystosi poliurija. Poliurijos priežastys yra šios: padidėjęs šlapimo osmosinis slėgis, pavyzdžiui, dėl jame esančios gliukozės, didesnis išgeriamo vandens kiekis, necukrinis diabetas (diabetes insipidus). Proteinurija. Kanalėlių proteinurija apibūdinama padidėjusiu mažos molekulinės masės baltymų (pvz., β 2 mikroglobulino, α 1 mikroglobulino) šalinimu dėl sumažėjusios reabsorbcijos kanalėliuose esant normaliam jų filtravimui glomeruluose. Taigi padidėjusi šių baltymų koncentracija šlapime yra jautrus inkstų kanalėlių pažaidos žymuo. Gliukozurija. Gliukozės buvimas šlapime, kai kraujyje gliukozės koncentracija normali, paprastai rodo, kad kanalėliai nesugeba reabsorbuoti gliukozės dėl specifinės kanalėlių pažaidos. Tai inkstų gliukozurija. Hiperaminoacidurija. Normaliai didžioji dalis aminorūgščių iš glomerulinio filtrato yra reabsorbuojama proksimaliniuose kanalėliuose (su šlapimu per parą išsiskiria ~1 g). Kai aminorūgšių koncentracija plazmoje viršija inkstų slenkstį ar kai sutrikusi jų reabsorbcija inkstų kanalėliuose, šlapime randamas didelis aminorūgščių kiekis rodo hiperaminoaciduriją. Taip gali būti esant paveldimam aminorūgščių apykaitos sutrikimui, pavyzdžiui, cistinurijai, ar dažniau dėl įgyto inkstų kanalėlių pažeidimo. Generalizuoto inkstų kanalėlių pažeidimo pavyzdys galėtų būti Fankonio sindromas. Jam būdinga acidozė inkstų kanalėliuose, hiperaminoacidurija ir kanalėlių proteinurija. Priežastis gali būti apsinuodijimas sunkiaisiais metalais, toksinų poveikis organizmui, paveldimos aminorūgščių apykaitos ligos (pvz., cistinozė). Inkstų akmenys. Inkstų akmenys sukelia didelį skausmą ir diskomfortą ir yra dažna šlapimo takų obstrukcijos priežastis. Akmenys gali būti sudaryti iš: kalcio fosfato: dažniausiai susidaro dėl pirminės hiperparatirozės ar acidozės inkstų kanalėliuose; magnio, amonio ir fosfato: pastarieji dažnai susiję su šlapimo takų infekcija; oksalato: dažniausiai dėl hiperoksalurijos; šlapimo rūgšties (uratiniai): dažniausiai dėl hiperurikemijos; cistino: šie akmenys yra reti ir būdingi paveldimai aminorūgščių apykaitos ligai cistinurijai. Svarbu nustatyti cheminę inkstų akmenų sudėtį ir išsiaiškinti jų susidarymo priežastis, nes tik tada galima tinkamai gydyti. 89
91 Api b e n d r i n i m a s Kanalėlių (tubulinė) proteinurijos vertinimas: cheminis šlapimo tyrimas yra tik vienas šlapimo analizės programos tyrimų; vertinant inkstų gebėjimą koncentruoti šlapimą, reikia nustatyti ir palyginti šlapimo ir serumo osmoliališkumą; inkstų gebėjimas koncentruoti šlapimą yra vertinamas atliekant specifinius tyrimus; inkstų kanalėlių pažaidą rodo specifiniai mažos molekulinės masės baltymai šlapime; inkstų akmenų cheminės sudėties nustatymas. Inkstų nepakankamumo laboratorinė diagnostika Inkstų nepakankamumas tai inkstų funkcijos praradimas. Esant ūminiam inkstų nepakankamumui (ŪIN), funkcija sutrinka greitai per kelias valandas ar dienas. Lėtinis inkstų nepakankamumas (LIN) vystosi mėnesiais ir metais, kol pasiekiama galutinė inkstų nepakankamumo stadija. Ūminis inkstų nepakankamumas gali būti grįžtamas, kai sunormalėja inkstų funkcija, ir lėtinis negrįžtamas. Ūminis inkstų nepakankamumas gali išsivystyti dėl įvairių priežasčių, pažeidžiančių inkstus ir (ar) jų kraujotaką. Dažniausiai išryškėja staigiu inkstų funkcijos blogėjimu: greitai didėja šlapalo ir kreatinino koncentracijos kraujo serume, mažėja šlapimo kiekis vystosi oligurija (jo susidaro mažiau kaip 400 ml/24 val.). Jei ligonis visai neišskiria šlapimo, vystosi anurija. Inkstų nepakankamumo, kurį rodo uremija, priežastys gali būti šios: 1) prereninė (ikiinkstinė), kai inkstai nepakankamai aprūpinami krauju; 2) postreninė (poinkstinė), kai yra sutrikęs šlapimo nutekėjimas, pavyzdžiui, dėl obstrukcijos; 3) reninė (inkstinė), kai pažeidžiamas inkstų audinys; pastarosios priežastis įvairios inkstų ligos ar ilgai nepašalintos prereninės ar postreninės priežastys. Anamnezė ir ligonio apžiūra gali padėti nustatyti besivystantį ūminį inkstų nepakankamumą. Pirmiausia būtina nustatyti priežastis, kurias galima greitai pašalinti ir taip atnaujinti inkstų funkciją: išsiaiškinti susijusias sunkias ligas, vaistų poveikį. Per pirmas 24 val. nuo ūminio inkstų nepakankamumo pradžios pokyčių kraujo serume ar šlapime gali ir nebūti. Prereninės inkstų nepakankamumo priežastys yra susijusios su sumažėjusiu neląstelinio skysčio tūriu, pavyzdžiui, netekus kraujo, nudegus, užsitęsus vėmimui ar viduriavimui, kai sumažėja širdies išstumiamo kraujo tūris. Šiais atvejais sutrinka kraujo prietaka į inkstus, mažėja GFG. Atlikus laboratorinius tyrimus, bus nustatytas: 90
92 Inkstų funkcija, jos tyrimas... padidėjęs šlapalo ir kreatinino kiekis serume (dėl šlapalo reabsorbcijos kanalėlių ląstelėse jo koncentracija padidėja labiau negu kreatinino, kuris nėra taip greitai reabsorbuojamas; metabolinė acidozė, nes sutrinka inkstų gebėjimas šalinti vandenilio jonus; hiperkalemija, kuri išsivysto dėl sumažėjusio glomerulų filtravimo greičio ir acidozės; didelis šlapimo osmoliališkumas. Postreninės priežastys lemia nepakankamą inkstų funkciją sumažėjus efektyviajam filtraciniam spaudimui glomeruluose, pavyzdžiui, kai yra inkstų akmenys, navikai (pvz., gimdos kaklelio, prostatos ar šlapimo pūslės vėžys). Jei ūminio inkstų nepakankamumo priežastys nepašalinamos, vystosi ūminė inkstų kanalėlių (tubulinė) nekrozė. Be to, ūminė kanalėlių nekrozė gali išsivystyti staiga netekus kraujo, esant sunkiai traumai, sepsiniam šokui, sergant glomerulonefritu, vartojant nefrotoksinių vaistų. Esant pradinėms ūminės kanalėlių nekrozės stadijoms, plazmoje šlapalo ir kreatinino padaugėja menkai, o vėliau jų koncentracijos gerokai išauga per kelias dienas. Tuo ši būklė skiriasi nuo lėtinio inkstų nepakankamumo, kai šlapalo ir kreatinino koncentracijos didėja lėtai ištisus mėnesius ar metus. Pažymėtina, kad pradinėje ūminio inkstų nepakankamumo stadijoje šlapalo ir kreatinino koncentracijos gali būti normalios; kalio kiekis kraujo plazmoje greitai didėja vyraujant katabolizmui ir sparčiai mažėja sunormalėjus šlapimo tekėjimo greičiui. Sveikimo fazėje didėjant GFG šlapalo ir kreatinino koncentracija kraujo plazmoje mažėja; kalio koncentracija, atsinaujinant kanalėlių funkcijai, taip pat sunormalėja. Lėtinis inkstų nepakankamumas yra progresuojanti negrįžtamoji inkstų audinio destrukcija, kuri, negydant dialize ar transplantacija, baigiasi mirtimi. Lėtiniu inkstų nepakankamumu gali komplikuotis visos inkstų ligos. Inkstų nepakankamumas vystosi dėl nefronų pažeidimo ir praradimo. Iš pradžių simptomų gali nebūti ar būti tik keletas, kol glomerulų filtracijos greitis tampa mažesnis kaip 15 ml/min. (10% jų normalios funkcijos). Kai inkstų nepakankamumo stadija galutinė, pažeidžiamos visos inkstų funkcijos ir tai sutrikdo daugelio medžiagų apykaitą, ypač mineralinių. Natrio ir vandens apykaita. Lėtiniu inkstų npakankamumu sergančių ligonių inkstuose natrio jonai yra reabsorbuojami, bet inkstų kanalėliai nereabsorbuoja vandens, taigi nekoncentruojamas šlapimas. Dėl to atsiranda poliurija. Kadangi vandens reabsorbcija yra sutrikusi, ligonių organizme kaupiasi vanduo (dėl polidipsijos). Kalio apykaita. Hiperkalemija yra progresuojančio lėtinio inkstų nepakankamumo požymis. Tai gyvybei grėsminga būklė. Mažėjant glomerulų filtracijos greičiui, mažiau šalinama kalio ir jo koncentracija plazmoje gali greitai padidėti. 91
93 Rūgščių ir šarmų pusiausvyra. Įsigalint lėtiniam inkstų nepakankamumui, inkstuose nebesulaikomi rūgštieji karbonatai ir nešalinami vandenilio jonai. Kaupiantis vandenilio jonams, vystosi metabolinė acidozė. Kalcio ir fosfatų apykaita. Progresuojant kanalėlių pažeidimui, inkstų ląstelės 25-hidroksicholekalciferolio neverčia 1,25-dihidroksicholekalciferoliu (detaliau skyriuje Kalcio ir fosforo apykaita, jos sutrikimai ir laboratorinė diagnostika ). Tada sumažėja kalcio absorbcija žarnyne ir reabsorbcija inkstuose vystosi hipokalcemija. Stengiantis papildyti kalcio kiekį plazmoje, skatinama paratiroidinio hormono sekrecija. Kraujyje padidėjusi parathormono koncentracija kenkia kaulam antrinis hiperparatiroidizmas gali sukelti inkstinę osteodistrofiją. Eritropoetino sintezė. Su lėtinėmis inkstų ligomis dažnai susijusi anemija. Normochrominė normocitinė anemija vystosi dėl sutrikusios eritropoetino gamybos. Klinikiniai požymiai. Progresuojant lėtiniam inkstų nepakankamumui, atsiranda patologinių požymių, nes inkstai nešalina įvairių organizmui toksiškų metabolitų ir dėl to sutrinka visų organų bei sistemų funkcijos. Pažeidžiama: centrinė ir periferinė nervų sistema prasideda letargija, periferinė neuropatija; virškinimo organų sistema atsiranda pykinimas, vėmimas, anoreksija; raumenų ir kaulų sistema, dėl to sulėtėja augimas, atsiranda miopatija, kaulų skausmai; lytinių ir šlapimo organų sistema vystosi impotencija, nikturija; širdies ir kraujagyslių sistema vystosi hipertenzija, perikarditas; oda atsiranda niežulys, purpurinis bėrimas. Dėl lėtinio inkstų nepakankamumo daugiau šlapimo susidaro gulint ar naktį. Jei dieną ir nėra poliurijos, galima nikturija. Biocheminiai laboratoriniai tyrimai labai padeda vertinti ligos sunkumą, koreguoti ir vertinti gydymo veiksmingumą. Daugumai pacientų yra būtinos dializės. Po sėkmingos transplantacijos inkstų funkcija sunormalėja. Hemodializė ir peritoninė dializė gali palaikyti ir pailginti gyvenimą, kai jau kitos gydymo priemonės neužtikrina skysčių, elektrolitų, rūgščių ir šarmų pusiausvyros. Gydant dialize naudojama pusiau pralaidi membrana, per kurią jonai ir mažos molekulės, kurių kiekis plazmoje yra padidėjęs, pereina į mažos koncentracijos plovimo skystį. Hemodializei naudojama dirbtinė membrana. Peritoninės dializės metu dializės skystis yra pilvaplėvės ertmėje ir molekulės juda iš pilvaplėvės sienelės kraujagyslių. Hemodializė ir peritoninė dializė gali palengvinti nemažai lėtinio inkstų nepakankamumo simptomų, išvalyti organizmo skysčius, grąžinti elektrolitų, rūgščių ir šarmų pusiausvyrą. Tačiau gydant šiuo būdu nesunormalėja pažeista medžiagų apykaita, neišvengiama endokrininių ir hematologinių lėtinio inkstų nepakankamumo padarinių. 92
94 Inkstų funkcija, jos tyrimas... Nors inkstų transplantacija atkuria beveik visas inkstų funkcijas, ligoniams būtina ilgą laiką vartoti imunosupresantus. Didelės ciklosporino koncentracijos veikia nefrotoksiškai, todėl būtina nuolat tirti kreatininą ir ciklosporiną kraujo serume, nes išlieka pavojus, kad inkstas arba bus atmestas, arba pažeistas. Api b e n d r i n i m a s Ūminis inkstų nepakankamumas yra per kelias valandas ar dienas išsivystantis inkstų funkcijos nepakankamumas, kurį galima konstatuoti remiantis kraujo serume didėjančiomis šlapalo ir kreatinino koncentracijomis. Ūminio inkstų nepakankamumo priežastys yra klasifikuojamos į prerenines, renines ir postrenines. Svarbu greitai nustatyti prerenines ar postrenines priežastis ir jas koreguoti, kol dar nepažeisti nefronai. Gydant ligonį būtina nuolat tirti kreatinino, natrio, kalio ir rūgščiųjų karbonatų koncentracijas kraujo serume, natrio ir kalio ekskreciją su šlapimu, taip pat osmoliališkumą. Gydant ligonį, sergantį inkstų liga, svarbu saikingai vartoti skysčius. Gyvybei pavojinga hiperkalemija yra ūminio inkstų nepakankamumo padarinys. Lėtinis inkstų nepakankamumas yra progresuojantis negrįžtamasis inkstų audinio pažeidimas dėl ligos, kuri, jei negydoma dialize ar inkstų transplantacija, baigiasi paciento mirtimi. Ligoniams, sergantiems lėtiniu inkstų nepakankamumu, simptomų gali ir nebūti, kol smarkiai nesumažėja GFG. Dėl lėtinio inkstų nepakankamumo sutrinka vandens ir natrio, kalcio ir fosforo apykaita, vystosi hiperkalemija ir anemija. Ūminė inkstų kanalėlių nekrozė yra dažniausia gyvybei pavojingos hiperkalemijos priežastis. Greitai didėjanti kalio koncentracija yra indikacija atlikti dializę. Hipertenzija yra inkstų ligos ir priežastis, ir pasekmė. Kraujospūdžio normos palaikymas yra vienas svarbiausių gydymo uždavinių ir gali pristabdyti lėtinio inkstų nepakankamumo progresavimą. 93
95 ŽMOGAUS KRAUJO PLAZMOS BALTYMAI, JŲ TYRIMAS, KLINIKINIS REZULTATŲ INTERPRETAVIMAS Bendrosios baltymų funkcijos Žmogaus organizmo pagrindą sudaro baltymai. Jie įeina į visų audinių sudėtį. Įvairių endogeninės ir egzogeninės kilmės medžiagų metabolizme dalyvauja baltymai, atliekantys specifines funkcijas (4 pav.). Žmogaus kraujo plazmoje yra apie 300 baltymų, kurie atlieka įvairias funkcijas. Daugelio baltymų funkcijos dar nenustatytos. Jie yra būtini žmogaus gyvybei palaikyti. Apie 90% bendrojo baltymo kiekio sudaro albuminai, imunoglobulinai, lipoproteinai, fibrinogenas, transferinas; kitų baltymų yra kur kas mažiau. Normaliai organizmo gyvybinei veiklai per parą su maistu vidutiniškai reikia gauti g baltymų. Bendrosios baltymų funkcijos yra šios: 1) palaiko koloidinį (onkotinį) slėgį ir kartu pastovų kraujo kiekį, nes, būdami koloidai, jie sujungia vandenį ir jį sulaiko. Taip pat baltymai lemia kraujo klampumą ir yra svarbūs hemodinamikai. Tuo požiūriu svarbiausi yra albuminai. Tačiau šiuose procesuose dalyvauja ir kiti panašios molekulinė masės baltymai; 2) pernašos (transportinė) funkcija čia svarbiausi yra albuminai. Jie sujungia daugelį medžiagų (riebalų rūgštis, bilirubiną), taip pat vaistus ir išnešioja šias medžiagas po organizmą. Pernašos baltymai tai haptoglobinas, transferinas, hemopeksinas, retinolį sujungiantis baltymas ir kiti; jie perneša tam tikras medžiagas; 4 pav. Žmogaus kraujo plazmos baltymų santykinis kiekis ir funkcijos 94
96 Žmogaus kraujo plazmos baltymai... 3) sujungia katijonus ir taip palaiko pastovią jų koncentraciją. Pavyzdžiui, 40 50% kalcio kraujo plazmoje yra sujungto su baltymais; taip pernešama geležis, magnis, varis ir kiti elementai; 4) kai kurie kraujo plazmos baltymai reikalingi kraujo krešėjimui tai kraujo plazmos krešėjimo faktoriai (pvz., fibrinogenas), krešulio hidrolizei veikia tirpinant krešulį (pvz., plazminogenas), ir kaip šių sistemų inhibitoriai; 5) palaiko pastovų kraujo ph, nes sudaro buferinių sistemų pagrindą; 6) apsauginė funkcija, kurią atlieka specifiniai baltymai imunoglobulinai, komplemento komponentai ir pagrindiniai apsauginiai baltymai: C reaktyvusis baltymas, α 1 rūgštusis glikoproteinas ir kiti vadinamieji ūminės fazės baltymai, proteazių inhibitoriai (α 1 antitripsinas, α 2 makroglobulinas). Tai nespecifiniai apsauginiai baltymai; 7) kraujo plazmos baltymai yra aminorūgščių šaltinis; 8) reguliacinė funkcija, kurią atlieka hormonai baltymai, polipeptidai ir oligopeptidai; 9) fermentinė funkcija visi kraujyje esantys fermentai yra baltymai tai ceruloplazminas, komplemento komponentai ir kiti. Kraujo plazmos baltymus galima suskirstyti į tris pagrindines funkcines grupes. Dvi iš jų sudaro tikrieji kraujo plazmos baltymai, kurie sekretuojami iš ląstelių į plazmą, kur ir atlieka savo funkcijas. Tokie yra pernašos ir apsauginiai baltymai. Trečioji grupė tai šimtai ląstelinių baltymų, kurių aptinkami tik pėdsakai. Jų atsiranda kraujyje pažeidus ląstelės membranas. Tai fermentai, svarbūs ligų diagnostikai. Pernašos (transportinių) baltymų grupei priklauso albuminai, lipoproteinai, transferinas, haptoglobinas, prealbuminai, hemopeksinas, hormonų ir vitaminų nešėjai. Apsauginiams baltymams priklauso krešėjimo faktoriai, proteazių inhibitoriai (ūminės fazės baltymai), imunoglobulinai, komplemento baltymai. Kraujo plazmos baltymų frakcionavimas Kraujo plazmoje yra dvi grupės baltymų: albuminai ir globulinai. Klinikinės biochemijos laboratorijose įprastai nustatomos bendroji baltymų ir albuminų koncentracijos. Šių koncentracijų skirtumas atitinka globulinų koncentraciją. Elektroforezės metodu kraujo plazmos baltymus galima suskirstyti į frakcijas, o imunocheminiais metodais nustatyti individualius (specifinius) baltymus. Baltymai pasižymi amfoterinėmis savybėmis, t. y. turi rūgščiąsias karboksilo ir bazines amino grupes. Jas lemia polinių aminorūgščių radikalų grupės. Taigi baltymų krūvis priklauso nuo tirpalo ph, ir tai svarbu frakcionuojant baltymus elektroforezės metodu (į klinikinę praktiką įdiegtas apie 1950 metus). Frakcionavimo medžiaga gali būti popierius, acetatceliuliozės plėvelės (išsiskiria 5 frakcijos), agaras 95
97 (išsiskiria 6 7 frakcijos), krakmolas, poliakrilamidas (išsiskiria frakcijų ir daugiau), agarozė. Globulinų (α 1, α 2, β 1, β 2, γ) frakcijas sudaro dešimtys individualių plazmos baltymų, kurie elektros lauke migruoja panašiu greičiu, kai ph 8,6 (7 lentelė). 7 lentelė. Pagrindinių kraujo plazmos baltymų pasiskirstymas frakcijomis Baltymų frakcijos Kraujo plazmos baltymai Albuminas Globulinai: α 1 α 2 β 1 β 2 γ Elektroforezė agarozės gelyje (% bendrojo baltymo kiekio) , Koncentracija, g/l Dar tikslesni metodai, kuriais išskiriami individualūs baltymai, yra pagrįsti imuninėmis baltymų savybėmis (imunoelektroforezė, imunofermentinis tyrimas ir kt.). Atliekant imunoelektroforezę, kurios pagrindas baltymų krūvis ir imuninės savybės, ir naudojant specifinius antiserumus, gaunami precipitacijos žiedai arba linijos, atitinkantys individualių baltymų kiekį. Kiti individualių serumo baltymų nustatymo metodai yra nefelometrinis antigeno ir antikūno komplekso tyrimas, radialinė imunodifuzija (G. Mancini metodas), raketinė imunoelektroforezė, imunoprecipitacija ir kiti. Jais galima nustatyti net ir labai mažą baltymų kiekį. Albuminai ir fibrinogenas, taip pat 75 90% α globulinų, 50% β globulinų yra sintetinami kepenyse. Kiti baltymai, kaip ir γ globulinai, sintetinami ekstrahepatiniuose audiniuose: γ globulinai plazminėse ląstelėse, specifiniai baltymai, pavyzdžiui, hormonai, endokrininėse liaukose, fermentai įvairiuose audiniuose. Toliau pateikiami pagrindiniai žmogaus kraujo plazmos baltymai, jų savybės ir funkcijos (8 lentelė). 8 lentelė. Pagrindiniai kraujo plazmos baltymai ir jų funkcijos Baltymas (skliaustuose sinonimai) Normalus kiekis kraujo plazmoje (serume), g/l (vidurkis) Prealbuminai 0,2 0,4 (0,3) Albuminai (~44) Elektroforezinis judrumas Molekulinė masė (daltonais) Funkcijos Sujungia ir perneša tiroksiną, retinolį Reguliuoja osmosinį slėgį; perneša riebalų rūgštis, bilirubiną, aldosteroną, vaistus, kontrastines medžiagas, anijonus, katijonus; yra aminorūgščių šaltinis. 96
98 Žmogaus kraujo plazmos baltymai... 8 lentelės tęsinys Baltymas (skliausteliuose sinonimai) α 1 rūgštusis glikoproteinas (orozomukoidas; α 1 seromukoidas) Normalus kiekis kraujo plazmoje (serume), g/l (vidurkis) α 1 0,5 1,2 (0,85) α 1 antitripsinas α 1 0,9 2,0 (1,45) α 1 antichimotripsinas Retinolį sujungiantis baltymas Tiroksiną sujungiantis baltymas α 1 0,3 0,6 (0,45) Elektroforezinis judrumas Molekulinė masė (daltonais) Funkcijos Ūminės fazės baltymas; padaugėja vykstant uždegiminei degeneracijai, neoplazijai; inaktyvina progesteroną; slopina trombocitų agregaciją Ūminės fazės baltymas; proteazių inhibitorius; inaktyvuoja proteolizinius fermentus (tripsiną, elastazę) Ūminės fazės baltymas; slopina chimotripsiną. α 1 0,03 0, Perneša retinolį. α 1 0,01 0, Sujungia ir perneša trijodtironiną ir tiroksiną (kartu su vienu iš prealbuminų) ir reguliuoja laisvo tiroksino kiekį kraujo plazmoje. Transkortinas α 1 0,03 0, Sujungia ir perneša kortizolį ir kortikosteroną. Transkobalaminas α 1 0,00044 Perneša B 12 vitaminą. I ir II α fetoglobulinas (α fetoproteinas) α lipoproteinai (didelio tankio lipoproteinai, DTL) α 1 Naujagimių 0,1; Suaugusiųjų <10 µg/l α 1 2,5 7,7 (3,6) Vaisiaus organizme iš dalies pakeičia albuminą, perneša hormonus, fermentus, sujungia steroidus, riebalų rūgštis, varį, triptofaną; yra imunosupresantas (apsaugo vaisių nuo motinos imuninio atsako) Perneša cholesterolį, kitus lipidus, riebaluose tirpius vitaminus. Gc globulinas α 1 0,2 0, Sujungia ir perneša D 3 vitaminą. Protrombinas α 1 0,05 0, Krešėjimo baltymas. (0,08) Ceruloplazminas α 2 0,2 0,6 (0,3) Ūminės fazės baltymas; perneša varį ir reguliuoja jo kiekį kepenyse; pagerina geležies naudojimą veikdamas kaip feroksidazė (oksiduojantis fermentas). Antitrombinas III α 2 0,2 0, Proteazių inhibitorius; inaktyvina krešėjimo baltymus: trombiną, IXa, Xa faktorius. Veikia prisijungdamas prie glikozaminoglikanų (pvz., heparinas). Haptoglobinas (α 2 seromukoidas) Tipai: Hp 1-1 Hp 2-1 Hp 2-2 α 2 0,3 2, Ūminės fazės baltymas; sujungia ir perneša laisvąjį hemoglobiną, susidariusį suirus eritrocitams. 97
99 8 lentelės tęsinys Baltymas (skliausteliuose sinonimai) Normalus kiekis kraujo plazmoje (serume), g/l (vidurkis) α 2 makroglobulinas α 2 1,3 3 (2,15) Elektroforezinis judrumas Molekulinė masė (daltonais) Funkcijos Endopeptidazių inhibitorius (plazmino, tripsino); sujungia insuliną; svarbus motinos ir vaisiaus ryšiui; slopina komplemento komponentus. αα 2 HS glikoproteinas Vidinis α tripsino inhibitorius C reaktyvusis baltymas α 2 0,4 0,85 (0,6) α 2 0,2 0,7 (0,45) α 2 γ <0,005 (<5 mg/l) Šio baltymo pavadinimas tai autorių pavardžių sutrumpinimas (Heremans, Schmid); neigiamas ūminės fazės baltymas; kaulinio užpildo, dentino sudedamoji dalis Proteazių inhibitorius Ūminės fazės baltymas; dalyvauja imuninio atsako reakcijose; aktyvina fagocitozę, komplemento komponentus; slopina trombocitų agregaciją. Cholinesterazė α 2 0, Dalyvauja acetilcholino hidrolizėje. Eritropoetinas α 2 <0,005 mg/l Apie 90% susidaro inkstuose, kita dalis kepenyse. Dėl hipoksijos sintezė ypač suintensyvėja. Reguliuoja ląstelių pirmtakių diferenciaciją į eritroidino tipo ląsteles. Transferinas β 1 2,0 3,6 (2,8) β lipoproteinai (mažo tankio lipoproteinai, MTL) β 1 2,9 9,5 (5,3) Hemopeksinas β 1 0,5 1,15 (0,8) Plazminogenas β 1, β 2 0,006 0,25 (0,12) Sujungia ir perneša geležį (trivalentę) (normaliai ja prisotintas 30%) Perneša lipidus: cholesterolį, fosfolipidus, taip pat riebaluose tirpius vitaminus Sujungia ir perneša hemą Verčiamas plazminu (fibrinolizinu) ir tirpdo krešulius (hidrolizuoja fibriną). β 2 mikroglobulinas β 2 0,7 1,8 mg/l Žmogaus leukocitų antigeno (ŽLA) sudedamoji dalis, esanti ląstelių membranose. Fibrinogenas (kai kurie autoriai nurodo, kad jis juda su β 1 globulinais) β (3,0) Krešėjimo baltymas: veikiamas trombino virsta fibrinu; ūminės fazės baltymas. 98
100 Žmogaus kraujo plazmos baltymai...! 8 lentelės tęsinys Baltymas (skliausteliuose sinonimai) Komplemento komponentai C1 C1q C1r C1s C2 C3 C4 C5 C6 C7 γ globulinai (imunoglobulinai, Ig) α 2, β 1 β 1 β 1 β 1 β 1 β 2 β 2 Normalus kiekis kraujo plazmoje (serume), g/l (vidurkis) 0,1 0,2 0,1 0,05 0,015 0,6 1,4 0,1 0,4 0,08 0,075 0,055 IgG γ 7 16 (~70% bendro Ig kiekio) IgA γ Vyrų 0,7 3,7, moterų 0,88 4,1 γ Elektroforezinis judrumas Molekulinė masė (daltonais) Funkcijos Tai baltymai, kurie dalyvauja imuninėse reakcijose, formuoja nespecifinį atsparumą infekcijoms, dalyvauja audinių pažeidimo patogenezėje. Jie dalyvauja pirmoje fagocitozės stadijoje (chemotaksis) ir antroje stadijoje (tikroji fagocitozė), tirpdo imuninius kompleksus ir ląstelių membranas, neutralizuoja virusus ir atlieka kitas funkcijas. Antikūnai Pagrindiniai antikūnai, pereinantys placentos barjerą; antikūnai prieš bakterijas, virusus, toksinus; skatina fagocitozę; jiems priklauso Rh antikūnai, antinuklearinis veiksnys; Gm antigeninės determinantės pernašos baltymai ir polimerai Antikūnai prieš įvairius antigenus: virusus, toksinus, bakterijas; dominuojantis imunoglobulinas įvairiuose organizmo skysčiuose; seilėse, ašarose, virškinimo sultyse atsiranda anksčiau negu plazmoje. IgD γ 0,003 0, Sujungia komplemento sistemos baltymus; randamas limfocitų paviršiuje ir yra svarbus imunoglobulinų diferenciacijai, imunoreguliacijai. IgM γ Vyrų 0,4 2,4, moterų 0,34 2, Dalyvauja pirminio imuninio atsako reakcijose; natūralūs antikūnai, pvz., ABO izoagliutininai; antikūnai prieš gramneigiamus mikroorganizmus; autoantikūnai, pvz., reumatoidinis faktorius; Vasermano antikūnai, kt. IgE γ Iki 100 U/ml Antikūnai reaginai, sukeliantys bronchinę astmą, dilgėlinę ir kitas alergines ligas; susiję su putliosionis ląstelėmis. Daugeliui šių baltymų būdingas polimorfizmas jie turi po kelias ar keliolika genetiškai nulemtų formų. Pavyzdžiui, albumino yra žinoma apie 20 genetinių variantų, ceruloplazmino 6, haptoglobino 3 įprasti (Hp 1-1, Hp 2-1 ir Hp 2-2) ir dar keli reti variantai, transferino apie 20 variantų ir kt. 99
101 Ka i ku r i ų kr a u j o pl a z m o s ba l t y m ų sa v y b ė s, patologinė fiziologija Bendrasis baltymų kiekis. Viršijanti rekomenduojamas normos ribas kraujo plazmos bendroji baltymų koncentracija dažniausiai nustatoma esant paraproteinui, o sumažėjęs bendras baltymų kiekis dažniausiai sumažėjus albuminų koncentracijai. Albuminai. Šis terminas kilo iš lotynų kalbos žodžio albus, reiškiančio baltą arba tiesiog kiaušinio baltymą. Taip istoriškai buvo vadinami visi kraujo plazmos baltymai. Žmogaus kraujo plazmos albuminai tai baltymai, sudaryti iš 580 aminorūgščių liekanų; išsidėstant polipeptidinei grandinei erdvėje susidaro 17 disulfidinių jungčių. Tai vienas iš keleto plazmos baltymų, kurie nėra glikoproteinai ir turi palyginti nedidelę ( Da) molekulinę masę. Albuminai sintetinami kepenyse (per parą g); dėl kepenų ligų sutrikus sintezei, jų kiekis plazmoje sumažėja. 50% visų kepenyse sintetinamų baltymų sudaro albuminai (gyvavimo pusperiodis apie 20 dienų). Pagrindinė albuminų funkcija yra reguliuoti osmosinį slėgį (sudaro onkotinį slėgį). Nuo jų priklauso 75 80% osmosinio efekto plazmoje, nes sudaro daugiau kaip pusę plazmos baltymų ir turi nedidelę molekulinę masę. Kitą osmosinio efekto plazmoje dalį sukuria elektrolitai ir kiti baltymai. Edema ir šokas tai dvi patologinės būklės, atsirandančios dėl plazmos baltymų (albuminų) koncentracijos pakitimo ir sutrikusios vandens apykaitos. Tik apie 40% albuminų cirkuliuoja kraujyje, kita dalis yra už kraujagyslių, audiniuose, ypač raumenyse, odoje, žarnyne. Kas valandą apie 5% albuminų iš plazmos grįžta krūtininiu limfiniu lataku. Be osmoso palaikymo, albuminai yra labai svarbūs įvairių medžiagų nešikliai. Dauguma šių medžiagų blogai tirpsta vandenyje. Pavyzdžiui, normaliai lipidų apykaitai būtini albuminai, ypač laisvųjų riebalų rūgščių pernašai iš kepenų į periferinius audinius ir atgal. Albuminai sudaro tirpų kompleksą su bilirubinu ir neša jį į kepenų parenchimines ląsteles, varį ir kitus sunkiųjų metalų jonus (gyvsidabrį, nikelį ir kt.) į kepenis. Skirtingų medžiagų, pavyzdžiui, kalcio, steroidinių hormonų, triptofano, koncentraciją kraujo plazmoje reguliuoja jų sąveika su albuminais. Be to, su albuminais jungiasi daugelis vaistų (sulfanilamidai, penicilinas, aspirinas). Albuminų molekulėje yra dvi sujungimo zonos, arba centrai. Jei kelios medžiagos geba jungtis su albuminais, galima konkurencija dėl šių centrų. Tai svarbi farmakologinė savybė, nes kai kurios medžiagos, susijungusios su albuminais, netenka aktyvumo (pvz., sulfanilamidai antibakterinių savybių). Be to, skiriant naujagimiams sulfanilamidų, antibiotikų, šešis kartus padidėja hemolizinės geltos dažnumas. Priežastis ta, kad šie vaistai trukdo bilirubinui sąveikauti su albumi- 100
102 Žmogaus kraujo plazmos baltymai... nais. Taip padaugėja laisvojo bilirubino, kuris pažeidžia ląstelių membranas. Be to, naujagimių hematoencefalinis barjeras nėra visiškai susiformavęs; patekus į smegenis bilirubinui, sutrikdomi apykaitos procesai, vystosi encefalopatija. α 1 rūgštusis glikoproteinas (orozomukoidas). Tai mažos molekulinės masės ( Da) baltymas. Jame yra daug angliavandenių (42%), suteikiančių rūgščių savybių. Ankstesnis pavadinimas seromukoidas. Seromukoidai tai grupė baltymų, kurie nenusėda iš kraujo serumo esant ph 4,5 arba kaitinant, arba paveikus rūgštimis. Į šios grupės sudėtį įeina α 1 rūgštusis glikoproteinas, α 1 antitripsinas, haptoglobinas, C reaktyvusis baltymas ir net dalis albuminų. Visos seromukoidų sudedamosios dalys, išskyrus albuminus, yra glikoproteinai. Uždegimo metu ar po traumos α 1 rūgščiojo glikoproteino koncentracija padidėja 3 4 kartus. Kai kurie α globulinams priklausantys baltymai yra proteazių inhibitoriai. Tai α 1 antitripsinas (α 1 proteinazių inhibitorius), α 2 makroglobulinas ir vidinis α tripsino inhibitorius. Jie slopina tripsino, elastazės, chimotripsino, kolagenazės, trombino, plazmino, renino, iš dalies kalikreino aktyvumą, taip pat daugelio bakterinių ir granulocitų proteazių aktyvumą. Jie vadinami tiesiog antifermentais. Šie baltymai atlieka apsauginę funkciją, nes slopina proteolizinius fermentus, patenkančius į kraujotaką iš suirusių ląstelių. α 1 antitripsinas pasižymi dideliu polimorfizmu. Už jo sintezę atsakingi 24 aleliai, kurie sudaro proteazinio inhibitoriaus, arba Pi, sistemą. Labiausiai paplitęs Pi M alelis. Pi MM fenotipas leidžia sintetinti 2 4 g/l šio inhibitoriaus. Pi S ir Pi Z alelių gebėjimas sintetinti baltymą yra sumažėjęs, todėl heterozigotų ir ypač homozigotų, turinčių šiuos alelius, α 1 antitripsino kiekis yra sumažėjęs. Pavyzdžiui, Pi MS fenotipas sintetina 80% normalaus baltymo kiekio, fenotipas Pi MZ 57,5%, Pi SS 60%, o Pi ZZ tik 15%. Švedų statistikos duomenimis, Pi MZ fenotipo dažnis populiacijoje yra 4%, Pi ZZ 0,07%. Fenotipų elektroforezinis judrumas taip pat skiriasi: žinomi 43 α 1 antitripsino variantai. Įgimta α 1 antitripsino stoka pasitaiko 1 : : 5000 naujagimių Lietuvoje (Vilniaus universiteto Vaikų ligų klinikos prof. V. Basio duomenys). Pi ZZ fenotipo dažnis yra 1 : : 4000 naujagimių, heterozigotiniai geno nešiotojai (Pi MZ) sudaro 4,3% gyventojų. Visiška ar dalinė α 1 antitripsino stoka (ne MM fenotipas) sukelia kepenų, plaučių ligas (plaučių emfizemą, nes plaučių elastiną hidrolizina elastazė), kurios dažniausiai išryškėja sulaukus metų. Trečdaliui vaikų, kuriems trūksta α 1 antitripsino, nustatoma kepenų patologija (cirozė). Esant ūminėms uždegiminėms ligoms ir audinių nekrozei, šio baltymo kiekis labai padidėja. Taip pat jo padaugėja sergant B hepatitu ir, kaip minėta, kepenų ciroze, o kitų ūminės fazės baltymų tada nepadaugėja (haptoglobino net sumažėja). Svarbu 101
103 tai, kad metastazavimo pradžioje taip pat labai padidėja α 1 antitripsino koncentracija. Nurodoma, kad tai svarbus malignizacijos rodiklis. α fetoglobulinas. Tiksli šio baltymo funkcija nežinoma. Normalios būklės suaugusių žmonių kraujo plazmoje α fetoglobulino yra labai nedaug (<10 µg/l), nors jo koncentracija vaisiuje yra kur kas didesnė (didžiausia antrą nėštumo trimestrą); matyt, vaisiuje jis iš dalies pakeičia albuminus. α fetoglobulino kiekis labai padidėja esant įgimtiems nervinio vamzdžio nesuaugimo defektams, hepatomai. Ceruloplazminas. Šis baltymas pavadintas taip todėl, kad yra dangaus mėlynumo spalvos. Varis sudaro 0,34% jo molekulinės masės. 93% viso kraujyje esančio vario įeina į ceruloplazmino sudėtį. Be to, šis baltymas oksiduoja įvairius aromatinius fenolius, poliaminus, geležį ir todėl pagal veikimą yra feroksidazė. Šia prasme ceruloplazminas labai svarbus kraujodaros procesui. Daugiausia vario išsiskiria iš organizmo su tulžimi. Ūminėje uždegimo fazėje padaugėjus ceruloplazmino, padidėja teigiamas oksidacinis kraujo plazmos potencialas. Sergant reta Vilsono liga, plazmos ceruloplazmino kiekis labai sumažėja. Tada padaugėja vario, ypač smegenyse ir kepenyse, dėl to išryškėja neurologinė ir kepenų pažeidimo simptomatika. Haptoglobinas. Apie ketvirtadalis visų α 2 globulinų yra haptoglobinas (Hp), kuris sudaro su hemoglobinu specifinius stabilius molekulinius kompleksus santykiu 1 : 1. Šie kompleksai susidaro in vivo vykstant eritrocitų hemolizei kraujotakoje. Dėl didelės molekulinės masės šie kompleksai negali būti šalinami per inkstus (glomerulinis filtras jų nepraleidžia). Taip inkstai apsaugomi nuo žalojančio hemoglobino poveikio ir kartu išsaugoma jo geležis, nepašalinta per inkstus su šlapimu. Haptoglobino ir hemoglobino kompleksai yra katabolizuojami hepatocituose, blužnyje, kaulų čiulpuose, t. y. šių organų mononuklearinės fagocitinės sistemos ar dar kitaip vadinamos retikuloendotelinės sistemos (RES) Kupferio ląstelėse. Taigi, sergant įvairių rūšių hemolizine anemija, kraujyje yra mažas haptoglobino kiekis. Be to, haptoglobinui būdingas peroksidazinis aktyvumas. Haptoglobinas išsiskiria dar viena svarbia fiziologine funkcija: jis sudaro kompleksus su įvairiomis baltyminėmis ir nebaltyminėmis medžiagomis, kurios atsiranda yrant pažeisto audinio ląstelėms, iš jų ir proteazėms, pvz., su B ir D katepsinais ir kitais alternatyviais komplemento aktyvacijos komponentais. Be to, dėl uždegimo, traumos ar infekcijų didėja hemolizė. Haptoglobino dalyvavimas inaktyvuojant lizosomų fermentus yra labai svarbi jo, kaip ūminės fazės baltymo, funkcija. Žmogaus haptoglobinai sudaryti iš dviejų porų neidentiškų grandinių, sujungtų disulfidiniais ryšiais. Subvienetų struktūra žymima raidėmis α ir β. Skiriami trys genetiniai haptoglobinų tipai, žymimi Hp 1-1, Hp 2-1 ir Hp 2-2; jie skiriasi tik α grandinės struktūra. Šio baltymo α grandinės ir imunoglobulinų lengvosios gran- 102
104 Žmogaus kraujo plazmos baltymai... dinės turi tuos pačius determinantus, ir tai rodo, kad šių grandinių genas pirmtakas yra bendras. Žmogui yra būdingas tam tikras haptoglobino tipas. Tipus, jų paplitimą nagrinėja genetikai, atlikdami populiacijos tyrimus, taip pat teismo medikai, nustatydami tėvystę. Transferinas yra svarbus β frakcijos baltymas, sudarantis apie 3% visų plazmos baltymų. Pagrindinė jo funkcija yra sujungti ir pernešti Fe 3+ į audinius, ypač į mononuklearinę fagocitinę sistemą, kur geležis atpalaiduojama nepažeidžiant baltymo. Be to, transferinas gali sujungti varį ir cinką. Jis taip pat padeda reguliuoti laisvosios geležies koncentraciją plazmoje, taip išvengiant nepageidaujamo jos kaupimosi audiniuose ar netekimo per inkstus. Viena transferino molekulė prijungia du Fe 3+ atomus, bet tik esant CO 2. Sveikų asmenų tik apie trečdalis baltymo molekulių yra prisotintų geležies. Transferino kraujo plazmoje ypač padaugėja nėštumo metu, trūkstant geležies. Be to, transferinas svarbus ir kaip bakteriostatikas. Naujagimių kraujo plazmoje transferino kiekis sudaro apie 50% suaugusiems būdingo kiekio, pirmus 3 mėnesius dar mažėja, vėliau pradeda didėti. Hemopeksinas tai baltymas, sujungiantis hemą ir padedantis išvengti jo ekskrecijos su šlapimu. Taip organizme išsaugoma geležis. Albuminai irgi sujungia hemą, bet daug silpniau negu hemopeksinas. Nei hemoglobinas, nei citochromas C, nei bilirubinas neprisijungia prie hemopeksino. Hemopeksinas, išskirtas iš sveikų asmenų, nėra prisotintas hemo. Tačiau išskirtas iš hemolizine anemija sergančių ligonių kraujo, jis yra prisotintas hemo: vienai hemopeksino molekulei tenka vienas hemas. Hemopeksino ir hemo kompleksą iš kraujo šalina kepenys, kur hemo geležis atsipalaiduoja ir yra vėl panaudojama. C reaktyvusis baltymas (CRB) sintetinamas kepenyse. Sveikų asmenų kraujo plazmoje jo koncentracija yra labai maža, o ūminio uždegimo metu gali padidėti kartus, todėl priklauso ūminės fazės baltymų grupei (jo koncentracijos padidėjimas kraujyje yra kaip atsakas į uždegiminių citokinų, pvz., interleukino-6, sekreciją). Iki šiol nėra aprašyta CRB genetinė stoka, ir tai rodo, kad CRB būtinas gyvybei. Šio baltymo gyvavimo kraujyje pusperiodis apie 19 valandų. Baltymo pavadinimas kilo iš jo gebėjimo esant aplinkoje kalcio jonų sudaryti precipitatus su pneumokokų C grupės polisacharidu. CRB skatina fagocituojančiųjų ląstelių aktyvumą, dalyvauja aktyvinant komplementą ir, matyt, kartu su juo sudaro amiloidinį baltymą. Biologinės C reaktyviojo baltymo ir serumo amiloido P (kito ūminio uždegimo baltymo) funkcijos remiasi jų gebėjimu sujungti endogenines ir egzogenines medžiagas, paskatinti jų šalinimą iš kraujo ir audinių. Veikiant kalcio jonams CRB sujungia endogeninius negyvybingų audinių ląstelių produktus. Svarbiausi egzogeniniai 103
105 substratai, kuriuos inaktyvina (opsonizuoja) CRB, yra bakterijos, grybai ir parazitai (CRB sujungia neigiamą krūvį turinčias, pavyzdžiui, fosfatidilcholino, molekules, kurios yra membranos fosfolipidų komponentai); pastaruosius paskui šalina fagocitinės ląstelės. CRB ne visada didėja dėl virusinės ir spirochetinės infekcijos. Todėl nesant traumos labai didelis CRB kiekis gali rodyti bakterinę infekciją. Kai CRB sujungia minėtas endogenines ir egzogenines medžiagas, jis taip pat aktyvina komplemento sistemą, skatina fagocitozę, makrofagų veiklą. Rekomenduojama C reaktyviojo baltymo normos reikšmė neturi viršyti 5 mg/l, o diagnozuojant širdies ligas ne didesnė kaip 3 mg/l. Dauguma klinikinių tyrimų įrodė, kad aterominės plokštelės progresavimas ir plyšimas gali būti nuspėjami remiantis padidėjusia CRB koncentracija. Miokardo infarktas paprastai yra susijęs su padidėjusia CRB koncentracija prieš kelias valandas iki krūtinės skausmų pradžios: ji pradeda didėti po 4 6 val. nuo simptomų pradžios, maksimumas pasiekiamas 3 4 dieną, o grįžta į normą po 7 10 dienų (kai, pvz., kreatinfosfokinazės MB izofermento aktyvumas taip pat sunormalėja). Padidėjęs CRB kiekis, esant neaiškiems simptomams, yra jautrus pažeidimo žymuo, nustatomas 49 50% ūminiu miokardo infarktu sergančių ligonių ir 100% ištikus Q bangos miokardo infarktui. Jei CRB koncentracijos padidėjimas laikosi ilgiau nei 10 dienų, būtina įtarti komplikacijas, ir tai yra blogas prognozės požymis. Padidėjęs CRB kiekis stabilia ar nestabilia krūtinės angina sergantiems ligoniams rodo gręsiančias koronarines komplikacijas. Minėtų ligų rizika padidėja tris kartus, kai CRB koncentracija viršija 3,6 mg/l. Atliktas gydytojų sveikatos tyrimas parodė, kad matuojant CRB koncentraciją galima nuspėti miokardo infarktą ir insultą: kai CRB < 0,55 mg/l rizika lygi 1,0, kai CRB kiekis yra 1,15 2,10 mg/l rizika lygi 2,6, o kai CRB > 2,11 mg/l rizika lygi 2,9. Be miokardo infarkto, CRB yra svarbus reumatinių, infekcinių, jungiamojo audinio ligų žymuo. Serumo amiloidas A (SAA) tai ūminės fazės baltymas. Po stimuliacijos navikų nekrozės faktoriumi α bei interleukinais Il-1, Il-6 SAA sintetinamas kepenyse, taip pat jo gamina aktyvinti makrofagai, fibroblastai. Sekretuotas SAA jungiasi prie didelio, mažo ir labai mažo tankio lipoproteinų, tačiau daugiausia prie DTL 3. Serumo amiloidas A yra jautrus uždegimo žymuo, panašus į CRB. Jo kiekis serume pradeda didėti praėjus porai valandų nuo pažeidimo, panašiai kaip ir C reaktyviojo baltymo, bet šis didėjimas ryškesnis (didėja nuo 100 iki 1000 kartų) ir koncentracija maksimumą pasiekia anksčiau negu CRB. SAA padeda geriau diferencijuoti minimalų uždegiminį atsaką, pvz., 2/3 persišaldžiusių žmonių nustatoma padidėjusi SAA koncentracija, bet tik mažiau kaip pusei padidėjusi CRB koncentracija. Serumo amiloidas A yra jautrus transplantato at- 104
106 Žmogaus kraujo plazmos baltymai... metimo rizikos žymuo. Nurodoma, kad 97% atmetimo epizodų buvo diagnozuoti nustačius padidėjusią SAA koncentraciją. Sveikiems asmenims rekomenduojama serumo amiloido A reikšmė neturi viršyti 10 mg/l (priklauso nuo tyrimo metodo). Fibrinogenas dimerinis baltymas, sintetinamas kepenyse. Tai paskutinis kraujo krešėjimo kaskados baltymas. Jo molekulinė masė Da, sudarytas iš trijų skirtingų porų neidentiškų grandinių: Aα, Bβ ir γ. Viena fibrinogeno heterogeniškumo priežasčių yra jo nevisiškoji proteolizė veikiant plazminui. Fibrinogenas virsta fibrinu (tai monomeras) veikiamas trombino, kuris atskelia du rūgščiuosius A ir B peptidus (fibrinopeptidus) atitinkamai iš α ir β grandinių. Juos pašalinus vyksta spontaniška fibrino siūlų agregacija, susidarant skersiniams kovalentiniams ryšiams taip susidaro fibrino pluoštai, paskui ir krešulys. Kita labai svarbi fibrinogeno funkcija yra dalyvavimas uždegimo procese tai jautrus uždegimo rodiklis: jo koncentracija pradeda didėti po val. nuo pažeidimo pradžios ir gali kelis kartus viršyti pradinį lygį. Kaip ūminės fazės baltymo, fibrinogeno 2 3 kartus padaugėja infekcinio proceso metu, o tai ir lemia eritrocitų nusėdimo greičio (ENG) pokyčius. Šio baltymo gerokai padaugėja dėl neoplazinio proceso, po traumų, operacijų. Padidėjusi fibrinogeno ir fibrino koncentracija pažeistame audinyje skatina granulocitų migraciją į pažeistą vietą; ten jie apsaugo nuo leukocitų ir pažeistų audinių ląstelių proteazių (katepsinų). Suintensyvėjusi fibrinogeno sintezė gali vykti kartu su jo katabolizmu. Jei katabolizmas labai intensyvus, fibrinogeno gali ne tik nepadaugėti, bet ir sumažėti žemiau normos. Tokia būklė būdinga diseminuotos intravazalinės koaguliacijos sindromui. Fibrinogeno ir fibrino skaidymo produktai pasižymi krešėjimą slopinančiu veikimu, nes slopina trombiną, verčiantį fibrinogeną fibrinu. Tai sunormina kraujotaką, gerina uždegimo pažeistų audinių drenažinę funkciją. Taigi fibrinogenas yra daugiafunkcis baltymas: jis yra galutinis kraujo krešėjimo kaskados baltymas; veikiamas trombino virsta fibrinu, kuris sudaro krešulio pagrindą; jis priklauso ūminės fazės baltymų grupei ir yra jautrus uždegimo rodiklis; kaip adhezijos molekulė, fibrinogenas sąveikauja su trombocitais, endotelio ląstelėmis, makrofagais, fibroblastais; be poveikio eritrocitų agliutinacijai, fibrinogenas dalyvauja bakterijų ir piktybinių ląstelių adhezijos prie ląstelių paviršiaus procese; yra nepriklausomas širdies ir kraujagyslių ligų, tokių kaip miokardo infarktas, insultas, rizikos veiksnys. Interleukinas-6 (Il-6) ir navikų nekrozės faktorius α (angl. tumor necrosis factor, TNF). Tarp daugelio citokinų, interleukino-6 ir navikų nekrozės faktoriaus 105
107 koncentracijos nustatymas yra rekomenduojami kasdienei klinikinei praktikai. Interleukinas-6 yra svarbus prognozinis sepsio, širdies nepakankamumo žymuo, padeda nustatyti aterosklerozinio proceso aktyvumą. Interleukinas-6 ir navikų nekrozės faktorius α dalyvauja ūminio miokardo infarkto bei lėtinio širdies nepakankamumo patogenezėje. Il-6 padidina krešėjimo veiksnių sintezę kepenyse, skatina trombocitų prokoaguliacines savybes, dėl to greičiau kreša kraujas. Klinikinių tyrimų duomenys rodo, kad didesnė Il-6 koncentracija susijusi su padidėjusia rizika susirgti miokardo infarktu. Rekomenduojama interleukino-6 reikšmė yra 5 pg/ml, o navikų nekrozės faktoriaus α 8 pg/ml. Komplemento komponentai. Ūminės fazės baltymams, kurių padaugėja esant uždegimui, traumai, priklauso trys komplemento komponentai: C3, C4 ir aktyvintasis kompleksas C56. Šiuo metu žinoma daugiau kaip 20 komplemento sistemos baltymų, kurie yra esterazių ir proteazių profermentai. Sistema aktyvinama kaskados principu ir dalyvauja ląstelių lizėje, t. y. tų ląstelių, kurios turi, nors ir nedidelį, svetimą komponentą. Imunoglobulinai. Imunoglobulinai, arba antikūnai, tai baltymai, gaminami kaulų čiulpų plazminėse ląstelėse kaip imuninio atsako sudėtinė dalis. Plazminės ląstelės tai B limfocitai, kurie transformuojasi paveikus išoriniam (kartais endogeninės kilmės) antigenui. Visi imunoglobulinai turi tą pačią pamatinę struktūrą. Jie sudaryti iš dviejų identiškų lengvųjų ir dviejų identiškų sunkiųjų polipeptidinių grandinių, sujungtų disulfidiniais ryšiais. Lengvosios grandinės yra dviejų tipų: kapa (κ) ar lambda (λ). Sunkiosios grandinės yra penkių tipų: alfa (α), gama (γ,) delta (δ), epsilon (ε) ir miu (µ). Imunoglobulinai vadinami pagal sunkiųjų grandinių tipą: IgA, IgG, IgD, IgE ir IgM. Imunoglobulinų molekulėje skiriamos dvi funkcinės dalys: Fab dalis, kuri turi kintamą sritį, atpažįstančią ir surišančią antigeną; Fc dalis, atsakinga už sąveiką su kitais imuninės sistemos komponentais, pavyzdžiui, komplementu. Įvairios imunoglobulinų klasės (9 lentelė) skiriasi erdvine struktūra ir funkcijomis. Svarbiausi antikūnai kraujo plazmoje yra IgG, IgA ir IgM. Imunoglobulinų kiekį galima nustatyti keliais būdais. Jei elektroforezės metu aptinkami pokyčiai γ globulinų zonoje, tada tiriamas individualus imunoglobulinas, taip pat jų lengvosios ar sunkiosios grandinės. Čia detaliau aptarti tik pagrindiniai kraujo plazmos baltymai, ypač tie, kurie dalyvauja uždegimo reakcijose. Krešėjimo baltymų, lipoproteinų, fermentų, savybės ir funkcijos išsamiau aprašytos kituose šiems klausimams skirtuose skyriuose. 106
108 Žmogaus kraujo plazmos baltymai... 9 lentelė. Imunoglobulinų klasės Imunoglobulinas Struktūra Lokalizacija Funkcija IgG Monomeras Neląstelinis skystis Neutralizuoja toksinus, aktyvina komplementą IgA Serume monomeras, Neląstelinis skystis ir Antimikrobinis veikimas sekrete dimeras sekretas IgM Pentameras + jungiančioji grandinė Daugiausia kraujyje Pirmasis, kuris atsiranda imuninio atsako metu IgD Monomeras Neląstelinis skystis ir ląstelių membrana Ląstelių paviršiaus antigenų receptorius IgE Monomeras Neląstelinis skystis Antialerginis, antiparazitinis Disproteinemijos Sergant daugeliu ligų, sutrinka procentinis baltymų frakcijų santykis, nors bendras baltymų kiekis gali būti normalus. Tokia būklė vadinama disproteinemija. Fiziologinės disproteinemijos. Šie kitimai susiję su tam tikrais žmogaus gyvenimo tarpsniais: nėštumu, kūdikyste, senatve. Nėštumo metu atsiranda veiksnių, kurie skatina baltymų sintezę; tai lyg ir organizmo pasirengimas būsimai baltymų netekčiai nukraujavus. Tačiau bendras baltymų kiekis paprastai sumažėja. Tai paaiškinama hidremija, t. y. nėščiosios organizme susilaiko vanduo ir kraujas prasiskiedžia. Nėštumo metu ypač padaugėja α 1, α 2, β 1 globulinų, fibrinogeno. β 2 ir γ globulinų kiekiai išlieka normalūs. Albuminų koncentracija pradeda mažėti nuo antro nėštumo mėnesio ir mažėja iki ketvirto mėnesio, o paskui nusistovi. Po gimdymo, jei nėra komplikacijų, buvę pakitimai išnyksta per 1,5 2 mėnesius. Visi kokybiniai baltymų mėginiai turi likti normalūs. Vaisiaus ir naujagimio kraujas. Trečiąjį nėštumo mėnesį vaisiaus kraujyje baltymų yra tik apie 15 g/l. Pamažu jų daugėja ir prieš gimimą pasiekia 58 g/l. Didėjant baltymų kiekiui, ypač gausėja γ globulinų. Gimimo metu jų kiekis siekia g/l. Naujagimio baltymų kiekis didėja, bet galutinai su suaugusio žmogaus susilygina apie šešioliktus gyvenimo metus. Vaisius iki pat gimimo ir gimus γ globulinų negamina, o juos per placentą perima iš motinos kraujo. Kūdikio organizme pamažu pradedami sintetinti γ globulinai, o gautieji iš motinos išnyksta. Jei moters γ globulinų gamyba yra sumažėjusi, naujagimis neturi jų atsargų. Kol pradės gaminti savus γ globulinus, praeis keli mėnesiai. Todėl šiuo laikotarpiu labai pavojingos įvairios infekcijos. Jei γ globulinų sintezė visai nevyksta, o motinos jau išnyksta, tai atsiranda antikūnų stokos sindromas (detaliau skyrelyje Patologinės disproteinemijos ). Senyvo amžiaus žmonių kraujas. Iki 80 metų amžiaus ypatingų baltymų sudėties skirtumų neturėtų būti. Po 80 metų gali sumažėti albuminų ir padaugėti globulinų, mažėjant bendram baltymų kiekiui. Senyvo amžiaus sveikiems asmenims dažnai 107
109 yra padidėjusi γ globulinų frakcija. Tačiau nustačius tokį padidėjimą, pirmiausia reikia ieškoti priežasties (įvairios lėtinės ligos, pvz., tuberkuliozė, bronchitas ir kt.). Tik atmetus šias priežastis, γ globulinų padaugėjimą galima aiškinti senyvu amžiumi. Patologinės disproteinemijos. Jos skirstomos į tris grupes: 1) reakcinė disproteinemija, 2) stokos disproteinemija, 3) genetinė disproteinemija. Reakcinė disproteinemija yra dažniausia ir apibūdinama kaip nespecifinė organizmo reakcija į kurį nors dirgiklį. Galimi dirgikliai: a) infekcija; b) įvairios toksinės medžiagos; c) medžiagos, kurios pasigamina uždegimo židinyje; d) audinių irimo produktai. Esant disproteinemijai paprastai albuminų koncentracija mažėja, o globulinų didėja. Kuo patologinis procesas ryškesnis ir kuo staigiau prasideda, tuo disproteinemija ryškesnė. Kuo ryškesnė eksudacija (esant pažeistai kapiliarų sienelei ir padidėjus pralaidumui), tuo ryškesnė ir disproteinemija. Ūminės fazės baltymų kiekis dažniausiai esti padidėjęs (baltymų elektroforezinio tyrimo rezultatų vertinimas pateikiamas atskirame skyrelyje). Stokos disproteinemija. Tai baltymų frakcijų santykio pakitimas dėl jų netekties. Stokos disproteinemijos dažniausios priežastys yra šios: a) ilgas badavimas; b) sutrikęs baltymų virškinimas (hidrolizė) ar aminorūgščių rezorbcija žarnyne; c) baltymų netekimas per inkstus (nefrozinis sindromas); d) kraujavimas; e) ilgai trunkanti gausi eksudacija, pūliavimas; f) odos ligos, kai procesas išplitęs dideliame paviršiuje. Svarbu žinoti, kad kartu su hipoproteinemija (ypač hipoalbuminemija) vystosi ir hipokalemija. Genetinė disproteinemija. Ji išsivysto dėl įgimtos konkretaus baltymo stokos esant neaktyviam jį koduojančiam genui. Žinomos šios genetinės disproteinemijos: 1) bisalbuminemija. Yra apie 20 paveldimų greitai ir lėtai migruojančių albuminų variantų. Tiriant elektroforeze tais atvejais gaunamos dvi albuminų frakcijos: A ir B; 2) analbuminemija. Reta būklė, kai visai nesintetinami albuminai arba jų labai nedaug. Kraujo tyrimas dažniausiai rodo kompensacinę hiperglobulinemiją. Tokie ligoniai jaučia nuovargį, silpnumą, atsiranda hipotonija, polinkis į edemas; 3) anorozomukoidemija. Jai būdingas polinkis į streptokokines infekcijas; 4) aceruloplazminemija. Trūkstant ceruloplazmino, susergama Vilsono liga; 5) abetalipoproteinemija. Būklė, kai organizme nesigamina β lipoproteinai. Sutrinka riebalų apykaita, atsiranda steatorėja, nervų sistemos pažeidimas ataksija, psichikos sutrikimų, atipinis pigmentinis retinitas (esant abetalipoproteinemijai, vandenyje netirpūs lipidai kaupiasi daug fosfolipidų turinčiuose au- 108
110 Žmogaus kraujo plazmos baltymai... diniuose ir juos pažeidžia). Šiai patologijai būdingas reiškinys akantocitozė, kai eritrocitai įgauna jūros žvaigždės formą (akantocitai); 6) atransferinemija. Sutrinka geležies pernešimas, vystosi geležies stokos mažakraujystė, miokarde hemosiderozė. Geležis tų organų ląstelėse kaupiasi kaip svetimkūnis; ima vešėti jungiamasis audinys, nyksta parenchima; 7) afibrinogenemija. Serga naujagimiai. Kraujuoja iš bambutės ir vidaus organų. Išryškėja melena (kraujas išmatose), galimas vėmimas krauju, atsiranda kraujo išsiliejimų odoje, gleivinėse, nes nesusidaro krešulys. Krešėjimas sunormalėja tik nuo fibrinogeno. Kraujavimo laikas ilgesnis, nors gali būti normalus. Dažnesnės yra antrinės afibrinogenemijos dėl: a) toksinio kepenų pažeidimo; b) fibrinolizinių fermentų aktyvumo padidėjimo (diseminuotos intravazalinės koaguliacijos sindromas, pvz., gimdant, esant sepsiui ir kt.); 8) agamaglobulinemija. Kliniškai išryškėja antikūnų stokos sindromu. Įgimtasis sindromas aprašytas 1952 metais. Serga tik berniukai, moterys šį defektą perduoda sūnums. Būdingi požymiai: a) nėra γ globulinų ar jų būna labai nedaug; b) mažas antikūnų titras (nėra antistreptolizino, antihialuronidazės ir kt.); c) nereaguojama į antigeną; d) labai didelis jautrumas infekcijai. Sindromas išryškėja ne tuoj pat gimus, o 9 24-ą gyvenimo mėnesį, kai jau visai išnyksta iš motinos gauti antikūnai. Kūdikis pasidaro neatsparus bakterinei, ypač kokinei, infekcijai (atsparumas virusinėms infekcijoms beveik nesumažėja). Įgytas (antrinis) antikūnų stokos sindromas dažnai pasitaiko, pavyzdžiui, ilgai didelėmis dozėmis vartojant gliukokortikoidų (sustiprėja baltymų katabolizmas), imunodepresantų, sergant sisteminėmis limfinio audinio ligomis. Įgimtas antikūnų stokos sindromas būdingas tik berniukams, o įgytas sindromas pasitaiko ir mergaitėms. Lab o r a t o r i n i a i kr a u j o se r u m o ba l t y m ų ty r i m o rodikliai ir jų klinikinis interpretavimas Bendro baltymų kiekio kraujo serume diagnostinė reikšmė. Bendras baltymų kiekis serume nustatomas unifikuotu biureto metodu. Normalus baltymų kiekis suaugusių asmenų kraujo serume yra g/l. Dėl fibrinogeno kraujo plazmoje baltymų yra 2 4 g/l daugiau. Toliau tekste pateikiamas normalus bendrasis baltymų kiekis (g/l) kraujo serume įvairiais amžiaus tarpsniais: virkštelės kraujas neišnešioti naujagimiai sveiki naujagimiai savaitės kūdikiai mėn. 1 metų kūdikiai metų vaikai
111 vyresni kaip 3 metų vaikai suaugusieji (ambulatoriniai pacientai) suaugusieji (stacionaro pacientai) vyresni kaip 60 metų būdingas sumažėjimas 2 g/l. Dėl įvairių patologinių būklių baltymo kiekis kraujo serume gali svyruoti. Diagnostinė reikšmė Hiperproteinemija (>90 g/l) dažniausiai yra susijusi su hipergamaglobulinemija. Ji būdinga: 1) lėtinėms uždegiminėms ligoms (kolagenozėms, reumatoidiniam artritui, kepenų cirozei ir kitoms ligoms); 2) polikloninėms arba monokloninėms gamapatijoms mielominei ligai, Valdenstremo (Waldenström) makroglobulinemijai. Sergant pastarosiomis ligomis, bendras baltymų kiekis gali siekti 200 g/l. Nedidelė hiperproteinemija galima sveikstant po hepatito, didelio nudegimo, perkaitus, netekus vandens (dėl gausaus vėmimo, prakaitavimo, viduriavimo). Be to, bendras baltymų kiekis padidėja esant veninei stazei. Ilgai laikomame kraujyje (serume) taip pat gali padaugėti baltymo. Hipoproteinemija (<60 g/l) dažniausiai atsiranda sumažėjus albuminų kiekiui. Ji nustatoma: 1) kai valgoma nepakankamai baltymų: badaujant su maistu negaunant baltymų, sutrikus virškinamojo trakto funkcijai, pvz., baltymų virškinimo procesui ar aminorūgščių įsiurbimui; 2) kai organizmas netenka daug baltymų: esant ūminiam ir lėtiniam kraujavimui, gastroenteropatijoms; ryški hipoproteinemija būdinga nefroziniam sindromui (baltymų kiekis gali sumažėti iki g/l; kai jo mažiau negu 30 g/l, atsiranda edemų); esant odos ligoms ir pažeidimams (nudegimams, egzemoms); 3) kai pažeidžiamos kepenų ląstelės ir sutrinka baltymų sintezė (ūminė kepenų atrofija, toksinis hepatitas). Be to, bendras baltymų kiekis sumažėja nėštumo metu, prasiskiedus kraujui (pvz., dėl širdies dekompensacijos, kai susilaiko vanduo; sergant lėtinėmis inkstų ligomis, kai susilaiko vanduo, druskos; po intraveninių infuzijų), sutrikus baltymų sintezei, aktyvuojantis proteolizei dėl lėtinių uždegiminių, piktybinių ligų. Išbuvus ilgesnį laiką horizontalioje padėtyje (pvz., naktį miegant), baltymų kiekis gali sumažėti g/l. Tyrimo rezultatus kartais iškreipia lipemija, hemolizė, hiperbilirubinemija. Kr a u j o se r u m o ba l t y m ų el e k t r o f o re z i n i o ty r i m o duomenų klinikinis interpretavimas Albuminai. Absoliutaus albuminų kiekio padidėjimo beveik nepasitaiko. Kartais gali padaugėti sulašinus daug albuminų, esant hipohidratacijai (pseudohiperalbuminemija). Hipoalbuminemijų priežastys gali būti įvairios: 1) sumažėjusi sintezė esant: 110
112 Žmogaus kraujo plazmos baltymai... įgimtai analbuminemijai (retai); baltymų stokai maiste; malabsorbcijos sindromui; ūminiam hepatitui (trunkančiam daugiau kaip 14 dienų); lėtinėms kepenų ligoms (cirozei, amiloidozei); lėtinėms uždegiminėms ligoms (kolagenozėms, sunkioms infekcijoms, karcinomatozei, reumatinei karštinei, pankreatitui); 2) padidėjęs netekimas: per odą (eksudacinės dermatopatijos, terminis nudegimas, išplitęs egzeminis pažeidimas, cheminis pažeidimas ir kt.); per inkstus (nefrozinis sindromas, lėtinis glomerulonefritas, cukrinis diabetas, sisteminė raudonoji vilkligė); per virškinamąjį traktą (lėtinės žarnyno ligos, pvz., opinis kolitas, Krono liga; ūminės žarnyno infekcijos, pvz., salmoneliozė; neoplazinis procesas, pvz., stemplės, skrandžio, storosios žarnos vėžys; žarnyno limfangiektazijos, pvz., limfomos, limfostazė krūtininiame limfiniame latake, esant stazei, pvz., širdies nepakankamumo, kardiomiopatijų, atrioventrikulinio vožtuvo nepakankamumo atvejais; skrandžio polipozė; pankreatitas; enteropatijos, pvz., dėl apšvitinimo; mukoviscidozė; žarnų nepraeinamumas; sisteminės ligos, pvz., raudonoji vilkligė, mielominė liga, makroglobulinemija, amiloidozė, sunkus reumatoidinis artritas; kraujavimas iš virškinamojo trakto; didelės chirurginės operacijos); 3) suintensyvėjęs katabolizmas esant: plačiam nudegimui; išplitusiai malignizacijai; komplikacijoms gydant kai kuriais steroidiniais hormonais ir antimetabolitais (priešnavikiniais) preparatais; sunkiai tirotoksikozei; Kušingo sindromui; nefroziniam sindromui; 4) baltymų pasiskirstymo intravazalinėje ir ekstravazalinėje erdvėje sutrikimai dėl: terminio nudegimo; perteklinio skysčių suleidimo; generalizuotosios edemos; 5) daugiaveiksnės priežastys: cirozė; įgimta širdies liga; nėštumas. 111
113 Kadangi albuminai sudaro apie 55±5% visų baltymų, tai dėl jų sumažėjimo dažniausiai išsivysto ir hipoproteinemija. Sumažėjus albuminų kiekiui iki 30 g/l ir mažiau, atsiranda edemų. Serume albuminų kiekis padidėja ilgai laikant timpą kraujo ėmimo metu. Taip pat albuminų tyrimo rezultatai gali pakisti ir dėl šių priežasčių: 1) padidėti dėl klinikinio poveikio in vivo (vartojant ampiciliną), cheminio poveikio in vitro (lipemija); 2) sumažėti dėl klinikinio poveikio in vivo (vartojant estrogenų ir jų darinių, geriamųjų kontraceptikų); 3) vartojant peniciliną gali išsivystyti bisalbuminemija. Dažniausiai, mažėjant albuminų koncentracijai, santykinai daugėja globulinų. Galimas ir absoliutusis globulinų padaugėjimas esant monokloninėms ar polikloninėms gamapatijoms. α 1 globulinai. Ši frakcija paprastai didėja dėl ūminės uždegimo fazės reakcijos. Šis reiškinys pirmiausia yra susijęs su α 1 antitripsino kiekio didėjimu. Nustatomas tiek santykinis, tiek absoliutusis α 1 globulinų kiekio didėjimas dėl įvairaus infekcinės ar alerginės kilmės uždegimo, pažeidus kepenis, yrant audiniams ar dėl ląstelių proliferacijos (piktybiniai navikai). Santykinis α 1 globulinų kiekis gali padidėti ir vartojant geriamųjų kontraceptikų. α 1 globulinų sumažėja retai ir dažniausiai dėl α 1 antripsino, α lipoproteinų stokos ar tiriant pastovėjusį serumą (ar plazmą). α 2 globulinai. Ši frakcija didėja: 1) esant uždegiminiams procesams, ypač kai yra ryški eksudacija, pūlinis procesas (pneumonija, pleuros empiema ir kt.); 2) sergant ligomis, kai patologinis procesas apėmęs jungiamąjį audinį (kolagenozės, reumatinės, autoimuninės ligos); 3) esant piktybiniams navikams; 4) sveikstant po terminių nudegimų; 5) retais atvejais esant M baltymui (monokloninei gamapatijai). α 2 globulinų frakcijos augimas susijęs su haptoglobino ir ceruloplazmino koncentracijos didėjimu. α 2 globulinų kiekis mažėja retai: sergant toksiniu hepatitu, cukriniu diabetu, hipoproteinemija, įgimta naujagimių mechaninė gelta, pankreatitu (retai). α (α 1 ir α 2 ) globulinų frakcijų pokyčių atsiranda praėjus val. po pažeidimo.! Šios frakcijos santykinį kiekį gali padidinti hemolizė in vitro. β globulinų kiekio pokyčiai dažniausiai yra susiję su lipoproteinų ir transferino kiekio kitimu. Pastarasis sudaro didžiumą β 1 globulinų frakcijos. Todėl β globulinų padaugėja sutrikus riebalų apykaitai: esant hiperlipoproteinemijoms, kepenų ligoms, cukriniam diabetui, nefroziniam sindromui, hipotirozei, taip pat kraujuojant opoms. Kadangi šioje frakcijoje daug komplemento komponentų, tai ji padidėja sergant uždegiminėmis ligomis. 112
114 Žmogaus kraujo plazmos baltymai... Šių globulinų kiekio sumažėjimas yra retesnis ir nustatomas esant hipobetalipoproteinemijoms. γ globulinai. Šią frakciją sudaro imunoglobulinai. Veikiant įvairiems veiksniams imunoreaktyvų audinį ir dėl kitų priežasčių (baltymo netekimo, sutrikusios jų sintezės ar skilimo ir kt.) γ globulinų sudėtis gali pakisti. Padidėjimas būna dažnesnis negu sumažėjimas ir jį lemia suintensyvėjusi imunoglobulinų sintezė. Tai vadinamosios polikloninės ir monokloninės gamapatijos. Būklės, susijusios su poliklonine gamapatija: 1) lėtinės kepenų ligos: pirminė biliarinė cirozė, lėtinis aktyvusis hepatitas, virusinis hepatitas; 2) kolageninės ligos: reumatoidinis artritas, sisteminė raudonoji vilkligė, polimiozitas, sklerodermija; 3) lėtinės bakterinės, grybelinės, parazitinės infekcijos: tuberkuliozė, osteomielitas, vidaus organų (sisteminė) grybelinė liga, sifilis, bronchitas; 4) kitos ligos: metastazinė karcinoma, cistinė fibrozė, sveikimas po traumos. Monokloninių gamapatijų priežastys (dėl jų dažniausiai sutrinka normalių γ globulinų frakcijos baltymų sintezė ir kraujyje atsiranda patologinių baltymų, vadinamų paraproteinais): dauginė mieloma, Valdenstremo makroglobulinemija, gerybinė idiopatinė monokloninė gamapatija, imunoglobulinų sunkiųjų grandinių liga, kolageno sintezės sutrikimai, autoimuninės ligos, specifinės limfomos, storosios žarnos, prostatos, krūties, genitalijų, skrandžio, plaučių neoplazma, mieloproliferacinės ligos (policitemija, mielofibrozė, eritroleukozė, ūminės leukemijos), 113
115 ! lipidų apykaitos sutrikimai, cukrinis diabetas. Visų frakcijų baltymų gali santykinai padaugėti esant hipohidratacijai ar organizmui netekus vandens (dehidratacija) ir sumažėti netekus daug baltymų per virškinamąjį traktą (pvz., esant gastroenteropatijoms). Kliniškai interpretuojant frakcijų kitimus iš proteinogramų, skiriami penki disproteinemijų (paprastai reakcinių) tipai: 1) α globulinų frakcijos didėjimas dažniausiai nustatomas ūminės infekcijos ir eksudacijos pradžioje. α 1 globulinų daugėjimas būdingesnis infekcinės ir alerginės kilmės uždegimams, kepenų pažeidimui, audinių irimui ar jų proliferacijai. α 2 globulinų padaugėja dėl ūminių uždegimų, kai yra ryški eksudacija, pūliavimas ar kai patologinis procesas apima jungiamąjį audinį. 2) β globulinų frakcijos didėjimas būdingas infekcinio ar uždegiminio proceso antrosios pusės reakcijai, kai ūminiai reiškiniai pradeda slopti, taip pat ligoms, kurios sutrikdo riebalų apykaitą, ar kraujuojant. 3) γ globulinų frakcijos kiekio didėjimas tai būdingas lėtinio uždegimo požymis (uždegimo vėlyvosios stadijos reiškinys). 4) α ir γ globulinų, β ir α globulinų ar α, β ir γ globulinų frakcijų daugėja tada, kai paūmėja lėtiniai procesai arba kai lėtinę ligą komplikuoja ir kuri nors ūminė uždegiminė liga. 5) Mišrusis variantas pasireiškia tuomet, kai reakcinė disproteinemija vystosi kartu su stokos disproteinemija (sergant kuria nors alinančia liga, pvz., tuberkulioze, nefroziniu sindromu, piktybine liga, kartu paūmėja uždegiminis procesas). Proteinogramoje bus požymių, būdingų ir stokos disproteinemijai (pvz., hipoproteinemija, hipoalbuminemija), ir reakcinei disproteinemijai (globulinų frakcijų pakitimai priklauso nuo proceso eigos). Kr a u j o pl a z m o s ba l t y m ų ki e k i o kitimas ir da l y v a v i m a s ūminio už d e g i m o (pažeidimo) r e a k c i j o s e Organizmas į pažeidimą (traumą, infekciją, kt.) atsako gana darniai, stengdamasis sustabdyti šį procesą, apsisaugoti nuo tolesnio pažeidimo ir pradėti regeneraciją. Šis atsakas yra lokalus ir sisteminis. Lokalaus (vietinio) atsako mechanizmą sudaro kraujagyslių pralaidumo kitimai ir aktyviųjų ląstelių komponentų atsipalaidavimas (lizosominių fermentų, vazoaktyviųjų peptidų, eikozanoidų). Sisteminis atsakas tai fagocitų aktyvacija, tolesnė eikozanoidų gamyba: prostaglandinų, prostaciklinų, tromboksanų, leukotrienų sintezė iš eikozapenteno, eikozatrieno, eikozatetraeno (arachido rūgšties), peptidinių hormonų arba citokinų atsipalaidavimas iš ląstelių. Sisteminė reakcija lemia uždegimą, daugėja cirkuliuojančių granulocitų, keičiasi metabolinis kepenų ir kitų audinių aktyvumas (sukeliama ūminės fazės baltymų sinte- 114
116 Žmogaus kraujo plazmos baltymai... zė). Ūminės reakcijos atsaką sužadina citokinas interleukinas-1 (IL-1). Monocitas (makrofagas) yra svarbiausia ląstelė, formuojanti uždegiminį atsaką po sąlyčio su patogenu ir yra pagrindinis IL-1 šaltinis. Kadangi IL-1 yra endogeninis pirogenas, jis sukelia ir temperatūros reakciją, be to, skatina interleukino-6 sintezę stromos ląstelėse ir sukelia ūminės uždegimo fazės (toliau ūminės fazės) baltymų, taip pat navikų nekrozės faktoriaus sintezę kepenyse (5 pav.). Audinio pažeidimas (pirminis) Citokinas (kraujas) Kepenys: suintensyvėjusi ŪFB sintezė Atsipalaidavę lizosomų fermentai Audinio pažeidimas (antrinis) Kraujas ŪFB lizosomų fermentų inhibitoriai 5 pav. Ūminės fazės baltymų (ŪFB) dalyvavimas uždegimo procese Humoraliniai veiksniai pažeidimo židinyje indukuoja informacinės RNR sintezę hepatocituose. Šis procesas vyksta jau trečią traumos ar pažeidimo valandą. Sintezės maksimumas yra ą ūminės uždegimo reakcijos valandą. Tuo pat metu hepatocitai sumažina kitų jiems įprastų baltymų sintezę, dėl to albuminų ir kitų plazmos baltymų, pavyzdžiui, transportinių, nepriklausančių adaptacinių grupei, kiekis sumažėja (pvz., lipoproteinų). Esant uždegimui, labiausiai padaugėja C reaktyviojo baltymo, serumo amiloido A, α 1 rūgščiojo glikoproteino, α 1 antitripsino. Dėl virusinių infekcijų C reaktyviojo baltymo gali ir nepadaugėti. Kitų baltymų fibrinogeno, haptoglobino, ceruloplazmino, C3 ir C4 komplementų kiekis padidėja ne taip ryškiai. Šie baltymai dar vadinami ūminės fazės baltymais (reaktantais). Dažniausiai ūminės fazės baltymų padaugėja 1,5 2,5 karto, bet gali ir iki 1000 kartų. Visi ūminės fazės baltymai yra fermentų, atsipalaiduojančių ląstelių destrukcijos metu ir galinčių sukelti antrinį pažeidimą, inhibitoriai. Ūminės fazės baltymams priskiriama dar viena svarbi imunodepresinė funkcija. Pavyzdžiui, nustatyta, kad apie piktybinį naviką ir ūminio fazės židinį susidaro sialoglikoproteinų sluoksnis, kuriame gausu ūminės fazės baltymų, ypač fibrinogeno, α 1 rūgščiojo glikoproteino, haptoglobino, α 1 antitripsino. Šitaip glikoproteinai suteikia šeimininko organizmui pakantumą navikinių antigenų atžvilgiu, o pažeidus audinį, jie stabdo imunokompetentinių ląstelių judėjimą uždegimo židinio link. 115
117 Padidėjimas, % II III I I ūminės fazės baltymai II komplemento ir krešėjimo faktoriai III imunoglobulinai IV pernašos (transportiniai) baltymai IV Dienos po pažeidimo 6 pav. Kraujo plazmos baltymų atsakas į uždegimą Kraujo plazmos baltymų atsakas į uždegimą laiko atžvilgiu gali būti įvairus (6 pav.). Ūminės reakcijos baltymų (C reaktyviojo baltymo, α 1 rūgščiojo glikoproteino, fibrinogeno, α 1 antitripsino ir haptoglobino) sintezė ir koncentracija kraujo plazmoje greitai ir gerokai padidėja vystantis ūminiam uždegimui. Šie baltymai svarbūs fagocitozei, apsaugo nuo fermentų, atsipalaiduojančių iš neutrofilų, parenchiminių ląstelių bei bakterijų. Pažeidimas apribojamas dėl fibrino precipitacijos. Antrosios grupės baltymai (komplemento komponentai C3, C4) ir krešėjimo faktoriai reaguoja vėliau, o imunoglobulinų padaugėja tik praėjus ūminei reakcijos fazei. Pa r a p r o t e i n e m i j o s Sergant tam tikromis ligomis, kraujo plazmoje randama baltymų, kurie savo fizikocheminėmis, antigeninėmis savybėmis, judrumu elektriniame lauke skiriasi nuo normalių. Šie baltymai įvairiais jų nustatymo ir tyrimo etapais buvo vadinami skirtingai metais Apitzas aprašė baltymus, kurių nėra sveikų asmenų kraujyje ir kuriuos gamina patologiškai pakitusios ląstelės. Šiuos baltymus pavadino paraproteinais ( šalia normalaus ), o būkles paraproteinemijomis. Normalius γ globulinus gamina plazminės ląstelės, o šiuos pakitusius baltymus (paraproteinus) patologiškai pakitusios plazmomielominės ląstelės. Į klinikinę praktiką įdiegus elektroforezės, imunodifuzijos metodus, buvo nustatyta, kad paraproteinai priklauso γ globulinų klasei ir savo antigeninėmis savybėmis panašūs į kai kuriuos žinomus IgA, G, M, D, E klasių imunoglobulinus. Remiantis šiais duomenimis, atsirado du nauji pavadinimai: disimunoglobulinemija ir disgamaglobulinemija. Klinikinės medžiagos analizė parodė, kad paraproteinai dažniausiai pasitaiko dėl dviejų nozologinių negalavimų: mielominės ligos ir Valdenstremo makroglobuline- 116
118 Žmogaus kraujo plazmos baltymai... mijos; be to, randami sergant kai kuriomis piktybinėmis ligomis, t. y. esant malignizacijai. Tai ir buvo pagrindas 1964 m. Riwa i pasiūlyti pavadinimą M komponentas (M gradientas, M baltymas). M raidė reiškia 3 pagrindines ligų grupes, prasidedančias šia raide. J. Valdenstremo nuomone, šį pavadinimą galima taikyti tik monokloninėms paraproteinemijoms, t. y. kai paraproteinai atsiranda dėl mielominės ligos ir makroglobulinemijos. Šie patologiniai baltymai giminingi normaliems imunoglobulinams. Tai buvo pagrindas nomenklatūrinei PSO komisijai pasiūlyti terminą patologiniai imunoglobulinai. Jų tyrimas parodė, kad ir sveikų žmonių organizme truputį esti tokių baltymų. Todėl manoma, kad egzistuoja nedaug tam tikrų ląstelių, susijungusių į kloną ar koloniją, kurios ir normaliomis sąlygomis gali sintetinti baltymus ar jų komponentus (vadinamąsias lengvąsias ir sunkiąsias jų grandines). Tačiau baltymo kiekis yra nedidelis ir įprastais metodais neaptinkamas. Tam tikromis sąlygomis šios ląstelės gali pradėti intensyviai daugintis (malignizuotis ir proliferuoti). Tada kraujyje atsiranda baltymų (ar, tiksliau pasakius, jų padaugėja), kurie turi visai vienodas molekules ir elektroforezės metu juda su jiems giminingais imunoglobulinais, sudarydami siaurą ryškią juostą. Tai F. M. Berneto (Burnet) sukurtos klonų teorijos esmė. Ši teorija atmeta terminą patologiniai imunoglobulinai, ir todėl pasiūlytas naujas terminas monokloniniai imunoglobulinai. Tačiau iki šiol galutinai neaišku, ar tai patologiniai imunoglobulinai, kuriuos sintetina patologiškai (piktybiškai) pakitusios ląstelės, ar selektyvusis genetiškai apibrėžtų normalių globulinų kiekio padidėjimas (dėl vienos ląstelių kolonijos proliferacijos jų pradedama gaminti labai daug). Egzistuojant terminų įvairovei, šiuo metu dauguma autorių vartoja paraproteinų ar M komponento (M baltymo) terminą ir jį apibūdina taip: paraproteinai tai yra imunoglobulinai, kurie neturi normalių antigeninių struktūrų ir kuriems būdingos patologinės ir individui specifinės str uktūros. Bendrasis paraproteinemijų apibūdinimas. Kiekvienas paraproteinas tai ne visas vieno iš normalių imunoglobulinų atvaizdas. Paprastai paraproteinai, ne taip kaip normalūs imunoglobulinai, sudaryti tik iš vienatipių lengvųjų grandinių, t. y. tik kappa (κ) arba lambda (λ) molekulių. Paraproteinų, sudarytų iš lengvųjų κ tipo grandinių, pasitaiko du kartus dažniau negu λ tipo. Dažniausiai būna paraproteinų, priklausiančių IgG klasei (70 80%), rečiau IgA (13 18%), dar rečiau M, D ir E klasėms. IgA mielominės ligos prognozė blogesnė, palyginti su IgG mieloma. IgG κ arba IgG λ mielominės ligos tipas yra dažniausias, o tai yra klonų teorijos naudai. Paraproteinemijų laboratorinė diagnostika. Paraproteinemijoms būdinga: 1) anemija (normochrominė dėl normalių kraujodaros ląstelių išstūmimo besidauginant plazmomielominėms ląstelėms); 117
119 2) didelis eritrocitų nusėdimo greitis (ENG); dažnai eritrocitai sulimpa į stulpelius dėl padidėjusio stambiamolekulių baltymų (padidėjus patologinių) kiekio; 3) padidėjęs bendrasis baltymų kiekis; 4) būdingas elektroforezinis vaizdas: sumažėja normalių γ globulinų santykinis kiekis; išryškėja siaura homogeninė juosta (M gradientas), kuri pagal paraproteinų judėjimo greitį išsidėsto γ globulinų zonoje tarp β ir γ globulinų, rečiau β globulinų ir labai retai α globulinų zonoje; 5) Bens-Džonso baltymas šlapime. Jį mielomine liga sergančių ligonių šlapime aptiko Henry Bence-Jones as 1848 metais. Nedaug šio baltymo yra kraujyje. Šiuos patologinius baltymus, pasižyminčius nefrotoksiškumu, sudaro polipeptidinių grandinių perteklius. Šios grandinės identiškos mielominio baltymo lengvosioms grandinėms (κ ar λ). Baltymas pasižymi ypatingomis stabilumo savybėmis. Tuo ir pagrįstas jo laboratorinis nustatymas: kaitinamas iki 56 o C temperatūros šis baltymas precipituoja, o kaitinamas toliau iki 100 o C ištirpsta; atšaldžius jis vėl iškrinta nuosėdomis. Ši reakcija nevyksta, kai šlapimo ph labai rūgšti (ph < 3,0 3,5) ar šarminė (ph > 6,5) ar esant mažam santykiniam šlapimo tankiui (bus maža Bens-Džonso baltymo koncentracija). Tiksliau šį baltymą galima nustatyti elektroforeze išsiskyrusi baltymo juosta atitiks paraproteino kraujyje zoną; 6) diagnozei taip pat labai svarbus imunoelektroforezinis kraujo serumo ir šlapimo tyrimas naudojant imuninius monospecifinius serumus prieš sunkiąsias ir lengvąsias imunoglobulinų grandines; 7) hiperkalcemija dėl kaulų destrukcijos; 8) diagnozė patvirtinama trepanobiopsija ar atlikus kaulų čiulpų punkciją ir radus plazmomielominių ląstelių. Nurodoma, kad M gradientas (elektroforezinis paraproteinų nustatymas) atsiranda prieš 5 metus iki išryškėjant klinikiniams ligos požymiams. Pasitaiko ir mielominės ligos variantas lengvųjų imunoglobulinų grandinių liga, taip pat kita reta patologija sunkiųjų imunoglobulinų grandinių liga. Šiais atvejais plazmomielominės ląstelės hiperprodukuoja ne visą pakitusį imunoglobuliną, o tik jo dalis nevisavertes lengvąsias ar sunkiąsias grandines. Dėl to nerasime mielominio baltymo, išryškėjančio tiriant elektroforeze, kaip M gradientas. Lengvųjų grandinių liga sudaro apie 20% visų mielominės ligos atvejų. Sergant šia liga, ENG yra normalus, nes nesikaupia stambiamolekuliai baltymai imunoglobulinai, nes jų kiekis sumažėja, ir eritrocitai nesulimpa į stulpelius; bendras baltymų kiekis kraujo plazmoje normalus, o γ globulinų sumažėjęs. Vienintelis būdingas 118
120 Žmogaus kraujo plazmos baltymai... laboratorinis požymis proteinurija, t. y. skiriasi patologiškai pakitę monokloniniai imunoglobulinų komponentai lengvosios grandinės. Sunkiųjų imunoglobulinų grandinių liga, kai gaminamas nevisaverčių sunkiųjų grandinių perteklius, dažniausiai išryškėja limfinių mazgų hiperplazija, splenomegalija. Dažniausiai iš pradžių diagnozuojama piktybinė limfoma. Dėl sunkiųjų grandinių ligos gaminamą monokloninį baltymą sudaro sunkiosios imunoglobulinų grandinės, todėl skiriami α, γ, µ ir δ sunkiųjų grandinių ligos variantai. Šių ligų diagnostikai svarbus imunoelektroforezinis kraujo serumo ir šlapimo tyrimas naudojant imuninius monospecifinius serumus prieš sunkiąsias ir lengvąsias imunoglobulinų grandines. Api b e n d r i n i m a s Labai padidėjusi bendroji baltymų koncentracija kraujyje dažniausiai priklauso nuo globulinų frakcijos padaugėjimo ir gali reikšti, kad esama paraproteinų. Bendroji baltymų koncentracija kraujyje dažniausiai sumažėja dėl hipoalbuminemijos. Albuminas yra svarbiausias kraujo plazmos onkotinį slėgį lemiantis baltymas. Dėl labai mažo albuminų kiekio kraujyje išsivysto edema. Hipoalbuminemija dažniausiai išryškėja sutrikus albuminų sintezei sergant kepenų ligomis ar kai albuminų netenkama daugiau, nei jų susintetinama (taip būna esant nefroziniam sindromui). Vienintelis nespecifinis ligos rodiklis, panašus į C reaktyvųjį baltymą (CRB), yra eritrocitų nusėdimo greitis (ENG). Jis taip pat atspindi ūminės uždegimo fazės atsako intensyvumą. ENG pokyčiai vystosi lėčiau negu CRB. Be to, ENG priklauso ir nuo eritrocitų skaičiaus bei morfologijos; jis yra didesnis, kai plazmoje yra daugiau fibrinogeno ar globulinų. Tačiau ENG, kaip nespecifinis ligos rodiklis, gali padėti tiriant paraproteinemijas, kurios nesužadina ūminės reakcijos atsako. Kraujo serumo baltymų tyrimu elektroforeze galima patvirtinti paraproteinų buvimą esant padaugėjusiai globulinų frakcijai. Imunoglobulinų koncentracijos nustatymas gali padėti nustatyti imuniteto deficitą ar atsaką į infekciją. Imunoglobulinų koncentracijos kartotinis tyrimas gali padėti nustatyti ligos progresavimą ar įvertinti gydymo veiksmingumą. Mielominės ligos diagnozei būtini du iš išvardytų požymių: paraproteinai serume ar šlapime, kaulų čiulpų infiltracija plazmomielominėmis ląstelėmis, radiologinis kaulų pažeidimo įrodymas. 119
121 Albuminas Laboratoriniai tyrimai Tiriamoji medžiaga. Serumas. Rekomenduojama reikšmė: g/l. Nėštumo metu mažėja dėl didėjančio plazmos tūrio. Diagnostinė vertė: Bet kuri būklė, kurios metu plazmoje mažėja vandens, padidina visų plazmos baltymų, taip pat albumino, koncentraciją. Ūminis ir lėtinis uždegimas: reumatinės ligos, nudegimas, granulominis procesas, dauguma bakterinių infekcijų, virusinės infekcijos, susijusios su audinių destrukcija, audinių nekrozė (ypač sergant piktybinėmis ligomis), vaskulitas, žarnų opinė liga, serozitas, poūmis bakterinis endokarditas, kai kurios parazitinės invazijos. Sintezės kepenyse sulėtėjimas: ūminės ir lėtinės kepenų ligos, amiloidozė, nepakankama mityba, piktybinis procesas, įgimtas širdies nepakankamumas, konstrikcinis perikarditas, širdies vožtuvų ligos. Retais atvejais dėl genetinių priežasčių albuminai gali būti visai nesintetinami, pvz., esant įgimtai analbuminemijai. Netekimas: nefrozinis sindromas, nudegimas, trauminė uremija (angl. crush syndrome), transudacija ar eksudacija, kraujavimas ir skysčių pakaitinis pylimas, virškinamojo trakto fistulės, kartotinė torakocentezė ar paracentezė, enteropatijos dėl jautrumo tam tikriems produktams (pvz., gliutelinui). Padidėjęs katabolizmas: karščiavimas, antimetabolitai, šeiminė idiopatinė hipoproteinemija, hipermetabolinės būklės dėl hormonų apykaitos sutrikimo (pvz., Kušingo sindromas, tirotoksikozė, kai kurie piktybiniai navikai, preeklampsija). Padidėjęs kraujo tūris (hipervolemija): nėštumas, egzogeninių estrogenų vartojimas, monokloninės imunopatijos (pvz., mielominė liga, Valdenstremo makroglobulinemija), įgimtas širdies nepakankamumas. Papildoma informacija. Albuminas yra vienas svarbiausių plazmos onkotinį slėgį reguliuojančių komponentų. Tačiau dėl kompensacinės hiperglobulinemijos sergant analbuminemija retai būna edema. Tai pagrindinis azoto šaltinis organizme. Perneša bilirubiną, tulžies rūgštis, metalų jonus, vaistus. V: progesteronas. V: alopurinolis, asparaginazė, azatioprinas, chlorpropamidas, dekstranas, estrogenai, ibuprofenas, izoniazidas, geriamieji kontraceptikai, prednizonas (didelės dozės), valproatai Tiriamoji medžiaga. Smegenų skystis. Rekomenduojama reikšmė: 0,15 0,45 g/l Tiriamoji medžiaga. Šlapimas, vienkartinė, geriausia pirmoji rytinė, porcija. Tiriama vienkartinėmis reagentų juostelėmis. Rekomenduojama reikšmė. Neturi būti. Diagnostinė vertė. Funkcinė ar gerybinė albuminurija: fizinė įtampa, karščiavimas, buvimas šaltyje, įgimtas širdies nepakankamumas, hipertenzija, aterosklerozė, nėštumas, ortostatinė proteinurija. Inkstinė proteinurija: bet kuri būklė, kurios metu didėja šlapimo takų pralaidumas, ar esant transudacijai, pvz.: glomerulonefritas, cukrinis diabetas, nefritas sergant sistemine raudonąja vilklige, fenacetino sukelta nefropatija, pielonefritas, cistos inkstuose, paveldimasis fruktozės netoleravimas, cistitas, šlapimo takų piktybiniai navikai, apsinuodijimas sunkiaisiais metalais, amiloidozė, sarkoidozė, inkstų transplantato atmetimas, dauginė mieloma, degeneracinės ar dirginamos apatinių šlapimo takų būklės. Papildoma informacija. Albuminas gali pradėti skirtis su šlapimu po sunkių fizinių pratimų (padidėja baltymų, kurių molekulinė masė < , netekimas). Per 24 val. baltymų ekskrecija įvairuoja ir neturi ypatingos reikšmės diagnostikai. 120
122 Žmogaus kraujo plazmos baltymai... Ortostatinė proteinurija gali būti diferencijuojama nuo patologinės tiriant du šlapimo ėminius: vienas surenkamas tuoj pat atsikėlus, kitas po to, kai pacientas 2 val. ar ilgiau buvo vertikalioje padėtyje. Reagentų juostelės yra jautrios albuminui. Neigiamas rezultatas neatmeta galimybės, kad šlapime nėra globulinų, hemoglobino, Bens-Džonso baltymo ar mukoproteinų. Reagentų juostelės nepatikimos esant mažai proteinurijai. Sergant tubuline proteinurija juostelės gali nieko nerodyti, nes jos metu albuminas su šlapimu nesiskiria. Padidėjęs ar sumažėjęs santykinis tankis gali iškreipti juostelių jautrumą. Teigiamą rezultatą tiriant juostelėmis reikia patvirtinti tiriant kartotinai skirtingu paros laiku. Šarminio šlapimo tyrimas gali duoti klaidingą teigiamą rezultatą (stovint šlapimas šarmėja). Didelis druskų kiekis mažina rezultatą. Amiloidas A (serumo amiloidas A, SAA) Tiriamoji medžiaga. Serumas. Rekomenduojama reikšmė. <6,4 mg/l (priklauso nuo metodo). Diagnostinė vertė. Esant uždegimui gali padidėti daugiau negu 3 kartus, ypač kai kartu yra antrinė amiloidozė ar antrinės priežastys nėštumo metu. Kepenyse gaminamo baltymo kiekis serume pradeda didėti po poros valandų nuo pažeidimo, panašiai kaip ir C reaktyviojo baltymo, bet šis didėjimas ryškesnis. Papildoma informacija. Tai ūminės fazės baltymas, sintetinamas kepenyse, aktyvintuose makrofaguose, fibroblastuose. Sekretuotas SAA jungiasi prie lipoproteinų, daugiausia prie DTL 3. SAA yra jautrus uždegimo žymuo, panašus į CRB. Jo kiekis serume pradeda didėti praėjus porai valandų nuo pažeidimo, bet šis didėjimas ryškesnis ir koncentracija maksimumą pasiekia anksčiau negu CRB. SAA yra jautrus transplantato atmetimo rizikos žymuo. Antistreptolizinas O Tiriamoji medžiaga. Serumas. Rekomenduotina reikšmė. <200 ku/l. Diagnostinė vertė. Streptokokinė infekcija. Padidėja 80 85% pacientų, sergančių ūmine reumatine karštine, ir 95% pacientų, sergančių ūminiu glomerulonefritu. Papildoma informacija. Streptolizinas O yra hemolizinas, kurį gamina A grupės streptokokai. Infekuoto asmens organizme streptolizinas O yra kaip svetimas baltymas, prieš kurį gaminasi antikūnai. Kiekio (titro) didėjimas prasideda po 1 savaitės nuo infekcijos pradžios ir maksimumą pasiekia 2 4 savaitę. Po 6 12 mėnesių pasiekia lygį iki infekcijos. Klaidingai teigiami rezultatai galimi padaugėjus mažo tankio lipoproteinų, esant ėminio bakteriniam užterštumui. α 1 Antitripsinas Tiriamoji medžiaga. Serumas. Rekomenduojama reikšmė. 0,9 2,0 g/l. Diagnostinė vertė. Uždegimas (pvz., infekcijos, reumatinės ligos), audinių nekrozė, piktybinis procesas, trauma (taip pat chirurginė), estrogenai (geriamieji kontraceptikai, nėštumas, ypač paskutinius tris mėnesius, kai kiekis padidėja 2 kartus). Kepenų parenchiminių ląstelių uždegimas yra dažnai susijęs su α 1 antitripsino koncentracijos padidėjimu, nekintant kitiems ūminės fazės baltymams. Nustatant vien α 1 antitripsiną, negalima diferencijuoti ūminės fazės atsako nuo hormonų (estrogenų) poveikio. Būtina tame pat ėminyje ištirti dar bent vieną ūminės reakcijos baltymą, pvz., C rektyvųjį baltymą ar haptoglobiną. Sumažėjęs kiekis ne visada rodo paveldimą stoką; tai gali būti susiję ir su padidėjusiu šio baltymo katabolizmu ar skaldymu. Pastarosios būklės galimos esant naujagimių idiopatiniam kvė- 121
123 pavimo sutrikimo sindromui, sunkiam naujagimių hepatitui, sunkiai kasos ar kepenų ligai. Šio baltymo kiekis taip pat mažėja sergant nefroziniu sindromu, jei kartu nėra uždegimo. Paciento ir kitų šeimos narių fenotipavimas rekomenduojamas patvirtinti genetinei jo stokai. Indikacijos nustatyti α 1 antitripsiną, be minėtų, yra sumažėjusi α 1 globulinų frakcija baltymų elektroforegramoje, naujagimių hepatitas (cholestazė), vaikų kepenų cirozė, lėtinė obstrukcinė plaučių liga, nustatyta metų amžiaus asmenims, kriptogeninė cirozė ar hepatoma, ūminės reakcijos atsako įvertinimas. Papildoma informacija. α 1 antitripsinas priklauso ūminės reakcijos baltymams. Baltymų elektroforegramoje tai pagrindinis α 1 globulinų frakcijos komponentas, be to, plazmoje tai didžiausios koncentracijos proteazių inhibitorius (Pi). Slopina daugelį proteolizinių fermentų, kurių aktyvumo centre yra aminorūgštis serinas. Svarbiausia fiziologinė funkcija yra proteazių, ypač elastazės, atsipalaiduojančios iš leukocitų fagocitozės metu, inhibicija. Tai nedidelė molekulė, todėl gali greitai pereiti iš plazmos į kitus organizmo skysčius, pvz., bronchų sekretą. Žinomi 75 paveldimi α 1 antitripsino variantai (Pi [proteazių inhibitorių] sistema). Keletas alelių yra susiję su šio baltymo kiekio sumažėjimu. Didelė paveldima baltymų stoka būdinga esant Pi ZZ ir SZ fenotipui ir yra susijusi su kepenų ciroze (ypač vaikystėje), suaugusiųjų lėtine plaučių liga (emfizema, lėtinis bronchitas). Asmenims, turintiems šio baltymo stoką, dažnesnė hepatoma. Jei serume ar plazmoje yra užterštų bakterijomis leukocitų, galima šio baltymo fragmentacija, ir tada tyrimo rezultatas gali būti klaidingai didelis ar mažas. V: estrogenai, oraliniai kontraceptikai, tamoksifenas. Klaidingai teigiamas rezultatas galimas esant reumatoidiniam faktoriui. bendrasis baltymas Tiriamoji medžiaga. Serumas. Rekomenduojama reikšmė g/l. Diagnostinė vertė. >90 g/l: hiperimunoglobulinemija, polikloninė ar monokloninė gamapatija. Pseudohiperproteinemija: stipri dehidratacija (in vivo), vandens išgaravimas iš ėminio. < 60 g/l: Baltymų netekimas: gastroenteropatijos, platūs nudegimai, nefrozinis sindromas. Sumažėjusi sintezė: lėtinės kepenų ligos, malabsorbcijos sindromas, bloga mityba, agamaglobulinemija. Papildoma informacija. Ilgas timpos užveržimo laikas padidina visų baltymų koncentraciją. Kraują paėmus iš aukščiau intravevinės infuzijos esančios vietos, gaunamos klaidingai mažos reikšmės dėl kraujo praskiedimo. Klaidingai didelis baltymo kiekis galimas dėl išgaravimo ilgai stovint ėminiui. Nepakankamai sumaišius atitirpintą po užšaldymo ėminį klaida gali siekti % tikrosios reikšmės. Atsikėlus ir kelias valandas pabuvus vertikalioje padėtyje, makromolekulių koncentracija smarkiai padidėja, palyginti su reikšmėmis pačioje pradžioje. Ligos prirakintų prie lovos pacientų bendrasis baltymas yra 3 g/l mažesnis negu tikėtina to amžiaus asmenims. Bendrasis baltymas serume sumažėja paskutinius tris nėštumo mėnesius. Gulinčio lovoje paciento tyrimo reikšmės smarkiai mažėja, pvz., po nakties gali sumažėti g/l. Intravevinės infuzijos praskiedžia kraują ir bendrojo baltymo kiekis krinta. Venostazė dėl nutekėjimo sutrikimo (pvz., periferinių kraujagyslių kolapsas) bendrojo baltymo kiekį padidina. Refraktometriniam bendrojo baltymo nustatymui turi reikšmės hiperglikemija tais atvejais išmatuota bendrojo baltymo koncentracija yra didesnė negu tikroji. Hiperlipidemija, hiperbilirubinemija ar hemolizė turi tokį pat poveikį. V: adrenalinas, anaboliniai steroidai, androgenai, insulinas, klofibratas, gliukokortikoidai, kortikotropinas, progesteronas. V: alopurinolis, estrogenai. 122
124 Žmogaus kraujo plazmos baltymai Tiriamoji medžiaga. Paros šlapimas. Rekomenduojama reikšmė. <0,11 g/l. Diagnostinė vertė. Nefrozinis sindromas, diabetinė nefropatija, dauginė mieloma, monokloninės gamapatijos, kitos mieloproliferacinės ir limfoproliferacinės ligos, nenormali absorbcija inkstų kanalėliuose (Fankonio sindromas, apsinuodijimas sunkiaisiais metalais, sarkoidozė), šlapimo takų navikai ir uždegimas, apatinių šlapimo takų degeneruojamos ir dirginamos būklės; po fizinių pratimų. Papildoma informacija. Klaidingai neigiami yra šarminio šlapimo tyrimo rezultatai. V: aminoglikozidai, amfotericinas B, aukso preparatai, bismuto druskos, chlorpropamidas, ciklosporinas, enalaprilis, grizeofulvinas, hidralazinas, interferonas, izoniazidas, kaptoprilis, gliukokortikoidai, litis, nesteroidiniai vaistai nuo uždegimo, penicilaminas, penicilinas, polimiksinas, sulfonamidai, tetraciklinas. V: indometacinas (esant nefroziniam sindromui) Tiriamoji medžiaga. Smegenų skystis. Rekomenduojama reikšmė. 0,15 0,45 g/l. Diagnostinė vertė. Ligos, kurioms būdingas įtekėjimo sindromas, t. y. pažeidžiamas hematoencefalinis barjeras, pvz., meningitas, encefalomielitas. Didelė bendrojo baltymo koncentracija galima sukrešėjus smegenų skysčio ėminiui, esant ksantochromijai, laisvam kraujui Tiriamoji medžiaga. Transudatas. Rekomenduojama reikšmė. <20 g/l. Tiriamoji medžiaga. Eksudatas. Rekomenduojama reikšmė. >20 g/l. Baltymų elektroforezė Tiriamoji medžiaga. Serumas. Rekomenduojama reikšmė. Albuminas 53 63%. Diagnostinė vertė. Žr. sk. Albuminas serume Rekomenduojama reikšmė. α 1 globulinas 2 4,5%. Diagnostinė vertė. α 1 antitripsino, kaip ūminės fazės baltymo, kiekis didėja sergant ūminėmis, poūmėmis ar lėtinėmis uždegiminėmis ir neoplazinėmis ligomis, kepenų ligomis. Paveldima α 1 antitripsino stoka, Tanžero (Tangier) liga (α 1 lipoproteinų stoka). Papildoma informacija. α 1 frakcijoje didžiausią dalį sudaro α 1 antitripsinas, α 1 lipoproteinai ir α 1 rūgštusis glikoproteinas. Pastarasis sunkiai jungiasi su dažais ir dėl to jį sunku matyti. V: testosteronas Rekomenduojama reikšmė. α 2 globulinas 6 11%. Diagnostinė vertė. Nefrozinis sindromas (susijęs su hipoalbuminemija); daugelis poūmių ir lėtinių uždegiminių ir piktybinių ligų, sveikimas po nudegimų. Retai, sergant cukriniu diabetu, pankreatitu, hemolize. Papildoma informacija. α 2 frakcijoje yra α 2 makroglobulino, haptoglobino, apolipoproteino B. α 2 makroglobulino labai padaugėja sergant nefroziniu sindromu. V: estrogenai, oraliniai kontraceptikai Rekomenduojama reikšmė. β globulinas: β 1 5 8%, β 2 3 5%. Diagnostinė vertė. Pirminės ar antrinės hiperlipoproteinemijos (ypač II tipo), monokloninės gamapatijos. Hipo-β-lipoproteinemija, IgA stoka. 123
125 Papildoma informacija. β 1 frakcijoje yra transferino (neigiamas ūminės reakcijos baltymas), hemopeksino, komplemento veiksnių, imunoglobulinų. Tiriant šviežią serumą, β frakcija dažniausiai yra susiskaidžiusi į dvi. Mažesniąją β 2 frakciją daugiausia sudaro lipoproteinai. Jei ėminys nėra šviežias, β 2 frakcijos beveik nematyti. V: estrogenai, geriamieji kontraceptikai Rekomenduojama reikšmė. γ globulinas 11 19%. Diagnostinė vertė. Polikloninės gamapatijos: lėtinės inkstų ligos, lėtinės infekcijos, autoimuninės ligos (pvz., reumatoidinis artritas, sisteminė raudonoji vilkligė). Polikloninės gamapatijos: β γ tiltelis: būdinga sergant hepatitu, ciroze. Polikloninės gamapatijos (oligokloninės), t. y. siaura juosta: lėtinis aktyvusis (lupus) hepatitas, cirkuliuojantys imuniniai kompleksai (pvz., reumatoidinis artritas). Monokloninės gamapatijos: plazminių ląstelių limfoproliferacinės ligos (pvz., dauginė mieloma, makroglobulinemija, amiloidozė, limfoma, lėtinė limfocitinė leukemija), nenustatytos reikšmės monokloninės gamapatijos. Imuninis nepakankamumas ar slopinimas; limfoproliferacinės ligos. Papildoma informacija. γ frakcijoje yra imunoglobulinų G, A, D, E, M. M baltymo buvimui γ, β ar α 2 frakcijose nustatyti būtina imunofiksacinė elektroforezė, nes, pvz., netoli γ frakcijos gali būti ir fibrinogeno; taip gali atsitikti vartojant oralinius antikoaguliantus, nepakankamai sukrešėjus kraujui, esant koagulopatijai. C reaktyviojo baltymo taip pat yra γ frakcijoje ir kai jo labai padaugėja, atsiranda siaura juosta, imituojanti mažą monokloninį imunoglobuliną. Esant specifinėms monogamapatijoms, nenormalus imunoglobulinas gali atsirasti kaip aiškiai išsiskirianti juosta, sudaryta tik iš lengvųjų grandinių. Taip gali atsitikti, kai yra inkstų nepakankamumas. Šios juostos dažniausiai yra siauros ir arti kitų normalių juostų. Jas galima ir pražiūrėti, jei neatliekama imunofiksacija. Tai taikytina ir šlapimo tyrimui. Ceruloplazminas (Cp) Tiriamoji medžiaga. Serumas. Rekomenduojama reikšmė. 0,2 0,6 g/l. Nėštumo metu kiekis didėja ir gali būti 2 3 kartus didesnis, palyginti su normaliomis reikšmėmis. Diagnostinė vertė. Nėštumas, gydymas estrogenais ar oraliniai kontraceptikai, uždegimas, audinių nekrozė, osteosarkoma, biliarinė cirozė, trauma. Ceruloplazmino daugėja lėčiau negu α 1 rūgščiojo glikoproteino, C reaktyviojo baltymo. Ceruloplazminas dar vadinamas poūmės uždegimo fazės reaktantu. Hepatolentikulinė degeneracija (Vilsono liga): sumažėja vario įtraukimas į apoceruloplazminą ir kitus baltymus, dėl to padidėja laisvojo vario kiekis kraujyje ir audiniuose (ypač kepenyse, smegenyse). Menkeso garbanotųjų plaukų sindromas: tai antrinė yda dėl sutrikusios vario absorbcijos iš virškinamojo trakto ir jo panaudojimo. Abu sutrikimai reti, bet jų ankstyva diagnostika svarbi, nes dažniausiai šias ligas galima efektyviai gydyti. Indikacijos nustatyti ceruloplazminą: klinikinis Vilsono ligos įtarimas, nepaaiškinama hepatito ar kepenų cirozės priežastis, lėtinis nervų ir raumenų koordinacijos sutrikimas (ypač paauglių ir jaunų asmenų), Kaizerio Fleišerio žiedai (rusvos spalvos žiedai aplink rainelę), galimas Menkeso garbanotųjų plaukų sindromas (sulėtėjęs plaukų augimas, jie nėra vešlūs, tiriant mikroskopiškai plieniniai ar garbanoti plaukai). Nustatyti ceruloplazmino kiekį svarbu vertinant ūminės reakcijos atsaką ir gydymo efektyvumą. Papildoma informacija. Ceruloplazminas priklauso α 2 globulinų frakcijai ir veikia kaip vario oksidazė. Svarbus reguliuojant oksidaciją, taip pat geležies bei kitų metalų jonų būklę; geriausiai prieinamą organizmui varį perneša albuminai, nors 90 95% plazmoje esančio vario įeina į ceru- 124
126 Žmogaus kraujo plazmos baltymai... loplazmino sudėtį. Serumo drumstumas nepageidaujamas matuojant nefelometriniu metodu. V: estrogenai, fenobarbitalis, karbamazepinas, metadonas, geriamieji kontraceptikai, tamoksifenas. V: asparaginazė. C reaktyvusis baltymas (CRB) Tiriamoji medžiaga. Serumas. Rekomenduojama reikšmė. 5 mg/l. Diagnostinė vertė. Uždegimas, audinių nekrozė ir trauma. Didėja labiau negu kiti ūminės uždegimo fazės baltymai (α 1 antitripsinas, haptoglobinas). Hormonai (endogeniniai, pvz., nėštumas, ar egzogeniniai) neturi įtakos CRB kiekiui. Gydymas steroidais ir nesteroidiniais vaistais nuo uždegimo gerokai sumažina CRB kiekį. Todėl klinikiniam vertinimui CRB yra vienas vertingiausių ūminės reakcijos baltymų. CRB pokyčiai uždegimo metu nustatomi ir naujagimystės tarpsniu; tai svarbu bakterinio sepsio diagnostikai. CRB ne visada didėja esant virusinei ir spirochetinei infekcijai. Todėl nesant traumos labai didelis CRB kiekis gali rodyti bakterinę infekciją. Bakterinio meningito metu ypač padidėjusi koncentracija, būdinga beprasidedančioms neurologinėms komplikacijoms. Nuoseklūs kiekio kitimai reikšmingi vertinant antimikrobinio gydymo efektyvumą. Po chirurginių intervencijų CRB kiekis staigiai didėja, bet paskui greitai mažėja, jei neišsivysto bakterinė infekcija. Todėl kiekio kitimai svarbūs pooperacinei būklei ir galimai infekcijai vertinti. CRB kiekį svarbu nustatyti vertinant reumatoidinio artrito, sisteminės raudonosios vilkligės, vaskulitų, miokardo infarkto klinikinę eigą. Šio baltymo stoka nežinoma. Naujagimių serume kiekis yra mažesnis, palyginti su suaugusiųjų. Papildoma informacija. CRB sintetinamas kepenyse; jo sintezę skatina antigenai, imuniniai kompleksai, bakterijos, grybai ir trauma (pradeda didėti praėjus 4 6 val. po pažeidimo). C reaktyvusis baltymas yra γ frakcijos baltymas, funkciškai panašus į imunoglobuliną G, išskyrus tai, kad CRB nėra antigenui specifiškas. Dalyvaujant kalcio jonams CRB sudaro kompleksus su fosfatidilcholino molekulėmis, esančiomis daugelio bakterijų (pvz., E. coli, S. pneumoniae), grybų ir kitų mikroorganizmų paviršiuje. Kompleksus sudaręs CRB yra stiprus opsoninas monocitams ir skatina fagocitozę. Be to, jis aktyvina klasikinį komplemento kelią. Gerai koreliuoja su eritrocitų nusėdimo greičiu, bet CRB pokyčiai greitesni. Manoma, kad CRB gali būti reikalingas susidarant embolams iš chilomikronų ar agreguotųjų lipoproteinų; tai būdinga vaskulitams. Serumo drumstumas gali turėti įtakos matuojant nefelometriniu metodu. Haptoglobinas (Hp) Tiriamoji medžiaga. Serumas. Rekomenduojama reikšmė. 0,3 2,0 g/l. Diagnostinė vertė. Šis ūminės fazės baltymas uždegimo metu kinta į abi puses: didėja dėl stimuliacijos interleukinais ir mažėja dėl kartu esančios nestiprios hemolizės. Taigi haptoglobino koncentracija gali padidėti, sumažėti ar likti nepakitusi. Kadangi uždegimo metu ne visi minėti procesai vyksta kartu, būtina kartu tame pačiame serumo ėminyje tirti kitus ūminės fazės baltymus, kuriems hemolizė turi mažiau įtakos. Gydymas gliukokortikoidais. Tai gali atrodyti keista, nes dauguma ligų, susijusių su in vivo hemolize, gydomos gliukokortikoidais. Gydant šiais vaistais prealbumino ir α 1 rūgščiojo glikoproteino kiekis dažniausiai taip pat padidėja. Biliarinė obstrukcija. Nefrozinis sindromas gali būti susijęs ir su dideliu, ir su mažu haptoglobino kiekiu nelygu, koks jo genetinis variantas. Hp 1-1 yra maža molekulė ir ji yra šalinama net esant nefroziniam 125
127 pažeidimui, o Hp 2-1 ir 2-2 sulaikomi. Kiekis gali didėti esant nefroziniam sindromui dėl uždegimo ir (ar) gydymo gliukokortikoidais. In vivo hemolizė: autoimuninė, izoimuninė (reakcija į kraujo perpylimą) ar mechaninė (dirbtiniai širdies vožtuvai, poūmis bakterinis endokarditas). Įvairios priežastys: neefektyvioji eritropoezė (folio rūgšties stoka, hemoglobinopatijos), eritrocitų membranų ar jų apykaitos ydos (paroksizminė naktinė hemoglobinurija, paveldima sferocitozė, gliukozės-6-fosfatdehidrogenazės stoka), padidėjusi blužnis. Ūminės ar lėtinės kepenų ligos (pvz., dėl sumažėjusio lipidų kiekio eritrocitų membranoje ar sutrikusios kraujo apytakos kepenyse ir blužnyje eritrocitai yra greičiau). Estrogenai (nėštumas, gydymas estrogenais, oraliniai kontraceptikai). Tyrimi indikacijos, be minėtųjų: anemija ar kitos galimos hemolizės priežastys, hipertenzija dėl nėštumo, reakcijos po kraujo perpylimo (tirti prieš ir po kraujo perpylimo), ūminės uždegimo fazės atsako vertinimas; vertinant α 2 frakcijos pokyčius atliekant serumo baltymų elektroforezę (haptoglobinas ir α 2 makroglobulinas sudaro didžiausią šios frakcijos dalį). Haptoglobino kiekio pokyčiai turi būti vertinami kartu su kitais ūminės uždegimo fazės baltymais, nes uždegimas skatina haptoglobino sintezę. (α 1 rūgštusis glikoproteinas yra geriausias šiam tikslui žymuo.) Papildoma informacija. Skiriami trys paveldimi haptoglobino fenotipai: Hp 1-1, 2-1 ir 2-2. Hp 1-1 plazmoje yra monomero formos, o Hp 2-1 ir 2-2 sudaro įvairaus dydžio gerokai didesnės molekulinės masės kompleksus. Pirminė haptoglobino funkcija yra sulaikyti organizme geležį. Hemoglobino ir haptoglobino kompleksas veikia ir kaip peroksidazė. Kartu su ceruloplazminu, kuris taip pat slopina peroksidaciją, haptoglobinas svarbus vietiškai apsaugant audinius nuo uždegimo. Haptoglobinas greitai sudaro kompleksus su hemoglobino β dimerais, kurie atsipalaiduoja vykstant hemolizei kraujagyslėse. Šiuos kompleksus iš kraujotakos greitai pašalina kepenų Kupferio ląstelės. V: androgenai (anaboliniai steroidai). V: vaistai, sukeliantys hemolizę (pvz., sulfalazinas), estrogenai, oraliniai kontraceptikai, transferinas. Imunoglobulinas A (IgA) Tiriamoji medžiaga. Serumas. Rekomenduojama reikšmė. Vyrų 0,70 3,70 g/l, moterų 0,88 4,10 g/l. Diagnostinė vertė. Polikloninis: lėtinės kepenų ligos, lėtinės infekcijos (ypač virškinamojo trakto ir kvėpavimo takų), apatinės virškinamojo trakto dalies navikai, uždegiminės žarnų ligos, reumatoidinis artritas ir kitos reumatinės ligos. Monokloninis: dauginė mieloma (IgA tipo); retai kitos piktybinės ligos (pvz., limfomos). Oligokloninis: kai kurios disgamaglobulinemijos. Dėl kompleksų susidarymo sergant daugine mieloma neretai galima matyti 2 4 juostas. Kadangi Ig A monokloninės juostos tiriant elektroforeze susidaro arti β 1 ir β 2 juostų, sunku įžiūrėti mažus monokloninius baltymus. Tada reikalingas kiekybinis tyrimas, kuris sumažina klaidingai neigiamų rezultatų skaičių. Izoliuota vienos ar abiejų IgA poklasių stoka nėra retas reiškinys. Paveldimoji IgA stoka nustatoma esant telangiektazinei ataksijai, mišriems imuninio nepakankamumo variantams. Asmenys, neturintys IgA, dažniau serga reumatinėmis ligomis, limfoma. Antrinis nepakankamumas galimas esant ne su IgA susijusiai dauginei mielomai ar makroglobulinemijai, taip pat nefroziniam sindromui. Papildoma informacija. Imunoglobulinas A (IgA) yra pagrindinis imunoglobulinas, randamas sekrete. Serume aptinkama bazinė IgA molekulė yra sudaryta iš dviejų identiškų sunkiųjų alfa (α) grandinių ir dviejų identiškų lengvųjų lambda (λ) ar kapa (κ) grandinių. Specifinis serumo IgA vaidmuo ne iki galo aiškus. Manoma, kad jis svarbus virusų neutralizavimui. 126
128 Žmogaus kraujo plazmos baltymai... Sekrecinis IgA yra dimeras, turintis sekrecinį komponentą, apsaugantį molekulę nuo proteolizinių fermentų. Sekrecinis IgA svarbus apsaugant kvėpavimo, lyties ir šlapimo takus bei virškinamąjį traktą nuo infekcijų. IgA nepereina placentos barjero, dėl to naujagimių serume IgA koncentracija labai maža. Motinos piene esantis IgA svarbus apsaugant naujagimius nuo virškinamojo trakto infekcijų. Apie 10 15% mielomų yra IgA kilmės. Dauguma IgA M komponentų turi tendenciją polimerizuotis ir dėl to tiriant serumo baltymus elektroforeze matyti 2, 3 ar daugiau juostų. Reta yra α grandinių liga (nėra lengvųjų grandinių komponentų). Tokie pacientai yra jaunesnio amžiaus, jiems dažniau pažeidžiamas virškinamasis traktas. Maždaug 1 iš 700 kaukazoidų turi izoliuotą genetinę IgA stoką. Iš jų 1/4 randama antikūnų prieš IgA ir jiems gali išsivystyti sunki anafilaksinė reakcija į plazmos ar kitų kraujo komponentų perpylimą. Galimas tik vieno IgA poklasio genetinis ar įgytasis imuninis nepakankamumas, kai bendrasis kiekis serume normalus. Todėl nustatyti poklasius ar antikūnus prieš IgA naudojant atitinkamus antiserumus rekomenduojama esant nepaaiškinamoms anafilaksinėms reakcijoms po kraujo plazmos ar imunoglobulinų perpylimo. Donorų plazma taip pat turi būti patikrinta. Paprastai IgA 1 sudaro 60 80%, o IgA 2 kitą dalį bendrojo IgA kiekio. Kiekybinio nustatymo indikacijos yra šios: pasikartojančios apatinių kvėpavimo takų ar virškinamojo trakto infekcijos; anafilaksinės reakcijos po kraujo perpylimo (tirti donorą ir recipientą); telangiektazinės ataksijos diagnostika; mielomos M komponentų diferenciacija; IgA mielomos progresavimo įvertinimas. Imunoglobulinas E (IgE) Tiriamoji medžiaga. Serumas. Rekomenduojama reikšmė. <100 ku/l (suaugusiųjų). Diagnostinė vertė. Polikloninis: kai kurios alerginės ligos (parazitinės infekcijos, bronchų ir plaučių aspergiliozė, kai kurių vaistų, ypač aukso junginių, sukeltos atopinės ligos, egzema); astma (60% atvejų), šienligė (30% atvejų), hiperimunoglobulino E sindromas. Monokloninis: IgE mieloma. Kai kurie ilgiau besivystantys navikai, telangiektazinės ataksijos, kai kurie agamaglobulinemijos atvejai (įgimta su lytimi susijusi), padidėjusio jautrumo atvejai. Papildoma informacija. 50% IgE yra kraujotakoje. IgE sintezė embrione, ypač jo plaučiuose ir kepenyse, prasideda jau apie 1-ą gyvenimo savaitę. IgE kiekis dažnai padidėja trūkstant IgA. IgE kiekis įvairuoja pagal genetinius veiksnius ir stimuliuojamąjį aplinkos poveikį. IgE taip pat randama kvėpavimo ir virškinamojo trakto gleivinėje. Imunoglobulinas G (IgG) Tiriamoji medžiaga. Serumas. Rekomenduojama reikšmė. 7,0 16 g/l (suaugusiųjų). Diagnostinė vertė. Polikloninis: autoimuninės ligos sisteminė raudonoji vilkligė, Šiogreno (Sjögren) sindromas, sarkoidozė, lėtinės kepenų ligos (pvz., Leneko cirozė), kai kurios parazitinė s ligos, lėtinės ar pasikartojančios infekcijos, kontraceptinės gimdos priemonės. Oligokloninis: piktybinis procesas, infekcijos (ypač vyresniame amžiuje), kai kurios disgamaglobulinemijos ir autoimuninės ligos. Monokloninis: dauginė mieloma (IgG tipo), limfomos, leukemija, kiti piktybiniai procesai, gerybiniai M komponentai (dažniau vyresnio amžiaus žmonėms). IgG kiekis prieš gimdymą siekia 110% kiekio motinos organizme, bet po gimdymo greitai krinta ir 2 4 gyvenimo mėnesį pasiekia žemiausią lygį (2 3 g/l). Paskui kiekis vėl didėja ir pasiekia suaugusiųjų lygį apie antrus gyvenimo metus. IgA stoka gali būti genetinė (pvz., sunkus mišrusis imuninis nepakankamumas) ar įgyta (ser- 127
129 gant ŽIV). Klinikinių sindromų diagnostikai būtinas humoralinių ir ląstelių imuninio atsako veiksnių įvertinimas. Imuninis nepakankamumas (genetinis ar įgytas) gali būti susijęs tik su vieno IgG poklasio stoka, o bendrasis serumo IgG kiekis gali išlikti normalus. Jei įtarus imuninį nepakankamumą ir ištyrus pagrindines imunoglobulinų klases (IgG, IgA ir IgM) lieka neaiškumų, būtina tirti poklasius. Terminiai nudegimai, pūslelinė, nefrozinis sindromas, enteropatijos netenkant baltymų, ne IgG mieloma ar makroglobulinemija, nėštumas (sumažėjimas dėl praskiedimo). Suintensyvėjusi apykaita: miotoninė distrofija, antikūnai prieš imunoglobulinus. Įvairios priežastys: gydymas imunosupresantais, monokloninė gamapatija, įtraukianti kitus, ne tik IgG imunoglobulinus. Papildoma informacija. Imunoglobulinas G (IgG) yra dominuojantis serume imunoglobulinas, sudarantis apie 75% visų imunoglobulinų ir 10 20% visų serumo baltymų. IgG yra dvipusė veidrodinio atspindžio molekulė, kurios kiekvieną pusę sudaro viena sunkioji grandinė gama (γ) ir viena lengvoji lambda (λ) arba kapa (κ) grandinė. Taigi yra keturi IgG poklasiai. IgG 1 koncentracija yra didžiausia. IgG yra labai svarbus organizmo ilgalaikei gynybai nuo infekcijos. IgG stoka yra susijusi su pasikartojančiomis, kartais sunkiomis pūlinėmis infekcijomis. IgG sintezė ir kiekis serume didėja kaip atsakas į lėtinę ar pasikartojančią infekciją ar autoimunines ligas. Dauguma kliniškai svarbių antikūnų priklauso IgG klasei (prieš branduolius, prieš eritrocitus, prieš pamatinę membraną). Dažniausia dauginės mielomos forma priklauso IgG klasei. 77% šių atvejų yra IgG 1 poklasio. IgG (ypač IgG 1 ) yra vienintelis imunoglobulinas, pereinantis placentą ir todėl labai svarbus vaisiaus gynybai nuo infekcijos. Per pirmąjį gyvenimo mėnesį, kai kūdikio organizme pradedami sintetinti savieji imunoglobulinai, motinos IgG yra katabolizuojami. Mažiausias imunoglobulinų kiekis yra apie trečią gyvenimo mėnesį. Daugumai kūdikių tai praeina nepastebimai, o kai kuriems apie šį gyvenimo laikotarpį išsivysto sunkios pūlinės infekcijos. IgG kiekis sergant ŽIV svyruoja nuo labai sunkaus imuninio nepakankamumo iki hiperimunoglobulinemijos priklausomai nuo klinikinės būklės ir ligos etapo. IgG, esantis kituose organizmo skysčiuose, pvz. smegenų, yra difundavęs iš plazmos. Imunoglobulinas M (IgM) Tiriamoji medžiaga. Serumas. Rekomenduojama reikšmė. Vyrų 0,4 2,4 g/l, moterų 0,34 2,10 g/l. Diagnostinė vertė. Polikloninis: izoliuotas IgM padaugėjimas gali rodyti virusinę infekciją (virusinis hepatitas, infekcinė mononukleozė) ar ankstyvą atsaką į bakterinę, parazitinę infekcijas. Dažnai kiekis padidėja sergant reumatoidiniu artritu, lėtine kepenų liga (pvz., biliarine ciroze), kitomis lėtinėmis ligomis. IgM padaugėja sergant disgamaglobulinemija, aktyviąja sarkoidoze, kolageninėmis ligomis, nefroziniu sindromu. Reumatoidinis faktorius paprastai yra IgM, nukreiptas prieš IgG kompleksus (aprašyti ir IgA bei IgG reumatoidiniai faktoriai). Monokloninis: Valdenstremo makroglobulinemija, piktybinė limfoma, šalčio agliutininų hemolizinė liga. Mišriosios (neizoliuotosios) imuninio nepakankamumo būklės: selektyvioji IgM stoka yra reta ir susijusi su pasikartojančiomis pūlinėmis infekcijomis. Antrinė stoka išryškėja asociacijoje su daugine mieloma (IgA ar IgG) ir enteropatijomis, kurių metu netenkama baltymų (bet ne nefroziniu sindromu). Asmenims, neturintiems IgM ar tik mažą jų kiekį, dažniau išsivysto limfoma. Padidėjusi netektis: enteropatijos, kurių metu netenkama daug baltymų; netekimas per odą (nudegimai). Suintensyvėjusi apykaita: antikūnai prieš imunoglobulinus (pvz., mišrieji krioglobulinai). Įvairios priežastys. Gydymas imunosupresantais, monokloninės gamapatijos dėl kitų, o ne IgM imunoglobulinų. 128
130 Žmogaus kraujo plazmos baltymai... Papildoma informacija. Imunoglobulinas M (IgM) yra pirmasis imunoglobulinas, atsirandantis kaip atsakas į antigeninį stimulą (pvz., infekcinį veiksnį). Dažniausiai antigenui specifinis IgM kiekis krinta kilus IgG atsakui. IgM antikūnai kai kuriais atvejais išlieka, pvz., esant virusinei ar gramneigiamai bakterinei infekcijai. Dauguma natūraliai atsirandančių izohemaglutininų yra IgM klasės (prieš kraujo A ir B grupes). IgM neįveikia placentos barjero. IgM yra didelis molekulinis kompleksas, sudarytas iš penkių monomerinių IgM molekulių. Kiekviena jų turi dvi sunkiąsias miu (µ) grandines ir dvi lengvąsias lambda (λ) ar kapa (κ) grandines. Šis kompleksas gali agliutinuoti dalelių ir ląstelių antigenus. IgM ir antigenų kompleksai aktyviai fiksuoja komplementą. Momomerinis IgM gali pasigaminti sergant kai kuriomis autoimuninėmis ir piktybinėmis ligomis. Valdenstremo makroglobulinemija yra susijusi su monokloniniu IgM padidėjimu, panašiai kaip M komponentas dėl IgG ir IgA dauginės mielomos. Dėl didelės molekulinės masės IgM M komponentas labai padidina kraujo klampumą, todėl sumažėja smegenų ir periferinė kraujotaka. Įgytieji šalčio hemolizinai ar agliutininai dažniausiai yra IgM. Jie neįveikia placentos barjero ir dėl to nėra susiję su hemolizine naujagimių liga. Kiekybinio nustatymo indikacijos yra šios: pasikartojančios ir lėtinės ar labai sunkios infekcijos (tirti dėl imuninio nepakankamumo); nustatyti monokloninius baltymus, matomus tiriant baltymus elektroforeze; įvertinti makroglobulinemijos gydymo veiksmingumą ar progresavimą. Imunoglobulinų lengvosios grandinės Tiriamoji medžiaga. Serumas. Rekomenduojama reikšmė. κ (kapa) 1,7 3,7 g/l, λ (lambda) 0,9 2,1 g/l, κ/λ 1,35 2,65. Diagnostinė vertė. Bet kuri būklė, kai padidėja imunoglobulinų katabolizmas (inkstų kanalėlių patologija, nefrotoksiniai vaistai, sisteminė raudonoji vilkligė) ir padaugėja lengvųjų grandinių, kurios skiriasi su šlapimu. Molekulės nėra monokloninės. Monokloninių lengvųjų grandinių buvimas duoda pagrindo įtarti piktybinę ligą, pvz.: dauginę mielomą, Valdenstremo makroglobulinemiją, amiloidozę, kartais epitelinius piktybinius navikus (žarnų, plaučių). Retai didelis lengvųjų grandinių kiekis atsiranda sergant sunkiomis infekcinėmis ligomis (poūmiu bakteriniu endokarditu). Gydant pirminį procesą baltymas išnyksta. Lengvųjų grandinių padaugėja sergant tam tikromis amiloidozės formomis, nes amiloidinis audinys turi baltymų, kurie reaguoja su antikūnais prieš lengvąsias grandines. Papildoma informacija. Visos imunoglobulinų molekulės savo sudėtyje turi lengvųjų grandinių, kurios yra dviejų tipų: kapa (κ) ir lambda (λ). Sunkiųjų grandinių N galo aminorūgštys ir lengvoji grandinė sudaro antigeną surišančią zoną, kuri išsiskiria labai įvairuojančiu specifiškumu. Laisvųjų grandinių padaugėja dėl imunoglobulinų sintezės ir apykaitos sutrikimų sergant daugeliu ligų, bet ypač sergant gerybinėmis ar piktybinėmis monogamapatijomis. Terminu Bens-Džonso baltymas dažnai netiksliai vadinamos visos lengvosios grandinės. Jis vartotinas apibrėžiant tik su šlapimu besiskiriančias lengvąsias grandines, kurioms būdingas klasikinis Henry Bence-Jones o aprašytas termolabilumas (precipituoja kaitinant, iškrinta nuosėdomis, kai temperatūra netoli virimo, ir vėl ištirpsta šaldant). Mažiau negu 10% visų tiriamųjų šlapimo ėminių, turinčių lengvųjų grandinių, reaguoja šiuo klasikiniu būdu. Sveiki inkstai skaido ir šalina lengvąsias grandines. Progresuojant inkstų nepakankamumui, jų kiekis kraujyje išauga. Geriausiai lengvąsias grandines tirti atliekant koncentruoto šlapimo elektroforezę ir imunofiksaciją su antikūnais prieš lengvąsias grandines. α 2 Makroglobulinas (α 2 M) Tiriamoji medžiaga. Serumas. Rekomenduojama reikšmė. 1,3 3,0 g/l. 129
131 Diagnostinė vertė. Gydymas estrogenais, nėštumas, cukrinis diabetas, kepenų cirozė, hepatitas, α 1 antitripsino stoka, smegenų infarktas, fiziniai pratimai. Sergant nefroziniu sindromu, kiekis padidėja proporcingai baltymų netekimui ir gali viršyti 6 g/l. Paveldima stoka neaprašyta. Kiekis mažėja, kai aktyvinamos proteazės, pvz., dėl ūminio pankreatito ir opaligės metų vyrų kraujyje jo kiekiai maži ir greičiausiai susiję su hormonų įtaka. Lėtinė bronchų obstrukcija, plaučių ligos, dauginė mieloma, preeklampsija, jaunatvinis (juvenilinis) reumatoidinis artritas. Kiekiai maži esant dirbtinei kraujo apytakai (pvz., atliekant avirą širdies operaciją), galutinėms labai sunkių ligų stadijoms. Tyrimo indikacijos, be minėtųjų, yra šios: klinikinės nefrozinio sindromo būklės vertinimas, būklių, kai suintensyvėja proteolizė, vertinimas (pvz., pankreatitas, opaligė, baltymų elektroforegramos α 2 juostos pokyčiai). Papildoma informacija. α 2 makroglobulinas yra vienas iš dviejų elektroforezės α 2 zonos pagrindinių baltymų (kitas yra haptoglobinas). α 2 M yra didelė molekulė, todėl nemaža šio baltymo koncentracija randama tik serume (plazmoje), o inkstų glomerulai jį sulaiko, išskyrus sergant labai sunkiu nefroziniu sindromu. Tai beveik visų endoproteazių inhibitorius. Taip pat suriša ir perneša cinką. α 2 M svarbus krešėjimo fiziologijoje: dalyvauja kraujo krešėjime, krešulio lizėje, komplemento kaskadoje, taip pat reikalingas leukocitų kolagenazės, lizosominių katepsinų, kasos tripsino ir chimotripsino aktyvumo kontrolei. Jis labai greitai prisijungia prie aktyviųjų proteazių, iš pradžių veikdamas kaip substratas, po to jas apvynioja ir sustabdo tolesnį proteolizinį aktyvumą. Tokius α 2 M ir proteazės kompleksus iš kraujotakos greitai pašalina kepenų Kupferio ląstelės. Juos skaido alveoliniai makrofagai. V: geriamieji kontraceptikai. V: dekstranas, streptokinazė. β 2 Mikroglobulinas (β 2 M) Tiriamoji medžiaga. Serumas. Rekomenduojama reikšmė. 0,7 1,8 mg/l. Diagnostinė vertė. Daugelis būklių, kai ląstelių apykaita intensyvesnė už normalią. Tai visi uždegimų tipai, autoimuninės būklės, limfoidiniai piktybiniai dariniai (dauginė mieloma), virusinės infekcijos (pvz., ŽIV, citomegalovirusinė). Sergančiųjų sistemine raudonąja vilklige kraujyje rasta aktyviųjų antikūnų prieš β 2 M. Taip pat didesnis kiekis nustatomas esant amiloidozei, dializuojamiems pacientams. Papildoma informacija. β 2 mikroglobulinas sintetinamas visose branduolį turinčiose ląstelėse. Jo aminorūgščių seka turi homologiją su audinių antigenų lengvosiomis grandinėmis. Tai integrali pagrindinio audinių suderinamumo komplekso (angl. major histocompatibility complex MHC) I klasės antigenų dalis, randama visuose organizmo skysčiuose. Klinikinė svarba iki galo neapibrėžta. β 2 mikroglobulino nustatymas sergantiems ŽIV asmenims gali padėti įvertinti šios ligos, taip pat leukemijos bei limfomos progresavimą. V: ciklosporinas, litis. Reumatoidinis faktorius (RF) Tiriamoji medžiaga. Serumas. Rekomenduojama reikšmė. <15 ku/l. Diagnostinė vertė. Reumatoidinis faktorius randamas sergant reumatoidiniu artritu, Šiogreno sindromu, sklerodermija, dermatomiozitu, Valdenstremo liga, sarkoidoze, sistemine raudonąja vilklige. Tik 75% pacientų, sergančių reumatoidiniu artritu, aptinkamas IgM klasės reumatoidinis faktorius. Didžiausi titrai nustatomi sergant sunkia aktyviąja reumatoidinio artrito forma, kartu esant vaskulitui, poodiniams mazgeliams % ligonių, sergančių Šiogreno sindromu, reumatoidinio faktoriaus titrai yra dideli. 130
132 Žmogaus kraujo plazmos baltymai... Papildoma informacija. Reumatoidinį faktorių sudaro antikūnai, reaguojantys su IgG ir priklausantys IgM klasei, nors apie 15% pacientų turi IgG klasės RF. Dauguma metodų aptinkama tik IgM klasės RF. Titrai 1 : 80 yra abejotini ir galimi sergant infekcine mononukleoze, ūminiu uždegimu, vyresnio amžiaus asmenims. Latekso agliutinacijos metodas yra jautresnis (75% teigiamas sergant reumatoidiniu artritu), bet ne toks specifiškas, palyginti su avių ląstelių mėginiu (75% tikrai teigiami). α 1 Rūgštusis glikoproteinas Tiriamoji medžiaga. Serumas. Rekomenduojama reikšmė. 0,5 1,2 g/l. Diagnostinė vertė. Uždegimas, pvz., esant infekcijai, traumai, chirurginei intervencijai. Ypač vertingas diferencijuojant ūminės uždegimo fazės atsaką (didėja), nuo estrogenų poveikio (nekinta ar mažėja), nes abu šie veiksniai didina ceruloplazmino, α 1 antitripsino ir kitų ūminės fazės baltymų kiekį. Kartu su haptoglobinu α 1 rūgštusis glikoproteinas yra vienas jautriausių baltymų, kurių kiekis didėja vykstant hemolizei in vivo. Padidėjęs jo kiekis, esant normaliai haptoglobino koncentracijai, rodo ūminę reakciją su silpna hemolize in vivo. Naujagimystėje ir ankstyvoje vaikystėje; vartojant 17-α hidroksiandrogenus; esant galutinėms kepenų ligų stadijoms; dėl nefrozinio sindromo gausiai netenkant baltymų; dėl genetinių priežasčių; gali sumažėti ankstyvuoju nėštumo laikotarpiu vartojant geriamuosius kontraceptikus. Indikacijos atlikti šį tyrimą: ūminio uždegimo, navikų recidyvo diagnostika (ypač tų navikų, kuriems būdinga nekrozė, pvz., plaučių plokščiųjų ląstelių vėžys, hipernefroma, krūties ir storosios žarnos adenokarcinoma), kartu su haptoglobinu hemolizės in vivo diagnostika ir gydymo gliukokortikoidais vertinimas. Papildoma informacija. α 1 rūgštusis glikoproteinas, arba orozomukoidas, yra labai rūgštus baltymas. Elektroforeziškai heterogeniškas, genetiškai polimorfiškas, koduojamas dviejų genų. Jo, kaip ūminės fazės baltymo, sintezė yra skatinama dviejų lipopolisacharidų, atsipalaidavusių iš interleukino-6 aktyvintų makrofagų. Fiziologinė reikšmė nėra iki galo aiški. Veikia trombocitų sulipimą, slopina imuninį reaktyvumą. Suriša nemažai vaistų, hormonų (progesteroną). Tai vienas pastoviausiai teigiamų ūminės uždegimo fazės žymenų. V: antiepileptiniai vaistai, karbamazepinas. V: estrogenai, geriamieji kontraceptikai, penicilaminas, tamoksifenas. 131
133 FERMENTŲ KLINIKINĖ BIOCHEMIJA IR INTERPRETAVIMAS Bendrosios žinios apie fermentus Fermentai tai baltymai, organiniai katalizatoriai, kuriuos gamina ląstelės, bet jų veikimas neapsiriboja vien intaktine ląstele. Taigi fermentai rodo įvairių organų tarpusavio ryšį. Vykstant fiziologiniams procesams ar kaip ligų pasekmė, jie patenka į organizmo skysčius (plazmą, šlapimą, virškinimo sultis ir kt.). Dauguma fermentų, pvz., pepsinas, tripsinas, kitos hidrolazės, yra paprastieji baltymai; kiti fermentai yra sudėtiniai baltymai, kuriuos sudaro baltyminė dalis (apofermentas) ir nebaltyminė kofaktorius (metalas ar organiniai junginiai). Kofaktorius, būdamas organiniu junginiu, vadinamas kofermentu (į daugelio jų sudėtį įeina vandenyje tirpių vitaminų). Kofermentai, su baltymu susijungę tvirtu ryšiu, sudaro prostetinę grupę, pvz., hemą (katalazėje), flavinadenindinukleotidą FAD (flavoproteinuose). Medžiaga, veikiama fermento, vadinama substratu. Mažiausių gyvojo pasaulio fermentų (bakterinių nukleazių) molekulinė masė yra apie daltonų (Da), didžiausių per 1 milijoną daltonų. Prisimintina, kad gliukozės molekulinė masė yra 180 Da, cholesterolio 386 Da. Dauguma proteolizinių fermentų, gaminamų ląstelėje, yra neaktyvios pirmtakų, vadinamų zimogenais, formos. Tokių aktyvių fermentų sintezė sukeltų pačios ląstelės destrukciją. Aktyvinimas yra susijęs su daline hidrolize, po kurios susidaro aktyvūs centrai arba yra pašalinamas slopinantis peptidas. Pavyzdžiui, pepsinas yra sintetinamas pepsinogeno forma. Jo molekulinė masė yra Da ir jį sudaro 362 aminorūgščių liekanos. Aktyvavimas vyksta rūgščioje terpėje autokatalizės būdu, dalyvaujant pepsinui, kai netenkama polipeptido, sudaryto iš 42 aminorūgščių liekanų nuo zimogeno N galo. Fermentai gali būti santykinai specifiški (kai veikia keletą substratų) ir absoliučiai specifiški (veikia tik vieną substratą). Pavyzdžiui, virškinimo fermentai, hidrolizuojantys peptidinius ryšius, priklauso santykinai specifiškų grupei, o fermentas ureazė veikia tik šlapalą ir dėl to yra absoliučiai specifiškas. Šis fermentas naudojamas šlapalo koncentracijai nustatyti. Fermentų aktyvumo veiksniai Kadangi fermentų kiekiai yra labai maži, kad juos išmatuotume kiekybiškai, tai matuojamas fermentų aktyvumas. Aktyvumo vienetas (U) tai fermento kiekis, kuris 132
134 Fermentų klinikinė biochemija ir interpretavimas pagamina 1 mikromolį produkto per 1 minutę standartinėmis sąlygomis (temperatūra, optimalus ph ir esant pakankamai substrato koncentracijai) µmol/min. Vartojamas ir specifinio aktyvumo terminas tai fermento vienetų skaičius 1 mg baltymo (µmol/min/mg, arba U/mg baltymo). Tarptautinės biochemikų sąjungos Fermentų nomenklatūros komisija rekomendavo fermentų aktyvumą išreikšti ne µmol/min, o SI vienetais moliais per sekundę (mol/s) ir pavadinti naująjį vienetą katalu (kat). 1 katalas rodo 1 molio substrato pavirtimą produktu per sekundę. Katalizinė fermento koncentracija tai aktyvumo vienetų skaičius, tenkantis 1 l organizmo skysčio (serumo, šlapimo ir kt.). Katalizinės fermento koncentracijos ir aktyvumo terminai gali būti vartojami sinonimiškai. Fermentai yra biologiniai katalizatoriai, jie labai padidina reakcijų greitį nuo 10 9 iki kartų. Fermentų katalizuojamų reakcijų greitį veikia daugelis veiksnių: 1) vandenilio jonų koncentracija, 2) temperatūra, 3) fermento koncentracija, 4) laikas, 5) substrato koncentracija, 6) reakcijos produktai, 7) šviesa ir kiti fizikiniai veiksniai, 8) įvairių jonų prigimtis ir kiekis, 9) alosterinis efektas, 10) hormonai ir kiti biocheminiai agentai. Vandenilio jonų koncentracija. Optimalus reakcijos ph yra toks, kuriam esant fermentinė reakcija vyksta greičiausiai. Todėl fermentų aktyvumas matuojamas buferiniuose tirpaluose silpnųjų rūgščių ir druskų mišiniuose, kurie geba surišti (neutralizuoti) rūgštis ir šarmus ir palaikyti pastovų ph. Pakitus aplinkos ph, fermentai gali netekti aktyvumo. Nustatant fermentų aktyvumą, būtina pasigaminti tam fermentui optimalaus ph buferinį tirpalą. Genų mutacijos, sukeliančios fermento ph pokyčius, yra svarbios fermentinėms funkcijoms. Tokie fermentai net ir fiziologinėmis sąlygomis gali nebūti aktyvūs, o sergant alkaloze visai netekti aktyvumo. Tada fermentinės reakcijos labai sulėtėja ar net nutrūksta. Temperatūros įtaką fermentinių reakcijų greičiui nusako reakcijos temperatūros koeficientas. Tai reakcijos greičio padidėjimas pakilus temperatūrai 10 C. Jis žymimas Q 10. Fermentų ši reikšmė dažniausiai svyruoja nuo 1,1 iki 3, t. y. pakėlus temperatūrą 10 C, fermentinių reakcijų greitis padidėja 1,1 3 kartus. Optimali gyvūniniams fermentams temperatūra yra C, augaliniams C. Jei temperatūra aukštesnė, reakcijos greitis pradeda lėtėti, nes prasideda baltymo dena- 133
135 tūracija. Dauguma fermentų denatūruojasi 60 C temperatūroje. Svarbus ir buvimo toje temperatūroje (ekspozicijos) laikas, nes trumpą temperatūros pakilimą fermentas gali atlaikyti. Paprastai fermentinės reakcijos atliekamos 25 C, 30 C ar 37 C temperatūroje. Kiekviena jų turi ir pranašumų, ir trūkumų. Laboratorijose paprastai būna apie 25 C temperatūra, todėl daugelį fermentų tyrimų galima atlikti nestatant bandinių į termostatą. 37 C temperatūra yra artimiausia fiziologinei. Be to, šią temperatūrą paprasčiau palaikyti negu žemesnę. Tačiau kai kurie fermentai 37 C temperatūroje lėtai inaktyvuojasi. Kuo aukštesnė temperatūra, tuo greičiau vyksta reakcija. Greituosiuose analizatoriuose paprastai fermentinės reakcijos vyksta 37 C ar 38 C temperatūroje. Hipotermijos sąlygomis dauguma fermentinių reakcijų sulėtėja. Tai susiję su sumažėjusiu deguonies poreikiu žemesnėje temperatūroje. Genų mutacijos, dėl kurių fermentai tampa termolabilūs, gali būti reikšmingos. Pavyzdžiui, eritrocitų membranos pakinta dėl redukuotojo glutationo stokos: reikiamą jo kiekį palaiko NADF, susidaręs pentozių cikle, kurio reguliacinis fermentas yra gliukozės-6-fostatdehidrogenazė. Šio fermento stoka ar neaktyvumas išryškėja eritrocitų hemolize. Yra žinoma šį fermentą lemiančio geno mutacija, pasižyminti sumažėjusiu termostabilumu. Dėl to sutrumpėja eritrocitų gyvavimo laikas, be to, tokie eritrocitai tampa jautrūs vaistų poveikiui, o tai irgi išryškėja hemolize. Fermento koncentracija. Fermentinės reakcijos greitis yra tiesiogiai proporcingas fermentino koncentracijai, jei yra pakankamas substrato kiekis. Laiko reikšmę reakcijos greičiui nusako produkto kiekis, pagamintas per laiko vienetą. Substrato koncentracija. Esant tam tikram fermento kiekiui, reakcijos greitis didėja, didėjant substrato koncentracijai. Iš pradžių šis ryšys yra tiesinis, tačiau vėliau stabilizuojasi (pasiekia plato fazę). Kol reakcijos greitis yra proporcingas substrato kiekiui, reakcija vyksta pagal pirmos eilės kinetikos dėsnius (pirma fazė). Antroje, arba stabilizacijos, fazėje reakcijos greitis esti pastovus ir vyksta pagal nulinės eilės kinetikos dėsnius. Šis taškas pasiekiamas tada, kai tolesnis substrato koncentracijos didėjimas neveikia reakcijos greičio, o reakcijos greitis yra maksimalus (V max ). Fermentiniams tyrimams būtina naudoti tokį substrato kiekį, kad reakcijos greitis būtų maksimalus ir tolesnė substrato koncentracijos kaita neveiktų fermentų aktyvumo. Paprasčiausia fermentinių reakcijų išraiška k 1 k 2 F + S FS F + P; k 1 k 2 čia: F fermentas, S substratas, P produktas, FS fermento ir substrato kompleksas. Kiekvienas reakcijos etapas apibūdinamas specifine greičio konstanta: susidarant FS iš F ir S, konstanta k 1, disocijuojant FS į F ir S k 1 ; P ir F susidarymas iš FS apibūdinamas konstanta k 2, o FS susidarymas iš P ir F k
136 Fermentų klinikinė biochemija ir interpretavimas L. Michaelis ir M. Menten pasiūlė modelį, kaip susieti fermentinės reakcijos greitį (V), esant tam tikrai substrato koncentracijai (S), su maksimaliu greičiu ir atitinkama substrato koncentracija, ir aprašė jį lygtimi V max [S] V =, K M +[S] V max kai V =, K M = [S]; 2 čia K M yra Michaelio konstanta, apibūdinanti fermento giminingumą substratui kuo ji mažesnė, tuo F ir S giminingesni. Daugelio fermentų ši konstanta svyruoja nuo ir daugiau. Fermentų inhibitoriai. Daug naujo apie fermentines reakcijas galima sužinoti naudojant inhibitorius substratų analogus. Tai svarbu ir medicinai. Skiriamos konkurencinės ir nekonkurencinės inhibicijos rūšys. Konkurencinei inhibicijai naudojami substrato analogai, kurie savo struktūra labai panašūs į substratą ir geba užimti aktyvųjį fermento centrą. Tačiau produktas susidaro lėtai ar visai nesusidaro. Kadangi substrato analogas konkuruoja su tikruoju dėl fermento aktyviojo centro, tai ir inhibavimas yra konkurencinis. Jis yra grįžtamasis procesas. Konkurencinių inhibitorių veikimą galima pašalinti padidinus substrato kiekį. Nekonkurencinė inhibicija tai kita grįžtamosios inhibicijos rūšis. Inhibitorius sąveikauja ne aktyviuoju centru, o kita fermento vieta, t. y. substratas ir inhibitorius nekonkuruoja dėl aktyviojo fermento centro. Šiuo atveju substrato koncentracijos didinimas nepanaikina inhibicijos, kaip yra vykstant konkurencinei inhibicjai. Konkurencinė inhibicija taikoma medicinoje. Modernioji vaistų terapija, kartu antivirusinių, antibakterinių, antinavikinių vaistų vartojimas, pagrįsti fermentų inhibicija. Ypač plačiai gydoma antimetabolitais. Tai junginiai, kurių struktūra, palyginti su natūraliu substratu, yra šiek tiek kitokia. Paprasčiausias jų atstovas yra sulfanilamidai. Tai stiprūs bakterijų augimo inhibitoriai bakteriostatikai. Jie nukonkuruoja p-aminobenzenkarboksirūgštį susidarant folio rūgščiai, o pastaroji būtina bakterijoms augti. Žinoma, kad bakterijos negali įsisavinti šeimininko folio rūgšties joms augti būtino vitamino, jį sintetina pačios. Vienas iš folio rūgšties sintezei būtinų komponentų yra p-aminobenzenkarboksirūgštis. Sulfanilamidai yra struktūriniai p-aminobenzoato analogai, todėl juos vartojant nutrūksta folio rūgšties susidarymas. Kadangi žmogus folio rūgštį gauna su maistu, tai jam sulfanilamidai tokiomis dozėmis, kurios slopina bakterijų augimą, nėra žalingi. Purinų ir pirimidinų bazių nukleotidų (nukleorūgščių komponentų) sintezei taip pat būtina folio rūgštis. Žinomas preparatas metotreksatas yra struktūrinis folio rūgšties analogas ir juo buvo efektyviai gydoma leukemija, ypač vaikų. Jis konku- 135
137 ruoja su dihidrofolio rūgštimi (DHFR) dėl fermento dihidrofolatreduktazės. Metotreksatas apie 1000 kartų geriau jungiasi su fermentu negu natūralus substratas ir yra stiprus konkurencinis inhibitorius. Jam veikiant nutraukiama timidino monofosfato sintezė ir ląstelių dalijimasis sustoja, leukeminės ląstelės nesidaugina. Tačiau greitai besidauginančios žmogaus kaulų čiulpų ląstelės yra taip pat jautrios šiam preparatui. Sukurti ir kiti panašaus veikimo antimetabolitai, kaip fluoruracilis (timino analogas), 6-merkaptopurinas (adenino ir guanino analogas). Specifiniai proteolizinių fermentų inhibitoriai egzistuoja gamtoje, pavyzdžiui, parazitinės kirmėlės Ascaris lumbricoides kūno paviršiuje turi keletą specifinių peptidų, kurie slopina tripsiną, chimotripsiną, dėl to parazitas gali įsiskverbti į šeimininko virškinamąjį traktą. Alosterinis efektas, susijęs su baltymo konformacijos pokyčiais. Medžiagų apykaitos reguliavimas priklauso nuo modifikuojančio įvairių veiksnių poveikio fermentų aktyvumui. Alosterinis efektas, arba alosterizmas, tai reguliacinio fermento polipeptidinių grandinių erdvinės struktūros (konformacijos) pasikeitimas. Reguliaciniai fermentai dažniausiai yra sudaryti iš kelių ar keliolikos polipeptidinių grandinių, kurios susijungusios elektrostatinėmis, vandenilinėmis, hidrofobinėmis ir kitomis jungtimis. Alosterizmas išryškėja tada, kai viena grandinė sujungia kurį nors efektorių (juo gali būti ir substratas); pakitus šio subvieneto erdvinei struktūrai, kinta ir gretimos grandinės struktūra. Dėl to gali padidėti (ar sumažėti) kitos grandinės giminingumas substratui ir taip padidinamas (arba sumažinimas) reakcijos greitis. Šis efektas būdingas daugeliui fermentų, sudarytų ne iš vienos polipeptidinės grandinės, bet bent iš dviejų. Alosterinį efektą galima iliustruoti hemoglobino pavyzdžiu (nors jis nėra fermentas, tačiau tai oligomerinis baltymas, sudarytas iš 4 polipeptidinių grandinių). Kiekviena grandinė gali prijungti deguonies molekulę. Bet šių grandinių trauka (gebėjimas sujungti) deguoniui yra nevienoda. Kai pirma grandinė prijungia deguonies molekulę, jos erdvinė struktūra pakinta ir pakeičia kitų grandinių struktūrą ir tada tos polipeptidinės grandinės lengviau prijungia deguonį. Tarp grandinių, sakoma, vyksta kooperatinė sąveika; ji būdinga alosteriniams fermentams. Mioglobinas yra sudarytas iš vienos polipeptidinės grandinės ir, prisjungiant deguonį, jo erdvinė struktūra nepakinta. Izo f e r m e n t a i Izofermentai (izozimai, arba izoenzimai) tai fermentų variantai, t. y. fermentai, turintys tą patį katalizinį aktyvumą (vykdantys tą pačią reakciją), bet egzistuojantys keliomis molekulinėmis formomis toje pačioje gyvūnų rūšyje; jie skirtingai migruoja elektriniame lauke. Izofermentai yra svarbūs reakcijų reguliavimui. Jie gali būti vieno geno produktai, kai fermentą baltymą koduoja vienas genas, bet po sintezės jis yra įvairių veiksnių modifikuojamas pakeičiant krūvį ar erdvinę struktūrą. Tačiau izofermentai gali būti ir daugiau nei vieno geno produktai. 136
138 Fermentų klinikinė biochemija ir interpretavimas Klasikinis tokio fermento pavyzdys laktatdehidrogenazė (LDH). Tai tetrameras iš dviejų rūšių polipeptidinių grandinių. Širdies raumenyje esanti LDH sudaryta iš keturių H grandinių (angl. heart širdis), o griaučių raumenyse keturių M grandinių (angl. muscle raumuo). Šias grandines koduoja skirtingi genai, ir skirtingi LDH izofermentai, katalizuojantys tą pačią reakciją, skiriasi katalizinėmis savybėmis. Abiejų rūšių LDH grandinės skiriasi aminorūgščių sudėtimi, taigi ir elektroforeziniu judrumu. Laktatdehidrogenazė, sudaryta tik iš H grandinių, žymima LDH-I. Tiriant elektroforeze, ji nuo starto linijos pasislenka toliausiai. Laktatdehidrogenazė, sudaryta iš trijų H grandinių ir vieno M grandinės, žymima LDH-II. Atitinkamai dvi H ir dvi M grandinės suformuoja LDH-III, viena H ir trys M grandinės LDH-IV, o keturios M grandinės sudaro LDH-V. Pastarasis izofermentas, tiriant elektroforeze, lieka starto linijoje. Taip elektroforegramoje gaunamas penkių juostų vaizdas. LDH-I ir LDH-II izofermentų didžiausias aktyvumas yra miokarde ir eritrocituose, LDH-III smegenyse ir inkstuose, LDH-V kepenyse, griaučių raumenyse. Kitas izofermentų turinčio fermento pavyzdys yra kreatinfosfokinazė (KFK). Tai dimeras iš dviejų rūšių polipeptidinių grandinių: M (raumenų tipo) ir B (smegenų tipo). Smegenyse randamos dvi B grandinės, raumenyse dvi M. Širdies raumenyje yra abiejų polipeptidinių grandinių MB derinys. Tiriant elektroforeze, greičiausiai anodo link juda KFK-I, po to KFK-II (MB izofermentas) ir lėčiausiai juda MM izofermentas tai KFK-III. Api b e n d r i n i m a s Fermentai tai organiniai katalizatoriai baltymai, kuriuos gamina gyvosios ląstelės, bet jų veikimas neapsiriboja vien intaktine ląstele. Fermentai specifiškumu gali būti santykinai specifiški ir absoliučiai specifiški (stereospecifiški). Fermento aktyvumo vienetas (U) tai fermento kiekis, kuris pagamina 1 mikromolį produkto per 1 minutę standartinėmis sąlygomis (temperatūra, optimalus ph ir esant pakankamai substrato koncentracijai), jis žymimas µmol/min. Izofermentai tai fermentų formos, kurios skiriasi savo erdvine struktūra, aptinkamos skirtinguose audiniuose, bet katalizuoja tą pačią reakciją. Klinikinė enzimologija Tiksliai nežinoma, kiek fermentų yra žmogaus organizme. Manoma, kad mažiausiai apie Šiuo metu žinoma tik apie 140 fermentų defektų ir ligų. 137
139 Medicinoje fermentai yra naudojami: kaip reagentai biologinių skysčių sudedamųjų dalių kiekiui nustayti, kaip patologijos ar ligos rodiklis, gydymui. Fermentai kaip reagentai naudojami įvairių medžiagų kiekiui biologiniuose skysčiuose nustatyti ir pasižymi šiais privalumais: jie yra specifiški substratui, labai jautrūs, netoksiški, o jų katalizuojamos reakcijos greitos. Pagal fermentinę technologiją reikia laikytis optimalių aplinkos sąlygų. Daug reakcijų yra sudarytos taip, kad nikotinamidadenindinukleotido ar jo fosfato oksiduotosios formos (NAD + ar NADF + ) yra naudojamos kaip kofermentai. Šių kofermentų redukuotosios formos NADH ir NADFH sugeria 340 nm ilgio bangas, o NAD + ir NADF + jų nesugeria. Taigi galima nustatyti fermentinę reakciją atsižvelgiant į šviesos sugerties kitimus pagal NADH susidarymą (optinis tankis didėja) ar kai NADH yra oksiduojamas ir virsta NAD + (optinis tankis sumažėja). Tai vadinamasis optinis Varburgo (Warburg) principas. Šiuo principu nustatomas fermentų aktyvumas kinetiniu metodu, t. y. atliekami matavimai laiko atžvilgiu (reakcijos pradžioje ir jai vykstant) matavimo aparato kiuvetėje. Tai gerokai padidina matavimų tikslumą. Toliau pateikiami kai kurie klinikinių biocheminių metodų pavyzdžiai, kai fermentai naudojami kaip reagentai. Gliukozės koncentracija gali būti nustatyta naudojant gliukozoksidazę, kurios veikiama gliukozė oksiduojama į gliukono rūgštį. Kitas šios reakcijos produktas yra vandenilio peroksidas (H 2 O 2 ). Jo kiekį galima užregistruoti įvairiais metodais. Viename jų naudojamas dar vienas fermentas peroksidazė, kuri vandenilio peroksidą (H 2 O 2 ) paverčia vandeniu (H 2 O) ir deguonimi (O 2 ). Deguonis oksiduoja O-dianizidą, susidaro spalvotas junginys. Iš spalvos intensyvumo sprendžiama apie gliukozės koncentraciją. Šį metodą galima taikyti ir kokybiniam, ir pusiau kokybiniam gliukozės kiekio nustatymui, pavyzdžiui, atliekant reakciją ant filtrinio popieriaus juostelių, impregnuotų fermentu. Lietuvoje pagamintų gliukozės analizatorių Eksan-G veikimo principas pagrįstas elektrocheminiu vandenilio peroksido (H 2 O 2 ) nustatymu. Susidaręs H 2 O 2 elektrochemiškai oksiduojamas elektrodo paviršiuje, o srovės išmatuojamas pokytis atitinka gliukozės koncentraciją. Šlapalo kiekį galima nustatyti fermentu ureaze, kuri šlapalą paverčia amoniaku ir anglies dioksidu: Ureazė Šlapalas + H 2 O 2NH 3 + CO 2 Šios reakcijos metu atsipalaidavęs amoniakas reaguoja su α oksoglutaratu ir virsta glutamo rūgštimi (dalyvaujant fermentui glutamatdehidrogenazei GDH). Šiai reakcijai reikia NADH; jai vykstant jis oksiduojamas į NAD + : 138
140 Fermentų klinikinė biochemija ir interpretavimas NH 3 + α oksoglutaratas GDH NADH NAD + Glutamo rūgštis + H 2 O Pagal optinio tankio kitimą ir nustatomas šlapalo kiekis. Yra ir kitų šios reakcijos modifikacijų. Pavyzdžiui, pusiau kokybinis metodas, kai filtrinio popieriaus juostelė impregnuojama fermentu ureaze ir dažikliu, pavyzdžiui, bromkrezolio žaliuoju. Atsipalaidavęs amoniakas pakeičia dažo spalvą, ir spalvos keitimosi intensyvumas rodo šlapalo koncentraciją. Lietuvoje gamintų analizatorių Eksan-U šlapalo nustatymo principas grindžiamas taip pat fermentine reakcija: ureazė skaldo šlapalą, susidaręs NH 3 keičia ph (terpė šarmėja); stiklo elektrodu registruojamas pašarmėjimas ir gauti rezultatai perskaičiuojami į šlapalo koncentraciją. Šlapimo rūgščiai nustatyti naudojamas fermentas urikazė. Ji šlapimo rūgštį paverčia alantoinu. Šlapimo rūgštis absorbuoja šviesą esant nm bangos ilgiui, o alantoinas jos neabsorbuoja. Šlapimo rūgšties kiekis yra proporcingas optinio tankio sumažėjimui. Yra ir kitų šio metodo modifikacijų. Alkoholio kiekį galima nustatyti vartojant fermentą alkoholdehidrogenazę (ADH). Ji paverčia alkoholį acetaldehidu. Reakcijoje dalyvauja oksiduotas NAD +, kuris redukuojamas į NADH. Susidaręs NADH gerai sugeria 340 nm ilgio bangas. Ekstinkcijos padidėjimas atitinka alkoholio koncentraciją. Šią reakciją galima modifikuoti naudojant dažiklį, kurio spalvos pasikeitimas atitiks substrato koncentraciją. Fermentinis cholesterolio nustatymas. Vienas iš būdų išmatuoti cholesterolio koncentraciją kraujyje yra pagrįstas elektrocheminiu vandenilio peroksido nustatymu. Vandenilio peroksidas (H 2 O 2 ) susidaro fermentiniu būdu oksiduojant cholesterolį: Cholesterolio esteriai Cholesterolesterazė H 2 O Cholesterolis + Riebalų rūgštis Cholesteroloksidazė Cholesterolis Cholestenonas + H 2 O 2 O 2 + H 2 O Susidaręs H 2 O 2 elektrochemiškai oksiduojasi ant platinos elektrodo. Srovės pokytis proporcingas cholesterolio arba cholesterolio esterių koncentracijai kraujo serume. Diagnostika tiriant fermentus. Fermentų aktyvumo (kiekio) kraujo serume tyrimo tikslas padėti nustatyti ligą, jos sunkumą, prognozę, gydymo veiksmingumą, diferencijuoti ligas ir aptikti jų komplikacijas. Kraujo plazmos fermentų aktyvumo 139
141 nustatymas grindžiamas prielaida, kad aktyvumo pokyčiai rodo specifinio audinio ar organo kitimus. Kraujo plazmoje randami fermentai yra dvejopos kilmės. Vienų fermentų yra labai daug, jie specifiniai plazmai ir turi funkcinę reikšmę. Tai kraujo krešėjimo (trombinas), fibrino tirpinimo (plazminas) fermentai, chilomikronų metabolizmo fermentas (lipoproteinlipazė), inkstų glomeruluose sintetinamas reninas ir kt. Kitų fermentų koncentracijos yra labai mažos, ir jie kraujo plazmoje funkcijų neatlieka. Sergant, kai pažeidžiami audiniai ir organai, šie nespecifiniai plazmai fermentai yra svarbiausi. Kiekvienas organas turi jam būdingus fermentus. Didelis jų kiekis kraujo plazmoje rodo to organo pažaidą. Normaliai šių fermentų aktyvumas kraujo plazmoje yra nedidelis. Tai fiziologinis įvairių audinių ląstelių apykaitos, ląstelių susidėvėjimo ir irimo proceso produktas. Fermentų aktyvumas kraujo plazmoje, palyginti su jų aktyvumu ląstelėse, yra labai mažas. Žmogaus organizme per sekundę žūva apie 50 milijonų ląstelių, bet tiek pat susidaro naujų. Didžiausią įtaką fiziologiniam, o esant pažeidimui ir patologiniam fermentų aktyvumui kraujyje turi kai kurios ląstelės. Kraujo ląstelės. Nuo jų atsinaujinimo daugiausia priklauso fiziologinis fermentų aktyvumas: pirma, dėl didelio eritrocitų skaičiaus ir, antra, dėl trumpo trombocitų gyvavimo (gyvavimo puslaikis 4 dienos). Pavyzdžiui, normalus fiziologinis laktatdehidrogenazės, rūgščiosios fosfatazės aktyvumas labai priklauso nuo eritrocitų, trombocitų. Kraujagyslių endotelis. Jo ląstelės taip pat atpalaiduoja fermentus tiesiai į kraują, o iš viso tai sudaro apie kelis milijardus ląstelių, kurios atsinaujina per keletą mėnesių. Kepenys, blužnis. Jos labai gerai aprūpintos krauju, jų parenchimos ląstelės turi glaudų sąlytį su cirkuliuojančiu krauju, taigi šie organai lemia fiziologinį fermentų aktyvumą kraujo serume. Raumenys. Jie sudaro kūno masės pagrindą ir funcinio aktyvumo metu atpalaiduoja fermentų molekules. Pavyzdžiui, serume kreatinfosfokinazės aktyvumas yra didesnis vakare negu ryte. Patologinis procesas pažeidžia membranos pralaidumą ar sukelia ląstelės žūtį, ir tada ląsteliniai fermentai atsipalaiduoja į tarpląstelinę erdvę ir kraujo plazmą. Pagrindinė fermentų atsipalaidavimo iš ląstelės mechanizmų hipotezė buvo sukurta remiantis J. Wilkinsono (1974) darbais, kuriuos pratęsė ir papildė R. Friedelis ir F. Diederichas ( ). Tyrimų esmė ta, kad mažinant adenozintrifosfato (ATF) koncentraciją limfocituose, lygiagrečiai didėja laktatdehidrogenazės koncentracija kraujyje. Remiantis šia hipoteze, fermentų atsipalaidavimo iš ląstelės mechanizmas yra toks: 1) ląstelė, kai joje energijos kiekis normalus, užima tam tikrą tūrį. Jį palaiko nuo ATF priklausomas jonų siurblys: pastarasis kaupia ląstelėje kalio jonus (K + ) ir šalina kalcio, natrio jonus (Ca 2+, Na + ) ir H 2 O; 140
142 Fermentų klinikinė biochemija ir interpretavimas 2) jei ATF kiekis ląstelėje sumažėja (ląstelė serga ), jonų siurblys susilpnėja ir ląstelė išburksta, joje padaugėja Ca 2+, kuris aktyvina kontraktilines skaidulas membranos vidinėje pusėje, dėl to membranoje atsiveria poros, pro kurias ląstelė netenka fermentų; tai pradinis ir grįžtamas pažeidimo etapas; 3) kai ląstelė visai nustoja gaminti ATF, ląstelės vientisumo neįmanoma palaikyti, ir visas jos turinys išsilieja į aplinką. Tai negrįžtama ląstelės žūties stadija. Yra ir kitų hipotezių. Pavyzdžiui, manoma, kad ląstelėje esantys kalcio jonai aktyvina su membrana susijusią fosfolipazę A 2. Šis fermentas membranos fosfolipidą lecitiną verčia lizolecitinu. Dėl to ląstelės membrana pakinta, padidėja jos pralaidumas, ir fermentai patenka į aplinką. Organui specifinių fermentų aktyvumo kraujo plazmoje ar serume tyrimas padeda nuspręsti, koks organas ir kiek jis pažeistas, t. y. diagnozuoti ligą. Net ir nedideli pažeidimai pakeičia ląstelės membranos pralaidumą, ir į plazmą patenka ląstelės citoplazmoje esantys fermentai, pavyzdžiui, alaninaminotransferazė. Esant didesniems pažeidimams, iki ląstelės nekrozės, kraujyje pasirodo fermentų, esančių įvairiose ląstelės struktūrose: mitochondrijose, membranose, lizosomose (pavyzdžiui, aspartataminotransferazės yra ir citoplazmoje, ir mitochondrijose; membranose yra šarminės fosfatazės, 5-nukleotidazės, γ glutamiltransferazės (pastarosios daugiausia mikrosomose). Organui specifinių fermentų normalus aktyvumas kraujo plazmoje tai pusiausvyra tarp jų patekimo į kraują ir šalinimo iš jo. Taigi ir fermentemijos lygis priklauso ne tik nuo ligos sunkumo ar fermento kiekio ląstelėje, bet ir nuo jo šalinimo iš kraujo greičio. Kartais lėtai šalinami fermentai kaupiasi kraujyje, todėl nustatomas didelis jų aktyvumas, nors ląstelėse jų kiekis ir nedidelis. Kai kurie fermentai (izofermentai) yra labai specifiški konkrečiam organui ar audiniui ir jų aktyvumo padidėjimas tiksliai rodo pažeidimo vietą ir pobūdį. Kiti ne tokie specifiški, nes juos gamina daug organų ir audinių. Tada diagnostinę svarbą turės kelių fermentų nustatymas. Tam padės ir dviejų ar daugiau fermentų aktyvumo santykio apskaičiavimas (pavyzdžiui, de Ritiso, Šmito ir kiti koeficientai), taip pat sukurtos diagnostinės schemos, algoritmai. Fermentų aktyvumo padidėjimas nepadeda nustatyti proceso etiologijos, jis yra kaip simptomas. Ligų, kurioms būdinga panaši fermentų aktyvumo kaita, priežastys yra įvairios: infekcija, alergija, intoksikacija, traumos ir kt. Organui specifinių fermentų aktyvumo padidėjimas yra svarbus klinikinei praktikai tik kartu su kita simptomatika. Tuo topodiagnostika (arba organodiagnostika) skiriasi nuo įgimtų fermentopatijų diagnostikos sergant jomis sutrinka medžiagų apykaitos procesai, ir aptiktas fermento defektas rodo ligos priežastį. Be minėtos klasifikacijos, kuri skiria funkcinius kraujo plazmai ir organui specifinius fermentus, yra ir kita, pagal kurią kraujo plazmos fermentai skirstomi į tris 141
143 grupes. Tai sekreciniai, indikaciniai ir ekskreciniai fermentai. Sekreciniai fermentai sintetinami kepenyse, išskiriami į kraujo plazmą ir ten atlieka savo funkcijas. Tipiški šiai grupei yra krešėjimo fermentai, serumo cholinesterazė. Indikaciniai (ląsteliniai) fermentai atlieka savo funkcijas ląstelėje. Vienų daugiau yra ląstelės citoplazmoje (laktatdehidrogenazė, alaninaminotransferazė), antrų mitochondrijose (glutamatdehidrogenazė), trečių lizosomose (rūgščioji fosfatazė, gliukuronidazė). Normaliai kraujo plazmoje aptinkami tik jų pėdsakai. Pažeidus audinius, daugumos šių fermentų aktyvumas kraujo plazmoje padidėja. Ekskreciniai fermentai sintetinasi kepenyse (kituose organuose) ir fiziologinėmis sąlygomis išsiskiria su tulžimi (šarminė fosfatazė, leucinaminopeptidazė). Kai šių fermentų išsiskyrimas su tulžimi sutrinka, padidėja jų aktyvumas kraujo plazmoje. Klinikinės enzimologijos tikslas nustatyti kuo daugiau organui specifinių (indikacinių) fermentų organizmo skysčiuose. Kol kas tokių fermentų, būdingų tik tam tikram audiniui ar organui, žinoma nedaug. Fermento aktyvumą kraujo plazmoje veikia įvairūs veiksniai, ir tai reikia žinoti vertinant fermentų aktyvumo rezultatus (7 pav.). Audinių pažeidimas Fermentų aktyvumas (kiekis) audiniuose Audinių proliferacija Šalinimas su šlapimu ar tulžimi Fermentų aktyvumas (kiekis) kraujo serume Irimas kraujo serume 7 pav. Fermentų aktyvumo veiksniai Miokardo infarktas ar infekcija, pavyzdžiui, sergant hepatitu, pažeidžia ląsteles, jų membranos pralaidumą, dėl to ląsteliniai fermentai patenka į kraujotaką. Dėl proliferacinių procesų (pavyzdžiui, prostatos karcinomos) padidėja fermentų sintezė ir jų patekimas į kraują. Kepenų ligos, sukeliančios biliarinę obstrukciją, suaktyvina kai kuriuos fermentus kraujo serume, nes blokuojamas jų šalinimas į tulžį. Taigi šiais atvejais fermentų aktyvumas (kiekis) kraujyje padidės. Iš kraujo jie šalinami su šlapimu, tulžimi ar skaidomi fermentų. Taigi po kurio laiko fermentų aktyvumas sumažės, jeigu jų kiekis nepasipildys iš pažeisto audinio. Toliau pateikiami kai kurie kliniškai (diagnostiškai) svarbių fermentų pavyzdžiai. Apie fermentus rašoma ir kituose knygos skyriuose. α amilazė tai angliavandenių apykaitos fermentas. Didžiausias jo aktyvumas yra kasoje ir paausinėse (seilių) liaukose, daug mažesnis kiaušidėse, plonojoje ir storojoje žarnose, griaučių raumenyse. Sveikų asmenų kraujyje ir šlapime randami du maždaug vienodos katalitinės koncentracijos α amilazės izofermentai: kasos (P) ir 142
144 Fermentų klinikinė biochemija ir interpretavimas seilių liaukų (S). Fermento aktyvumas nepriklauso nuo lyties, maisto sudėties, paros laiko. α amilazės molekulinė masė nedidelė apie Da, todėl ji, ne taip kaip daugelis fermentų, lengvai filtruojama inkstų glomeruluose ir randama šlapime. Jos gyvavimo kraujyje puslaikis yra 9,3 17,7 valandos. Sveikų asmenų kraujo plazmoje gali būti makroamilazės, kuri nefiltruojama per inkstus dėl didelės molekulinės masės ( Da). Tai α amilazė, prisijungusi prie imunoglobulinų (dažniausiai IgA, mažiau IgG) Fab srities. Kai kuriuose tokiuose kompleksuose dar aptinkama albuminų, α 1 antitripsino. Esant patologijai, makroamilazės gali taip pat padaugėti. Po kai kurių tirpalų, kuriuose yra dekstrano, krakmolo, infuzijos galima pseudomakroamilazemija, kai susidaro α amilazės kompleksai su minėtomis medžiagomis. α amilazei nustatyti yra tiriamas kraujo serumas, šlapimas, dvylikapirštės žarnos turinys. Tai vienas pirmųjų diagnostikai panaudotų fermentų. Diagnostinė reikšmė. α amilazės rekomenduojamas (normalus) kiekis yra U/l, o kasos amilazės U/l. Didelį (5 ir daugiau kartų viršijantį normą) kasos α amilazės aktyvumo padidėjimą sukelia ūminis pankreatitas, kasos cista ar pseudocista, morfijaus vartojimas. Aktyvumas padidėja 3 5 kartus esant liaukų uždegimui, kasos galvos vėžiui, žarnų infarktui ar nepraeinamumui, prakiurusiai skrandžio opai, peritonitui, diabetinei ketoacidozei, tulžies takų ligoms, negimdiniam nėštumui, kai kuriems plaučių ir kiaušidžių navikams, gaminantiems amilazę, taip pat sergant tymais. Sergant ūminiu pankreatitu, α amilazės aktyvumas kraujo serume pradeda didėti 4 6-ą valandą nuo simptomų pradžios. Pikas pasiekiamas ą valandą ir aktyvumas sunormalėja po 2 8 dienų. Hiperamilazurija paprastai nustatoma praėjus 5 6 valandoms po jos padaugėjimo kraujo serume ir laikosi kelias dienas net kai jos kiekis sunormalėja. α amilazės aktyvumas gali sumažėti nudegus, sergant hipotiroze, cukriniu diabetu, esant kacheksijai. Ligų diagnostikai tai nėra labai svarbu. Dėl klinikinio poveikio α amilazės aktyvumą didina preparatai, sukeliantys Odi sfinkterio susitraukimą, pavyzdžiui, narkotiniai analgetikai, sekretinas. Dėl cheminio poveikio šio fermento aktyvumą gali padidinti tiriamosios medžiagos užteršimas seilėmis, kai kurie vaistai (galintys sukelti ir pankreatitą), pavyzdžiui, geriamieji kontraceptikai, sulfanilamidai, tetraciklinas, salicilatai, gliukokortikoidai, tiazido grupės diuretikai. Oksalatai, citratai mažina α amilazės aktyvumą. Lipazė. Žmogaus kasos (pankreatinė) lipazė tai glikoproteinas (molekulinė masė Da), sintetinamas kasos egzokrininės dalies ląstelių. 99% gaminamos lipazės iš ląstelių skiriasi į kasos latakus, o apie 1% patenka į limfą ir paskui į kraujotaką. Lipazė hidrolizuoja vandenyje netirpių ilgagra¹dinių riebalų rūgščių ir glicerolio esterius, įeinančius į micelinius kompleksus su tulžies rūgštimis, kai ph 8,8 9,2. Gyvavimo kraujyje puslaikis yra 6,9 13,7 val. Šis fermentas lengvai filtruojamas per 143
145 inkstų glomerulų membraną, paskui, skirtingai nuo α amilazės, visas reabsorbuojamas ir suskaldomas. Todėl lipazė šlapime aptinkama imunofermentiniais metodais tik esant ryškiai proteinurijai. Diagnostinė reikšmė. Rekomenduojamas (normalus) lipazės kiekis yra U/l. Seragnt ūminiu pankreatitu, padidėja mambranų pralaidumas ir daugiau lipazės patenka į kraujotaką. Jos kiekis dar išauga įvykus ląstelių nekrozei, pavyzdžiui, sergant hemoraginiu pankreatitu. Sergant lėtiniu pankreatitu (ypač jam paūmėjus) ir išsivysčius fibrozei, esant kasos takų obstrukcijai (dėl akmenligės, naviko, Odi sfinkterio spazmo), padidėja spaudimas ištekamuosiuose kasos latakėliuose, fermentas prasisunkia į perikapiliarines ertmes ir patenka į kraują. Fermento kiekis taip pat padidėja sergant kitomis pilvo organų ligomis, kai kartu pažeidžiama kasa. Šarminė fosfatazė. Šis fermentas nepasižymi substratiniu specifiškumu ir hidrolizuoja įvairius eterius su fosforo rūgštimi: glicerolfosfatą, nukleotidus ir kt. Šio fermento veikimo optimalus ph yra 10,0. Šarminę fosfatazę gamina kepenys, kaulai, žarnynas, gimda (arba placenta), inkstai ir plaučiai. Šio fermento izofermentai: kepenų (45 55%), kaulų (43 53%), žarnų (0 10%) ir placentos. Sveiko asmens kraujyje beveik visą šarminės fosfatazės aktyvumą sudaro kepenų ir kaulų izofermentai. Dar yra žinomi šie izofermentai: didelės molekulinės masės šarminės fosfatazės izofermentas, šarminės fosfatazės ir lipoproteino X kompleksas, randamas esant cholestazei. Šarminės fosfatazės izofermentų katalizinės savybės, elektroforezinis judrumas, termostabilumas yra skirtingi. Atspariausia temperatūrai yra placentos šarminė fosfatazė, o kaulų izofermentas jai yra labai jautrus. Ne tokia jautri temperatūros padidėjimui yra žarnų ir kepenų šarminė fosfatazė. Tiriant elektroforeze, α 2 globulinų zonoje normaliai išsiskiria 1 2 frakcijos. Tiriamoji medžiaga yra kraujo serumas. Jį būtina atšaldyti. Diagnostinė reikšmė. Rekomenduojamas (normalus) kiekis yra U/l. Šarminės fosfatazės kraujo serume padaugėja aktyvaus kaulų augimo tarpsniu, t. y. tarp 4 ir 17 gyvenimo metų, dėl kaulų izofermento kiekio padidėjimo; po 66 metų šarminė fosfatazė serume gali labai suaktyvėti dėl kepenų izofermento. Esant patologijai, jo aktyvumas padidėja tada, kai pažeidžiami ir šį fermentą gaminantys audiniai arba suintensyvėja kaulinio audinio apykaita, pavyzdžiui, gyjant lūžiams. Dažniausios ligos, kuriomis sergant didėja šarminės fosfatazės aktyvumas, yra šios: kaulų ligos: vėžio metastazės kauluose; osteogeninė sarkoma; mielominė liga; limfogranulomatozė; pažeidžianti kaulus Pedžeto (Paget) liga; Gošė (Gaucher) liga, vysktant kaulų reabsorbcijai; osteomaliacija; kepenų ligos: tulžies takų obstrukcija (intrahepatinė ar ekstrahepatinė); biliarinė cirozė; infekcinė mononukleozė; vaikų citomegalovirusinė infekcija; cholangitas ir cholangiolitas; kepenų pūlinys (abscesas); 144
146 Fermentų klinikinė biochemija ir interpretavimas inkstų ligos: inkstinis rachitas dėl atsparumo D vitaminui, rachito ir antrinės hiperparatirozė; kitos ligos: pirminė ir antrinė hiperparatirozė (kai procesas apėmęs kaulus); sepsis, opinis kolitas; žarnyno bakterinės infekcijos; tirotoksikozė. Šio fermento aktyvumas taip pat gali padidėti moterims po menopauzės, nėštumo metu (dėl placentos izofermento kiekio padidėjimo), augantiems vaikams. Šarminės fosfatazės aktyvumas sumažėja dėl hipotirozės, didelės C vitamino stokos, ryškios anemijos, achondroplazijos, kretinizmo, kaupiantis kauluose radioaktyviosioms medžiagoms, kai trūksta fosforo. Šarminės fosfatazės aktyvumo tyrimo rezultatams gali turėti įtakos šie veiksniai: jį didina klinikiniams tikslams vartojamas albuminas, pagamintas iš placentinės plazmos, hepatotoksiniai vaistai; mažina dėl cheminio poveikio (slopina fermentą) etilendiamintetraacto rūgštis (EDTA), vartojama kaip antikoaguliantas. γ glutamiltransferazė (glutamiltranspeptidazė, GGT). Tai mikrosomų fermentas, katalizuojantis glutamo rūgšties γ glutamilo grupės pernašą pro membraną nuo tripeptido glutationo su aminorūgštimi. Fermentas yra išsidėstęs ant ląstelių citoplazminės membranos taip, kad jo aktyvusis centras nukreiptas į išorę. Fermentas yra aktyvus beveik visuose organuose, kurie pasižymi sekreciniu ar absorbciniu aktyvumu: kepenyse, kasoje, žarnose, širdyje, smegenyse, prostatoje, o didžiausias inkstuose. Iš plazmos GGT yra šalinama į tulžį (tulžyje aktyvumas yra apie 10 kartų didesnis negu kraujyje). Nedaug jo suyra inkstuose ir pašalinama su šlapimu. Fermentas psižymi heterogeniškumu: sudaro kompleksus su lipoproteinais (ypač DTL, taip pat MTL). Kraujyje randama ir tirpioji forma tai GGT, atsipalaidavusi iš kepenų ląstelių membranų. Jos gyvavimo kraujyje puslaikis yra 9 val., o susijungusios su DTL apie 20 val. Šis fermentas yra jautresnis kepenų ligų, ypač esant tulžies stazei, rodiklis ir jo kiekis pradeda didėti anksčiau negu šarminės fosfatazės, ypač vaikams. Jis teigiamas 90% ligonių, sergančių kepenų ligomis, ir yra vertingas hepatotoksiškumo rodiklis. Naujagimių GGT dydžiai yra apie 5 kartus didesni negu vaikų, o neišnešiotųjų naujagimių apie 10 kartų. Diagnostinė reikšmė. Rekomenduojama reikšmė kraujo serume yra 2 30 U/l. Nors šis fermentas yra labai aktyvus inkstuose, klinikinėje praktikoje jis dažniausiai naudojamas kepenų ir tulžies takų ligų diferencinei diagnostikai, ypač alkoholinės kilmės hepatitui nustatyti. Fermentas labai suaktyvėja esant intrahepatinių ir ekstrahepatinių tulžies takų obstrukcijai. Kadangi šio fermento yra ląstelės membranoje, tai ją pažeidus ar padidėjus spaudimui tulžies takuose (cholestazė) GGT aktyvumas kraujo serume greitai padidėja. Aktyvumas padidėja ir sergant infekcine mononukleoze, pankreatitu, miokardo infarktu, insktų funkcijos nepakankamumu, cukriniu diabetu, lėtine obstrukcine plaučių liga. Šiuo rodikliu nustatomas alkoholizmo gydymo veiksmingumas. 145
147 Barbitūratai, narkotikai, etanolis, streptokinazė gali padidinti šio fermento aktyvumą (sužadina fermento sintezę). Rūgščioji fosfatazė. Kaip ir gliukuronidazė, lizocimas ir kt., šis fermentas priklauso lizosomų hidrolazėms. Jo veikimo optimalus ph yra 4,9. Dėl nekrozės, kai padidėja citoplazmos rūgštingumas, lizosomos ýra ir iš jų išsilieję fermentai suardo ląstelę. Taigi patekę į kraują lizosomų fermentai rodo smarkų ląstelių pažeidimą. Didžiausias rūgščiosios fosfatazės aktyvumas (skaičiuojant 1 g audinio) yra prostatoje. Čia jis 100 kartų didesnis, palyginti su jo aktyvumu kituose audiniuose. Mažesnis aktyvumas yra kepenyse, blužnyje, eritrocituose, trombocituose, kaulų čiulpuose. Taip pat šio fermento rasta motinos piene. Vyrų kraujo plazmoje esančios rūgščiosios fosfatazės pusę kiekio yra iš prostatos, moterų kraujo plazmos rūgščioji fosfatazė iš kepenų, eritrocitų ir trombocitų. Tai nėra homogeninis fermentas. Fermento iš prostatos ir trombocitų aktyvumas yra slopinamas tartrato (vyno rūgšties druskos) tuo remiasi ir nustatymo metodas. Bendrojo rūgščiosios fosfatazės aktyvumo dalis, kuri yra slopinama tartrato, priskiriama prostatos rūgščiajai fosfatazei. Kraujo serumas be hemolizės pėdsakų tiriamas tuoj paėmus kraują; jei tiriama ne iš karto, norint išvengti aktyvumo sumažėjimo, įpilama citratinio buferinio tirpalo ar acto rūgšties arba laikoma 4 20 o C temperatūroje. Diagnostinė reikšmė. Rekomenduojama reikšmė kraujo serume yra 10 U/l. Rūgščiosios fosfatazės aktyvumas labai padidėja (jei metodas nėra specifiškas prostatos izofermentui) yrant trombocitams, sergant hemolizine liga, esant metastazių kauluose, kai kuriais mielominės ligos atvejais. Šio fermento aktyvumas taip pat padidėja sergant prostatos vėžiu, ypač metastazuojančiu, Gošė (Gaucher), Nimano Piko (Niemann Pick) ligomis, esant prostatos infarktui, po šlapimo pūslės kateterizacijos, praėjus 1 2 dienoms po prostatos operacijos ar jos biopsijos. Kaip jau minėta, rūgščiosios fosfatazės aktyvumo tyrimo rezultatus padidina hemolizė, o šį fermentą slopina oksalatai, fluoridai, heparinas. Tartratas ir etanolis nuslopina tik prostatos rūgščiosios fosfatazės aktyvumą. Serumo aminotransferazės. Klinikoje vartojamos dvi aminotransferazės: asparta - taminotransferazė (AST), arba serumo glutamatoksaloacetattransaminazė (SGOT), ir alaninaminotransferazė (ALT), arba serumo glutamatpiruvattransaminazė (SGPT). Šie fermentai katalizuoja amino grupės pernešimą nuo aminorūgščių L asparto ar L alanino į atitinkamą ketorūgštį. Šiuos fermentus gamina daugelis organizmo ląstelių, todėl jie nepasižymi dideliu specifiškumu organams. AST aktyvumas didžiausias (aktyvumo mažėjimo kryptimi) širdies ir griaučių raumenyse, kepenyse, eritrocituose; mažas odoje, inkstuose, kasoje. ALT daugiausia randama (aktyvumo mažėjimo kryptimi) kepenyse, inkstuose, širdies ir griaučių raumenyse, kasoje, blužnyje. Eritrocituose šio fermento aktyvumas 6 kartus didesnis negu serume. AST tirpios (citoplazminės) formos molekulinė masė yra Da, o mitochondrinės 146
148 Fermentų klinikinė biochemija ir interpretavimas formos Da. ALT yra viena forma (molekulinė masė Da). AST gyvavimo kraujyje puslaikis yra 17 val., o ALT 47 valandos. Žinotina, kad ALT yra ląstelės citoplazmoje; todėl, kai tik pažeidžiama ląstelė (pavyzdžiui, hepatocitas), šis fermentas greitai patenka į tarpląstelinę erdvę ir jo aktyvumas kraujo plazmoje padidėja. 30% AST aktyvumo tenka citoplazmai ir 70% mitochondrijoms. Taigi ląstelė, kad AST patektų į tarpląstelinę erdvę, turi būti labiau pažeista. Todėl, pavyzdžiui, esant hepatitui, ji suaktyvėja vėliau negu ALT. Dažniausiai šie fermentai naudojami širdies ir kepenų ligų diagnostikai. Padidėjęs AST aktyvumas sergančiojo miokardo infarktu kraujo plazmoje pirmą kartą buvo nustatytas 1954 m. ir atvėrė naują fermentodiagnostikos erą. Tačiau atradus labiau specifiškų širdies raumens pažeidimo žymenų, šis žymuo nebetaikomas. Šių fermentų aktyvumui nustatyti tiriamas kraujo serumas. Kai kurių ligų diferencinei diagnostikai svarbu nustatyti šių fermentų aktyvumo santykį tai de Ritis o koeficientas (AST/ALT). Normalus jis lygus 1,33 + 0,42. Santykis <1 būdingas vidutinio pažeidimo laipsnio kepenų ligoms, o santykis >1 ir ypač >2 nurodo į sunkų, dažnai su hepatocitų nekroze kepenų pažeidimą. Diagnostinė aspartataminotransferazės nustatymo reikšmė. Rekomenduotina reikšmė kraujo serume: vyrų 40 U/l, moterų 35 U/l. Aktyvumas labai padidėja sergant greitosiomis hepatito formomis, ypač virusiniu hepatitu, miokardo infarktu, esant cirkuliaciniam kolapsui (šokui), ūminiam pankreatitui, infekcinei mononukleozei (5 ir daugiau kartų); 3 5 kartus šio fermento aktyvumas padidėja esant bet kurios kilmės hepatocitų pažeidimui ar nekrozei, pavyzdžiui, cholestazinei ir obturacinei geltai, lėtiniam hepatitui; vaistų sukeltam kepenų pažeidimui, alkoholiniam hepatitui; aritmijoms, įgimtajai širdies ydai; raumenų distrofijai, nekrozei ar traumai. Nedidelis šio fermento aktyvumas būdingas perikarditui, kepenų cirozei, plaučių infarktui, smegenų kraujotakos sutrikimams. AST lygis po injekcijų į raumenis, nedidelio fizinio krūvio dažniausiai išlieka normalus. Diagnostinė alaninaminotransferazės nustatymo reikšmė. Rekomenduotina reikšmė kraujo serume: vyrų 40 U/l, moterų 35 U/l. Šio fermento aktyvumas labai padidėja (20 ir daugiau kartų) esant bet kurios kilmės hepatocitų pažaidai, jų nekrozei (ūminiam hepatitui ar lėtiniam paūmėjimui, toksiniam hepatitui). Kelis kartus šio fermento aktyvumas padidėja dėl griaučų raumenų traumos (pavyzdžiui, po operacijos), miozito, miokardito, kepenų cirozės, alkoholinio kepenų suriebėjimo, mechaninės geltos, kepenų auglių, infekcinės mononukleozės, miokardo infarkto, hemolizinės anemijos, pankreatito. Pabrėžtina, kad ALT aktyvumas didėja jau prodrominiu ikigeltiniu ligos tarpsniu ar esant begeltei hepatito formai. Fermento aktyvumas pasiekia maksimumą 6 10-ą dieną, sunormalėja ą dieną. Jei išlieka padidėjęs dienų, tai greičiausiai ūminis hepatitas tampa lėtiniu. 147
149 Padidėjęs AST aktyvumas būna ir po miokardo infarkto, ir sergant kepenų ligomis, o ALT sergant kepenų ligomis. Taigi, tiriant šiuos du fermentus, galima diferencijuoti dvi patologijas. Tam padeda ir de Ritiso koeficientas: sergant širdies ligomis, jis didėja, o dėl kepenų ligų mažėja. ALT aktyvumą didina hepatotoksiniai ir cholestazę sukeliantys preparatai (pavyzdžiui, acetilsalicilo rūgštis, nikotino rūgštis, barbitūratai, penicilinas, sulfanilamidai, opijaus preparatai ir kt.); šiek tiek gali padidinti injekcijos į raumenis. Kreatinkinazė (KK, kreatinfosfokinazė KFK) yra randama tarp mitochondrijų kristų, ji įeina ir į miofibrilės sudėtį. Šis fermentas skatina fosforilinės grupės pernašą iš adenozintrifosfato į kreatiną ir atvirkščiai. Reakcijos metu susidaręs kreatinfosfatas yra pagrindinis energijos šaltinis raumeniui susitraukti. Kreatinkinazė yra dimerinis baltymas, susidedantis iš dviejų rūšių polipeptidinių grandinių: B (smegenų) ir M (raumenų), kurias koduoja du skirtingi struktūriniai genai. Skiriami trys izofermentai, kuriuos galima nustatyti elektroforezės, chromatografijos ir kitais metodais: KK-I sudaro dvi BB grandinės, KK-II sudaro M ir B grandinės, KK-III sudaro dvi MM grandinės. Didžiausias izofermento BB aktyvumas yra smegenyse ir lygiuosiuose raumenyse; kituose audiniuose jo aktyvumas labai mažas. Pagrindinis KK-MB izofermento šaltinis yra širdies raumuo (aktyvumas sudaro apie 25 46% bendrojo kreatinkinazės aktyvumo ir todėl yra vadinamas širdies izofermentu) ir griaučių raumenys (mažiau negu 5%). MM izofermento daugiausia yra griaučių raumenyse, taip pat širdies raumenyje (ką tik paimto audinio šis santykis yra 4:1). Aprašyti ir netipiški kreatinfosfokinazės izofermentai, kurie tiriant elektroforeze išryškėja tarp MB ir MM frakcijų. Manoma, kad tai jų kompleksai su imunoglobulinais. Mitochondrinė KK (Mi izofermentas, arba KK-IV), kuri gali būti dimero, rečiau didesnio oligomero formos (makrokreatinkinazė), yra blogas prognozės požymis. Tiriamas kraujo serumas. Tai atlikti reikia greitai (arba laikyti serumą nuo 4 o C iki 20 o C temperatūroje). Keturių dienų naujagimių šio fermento aktyvumas yra apie 3 kartus didesnis už suaugusiųjų, o 6 savaičių 12 metų vaikų kaip suaugusiųjų. Normaliai kraujo serume bendrojo BB izofermento (KK-I) aktyvumo yra tik pėdsakai ar visai jų nėra; MB izofermentas (KK-II) sudaro mažiau negu 4 6% bendrojo aktyvumo; MM izofermentas (KK-III) tai pagrindinis kraujo serumo kreatinfosfokinazės komponentas, sudarantis % aktyvumo. Diagnostinė bendrojo kreatinfosfokinazės aktyvumo nustatymo reikšmė. Rekomenduojama reikšmė kraujo serume: vyrų U/l, moterų U/l. Aktyvumo sumažėjimas diagnostinės reikšmės neturi. Jis rodo mažą raumenų masę arba nejudrią gyvenseną. Padidėjimas būdingas griaučių raumenų arba širdies ligoms, rečiau lygiųjų raumenų patologijai. Padidėjimą sukelia: traumos; operacijos; miokardo infarktas; raumenų aprūpinimo deguonimi sumažėjimas; įvairios kilmės miopatiniai pažeidimai, pavyzdžiui, poli- 148
150 Fermentų klinikinė biochemija ir interpretavimas miozitas, dermatomiozitas, miokarditas; alkoholizmas; raumenų distrofija, ypač Diušeno; apsinuodijimai, kurie gali komplikuotis koma; piktybinė hiperpireksija ir ilgalaikė hipotermija; kai kurios infekcinės ligos, pavyzdžiui, vidurių šiltinė; rečiau aritmijos, širdies nepakankamumas, tachikardija, plaučių arterijos embolija, stabligė, generalizuotieji traukuliai. Esant miokardo infarktui, KK aktyvumas didėja greičiausiai, palyginti su kitais fermentais. Maksimumą pasiekia ą valandą ir po 3 6 dienų sunormalėja. Diagnostinė kreatinkinazės izofermentų nustatymo reikšmė. BB izofermento daugėja sergant kai kuriomis vėžio formomis (plaučių, žarnyno, šlapimo pūslės, prostatos), esant širdies raumens sužalojimai, šokui, atliekant atviras širdies operacijas, sergant jungiamojo audinio ligomis. MB izofermento padaugėjimą sukelia miopatijos ir širdies raumens uždegimas, stenokardija (retai), miokardo infarktas (dažnai; aktyvumas greitai pasiekia maksimumą ir greitai sunormalėja), hipotermija ir hipertermija, raumenų distrofija, kai kurios infekcijos, ypač pažeidžiančios širdį ir griaučių raumenis, šokas, apsinuodijimai, užsitęsusios aritmijos. MM izofermento koncentracija padidėja visais atvejais, kaip ir bendrasis kreatinfosfokinazės aktyvumas. Padidėjęs kreatinfoskinazės aktyvumas nustatomas tiriant hemolizuotą mėginį, o sumažėjęs kai mėginį veikia tiesioginiai saulės spinduliai ar fluorescencija. Tyrimo rezultatams neturi įtakos bilirubinas, lipemija, heparinas. Dėl klinikinio poveikio kreatinfosfokinazės akyvumas padidėja vartojant klofibratą, etanolį (alkoholikams), apsinuodijus barbitūratais, po injekcijų į raumenis. Fizinis krūvis gali pakeisti frakcijų santykį: labai padaugėja MB ir MM frakcijų (esant normai, MB frakcija tesudaro ~5% bendrojo aktyvumo). Laktatdehidrogenazė (LDH) randama ląstelės citozolyje bei mitochondrijose. Tai oksidoreduktazių klasės fermentas, katalizuojantis grįžtamąją pieno rūgšties oksidaciją į piruvo rūgštį, tuo pat metu redukuojantis NAD + į NADH. Tai tetramerinis baltymas iš dviejų polipeptidinių grandinių tipų: M (daugiausia sintetinamas kepenyse, raumenyse) ir H (širdies raumenyje). Šios grandinės gali sudaryti penkis LDH izofermentus: greičiausiai anodo link juda LDH-I (sudaro keturios H grandinės), po to LDH-II (3 H + 1 M), LDH-III (2 H + 2 M), LDH-IV (1 H + 3 M), ir starto linijoje lieka LDH-V izofermentas (sudaro keturios M grandinės). H grandinė labiau sintetinama tuose organuose, kuriuose daugiau energijos gaminama kvėpavimo, o ne glikolizės būdu (galvos smegenyse, širdyje), todėl šio tipo fermentas vadinamas širdies LDH. M grandinė būdingesnė organams, kuriuose vyrauja glikolizė (griaučių raumenims, kepenims, inkstams, taip pat augliams). Tai raumenų LDH tipas. Didžiausias LDH-I ir LDH-II aktyvumas nustatomas miokarde ir eritrocituose, LDH-III smegenyse ir inkstuose, LDH-V kepenyse, griaučių raumenyse. 149
151 Tiriamas kraujo serumas ar plazma (heparinizuota), laikoma kambario temperatūroje (nešaldoma). Atskirta nuo krešulio greitai tiriama; nedidelė hemolizė labai padidina LDH aktyvumą. Norint įsivaizduoti, kaip fermento aktyvumas kinta pagal amžių, pateikiamos jo normos ribos, nustatytos Tarptautinės klininkinės chemijos ir laboratorinės medicinos federacijos patvirtintu metodu (10 lentelė). 10 lentelė. Laktatdehidrogenazės aktyvumo (U/l) priklausomybė nuo amžiaus Tiriamoji grupė Mergaičių ir moterų Berniukų ir vyrų Naujagimiai Vaikai iki 1 metų Vaikai 1 3 metų Vaikai metų Vaikai metų Suaugusieji Izofermentai tiriami elektroforeze agare ar acetatceliuliozėje. LDH-V izofermentas yra nestabilus laikomo kambario temperatūroje po 48 val. aktyvumas sumažėja 13%, 4 o C temperatūroje 18% (11 lentelė). 11 lentelė. Normali procentinė LDH izofermentų sudėtis LDH izofermentai LDH-I LDH-II LDH-III LDH-IV LDH-V % bendrojo aktyvumo (elektroforezė agarozėje) 16,1 31,5 20,2 41,6 17,0 26,2 5,9 12,3 3,2 17,3 Diagnostinė bendrojo LDH aktyvumo nustatymo reikšmė. Rekomenduojama reikšmė kraujo serume U/l. Fermento aktyvumas labai padidėja (5 ir daugiau kartų) esant megaloblastinei anemijai, piktybinei anemijai, išplitusiai karcinomatozei, virusiniam hepatitui, šokui, hipoksijai, hipertermijai. LDH aktyvumas padidėja 3 5 kartus sergant kepenų ciroze, obstrukcinė gelta, įvairiomis inkstų ligomis, griaučių raumenų ligomis, miokardo, plaučių infarktu, hemolizine anemija, leukoze, vystantis navikui. Miokardo infarkto metu LDH aktyvumas didėja lėčiau negu KK ar AST, maksimumą pasiekia po valandų (2 3 dienų), sunormalėja po 6 7 dienų. Gali likti padidėjęs iki 14 dienų. Aktyvumas šiek tiek padidėja pažeidus ląsteles (kai citoplazmos turinys išsilieja į tarpląstelinę erdvę), esant širdies funkcijos nepakankamumui, hepatitui (nevirusiniam), limfomai, hipotirozei. Diagnostinė LDH izofermentų nustatymo reikšmė. Vertinant LDH izofermentų tyrimo rezultatus, būtina žinoti ligos anamnezę. 150
152 Fermentų klinikinė biochemija ir interpretavimas LDH-I ir (arba) LDH-II padaugėja staiga ištikus miokardo infarktui, sergant piktybine anemija, megaloblastine anemija ar pjautuvine anemija, esant ūminei nekrozei, hemolizei in vivo ir in vitro. LDH-IV padaugėjimą sukelia navikai iš embrioninių ląstelių (teratoma, seminoma, kiaušidžių disgerminoma). LDH-V padaugėja pažeidus griaučių raumenis, sergant uždegiminėmis ar degeneracinėmis griaučių raumenų ligomis, kepenų ligomis (ciroze, hepatitu ir kt.), vėžiu. Normalus LDH-I/ LDH-II santykis yra 0,45 0,74, o po miokardo infarkto jis didesnis kaip 0,8. Dažnai matyti normalus izofermentų išsidėstymo vaizdas esant padidėjusiam bendrosios LDH aktyvumui kraujo serume. Tai būdinga daugeliui ligonių, sergančių širdies, kepenų, judamojo aparato, navikinėmis ligomis. Viduriniosios zonos (LDH-II, LDH-III, LDH-IV) izofermentų smarkiai padaugėja yrant trombocitams (plaučių arterijos embolija, didelio tūrio apimties hemotransfuzijos ir kt.), esant limfinės sistemos patologijai. Dėl klinikinio poveikio LDH aktyvumą didina šie vaistai: nuskausminamieji, klofibratas, dikumarinas, etanolis, metotreksatas, narkotiniai analgetikai, chinidinas, sulfanilamidai. Oksalatai ir šlapalas mažina šio fermento aktyvumą. Hemolizė keičia ne tik bendrosios LDH aktyvumą, bet ir izofermentų santykį. Be to, LDH-I/LDH-II santykis priklauso ir nuo frakcionavimo metodo: acetatceliuliozėje šis santykis yra >1, o išskiriant agarozėje <1. α hidroksibutiratdehidrogenazė (α HBDH) tai LDH-I + LDH-II, t. y. dviejų izofermentų, suma. Jų yra gausu, kaip jau minėta, širdies raumenyje, inkstuose, eritrocituose. Ištikus miokardo infarktui, padidėjęs šių fermentų kiekis laikosi ilgiau negu bendrasis LDH kiekis, t. y. 2 3 savaites po infarkto. Širdies raumens pažeidimo, kepenų, inkstų ligų fermentinė laboratorinė diagnostika aptarta ir kituose knygos skyriuose. Api b e n d r i n i m a s Padidėjęs fermentų aktyvumas kraujo serume rodo ląstelių pažeidimą ar proliferaciją. Kraujo plazmoje esančių organui specifinių fermentų normalus aktyvumas atspindi pusiausvyrą tarp jų patekimo į kraują ir šalinimo iš jo. Klinikinės enzimologijos tikslas nustatyti kuo daugiau specifinių organams (indikacinių) fermentų organizmo skysčiuose. α amilazė yra vienas pirmųjų diagnostikai panaudotų fermentų. 151
153 Laboratoriniai tyrimai Alaninaminotransferazė (ALT; serumo glutamatpiruvattransaminazė; SGPT) Tiriamoji medžiaga. Serumas. Rekomenduojama reikšmė. Vyrų 40 U/l, moterų 35 U/l. Diagnostinė vertė. Kepenų ląstelių nekrozė, šokas, dešinės širdies funkcijos nepakankamumas, ūminė anoksija (pvz., status asthmaticus), didelė trauma, kairės širdies pusės funkcijos nepakankamumas. Kepenų cirozė, mechaninė gelta, kepenų navikai, platus miokardo infarktas, miozitas, miokarditas, raumenų distrofija, hemolizinė liga, preeklampsija, raumenų trauma, suriebėjusios kepenys, didelis nudegimas, sunkus pankreatitas, piktnaudžiavimas alkoholiu. Piridoksalfosfato stoka. Papildoma informacija. Daugiausia yra kepenyse, inkstuose, mažiau giaučių ir širdies raumenyse. Pėdsakai randami odoje, kasoje, blužnyje, plaučiuose. Lokalizija ląstelėje citoplazma. Eritrocituose aktyvumas 6 kartus didesnis negu plazmoje. Padidėjęs ALT aktyvumas po ūminio hepatito gali reikšti didelę riziką išsivystyti lėtiniam hepatitui. Suaktyvėjusi ALT dažniau nustatoma nutukusiems ar piktnaudžiaujantiems alkoholiu negu serganiems hepatitu pacientams. Jei ALT smarkiai padidėjusi vaikui, patyrusiam pilvo traumą, galima įtarti kepenų pažaidą. V: hepatotoksiniai vaistai ar vaistai, sukeliantys cholestazę. Daugelio vaistų sukeltas ALT padidėjimas yra praeinantis, bet kai kada gali reikšti jų toksinį poveikį kepenims. Tokiems vaistams priklauso aminoglikozidai, cefalosporinai, chininas, ciklosporinas, ciprofloksacinas, fenofibratas, gancikloviras, heparinas, interferonas, interleukinas-2, kaptoprilis, klaritromicinas, klofibratas, levamizolis, levadopa, linkomicinas, metoprololis, nifedipinas, omeprazolis, penicilinas, piroksikamas, ranitidinas, retinolis, streptozocinas, tioguaninas, verapamilis. α Amilazė Tiriamoji medžiaga. Serumas. Rekomenduojama reikšmė U/l. Diagnostinė vertė. α amilazės aktyvumas yra mažas naujagimių kraujyje pirmaisiais dviem mėnesiais; padidėja iki suaugusiųjų normos reikšmių pirmųjų metų pabaigoje. Parotitas, pankreatitas, žarnų obstrukcija ar infarktas, žarnų užsisukimas, ektopinis nėštumas, tulžies takų obstrukcija, diabetinė ketoacidozė, kasos cista ir pseudocista, peritonitas, kai kurie plaučių ir kiaušidžių navikai, inkstų nepakankamumas, ERCP, pilvo, galvos traumos, virusinė infekcija, po operacijos, alkoholio vartojimo. Kasos nepakankamumas, cistinė fibrozė, sunki kepenų liga, pankreatektomija. Papildoma informacija. Didžiausias α amilazės aktyvumas yra seilių liaukose ir kasoje. Daug mažesnis aktyvumas yra kiaušidėse, plonojoje ir storojoje žarnoje, griaučių raumenyse. Vyrų ir moterų amilazės aktyvumas nesiskiria ir nepriklauso nuo maisto ar paros meto. Skiriami du pagrindiniai α amilazės izofermentai: P ir S, egzistuoja ir daugiau (apie 17) izofermentų ir izoformų dėl skirtingų genetinių variantų ir potransliacinės modifikacijos. P tipo izoamilazė per inkstus šalinama greičiau negu S tipo. Makroamilazė, manoma, yra imuninis kompleksas su antikūnais. V: vaistai, sukeliantys Odi sfinkterio spazmą (pvz., narkotiniai analgetikai, sekretinas). Kai kurie vaistai (pvz., kaptoprilis) skatina amilazės gamybą, ir tai gali sukelti pankreatitą: tai alkoholis, asparaginazė, azatioprinas, cimetidinas, estrogenai, fenilbutazonas, furozemidas, ibuprofenas, indometacinas, kaptoprilis, klofibratas, gliukokortikoidai, metildopa, nitrofurantoinas, oraliniai kontraceptikai, sulfonamidai, tetraciklinas, tiazidiniai diuretikai, valproatai. Ch: užteršimas, pvz., seilėmis. V: anaboliniai steroidai. 152
154 Fermentų klinikinė biochemija ir interpretavimas Ch: lipemija, citratas, EDTA, fluoridas, oksalatai. Tiriamoji medžiaga. Šlapimas (atsitiktinė ar 24 val. porcija). α amilazė labai nestabili rūgštiniame šlapime. Jei šlapimą reikia laikyti, jo ph sureguliuojamas iki šarminės reakcijos. Rekomenduojama reikšmė: atsitiktinėje porcijoje 1000 U/l; 24 val. šlapime 900 U/24 val. Didėjimo šlapime priežastys, kaip ir serume. Sergant ūminiu pankreatitu šlapime amilazės padaugėja vėliau negu serume. Tačiau esant inkstų nepakankamumui ar makroamilazemijai, gali būti norma ar sumažėti. Šlapime amilazė gali išlikti padidėjusi iki 2 savaičių po ūminio pankreatito formuojantis pseudocistai Tiriamoji medžiaga. Ascitinis ar pleuros skystis. Normaliai α amilazės aktyvumas toks pat ar šiek tiek mažesnis negu serume. Ascitiniame skystyje: pankreatitas, žarnų nepraeinamumas ar infarktas, žarnų užsisukimas, tulžies takų ligos, kiaušidžių vėžys, trūkęs ektopinis nėštumas, diseminuotas antrinis piktybinis navikas, peritonitas, kasos cista ar pseudocista. Pleuros skystyje: pralaidumas iš pilvo ertmės ar amilazę gaminantis plaučių navikas; bronchų, kasos ar kiaušidžių navikas; stemplės plyšimas; plaučių tuberkuliozė, embolija ar infarktas; įgimtas širdies nepakankamumas. Aspartataminotransferazė (AST; serumo glutamatoksaloacetattransaminazė, SGOT) Tiriamoji medžiaga. Serumas. Rekomenduojama reikšmė. Vyrų 40 U/l, moterų 35 U/l. Diagnostinė vertė. Žaibinė hepatito, ypač virusinio, forma. Kepenų ląstelių nekrozė ar pažeidimas (parenchiminė, mechaninė gelta, lėtinis hepatitas, vaistų sukeltas kepenų pažeidimas); alkoholinis hepatitas (paprastai AST > ALT), virusinis ir lėtinis hepatitas (dažniausiai ALT > AST; jei AST > ALT prognozė bloga); metastazės kepenyse ir hepatoma; infekcinė mononukleozė, širdies ar griaučių raumenų nekrozė ir trauma, širdies ar griaučių raumenų uždegimas, būklė po ūminio miokardo infarkto (AST > ALT), sunkus fizinis darbas, širdies nepakankamumas, sunkus nudegimas, karščio smūgis (padidėja apie 20 kartų), hipotirozė (40 90% atvejų), žarnų nepraeinamumas (gali rodyti plonosios žarnos infarktą), pieno rūgšties acidozė, piktybinė hipertermija, būklė po komisurotomijos, reumatinė polimialgija, tifoidinis karščiavimas, fon Gyrkės (van Gierke) liga, toksinis šokas. Išlieka normali po injekcijų į raumenis, lengvų fizinių pratimų. Gali padidėti ar išlikti normali sergant nervų ligomis, kepenų ciroze, smegenų infarktu ar kraujuojant į smegenis, ūminiu pankreatitu, inkstų infarktu, hemolizine anemija, hemofilija, esant nutukimui. Papildoma informacija. Šio fermento yra visuose audiniuose, tačiau didžiausias jo aktyvumas kepenyse, širdies ir griaučių raumenyse, eritrocituose, o mažiausias odoje, inkstuose, kasoje. 30% AST aktyvumo tenka citoplazmai ir 70% mitochondrijoms. Vaikams, patyrusiems uždarą pilvo traumą, kai AST kiekis labai didelis, galima įtarti kepenų pažeidimą. Jei kepenų pažeidimas sunkus, suaugusiems AST aktyvumas smarkiai padidėja per 24 val., o per kitas 4 dienas mažėja. Jei išlieka padidėjęs ilgiau kaip 4 dienas, ieškoti priežasties. V: hepatotoksiniai vaistai ar vaistai, sukeliantys cholestazę. Daugelis vaistų gali sukelti laikiną padidėjimą, bet kai kurias atvejais jie gali veikti hepatotoksiškai. Tokiems vaistams priklauso aminoglikozidai, cefalosporinai, ciklosporinas, etakrino rūgštis, etambutolis, fenofibratas, fluorochinolonai (pvz., ciprofloksacinas), gancikloviras, heparinas, HMG-KoA reduktazės inhibi- 153
155 toriai (simvastatinas), interferonas, kaptoprilis, klofibratas, levamizolis, levadopa, linkomicinas, metoprololis, nifedipinas, omeprazolis, penicilinai, piroksikamas, piridoksinas, ranitidinas, streptozocinas, tiklopidinas, tioguaninas, tobramicinas, verapamilis. Ch: askorbo rūgštis, cianidas, formaldehidas, metronidazolis, penicilamidas, sukcinatas, tartratas. γ glutamiltransferazė (GGT) Tiriamoji medžiaga. Serumas. Rekomenduojama reikšmė U/l. Diagnostinė vertė. Obstrukcinės kepenų ligos ir posthepatinė obstrukcija. Kepenų ligos (pvz., uždegimas, cirozė), infekcinė mononukleozė, inkstų transplantatas, hipertirozė, miotoninė distrofija, cukrinis diabetas, pankreatitas, alkoholio sukeltas kepenų pažeidimas. Hipotirozė. γ glutamiltransferazė yra vertingas kasos, prostatos, vėžio ir hepatomos žymuo, nes fermento kiekis koreliuoja su proceso remisija ir recidyvu. Fermento kiekį galima naudoti apskaičiuojant santykį su DTL cholesteroliu (piktnaudžiavimas alkoholiu), šarmine fosfataze (alkoholinis kepenų pažeidimas), aspartataminotransferaze (diferencijuojant naujagimių hepatitą nuo tulžies takų atrezijos). Papildoma informacija. Tyrimu galima nustatyti ankstyvą vyrų alkoholizmo riziką (bet ne moterų), įvertinti alkoholikų gydymo efektyvumą. Nurodoma, kad šis fermentas yra jautresnis vaikų kepenų ligų indikatorius negu šarminė fosfatazė. GGT gali sudaryti kompleksus su apoliproteinais ir imunoglobulinu A. Fermentas yra indukuojamas tokių vaistų, kaip fenobarbitalis, taip pat etanolis. Fermentas pasižymi heterogeniškumu, kuris išryškėja atliekant elektroforezę, elektrofokusavimą. Izoformoms būdingas skirtingas angliavandenių kiekis. V: acetaminofenas (apsinuodijimas), barbitūratai, cefalosporinai, estrogenai, etanolis, kaptoprilis (retai), geriamieji kontraceptikai (ir nėštumas), streptokinazė. V: askorbo rūgštis (ilgą laiką vartojant 1 g per dieną), bezafibratas, fenofibratas, klofibratas. Kreatinkinazė (KK) Tiriamoji medžiaga. Serumas. Rekomenduojama reikšmė. Vyrų U/l, moterų U/l Diagnostinė vertė. Trauma, chirurginė intervencija, miokardo infarktas, kraujo nepritekėjimas į raumenis, bet kurios kilmės miopatiniai sutrikimai (pvz., rabdomiolizė, polimiozitas, dermatomiozitas, miokarditas, alkoholizmas), raumenų distrofijos, pvz., Diušeno (Duchenne) raumenų distrofija, Rejė (Reye) sindromas, apsinuodijimas iki komos, piktybinė hiperpireksija, užsitęsusi hipotermija, infekcinės ligos, aritmijos (retai), įgimtas širdies nepakankamumas, tachikardija, plaučių embolija, stabligė, generalizuoti traukuliai, platus smegenų infarktas, nėštumas, hipoksinis šokas, prostatos, šlapimo pūslės, virškinamojo trakto navikai, plaučių edema, baltoji karštligė, ūminė psichozinė reakcija, galvos trauma, virškinamojo trakto infarktas. Dažniausiai padidėjimas siejasi su širdies ar skersaruožių raumenų ligomis, rečiau lygiųjų raumenų pažeidimu. Geriamieji kontraceptikai slopina aktyvumo padidėjimą. Reikšmės, mažesnės už normą, beveik praktiškai neturi diagnostinės reikšmės. Jos rodo mažą raumenų masę, sėslų gyvenimo būdą. Gulėjimas lovoje (per naktį) gali sumažinti kreatinkinazės aktyvumą 20%. Papildoma informacija. Kreatinkinazės, kaip miokardo infarkto žymens, jautrumas yra apie 97%, specifiškumas apie 67%. V: raumenų darbas (smarkiai padidėja), aminokaprono rūgštis, amfotericinas B, kaptoprilis, chlorpromazinas, klofibratas, klonidinas, kolchicinas, ciklopropanas, dietileteris, etanolis (alkoholikai), gemfibrozilis, haloperidolis, halotanas, HMG-KoA reduktazės inhibitoriai, lidokainas, 154
156 Fermentų klinikinė biochemija ir interpretavimas litis, D penicilaminas, propranololis, chinidinas; apsinuodijimas barbitūratais, anglies monoksidu, narkotikais (pvz., kokainu), injekcijos į raumenis. Ch: hemolizė. Ch: heparinas, labai didelis ar mažas magnio kiekis, užteršimas oksiduojančiomis medžiagomis (pvz., hipochloritu). Kreatinkinazė MB (KK-MB) Tiriamoji medžiaga. Serumas. Rekomenduojama reikšmė. 5 µg/l. Diagnostinė vertė. Žr. sk. Kreatinkinazės izofermentai. Kreatinkinazės izofermentai Tiriamoji medžiaga. Serumas. Rekomenduotina reikšmė. KK I (KK-BB): nėra ar pėdsakai. KK II (KK-MB): < 6%. KK III (KK-MM): pagrindinis serumo komponentas, >94 100%. Diagnostinė vertė. KK-BB: daugelio organų vėžys (šlapimo pūslės, krūties, gimdos kaklelio, kraujodaros organų, tulžies pūslės, plaučių, prostatos, gimdos, sėklidžių), galvos trauma, po neurochirurginių operacijų, po subarachnoidinio kraujavimo, Rejė sindromas, intensyvios slaugos pacientams, po aortokoronarinio šuntavimo operacijos, dėl lėtinio inkstų nepakankamumo, hipotermijos, normalaus gimdymo metu, naujagimiams (ypač jei yra galvos smegenų trauma). KK-MB: Chirurginė trauma (retai), įtempti fiziniai pratimai, širdies miopatijos ir uždegimas, nestabili krūtinės angina, šokas, miokardo infarktas (kiekio greitas pakilimas ir greitas kritimas), subarachnoidinis kraujavimas (susijęs su miokardo infarktu), hipotermija ir hipertermija, piktybinė hipertermija, raumenų distrofijos, Rejė sindromas, širdies ir griaučių raumenų infekcijos, apsinuodijimas (pvz., etanoliu), ilgai trunkančios aritmijos, lėtinis inkstų nepakankamumas. KK-II masės nustatymas yra ankstyvesnis miokardo infarkto žymuo negu aktyvumo nustatymas. KK-MM: Dauguma būklių, aprašytų skyrelyje apie kreatinkinazę. Raumenų mankšta gali labai padidinti KK-MB ir KK-MM, o KK-MB sudaryti <5%. Dėl neurogeninės raumenų atrofijos KK-MB ir KK-MM gali ir nepakisti. Papildoma informacija. Didžiausias KK-BB aktyvumas yra smegenyse ir lygiuosiuose raumenyse. Pagrindinis KK-MB šaltinis yra širdies raumuo (apie 20 40% bendrojo aktyvumo); šio izofermento taip pat yra griaučių raumenyse (<5%). KK-MM daugiausia yra griaučių raumenyse, taip pat širdies raumenyje (audinio svoriui santykis atitinkamai yra 4 : 1). Kartais elektroforegramoje matyti papildomos KK zonos, kurias sudaro KK-Mi I ir II tipų makrokreatinkinazė. Makrokreatinkinazės I tipas tai IgG (rečiau IgA) kompleksas su KK-I (rečiau su KK-II), kuris elektriniame lauke migruoja tarp KK-III ir KK-II. Bendras KK aktyvumas gali būti normalus ar padidėjęs. Makrokreatinkinazės I tipas nustatomas maždaug 2% hospitalizuotų pacientų, dažniau vyresnio amžiaus moterims. Makrokreatinkinazės II tipas yra oligomerinis KK-Mi kompleksas, kuris migruoja link katodo ar arti KK-III. Jo buvimas rodo blogą prognozę (išskyrus vaikus). Neretai yra susijęs su piktybiniu procesu organizme. Bendroji KK paprastai yra padidėjusi. Laktatdehidrogenazė (LDH) Tiriamoji medžiaga. Serumas. Rekomenduojama reikšmė U/l. Diagnostinė vertė. Megaloblastinė ir B 12 vitamino stokos anemija, išplitusi karcinomatozė, virusinis hepatitas, šokas, hipoksija, sunki hipertermija. 155
157 Kepenų cirozė, mechaninė gelta, inkstų ligos, griaučių raumenų ligos, navikinės ligos, įgimtas širdies nepakankamumas. Bet kuris ląstelių pažeidimas, kai jos netenka citoplazmos; miokardo ar plaučių infarktas, leukemija, hemolizinė anemija, hepatitas (ne virusinis), limfoma, inkstų infarktas, ūminis pankreatitas. Genetinė H ir M subvienetų stoka. Papildoma informacija. Matuojant LDH kiekį pirmenybė teikiama piruvato virtimo laktatu reakcijai. Šios reakcijos greitis esant pakankamam fermento kiekiui yra 2 3 kartus didesnis negu laktato virtimo piruvatu reakcijos. Todėl galima naudoti mažesnį tiriamosios medžiagos kiekį, o reakcija vyksta trumpiau. Tačiau vykstant piruvato virtimo laktatu reakcijai greičiau prarandamas linijiškumas, greitesnė substrato inhibicija. V: anestetikai, cefalosporinai, chinidinas, etanolis, fluoruracilas, heparinas, interferonai, metotreksatas, metoprololis, penicilaminas, sulfonamidai, valproatai. V: fluoridai, klofibratas. Laktatdehidrogenazės izofermentai Tiriamoji medžiaga. Serumas. Rekomenduojama reikšmė (%): LDH-I 16,1 31,5 LDH-II 20,2 41,6 LDH-III 17,0 26,2 LDH-IV 5,9 12,3 LDH-V 3,2 17,3. Diagnostinė vertė. LDH izofermentų pokyčių negalima vertinti nežinant klinikos. LDH-I ir (ar) LDH-II: po ūminio miokardo infarkto; sergant hemolizine, B 12 vitamino stokos, megaloblastine anemija; esant ūminei inkstų žievės nekrozei; vykstant in vivo ar in vitro hemolizei. LDH-I: esant embrioninių ląstelių navikams (pvz., teratoma, sėklidžių seminoma, kiaušidžių disgerminoma), griaučių raumenų pažeidimui. LDH-V: esant griaučių raumenų pažeidimams, griaučių raumenų uždegiminėms ar degeneracinėms ligoms, kepenų pažeidimui (cirozė, hepatitas), sergant vėžiu (nejautrus ir nespecifinis žymuo). Normalus elektroforezinis izofermentų pasiskirstymo vaizdas, esant nenormaliam bendrosios LDH kiekiui, nustatytas daugeliui pacientų, sergančių širdies, kepenų, griaučių raumenų, navikinėmis, sisteminėmis ligomis. LDH-II, LDH-III ir LDH-IV padidėjimas esant masyviam trombocitų irimui (pvz., plaučių embolija, po didelio kiekio kraujo perpylimo), taip pat kai procesas apėmęs limfinę sistemą (infekcinė mononukleozė, limfoma, limfocitinė leukemija), esant griaučių raumenų pažeidimui. Mažiausio stabilumo yra LDH-V izofermentas. Lipazė Tiriamoji medžiaga. Serumas. Rekomenduotina reikšmė U/l. Diagnostinė vertė. Pankreatitas, tulžies pūslės akmenligės priepuolis, žarnų užsisukimas, kasos cista ar pseudocista, peritonitas. Esant ūminiam pankreatitui, serumo lipazės aktyvumas ilgiau išlieka padidėjęs, negu serumo amilazės. Lipazės kiekis yra normalus sergant nekomplikuotuoju parotitu. Pankreatito metu lipazė ir amilazė papildo viena kitą. Lipazė turi didesnį klinikinį jautrumą ir specifiškumą negu amilazė. Ascitiniame skystyje sergant pankreatitu lipazės aktyvumas yra labai didelis. Lipazės aktyvumas galimas ir pleuros transudate; retais atvejais šį fermentą gali gaminti plaučių navikas. ERCP padidina serumo lipazės aktyvumą. 156
158 Fermentų klinikinė biochemija ir interpretavimas Papildoma informacija. Serume randamos dvi ar daugiau lipazės izoformos. Makrolipazė (lipazės kompleksas su IgG) gali būti randama sergant piktybine ne Hodžkino limfoma ir kriptogenine kepenų ciroze. V: vaistai, sukeliantys Odi sfinkterio spazmą (narkotiniai analgetikai, sekretinas) ar pankreatitą; heparinas (atpalaiduoja kepenų lipazę ir lipoproteinlipazę). Ch: chininas, EDTA, sunkieji metalai. Rūgščioji fosfatazė (RF) Tiriamoji medžiaga. Serumas. Rekomenduojama reikšmė. 10 U/l (priklauso nuo metodo; kraujo serumas be hemolizės pėdsakų tiriamas tuoj paėmus kraują). Diagnostinė vertė. Yrant trombocitams, sergant hemolizine liga, esant metastazėms kauluose, kai kuriais mielominės ligos atvejais. Šio fermento aktyvumas taip pat padidėja sergant prostatos vėžiu, ypač metastazuojančiu, Gošė, Nimano Piko ligomis, esant prostatos infarktui, po šlapimo pūslės kateterizacijos, praėjus 1 2 dienoms po prostatos operacijos ar jos biopsijos. Papildoma informacija. RF yra lizosominis fermentas, glikoproteinas. Didžiausias RF aktyvumas 1 g audinio yra prostatoje. Mažesnis aktyvumas ne prostatai specifinės rūgščiosios fosfatazės yra kepenyse, blužnyje, eritrocituose, trombocituose, kaulų čiulpuose. Pusę bendro vyrų RF aktyvumo sudaro prostatos izofermentas, o likusi aktyvumo dalis yra iš kepenų, trombocitų, eritrocitų. (Apie prostatos rūgščiąją fosfatazę detaliau skyriuje Molekuliniai navikų žymenys ir jų panaudojimas ligų diagnostikai ). Lengva hemolizė. Šarminė fosfatazė (ŠF) Tiriamoji medžiaga. Serumas. Kambario temperatūroje aktyvumas didėja. Reikia tirti greitai ar laikyti šaldytuve. Atšildant užšaldytą ėminį gali padidėti 30%. Rekomenduojama reikšmė U/l. Diagnostinė vertė. Suintensyvėjusi kaulų apykaita: gyjant lūžiams, pirminė ir antrinė hiperparatirozė (jei yra pažeisti kaulai), osteomaliacija, juvenilinis rachitas (D vitamino stoka maiste). Kaulų ligos: metastazinis kaulų vėžys, osteogeninė sarkoma, mieloma, Hodžkino liga (jei pažeisti kaulai), Gošė liga vykstant kaulų rezorbcijai, Pedžeto liga, Kušingo sindromas, ureminė osteodistrofija, inkstų kanalėlių pažeidimas, susijęs su fosfato ir (ar) kalcio netekimu (išsivysto rachitas). Inkstų ligos: inkstinis rachitas dėl D vitaminui atsparaus rachito, susijusio su antrine hiperparatiroze. Kepenų ligos: infekcinė mononukleozė, nekomplikuota ekstrahepatinė obstrukcija (padidėja >3 kartus), kūdikių citomegalovirusinė infekcija, cholangitas ir cholangiolitas, hepatocitų nekrozė su gelta ar be jos (padidėja >3 kartus), portinė cirozė (retai), kepenų pūlinys, pirminis hepatoceliulinis vėžys, aktyvi hepatocitų ar tulžies takų regeneracija (proliferacija); mazgai kepenyse (metastazinis navikas, parazitai, amiloidas, tuberkulas, sarkoidas ar leukemija), hepatitas dėl infekcijos, cheminių medžiagų, narkotikų, širdies nepakankamumo; prieštraukulinių vaistų ilgalaikis vartojimas. Įvairios priežastys: ekstrahepatinis sepsis, opinis kolitas, regioninis enteritas, bakterinė infekcija pilvaplėvės ertmėje, tirotoksikozė, gerybinė laikinoji hiperfosfatemija (vaikams), plaučių ir inkstų infekcijos, pankreatitas, alkoholio vartojimas (fermento indukcija). Hipotirozė, skorbutas, didelė anemija, achondroplazija, kretinizmas, radioaktyviųjų medžiagų kaupimasis kauluose, hipofosfatemija, B 12 vitamino stoka, cinko ar magnio stoka. Papildoma informacija. Daugiausia gamina kepenys, kaulai, žarnos, gimdos gleivinė (placenta) ir plaučiai. Virškinimo procesas didina šarminės fosfatazės, žarnų izofermento kiekį serume, ypač jei asmenys turi O ar B kraujo grupę. Šarminės fostazės aktyvumas didėja vaikams jų greito augimo tarpsniu, moterims paskutinius tris nėštumo mėnesius (nukrinta iki normos per 3 6 savaites po gimdymo), po menopauzės. 157
159 V: hepatotoksiniai vaistai. Kiti vaistai gali sukelti praeinantį kiekio padidėjimą, o kai kuriais atvejais rodo toksiškumą kepenims. Tokiems vaistams priklauso aminoglikozidai, kaptoprilis, cefalosporinai, kolchicinas, ciklosporinas, dikumarolis, enalaprilis, etambutolis, gancikloviras, gentamicinas, interferonas, levamizolis, linkomicinas, nifedipinas, vaistai nuo uždegimo, omeprazolis, penicilinai, streptozocinas, tioguaninas, tiklopidinas, verapamilis. Ch: askorbo rūgštis, magnis. V: azatioprinas, estrogenai, klofibratas, geriamieji kontraceptikai. Ch: citratas, cianidas, cinko, magnio druskos (perteklius), EDTA, fluoridas, fosfatas, manganas, oksalatas, teofilinas. Šarminės fosfatazės izofermentai Tiriamoji medžiaga. Serumas. Rekomenduojama reikšmė. Kepenų izofermentas 45 55%, kaulų 45 53%, žarnų 0 10%. Nėščiosioms nustatomas placentos izofermentas. Diagnostinė vertė. Kaulų izofermentas: padidėjusi kaulo gamyba (pvz., sergant Pedžeto liga); fiziologinis kaulų augimas (pvz., vaikams), gyjant kaulų lūžiams, osteomaliacija ir osteoporozė, pomenopauzinė osteoporozė, osteomaliacija hiperparatirozės metu, stoka maiste (pvz., D vitamino stokos sukeltas rachitas), D vitaminui atsparus rachitas, prieštraukulinių vaistų sukeltas rachitas, inkstų kanalėlių acidozės sukeltas rachitas; malabsorbcijos sindromas, kaulų osteosarkoma, prostatos, krūties vėžio metastazės kauluose, regeneracija po sėkmingo gydymo (pvz., osteolizinio metastazinio kaulų vėžio, limfomos, leukemijos); kaupimo ligos (pvz., Goše liga, Nimano Piko liga), inkstų osteodistrofija (ureminė kaulų liga arba inkstinis rachitas). Osteopenija dėl genetinės hipofosfatemijos, hipotiroidinis kretinizmas, ilgalaikė magnio, cinko, B 12 vitamino stoka maiste. Kepenų I izofermentas (suintensyvėjusi biosintezė): fermento kaupimasis kepenyse ir sutrikęs šalinimas, vaskulitas, nėštumas. Kepenų II izofermentas (intraląstelinis fermentas): parenchiminių ląstelių pažeidimas. Tulžies šarminė fosfatazė: cholestazė (didelės molekulinės masės lipoproteinas X). Žarnų šarminė fosfatazė: kai kuriems pacientams, sergantiems žarnų ligomis, turintiems O ir B kraujo grupes (ypač pavalgius). Placentos šarminė fosfatazė atsiranda motinos serume (ypač padaugėja III nėštumo trečdalį). Neindefikuotieji izofermentai dažniausiai yra neoplazinės kilmės. Tiriant elektroforeze, jie juda panašiai kaip placentos izofermentas. Papildoma informacija. V: detaliau skyrelyje Šarminė fosfatazė. 158
160 MIOKARDO INFARKTAS IR JO LABORATORINĖ DIAGNOSTIKA Diagnostiniai miokardo infarkto kriterijai Miokardo infarktas (MI) tai dažna ir sunki patologija, svarbiausia suaugusių žmonių sergamumo ir mirtingumo priežastis. Jį sukelia nekroziniai miokardo pažeidimai staiga sutrikus aprūpinimui krauju dėl vainikinių kraujagyslių trombozės. Dėl aterosklerozės išsivysčiusi koronarinė širdies liga bei trombų susidarymas yra svarbiausi ūminio miokardo infarkto patogenezės veiksniai. Kuo ankstesnė ir tikslesnė vainikinių kraujagyslių trombozės diagnostika, tuo geresni specifinio trombolizinio gydymo rezultatai. Pasaulio sveikatos organizacija yra apibrėžusi miokardo infarkto diagnostikos kriterijus: krūtinės skausmas, trunkantis apie 30 minučių; tipiškų elektrokardiogramos pokyčių atsiradimas; būdingas fermentų aktyvumo kitimas metais Europos kardiologų draugija patikslino ūminio miokardo infarkto diagnostikos kriterijus. Tai širdies žymenų (pirmenybė teikiama troponinui) padidėjimas ir (arba) sumažėjimas, kai viena reikšmė viršija 99-ąjį procentilį normalios vertės kartu su vienu iš miokardo išemijos požymių: išemijos klinikiniai simptomai (krūtinės skausmas, trunkantis apie 30 minučių); išemijai būdingi EKG pokyčiai; radiologiniai miokardo gyvybingumo praradimo ar miokardo sienelės paslankumo sutrikimo požymiai. Diagnozė neretai išryškėja jau renkant anamnezę pagal būdingus skausmus krūtinės srityje. Tačiau yra ir kitų tokių skausmų priežasčių. Užrašytoje elektrokardiogramoje dažniausiai matyti pakitimai, būdingi miokardo infarktui. Tačiau elektrokardiografinis vaizdas gali neišryškėti iki 24 valandų po infarkto. Be to, elektriškai ir kliniškai nebylūs infarktai sudaro apie 20 25% visų miokardo infarkto atvejų. Jie dažnesni vyresnio amžiaus asmenims, sergantiems cukriniu diabetu, turintiems padidėjusį kraujospūdį. Elektrokardiogramos pokyčių įvairovė priklauso nuo infarkto vietos, pažaidos ploto. Iš elektrokardiogramos naujas infarktas anksčiau jau pažeistame širdies raumenyje gali būti sunkiai interpretuojamas. Ūminis miokardo infarktas yra kaitus procesas. Širdies žymens atsipalaidavimas iš išemijos zonos į kraują, kur jis nustatomas, priklauso nuo jo lokalizacijos ląstelėje, 159
161 kraujagyslių tinklo zonoje ir aplink ją žymens baltymo molekulės dydžio. Prisimintina, kad krūtinės skausmo pradžia ne visada yra žinoma, ypač jei asmuo vyresnio amžiaus. Šiais atvejais nustatyti fermentų aktyvumą ar kitus širdies raumeniui būdingus žymenis yra labai svarbu ir ligos diagnostikai, ir prognozei. Širdies raumens pažeidimą rodantys biocheminiai žymenys: bendrasis kreatinkinazės aktyvumas, kreatinkinazės MB izofermentas, laktatdehidrogenazė ir jos izofermentai I ir II, mioglobinas, troponino komplekso elementai: širdies troponinas I ir troponinas T. Iš naujų tyrimų, kurie diegiami į klinikinę praktiką, paminėtini glikogenfosforilazės, riebalų rūgštis sujungiančio baltymo. Svarbu kuo greičiau nustatyti miokardo infarktą, nes anksčiau pradėtas gydymas yra veiksmingesnis ir ligos prognozė geresnė. Pirmasis biocheminis žymuo, naudotas ūminio miokardo infarkto diagnostikai, aspartataminotransferazė (AST). Pirmą kartą ji buvo aprašyta 1954 metais. Pamažu ją pakeitė kitas fermentas kreatinkinazė, aprašyta 1965 metais. Tobulėjant elektroforezės metodams, kreatinkinazės ir laktatdehidrogenazės izofermentai buvo pripažinti kaip didesnio specifiškumo biocheminiai žymenys metais miokardo infarkto diagnostikai buvo pritaikytas kreatinkinazės MB izofermento nustatymas imunoinhibicijos metodu bei radioimuninis mioglobino tyrimas metais Pasaulio sveikatos organizacija apibrėžė ūminio miokardo infarkto triadą, kurios vienas punktas buvo specifinių fermentų aktyvumo padidėjimas. Šių žymenų taikymas diagnostikai gerokai išsiplėtė sukūrus antikūnus prieš kreatinkinazės MB izofermentą. Pagaminti komerciniai diagnostiniai rinkiniai plačiai taikomi Lietuvoje. Troponinas T ūminio miokardo infarkto diagnostikai pirmą kartą buvo pritaikytas 1989 metais, o troponinas I 1992 metais. Patofiziologinis miokardo išemijos mechanizmas Nutrūkus kraujo pritekėjimui į širdies raumens ląsteles, sutrinka su membrana susijusių jonų siurblių veikla. Ląstelė pirmiausia netenka K +, Mg 2+, Zn 2+, kitų jonų (12 lentelė). Todėl pirmieji laboratoriniai ūminės miokardo išemijos laboratoriniai požymiai yra šių jonų koncentracijos padidėjimas kraujyje. Tęsiantis išemijai sutrinka ląstelės medžiagų apykaita (reguliavimas) ir ląstelė pro pažeistą membraną pradeda netekti ląstelinių metabolitų. Dėl išemijos anksčiausiai sutrinka angliavandenių apykaita ir šį sutrikimą diagnostiškai geriausiai parodo pieno rūgšties (laktato) koncentracijos didėjimas kraujyje. 160
162 Miokardo infarktas ir jo laboratorinė diagnostika 12 lentelė. Patofiziologinis miokardo išemijos mechanizmas Laikas Ląstelių pokyčiai Biochemija 0 min. Miokardo išemija su membrana susijusių jonų siurblių disfunkcija Ląstelinių K +, Zn 2+, Mg 2+, PO 4 ir kitų jonų netekimas 60 min. Ląstelinio metabolizmo reguliacijos sutrikimas Ląstelių membranų modifikacija Ląstelės nekrozė Ląstelinių laktato, adenozino ir kitų metabolitų netekimas Ląstelinių mioglobino, fermentų ir kitų makromolekulių netekimas Ląstelės citoplazmos turinio netekimas Dėl jonų netekimo ir medžiagų apykaitos sutrikimo apie 60-ą širdies raumens išemijos minutę pradeda modifikuotis ląstelės membrana. Ji tampa pralaidi makromolekulėms mioglobinui, fermentams, kitiems specifiniams baltymams. Prasideda ląstelės nekrozė, dėl to visas ląstelės turinys išsilieja į aplinką, t. y. į limfą. Jonai ir metabolitai į bendrą kraujo cirkuliaciją patenka tiesiai iš vainikinių kraujagyslių. Kadangi apie 20 50% fermentų bei kitų makromolekulių į kraują patenka su limfa, taip pat dėl širdies raumens kapiliarų pamatinės membranos storio tarp išemijos pradžios ir fermentų aktyvumo padidėjimo kraujo serume praeina 3 6 valandos. Taigi jonų padidėjimas kraujo serume yra nespecifinis ir greitai praeinantis, o makromolekulių padaugėjimas yra ilgalaikis ir itin specifiškas. Elektrolitų, metabolitų koncentraciją po išemijos atitinkami mechanizmai greitai sunormina, o fermentų aktyvumo, kitų makromolekulių kiekis išlieka padidėjęs ilgiau. Širdies ra u m e n s žy m e n ų st r u k t ū r a ir lokalizacija ląstelėje Apie kreatinkinazę ir laktatdehidrogenazę rašyta skyriuje Fermentų klinikinė biochemija ir interpretavimas. Troponinas kartu su tropomiozinu priklauso struktūriniams baltymams, reguliuojantiems raumens susitraukimą. Troponinas susideda iš trijų komponentų: troponino C, troponino I ir troponino T. Kiekvienas iš jų atlieka specifines funkcijas. Troponinas C yra Ca 2+ sujungiantis baltymas. Troponinas I slopina aktomiozino ATF-azės aktyvumą ir šį slopinimą grįžtamuoju ryšiu reguliuoja Ca 2+ prisotintas troponinas C. Taigi troponinas I ir troponinas C tiesiogiai sąveikauja tarpusavyje, o troponinas T atlieka šių abiejų troponinų fiksatoriaus ant aktino bei tropomiozino filamentų funkciją. Žmogaus širdies troponino I aminorūgščių seka yra apie 60% homologiška su kitomis izoformomis, tačiau N gale turi papildomą 31 aminorūgšties seką. Dėl tokios unikalios struktūros ir ankstyvo atsipalaidavimo iš pažeisto širdies raumens jis 161
163 tampa labai svarbiu širdies pažeidimo žymeniu. Troponinas I randamas trijų izoformų: greito ir lėto susitraukimo griaučių raumenyse ir vienos rūšies širdies raumenyje. Širdies troponinas T 90% homologiškas su griaučių raumenų formomis, tačiau skirtumas pakankamas specifiškai jį atpažinti naudojant monokloninius antikūnus. Diagnostinis abiejų troponinų jautrumas diagnozuojant ūminį miokardo infarktą yra panašus. Mioglobinas raumenyse randamas baltymas hemoproteinas, kurio struktūroje yra hemo. Tai deguonį sujungiantis baltymas, kuris atlieka O 2 pernašos funkciją. Mioglobinas yra pagrindinė raumens sutraukiamojo aparato storųjų skaidulų sudedamoji dalis. Fiziologinėmis sąlygomis mioglobino sujungtas deguonis nenaudojamas ir gali atsipalaiduoti tik esant kritiškai mažam daliniam deguonies slėgiui. Glikogenfosforilazė yra vidiniame sarkoplazminio tinklo paviršiuje. Glikogenfosforilazė ir ypač jos BB izofermentas yra labai jautrūs kardiomiocitų išemijos žymenys. Šis izofermentas kliniškai yra jautresnis ūminio miokardo infarkto žymuo, palyginti su KK-MB, mioglobinu ar troponinais. Riebalų rūgštis sujungiantis baltymas yra difuziškai pasklidęs sarkoplazmoje (kaip ir mioglobinas), jo funkcija yra sujungti ir pernešti kardiomiocituose ilgųjų grandinių riebalų rūgštis. Po miokardo infarkto šio baltymo atsiranda kraujyje ir šlapime, o kiekio pokyčiai yra panašūs į mioglobino koncentracijos kaitą. Biochemikai aktyviai ieško ir naujų širdies raumens pažeidimo žymenų. Viena paieškos krypčių rasti žymenį, kuris pradėtų kisti anksčiau ir specifiškiau už mioglobiną. Tačiau klinikinėje laboratorinėje praktikoje naujų technologijų tobulėjimas ir tokių tyrimų kaina turi sudaryti pusiausvyrą. Jei naujas tyrimas nepagerins ligos baigties ar nesumažins diagnostikos ir gydymo išlaidų, tai bus labai sunku pateisinti jo diegimą į klinikinę praktiką. Tačiau naujų žymenų paieškos ir bandymai vyksta, nes plečiasi koronarinės širdies ligos ir patofiziologinių širdies raumens pažeidimo mechanizmų samprata. Mi o k a r d o in f a r k t o žy m e n ų kitimas pagal laiką Mioglobino pradeda daugėti po 2 4 val. nuo krūtinės skausmų pradžios, maksimumą pasiekia po 6 12 valandų ir tampa normalus per 24 valandas (8 pav.). Jei po 6 10 valandų nuo skausmų pradžios mioglobino koncentracija normali, tai su didele tikimybe miokardo infarkto diagnozę galima atmesti. Po reperfuzijos procedūros atkūrus kraujotaką, mioglobino koncentracija labai padidėja ir po to staiga sumažėja. Šis pakilimas yra didesnis, o sunormalėja anksčiau (po val.) negu konservatyviai gydomų ligonių (po val.). Staigus koncentracijos padidėjimas daugiau kaip 4 kartus per 90 minučių po trombolizinio gydymo rodo sėkmingą reperfuziją. Rekomenduojamas mioglobino kiekis kraujo serume <70 µg/l. 162
164 Miokardo infarktas ir jo laboratorinė diagnostika KK TNI MIO KK-MB LDH 8 pav. Miokardo infarkto žymenų kitimas pagal laiką Kreatinkinazė atsipalaiduoja per 3 12 valandų nuo krūtinės skausmų pradžios, pakilimo maksimumas yra ą valandą ir sunormalėja po valandų. Rekomenduojama kreatinkinazės reikšmė kraujo serume: vyrų U/l, moterų U/l (gulėjimas lovoje, pvz., per naktį, gali sumažinti KK aktyvumą 20%). Kreatinkinazės MB izofermento kaita matuojant aktyvumą kraujo serume yra panaši į kreatinkinazės aktyvumo pokyčius. KK-MB frakcija normaliai sudaro 2 3% bendrojo kreatinfosfokinazės aktyvumo, o po miokardo infarkto jos dalis padidėja iki 22% (vidutiniškai 13%). Matuojamos KK-MB masės koncentracijos kaita per pirmas 6 7 val. nuo krūtinės skausmų pradžios yra panaši į diagnostinį mioglobino jautrumą, o klinikinis specifiškumas netgi didesnis. KK-MB masės koncentracija pradeda didėti po 2 6 val., maksimumas pasiekiamas per val. ir sunormalėja per 3 dienas. Diagnozei patvirtinti tyrimą būtina pakartoti. KK-MB masės koncentracijos padidėjimas daugiau kaip 4 kartus per 90 minučių po trombolizinio gydymo rodo sėkmingą reperfuziją. Esant nestabiliajai krūtinės anginai ir padidėjusiai KK -MB masės koncentracijai, mirtingumo ir miokardo infarkto rizika gerokai išauga, palyginti su tais nestabiliąja krūtinės angina sergančiais ligoniais, kurių KK-MB masės koncentracija yra normali. Laktatdehidrogenazės daugėja lėčiau: šio fermento aktyvumas maksimumą pasiekia 2 3 parą ir sunormalėja po 6 7 parų (gali išlikti padidėjusi iki 14 dienų). Diagnostikai yra svarbūs jos izofermentai. Laktatdehidrogenazės I izofermento pradeda daugėti po 6 12 val. nuo skausminio sindromo pradžios, maksimalus kiekis pasiekiamas 2 6-ą dieną ir sunormalėja po 7 14 dienų. Matuojamas ir LDH-I/LDH-II santykis: sveikų asmenų jis yra 0,45 0,74, po miokardo infarkto >0,8. 163
165 Troponino T kiekis didėja praėjus 3 8 val. po infarkto, maksimumą pasiekia po val. ir išlieka padidėjęs apie 7 dienas (gali iki 20 dienų). Troponino T aktyvumas bazinį lygį gali viršyti apie kartų. Taigi jo didėjimo mastai smarkiai viršija KK-MB ar mioglobino kiekio padidėjimą. Jei troponino T kiekis padidėjęs, pasikartojusį infarktą sunku nustatyti. Esant neigiamam rezultatui, tyrimas pakartojimas po 2 val. Jei po 8 val. nuo krūtinės skausmų pradžios jis neigiamas, su didele tikimybe miokardo infarkto diagnozė gali būti atmesta. Maždaug 50% ligonių, sergančių ūminiu miokardo infarktu, troponino T padaugėja po 3 4 val. nuo krūtinės skausmų pradžios. Kadangi troponinas T atsipalaiduoja tik iš negyvybingo širdies raumens audinio, tai 3 4-ą dieną įvertinus padidėjimo mastą galima nustatyti ir infarkto stiprumą. Po anksti atliktos sėkmingos reperfuzijos troponino T koncentracija labai padidėja. Jos padidėjimas daugiau kaip 6,8 karto per 90 minučių po trombolizinio gydymo rodo sėkmingą reperfuziją. Maždaug trečdaliui ligonių, sergančių sunkia nestabiliosios krūtinės anginos forma, gali būti randama nedaug padidėjusi troponino T koncentracija tai gali rodyti įvykusį mikroinfarktą. Dėl stabiliosios krūtinės anginos troponino T kiekis nepadidėja. 2 3% ligonių, sergančių lėtiniu inkstų funkcijos nepakankamumu ir gydomų hemodializės procedūromis, gali būti padidėjęs troponino T ar ir troponino I kiekis. Tai paaiškina didelį KŠL paplitimą tarp šios grupės ligonių. Troponino T rekomenduojama koncentracija kraujyje iki 0,1 µg/l. Ištikus miokardo infarktui, troponino I kiekis pradeda didėti po 3 8 val., didžiausias pakilimas yra po val. nuo simptomų pradžios. Koncentracija sunormalėja vidutiniškai po 7 dienų (5 10 dienų). Po reperfuzijos troponino I kiekis padidėja staigiau ir didesniu mastui nei troponino T kiekis. Po sėkmingos trombolizės pakilimas yra po 2 6 val., didžiausią reikšmę pasiekia po 8 16 val. ir sunormalėja po 3 7 dienų. Po širdies transplantacijos (nesivystant atmetimo reakcijai) troponino I kiekis grįžta į pradinį greičiau (po 2 3 savaičių) negu troponino T (po 2 3 mėnesių). Tyrimais įrodyta, kad ūminis ar lėtinis griaučių raumenų pažeidimas, maratoninis bėgimas ar dializės procedūros nepadidina širdies troponino I kiekio. Troponino I rekomenduojama koncentracija kraujo serume <0,5 µg/l. Kreatinkinazės ir laktatdehidrogenazės aktyvumo kitimai įvykus miokardo infarktui nepasižymi dideliu jautrumu ar specifiškumu, ypač esant nestabiliajai krūtinės anginai, miokarditui, toksiniam širdies pažeidimui ar inkstų funkcijos nepakankamumui, todėl šie žymenys vis rečiau naudojami tiksliai ūminio miokardo infarkto diagnostikai. Glikogenfosforilazė ir ypač jos BB izofermentas yra labai jautrūs kardiomiocitų išemijos žymenys. Pastarasis kliniškai yra jautresnis ūminio miokardo infarkto žymuo negu KK-MB, mioglobinas ar troponinai: jo koncentracija pradeda didėti po infarkto praėjus po 1 4 val., maksimumą pasiekia po 6 12 val., o sunormalėja po paros. 164
166 Miokardo infarktas ir jo laboratorinė diagnostika 9 pav. Miokrdo infarkto biocheminių žymenų specifiškumas Norint tinkamai pasirinkti miokardo infarkto žymenį tiriant ligonį, atvykusį dėl krūtinės skausmų, visada reikia atsižvelgti į laiką, praėjusį nuo skausmų pradžios. Ankstyvajai ūminio miokardo infarkto diagnostikai tinkamiausi yra mioglobinas, KK MB izofermentas, vėlyvajai troponinai, laktatdehidrogenazė. Tarp šių laikotarpių geriausia pasirinkti troponinus dėl jų didžiausio specifiškumo (9 pav.). Kaip matyti iš 8 paveikslo, ryškiausias koncentracijos padidėjimas įvykus miokardo infarktui būdingas troponinui I, taip pat troponinui T bei kreatinkinazės širdies izofermentui. Kritine riba atmetant ar patvirtinant miokardo infarktą gali būti troponino I koncentracijos padidėjimas apie 3 kartus, o mažesnės jo koncentracijos vertinamos kaip nestabiliosios krūtinės anginos požymis ir rizika išsivystyti miokardo infarktui. Taigi kraujo serumo fermentų ir specifinių baltymų kiekio matavimas labai padeda gydytojui diagnozuoti, prognozuoti ir vertinti miokardo infarkto gydymo sėkmę. Api b e n d r i n i m a s Klasikiniai miokardo infarkto simptomai yra stiprus skausmas, plintantis į kairę ranką, mentę. Tačiau jis būna ne visada. Taigi galimi nebylūs infarktai ir jie aptinkami užrašytoje elektrokardiogramoje, tačiau elektrokardiografiniai požymiai taip pat ne visada anksti išryškėja. Kuo anksčiau nustatomas miokardo infarktas ir anksčiau pradedamas gydymas, tuo ligos gydymo rezultatai ir prognozė yra geresni metais Europos kardiologų draugija patikslino ūminio miokardo infarkto diagnostikos kriterijus. Tai širdies žymenų (pirmenybė teikiama troponinui) aktyvumo padidėjimas ir/arba 165
167 sumažėjimas, kai viena reikšmė viršija 99-ąjį procentilį normalios vertės kartu su vienu iš miokardo išemijos požymių: išemijos klinikiniai simptomai (krūtinės skausmas, trunkantis apie 30 minučių); išemijai būdingi EKG pokyčiai; radiologiniai miokardo gyvybingumo praradimo ar miokardo sienelės paslankumo sutrikimo požymiai. Tarp išemijos pradžios ir serumo fermentų kiekio padidėjimo susidaro 3 6 valandų tarpas, nes apie 20 50% fermentinių baltymų į kraują patenka su limfa. Ankstyvajai miokardo infarkto diagnostikai tinkamiausi širdies raumens pažeidimo žymenys yra mioglobinas, kreatinkinazės MB izofermentas. Vėlyvajai miokardo infarkto diagnostikai tinkamiausi žymenys yra troponinai, laktatdehidrogenazė. Tarp šių laikotarpių geriausia pasirinkti troponinus dėl didžiausio jų specifiškumo. Mioglobinas Tiriamoji medžiaga. Serumas. Rekomenduojama reikšmė. <70 µg/l. Diagnostinė vertė. Miokardo infarktas (didėja anksčiau negu kreatinkinazė ir jos MB frakcija), uremija, trauma, traukuliai, uždegiminė miopatija, injekcijos į raumenis, fiziniai pratimai, nudegimai. Mioglobinas yra nespecifinis miokardo infarkto žymuo. Taip pat didėja esant bet kuriam procesui, susijusiam su griaučių ir širdies raumenų pažeidimu, nekroze ar ląstelių lize, pvz. elektrinis šokas, išemija, rabdomiolizė, miopatija, raumenų distrofija, miozitas. Kai kraujyje yra antikūnų prieš mioglobiną (pvz., polimiozito metu), taip pat sergant reumatoidiniu artritu, myasthenia gravis (ne visada). Papildoma informacija. Mioglobino yra visose griaučių ir širdies raumenų ląstelėse. Reikšmės serume tiesiogiai susijusios su raumenų mase. Mioglobino padidėjimas yra laikinas radinys: jis būna 1 4 val. nuo simptomų pradžios po miokardo infarkto ir per 24 val. sunormalėja. V: lovastatinas. Troponinas I Laboratoriniai tyrimai Tiriamoji medžiaga. Serumas. Rekomenduojama reikšmė. <5 µg/l. Diagnostinė vertė. Miokardo infarktas. Koronarinė širdies liga, ūminis griaučių raumenų pažeidimas (kai kada). Papildoma informacija. Troponinas I (specifinis širdžiai) yra vienas iš trijų troponinų reguliavimo komplekso baltymų. Troponinai dalyvauja aktino ir miozino jungimosi reakcijoje. Troponinas I turi tris izoformas: greito ir lėto susitraukimo griaučių raumenyse ir širdies raumenyje. Žmogaus širdies troponinas I turi 60% homogeninių sekų su kitomis izoformomis ir dar 31 papildomą aminorūgščių seką N-gale. Taigi tokia unikali struktūra ir ankstyvas atsipalaidavimas iš pažeisto širdies raumens daro jį labai svarbų širdies pažeidimo diagnozei. Įvykus miokardo infarktui, troponino I kiekis padidėja 2 6 kartus. Pradeda didėti po 4,6±1,6 val., pradinis didžiausias pakilimas yra po val. nuo infarkto, o antras mažesnis po val. Antrasis pakilimas būna ne visiems pacientams. Kiekis sunormalėja po 7 dienų. Po sėkmingos 166
168 Miokardo infarktas ir jo laboratorinė diagnostika trombolizės pakilimas yra po 4,3±2,1 val., pikas po 12,2±,6 val. ir sunormalėja po 117±46 val. Ištirta, kad ūminis ar lėtinis griaučių raumenų pažeidimas, maratoninis bėgimas ar dializės procedūros nepadidina širdies troponino I kiekio. Troponinas T Tiriamoji medžiaga. Serumas. Rekomenduojama reikšmė. Iki 0,1 µg/l. Diagnostinė vertė. Miokardo infarktas, mikroinfarktas, nestabilioji krūtinės angina, miokardo pažeidimas atliekant perkutaninę transluminę vainikinių arterijų angioplastiką, koronorografiją, esant miokarditui, miokardo kontuzijai, griaučių raumenų miopatijai (retai). Papildoma informacija. Širdies troponinas T yra vienas iš trijų troponinų reguliacinio komplekso baltymų, dalyvaujančių aktino ir miozino jungimosi reakcijoje. Širdies troponinas T 90% homologiškas su griaučių raumenų formomis, tačiau skirtumas pakankamas specifiškai jį atpažinti naudojant monokloninius antikūnus. Širdies troponino T kiekis didėja praėjus 2 6 val. po infarkto ir išlieka padidėjęs apie 6 dienas (gali iki 20 dienų). Padidėjimas bazinį kiekį viršija apie 40 kartų. Jei kiekis yra padidėjęs, pasikartojusį infarktą sunku nustatyti. Klaidingai teigiamas padidėjimas kartais nustatomas esant lėtiniam inkstų nepakankamumui, lėtinėms raumenų ligoms. 167
169 GLIUKOZĖS APYKAITA, CUKRINIS DIABETAS IR JO LABORATORINĖ DIAGNOSTIKA Gliukozės svarba žmogaus organizmui Su maistu į virškinamąjį traktą patekę angliavandeniai yra skaidomi iki monosacharidų ir absorbuojami. Krakmolas suskaidomas iki gliukozės; fruktozė (iš vaisių, medaus sacharozės) ir galaktozė (iš laktozės) yra absorbuojamos, nešamos į kepenis ir ten paverčiamos gliukoze. Gliukozė vienintelis angliavandenis kraujyje. Vien suaugusio žmogaus smegenys kasdien sunaudoja apie 120 g gliukozės, kad pagamintų reikiamą ATF kiekį. Jeigu žmogus nustoja valgyti, tai visas jo kepenyse esantis glikogenas yra suvartojamas per valandų; t.y. angliavandenių atsargų užtenka tarp vakarienės ir pusryčių. Gliukozės koncentracija kraujyje atspindi jos sintezės ir suvartojimo pusiausvyrą. Ji beveik tolygiai pasiskirsto tarp kraujo plazmos ir forminių elementų. Kraujyje gliukozės koncentracija yra 15% mažesnė negu plazmoje. Arteriniame kraujyje jos kiekis yra didesnis negu veniniame (dėl intensyvaus jos panaudojimo audinių ląstelėse), o kapiliariniame kraujyje jos yra apie 7% daugiau negu veniniame kraujyje. Gliukozės koncentracija sveikų žmonių kraujyje kinta su amžiumi: naujagimių kraujyje gliukozės koncentracija yra lygi jos koncentracijai motinos kraujyje; po gimimo gliukozės greitai mažėja ir jau po 3 6 valandų jos yra apie 2,5 mmol/l. Tai fiziologinė hipoglikemija, kurią galima paaiškinti staigiu ryšio su motinos organizmu nutraukimu, kai naujagimio organizmas prisitaiko prie naujų sąlygų ir suvartoja daugiau gliukozės. Be to, po gimimo kepenų struktūros dar nėra susiformavusios ir glikogenolizės fermentų aktyvumas dar nepakankamas. Jau pirmą gyvenimo savaitę gliukozės kiekis pradeda didėti ir 5 6 dieną po gimimo siekia vidutiniškai 3 mmol/l tai kūdikiams rekomenduojama norma. Po pirmųjų gyvenimo metų gliukozės kiekis kraujyje didėja ir suaugusiųjų normą pasiekia apie 15-us gyvenimo metus. Insulinas yra svarbiausias hormonas, mažinantis gliukozės koncentraciją kraujyje. Tai nedidelės molekulinės masės polipeptidas, sintetinamas kasos Langerhanso salelių beta (β) ląstelėse. Jis veikia per ląstelių membranų receptorius. Svarbiausi organai taikiniai yra kepenys, raumenys ir riebalinis audinys. Insulinas skatina gliukozės patekimą į ląsteles ir jos, kaip energijos šaltinio, kaupimą (10 pav.). Pažymėtina, kad nesant insulino gliukozė negali patekti į daugelio audinių ląsteles. 168
170 Gliukozės apykaita, cukrinis diabetas ir jo laboratorinė diagnostika Gliukoneogenezė Glikogenolizė Lipolizė Ketogenezė Proteolizė Insulinas + Aktyvi pernaša, ypač K + ir PO 3 4, gliukozės į raumenų ir riebalų ląsteles Glikolizė Glikogenezė Lipogenezė Baltymų sintezė + skatina; slopina 10 pav. Insulino poveikis Priešingai insulinui veikia kiti hormonai. Tai gliukagonas, adrenalinas, gliukokortikoidai, augimo hormonas, kurie didina gliukozės koncentraciją. Gliukozės koncentracija kraujyje kaip tik ir priklauso nuo skirtingų hormonų veikimo pusiausvyros. Cukrinis diabetas yra dažniausia endokrininė patologija klinikinėje praktikoje. Ją galima apibrėžti kaip sindromą, kurio svarbiausias požymis yra hiperglikemija dėl absoliučiosios ar santykinės insulino stokos ir (ar) audinių atsparumo insulinui. Sergant cukriniu diabetu, sutrinka visų medžiagų apykaita (13 lentelė). 13 lentelė. Cukrinio diabeto sukeliami medžiagų apykaitos pokyčiai ir požymiai Sutrikusiai Būdinga Požymiai angliavandenių apykaitai hiperglikemija, poliurija, dėl nepakankamo gliukozės gliukozurija polidipsija, naudojimo suintensyvėjus jos išorinių lyties sintezei ir glikogeno skilimo organų niežulys lipidų apykaitai hiperlipidemija, pykinimas, dėl riebalų sintezės slopinimo, hiperketonemija, žiaukčiojimas, suintensyvėjusios lipolizės ir ketonurija, svorio netekimas, padidėjusio ketoninių medžiagų ketoacidozė būdingas acetono susidarymo kvapas iš burnos baltymų apykaitai dėl hiperglikemija, jėgų netekimas, suintensyvėjusio baltymų skilimo gliukozurija, svorio kritimas, bei padidėjusios gliukozės sintezės aminoacidurija, raumenų masės iš aminorūgščių ir sumažėjusios padidėjęs šlapalo netekimas baltymų sintezės kiekis kraujyje Šie pokyčiai ir jų išsivystymo eiliškumas dar geriau matomi schemoje (11 pav., žr. p. 176). Pirminis cukrinis diabetas gali būti klasifikuojamas į nuo insulino priklausomą cukrinį diabetą (I tipo CD) ir į nuo insulino nepriklausomą cukrinį diabetą (II tipo 169
171 CD). Šios klinikinės formos skiriasi epidemiologija, klinikiniais požymiais ir patofiziologija. Antrinis cukrinis diabetas gali išsivystyti dėl kasos bei kitų endokrininių liaukų ligų, pavyzdžiui, esant Kušingo sindromui, nutukimui, hipertonijai, hiperurikemijai, hiperlipoproteinemijai, sergant kepenų, tulžies pūslės, kvėpavimo, šlapimo takų ligomis, esant lėtiniams odos pažeidimams, gydant kai kuriais vaistais. Nuo insulino priklausomas cukrinis diabetas (I tipo CD). Šia cukrinio diabeto forma serga apie 15% visų diabeto ligonių. Jis gali prasidėti bet kuriame amžiuje, bet dažniausiai jauniems 9 14 metų asmenims. Absoliučioji insulino stoka susidaro dėl visiškosios insuliną gaminančių β ląstelių destrukcijos. Galima ir aplinkos veiksnių įtaka, pavyzdžiui, virusinės infekcijos. Antikūnų prieš Langerhanso salelių β ląsteles buvimas kraujo serume yra svarbus diabeto vystymosi žymuo (14 lentelė). 14 lentelė. Nuo insulino priklausomo (I tipo) ir nuo insulino nepriklausomo (II tipo) cukrinio diabeto požymiai Požymis I tipo CD II tipo CD Epidemiologija: dažnumas šiaurės Europoje dominuoja Klinikinė charakteristika: amžius svoris pradžia ketozė endogeninis insulinas susijęs su žmogaus leukocių antigenais antikūnai prieš salelių ląsteles 0,02 04% Tarp šiaurės europiečių <30 m. mažas greita ryški mažai (nėra) taip taip 1 3% (turi tendenciją didėti) Paplitęs visur, rečiau kaimo vietovėse >40 m. normalus ar padidėjęs lėta nėra; galima esant stresui randamas ne ne Patofiziologija etiologija paveldėjimo tipas aplinkos veiksniai kasos salelių β ląstelių autoimuninė destrukcija poligeninis (daugiaveiksnis) virusai, toksinai neaiški, dažnai sutrikusi insulino sekrecija ir rezistencija insulinui monogeninis (?) nutukimas, fizinis nejudrumas Nuo insulino nepriklausomas cukrinis diabetas (II tipo CD). Šia cukrinio diabeto forma serga 85% visų cukriniu diabeto ligonių ir žmonės gali pasiligoti įvairiame amžiuje. Dažniausiai serga metų amžiaus asmenys. Šiam cukriniam diabetui būdinga periferinių audinių atsparumas insulinui, taigi insulino kiekis kraujyje gali būti normalus ar net padidėjęs. Dažniausias klinikinis požymis yra nutukimas. Vėlyvosios cukrinio diabeto komplikacijos. Cukriniam diabetui būdinga ne tik hiperglikemija, bet ir besivystančios komplikacijos: Mikroangiopatijos tai smulkiųjų kraujagyslių sienelių pamatinės membranos sustorėjimas. 170
172 Gliukozės apykaita, cukrinis diabetas ir jo laboratorinė diagnostika Retinopatija, dėl kurios galima apakti (dėl hemoragijų iš proliferuojančių tinklainės kraujagyslių į stiklakūnį), ir makulopatija (dėl eksudacijos iš kraujagyslių ar edemos, kurie ir pažeidžia geltonąją dėmę). Nefropatija lemia inkstų veiklos nepakankamumą. Ankstyvosiose stadijose yra inkstų hiperfunkcija, kuriai būdinga paspartėjusi glomerulų filtracija, padidėję glomerulai ir mikroalbuminurija. Vėlesnėse stadijose proteinurija didėja, blogėja inkstų veikla ir išryškėja uremija. Neuropatija išryškėja viduriavimu, hipotenzija stovint, impotencija, neurogeninėmis šlapimo pūslės ir neuropatinėmis kojų opomis dėl kraujagyslių nervų mikroangiopatijos ir sutrikusios gliukozės apykaitos nervų ląstelėse. Makroangiopatija (ar pagreitėjusi aterosklerozė) lemia priešlaikinę koronarinę širdies ligą. Greičiau besivystančios aterosklerozės patogenezėje svarbiausią vaidmenį atlieka hiperlipidemija ir suintensyvėjęs baltymų glikozilinimas. Dažniausia iš hiperlipidemijų yra hipertriacilglicerolemija, kartu kraujo plazmoje padaugėja labai mažo tankio lipoproteinų cholesterolio ir sumažėja didelio tankio lipoproteinų cholesterolio kiekiai. Apie 60% diabeto ligonių miršta nuo kraujagyslių ligų ir 35% nuo koronarinės širdies ligos. Tarp sergančiųjų diabetu aklumas dažnesnis 25 kartus, o inkstų veiklos nepakankamumas 17 kartų. Api b e n d r i n i m a s Gliukozė yra svarbiausias organizmo angliavandenis; visi kiti angliavandeniai virškinimo metu yra verčiami gliukoze ar absorbuojami. Insulinas mažina gliukozės koncentraciją kraujyje skatindamas gliukozės patekimą į audinius ir glikogeno sintezę. Cukriniam diabetui yra būdinga hiperglikemija, absoliučioji ar santykinė insulino stoka ir vėlyvosios komplikacijos. Nuo insulino priklausoma cukrinio diabeto priežastis yra visiška insulino stoka; juo dažniausiai serga jauni asmenys. Nuo insulino nepriklausomas cukrinis diabetas nustatomas 85% visų diabeto ligonių ir juo serga bet kurio amžiaus asmenys. Vėlyvąsias cukrinio diabeto komplikacijas sukelia mikroangiopatijos ir makroangiopatijos. Kiti būdingi hiperglikemijos požymiai yra šie: troškulys, poliurija, polidipsija, dažnas šlapinimasis, svorio netekimas, išorinių lyties organų niežulys. Šie požymiai būdingi ir I tipo CD, ir II tipo CD. Svarbu prisiminti, kad pradinėse II tipo CD stadijose simptomų gali visai nebūti. 171
173 Cukrinio diabeto diagnostika ir tyrimas Diagnozuoti cukrinį diabetą būtina kuo anksčiau, nes ši ligai gali sukelti sunkių medicininių ir socialinių padarinius. Tuo tikslu yra atliekama nemažai biocheminių tyrimų. Gliukozė šlapime. Gliukozės nustatymas šlapime yra pirmojo pasirinkimo tyrimas. Sveiko žmogaus šlapime gliukozės neturi būti. Jos nebūna, kol gliukozės koncentracija kraujyje neviršija 9 10 mmol/l (inkstų slenkstis gliukozei). Tačiau kai kuriems sveikiems asmenims gliukozė gali pradėti skirtis su šlapimu ir esant mažesnei jos koncentracijai kraujyje. Šių individų inkstų slenkstis gliukozei yra žemas, dėl to išsivysto gliukozurija ir be cukrinio diabeto. Inkstų slenkstis gliukozei didėja su amžiumi, todėl kai kuriems sergantiesiems cukriniu diabetu gliukozurijos gali ir nebūti. Prisimintina, kad gliukozurija dar nėra cukrinio diabeto įrodymas, nes galima inkstų kilmės, alimentinė gliukozurija, taip pat gliukozurija nėštumo metu. Vertinant gliukozės kiekio šlapime tyrimą būtina prisiminti, kad gliukozė šlapime tai suminės glikemijos per šlapimo gamybos laiką rodiklis ir ji neatspindi tikslaus gliukozės kiekio kraujyje tyrimo metu. Gliukozės koncentracijos kraujyje tyrimas. Įprastai gliukozės koncentracija kraujyje matuojama imant jo į mėgintuvėlius su natrio fluoridu (glikolizės inhibitoriumi). Individualiai gliukozės koncentraciją galima nustatyti juostelėmis pagal spalvą. Labai svarbu matavimo procedūrą atlikti tiksliai pagal instrukciją, o smarkiai nukrypęs nuo normos rezultatas turi būti kartotinai įvertintas laboratorijoje. Gliukozės kiekio kraujyje kitimo priežastys yra šios: nuolatinė hiperglikemija: cukrinis diabetas, Kušingo sindromas, akromegalija, nutukimas; laikinoji hiperglikemija: feochromocitoma, sunkios kepenų ligos, ūminė streso reakcija, šokas, traukuliai; nuolatinė hipoglikemija: insulinoma, antinksčių žievės nepakankamumas, neišsivysčiusi kankorėžinė liauka, galaktozemija, ektopinė insulino gamyba navikiniame audinyje; 172
174 Gliukozės apykaita, cukrinis diabetas ir jo laboratorinė diagnostika laikinoji hipoglikemija: didelio alkoholio kiekio suvartojimas iškart, vaistų (salicilatų, vaistų nuo tuberkuliozės), poveikis, sunkios kepenų ligos, kai kurios glikogenozės, funkcinė hipoglikemija, paveldimas gliukozės įsisavinimo sutrikimas. Gliukozės koncentracija kraujyje (atsitiktinis ėminys). Tai tyrimas, atliekamas skubios pagalbos atveju. Jei koncentracija neviršija 8 mmol/l, tai greičiausiai nėra cukrinis diabetas. Jeigu koncentracija viršija 11 mmol/l tai dažniausiai rodo, kad asmuo serga cukriniu diabetu. Gliukozės koncentracija nevalgius. Gliukozės koncentracija matuojama ryte (bent 10 val.) nevalgius. Rekomenduojama gliukozės koncentracija yra (mmol/l): kapiliariniame kraujyje 3, , kraujo serume 4,2 6,1, plazmoje 4,2 6,1. Diagnostikai šis tyrimas yra vertingesnis negu atsitiktinis ėminys. Nesergančiųjų cukriniu diabetu gliukozės koncentracija neviršija 6 mmol/l. Vertinant prisimintina, ar gliukozės koncentracija buvo matuota kraujyje, plazmoje ar kapiliariniame kraujyje. Gliukozės tolerancijos mėginys. Klasikiniu atveju cukrinio diabeto diagnostika remiasi paciento atsako į gliukozės krūvį įvertinimu. Mėginio tyrimo rezultatams gali turėti įtakos daug veiksnių: iki tyrimo suvartotas angliavandenių kiekis, paskutinio valgymo laikas, stresas (pvz., infekcija, chirurginė intervencija), taip pat turi reikšmės amžius, kūno svoris, vartojami vaistai (ypač estrogenai, gliukokortikoidai). O gliukozės toleravimo tyrimo metu asmuo neturi būti įtakojamas tokių veiksnių, kaip nerimas, kava, rūkymas, fizinis aktyvumas, taip pat svarbi kūno padėtis, paros laikas. Taigi prieš tiriant gliukozės toleranciją, būtina: 1) normaliai maitintis 3 dienas ir nekeisti režimo bei vartojamo cukraus kiekio; 2) nevartoti 3 dienas vaistų, veikiančių šią apykaitą: salicilatų, vaistų nuo tuberkuliozės, anoreksinių (apetitą mažinančių), psichostimuliuojamųjų, kontraceptinių (nes į jų sudėtį įeina estrogenas), diuretikų; 3) nerūkyti; 4) tyrimą atlikti ryte nevalgius, ramybės būklės. Bazinis kraujo ėminys atliekamas ryte nevalgius (po nakties badavimo) nustatoma gliukozės koncentracija. Po to pacientui duodama išgerti 75 g gliukozės, ištirpintos 300 ml vandens. Vaikams skiriama 1,75 g gliukozės/kg svorio. Šį kiekį reikia išgerti per 5 min. Po 2 valandų vėl matuojama gliukozės koncentracija kraujyje. Galima kartu tirti ir gliukozės kiekį šlapime: esamu laiku ir po 2 val. Asmuo viso tyrimo metu turi patogiai sėdėti ir, kaip minėta, nerūkyti, nesimankštinti bei iki tyrimo 3 dienas laikytis įprastos dietos. 173
175 Gliukozės tolerancijos mėginiui atlikti yra keletas indikacijų: ribinė gliukozės koncentracija ryte nevalgius ar po valgio, nuolatinė gliukozurija, nėščiųjų gliukozurija, nėščiosios, kurių šeimoje yra sergančiųjų cukriniu diabetu ar kurios prieš tai gimdė didelio svorio naujagimius, ar jei buvo nepaaiškintos persileidimo (vaisiaus netekimo) priežastys. Sveikų asmenų gliukozės tolerancijos mėginio rezultatų reikšmės: gliukozės koncentracija kapiliariniame kraujyje nevalgius 3,33 5,55 mmol/l, po 2 val. 3,33 7,79 mmol/l; gliukozės koncentracija kraujo plazmoje (serume) nevalgius 4,2 6,1 mmol/l, po 1 val. 10 mmol/l; po 2 val. 7,7 mmol/l. Pasaulio sveikatos organizacija (PSO) patvirtino cukrinio diabeto diagnostikos kriterijus remiantis gliukozės nustatymu kraujyje bei gliukozės krūvio (tolerancijos) mėginiu (15 lentelė). Gliukozės tolerancijos mėginio interpretavimas. Asmenims, neturintiems cukrinio diabeto simptomų, tyrimas diagnostine prasme šiai ligai svarbus tada, kai po 2 val. nustatoma padidėjusi gliukozės koncentracija ar kai jos lygis viršija 11 mmol/l bet kuriuo kitu tyrimo registravimo metu. Jei paciento gliukozės koncentracija ryte nevalgius normali ir tik po 2 val. ji pasiekia cukriniam diabetui būdingą lygį, tyrimą reikia kartoti po 6 savaičių. 15 lentelė. PSO cukrinio diabeto ir sutrikusios gliukozės tolerancijos diagnostiniai kriterijai Gliukozės koncentracija (mmol/l) (atsitiktinis ėminys) Tiriamoji medžiaga Cukrinis diabetas Galimas cukrinis Cukrinio diabeto diabetas nėra Veninė plazma Veninis kraujas Kapiliarinė plazma Kapiliarinis kraujas 11,1 0,0 12,2 11,1 5,5 <11,1 4,4 <10,0 5,5 <12,2 4,4 <11,1 <5,5 <4,4 <5,5 <4,4 Standartizuotas gliukozės tolerancijos mėginys (mmol/l) Tiriamoji medžiaga Tyrimo sąlygos Sutrikusi gliukozės Cukrinis diabetas ir laikas tolerancija Veninė plazma Badaujant 7,0 <7,0 Po 2 val. 11,1 7,8 <11,1 Veninis kraujas Badaujant Po 2 val. 6,1 10,0 <6,1 6,7 <10,0 Kapiliarinė plazma Badaujant Po 2 val. 7,0 12,2 <7,0 8,9 <12,2 Kapiliarinis kraujas Badaujant Po 2 val. 6,1 11,1 <6,1 7,8 <11,1 174
176 Gliukozės apykaita, cukrinis diabetas ir jo laboratorinė diagnostikaa Sutrikęs gliukozės toleravimas dar nėra liga. Tai signalas, kad paciento būklė yra tarp normalios ir cukrinio diabeto, t.y. kad yra padidėjusi šios ligos rizika. Tokius asmenis reikia tirti kasmet, turi būti skiriamas gydymas dieta. Ketonai kraujo plazmoje ir šlapime. Cukriniu diabetu sergančiųjų kraujo plazmoje gali pradėti kauptis ketoninės medžiagos (acetonas, acetoacto rūgštis ir β hidroksisviesto rūgštis), rodančios ketoacidozę. Ketoninių medžiagų galima nustatyti ir sveikiems individams, pavyzdžiui, badaujantiems. Tiriant ketonines medžiagas sausomis juostelėmis, nustatoma tik acetoacto rūgštis, bet nenustatoma β hidroksisviesto rūgštis, todėl ketonemijos (ketonurijos) galima ir neaptikti. Ilgalaikė sergančiųjų cukriniu diabetu stebėsena. Esant didelei gliukozės koncentracijai kraujyje, gliukozė nefermentiniu būdu jungiasi prie daugelio baltymų lizino liekanos tai glikozilinimo procesas. Jo laipsnis priklauso nuo gliukozės koncentracijos. Tai negrįžtamas procesas esant fiziologinei vandenilio jonų koncentracijai; gliukozės molekulė lieka prisitvirtinusi prie baltymo, kol jis nesuyra. Taigi glikozilinto baltymo dalis atspindi vidutinį gliukozės kiekį kraujyje to baltymo gyvavimo metu. Glikozilintas hemoglobinas (hemoglobinas A 1C ). Glikozilintas hemoglobinas atspindi vidutinę glikemiją per 1,5 mėnesio iki jos matavimo, t. y. per hemoglobino gyvavimo puslaikį. Šis tyrimas yra geras veiksmingo cukrinio diabeto gydymo efektyvumo rodiklis. Sveikų asmenų glikozilintas hemoglobinas sudaro 4,8 6,0%. Fruktozaminas. Be hemoglobino, glikozilinami ir visi kiti baltymai. Glikozilinimo laipsnį rodo ir fruktozamino kiekio matavimai. Fruktozaminas tai neprisijungusios gliukozės produktas. Kadangi kraujo plazmoje daugiausia yra albuminų, tai glikozilintas albuminas yra svarbiausias serumo fruktozamino šaltinis. Šio baltymo gyvavimo puslaikis yra trumpesnis negu hemoglobino, todėl fruktozamino tyrimas papildo Hb A 1C matavimo duomenis ir suteikia informacijos apie gliukozės kiekį per 3 savaites iki matavimo. Mikroalbuminurija. Terminas apibūdina albumino ekskreciją tarp normalios (2,5 25 mg per dieną) ir makroalbuminurijos (>250 mg per dieną). Paprastu tyrimu juostelėmis tokios albuminų ekskrecijos nustatyti neįmanoma. Tam reikia tikslaus 24 val. šlapimo ėminio tyrimo. Mikroalbuminurija yra ankstyvasis pradinio grįžtamo inkstų pažeidimo rodiklis. Api b e n d r i n i m a s Gliukozės nustatymas šlapime yra pirmučiausias tyrimas. Cukrinis diabetas diagnozuojamas remiantis gliukozės koncentracijos kraujyje tyrimu ar kartu atliekant gliukozės tolerancijos mėginį. 175
177 Asmenims, neturintiems cukrinio diabeto simptomų, gliukozės tolerancijos tyrimas gali rodyti cukrinį diabetą tik kai yra gliukozės koncentracijos padidėjimas po 2 val. ir kai bent viename iš kitų matuotų taškų gliukozės koncentracija yra didesnė negu 11 mmol/l. Glikozilinto hemoglobino (HbA 1c ) ir fruktozamino kiekiai rodo baltymų glikozilinimo laipsnį ir yra svarbūs ilgalaikio cukrinio diabeto gydymo efektyvumo rodikliai. Mikroalbuminurija yra ankstyvos grįžtamos diabetinės nefropatijos požymis. Gliukozės tyrimo rezultatai iš pirmo žvilgsnio gali būti geri ir rodyti efektyvų gydymą, tačiau ne visuomet. Gydytojas turi įvertinti tikrąjį glikemijos lygį atlikdamas glikozilinto hemoglobino ar fruktozamino tyrimą. Diabetinė ketoacidozė Svarbiausi veiksniai, provokuojantys diabetinės ketoacidozės išsivystymą, yra infekcija, miokardo infarktas, trauma, praleista insulino dozė. Visi sutrikimai, išsivystantys diabetinės ketoacidozės metu, yra susiję su insulino stoka (11 pav.). Sumažėjusi gliukozės pernaša į audinius sukelia hiperglikemiją, dėl to atsiranda gliukozurija. Suintensyvėjus lipolizei susidaro riebalų rūgščių perteklius. Jų dalis yra verčiama ke- Insulino stoka Sutrikęs gliukozės patekimas į ląsteles Suintensyvėjusi lipolizė, sutrikęs Krebso ciklas Hiperglikemija Oksaloacetato stoka, sutrikęs Krebso ciklas Padidėjęs laisvųjų riebalų rūgščių kiekis (LRR) Polifagija Gliukozurija Gliukagono perteklius Poliurija Polidipsija Skysčių tūrio sumažėjimas Padidėjusi LRR oksidacija (kepenyse) Diabetinė koma Ketoacidozė 11 pav. Metaboliniai pokyčiai sergant cukriniu diabetu 176
178 Gliukozės apykaita, cukrinis diabetas ir jo laboratorinė diagnostika tonais, dėl to vystosi hiperketonemija, metabolinė acidozė ir ketonurija. Dėl gliukozurijos vystosi osmosinė diurezė, organizmas netenka vandens ir elektrolitų natrio, kalio, kalcio, magnio, fosfatų, chloridų, dėl dehidratacijos prereninė uremija, o tai gali būti hipovoleminio šoko priežastis. Sunki metabolinė acidozė iš dalies yra kompensuojama padidėjusio ventiliacijos greičio (Kusmaulio kvėpavimas). Neretai būdingas vėmimas, kuris dar padidina vandens ir elektrolitų netektį. Taigi vystantis diabetinei ketoacidozei susidaro lyg užburtas ratas, kuris turi būti nutrauktas, kad sunormalėtų angliavandenių ir riebalų apykaita. Laboratoriniai tyrimai. Iš pradžių juostelėmis reikia tirti šlapime gliukozę, ketonines medžiagas, o kraujyje gliukozės koncentraciją. Diagnozei patvirtinti laboratorijoje tiriama gliukozės, natrio, kalio, chloridų, rūgščiųjų karbonatų, šlapalo ir kreatinino koncentracija kraujo serume. Taip pat ištiamos kraujo dujos. Būtina atkreipti dėmesį į kai kuriuos metodologinius laboratorinio tyrimo ypatumus. Ketoninių medžiagų buvimas serume daro įtaką kreatinino koncentracijos matavimui, todėl nustatytas per didelis kreatinino kiekis gali klaidinti (ypač esant ūminei fazei). Patikimai kreatinino kiekis gali būti nustatytas tik kai hiperketonemija išnyksta. Diabetinės ketoacidozės metu gali padidėti α amilazės aktyvumas serume, todėl diferencijuojant nuo pankreatito reikia atkreipti dėmesį į nepraeinantį pilvo skausmą. Gliukozės koncentraciją kraujyje reikia tirti kas valandą prie ligonio lovos, kol ji pasieks 15 mmol/l, o laboratorijoje kas 2 4 val. Kraujo dujų tyrimą per pirmas 4 valandas kartoti kas 2 val., kalio koncentraciją tirti per pirmas 6 valandas kas 2 val., o šlapalo, elektrolitų koncentracijas tirti kas 4 val. Cukrinio diabeto ligoniams gali išsivystyti dar du sunkūs medžiagų apykaitos sutrikimai: hiperosmosinė neketoninė koma ir laktinė acidozė. Hiperosmosinė neketoninė koma dažniau išsivysto vyresniojo amžiaus ligoniams, sergantiems nuo insulino nepriklausomu cukriniu diabetu. Vystosi lėtai, per kelias dienas ar savaites. Organizme insulino kiekis yra pakankamas, kad neišsivystytų ketozė, bet tai neapsaugo nuo hiperglikeminės osmosinės diurezės. Šios būklės dažnesnės vandens netekusiems ligoniams, sergantiems dar ir kita sunkia liga, vartojantiems gliukortikoidų, diuretikų, maitinamiems parenteriniu būdu, dializuojamiems ar po chirurginės intervencijos. Labai didelė gliukozės koncentracija kraujyje (35 50 mmol/l ir daugiau) sukelia dehidrataciją ir dėl to netenkama sąmonės. Laktinė acidozė. I tipo laktinė acidozė išsivysto esant hipoksijai ir perteklinei pieno rūgšties gamybai periferiniuose audiniuose. Hipoksija nebūdinga II tipo laktinei acidozei, kurią sukelia sutrikusi pieno rūgšties apykaita kepenyse. Abiejų tipų laktinei acidozei būdinga sunki metabolinė acidozė, maža ketoninių medžiagų ir didelė laktatų koncentracija kraujyje. 177
179 Api b e n d r i n i m a s Jei sergančiam cukriniu diabetu ligoniui išsivysto diabetinė ketoacidozė, jį būtina tirti ir ieškoti infekcijos, nes tai viena dažniausių minėtos komplikacijos priežasčių. Kraują, šlapimą, skreplius, žaizdų skystį būtina siųsti mikrobiologiniam tyrimui. Diabetinė ketoacidozė išsivysto dėl medžiagų apykaitos sutrikimo esant insulino stokai. Kitos retesnės, tačiau sunkios cukrinio diabeto komplikacijos yra hiperosmosinė neketoninė koma ir laktinė acidozė. Hipoglikemija Hipoglikemija tai laboratorinė diagnozė, kai gliukozės koncentracija kraujyje yra mažesnė negu 2,5 mmol/l. Hipoglikemijos priežastys gali būti įvairios: endokrininės, kepenų ligos, paveldimi medžiagų apykaitos sutrikimai, chirurginės virškinamojo trakto procedūros. Svarbiausia priežastis sutrikusi gliukozės sintezės ir suvartojimo pusiausvyra. Jei gliukozės koncentracija yra mažesnė negu 1,65 mmol/l, tai yra vadinamoji organinė hipoglikemija, o jei viršija 1,65 mmol/l, bet yra mažesnė negu 3,33 mmol/l, funkcinė hipoglikemija. Sumažėjus gliukozės kiekiui kraujyje iki 1,39 mmol/l, gali įvykti kvėpavimo centro paralyžius. Maža gliukozės koncentracija skatina katecholaminų sekreciją, kuria bandoma koreguoti hipoglikemiją slopinant insulino ir skatinant gliukagono, kortizolio ir augimo hormonų sekreciją. Kaip tik katecholaminai sukelia hipoglikemijai būdingus simptomus: prakaitavimą, drebulį, tachikardiją, pykinimą, silpnumą. Dėl hipoglikemijos smegenys yra blogai aprūpinamos gliukoze ir dėl to gali vystytis smegenų pažeidimas, ypač kūdikiams. Laboratorinė diagnostika. Biocheminis tyrimas gali patvirtinti hipoglikemiją ir padėti atrasti priežastį. Tiriama: gliukozės koncentracija kraujyje. Hipoglikemijos diagnostikai tiriamas kraujas (iš šlapimo tyrimo hipoglikemijos nenustatoma); insulino kiekis kraujyje jis gali padėti nustatyti diagnozę ir atmesti insuliną. insulino ir gliukozės santykis gali padėti tiksliau įvertinti insulino kiekį. C peptido nustatymas kraujo plazmoje. Insulinu gydomiems pacientams negalima įvertinti insulino sekrecijos, nes gydymo tikslais gautas insulinas yra taip pat išmatuojamas. Tačiau ir insulinas, ir su juo susijęs C peptidas yra sekretuojami Langerhanso salelių β ląstelių ekvimoliniais kiekiais. Todėl, matuojant C peptido koncentraciją kartu su insulino kiekiu, galima diferencijuoti hipoglikemiją dėl insulinomos (C peptido koncentracija didelė) ir dėl egzogeninio insulino (C peptido koncentracija maža). 178
180 Gliukozės apykaita, cukrinis diabetas ir jo laboratorinė diagnostika Hipoglikemijos priežastys. Hipoglikemija cukrinio diabeto ligoniams išsivysto dėl šių priežasčių: nepakankamo angliavandenių vartojimo, per didelės insulino dozės, fizinės įtampos (mankštinantis), per didelis alkoholio kiekio suvartojimo. Kitos hipoglikemijos priežastys: hipoglikemija dėl badavimo ir hipoglikemija kaip atsakas į stimulą (reakcinė hipoglikemija). Hipoglikemija badaujant. Jos priežastys yra šios: insulinoma. Kasos Langerhanso salelių β ląstelių navikai gali gaminti per daug insulino. Šie navikai dažnai yra gerybiniai arba gali būti dauginio endokrininio neoplastinio sindromo dalis, kai navikas yra ne mažiau kaip dviejose endokrininėse liaukose. Esant insulinomai, hipoglikemija atsiranda badaujant. Diagnostika remiasi hipoglikemijos nustatymu, kai serumo insulino koncentracija didelė; vėžys. Hipoglikemija yra susijusi su toli pažengusiu piktybiniu procesu; kepenų ligos. Nors kepenyse yra didelės glikogeno atsargos, jų pažeidimas gali sukelti hipoglikemiją; Adisono liga. Kortizolis didina gliukozės koncentraciją kraujyje; jo ar kitų gliukokortikoidų stoka yra reta hipoglikemijos priežastis; sepsis. Sunki infekcija gali lemti hipoglikemiją, nors mechanizmas iki galo neištirtas. Reakcinė hipoglikemija. Šiuo atveju hipoglikemija išsivysto kaip atsakas į: vaistus: hipoglikemija dėl per didelės insulino dozės yra tokia pat dažna, kaip ir insulinoma. Tuomet svarbu išmatuoti ir insulino, ir C peptido koncentraciją; maistą: hipoglikemija pavalgius. Nemažai asmenų skundžiasi hipoglikemijos simptomais po valgio. Svarbu išmatuoti gliukozės koncentraciją kaip tik tada, kai yra tokių negalavimų. Ši būklė būdinga ligoniams po skrandžio operacijų (greito skrandžio išsituštinimo sindromas). Tai gali būti ir ankstyvas cukrinio diabeto požymis. Kai kuriems asmenims hipoglikemija atsiranda gausiai pavalgius ar, pavyzdžiui, išgėrus gliukozės atliekant gliukozės tolerancijos mėginį dėl per stipraus atsako ir insulino atsipalaidavimo iš ląstelių (idiopatinė hipoglikemija pavalgius); alkoholį: suvartojus per daug alkoholio, po badavimo gali išsivystyti hipoglikemija. Naujagimių hipoglikemija. Nustatyti ir gydyti naujagimių hipoglikemiją yra ypač svarbu, nes yra didelė smegenų pažeidimo rizika. Naujagimių hipoglikemijos priežastys yra šios: 179
181 cukriniu diabetu sergančių motinų vaikai. Vaisiaus, kurį veikia motinos hiperglikemija, organizme vystosi kasos salelių β ląstelių hiperplazija ir dėl to padidėja insulino sekrecija. Po gimimo naujagimio organizmas nesugeba slopinti per didelės insulino gamybos ir dėl to vystosi hipoglikemija; intrauterinio augimo sulėtėjimas. Smulkūs pagal savo amžių naujagimiai ir kūdikiai neturi pakankamų glikogeno atsargų kepenyse. Ši būklė ypač sunki gimusiųjų prieš laiką, nes glikogenas pradedamas sintetinti per paskutiniąsias keturias nėštumo savaites; paveldimos medžiagų apykaitos ligos. Dažniausios jų yra galaktozemija ir glikogeno kaupimo ligos (glikogenozė), kurioms būdinga hipoglikemija. Api b e n d r i n i m a s Hipoglikemija tai ne diagnozė, bet požymis, susijęs su kai kuriomis patologinėmis būklėmis. Gydymui skiriama gliukozės neatsižvelgiant į priežastį. Dažniausios cukrinio diabeto ligonių hipoglikemijos priežastys yra insulino perteklius, per didelis alkoholio ar nekaloringo maisto vartojimas. Insulinomai būdinga hipoglikemija, esant didelei insulino koncentracijai plazmoje. Hipoglikemija gali pažeisti naujagimių smegenis. Laboratoriniai tyrimai C peptidas Tiriamoji medžiaga. Serumas. Rekomenduojama reikšmė pmol/l (1,1 5 ng/ml). Diagnostinė vertė. Insulinoma, kasos ar β ląstelių transplantacija, geriamųjų hipoglikeminių vaistų vartojimas, inkstų nepakankamumas, nuo insulino nepriklausomas (II tipo) cukrinis diabetas. Hipoglikemija vartojant insuliną, radikalus kasos pašalinimas, nuo insulino priklausomas (I tipo) cukrinis diabetas. Kitos indikacijos: β ląstelių funkcijos ir endogeninės insulino sekrecijos vertinimas, kai skiriama egzogeninio insulino ar kai cirkuliuojantys antikūnai prieš insuliną trukdo nustatyti insuliną. C peptido tyrimas prieš ir po stimuliacijos gliukagonu gali padėti vertinant cukrinio diabeto gydymą insulinu. Papildoma informacija. Nustatyta stipri koreliacija tarp insulino ir C peptido kiekio serume. C peptidas yra biologiškai neaktyvus. Insulinas nesukelia kryžminės reakcijos nustatant C peptidą, o proinsulinas gali reaguoti, tačiau jis sudaro <1% C peptido kiekio. Serume molinis santykis C peptidas/insulinas yra >5 dėl ilgesnio C peptido gyvavimo puslaikio, palyginti su insulinu (atitinkamai 20 min. ir 5 10 min.). Be to, insulinas metabolizuojamas kepenyse, o C peptido didžiausias kiekis suskaidomas inkstuose ir iš dalies šalinamas su šlapimu. V: geriamieji kontraceptikai. 180
182 Gliukozės apykaita, cukrinis diabetas ir jo laboratorinė diagnostika Fruktozaminas Tiriamoji medžiaga. Serumas. Rekomenduojama reikšmė. <285 µmol/l. Diagnostinė vertė. Fruktozaminas atspindi vidutinę gliukozės koncentraciją kraujyje per paskutines 2 3 savaites, o glikozilintas hemoglobinas per 4 6 savaites. Tyrimas naudojamas sergančiųjų cukriniu diabetu trumpalaikei gliukozės koncentracijos kontrolei. Papildoma informacija. Fruktozamino terminas apibūdina serumo baltymus, kurie buvo glikozilinti. Tai yra gliukozės jungimosi prie serumo baltymų (albumino) nefermentinės reakcijos produktai. Ch: bilirubinas, triacilgliceroliai. Ch: askorbo rūgštis. Glikozilintas hemoglobinas (Hemoglobinas A 1C, Hb A 1C ) Tiriamoji medžiaga. Kraujas (EDTA). Rekomenduojama reikšmė. 4,8 6,0% (bendrojo Hb). Diagnostinė vertė. Esant hiperglikemijai glikozilinto hemoglobino per eritrocitų gyvavimo trukmę (120 dienų) daugėja. Papildoma informacija. Tyrimas vertingas ne tik cukrinio diabeto diagnostikai, bet ypač ilgalaikei gydymo kontrolei. Glikozilintas hemoglobinas rodo vidutinę kraujo gliukozės koncentraciją per paskutines 4 8 savaites. Glikozilinto hemoglobino susidarymas yra negrįžtamas procesas, todėl keturių savaičių laikotarpis gali būti per mažas, kad būtų galima spręsti apie tinkamą gydymą. V: hidrochlortiazidas, karbamilintas hemoglobinas (susidaro esant uremijai), morfinas, propranololis. Gliukozė Tiriamoji medžiaga. Serumas (plazma). Rekomenduojama reikšmė (mmol/l): naujagimių 1 d. 2,2 2,3 >1 d. 2,8 4,4; vaikų 3,3 5,6; suaugusiųjų 4,2 6, Tiriamoji medžiaga. Kapiliarinis kraujas (heparinas). Rekomenduojama reikšmė. 3,33 5,55 mmol/l. Diagnostinė vertė. Pirminė priežastis: cukrinis diabetas (jauniems ir suaugusiems individuams). Fiziologinės priežastys: intensyvūs fiziniai pratimai, emocinis susijaudinimas, padidėjęs adrenalino kiekis po injekcijų, šoko, nudegimų, infekcijos (ne visada). Endokrininės priežastys: feochromocitoma, tirotoksikozė, akromegalija, gigantizmas, Kušingo sindromas, gliukagonoma, somatostatinoma. Kasos ligos: ūminis ir lėtinis pankreatitas, pankreatitas dėl tymų, cistinė fibrozė, hemochromatozė, kasos navikas. Kitos priežastys: smegenų kraujotakos sutrikimas, ūminis miokardo infarktas ar krūtinės angina, lėtinės kepenų ligos, lėtinės inkstų ligos. Susijusios su antikūnais prieš insulino receptorius: acanthosis nigricans. B 1 vitamino stoka: Vernikės (Wernicke) encefalopatija. Kasos ligos: salelių ląstelių navikas, gliukagono stoka. Navikai: antinksčių vėžys, skrandžio vėžys, fibrosarkoma. Sunkios kepenų ligos: apsinuodijimas (pvz., arsenu, anglies tetrachloridu, chloroformu, fosforu, alkoholiu, salicilatais, fenforminu, antihistamininiais vaistais). Endokrininės ligos: hipofizės hipofunkcija, Adisono liga, hipotirozė. 181
183 Funkciniai sutrikimai: po gastrektomijos, gastroenterostomijos, esant autonominės nervų sistemos sutrikimams. Anomalijos vaikų amžiuje: prieš laiką gimęs, sergančios cukriniu diabetu motinos kūdikis, ketoninė hipoglikemija. Fermentų stokos ligos: Gyrkės (von Gierke) sindromas, galaktozemija, klevo lapų sirupo liga, fruktozės netoleravimas. Papildoma informacija. Kraujo gliukozės koncentracija sudaro 90% plazmos gliukozės. Gliukozės koncentracija yra didesnė arteriniame negu veniniame kraujyje. Jei hematokritas > 55%, gliukozės kiekio tyrimo rezultatai mažesni, o jei < 35% didesni. Neselektyvieji β adrenoblokatoriai (pvz., propranololis) sutrikdo glikogenolizę ir hiperglikeminį atsaką į endogeninį adrenaliną; dėl to hipoglikemija gali ilgai laikytis, o sveikimas sulėtėti. V: adrenalinas, β adrenerginiai agonistai, AKTH, diuretikai (pvz., furozemidas, tiazidai, triamterenas, chlortalidonas, etakrino rūgštis), estrogenai, dopaminas, fenotiazinai, fruktozė, gliukagonas, indometacinas, kofeinas, kalcitoninas, kortikosteroidai, morfinas, nikotino rūgštis (didelės dozės), geriamieji kontraceptikai, rifampinas, somatostatinas, teofilinas, D tiroksinas. V: acetaminofenas (toksinės dozės), β adrenoblokatoriai, anaboliniai steroidai (diabetikams), antihistamininiai vaistai, aspirinas (toksinės dozės), bezafibratas, etanolis, guanetidino analogai, indometacinas (galimas įvairus poveikis), kaptoprilis, marihuana, monoaminookisdazės (MAO) inhibitoriai, nifedipinas, spironolaktonas Tiriamoji medžiaga. Šlapimas. Tirti tuoj pat reagentų juostelėmis Rekomenduojama reikšmė. Neturi būti. Diagnostinė vertė. Bet kuri gliukozės kraujyje didėjimo priežastis, labai greita absorbcija iš žarnyno (po gastrektomijos, esant normaliam nėštumui), endokrininės ligos (cukrinis diabetas, tirotoksikozė, gigantizmas, akromegalija, Kušingo sindromas, antinksčių hiperplazija); sunki trauma, insultas, miokardo infarktas, kolapsas, gydymas geriamaisiais steroidais, nudegimai, infekcija, feochromocitoma. Sumažėjęs inkstų slenkstis: kanalėlių intersticinės ligos. Papildoma informacija. Reagentų juostelės gali rodyti ir klaidingai neigiamą rezultatą, jei yra sumažėjęs šlapimo ph ir padidėjusi ketonų bei druskų koncentracija. Sergančiųjų cukriniu diabetu inkstų slenkstis gliukozei yra padidėjęs (>13,9 mmol/). Didelis santykinis tankis slopina reagentų juostelių spalvos ryškumą, o mažas santykinis tankis ją intensyvina. Ilgai laikant šlapimą kambario temperatūroje gliukozės koncentracija mažėja dėl glikolizės esant mikrobiniam užterštumui. Santykinis tankis >1,020 ir padidėjęs ph mažina jautrumą ir dėl to gliukozės koncentracija yra klaidingai maža. Klaidingai neigiamas rezultatas galimas naudojant natrio fluoridą kaip konservantą. V: D tiroksinas, diuretikai (pvz., chlortalidonas, etakrino rūgštis, furozemidas, tiazidai), EDTA, karbamazepinas, gliukokortikoidai, ličio karbonatas, nikotino rūgštis, vaikų apsinuodijimas švinu. Ch: hipochloritas, detergentai, naudojami indams plauti, vandenilio peroksidas. Ch: askorbo rūgštis, aspirinas, gyvsidabriniai diuretikai, levadopa, tetraciklinas su askorbo rūgštimi Tiriamoji medžiaga. Smegenų skystis. Rekomenduojama reikšmė. 2,2 3,9 mmol/l. Diagnostinė vertė. Diabetinė hiperglikemija, epideminis encefalitas, centrinės nervų sistemos sifilis, padidėjęs gliukozės kiekis kraujyje. Subarachnoidinė hemoragija, nebakterinis meningoencefalitas. Ūminis piogeninis meningitas, tuberkuliozinis meningitas, kriptokokinis meningitas, pirminis amebinis meningoencefalitas, encefalitas dėl tymų, pirminis ar metastazinis smegenų dangalų navikas, sarkoidozė. 182
184 Gliukozės apykaita, cukrinis diabetas ir jo laboratorinė diagnostika Papildoma informacija. Esant piogeniniam meningitui, gliukozės koncnetracija greitai normalėja pradėjus gydymą antibiotikais. Ilgiau laikant smegenų skystį kambario temperatūroje gliukozės koncentracija mažėja dėl glikolizės, esant mikrobiniam užterštumui. Gliukozės tolerancijos mėginys Tiriamoji medžiaga. Kapiliarinis kraujas. Suaugusiesiems duodama išgerti 75 g gliukozės; nėščioms moterims 100 g gliukozės, vaikams 1,75 g/kg kūno svorio. Tyrimas atliekamas 2 kartus: nevalgius ir po 2 val. išgėrus gliukozės. Rekomenduojama reikšmė. Suaugusiųjų: nevalgius 3,33 5,55 mmol/l; po 2 val. 3,33 <7,79 mmol/l. Diagnostinė vertė. Cukrinis diabetas. Gliukozės koncentracija po 2 val. turi būti 11,1 mmol/l tiriant daugiau negu vieną kartą. Nevalgius gliukozės koncentracija turi būti 6,1 mmol/l. Sutrikęs gliukozės toleravimas. Nevalgius gliukozės kiekis turėtų būti < 6,1 mmol/l, po 2 val. 7,8 11,1 mmol/l. Toleravimas. Sumažėjusi gliukozės absorbcija iš virškinamojo trakto: virškinamojo trakto ligos (celiakija, spru), antinksčių nepakankamumas (pvz., Adisono liga, hipofizės hipofunkcija), hipotirozė. Padidėjusi insulino sekrecija: kasos salelių ląstelių navikas ar hiperplazija. Toleravimas. Padidėjusi gliukozės absorbcija iš virškinamojo trakto: hipertirozė, gastrektomija, gastroenterostomija, vagotomija, per didelis gliukozės vartojimas. Sumažėjęs gliukozės sunaudojimas audiniuose: cukrinis diabetas, centrinės nervų sistemos pažeidimas, hiperlipidemija, hemochromatozė, Kušingo sindromas. Sumažėjusi glikogenezė (suintensyvėjusi glikogenolizė ir gliukoneogenezė): sunkios kepenų ligos, Gyrkės liga, hipertirozė, stresas, infekcijos, feochromocitoma, nėštumas. Papildoma informacija. Tyrimą galima atlikti ambulatoriškai. Tyrimo metu pacientas gali lengvai vaikščioti. Tyrimą pradėti iki 10 val. ryto. Gliukozės tolerancijos mėginys nerekomenduojamas numatant cukrinio diabeto komplikacijas. Suaugusiems individams ir vaikams mėginys nerekomenduojamas kaip atrankinis cukrinio diabeto rizikai įvertinti, tačiau gali būti naudojamas nėščių moterų atrankinei patikrai. Tiesioginiam rezultatų vertinimui pacientą būtina parengti. Pacientas turi pakankamai valgyti, nepatirti streso (neturi būti neseniai atliktos chirurginės procedūros, neseniai persirgtos infekcinės ar kitos ligos), turi būti ištirtos kitos endokrininės funkcijos (antinksčių, skydliaukės, augimo hormono), nuolat vartojami vaistai gali būti tęsiami. Rekomenduojama prieš tyrimą val. nevalgyti. Per šį laiką negerti kavos ir nerūkyti. Toleranciją: aspirinas (mažos dozės), fenforminas, fenobarbitalis, kofeinas, klofibratas, metforminas, nifedipinas, prazocinas. Toleranciją: β adrenoblokatoriai (pvz., propranololis), cimetidinas, diuretikai (pvz., tiazidai, etakrino rūgštis), estrogenai, heroinas, kalcitoninas, katecholaminai, gliukokortikoidai, metadonas, nifedipinas (diabetikams), geriamieji kontraceptikai, salicilatai (didelės dozės), skydliaukės hormonai. Insulinas Tiriamoji medžiaga. Serumas. Rekomenduojama reikšmė pmol/l (6 29,1 mu/ml). Diagnostinė vertė. Insulinoma (kasos salelių navikas), nuo insulino nepriklausomas cukrinis diabetas (II tipo), kepenų ligos, akromegalija, Kušingo sindromas, šeiminis fruktozės ir galaktozės netoleravimas, nutukimas, slaptas insulino ar geriamųjų hipoglikeminių medžiagų vartojimas. 183
185 Nuo insulino priklausomas cukrinis diabetas (I tipo), hipofizės hipofunkcija. Papildoma informacija. Klinikine prasme insulino kiekio matavimas nėra labai vertingas rodiklis, išskyrus badavimo hipoglikemijos diagnostiką. Esant badavimo hipoglikemijai ir didelei serumo insulino koncentracijai, galima įtarti insulinomą. V: aminorūgštys, chlorpropamidas, fruktozė, gliukagonas, gliukozė, augimo hormonas, levadopa (gydant parkinsonizmą), nikotino rūgštis (didelės dozės), geriamieji kontraceptikai, pankreoziminas (į veną), fentolaminas (infuzijos), prednizolonas, chinidinas, sekretinas (į veną), spironolaktonas, sacharozė, tolazamidas, tolbutamidas. V: β adrenoblokatoriai (pvz., propranololis), asparaginazė, bezafibratas, kalcitoninas, chlorpropamidas (kai didelė pradinė koncentracija), cimetidinas, klofibratas, etakrino rūgštis, etanolis, eteris, furozemidas, metforminas, nifedipinas, fenforminas, fenobarbitalis, fenitoinas, tiazidiniai diuretikai. Ketoninės medžiagos (acetoacetatas) Tiriamoji medžiaga. Šlapimas. Nustatoma reagentų juostelėmis. Rekomenduojama reikšmė. Neturi būti. Diagnostinė vertė. Diabetinė ketoacidozė, insulino perteklius gydant diabetą, ilgas badavimas (ketoninė hipoglikemija, dažnesnė 1 6 metų amžiaus vaikams), angliavandenių stoka maiste esant normaliam riebalų vartojimui (svorį mažinančios dietos), nervinė anoreksija, pasikartojantis vėmimas, glikogeno kaupimo ligos (I, III VI tipo), šakotųjų grandinių ketonurija, metilmalono acidurija, netreniruotų asmenų intensyvi fizinė mankšta; nėštumas, stresas, po anestezijos. Būklės, kai: 1) suintensyvėja apykaita (pvz., aukšta temperatūra, sunki tirotoksikozė, aktyvi akromegalija); 2) augimo hormono, kortikotropino, gliukokortikoidų, insulino perteklius; 3) katecholaminų perteklius ir dėl to išsivysčiusi hiperglikemija; sumažėjusi insulino sekrecija; padidėjusi ketoninių medžiagų gamyba. Šie sutrikimai labai ryškūs, jei yra ir cukrinis diabetas. Diabetinei ketoacidozei geriausias klinikinės būklės indikatorius yra β hidroksisviesto rūgšties vyraujančio ketono nustatymas (lyginant su acetoacetatu). Papildoma informacija. β hidroksisviesto rūgštis yra vyraujantis ketonas, tačiau jis nėra matuojamas reagentų juostelėmis. Klaidingai teigiamas rezultatas galimas, kai šlapime daug pigmentų. V: apsinuodijimas aspirinu, etanolis, fenforminas, inozitolis, izopropanolis, metforminas, metioninas, nikotino rūgštis, valproinė rūgštis. 184
186 BILIRUBINO APYKAITA, JOS LABORATORINIAI RODIKLIAI IR KITIMAS SERGANT GELTA Viena iš svarbiausių eritrocitų funkcijų yra nešti su krauju hemoglobiną (Hb), o šis perneša deguonį ir anglies dioksidą. Šią funkciją eritrocitai geriausiai atlieka esant 34% Hb tirpalui, o hemoglobino funkcinį aktyvumą lemia medžiagų apykaita. Žmogaus organizme yra grupė sudėtingųjų baltymų hemoproteinų, kurių prostetinę grupę sudaro hemas. Hemas tai protoporfirino IX ir geležies darinys. Yra daug porfirinų rūšių, bet tik keletas jų randama žmogaus organizme ir tik trys yra kliniškai svarbūs: uroporfirinas, koproporfirinas ir protoporfirinas IX. Žinomos keturios izomerinės jų formos, bet gamtoje randami tik I ir III izomerai. Protoporfirino IX pirmtakas kaip tik ir yra porfirino III izomeras. Hemo turintys junginiai yra hemoglobinas, mioglobinas, kai kurios oksidoreduktazės katalazė, citochromai, glutationperoksidazė. Yrant šiems junginiams atsipalaiduoja hemas, o jo irimo produktas yra bilirubinas. Kasdien žmogaus organizme pagaminama apie mg bilirubino % bilirubino susidaro yrant hemoglobinui, o kita dalis (15 30%) kitiems hemo turintiems junginiams mioglobinui, citochromams, katalazei, peroksidazei; apie 1 2% bilirubino susidaro yrant nesubrendusiems eritrocitams kaulų čiulpuose. Eritrocitų gyvavimo trukmė ir suirimas Subrendusios ląstelės nuolat ýra ir turi būti pakeistos naujomis. Kasdien pagaminama apie 20 mililitrų eritrocitų, t. y. 0,85 jų bendros masės (apskaičiuota pagal tulžies pigmentų ekskreciją). Suaugusio žmogaus organizme kas valandą pagaminama eritrocitų. Žinduolių eritrocitai neturi branduolio, apykaita juose neintensyvi. Jie yra vieni iš nedaugelio gana ilgai gyvuojančių organizmo ląstelių. Eritrocitų gyvavimo trukmė buvo matuojama įvairiais būdais. Izotopais žymint aminorūgštis buvo apskaičiuota eritrocitų gyvavimo trukmė: pavyzdžiui, žmogaus 126±7 dienos, šunų 107 dienos, kačių ir triušių 68 dienos. Kitais metodais nustatyta eritrocitų gyvavimo trukmė dienų. Kai eritrocitai išnykdavo iš kraujo, 15 N žymė buvo randama tulžies pigmentuose. Eritrocitų irimą (žūtį) lemiantys veiksniai yra neaiškūs. Tikriausiai senstantys eritrocitai, kurių paviršiaus receptorių struktūra pasikeičia, tampa jautresni fagocitozei. 185
187 Esant patologijai, kai eritrocitai pažeisti ir sutrumpėja jų gyvavimo trukmė, eritrocitų šalinimo būdas priklauso nuo pažeidimo: jei pažeidimas nedidelis, tai eritrocitai daugiausia fagocituojami blužnyje, o jei didelis ir kepenyse. Taigi dieną atsipalaidavusius iš kaulų čiulpų eritrocitus fagocituoja kaulų čiulpų, blužnies, kepenų makrofagai ir kitų organų mononuklearinės fagocitinės sistemos (anksčiau vadintos retikuloendoteline sistema RES) ląstelės. Kai eritrocitai pradeda irti periferiniame kraujyje (intravazinė hemolizė), iš jų atsipalaidavusį hemoglobiną tuoj pat sujungia kraujyje esantis baltymas haptoglobinas (Hp). Jis padeda organizmui išlaikyti geležį ir kitus junginius, t. y. jie nepasišalina per inkstus. Tokie Hb Hp kompleksai greitai fagocituojami makrofagų ir atitinkami fermentai pradeda skaidyti hemoglobiną (12 pav.). 12 pav. Bilirubino apykaitos schema 186
188 Bilirubino apykaita, jos laboratoriniai rodikliai... He m o g l o b i n o ka t a b o l i z m a s, bilirubino ir jo ap y k a i t o s pr o d u k t ų su s i d a r y m a s Pirmiausia hemoglobinas skyla į baltymą globiną ir hemą. Globinas yra suardomas iki aminorūgščių, kurios naudojamos ir naujų baltymų sintezei. Hemą veikia mikrosomų hemo oksigenazė. Pastarosios aktyvumui būtinas O 2, citochromo C reduktazė bei NADFH. Reakcijoje pasigamina CO, Fe 2+ ir biliverdinas. Pastarasis yra žalios spalvos pigmentas. Mikrosomų hemo oksigenazė Hemas Biliverdinas + CO + Fe 2+ NADFH, O 2, citochromo C reduktazė Šio fermento substratai taip pat gali būti methemoglobinas, hemoglobino ir haptoglobino, hemoglobino ir hemopeksino kompleksai. Fermentas neveikia hemo, esančio oksihemoglobino, karboksihemoglobino ir mioglobino sudėtyje. Geležis būtina, nes laisvasis porfirinas nėra minėtojo fermento substratas. Daugiausia biliverdino pasigamina mononuklearinės fagocitinės sistemos ląstelėse iš Hb hemo (85 90%). Tačiau ir kitų baltymų, tokių kaip citochromo P 450, triptofanpirolazė, citochromas b 5, katalazė, kurių gyvavimo puslaikis yra 2 50 val., hemą irgi suardo hemo oksigenazė. Kai kurie metalai, pavyzdžiui, kobaltas, skatina šio fermento aktyvumą ir didina citochromo P 450 irimo greitį. Geležį, atsipalaidavusią iš hemo, kraujo plazmos baltymas transferinas perneša į jos kaupimo vietas, pavyzdžiui, į kaulų čiulpus, kur ji panaudojama Hb ir kitų hemoproteinų sintezei. Viena transferino molekulė prisijungia du Fe 3+ atomus. Per parą sveiko žmogaus organizme apie 20 mg geležies panaudojama Hb sintezei gaminantis naujiems eritrocitams. Apie 2/3 šio geležies kiekio gaunama iš suirusių eritrocitų šaltinio ir tik nedaug (apie 1 mg per dieną) iš organizmo pasišalina su šlapimu ir prakaitu. Veikiamas fermento biliverdinreduktazės biliverdinas redukuojamas į bilirubiną (Bi). Tai citoplazmos mononuklearinės fagocitinės sistemos ląstelių fermentas, kurio aktyvumui būtinas kofermentas NADFH. Biliverdinas Biliverdinreduktazė NADFH Bilirubinas Dėl stipraus grįžtamojo ryšio su albuminu laisvojo bilirubino koncentracija kraujyje yra labai maža. Tačiau tai labai svarbi frakcija, nes gali pereiti hematoencefalinį barjerą, ypač naujagimių. Bilirubinas iš ekstrahepatinių mononuklearinės fagocitinės sistemos ląstelių su krauju nešamas į kepenis (hepatocitus). Kadangi jis netirpus, kraujyje sudaro kompleksą su albuminais, kuris yra gana patvarus (tačiau grįžtamasis); jo nepraleidžia 187
189 inkstai ir normaliai šio bilirubino (nekonjuguotojo, netiesioginio, laisvojo) šlapime nėra. 1 g albuminų sudaro kompleksą su 3 moliais (22,5 mg) bilirubino. Kraujo plazmoje bilirubinas su albuminu sąveikauja dviejose vietose, t. y. albuminuose egzistuoja dvi sujungimo zonos. Dėl pirmojo sujungimo centro bilirubinas konkuruoja su laisvosiomis riebalų rūgštimis (jų daug, pavyzdžiui, motinos piene), o dėl antrojo su kitais anijonais, pavyzdžiui, salicilo rūgšties, sulfamilamidų, heparino. Kai visos albuminų surišimo galimybės išnaudotos (tai priklauso ir nuo laisvųjų riebalų rūgščių kiekio), bilirubinas patenka į audinius, pavyzdžiui, į nervinį, ir jį pažeidžia taip išsivysto branduolinė gelta. Laisvojo bilirubino gyvavimo puslaikis yra panašus į albuminų dienų, taigi jo gali likti ilgiau, negu atslūgsta gelta. Bilirubinas į hepatocitą patenka dėl ląstelių paviršiuje esančių receptorių albuminui ir specialių nešančiųjų baltymų. Hepatocituose albuminai yra atskiriami, o bilirubinas konjuguoja su gliukurono rūgštimis. Šią reakciją katalizuoja fermentas bilirubin-uridindifosfat-gliukuroniltransferazė (bilirubin-udf-gliukuroniltransferazė), kurios katalizuojamoje reakcijoje bilirubino šoninės grandinės propiono rūgšties COOH grupė jungiasi su aktyviosios gliukurono rūgšties (UDF-gliukurono rūgšties) formos OH grupe. Taip susidaręs bilirubino monogliukuronidas (monokonjuguotasis bilirubinas) prisijungia dar vieną aktyviąją gliukurono rūgštį ir sudaro bilirubino digliukuronidą (dikonjuguotąjį, arba tiesioginį, bilirubiną) % bilirubino yra prisijunguios po dvi gliukurono rūgšties molekules. Bilirubino konjugatų į kraujo tėkmę patenka nedaug arba jo būna tik pėdsakai. Šie konjugatai (monogliukuronidai ir digliukuronidai) dar vadinami tulžies pigmentais. Tirpūs konjugatai pereina į tulžies kanalėlius ir į tulžį. Gliukokortikoidai slopina šio bilirubino konjugavimą skatinančio fermento aktyvumą, o fenobarbitalis didina. Taigi konjuguodamasis bilirubinas tampa: 1) tirpesnis; 2) sekretuojamas į tulžies takus ir 3) ne toks toksiškas. Van den Bergo reakcija Pirmą kartą bilirubiną kraujo serume nustatė H. van den Bergas (van den Bergh) ir P. Miuleris (Muller). Šie autoriai ištyrė, kad bilirubinas gali reaguoti su diazotinėmis druskomis, pavyzdžiui, diazoto sulfanilo rūgštimi, kuri yra svarbiausias Erlicho diazo reagento komponentas, ir pasigamina dažančioji medžiaga (sulfanilo rūgščiai reaguojant su natrio nitritu susidaro diazofenilsulfo rūgštis). Ši reakcija naudojama bilirubinui nustatyti serume (ji nevyksta su kitais redukuotaisiais produktais, tarp jų ir su biliverdinu). Pridėjus diazoto sulfanilo rūgšties, bilirubino konjugatai nuspalvina kraujo serumą tuoj pat tai tiesioginė van den Bergo reakcija. Šis tiesioginis (konjuguotasis, surištasis) bilirubinas, susidaręs sveiko organizmo hepatocituose, sudarytas iš 70 80% bilirubino digliukuronidų, dar vadinamų tulžies pigmentu II, ir 20 30% bilirubino monogliukuronidų tulžies pigmento I. Pastarojo daugėja sergant Žilbero (Gilbert) ir Kriglerio Nadžaro (Crigler Najjar) gelta. 188
190 Bilirubino apykaita, jos laboratoriniai rodikliai... Nekonjuguotasis, o tik tvirtai prisijungęs prie kraujo plazmos baltymų, bilirubinas su šiuo reagentu reaguoja įpylus etilo alkoholio, todėl reakcija vadinama netiesiogine van den Bergo reakcija, ir toks bilirubinas netiesioginiu (nekonjuguotuoju, nesurištuoju, laisvuoju) bilirubinu. Sveiko suaugusio žmogaus kraujyje tokio bilirubino yra apie 75%, t. y. mažiau negu 15,7 µmol/l. Nekonjuguotasis (netiesioginis) bilirubinas yra stipriai susijungęs su plazmos albuminais, jis nedisocijuoja ir šlapime jo nerandama. Bilirubino konjugatai labai silpnai sąveikauja su plazmos baltymais, jie pereina inkstų filtrą ir, kai jų daug kraujo plazmoje, pasirodo šlapime. Ilgai vyravo nuomonė, kad tiesioginis bilirubinas yra ta pati medžiaga kaip konjuguotasis bilirubinas, netiesioginis bilirubinas yra nekonjuguotasis jo atitikmuo, o bendrasis bilirubinas yra sudarytas iš konjuguotosios ir nekonjuguotosios formų. Ne taip seniai nustatyta, kad kraujo serume yra keturių rūšių bilirubino. Tiesiogiai reaguojantis bilirubinas sudarytas iš monokonjuguotojo, dikonjuguotojo bilirubino ir delta frakcijos tai bilirubinas, stipriai (kovalentiškai) susijungęs su kraujo plazmos albuminais. Nekonjuguotasis (netiesioginis) bilirubinas su diazo reagentu reaguoja netiesiogiai, t. y. tik įdėjus akceleratoriaus, pavyzdžiui, alkoholio ar kofeino. Kadangi literatūroje galima aptikti daug įvairių bilirubino pavadinimų, tai pateikiami kai kurie šių junginių sinonimai (16 lentelė). 16 lentelė. Bilirubino junginių sinonimai Nekonjuguotasis bilirubinas Netiesioginis bilirubinas Hemobilirubinas (randamas kraujyje) Laisvasis bilirubinas Konjuguotasis bilirubinas Tiesioginis bilirubinas Cholebilirubinas (randamas tulžyje) Silpnai surištieji bilirubino mono- ir digliuguronidai Cheminės bilirubino savybės pateikiamos 17 lentelėje. 17 lentelė. Cheminės bilirubino savybės Savybės Konjuguotasis (tiesioginis) bilirubinas Nekonjuguotasis (netiesioginis) bilirubinas Struktūra Bilirubino digliukuronidas Bilirubinas, susijungęs su albuminais Sąveikos tipas Polinis Nepolinis Tirpumas: vandenyje alkoholyje van den Bergo reakcija Tiesioginė Netiesioginė Polinkis jungtis su smegenų audiniu (afiniškumas) + + Silpnas + Stiprus kernicterus (bilirubino kaupimasis smegenų pamatiniuose nerviniuose mazguose) galimas tik esant labai dideliam netiesioginio bilirubino kiekiui. 189
191 Svarbi bilirubino savybė yra ta, kad jis netirpsta vandenyje, o tirpsta daugelyje nepolinių tirpiklių. Kristalografiniais bilirubino molekulės tyrimais patvirtintos dvi svarbios struktūrinės jos savybės: 1) dvigubųjų jungčių Z Z (trans) struktūra tarp 4, 5 ir 15, 16 anglies atomų, 2) susuktojo vandenilinio ryšio struktūra, kuria propiono rūgšties karboksilinės grupės yra prijungtos prie pirolo žiedo azoto. Šviesoje bilirubino Z Z struktūra virsta E E (cis) ir kitomis struktūromis. Toks bilirubinas negali turėti minėtojo vandenilinio ryšio ir dėl tokios struktūros geriau tirpsta vandenyje, greičiau šalinamas su šlapimu negu su Z Z struktūros bilirubinas. Tuo grindžiamas naujagimių, turinčių ryškią geltą, švitinimas ultravioletine šviesa, nes dėl jos poveikio nekonjuguotasis bilirubinas tampa tirpesnis ir greičiau pašalinamas iš organizmo per inkstus. Rekomenduojamos bilirubino koncentracijos reikšmės Sveiko suaugusio žmogaus kraujo serume bendroji bilirubino koncentracija yra <17,1 µmol/l % šio kiekio sudaro nekonjuguotasis (netiesioginis) bilirubinas. Bilirubino koncentracijos priklausomybė nuo žmogaus amžiaus pateikiama 18 lentelėje. 18 lentelė. Bilirubino koncentracijos normos ir priklausomybė nuo amžiaus Bilirubinas Bendrasis bilirubino kiekis: Amniono skystis 28 savaitę 40 savaitę Koncentracija (µmol/l) 1,28 0,43 Naujagimių: neišnešiotųjų gimusiųjų laiku Kraujo serumas iš virkštelės <34,2 <34,2 Naujagimių kraujo serumas: Iki 1 dienos 1 2 dienų 3 5 dienų >5 dienos <137 <205 <274 <34,2 <103 <137 <205 3,4 17,1 Suaugusiųjų kraujo serumas: bendrasis bilirubino kiekis konjuguotasis nekonjuguotasis Šlapimas 5 21 <5,3 <15,7 Nėra Esant patologijai, kai bilirubino susidaro daugiau arba sutrinka jo šalinimas, jo kiekis kraujyje padidėja. Jei bilirubino kiekis kraujo serume viršija 34,2 µmol/l, pageltonuoja odena bei odos paviršius (icterus) susergama gelta. Bilirubino kitimas žarnyne Žarnyne bilirubino konjugatus hidrolizuoja žarnyno bakterijos jų β gliukuronidazė atskelia gliukurono rūgštį, o paskui bilirubinas, katalizuojamas reduktazės, virs- 190
192 Bilirubino apykaita, jos laboratoriniai rodikliai... ta bespalviu urobilinogenu (prisijungia vandenilio jonai). Tai plonųjų žarnų, arba tikrasis, urobilinogenas. Bilinogenai (urobilinogenas, mezobilinogenas, sterkobilinogenas) yra bespalviai tol, kol yra oksiduojami veikiant oro deguoniui ir virsta bilinais spalvotais junginiais. Apie 20% urobilinogeno rezorbuojama į vartų venos sistemą (enterohepatinė cirkuliacija) ir vėl patenka į hepatocitus (žr. 12 pav.). Juose, vienų autorių teigimu, dalis urobilinogeno skaidoma iki dipirolų, o kiti autoriai (dauguma) nurodo, kad rezorbuotas urobilinogenas verčiamas bilirubinu ir vėl išskiriamas į tulžį. Taigi, jei hepatocitai nepažeisti ir funkcionuoja normaliai, urobilinogeno kraujyje ir šlapime nerandama. Patekęs į kraują, pavyzdžiui, esant pažeistai hepatocito membranai, šis urobilinogenas skiriasi su šlapimu tai tikrasis, arba plonųjų žarnų, urobilinogenas. Likęs didžiausias urobilinogeno kiekis žarnyne, toliau veikiant žarnyno bakterijų dehidrogenazėms, redukuojamas į sterkobilinogeną (prisijungia 4H + ). Nedidelė dalis sterkobilinogeno gali būti rezorbuojama per storosios žarnos sienelę į apatinių tiesiosios žarnos venų sistemą ir po to į apatinę tuščiąją veną; iš čia jis nunešamas į inkstus, lengvai filtruojasi ir išsiskiria su šlapimu. Išsiskyrusi su šlapimu ši medžiaga turi keletą sinoniminių pavadinimų: tai sterkobilinogenas, storųjų žarnų, arba netikrasis, urobilinogenas, urosterkobilinogenas (su šlapimu besiskiriantis sterkobilinogenas). Kasdien apie 2% į enterohepatinę kraujo cirkulaciją per tiesiosios žarnos venas patekusio sterkobilinogeno (netikrojo urobilinogeno) išskiriama su šlapimu (apie 1 2 mg). Per parą su išmatomis pašalinama mg sterkobilinogeno ir sterkobilino. Urobilinogenas ir sterkobilinogenas ore oksiduojami į urobiliną ir sterkobiliną oranžinį gelsvai raudoną pigmentą, kuris ir nudažo šlapimą bei išmatas jiems būdinga spalva. Bilirubino apykaita organizme Sveiko vyro litre kraujo yra g, moters g Hb. Eritrocitai gyvuoja dienų, taigi per parą yra suardoma apie 6,25 g Hb. Hemoglobino molekulę sudaro 96% baltymo ir 4% hemo. Vadinasi, per 24 val. suyra apie 250 mg hemo. Per parą iš įvairių šaltinių susidaro mg bilirubino, kurio 85% yra iš suirusių eritrocitų, kiti 15% pasigamina iš suirusių eritrocitų pirmtakų kaulų čiulpuose bei vykstant mioglobino, citochromų, katalazės katabolizmui. Su išmatomis ir šlapimu pasišalina apie mg sterkobilinogeno ir sterkobilino. Jeigu tarsime, kad nėra didelio skirtumo tarp hemo (564), bilirubino (552) ir sterkobilinogeno molekulinių masių, tai iš pateiktų duomenų bus aišku, kad organizme suirę porfirino žiedo produktai beveik visiškai pašalinami. Naujieji porfirinai nuolat sintetinami eritrocituose, hepatocituose ir kituose organuose iš aminorūgšties glicino ir sukcinil- KoA, susidarančio Krebso cikle. 191
193 Bilirubino kraujo serume ir šlapime tyrimas Bilirubino kraujo serume nustatymo metodai Kolorimetriniai metodai. Dauguma šių metodų remiasi van den Bergo reakcija su diazo reagentu. Ji, kaip jau minėta, vyksta dviem stadijomis. Taip galima nustatyti reakcijos pobūdį: tiesioginė, netiesioginė, sulėtėjusi. Dabar labiausiai paplitęs kaip tik šiai grupei priklausantis metodas, kurio principus aprašė L. Jendrasikas (Jendrassik) ir P. Grofas (Grof). Juo galima nustatyti bendrojo ir konjuguotojo bilirubinų kiekį, o iš jų skirtumo apskaičiuoti ir nekonjuguotojo (netiesioginio) bilirubino koncentraciją. Jendrasiko Grofo diazo reakcija pagrįstu metodu gauti rezultatai gerai sutampa su rezultatais, gautais chromatografiniais metodais. Spektrofotometriniai metodai. Jie grindžiami tuo, kad bilirubinas sugeria nm ilgio bangas. Chromatografiniai metodai. Didelio slėgio chromatografija yra tiksliausias nekonjuguotojo, monokonjuguotojo ir dikonjuguotojo bilirubino nustatymo metodas, tačiau techniškai jis nėra tinkamas klinikinei laboratorijai, nes reikalinga brangi ir sudėtinga aparatūra. Bilirubino šlapime nustatymas. Kokybinis bilirubino šlapime (tai konjuguotasis bilirubinas, arba tulžies pigmentai) nustatymas yra vertingas geltos diferencinės diagnostikos rodiklis. Dažniausiai naudojamos juostelės, impregnuotos diazo reagentu. Jomis šlapime galima nustatyti 85,5 µmol/l bilirubino koncentraciją. Tai specifinė reakcija, kurios jautrumą gali sumažinti askorbo rūgštis, nitritai. Netikslaus bilirubino kiekio nustatymo priežastys. Vaistai ar kitos medžiagos, kurios nudažo šlapimą raudona spalva ar suteikia jam raudoną spalvą rūgščioje aplinkoje, pavyzdžiui, fenazopiridinas, gali būti klaidingai teigiamos reakcijos priežastis. Didelis askorbo rūgšties kiekis, taip pat nitritai mažina reakcijos jautrumą. Klinikinė urobilinurijos reikšmė. Urobilinurija, kai su šlapimu skiriasi urobilinogenas (tikrasis, arba plonųjų žarnų), yra būdingas kepenų ląstelių pažeidimo rodiklis. Ji esti sergant parenchiminiu hepatitu, kepenų ciroze, esant apsinuodijimui, sepsiui, nėštumo toksikozei, hemolizei. Tada sutrinka rezorbuoto urobilinogeno sulaikymas hepatocituose. Sergant širdies ligomis, urobilinurija yra ankstyvasis stazės kepenyse rodiklis ir rodo dešinės širdies pusės dekompensaciją. Urobilinuriją dėl sterkobilinurijos, kai su šlapimu skiriasi urosterkobilinogenas (netikrasis, arba storosios žarnos), sukelia: 1) padidėjęs sterkobilinogeno susidarymas dėl hemolizės, kraujavimo iš vidaus organų, hemoraginės diatezės, Werlhofo ligos; 2) padidėjęs sterkobilinogeno išskyrimas storosios žarnos venų rezginiuose dėl lėtinio vidurių užkietėjimo, žarnų nepraeinamumo, enterokolito. Bilirubino apykaitos sutrikimai Toliau tekste pateikiama viena geltos tipų klasifikacijos schema. 192
194 Bilirubino apykaita, jos laboratoriniai rodikliai... Geltų klasifikacija (pagal pažaidos tipą ir vietą) Hiperbilirubinemija dėl nekonjuguotojo (netiesioginio) bilirubino koncentracijos padidėjimo kraujo serume Padidėjęs nekonjuguotojo (netiesioginio) bilirubino susidarymas iš hemo Hemolizė: Paveldima; Įgyta. Neefektyvi eritropoezė. Padidėjusios eritrocitų masės greita apykaita (naujagimiai). Sumažėjusi nekonjuguotojo (netiesioginio) bilirubino pernaša su krauju į hepatocitus Dešinės širdies pusės nepakankamumas. Portokavalinis šuntas. Sumažėjusi nekonjuguotojo (netiesioginio) bilirubino pernaša per hepatocito membraną Konkurencinis inhibavimas: Vaistai; Žilbero sindromas? Sepsis, badavimas? Sumažėjęs nekonjuguotojo (netiesioginio) bilirubino kaupimasis citoplazmoje Konkurencinis inhibavimas. Karščiavimas. Sumažėjęs konjugavimas Naujagimių gelta (fiziologinė). Inhibavimas vaistais. Paveldima (Kriglerio Nadžaro sindromas); I tipo (visiška fermento stoka); II tipo (dalinė fermento stoka). Kepenų ląstelių funkcijos sutrikimas. Žilbero sindromas. Hiperbilirubinemija dėl konjuguotojo (tiesioginio) bilirubino kiekio padidėjimo kraujo serume Sumažėjusi konjuguotojo (tiesioginio) bilirubino sekrecija tulžies kanalėliuose Hepatocitų patologija: Hepatitas; Cholestazė (intrahepatinė). Dabino Džonsono ir Rotoro sindromai. Vaistai (estradiolis) Sumažėjęs nutekėjimas Ekstrahepatinė obstrukcija: Akmenys; Navikai (vėžys); Susiaurėjimas; Atrezija; Pirminis sklerozuojantis cholangitas. Intrahepatinė obstrukcija: Vaistai; Granulomos; Pirminė biliarinė cirozė; Navikai. 193
195 Sergant daugeliu ligų, gali sutrikti vienas ar daugiau bilirubino susidarymo, apykaitos ir ekskrecijos etapų. Priklausomai nuo pažeidimo, hiperbilirubinemijos priežastys gali būti nekonjuguotojo (netiesioginio), konjuguotojo (tiesioginio) ar abiejų tipų bilirubino koncentracijų padidėjimas kraujo serume. Hiperbilirubinemija dė l ne k o n j u g u o t o j o (netiesioginio) bilirubino koncentracijos padidėjimo kraujo serume Dažniausiai nekonjuguotojo bilirubino padaugėja naujagimiams, ir tai yra fiziologinė naujagimių gelta. Visų naujagimių kraujo serume nekonjuguotojo (netiesioginio) bilirubino kiekis viršija sveikų suaugusiųjų reikšmes. Dažniausiai pirmomis 48 valandomis po gimimo jis pakyla iki 103 µmol/l (neišnešiotų naujagimių iki 137 µmol/l ir retais atvejais gali siekti 171 µmol/l), didžiausias būna 3 5 dieną po gimimo ir sunormalėja per 7 10 dienų. Laikino nekonjuguotojo bilirubino padaugėjimo kraujyje priežastys yra šios: 1) padidėjęs bilirubino susidarymas dėl embrioninės megaloblastinės kraujodaros sistemos elementų irimo; 2) bilirubino apykaitoje ir ekskrecijoje dalyvaujančių fermentinių sistemų nepakankamas aktyvumas (nesubrendimas), pavyzdžiui, bilirubin-udf-gliukuroniltransferazė pradeda gamintis tik gimus. Suintensyvėjusi eritrocitų hemolizė (esant hemolizinei anemijai) ir neefektyvi eritropoezė taip pat yra hiperbilirubinemijos priežastys. Kepenų pažaida nebūdinga. Bendrasis bilirubinų kiekis kraujo serume paprastai neviršija 70 µmol/l vyrauja nekonjuguotoji jo forma. Esant retam paveldimajam I ir II tipo Kriglerio Nadžaro (Crigler Najjar) sindromui visai nėra bilirubin-udf-gliukuroniltransferazės arba jos aktyvumas būna labai sumažėjęs. Dažnesnis yra kitas paveldimasis Žilbero (Gilbert) sindromas tai heterogeninė patologija, kuriai būdingas sumažėjęs minėto fermento aktyvumas; tačiau ligą taip pat gali lemti ir pernašos per membraną defektas. Sergant I tipo Kriglerio Nadžaro sindromu, šio fermento visai nesusidaro, o II tipui būdingas sumažėjęs, bet kepenų audinyje išmatuojamas bilirubin-udf-gliukuroniltransferazės aktyvumas. Kadangi sergant minėtomis ligomis bilirubinas negali būti konjuguojamas normaliu greičiu, tai jo ekskrecija labai sumažėja, o nekonjuguotojo (netiesioginio) bilirubino koncentracija kraujyje padidėja. Sergant I tipo Kriglerio Nadžaro sindromu, bendroji bilirubinų koncentracija paprastai siekia µmol/l. Tokie pacientai anksti miršta dėl išsivysčiusio kernicterus (bilirubinas nudažo smegenų pamatinius nervinius mazgus). Esant II tipo Kriglerio Nadžaro bei Žilbero sindromams, bendroji bilirubinų koncentracija kraujo serume paprastai neviršija atitinkamai 342 µmol/l ir 51,3 µmol/l. Tuomet prognozė yra gera. 194
196 Bilirubino apykaita, jos laboratoriniai rodikliai... Hiperbilirubinemija dė l ko n j u g u o t o j o (tiesioginio) bilirubino kiekio padidėjimo kraujo serume Sergant tulžies sistemos ligomis (klasikiniu atveju pažeisti hepatocitai esant parenchiminiam hepatitui), sutrinka bilirubino patekimas į hepatocitus, kaupimasis juose ir ekskrecija. Šioms ligoms būdinga įvairiai padidėjusi ir konjuguotojo (tiesioginio), ir nekonjuguotojo (netiesioginio) bilirubino koncentracija kraujo serume. Kai kurioje nors tulžies takų sistemos vietoje atsiranda kliūtis, visiškai ar iš dalies sutrikdanti tulžies nutekėjimą, kraujo plazmoje padidėja įvairių tulžies sudedamųjų dalių kiekiai (konjuguotojo bilirubino, cholesterolio, γ glutamiltransferazės, šarminės fosfatazės) ir atsiranda tulžies rūgščių. Be to, tulžies takų obstrukcija ir tulžies nutekėjimo sutrikimas skatina kai kurių fermentų (γ glutamiltransferazės ir šarminės fosfatazės) sintezę, ir tai dar labiau padidina šių medžiagų koncentraciją kraujyje. Kai kurių vaistų, lytinių hormonų sukelta cholestazė, taip pat tam tikru mastu alkoholinis hepatitas ir ūminis virusinis hepatitas yra dažniausios intrahepatinės cholestazės priežastys. Patologinis procesas šiais atvejais pažeidžia smulkiuosius tulžies latakus, o stambieji latakai lieka sveiki. Esant mechaninei tulžies takų obstrukcijai (kasos galvos vėžys, bendrojo tulžies latako vėžys, tulžies pūslės akmenligė, kasos galvos fibrozė ir kt.) kraujyje smarkiai padidėja konjuguotojo bilirubino kiekis. Dabino Džonsono (Dubin Johnson) sindromas tai reta gerybinė bilirubino ekskrecijos patologija. Bilirubinas normaliai patenka į hepatocitą, yra konjuguojamas, bet sutrinka šio bilirubino ekskrecija į tulžies takus. Būdingas požymis hepatocituose kaupiasi pigmentinės granulės. Dažniausiai tokių ligonių kraujyje bendrasis bilirubinų kiekis svyruoja nuo 34,2 iki 85,5 µmol/l (vyrauja konjuguotoji jo forma). Kliniškai panašus yra Rotoro (Rotor) sindromas, tačiau šiuo atveju hepatocituose nebūna pigmentinių granulių. Delta hiperbilirubinemija Delta bilirubinas tai bilirubino forma, kuri kovalentiškai yra susijungusi su albuminais. Sveikų asmenų kraujyje šios formos nėra. Taip pat ji nebūdinga naujagimių fiziologinei geltai, Žilbero sindromui ir hemolizinei geltai. Ši susijungusio su albuminais bilirubino frakcija randama suaugusiųjų, vaikų ar naujagimių kraujyje tik sutrikus konjuguotojo bilirubino ekskrecijai iš hepatocitų. Sveikstant delta bilirubinas sudaro didesnę bendrąją bilirubinų dalį, nes jis lėčiau šalinamas iš kraujo. Ilgesnis šio bilirubino gyvavimo puslaikis ir tai, kad jo neišsiskiria su šlapimu, paaiškina, kodėl ligonių, sergančių kepenų ligomis ir hiperbilirubinemija, bilirubino kiekis šlapime yra normalus. Toliau tekste pateikiami bilirubino apykaitos sutrikimai sergant dažniausiai pasitaikančių tipų gelta (19 lentelė). 195
197 19 lentelė. Geltos tipų klasifikacija ir bilirubino apykaitos rodikliai Bilirubino apykaitos reikšmė Hiperbilirubinemijos klasifikacija Defektas Etiologijos pavyzdžiai serumo Bi (konjuguotojo bilirubino dalis iš bendro Bi), % šlapimo bilirubinas urobi linogenas sterkobilinogenas Hiperbilirubinemija dėl nekonjuguotojo (netiesioginio) bilirubino kiekio padidėjimo Prehepatinė Bi hiperprodukcija Hemolizė Hematoma <20 ( ) Hepatinė Sutrikusi pernaša iš kraujo į hepatocitą Žilbero sindromas # Kai kurie toksinai <20 N N Nesugebėjimas konjuguoti Kriglerio Nadžaro sindromas Naujagimių gelta Kai kurie vaistai (pvz., novobiocinas) <20 N N Hiperbilirubinemija dėl konjuguotojo (tiesioginio) bilirubino kiekio padidėjimo Hepatinė Hepatoceliulinė Hepatocitų pažeidimas Virusinis ar toksinis hepatitas cirozė, alkoholinis hepatitas, kitos hepatocitų pažeidimo priežastys >40 + N, ar Hepatokanalikulinė Intrahepatinė cholestazė dėl pažeistos konjuguotojo bilirubino pernašos į tulžies kanalėlius Kai kurie vaistai (pvz., anaboliniai steroidai, chlorpromazinas), virusinis hepatitas, pirminė biliarinė cirozė. Kai kurios šeiminės geltos formos >50 + N, ar Posthepatinė Tulžies nutekėjimo sutrikimas Kasos ar bendrojo tulžies latako vėžys. Tulžies takų akmenligė. Kitos mechaninės tulžies nutekėjimo sutrikimo priežastys >50 + Rodyklės rodo kitimų pobūdį. Rodyklė skliaustuose reiškia, kad pakitimas gali būti arba jo nebūti. N norma, padidėjęs, sumažėjęs, + reakcija teigiama arba yra. Normaliai šlapime randama labai nedaug urobilinogeno. Sveikų asmenų išmatose sterkobilinogeno kiekis labai įvairus. Šalinant daugiau negu 250 mg per dieną, kiekis yra padidėjęs, o mažiau negu 5 mg per dieną sumažėjęs. # Gali būti sutrikęs ir konjugavimas. Bi bilirubinas. 196
198 Bilirubino apykaita, jos laboratoriniai rodikliai... Pa r e n c h i m i n ė ge l t a Esant parenchiminei geltai (pvz., sergant virusiniu hepatitu), sutrinka kepenų ląstelių gebėjimas: 1) konjuguoti bilirubiną su gliukurono rūgštimi, 2) išskirti konjuguotąjį (tiesioginį) bilirubiną į tulžies takus, 3) sulaikyti ir vėl išskirti ar perdirbti urobilinogeną. Ląstelėse vyksta destrukciniai nekroziniai pakitimai, atsiranda uždegiminis (infiltracinis) stromos pažeidimas. Dėl to sulėtėja, tirštėja tulžies tėkmė, padidėja spaudimas tulžies takuose, sutrinka bilirubino ekskrecija iš kepenų ląstelių į tulžies takus. Iš suirusių nekrozinių ląstelių konjuguotasis bilirubinas patenka į kraujo kapiliarus. Matyt, sutrinka ir fermentinė konjuguotojo bilirubino pernaša per kepenų ląstelių membraną. Kraujyje randama konjuguotojo bilirubino. Kuo labiau sutrikusi bilirubino ekskrecija į tulžies takus, tuo didesnė bilirubino gliukuronidų koncentracija kraujyje. Gliukurono rūgšties buvimas lemia geresnį konjuguotojo bilirubino tirpumą, jis lengviau pereina inkstus ir išsiskiria su šlapimu tai tulžies pigmentai šlapime. Pastarieji nudažo šlapimą rudai raudona spalva. Ilgai laikomo ore šlapimo bilirubinas oksiduojasi į biliverdiną, ir šlapimas įgauna žaliai rusvą spalvą. Tulžies pigmentų šlapime šaltinis yra tik kraujyje esantis konjuguotasis (tiesioginis) bilirubinas. Tulžies pigmentai šlapime pasirodo tik padidėjus kraujyje konjuguotojo bilirubino koncentracijai daugiau kaip 27,4 34,2 µmol/l. Tai vadinamasis inkstų slenkstis konjuguotajam bilirubinui, o mažesnės šios medžiagos koncentracijos neaptinkamos galbūt dėl per mažo metodo jautrumo. Ne visas konjuguotasis bilirubinas, patekęs į kraują, išsiskiria su šlapimu, dalį jo sulaiko kraujas, kiti audiniai. Todėl nėra proporcingumo tarp didėjančios konjuguotojo bilirubino koncentracijos kraujyje ir atsirandančių tulžies pigmentų šlapime. Konjuguotojo bilirubino koncentracija kraujyje yra vertingesnis rodiklis negu bilirubino (tulžies pigmentų) kiekis šlapime, nes geriau parodo ekskrecinės kepenų ląstelių funkcijos pažeidimą. Kuo daugiau konjuguotojo bilirubino pateks į kraują, tuo mažiau jo skirsis su tulžimi į žarnyną, mažiau gaminsis urobilinogeno ir sterkobilinogeno (pastarojo išmatose mažės). Vienas ankstyviausių kepenų pažeidimo rodiklių yra sutrikęs jų gebėjimas sulaikyti ir reekskretuoti urobilinogeną, patekusį iš žarnyno. Ši funkcija sutrinka dar iki vystantis geltai. Urobilinogenas (tikrasis) nesulaikomas kepenyse, patenka į kraujo tėkmę ir skiriasi su šlapimu. Išsivysto urobilinurija. Sveiko žmogaus šlapime urobilinogeno (urobilino) nebūna. Didėjant intrahepatinei stazei, mažėja į žarnyną patenkančio bilirubino kiekis, dėl to ir urobilinogeno susidarymas bei reabsorbcija. Tuomet urobilinurija mažėja ir ligos įkarštyje gali visai išnykti. Taigi urobilino mažėjimas šiuo atveju susijęs ne su hepatocitų funkcijos normalėjimu, o su dar didesniu tulžies skyrimo funkcijos sutrikimu. Esant labai sunkiam kepenų parenchimos pažeidimui, išmatose ilgai nebūna sterkobilinogeno (sterkobilino) jos būna šviesios, šlapime neaptinkama urobilino (ti- 197
199 krojo urobilinogeno), kraujyje susidaro didelė konjuguotojo (tiesioginio) bilirubino koncentracija, o šlapime tulžies pigmentų. Tai gali būti pirminiai atrofinio proceso požymiai. Esant dar didesniems kepenų ląstelių pažeidimams, sutrinka fermentinės reakcijos, kurių metu susidaro gliukuronidai. Pradeda vyrauti monogliukuronidai (40 50% ir net 90%), o atitinkamai mažėja digliukuronidų. Keičiasi ir van den Bergo reakcijos greitis. Urobilinogeną sulaikanti kepenų funkcija sunormalėja lėtai. Todėl sveikstant ir mažėjant konjuguotojo bilirubino koncentracijai kraujyje ir daugėjant sterkobilinogeno išmatose, vėl vystosi urobilinurija. Sergant parenchiminiu hepatitu, neretai padidėja ir nekonjuguotojo (netiesioginio) bilirubino koncentracija kraujyje. Tai aiškinama: 1) dideliais destrukciniais ląstelių pokyčiais (sutrinka baltymų sintezės procesai), 2) kepenų ląstelėse dėl stazės susikaupusiu dideliu bilirubino gliukuronidų kiekiu (jie pradeda slopinti bilirubin- UDF-gliukuroniltransferazę). Esant didelei konjuguotojo bilirubino koncentracijai ir vyraujant bilirubino monogliukuronidams, nekonjuguotojo bilirubino koncentracija dažniaisiai didėja lėtai. Tačiau tik esant kepenų atrofijai nekonjuguotojo bilirubino koncentracija gerokai padidėja, o konjuguotojo sumažėja. Nekonjuguotojo bilirubino koncentracijos padidėjimas (per 34,2 µmol/l) sergant parenchimine gelta yra bloga lemiantis požymis. Hemolizinė gelta Ji išsivysto dėl eritrocitų irimo. Kur kas daugiau į kepenis nešama nekonjuguotojo (netiesioginio) bilirubino. Tai lemia tulžies pigmentų kaupimąsi kraujyje tokiu greičiu, kuris viršija kepenų ląstelių gebėjimą jį pašalinti. Kraujyje kaupiasi bilirubinas, prisijungęs prie albuminų, todėl netiesioginė van den Bergo reakcija rodo padidėjusį netiesioginio bilirubino kiekį kraujyje. Bilirubinurijos nėra, nes nekonjuguotasis bilirubinas nepereina inkstų. Jei nėra tulžies stazės, tai kraujyje konjuguotojo bilirubino nedaugėja. Kai į tulžies takus patenka ypač daug konjuguotojo bilirubino, tulžis tirštėja, sulėtėja jos tėkmė, gali iškristi bilirubino druskų kristalai. Tai lemia tulžies stazę ir konjuguotojo bilirubino patekimą į kraują. Tačiau, sergant hemolizine gelta, nekonjuguotojo bilirubino kiekis gerokai viršija konjuguotojo kiekį kraujyje. Kepenys ekskretuoja maksimalų bilirubino konjugatų kiekį, todėl padidėja sterkobilinogeno ir urosterkobilinogeno ekskrecija. Mechaninė gelta Ši gelta atsiranda dėl tulžies takų obstrukcijos: tulžies nepatenka į žarnų spindį, tulžies kapiliarai išsiplečia, vyksta jų destrukcija. Ankstyvosiose ligos stadijose normaliai funkcionuojančios kepenys išskiria į tulžį bilirubino konjugatus. Tačiau 198
200 Bilirubino apykaita, jos laboratoriniai rodikliai... susidariusi tulžis negalėdama nutekėti regurgituoja į kraują ir jame pradeda daugėti konjuguotojo bilirubino (tai rodo tiesioginė van den Bergo reakcija), o šlapime bus tulžies pigmentų. Jei kepenų funkcija nesutrikusi, tai svarbiausias rodiklis ir bus konjuguotojo bilirubino kiekio padidėjimas kraujo serume. Jei yra visiška tulžies takų obstrukcija, tulžies nepatenka į žarnyną, nesigamina sterkobilinogenas (jo nebus išmatose) ir iš jo urosterkobilinogenas (jo nebus šlapime). Kai besitęsianti tulžies takų obstrukcija pažeidžia kepenų ląsteles, tada ir tiesioginio, ir netiesioginio bilirubino kiekis padidės. Išmatos būna molio spalvos (acholiškos), šlapime urosterkobilinogeno nėra ar yra labai mažai, nors daug bilirubino pašalinama su šlapimu. Retai, pavyzdžiui, sergant cholangitu, kai užsikemša tulžies pūslė, atsiranda urobilinurija, nes tulžies pūslėje esanti mikroflora turi dehidrogenazių, kurios bilirubiną redukuoja į urobilinogeną. Su paveldimumu susijusi gelta Jos priežastis genetinės informacijos, atsakingos už fermentų ir baltymų, dalyvaujančių bilirubino apykaitoje, stoka ar pakitimas. Skiriama gelta, susijusi su: 1) bilirubino patekimo į kepenų ląsteles pakitimais (pavyzdys Žilbero sindromas), 2) konjugavimo pakitimais (Kriglerio Nadžaro sindromas), 3) bilirubino gliukuronidų pernašos iš kepenų ląstelių į tulžies takus pakitimais (Dabino Džonsono sindromas). Šie sindromai aptariami skyriuje apie hiperbilirubinemiją dėl nekonjuguotojo ir konjuguotojo bilirubino kiekio padidėjimo. Api b e n d r i n i m a s Skiriamos trys pagrindinės bilirubino koncentracijos padidėjimo kraujyje priežastys: hemolizė, kai hemoglobino irimo produkto bilirubino yra daugiau, nei kepenys geba jo konjuguoti; pažeistas hepatocitas, kuriame nebevyksta konjugavimas; kliūtis tulžiai nutekėti. Kraujyje yra ir konjuguotojo, ir nekonjuguotojo bilirubino. Konjuguotasis bilirubinas vandenyje yra tirpus, o nekonjuguotasis netirpus (jis yra neurotoksiškas) ir sudaro kompleksą su albuminais. Gelta rodo, kad kraujyje yra padidėjusi bilirubino koncentracija. Naujagimiams svarbu nustatyti nekonjuguotojo bilirubino koncentraciją, kad žinotume, kada pradėti gydymą. Dažniausia suaugusiųjų geltos priežastis yra tulžies takų obstrukcija. Jai būdingas ir konjuguotojo bilirubino, ir šarminės fosfatazės padidėjęs kiekis kraujyje. 199
201 Laboratoriniai tyrimai bendrasis Bilirubinas Tiriamoji medžiaga. Serumas (saugoti nuo tiesioginių saulės spindulių). Rekomenduojama reikšmė (<17) µmol/l. Diagnostinė vertė. Hepatocitų pažeidimas (uždegiminis, toksinis, neoplazinis), intrahepatinė ir ekstrahepatinė tulžies takų obstrukcija, hemolizinė liga, naujagimių fiziologinė gelta, Kriglerio Nadžaro sindromas, Žilbero sindromas, Dabino Džonsono sindromas, fruktozės netoleravimas, hipotirozė, praeinanti šeiminė naujagimių hiperbilirubinemija. Papildoma informacija. V: hepatotoksiniai vaistai ir vaistai, sukeliantys cholestazę, hemolizę Tiriamoji medžiaga. Šlapimas (neseniai paimtas, saugoti nuo tiesioginių saulės spindulių). Rekomenduojama reikšmė. Neturi būti. Diagnostinė vertė. Būklės, kurių metu didėja konjuguotojo (tiesioginio) bilirubino (išvardyta pirmiau). Papildoma informacija. Ekstrahepatinių tulžies takų obstrukcija yra klasikinė bilirubinurijos priežastis. Bilirubino ir urobilinogeno nustatymas šlapime yra svarbūs geltos diferencinei diagnostikai. Bilirubinurija būdinga mechaninei ir parenchiminei, bet ne hemolizinei geltai. Naujagimiams ištyrus šlapime bilirubiną, galima anksti diagnozuoti atreziją ir laiku ją gydyti chirurgiškai. Sergant virusiniu hepatitu, bilirubinas šlapime pasirodo anksčiau negu išsivysto gelta. Bilirubino ekskreciją skatina alkalozė. Ch: fenotiazinai, fenazopiridino metabolitai, didelis urobilino, indikano kiekis, vaistų nuo uždegimo metabolitai ar salicilatai gali suteikti geltoną ir net raudoną spalvą. Ch: didelis askorbo rūgšties kiekis, nitritai (esant šlapimo takų infekcijai). konjuguotasis (tiesioginis) Bilirubinas Tiriamoji medžiaga. Serumas (saugoti nuo tiesioginių saulės spindulių). Rekomenduojama reikšmė. <5,3 µmol/l. Diagnostinė vertė. Intrahepatinė ir ekstrahepatinė tulžies takų obstrukcija, hepatocitų pažeidimas, cholestazė (gali būti sukelta vaistų), Dabino Džonsono sindromas, Rotoro sindromas. Papildoma informacija. Įprastais metodais nustatomą šį bilirubiną sudaro konjuguotasis ir δ (delta) bilirubinas. nekonjuguotasis (netiesioginis) Bilirubinas Tiriamoji medžiaga. Serumas (saugoti nuo saulės spindulių). Apskaičiuojamas pagal bendrojo ir konjuguotojo bilirubino kiekį. Rekomenduojama reikšmė. <15,7 µmol/l. Diagnostinė vertė. Hemolizė ar būklės, susijusios su hemoglobino irimu (pvz., didelės besirezorbuojančios hematomos), sveikimo fazė po ūminio hepatito ir sepsio, praeinanti naujagimių hiperbilirubinemija, Žilbero sindromas, Kriglerio Nadžaro sindromas, neefektyvi eritropoezė esant B 12 vitamino, folio rūgšties stokai. 200
202 KEPENYS IR JŲ PAŽEIDIMO LABORATORINĖ DIAGNOSTIKA Kepenų struktūra ir funkcijos Kepenys yra didžiausia žmogaus organizmo liauka. Jų masė yra 1,5 2 kg. Kepenys užima tarpinę vietą tarp vidinės ir išorinės organizmo terpės. Maisto medžiagos iš virškinamojo trakto pirmiausia patenka į kepenis ir ten perdirbamos. Kepenys palaiko baltymų, angliavandenių ir lipidų homeostazę. Hepatocituose vyksta medžiagų apykaitos procesai glikolizė, Krebso ciklas, oksidacinis fosforilinimas, aminorūgščių sintezė, šlapalo sintezė, kraujo baltymų sintezė ir kiti. Be hepatocitų, kepenyse yra mononuklearinės fagocitinės sistemos ląstelės, svarbios kraujo ląstelių gamybai ir ardymui. Hepatocitai metabolizuoja, detoksikuoja ir šalina endogeninės ir egzogeninės kilmės medžiagas. Taigi kepenys yra lyg centrinė organizmo laboratorija. Jungiamasis audinys kepenyse sudaro stromą, suskirstančią kepenų parenchimą į nedideles skilteles, kurių suaugusio žmogaus kepenyse yra apie Kepenų skiltelę sudaro hepatocitai, tarp kurių yra siauri, apie 0,5 1 µm, tarpai tai tulžies takai, kurie pradžioje neturi savo sienos (13 pav.). Hepatocitai, dalyvaujantys susidarant tulžies takams, besiliečiančiuose paviršiuose turi įdubimą. Dviejų hepatocitų sąlyčio vietoje susidaro ertmelė. Nuo šių ertmelių ir prasideda tulžies takai, kurie jungdamiesi sudaro takus tarp skiltelių. Taip iš hepatocito per jo membraną šalinamos medžiagos patenka tiesiai į tulžį. Kraujo kapiliarai ir tulžies takai nesusisiekia, nes juos skiria hepatocitai. Kitas hepatocito paviršius kontaktuoja su krauju pro sinusoidinio kapiliaro sienelę. Sergant kai kuriomis ligomis, kai pažeidžiama hepatocito membrana, tulžis gali iš jo patekti tiesiai į kraują išsivysto gelta. Endotelinė ląstelė Kraujo tėkmė Kupferio ląstelė Hepatocitas Tulžies kapiliaras 13 pav. Kepenų skiltelės schema 201
203 Be hepatocitų, kaip minėta, kepenyse yra endotelinės ir makrofagų tipo mononuklearinės fagocitinės sistemos (anksčiau vadintos retikuloendoteline sistema RES) ląstelės; pastarosios vadinamos Kupferio ląstelėmis. Kupferio ląstelės sandara specifinė: jos turi vakuoles, lizosomas, grūdėtąjį endoplazminį tinklą po visą citoplazmą tai skiria šias ląsteles nuo endotelinių ląstelių. Kupferio ląstelės, kaip ir kiti makrofagai, yra išsivysčiusios iš kaulų čiulpų ląstelių pirmtakų. Šios ląstelės fagocituoja įvairias kraujo medžiagas, todėl jų citoplazmoje galima rasti eritrocitų nuolaužų, hemosiderino, riebalų lašelių ir kt. Hepatocitai yra netaisyklingos daugiakampės formos µm skersmens ląstelės. Jos turi apvalų 6 8 µm dydžio branduolį, o jame yra 1 2 branduolėliai. Apie 20% ląstelių turi 2 branduolius ir tai rodo vykstančius kepenyse regeneracinius procesus. Sergant įvairimis kepenų ligomis, ląstelių su 2 branduoliais padaugėja. Hepatocitų citoplazma pagal jos funkcinę būklę ar distrofinio pažeidimo laipsnį nusidažo bazofiliškai ar šviesiai violetine spalva. Joje daug mitochondrijų. Citoplazmoje yra riebalų lašelių, glikogeno, hemosiderino, B 1 vitamino, kitų medžiagų. Dėl įvairių patologinių procesų pažeisto hepatocito branduolyje ir citoplazmoje atsiranda įvairių pokyčių: chromatinas tampa grublėtas, galimi parachromatino židiniai, branduolys ir branduolėliai padidėja, o degeneracinius citoplazmos pokyčius rodo jos vakuolizacija, riebalinės distrofijos ir kiti požymiai. Kepenys, kaip centrinė organizmo laboratorija, atlieka daug gyvybiškai svarbių funkcijų: I. Medžiagų sintezės funkcija. Parenchiminėse ląstelėse, t. y. hepatocituose, sintetinami: baltymai: visi albuminai (sveikos kepenys per parą pagamina g albuminų), 75 90% α globulinams prilausančių baltymų, 50% β globulinams priklausančių baltymų; γ globulinai sintetinami kitose mononuklearinės fagocitinės sistemos ląstelėse; jei visus kepenyse sintetinamus baltymus prilygintume 100%, tai 10% jų sudarytų albuminai ir 90% globulinai; nebaltyminės medžiagos šlapalas, kreatinas, ketoninės medžiagos ir kitos. II. Detoksikacinė funkcija. Kepenys šalina daug įvairių jose neutralizuojamų medžiagų: vaistų, medžiagų apykaitos produktų, tokių kaip amoniakas; ši funkcija yra glaudžiai susijusi su medžiagų sintezės funkcija, pavyzdžiui, iš toksinio amoniako sintetinamas šlapalas, o bilirubinas iš organizmo šalinamas konjuguojant jį su gliukurono rūgštimi. Ši funkcija yra susijusi ir su kita ekskrecine funkcija. III. Ekskrecinė funkcija. Su tulžimi iš kepenų ir iš organizmo kaip galutiniai medžiagų apykaitos produktai pasišalina iki 40% kietųjų medžiagų, pavyzdžiui, bilirubinas. Didesnė jų dalis žarnyne vėl įsiurbiama. 202
204 Kepenys ir jų pažeidimo laboratorinė diagnostika IV. Sekrecinė funkcija. Hepatocituose sintetinamos ir sekretuojamos tulžies rūgštys. Patekusios į tulžį jos padeda virškinti riebalus. V. Deponavimo funkcija. Kepenyse yra kaupiamas glikogenas, B 12, B 6, PP vitaminai, pantoteno rūgštis. Suaugusio žmogaus kepenys sudaro 2,5% viso kūno svorio (apie 1,5 kg); apie 5% jose tenka glikogenui, apie 5% riebalams (~3% jų sudaro fosfolipidai, ~2% neutralūs riebalai, ~0,5% cholesterolis). Taip pat kepenyse yra kaupiami kalis, natris, kalcis, cinkas, varis, geležis ir naudojami pagal poreikį, pavyzdžiui, varis įeina į ceruloplazmino, citochromo a 3 sudėtį, geležis naudojama hemo sintezei. VI. Kraujodaros funkcija. Kepenyse, kaip minėta, kaupiasi geležis, kuri naudojama hemoglobino sintezei. VII. Vandens apykaitos palaikymo funkcija. 70% kepenų masės sudaro vanduo, 30% sausosios medžiagos, iš jų 50% baltymai. VIII. Onkotinio slėgio reguliavimo funkcija artimai susijusi su vandens apykaitos palaikymo ir kepenų svarba sintetinant įvairias medžiagas, nes albuminai yra svarbiausi šiame reguliavimo mechanizme. IX. Kraujo kiekio kraujagyslėse palaikymo funkcija. Kepenys gali sulaikyti 5 kartus daugiau kraujo, negu jo cirkuliuoja kraujagyslėse. Nukraujavus šis kraujas išmetamas į kraujotaką. Per parą kepenimis prateka apie 2000 litrų kraujo: apie 20% jo patenka pro kepenų arteriją, maždaug 80% pro vartų veną. X. Apsauginė funkcija. Apie 2/3 (70%) kepenų ląstelių sudaro hepatocitai ir apie 1/3 (30%) mezenchiminio audinio ląstelės. Labai nedaug yra jungiamojo audinio, kuris sudaro stromą. Taigi kepenys yra itin svarbios mononuklearinės fagocitinės sistemos ląstelių atžvilgiu, nes jose gaminasi imunoglobulinai (γ globulinai). Kepenų ligų sindromai ir jų laboratorinė diagnostika Pažeidus hepatocitą ir sutrikus jo veiklai, vystosi liga. Norint nustatyti ligą, jos stadiją, skirti gydymą, atliekami laboratoriniai tyrimai; remiantis jų rezultatais įvertinama, kuri hepatocito funkcija yra pažeista ir kaip smarkiai. Kadangi hepatocitas atlieka nemažai jau minėtų funkcijų, tai, joms sutrikus, galimi įvairūs sindromai, t. y. tuomet išryškėja ligos laboratorinių simptomų kompleksai. Svarbiausi yra šie: 1) citolizės sindromas, 2) cholestazės (ekskrecinis biliarinis) sindromas, 3) uždegiminis (mezenchiminis uždegiminis) sindromas, 4) kepenų (hepatocitų) nepakankamumo sindromas. Dėl savo specifinių laboratorinių požymių dar gali būti skiriami: 5) vartų ir tuščiosios venų nuosruvio sindromas, 6) navikinis sindromas. 203
205 Šie pastarieji sindromai yra panašūs į kai kuriuos pagrindinius sindromus. Citolizės sindromas, arba ląstelių pažeidimo sindromas. Šiam sindromui būdingas sutrikęs hepatocitų membranos pralaidumas arba ląstelių distrofiniai pokyčiai iki jų nekrozės. Pažeisti hepatocitą gali virusai, toksinai. Šio sindromo stadijos yra dvi: 1. Biocheminė (iki morfologinių pakitimų) stadija, kai diagnozei svarbiausi yra biocheminiai pokyčiai, dažniausiai pakitęs fermentų aktyvumas. Kepenų biopsija šiuo atveju nebus informatyvi. Tai grįžtamoji pokyčių stadija. 2. Morfologinė stadija. Biochemiškai šių stadijų nebus galima atskirti, bet padės biopsinės medžiagos tyrimas. Citolizės sindromui būdingas pakitęs indikacinių fermentų aktyvumas: aspartataminotransferazės (AST) ir alaninaminotransferazės (ALT). Šių dviejų fermentų svarba ir rezultatų interpretacija skiriasi. Alaninaminotransferazės daugiausia yra ląstelės citoplazmoje. Todėl pažeidus hepatocitą ir pirmiausia pakitus jo membranos pralaidumui, alaninaminotransferazė greitai pereina pažeistą membraną, patenka į tarpląstelinę erdvę ir iš jos į kraują. Aspartataminotransferazės apie 30% yra citoplazmoje ir apie 70% mitochondrijose. Todėl tik esant didesniam hepatocito pažeidimui mitochondrijų fermentas per ląstelės membranas išeina į tarpląstelinę erdvę. Taigi jos aktyvumas padidėja vėliau negu alaninaminotransferazės. Pradinėje ūminio hepatito stadijoje vertingesnis rodiklis yra alaninaminotransferazės kiekio padidėjimas kraujo serume, o padidėjęs aspartataminotransferazės aktyvumas nustatomas patologinio proceso viršūnėje bei rodo hepatocitų pakenkimo sunkumą. Sveikstant aspartataminotransferazės kiekis normalizuojasi vėliau negu alaninaminotransferazės, o procesui perėjus į lėtinį, AST aktyvumas išlieka padidėjęs, ypač ligai paūmėjus. Taigi alaninaminotransferazės kiekis kraujo serume padeda nustatyti: hepatitą, kai ligos stadija ankstyva, begeltes ir slaptąsias ligos formas, ligos sunkumą, įvertinti prognozę, atskirti hepatitą nuo kitų panašios klinikos ligų. Indikaciniams fermentams taip pat priklauso laktatdehidrogenazė ir jos penktasis (LDH-V) izofermentas. Vertinant šių trijų fermentų svarbą citolizės sindromo diagnostikai, jie išsidėsto taip: ALT>AST>LDH. Be šių pagrindinių laboratorinių citolizės sindromo požymių, kraujyje bus padidėjusi geležies, B 12 vitamino koncentracija. Cholestazės sindromas. Šiam sindomui būdingas padidėjęs ekskrecinių fermentų aktyvumas kraujyje. Normaliai ekskreciniai fermentai turi su tulžimi pa- 204
206 Kepenys ir jų pažeidimo laboratorinė diagnostika tekti į virškinamąjį traktą. Esant kliūčiai, tulžis teka priešinga kryptimi ir pro kitą hepatocito membranos pusę patenka į kraują. Tokiai būklei užsitęsus dažniausiai pažeidžiami ir hepatocitai, todėl vėliau prie cholestazės prisidės ir citolizės sindromo požymiai. Svarbiausi ekskreciniai fermentai yra šie: šarminė fosfatazė (bendroji), šarminės fosfatazės izofermentai, ir šiuo atveju svarbiausias yra kepenų izofermentas, g gliutamiltransferazė (GGT). Pastarosios taip pat yra daug endotelinėse ląstelėse. Nedidelės alkoholio dozės indukuoja GGT sintezę. Jei alkoholio dozė didelė, tai prie cholestazės prisidės ir citolizės sindromo požymiai. Šių fermentų kiekio kitimai gali būti įvairūs, ir tai padeda atskirti ligas: a) Jeigu bendros šarminės fosfatazės kiekis padidėja, o GGT aktyvumas išlieka normalus patologijos reikia ieškoti kaulų sistemoje, nes kraujyje didelę dalį bendro šarminės fosfatazės aktyvumo, be kepenų, sudaro kaulų izofermentas. b) Jei padidėja ir šarminės fosfatazės, ir GGT kiekiai, tai būdinga tipiniam cholestazės sindromui. c) Jei padidėja GGT aktyvumas, o šarminės fofatazės kiekis yra normalus gali išsivystyti cholestazės sindromas, nes GGT aktyvumas esant stulžies stazei didėja greičiau negu šarminės fosfatazės. Jeigu nėra alkoholio ar vaistų poveikio, o GGT kiekis yra padidėjęs galimos metastazės, nes joms atsiradus ir didėjant išauga ir GGT aktyvumas. Be šių cholestazės sindromui būdingų fermentų kiekio padidėjimo, nustatomi ir kiti laboratoriniai požymiai: hiperbilirubinemija kraujyje daugėja konjuguotojo (tiesioginio) bilirubino koncentracija; hipercholesterolemija, nes cholesterolis iš organizmo šalinamas su tulžimi; kraujyje daugėja vario ir ceruloplazmino, nes pagrindinis vario šalinimo iš organizmo būdas yra jo ekskrecija su tulžimi, o į hepatocitus vario atneša ceruloplazminas. Uždegiminis (arba mezenchiminis uždegiminis) sindromas. Tai mononuklearinės fagocitinės sistemos ląstelių dirginimo sindromas. Pažeidus hepatocitus ir jiems ýrant, aplinkiniai audiniai yra dirginami ir kaip atsakas vystosi uždegiminė ląstelinė infiltracija. Ląstelės pradeda gaminti daugiau joms būdingų medžiagų, dėl to koloidiniai baltymų mėginiai būna teigiami. Jie charakterizuoja baltymų frakcijų santykio pakitimą. Tokių mėginių yra apie 100 ir dar apie 200 jų modifikacijų. Tačiau net ir buvę populiarūs timolio ir Veltmano mėginiai prarado savo diagnostinę svarbą. 205
207 Dėl ūminių virusinių hepatitų daugėja smulkiadispersių baltymų ir pakinta baltymų frakcijų santykis: daugėja γ globulinų, didėja eritrocitų nusėdimo greitis, vystosi monocitozė. Tiksliausiai baltymų frakcijų santykių pokyčius galima pamatyti atliekant baltymų elektroforezę, kuri ir pakeitė pirmiau minėtus mėginius. Esant šiam sindromui gali daugėti tam tikrų imunoglobulinų, atsiranda antikūnų prieš lygiuosius raumenis, mitochondrijas, branduolius, gali būti teigiamas Kumbso mėginys. Taigi mezenchiminiam uždegiminiam sindromui bus būdingas toks tyrimų kompleksas: baltymų frakcijų tyrimas elektroforezės metodu, imunoglobulinų tyrimas, antikūnų prieš mitochondrijas, lygiuosius raumenis, branduolius nustatymas, Kumbso mėginys. Kepenų nepakankamumo sindromas. Jau pats pavadinimas rodo, kad svarbiausi laboratoriniai šio sindromo požymiai bus susiję su pažeista kepenų geba sintetinti medžiagas, ir pirmiausia kraujyje sumažės tų medžiagų, kurios sintetinamos tik jose. Taigi kepenų nepakankamumo sindromui būdinga: hipoalbuminemija, bendro baltymų kiekio kraujyje sumažėjimas, krešėjimo baltymų protrombino, prokonvertino, fibrinogeno kiekio mažėjimas. Sutrikus krešėjimo funkcijai, kyla kraujavimo pavojus. Nustačius šiam sindromui būdingus laboratorinius rodiklius (o jie būdingi esant smarkiam kepenų pažeidimui ar ligai įsigalėjus), būtina stebėti ligonį, kad neišsivystytų gyvybei pavojingų komlikacijų. Kepenų navikų sindromas. Šis sindromas būdingas kepenyse besivystančiam navikiniam procesui. Dėl suardytos tulžies takų architektūros būdingi cholestazės sindromo požymiai (kraujyje padaugėja šarminės fosfatazės ir jos kepenų izofermentų, GGT), taip pat nustatysime specifinius kepenų vėžio žymenis, pavyzdžiui, α fetoproteinas yra pirminio kepenų vėžio žymuo. Vartų ir tuščiosios venų (portokavalinio) nuosruvio sindromas. Normaliai kraujas iš vartų venos (v. portae) turi pereiti hepatocitų barjerą. Juose sulaikomos ir detoksikuojamos su maistu gautos ar virškinamajame trakte susidariusios medžiagos. Tik po to jos iš hepatocito patenka į apatinę tuščiąją veną (v. cava inferior), t. y. į bendrą kraujotaką. Kai kepenys yra peraugusios jungiamuoju audiniu ar visiškai suirusi jų architektūra, formuojasi nuosruviai, kuriais kraujas iš vartų venos patenka tiesiai į apatinę tuščiąją veną. Taigi ir visos medžiagos, kurios turėjo būti sulaikytos hepatocituose, atsiranda kraujyje. Tai: amoniakas, indikanas, fenoliai, 206
208 Kepenys ir jų pažeidimo laboratorinė diagnostika aminorūgštys, kurios nebūdingos žmogaus organizmui, bet gaunamos su maistu. Kad būtų lengviau nustatyti pirminį pažeidimą, įvairių ligų, pirmiausia kepenų, diagnostikai naudojami šie koeficientai: 1. Geležies ir vario kiekių kraujyje santykis ( ). Sveikų asmenų jis yra 0,8 1,2. Jei santykis didėja (taip būna, kai kraujo serume daugiau geležies), gali būti suardyta hepatocitų struktūra, nes juos pažeidus kaupiama geležis išeina į kraujo plazmą. Susidarant cholestazei santykis mažėja, nes daugėja vario (jo kiekio didėjimas būdingas cholestazei). 2. Aspartataminotransferazės (AST) ir alaninaminotransferazės (ALT) santykis ( ), kuris sveikų asmenų yra 1,33 ± 0,42. Jei santykis didėja, kraujyje didėja AST aktyvumas. Tai būdinga smarkiam hepatocitų pažeidimui ar jau sveikimo tarpsniu, nes tada ALT normalizuojasi greičiau. Galima įtarti ir miokardo infarktą, tik būtina surinkti anamnezę, įvertinti kitus klinikinius požymius. 3. Šmito koeficientas tai aspartataminotransferazės ir alaninaminotransferazės aktyvumų sumos santykis su glutamatdehidrogenazės aktyvumu ( ). Sveikų asmnenų šis santykis yra 20. Esant ūminiam kepenų pažeidimui, santykis didėja ir gali siekti 30 50, o jei procesas lėtinis, santykis sumažėja (10 15). Dažniausios kepenų ligos Jos yra ūminės ir lėtinės. Svarbiausios ūminio kepenų pažeidimo priežastys yra šios: apsinuodijimas, infekcija, nepakankama kraujotaka. Ūminis kepenų nepakankamumas yra būklė, kurią reikia neatidėliojant gydyti, nes dėl jos sutrinka visos metabolinės funkcijos ir jų negali kompensuoti joks kitas organas. Sutrinka elektrolitų, rūgščių ir šarmų pusiausvyra, atsiranda hipoglikemija. Dėl kepenų nepakankamumo gali vystytis ir inkstų nepakankamumas, nes toksinai, kurie turėtų būti neutralizuojami kepenyse, pažeidžia inkstų glomerulus. Kraujyje didėja amoniako koncentracija, nes jis nėra verčiamas šlapalu (šlapalo sintezė vyksta tik kepenyse). Esant ūminiam hepatocitų pažeidimui mažėja albuminų sintezė, vystosi hipoalbuminemija. Dėl to atsiranda edemų ir (ar) ascitas. Sutrikus krešėjimo faktorių sintezei vystosi hemoragijos ar kraujas pradeda krešėti pačiose kraujagyslėse, jei būklė labai sunki. Lėtinis kepenų pažeidimas gali būti alkoholinio kepenų suriebėjimo, lėtinio aktyvaus hepatito, pirminės biliarinės cirozės priežastis. 207
209 Visos šios būklės gali progresuoti iki kepenų cirozės, kuri yra galutinis, dažniausiai negrįžtamas lėtinio kepenų pažeidimo etapas: kepenys susitraukia, sudarkoma jų architektūra, o likusiame audinyje vystosi fibrozė. Dažniausios jos priežastys yra ilgalaikis gausus alkoholio vartojimas (tuomet daugiau gaminama laisvųjų radikalų, kurie skatina kepenų uždegimą, daugiau endotoksinų patenka į kepenis ir taip skatinamas jų pažeidimas), virusinis hepatitas (ypač B hepatitas), autoimuninės ligos, retai paveldima α 1 antitripsino stoka (būdinga vaikams), Vilsono liga (paveldima vario apykaitos liga, kai kraujyje yra mažai ceruloplazmino, dėl to sutrinka vario šalinimas, jis kaupiasi kepenyse ir kituose audiniuose); suaugusiems individams cirozė gali išsivystyti sergant hemochromatoze, kai hepatocituose ar kitų audinių ląstelėse kaupiasi netirpus baltymas hemosiderinas (tai geležies įsotintasis feritinas). Kepenyse dažnai vystosi antrinės metastazės iš pirminių navikų. Gelta dažnas vėžio požymis. Pirminė hepatoma gali išsivystyti sergant ciroze ar hepatitu. Apie kepenų būklę dažniausiai sprendžiama remiantis kraujo serumo biocheminiais tyrimais bilirubino, aminotransferazių, šarminės fosfatazės, g glutamiltransferazės (20 lentelė). 20 lentelė. Kepenų ligų laboratorinė diferencinė diagnostika Kepenų ligos AST ALT GGT ŠF Bendrasis bilirubinas Ūminis virusinis hepatitas (be geltos) Ūminio virusinio hepatito cholestazinė forma Ūminis alkoholinis hepatitas Lėtinis persistentinis hepatitas Lėtinis aktyvus hepatitas ++ iki iki +++ (+) iki ++ (+) iki + N iki iki iki iki N iki (+) iki+ N N iki (+) + iki ++ + iki ++ + iki ++ N iki (+) N iki + Tulžies takų nepraeinamumas: ūminis lėtinis + iki++ N iki + + iki ++ N iki + + iki iki +++ (+) iki ++ N iki + N iki + + iki +++ Kepenų navikai (+) iki + (+) iki iki +++ N iki ++ + padidėjimo laipsnis; N norma. 208
210 Kepenys ir jų pažeidimo laboratorinė diagnostika Api b e n d r i n i m a s Kepenys yra centrinė organizmo laboratorija, atliekanti daug gyvybiškai svarbių funkcijų. Sutrikus bent vienai iš jų atsiranda pokyčių, kuriuos galima nustatyti laboratoriniais tyrimais. Apie kepenų būklę sprendžiama remiantis kraujo serumo biocheminiais tyrimais (bilirubino, aminotransferazių, šarminės fosfatazės, GGT). Kadangi hepatocitas atlieka nemažai funkcijų, joms sutrikus galimi įvairūs sindromai, t. y. ligos laboratorinių simptomų kompleksai. Citolizės sindromui yra būdingas pakitęs indikacinių fermentų aktyvumas, t. y. tų fermentų, kurie normaliai savo funkciją atlieka ląstelėje ir į aplinką patenka tik pažeidus ląstelę. Cholestazės sindromui būdingas ekskrecinių fermentų aktyvumo padidėjimas kraujyje. Normaliai šie fermentai turi su tulžimi patekti į virškinamąjį traktą; susidarius kliūčiai, tulžis teka priešinga kryptimi ir pro kitą hepatocito membranos pusę patenka į kraują. Laboratoriniai pokyčiai sergant uždegiminiu (arba mezenchiminiu uždegiminiu) sindromu išsivysto dėl to, kad pažeistas hepatocitas dirgina aplinkinius audinius ir ląstelės pradeda gaminti daugiau joms būdingų medžiagų. Svarbiausi kepenų nepakankamumo sindromo laboratoriniai požymiai yra susiję su pažeista medžiagų sintezės funkcija kraujyje sumažės tų medžiagų, kurios sintetinamos tik kepenyse. α fetoproteinas yra svarbus pirminio kepenų vėžio žymuo. Kai kepenys yra peraugusios jungiamuoju audiniu ar visiškai suirusi jų architektūra, formuojasi nuosruviai, kuriais kraujas iš vartų venos patenka tiesiai į apatinę tuščiąją veną, todėl kraujyje bus aptinkama medžiagų, kurios normaliai turėtų būti neutralizuojamos kepenyse. Kepenų ligų diagnostika pagal sindromus ypač svarbi mišrių pažeidimų atvejais, nes ji padeda nustatyti, kuris pažeidimas pirminis, ir taip padėti gydytojui apsispręsti dėl gydymo. Specifinei diagnozei biocheminiai tyrimai ne visada padeda. Tiksliai diagnozei reikia atlikti kepenų biopsiją, kurios metu privalu patikrinti paciento kraujo krešėjimo būklę (ji turi būti patenkinama). 209
211 KALCIO IR FOSFORO APYKAITA, JOS SUTRIKIMAI IR LABORATORINĖ DIAGNOSTIKA Kalcio pasiskirstymas organizme. Kalcio homeostazę organizme palaiko trys organai: žarnynas, inkstai ir griaučiai (14 pav.). Laktacijos metu dar svarbios yra pieno liaukos, o nėštumo metu placenta ir vaisius; be to, ir prakaito liaukos reikšmingos šalinant kalcį iš organizmo. Kalcis yra absorbuojamas ir sekretuojamas į žarnyną, o jo absorbcija yra palaikoma tokio paties lygio, kaip ir jo kasdienis šalinimas su šlapimu (2,5 6,2 mmol/24 val.). Kalcio kiekis, kuris yra skystyje už ląstelių ribų, yra labai mažas, palyginus su jo kiekiu kauluose. Tačiau net ir suaugusiųjų kauluose esantis kalcis nėra statiškas: kasdien dalis kaulo yra rezorbuojama ir kalcis sugrįžta į neląstelinį skystį. Tuo pat metu susiformuoja tokia pati naujo kaulo dalis. Iš 1 1,5 kg kalcio, esančio suaugusio žmogaus organizme, 99% yra kauluose, kur jis sudaro hidroksiapatito kristalus tai mineralinis griaučių komponentas. Kasdien į organizmą patenka iki 25 mmol (400 mg) kalcio. Sveiko suaugusio žmogaus kraujyje kalcio yra apie 2,4 mmol/l (2,12 2,6 mmol/l). Naujagimių iki 30 dienų kalcio koncentracija kraujo serume yra 1,75 2,87, o vaikų iki 1 metų 2,15 2,79 mmol/l. Kalcis kraujyje būna trijų formų: 1) laisvasis, arba jonizuotasis, kalcis tai fiziologiškai aktyvi jo forma, kuris sudaro apie 50% bendro kraujo kalcio kiekio (1,05 1,30 mmol/l). Laisvojo (jonizuotojo) kalcio koncentracija yra svarbi palaikant nervų funkciją, membranų pralaidumą, raumenų susitraukimą, liaukų sekreciją, kraujo krešėjimą. Paratiroidinės liaukos reaguoja į sumažėjusią nesujungtojo kalcio koncentraciją ir Maistas (25 mmol) Virškinamasis traktas 10 mmol 5 mmol Neląstelinis skystis (20 mmol) (plazmoje 2,4 mmol/l) Kaulai mmol 8 mmol 8 mmol Išmatos (20 mmol) Šlapimas 5 mmol Ląstelės 300 mmol 14 pav. Kalcio homeostazė 210
212 Kalcio ir fosforo apykaita, jos sutrikimai... jų parathormonas šią koncentraciją padidina, kaip ir D 3 vitamino aktyvioji forma, o mažina kalcitoninas; taigi pastovią kalcio koncentraciją palaiko visi trys hormonai; 2) sudaręs kompleksus su įvairiais anijonais, svarbiausia fosfatų, citrato; ši forma sudaro apie 5% bendro kraujo kalcio kiekio; 3) susijungęs su kraujo plazmos baltymais, svarbiausia albuminu; tokio yra apie 45%. Sujungimas priklauso nuo ph ir mažėja esant acidozei, nes albumino aminorūgščių šoninės grandinės turi teigiamą krūvį. Ir atvirkščiai sujungimas didėja esant alkalozei. Taigi, nesujungtojo kalcio procentas didėja esant acidozei ir mažėja esant alkalozei. Fosforo pasiskirstymas organizme. Fosforo homeostazę organizme palaiko trys organai: plonoji žarna, inkstai ir griaučiai. (Kliniškai pasakymas fosforo koncentracija gali būti keičiamas fosfatų koncentracija.) Fosforo organizme yra daug, apie g (išmatuoto kaip neorganinis fosforas) % jo įeina į griaučių sudėtį kaip hidroksiapatitas, o kita dalis pasiskirsto visuose audiniuose ir skysčiuose tai svarbus ląstelinis ir neląstelinis anijonas. Ląstelėse daugiausia fosforo (fosforo rūgštyje) yra kovalentiškai susijungusio su lipidais, baltymais, angliavandeniais ir kitomis organinėmis medžiagomis, kurios atlieka gyvybiškai svarbias funkcijas: tai fosfolipidai, nukleorūgštys, membranų ir citozolio sudėtiniai elementai, makroerginiai junginiai. Kasdien į organizmą patenka iki 50 mmol (1,5 g) fosforo (15 pav.). Daugiausia fosforo neląsteliniame skystyje yra neorganinės formos: esant fiziologinei vandenilio jonų koncentracijai, fosforas yra dviejų monofosfatų ir difosfatų formų. Abi formos sudaro vadinamąjį neorganinį fosforą (P i ) jo koncentracija suaugusiųjų kraujo serume yra 0,81 1,58 mmol/l, vaikų 1,29 1,94 mmol/l. Terminas neorganinis fosforas vartojamas norint atskirti šią formą nuo organiškai prisijungusio fosforo, pavyzdžiui, ATF formos. Apie 20% plazmos fosforo yra susijungusio su baltymais, tačiau, skirtingai nuo kalcio, tai neturi klinikinės reikšmės. Apie 90% fosforo fosfatų pavidalu yra filtruojama glomeruluose ir paskui apie 85 95% jo reabsorbuojama. Su šlapimu jo išsiskiria mmol per 24 val. Fosfatų patekimas su maistu 40 mmol per dieną 14 mmol per dieną Kaulai mmol Minkštieji audiniai Šlapimas 3000 mmol 26 mmol per dieną Plazma 1 mmol/l 15 pav. Normali fosfatų pusiausvyra organizme 211
213 Kalcio ir fosforo homeostazės reguliavimas. Kalcio ir fosforo apykaitą reguliuoja nemažai mechanizmų: 1. Apykaitos būklė kauluose: visi veiksniai, kurie skatina kaulų rezorbciją, didina kalcio ir fosforo kiekį kraujyje, o veiksniai, skatinantys kaulinio audinio sintezę, tą kiekį mažina. 2. Parathormonas (PTH), kuris veikdamas per ciklinį adenozinmonofosfatą (camf) atpalaiduoja kalcį ir fosforą iš kaulų, t. y. skatina kaulo rezorbciją; taip pat jis stimuliuoja kalcio reabsorbciją inkstų kanalėliuose, kraujyje atsiranda hiperkalcemija (jis nepašalinamas su šlapimu) ir slopina fosfatų reabsorbciją (kraujyje atsiranda hipofosfatemija); pašalinti su šlapimu fosfatai atlieka šlapimo buferio funkciją. Parathormonas tai polipeptidas iš 84 aminorūgščių liekanų; jo molekulinė masė yra 9500 daltonų. Paratiroidinės liaukos, kaip atsaką į mažą nesujungto kalcio koncentraciją kraujyje sekretuoja hormono pirmtaką, kurį sudaro 115 aminorūgščių, ir atskėlus nuo N galo du peptidus (iš pradžių atskeliamas 25 aminorūgščių likučių turintis peptidas, po to 6) susidaro aktyvusis hormonas 84 aminorūgščių polipeptidas. 3. D 3 vitaminas (25-hidroksicholekalciferolis) ir jo aktyvioji forma, pasigaminusi inkstuose 1,25-dihidroksicholekalciferolis (1,25-DHCC, kalcitriolis); pastarasis skatina kalcio ir fosfatų absorbciją iš žarnyno, slopina kalcio ir fosfatų išskyrimą su šlapimu. Jis gaminamas iš cholesterolio, hidroksilinamo kepenyse 25-oje padėtyje ir inkstuose 1-oje padėtyje. Hidroksilinimas inkstuose priklauso nuo parathormono; jis taip pat svarbus absorbuojant kalcį ir fosfatus iš žarnyno. 1,25-DHCC veikia kaip steroidinis hormonas: indukuoja kalcio (ir fosfatų) pernašos baltymo sintezę; šis baltymas dalyvauja kalcio ir fosfatų absorbcijoje žarnyne ir reabsorbcijoje inkstuose. Taip veikiant 1,25-DHCC padidėja kalcio ir fosfatų koncentracija kraujyje. D vitaminą sudaro grupė riebaluose tirpių ir struktūriškai panašių sterolų. Svarbiausi jų yra D 2 ir D 3 vitaminai (kalciferoliai). Fiziologiškai aktyviosios formos sintetinamos iš provitaminų. Provitaminai gaunami su maisu: D 2 (ergosterolio) daug yra augalinės kilmės maisto roduktuose, D 3 (cholekalciferolio) daugiausia yra gyvūninės kilmės maisto produktuose, ypač žuvų taukuose ir kepenyse, taip pat piene; D 3 provitaminas sintetinamas ir kepenyse. Veikiant ultravioletinei šviesai, odoje pasigaminęs D 3 kartu su D 3 ir D 2 vitaminais, gautais su maistu, kraujyje pernešami susijungę su D vitaminą sujungiančiu baltymu. Patekę į kepenis jie hidroksilinami 25-oje padėtyje į 25-hidroksicholekalciferolį. Inkstuose iš D 3 vitamino susidaręs 25-hidroksicholekalciferolis toliau hidroksilinamas į 1,25-dihidroksicholekalciferolį (kalcitriolį). Receptoriai, atpažįstantys 1,25-dihidroksicholekalciferolį, yra išsidestę plonojoje žarnoje, kauluose, inkstuose ir kituose organuose. 212
214 Kalcio ir fosforo apykaita, jos sutrikimai hidroksicholekalciferolio koncentracija kraujyje atspindi D vitamino įsisavinimą žarnyne ir jo sintezę iš provitamino veikiant ultravioletinei šviesai. Kraujo plazmoje daugiau kaip 95% 25-hidroksicholekalciferolio yra susidariusio iš D 3 vitamino. 4) Kalcio apykaitos reguliacijoje, ypač kauluose, dalyvauja skydliaukės C ląstelėse gaminamas hormonas kalcitoninas 32 aminorūgščių polipeptidas; jis mažina kalcio koncentraciją kraujyje. Padidėjęs šio hormono kiekis susijęs su susilpnėjusia kaulų remodeliacija; kitų hormonų poveikis kalcio apykaitai nėra susijęs su jo koncentracija kraujyje tai skydliaukės, augimo, antinksčių žievės bei lytiniai hormonai. 5) Rūgščių ir šarmų pusiausvyra: kalcio susijungimas su baltymais priklauso nuo ph ir mažėja esant acidozei, nes albumino aminorūgščių šoninės grandinės įgyja teigiamą krūvį. Ir atvirkščiai sujungimas didėja esant alkalozei. 6) Kraujo plazmoje kalcis ir fosfatai dažnai veikia priešingai, pavyzdžiui, kai fosfatų koncentracija didėja, kalcio mažėja. Kalcio kiekio kraujyje tyrimas. Laboratorijoje dažniausiai matuojamas bendrasis kalcio kiekis tai laisvasis ir sujungtasis kalcis kartu. Tuomet labai svarbu teisingai interpretuoti rezultatus. Albumino koncentracijos svyravimai keičia ir bendrojo kalcio koncentraciją (16 pav.). Jei albuminų koncentracija mažėja, bendrasis kalcio kiekis serume taip pat mažėja, nes mažėja sujungtojo kalcio frakcija. Laisvojo (jonizuotojo) kalcio frakcija išlieka normali ją palaiko parathormonas. Prisimintina, kad homeostazės mechanizmai, reguliuojantys kalcio koncentraciją, reaguoja į jonizuotojo kalcio kiekį, o ne į bendrąjį kalcio kiekį. Asmenų, kurių albuminų koncentracija kraujyje yra sumažėjusi 16 pav. Albumino koncentracijos įtaka bendrajam kalcio kiekiui kraujo serume 213
215 (o tokių ligonių ligoninėje būna daug), bendrasis kalcio kiekis taip pat yra sumažėjęs esant nepakitusiam jonizuotojo kalcio kiekiui. Taigi šios būklės negalima vadinti hipokalcemija. Fosforo (neorganinio) kiekio kraujyje tyrimas. Tiriant fosforo koncentraciją kraujo serume žinotina, kad eritrocituose yra daug fosfatazės ir neorganinių fosfatų, todėl paėmus kraujo serumas turi būti greitai atskiriamas nuo eritrocitų. Dauguma neorganinio fosforo nustatymo metodų remiasi fosforo jono komplekso su molibdatais susidarymu. Ka l c i o ir fo s f o r o ap y k a i t o s sutrikimai ir laboratorinė diagnostika Kalcio ir fosforo apykaita sutrinka dėl daugelio ligų. Pažymėtina, kad kalcio ir fosforo stoka maiste retai sutrikdo medžiagų apykaitą. Didelis fosfatų kiekis, esantis karvės piene, gali sulėtinti kalcio absorbciją žarnyne ir sukelti tetaniją naujagimiams ir kūdikiams. Kita su mityba susijusi kalcio ir fosforo apykaitos sutrikimų priežastis yra intoksikacija D 3 vitaminu, ilgą laiką kaip maisto papildą vartojant šį vitaminą (D 3 hipervitaminozė). Hipokalcemija būdinga šioms patologinėms būklėms: hipoparatirozei ji gali būti idiopatinė, atsiradusi po operacijų kaklo srityje ar dėl magnio stokos; D 3 vitamino stokai, kai jo trūksta maiste ar sutrikęs pasisavinimas žarnyne, kai nebūnama saulėje. Dėl to gali sutrikti medžiagų apykaita kauluose suaugusiesiems išsivystyti osteomaliacija, vaikams rachitas; inkstų ligoms. Dėl patologijos inkstuose nesintetinamas 1,25-DHCC iš 25- hidroksicholekalciferolio. Dėl hipokalcemijos padidėjusi parathormono sekrecija gali sukelti kaulų ligas; pseudohipoparatirozei. Šiais atvejais parathormonas yra sekretuojamas, bet ląstelėse nėra jo receptorių; retos priežastys: piktybiniai navikai, ūminė rabdomiolizė, ūminis pankreatitas, kaulų čiulpų transplantacija. Kliniškai hipokalcemijai būdingi nervų sistemos pažeidimo simptomai, kaip tetanija, smegenų veiklos pokyčiai, katarakta, širdies kraujagyslių veiklos sutrikimo požymiai, kurie gali būti matomi elektrokardiogramoje. Hiperkalcemija. Dažniausios hiperkalcemijos priežastys yra pirminė hiperparatirozė ar hiperkalcemija, atsirandanti dėl piktybinio proceso. Diagnozė paprastai nustatoma biocheminiu tyrimu dar iki sunkaus kaulų ar inkstų pažeidimo. Pirminės hiperparatirozės dažniausia priežastis yra prieskydinių liaukų adenoma, kuri sekretuoja parathormoną, kad ir kokia būtų kalcio koncentracijos kraujyje. Hiperkalcemija dėl piktybinio proceso organizme yra viena dažniausia didelės kalcio 214
216 Kalcio ir fosforo apykaita, jos sutrikimai... koncentracijos kraujyje priežastis. Kai kurie navikai sekretuoja baltymą, turintį parathormonui būdingų savybių. Rečiau pasitaikančios hiperkalcemijos priežastys yra šios: netinkamas D 3 vitamino ar vaistų dozavimas, pavyzdžiui, gydant hipoparatirozę ar inkstų ligas; granulomatozė (sarkoidozė ar tuberkuliozė), kurios metu ar esant navikams (pvz., limfomai) sintetinamas 1,25-dihidroksicholekalciferolis; tirotoksikozė (retai) gali skatinti apykaitos procesus kauluose ir hiperkalcemiją; gydymas diuretikais hiperkalcemija yra nelabai ryški; imobilizacija, ypač jauniems asmenims ir sergantiesiems Pedžeto liga; inkstų ligos: lėtinė antrinė hiperparatirozė gali skatinti parathormono sekreciją nesvarbu, kokia kalcio koncentracija (reguliavimas grįžtamuoju ryšiu). Tai tretinė hiperparatirozė; gydymas kalcio preparatais; ūminio inkstų nepakankamumo diurezinė fazė ar sveikimas po rabdomiolizės; retas vadinamasis pieno šarminis sindromas gali išsivystyti vartojant daug kalcio kartu su rūgščiaisiais karbonatais, pavyzdžiui, geriant daug antacidų (ši būklė yra reta); šarminė hipokalciurinė hiperkalcemija. Parathormono kiekis normalus, nors yra hiperkalcemija, tačiau dažniausiai tokiems pacientams neatsiranda hiperkalcemijos požymių. Tuomet rašoma pirminės hiperparatirozės diagnozė, nes parathormono randama esant didelei kalcio koncentracijai. Apžiūrint nėra prieskydinių liaukų adenomos, o ištyrus ir kitus šeimos narius, nustatoma besimptomė hiperkalcemija. Dažniausiai tokios būklės gydyti nereikia: hiperkalcemija nėra didelė, ir šią būklę galima atskirti nuo pirminės hiperparatirozės nustačius kalcio ekskreciją su šlapimu ji yra per daug maža, palyginti su kalcio koncentracija kraujyje. Hiperkalcemijos klinikai yra būdingi: neurologiniai ir psichikos sutrikimai, pavyzdžiui, letargija, sudirgimas, depresija; virškinamojo trakto funkcijos sutrikimas anoreksija, pilvo skausmas, pykinimas, vėmimas, vidurių užkietėjimas; inkstų veiklos sutrikimas, dėl kurio kankina troškulys, išsivysto poliurija, inkstų akmenligė; širdies aritmija. 215
217 Api b e n d r i n i m a s Interpretuojant bendrojo kalcio kiekio kraujo serume tyrimo rezultatus, būtina vertinti serumo albuminų koncentraciją. Jei esant hipokalcemijai nustatoma maža paratiroidinio hormono koncentracija, tai yra hipoparatirozė. Jei paratiroidinio hormono koncentracija padidėjusi esant mažam kalcio kiekiui, tai greičiausiai hipokalcemijos priežastis yra D 3 vitamino stoka. Ligoniams, kuriems yra inkstų veiklos nepakankamumas, dažnai nustatoma hipokalcemija dėl inkstų negebėjimo hidroksilinti 25-hidroksicholekaciferolio į 1,25-dihidroksicholekaciferolį. Dėl to gali išsivystyti antrinė hiperparatirozė ir kaulų liga. Bendrojo kalcio kiekio ir albuminų koncentracijos kraujyje nustatymas gali padėti išsiaiškinti būklės sunkumą dėl hiperkalcemijos. Hiperkalcemija dažniausiai vystosi esant prieskydinių liaukų adenomai ar esant piktybiniam procesui. Esant adenomai, serumo parathormono koncentracija bus didelė, o esant piktybiniam procesui, didelė kalcio koncentracija slopina prieskydinių liaukų funkciją ir parathormono beveik neaptinkama. Serumo kalcio koncentracija per 3,5 mmol/l yra pavojinga gyvybei. Bifosfanatai sumažina kalcio kiekį serume, slopindami kaulo rezorbciją. Detaliau skyriuje Kaulinio audinio medžiagų, ligos ir laboratorinė diagnostika. Laboratoriniai tyrimai bendrasis Kalcis (Ca) Tiriamoji medžiaga. Serumas. Kraujo imti tik trumpam užspaudus veną, nemasažuojant ir nejudinant rankos. Rekomenduojama reikšmė. 2,12 2,60 mmol/l. Diagnostinė vertė. Hiperparatirozė; piktybinės ligos, apėmusios kaulus (ypač krūties, plaučių, inkstų, metastazinis vėžys, dauginė mieloma, limfomos, leukemija); piktybinės ligos, neapėmusios kaulų (pvz., plokščialąstelinis plaučių vėžys, inkstų vėžys); piktybiniai stemplės, kasos, tulžies pūslės, kepenų navikai; tikroji policitemija; feochromocitoma (susijusi su prieskydinių liaukų hiperplazija); sarkoidozė; intoksikacija D vitaminu, Pedžeto liga esant imobilizacijai; tirotoksikozė, akromegalija, ūminės inkstų kanalėlių nekrozės diurezinė fazė, idiopatinė kūdikių hiperkalcemija, dehidratacija (vemiant, viduriuojant, vartojant alkoholio), šeiminė hipokalciurinė hiperkalcemija. Idiopatinė, chirurginė ar įgimta hipoparatirozė; pseudohipoparatirozė; D vitamino stoka (pvz., sutrikęs įsiurbimas iš žarnyno); lėtinis inkstų nepakankamumas; magnio stoka; užsitęsęs gydymas vaistais nuo traukulių; ūminis pankreatitas; hiperfosfatemija; didelės apimties kraujo perpylimas; raupsai; priekinės hipofizės dalies hipofunkcija; cistinozė; osteomaliacija; proksimalinio ir distalinio inkstų kanalėlių liga; alkoholizmas; kepenų cirozė; hipoalbuminemija; nepakankama mityba. Papildoma informacija. Mažiausias kalcio kiekis yra val. nakties, didžiausias 20 val. Koncentracija įvairuoja su amžiumi ir didžiausia yra naujagimystės tarpsniu. Vyrams po 216
218 Kalcio ir fosforo apykaita, jos sutrikimai m. amžiaus palaipsniui mažėja. Vertikalioje kūno padėtyje po 15 min. kalcio kiekis gali padidėti 4 7% (jonizuotojo kalcio kiekis beveik nesikeičia). Serumo kalcio kiekis kinta keičiantis baltymų koncentracijai. Baltymų (albuminų) kiekio pasikeitimas 10 g/l atitinka kalcio koncentracijos pasikeitimą 0,2 mmol/l. Klaidingas kalcio kiekio padidėjimas galimas esant venostazei kraujo ėmimo metu, kraujui stovint. Kartotiniai kalcio kiekio tyrimai rekomenduojami hiperparatirozės diagnostikai. Traukuliai gali išsivystyti serumo kalcio kiekiui nukritus mažiau kaip iki 1,50 1,75 mmol/l; dėl metabolinės ir respiracinės alkalozės traukuliai gali atsirasti ir esant normaliam kalcio kiekiui serume (bet mažam jonizuotojo kalcio kiekiui). V: antacidiniai (šarminiai) vaistai, androgenai, dietilstilbestrolis, ilgą laiką vartojami diuretikai (pvz., etakrino rūgštis, furozemidas, tiazidai), ergokalciferolis, kalcio druskos, litis, progesteronas, tamoksifenas, testolaktonas, D, A vitaminai. Ch: Ca druskos (pvz., užteršus distiliuotą vandenį riebalų emulsija). V: aminoglikozidai (pvz., gentamicinas), barbitūratai, diuretikai (pradinis poveikis), ergokalciferolis, estrogenai (pomenopauzė), fluoridai, gastrinas, gliukagonas, gliukozė, insulinas, kalcitoninas, karbamazepinas, gliukortikoidai, magnio druskos, meticilinas, druska (izotoninio tirpalo poveikis esant hiperkalcemijai), tetraciklinas (nėštumo metu), vidurius laisvinantys vaistai (perteklinis vartojimas). Ch: baltymas, fluoridai, oksalatai, sulfatai Tiriamoji medžiaga. Paros šlapimas. Rinkti į indą, įpylus 10 ml HCl (6 mol/l) arba surinkus parūgštinti iki ph < 2,0, kad ištirptų kalcio druskos. Rekomenduojama reikšmė. 2,5 6,2 mmol/24 val. Diagnostinė vertė. Per ilgas buvimas saulėje; hiperparatirozė; metastazės kauluose (vėžys, sarkoma), mielominė liga; osteoporozė (ypač po imobilizacijos, sergant Kušingo sindromu, akromegalija), intoksikacija D vitaminu (hiperkalciurija dažnai yra ankstesnė negu kalcio padidėjimas serume); distalinio inkstų kanalėlio acidozė; idiopatinė hiperkalciurija; tirotoksikozė; Pedžeto liga; Fankonio sindromas; hepatolentikulinė degeneracija, sarkoidozė, krūties, šlapimo pūslės navikai, deformuojantis osteitas, imobilizacija. Hipoparatirozė, pseudohipoparatirozė, rachitas, osteomaliacija, visi atvejai, kai kalcio mažai serume (kitos priežastys nei inkstų ligos), nefrozė (dažnai), ūminis nefritas, piktybiniai kaulų navikai, hipotirozė, steatorėja, hipokalciurinė hiperkalcemija. Papildoma informacija. Ir sveikų, ir sergančių asmenų tyrimo reikšmės labai įvairuoja. Kalcio ir baltymų vartojimas bei fosfatų ekskrecija pakeičia kalcio šalinimą. Šlapimo kalcio kiekis mažėja nėštumo pabaigoje. Apie 1/3 pacientų, kuriems yra hiperparatirozė, normaliai šalina kalcį. Kalcio ekskreciją galima išreikšti ir santykiu su kreatininu. Pastovią raumenų masę turinčių sveikų asmenų Ca (mmol/l)/kreatininas (mmol/l) = < 0,40. Jei > 0,57 mmol/l, yra hiperkalciurija. V: amonio chloridas, augimo hormonas, cholestiraminas, pradinis diuretikų (pvz., furozemido, manitolio, tiazidų, triamtereno) poveikis; ergokalciferolis, gliukozė, kadmis, kalcio druskos, kalcitoninas, gliukokortikoidai, parathormonas (mobilizacija iš kaulų), spironolaktonas (farmakologinė dozė turi 40 mg Ca), D vitaminas. Ch: Ca druskos V: rūgštieji karbonatai, diuretikai, estrogenas, litis, neomicinas, geriamieji kontraceptikai, parathormonas (didina reabsorbciją kanalėliuose), tiazidai. Ch: šarminis šlapimas (dėl precipitavusių Ca druskų), oksalatai. Šios priežastys pašalinamos parūgštinus šlapimą. jonizuotasis Kalcis (Ca j ) Tiriamoji medžiaga. Serumas. Rekomenduojama reikšmė. 1,05 1,30 mmol/l. Tiriamoji medžiaga. Smegenų skystis. Rekomenduojama reikšmė. 1,05 1,3 mmol/l. 217
219 Diagnostinė vertė. Pirminė hiperparatirozė, parathormoną gaminantis navikas, perteklinis D vitamino vartojimas, piktybiniai procesai (gali padidėti ir esant normaliam bendrojo kalcio kiekiui). Pirminė hipoparatirozė; pseudohipoparatirozė, D vitamino, magnio stoka; po kraujo, kuriame yra sujungiančių kalcį anijonų (pvz., citratas), perpylimo; po didelės chirurginės operacijos, traumos, sepsio, nudegimų, pankreatito, daugelio organų funkcijos nepakankamumo; po hemodializės, kai dializate yra mažas kalcio kiekis; alkalemija ar joninės gebos padidėjimas (pvz., padaugėjus Na). Papildoma informacija. Tyrimas vertingas nustatant fiziologiškai aktyvaus arba laisvo kalcio kiekį pacientams, kurių baltymų apykaita sutrikusi (lėtinis inkstų nepakankamumas, nefrozinis sindromas, malabsorbcija, dauginė mieloma), taip pat esant rūgščių ir šarmų pusiausvyros sutrikimams. Jonizuotojo kalcio kiekis geriau atspindi kalcio apykaitą negu bendrojo kalcio kiekis. Žymus jonizuotojo kalcio sumažėjimas, nepriklausomai nuo bendrojo kalcio kiekio, gali padidinti nervų ir raumenų jaudrumą ir dėl to prasidėti traukuliai. Jonizuotojo kalcio koncentracija smegenų skystyje glaudžiai siejasi su serumo jonizuotojo kalcio kiekiu. Bendrojo ir jonizuotojo kalcio padidėjimas nustatomas kartu su baltymo kiekio didėjimu smegenų skystyje. Kiekvienas heparino vienetas mililitre kraujo sumažina jonizuotojo kalcio kiekį 0,01 mmol/l. V: sumažėjęs plazmos ph, hidrochlortiazidas (nuolatinis vartojimas), litis. V: furozemidas (pradinis poveikis), vaistai nuo traukulių, padidėjusi joninė geba ir kraujo ph. Ch: Ca surišančiosios medžiagos (citratas, EDTA, heparinas, oksalatas). Hiperfosfatemija. Nedidelė hiperfosfatemija kliniškai nėra svarbi. Ji galima treniruotiems asmenims. Esant hiperfosfatemijai, minkštuosiuose audiniuose kaupiamas kalcis. Didelės fosforo koncentracijos kraujyje priežastys yra šios: inkstų veiklos nepakankamumas, nes sutrinka fosfatų ekskrecija. Tai dažniausia hiperfosfatemijos priežastis; hipoparatirozė. Sumažėjus cirkuliuojančio parathormono kiekiui, mažėja fosfatų šalinimas per inkstus, dėl to kraujo serume jo koncentracija didėja; hemolizė ji galima pačiose kraujagyslėse in vivo ar blogai paėmus kraujo; pseudohipoparatirozė dėl jos vystosi audinių atsparumas parathormonui. Hipofosfatemija. Didelė hipofosfatemija (<0,3 mmol/l) yra reta ir išryškėja raumenų silpnumu. Dėl to gali išsivystyti kvėpavimo nepakankamumas. Būtina greitai sušvirkšti fosfatų. Mažos fosforo koncentracijos kraujyje priežastys yra šios: hiperparatirozė: esant didelei parathormono koncentracijai, didėja fosfatų šalinimas per inkstus ir serume jo koncentracija sumažės; įgimtas fosfatų reabsorbcijos inkstų kanalėliuose nepakankamumas. Šiais atvejais organizmas netenka fosforo; neabsorbuojamų antacidų (pvz., aliuminio hidroksidas) vartojimas, nes jie slopina fosfatų absorbciją; gydant diabetinę ketoacidozę. Dėl insulino poveikio gliukozė, taip pat fosfatai lengviau patenka į ląsteles ir kraujyje bus hipofosfatemija; stoka maiste. Hipofosfatemija randama, kai badaujantys pacientai yra pirmą kartą maitinami. Ji būdinga ir sergant alkoholizmu; onkogeninė hipofosfatemija. Tai reta priežastis, ir medžiaga, kurią gamina navikas, nenustatyta. 218
220 Kalcio ir fosforo apykaita, jos sutrikimai... Api b e n d r i n i m a s Hiperfosfatemija dažniausiai yra susijusi su inkstų pažeidimu. Hipofosfatemija gali išsivystyti esant didelei parathormono koncentracijai kraujyje ar įgimtiesiems fosfatų reabsorbcijos inkstuose sutrikimams. Laboratoriniai tyrimai neorganinis Fosforas (P i ) Tiriamoji medžiaga. Serumas. Rekomenduojama reikšmė. 0,81 1,58mmol/l. Diagnostinė vertė. Osteoliziniai metastaziniai kaulų navikai, mielogeninė leukemija, sarkoidozė, apsinuodijimas D vitaminu, gyjantys kaulų lūžiai, inkstų nepakankamumas, hipoparatirozė, piktybinė hiperpireksija po anestezijos, akromegalija, portinė cirozė, plaučių embolija, laktatinė acidozė, respiracinė acidozė. Osteomaliacija, steatorėja, inkstų kanalėlių acidozė, augimo hormono stoka, ūminis alkoholizmas, gramneigiamų bakterijų septicemija, hipokalemija, šeiminis hipofosfateminis rachitas, D vitamino stoka, nepakankama mityba, malabsorbcija, stiprus viduriavimas, vėmimas, pirminė hiperparatirozė, parathormoną gaminantis navikas, šeiminė hipokalciurinė hiperkalcemija, sunki hiperkalcemija (bet kuri priežastis), ūminė podagra, apsinuodijimas salicilatais, kvėpavimo takų infekcija, cukrinio diabeto gydymas (hiperinsulinemija), respiracinė alkalozė, vėžio metastazės į kaulus, inkstų kanalėlių defektai (Fankonio sindromas), diurezinė fazė po stiprių nudegimų. Papildoma informacija. Serumo fosforo kiekiui būdingas cirkadinis ritmas: daugiausia yra vėlai ryte, o mažiausia vakare. Jo kiekis greitai kinta reaguojant į aplinkos veiksnius, tokius kaip mityba (angliavandeniai), fosfatus surišančių antacidų vartojimas, augimo hormono sekrecijos svyravimai, insulinas, inkstų funkcijos pokyčiai. Nustatytas sezoninis svyravimas: didžiausias kiekis gegužę birželį, mažiausias žiemą. Per pirmą menopauzės dešimtmetį reikšmės didėja ( 0,06 mmol/l). Gulėjimas lovoje padidina koncentraciją 0,16 mmol/l. Serume kiekis gali laikinai sumažėti valgant. Per mėnesines koncentracija taip pat maža. Paėmus kraujo serumas turi būti greitai atskirtas nuo eritrocitų, nes fozfatazė ir neorganiniai fosfatai, kurių daug eritrocituose, pereina į serumą ir galimos klaidingai didelės reikšmės. Hipofosfatemija randama maždaug pusei sergančiųjų pirmine hiperparatiroze. V: anaboliniai steroidai, androgenai, β adrenoblokatoriai, etanolis, ergokalciferolis, furozemidas, augimo hormonas, hidrochlortiazidas, meticilinas (nefrotoksiškumas), fosfatai, tetraciklinas (nefrotoksiškumas), D vitaminas. Ch: bilirubinas, detergentai (užteršti indai), hemoglobinas, lipemija, metotreksatas, riebalų emulsija. V: adrenalinas, aliuminio turintys antacidai, aminorūgštys, anesteziniai vaistai, estrogenai, fruktozė, gliukokortikoidai, gliukozė, hidrochlortiazidas (ilgalaikis gydymas), insulinas, izoniazidas, kalcitoninas, karbamazepinas, geriamieji kontraceptikai. Ch: citratas, manitolis, oksalatas, tartratas (neleidžia susidaryti spalvai) Tiriamoji medžiaga. Paros šlapimas. Rekomenduojama reikšmė. 29,0 42,0 mmol/24 val. Diagnostinė vertė. Hiperparatirozė, D vitaminui atsparus rachitas, imobilizacija esant lūžiui ar paraplegijai; apsinuodijimas D vitaminu, inkstų kanalėlių pažeidimas (Fankonio sindromas), šeiminė hipofosfatemija, neinkstinė acidozė (padidėjęs fosfatų šalinimas). Hipoparatirozė, pseudohipoparatirozė, prieskydinių liaukų pašalinimas. 219
221 Papildoma informacija. Neorganinio fosforo išsiskyrimas per parą svyruoja: didžiausias kiekis šalinamas antroje dienos pusėje. Priklauso nuo mitybos. Fosfaturijos matavimas neaikytinas osteomaliacijos diagnostikai. Matuojant kalcio ir fosfatų ekskreciją, būtina tirti kreatinino klirensą. V: L alaninas, asparaginazė, aspirinas, rūgštieji karbonatai, bismuto druskos, kalcitoninas, gliukokortikoidai, hidrochlortiazidas, fosfatai, parathormonas, triptofanas, valinas, D vitaminas. V: alaninas, aliuminio turintys antacidai. Ch: manitolis. 220
222 KAULINIO AUDINIO MEDŽIAGŲ APYKAITA, LIGOS IR LABORATORINĖ DIAGNOSTIKA Kaulo sudėtis Žmogaus griaučius sudaro 206 kaulai, kurie yra svarbūs mineralinių medžiagų homeostazei, hemopoezei, yra mechaninis ramstis ir apsauga judant; jie lemia kūno dydį ir formą. Kaulas yra vienas jungiamojo audinio tipų, unikalus tuo, kad jame kaupiamos mineralinės medžiagos (mineralizuojasi). Makroskopiškai kaulą sudaro dvi dalys: išorinė žievinė (kortikalinė), arba kompaktinis kaulas (jis sudaro apie 70% griaučių), ir vidinė akytoji (trabekulinė, arba spongiozinė) dalis. Ši struktūra, t. y. žievinis kiautas ir vidinis trabekulinis tinklas, leidžia optimaliai atlikti mechaninę funkciją esant mažiausiai kaulų masei. Mikroskopiškai galima išskirti pintinę ir plokštelinę struktūras. Pintinė struktūra būdinga embrionui ir augant; ją sudaro laisvai išsidėsčiusios kolageno skaidulos. Vėliau jas pakeičia plokštelės, ir pintinės struktūros suaugusio žmogaus organizme nerandama, išskyrus patologines būkles: sergant Pedžeto (Paget) liga, fluoroze ar gyjant lūžiams. Plokštelinė struktūra tai taisyklingos kolageno plokštelės. Žievinę kaulo dalį sudaro osteonai, arba Haverso sistema. Tai apie 2 mm ilgio ir 200 µm skersmens vamzdeliai iš koncentriškai išsidėsčiusių plokštelių, tarp kurių yra įsiterpę osteocitai. Centre yra kanalas su maitinančiomis kraujagyslėmis. Jos sudaro anastomozes su kitais osteonais. Įvairios struktūros nuo centrinės kraujagyslės yra ne toliau kaip 100 µm, maisto medžiagos lengvai difunduoja bei pasiekia visas struktūras. Osteonus vieną nuo kito skiria cementinės linijos. Trabekulinė dalis sudaryta iš subvienetų paketų, skiriamų, kaip ir osteonai, cementinių linijų. Trabekulėse nėra kraujagyslių, jos yra maitinamos iš paviršiaus. Todėl trabekulės nėra storos (tik µm tai dvigubas atstumas nuo mitybos vietos). Kaulą sudaro mineralinis ir organinis užpildas (tarpląstelinė medžiaga), ląstelės ir vanduo (21 lentelė). Biochemiškai kaulinio audinio tarpląstelinį užpildą sudaro organinės (35%) ir neorganinės medžiagos (65%). 221
223 21 lentelė. Kaulo sudėtis Mineralinė tarpląstelinė medžiaga 65%, daugiausia kalcio hidroksiapatito. Organinė tarpląstelinė medžiaga 35%, daugiausiai kolageno (90%), taip pat kitų baltymų, lipidų. Ląstelės sudaro 2% kaulo masės. Tai: 1) kaulą formuojančios ląstelės osteoblastai, osteocitai, 2) ląstelės, atsakingos už kaulo rezorbciją, osteoklastai. Vanduo. Neorganinės kaulo sudėtinės medžiagos. Svarbiausia jų yra kalcio hidroksiapatitas ((Ca 10 (PO 4 ) 6 (OH) 2 ). Be jo, kaule yra karbonato, citrato, magnio, stroncio, fluorido. Kalcio hidroksiapatitas kaului suteikia stiprumo ir kietumo. Jame sukaupta apie 99% organizme esančio kalcio, 80% fosforo, 65% natrio ir magnio. Todėl bendresnis kaulo mineralinių medžiagų apibūdinimo terminas kalcio fosfatas. Kai kurios medžiagos, pavyzdžiui, tetraciklinas, polifosfatai, bifosfanatai, turi afinitetą, t. y. panašios į kalcio fosfatą, taigi ir į kaulą, medžiagos. Dažniausiai šios medžiagos kaupiasi naujo kaulo formavimosi vietose. Todėl tetraciklinu (fluorescuojančia medžiaga kaip žymeniu) ir buvo tiriamas kaulo formavimasis. Bifosfanatai dėl jų stipraus ryšio su kaulo mineralais vartojami gydymui. Kaulo užpildo mineralizacija tai ne paprasta druskų precipitacija, bet sudėtingas ir dar ne iki galo atskleistas biocheminis procesas. Nemineralizuotas kaulas yra vadinamas osteoidu. Nuo užpildo susiformavimo iki jo mineralizacijos praeina dienų. Organines kaulo tarpląstelines medžiagas sudaro baltymai (22 lentelė). 22 lentelė. Kaulo tarpląstelinės medžiagos baltymai I. Osteoblastų sintetinami baltymai 1. Kolagenas I tipas 2. Ląstelių adhezijos baltymai osteopontinas, fibronektinas, trombospondinas 3. Kalcį surišantys baltymai osteonektinas, kaulo sialoproteinai 4. Mineralizacijos baltymai osteokalcinas 5. Fermentai kolagenazė, šarminė fosfatazė 6. Augimo faktoriai į insuliną panašus augimo faktorius (angl. insuli-like growth factor, IGF-1) transformuojantis augimo faktorius (angl. transforming growth factor β, TGF β) iš trombocitų išsiskyręs augimo faktorius (angl. platelet derived growth factor, PDGF) 7. Citokinai IL-1 (interleukinas-1) IL-6 (interleukinas-6) 8. Prostaglandinai II. Baltymai iš kraujo plazmos albuminas 222
224 Kaulinio audinio medžiagų apykaita... Kaulinio audinio tarpląstelinės medžiagos svarbiausi baltymai yra I tipo kolagenas ir nekolageniniai baltymai, kurie sintetinami osteoblastuose. I tipo kolagenas (jis sudaro apie 90% organinių medžiagų arba suaugusio žmogaus organizme apie 2 3 kg) yra organizuotas į fibriles. Tai panaši į susuktą virvę trimatė struktūra, suteikianti kaului stiprumo. I tipo kolagenas sintetinamas kaip didesnės molekulinės masės pirmtakas I tipo prokolagenas. Patekęs į tarpląstelinę erdvę jis yra veikiamas proteolizinių fermentų ir nuo jo molekulės C ir N galo atskyla propeptidai. Iš karto po šios reakcijos kolageno molekulės suformuoja kolageno fibriles. Pastarosios yra stabilizuojamos tarp kolageno fibrilių susidariusių kryžminių (piridino) jungčių. Kaulo užpildas nuolat atsinaujina, t. y. kolageno molekulės, vykstant proteolizei, suardomos į fragmentus piridino kryžmines jungtis, N ir C galo telopeptidus, kurie patenka į kraują ir skiriasi su šlapimu. Nekolageniniai baltymai yra grupuojami pagal savo funkcijas: adheziniai, kalcį rišantys, mineralizacijos, fermentai, citokinai, augimo veiksniai. Iš jų tik osteokalcinas yra būdingas (unikalus) kauliniam audiniui. Jo kiekį galima nustatyti kraujyje, taigi jis yra specifinis osteoblastų aktyvumo žymuo. Kaulo ląstelės sudaro tik apie 2% jo masės; jos yra atsakingos už kaulo komponentų sintezę. Kaulo ląstelės sudaro dvi skirtingas šeimas. I. Kaulą formuojančios ląstelės: kaulo ląstelių pirmtakai, osteoblastai, osteocitai. 1) kaulo ląstelių pirmtakai tai kaulų čiulpų stromos kamieninės (mezenchiminės) ląstelės; stimuliuojamos jos pradeda dalytis ir diferencijuojasi į osteoblastus. Šis reiškinys yra gyvybiškai svarbus kaulo augimui ir audinio atsinaujinimui; 2) osteoblastai yra kaulo paviršiuje (panašiai kaip epitelis odos paviršiuje); jie sintetina, transformuoja ir išdėsto užpildo baltymus, taip pat inicijuoja mineralizacijos procesą; dažniausiai jie sudaro iki 400 ląstelių grupes. Tarp užpildo susidarymo ir kalcifikacijos po osteoblastais susidaro nemineralizuotas sluoksnis. Kai užpildo formavimasis lėtėja, tai ir šis sluoksnis plonėja, bet užtrukus mineralizacijai jis storėja (pvz., esant osteomaliacijai, kai sutrinka mineralizacija). Apie kaulo susidarymo mechanizmus dar mažai žinoma. Svarbu surasti molekules, skatinančias kaulo susidarymą. Dabar žinomos šios: fluoridas, parathormonas, tam tikri citokinai, prostaglandinai. Iki šiol, pavyzdžiui, osteoporozė, gydoma fluoridais. Gliukokortikoidai, priešingai, slopina kaulo susidarymą, todėl ilgalaikis jų vartojimas sukelia osteoporozę. Osteoblastai turi receptorius hormonams (parathormonui, estrogenams), D 3 vitaminui (1,25-dihidrocholekalciferoliui), citokinams, augimo faktoriams; įmūrytas į kaulinę tarpląstelinę medžiagą osteoblastas virsta osteocitu. Nustoję gaminti kaulinę tarpląs- 223
225 telinę medžiagą osteoblastai suplokštėja tai besiilsintieji osteoblastai, arba pamušalinės ląstelės. Vėl stimuliuojamos jos pradeda daugintis ir gaminti tarpląstelinę medžiagą; 3) osteocitai tai subrendę osteoblastai, metaboliškai ne tokie aktyvūs, kaip jų pirmtakai; nuo osteocitų labai priklauso kraujo plazmos kalcio ir fosforo kiekio svyravimas. Nors ir įmūryti į kaulinę tarpląstelinę medžiagą, osteocitai susisiekia su kaulo paviršiaus ląstelėmis ir kitais osteocitais kanalėlių sistema per ilgas citoplazmines ataugėles. II. Osteoklastai priklauso kitai kaulo ląstelių šeimai. Tai ląstelės, atsakingos už kaulinio audinio rezorbciją. Jos išsivysto iš granulocitų monocitų pirmtakų, esančių kaulų čiulpuose. Tai daugiabranduolės (6 12 branduolių) ląstelės kaulo paviršiuje. Osteoklastai atlieka labai specifinę funkciją tai vienintelės kaulų ląstelės, galinčios tirpdyti ir fagocituoti neląstelinį mineralizuotą audinį. Šis procesas vadinamas kaulinio audinio rezorbcija. Tam osteoklastai gamina dviejų rūšių medžiagas. Pirmoji medžiaga tai vandenilio jonai, kurie tirpdo kaulo mineralines medžiagas; jie pasigamina iš angliarūgštės (H 2 CO 3 ) veikiant karboanhidrazei. Antroji medžiaga tai įvairūs proteoliziniai fermentai (katepsinai, kolagenazė), kurie suvirškina užpildą. Minėtieji fermentai hidrolizuoja baltymus iki aminorūgščių, atpalaiduoja augimo faktorius. Taigi šių procesų metu kaulas ýra ir atsipalaiduoja medžiagos, skatinančios jo atsinaujinimą. Dabar mokslininkus domina šių procesų inhibitorių paieškos, nes šios medžiagos pristabdytų kaulo destrukciją. Osteoblastų ir osteoklastų veikla yra koordinuota, t. y. kaulo formavimosi ir jo rezorbcijos procesai sudaro pusiausvyrą, todėl griaučių masė tam tikru vystymosi laikotarpiu nekinta. Kaulinio audinio apykaita Kaulo formavimasis prasideda nesubrendusio ir neorganizuoto kaulinio užpildo gamyba iš kolageno fibrilės, kaulų fermentai ir baltymai. Taip susidaro osteoidas. Tada pradeda daugėti (kelias dienas) kalcio fosfato, kuris vėliau virsta hidroksiapatito kristalais. Kai kaulas auga ir didėja (yra modeliuojamas), vyrauja kaulo formavimasis. Kai kaulas subręsta, jis yra ardomas ir vėl atnaujinamas tai kaulo rekonstravimas, arba remodeliavimas (17 pav.). Didžiausia kaulo masė susiformuoja ankstyvoje individo suaugimo stadijoje, kai 5 10% griaučių kasmet yra rekonstruojama, t. y. kaulo formavimasis ir rezorbcija sudaro pusiausvyrą. Trečiuoju gyvenimo dešimtmečiu kaulinio audinio rezorbcija ima viršyti formavimąsi; taigi griaučių masė pradeda mažėti. Tačiau ir suaugusiųjų organizme kaulas kinta, per metus pasikeičia 3 5% kaulo masės. Rekonstrukciją spartina parathormonas, tiroksinas, augimo hormonas, D 3 vitami- 224
226 Kaulinio audinio medžiagų apykaita... Atsipalaidavę užpildo augimo faktoriai Besiilsintieji osteoblastai Osteoklastai Hormonai Citokinai Osteocitai A B Aktyvūs osteoblastai D 17 pav. Kaulo remodeliavimas A kaulinio audinio rezorbcija; B osteoblastų stimuliacija; C kaulinio audinio formavimasis; D poilsis C nas (1,25-DHCC), mažina kalcitoninas, estrogenai, gliukokortikoidai. Jį taip pat skatina mikrolūžiai, fizinė apkrova. Akytojo kaulo, kuris sudaro apie 20% griaučių masės, rekonstravimo (atsinaujinimo) procesas sudaro 80%, o žievės, kurios kaule yra 80%, atsinaujinimas sudaro apie 20% viso proceso. Tai paaiškina, kodėl osteoporozė, kuri yra nenormalaus atsinaujinimo padarinys, pirmiausia išryškėja akytajame kaule. Kaulinis audinys formuojasi vaikystėje ir vis kitoje vietoje, negu jis suardomas. Todėl griaučių forma keičiasi. Tai leidžia ne tik formuotis normaliai kaulo architektūrai augimo metu, bet ir jai keistis suaugusiame organizme kintant fiziniam krūviui. Tai yra ir stuburo slankstelių apimties didėjimo su amžiumi priežastis. Rekonstravimas yra pagrindinis procesas, vykstantis suaugusiame organizme. Jis taip pat labai svarbus jonų bankas. Griaučių sistemos formavimuisi ir rekonstravimui osteoblastai vykdo labai svarbią vietinės kontrolės funkciją, nes jie ne tik gamina kaulo užpildą, bet yra svarbūs osteoklastų aktyvumo mediatoriai. Dauguma pirminių kaulo rezorbcijos stimuliatorių, kaip parathormonas, interleukinas-1 (ir IL-6), navikų nekrozės faktorius, beveik neturi įtakos osteoklastams. Šioms medžiagoms receptorius turi osteoblastai ir, gavę atitinkamą signalą, jie atpalaiduoja tirpų mediatorių, kuris sužadina osteoklastus ir jų vykdomą kaulo rezorbciją. Paprastai aktyvacija vyksta pavienėse kaulo vietose. Osteoklastams rezorbuojant nedidelę kaulo dalį, susidaro rezorbcinė ertmė (lakūna). Rezorbcijos fazė trabekuliniame kaule trunka apie tris savaites. 225
227 Linijnis osteoklastų rezorbcijos greitis yra apie 50 µm per dieną, o jų formavimasis yra lėtesnis, t. y. apie 1 µm per dieną. Dėl vietinių veiksnių aktyvacijos preosteoblastai pritraukiami prie tos ertmės (lakūnos) ir apie 5 6 dienas bręsta. Subrendę osteoblastai pripildo šią ertmę ir taip susidaro naujas kaulinis audinys. Toks kaulas formuojasi apie 3 mėnesius. Per gyvenimą griaučiai atsinaujina 6 8 kartus. Pagrindiniai hormonai, reguliuojantys kaulo rezorbciją (18 pav.), yra parathormonas, 1,25-dihidroksicholekalciferolis (kalcitriolis) ir kalcitoninas. Pirmieji du rezorbciją skatina, trečiasis slopina. Estrogenai moterų organizme ir testosteronas vyrų organizme slopina kaulo rezorbciją slopindami interleukino-6 (IL-6) sintezę. Menopauzė, kiaušidžių ar sėklidžių pašalinimas staigiai padidina kaulinio audinio rezorbciją, greičiausiai aktyvuojant IL-6. Svarbiausi citokinai, skatinantys kaulinio audinio rezorbciją, yra IL-1, IL-3, IL-6, IL-11, navikų nekrozės faktorius, makrofagų kolonijas stimuliuojantis faktorius, prostaglandinai ir kiti γ interferonas, IL-4, IL-13 kaulinio audinio rezorbciją slopina. Kaulo rezorbcija Didėja Mažėja Sisteminis poveikis Parathormonas 1,25-DHCC (kalcitriolis) Tiroksinas Kalcitoninas Estrogenai Vietinis poveikis Interleukinas-1,-6,-11 Navikų nekrozės faktorius Prostaglandinai Interleukinas-4 18 pav. Kaulo rezorbcijos reguliacija Apibendrinant galima pasakyti, kad remodeliavimo procese osteoblastų/osteoklastų aktyvumas yra lygus 1, kaulo formavimosi metu osteoblastų/osteoklastų aktyvumas yra > 1, kaulo rezorbcijos metu osteoblastų/osteoklastų aktyvumas yra < 1. Nuolatinis kaulinio audinio atsinaujinimas suteikia gyvybingumo įmūrytiems osteoblastams (osteocitams), pripildo kaulų mikrolūžius, pritaiko kaulo architektūrą prie skirtingo mechaninio poveikio. Kaulo atsinaujinimo procesą reguliuoja įvairūs augimo, nerviniai ir fiziniai veiksniai bei hormonai. Kaulinio audinio apykaitos pusiausvyra tai skirtumas tarp rezorbcijos gylio ir kaulo sienos storio (naujo kaulinio audinio kiekio). Šią kaulinio audinio gamybos pusiausvyrą gali sutrikdyti metabolinės kaulų ligos, dėl kurių pakinta kaulo masė, stiprumas, o tai padidina kaulų lūžių riziką. 226
228 Kaulinio audinio medžiagų apykaita... Kaulo ligos Kaule, kaip ir kituose organuose bei sistemose, galimi kraujo apykaitos, uždegiminiai, neoplaziniai, metaboliniai ar įgimti pakitimai (23 lentelė). 23 lentelė. Kaulo ligos I. Vystymosi anomalijos: apsigimimai (pirštakaulių neišsivystymas ar papildomas jų skaičius, sindaktilija); achondroplazija kaulo augimo plokštelės liga, kurios padarinys nykštukiniai žmonės. II. Ligos, susijusios su užpildo pakitimais: osteogenesis imperfecta (I tipo kolageno sintezės sutrikimas); mukopolisacharidozės (kaulų defektai, susiję su hialininės kremzlės anomalijomis); osteoporozė. III. Ligos, susijusios su osteoklastų disfunkcija: osteopetrozė (difuzinė simetrinė kaulo sklerozė kaulai kaip akmuo); Pedžeto (Paget) liga (osteitis deformans) tai tarpląstelinio audinio pamišimo liga osteoklastų vykdoma gili kaulo rezorbcija ir paskesnis nevaldomas kaulo formavimasis. IV. Ligos, susijusios su nenormalia mineralų homeostaze: rachitas (pvz., dėl D 3 vitamino stokos); osteomaliacija tai susilpnėjusi kaulo mineralizacija sutrikus kalcio ir fosforo apykaitai; hiperparatirozė; inkstinė osteodistrofija (sergant lėtinėmis inkstų ligomis). V. Kaulų lūžiai. VI. Osteonekrozė kaulo ir kaulų čiulpų infarktų padarinys. VII. Infekcijos osteomielitas (piogeninis, tuberkuliozinis, sifilinis). VIII. Kaulų navikai ir navikinės pažaidos. Osteoporozė Tai terminas, apibūdinantis griaučių akytumą dėl sumažėjusios kaulo masės. Osteoporozė viena dažniausių kaulų metabolinių ligų. Tai procesas, sukeltas ne vieno etiologinio veiksnio, o susijęs su daugybe epidemiologinių, klinikinių ir biocheminių veiksnių, dėl kurių poveikio mažėja kaulo masė. Kartais vartojamas terminas kaulo atrofija, bet tai ne visai tikslus terminas, nes osteoporozė gali būti padidėjusios kaulo rezorbcijos ar sulėtėjusio kaulo formavimosi, ar abiejų šių veiksnių padarinys. Normali osteoido mineralizacija savybė, kuri skiria osteoporozę nuo osteomaliacijos. Osteoporozė gali būti vietinė, pavyzdžiui, nejudrios galūnės osteoporozė, ar visų griaučių. Osteoporozė gali būti pirminė ir antrinė. Antrinė osteoporozė yra susijusi su kitomis priežastimis negu amžius ir menopauzė (24 lentelė). Rentgenogramose matomas difuzinis kaulo tankio sumažėjimas, kurio padariniai griaučių deformacijos, lūžiai, kompresijos, kaulų skausmai. Moterims osteoporozė yra 3 4 kartus dažnesnė negu vyrams. 227
229 24 lentelė. Osteoporozės priežastys Pirminės: pomenopauzė senatvė idiopatinė jaunatvinė idiopatinė suaugusiųjų Antrinės: endokrininės ligos: hiperparatirozė hipertirozė hipotirozė hipogonadizmas akromegalija Kušingo sindromas prolaktinoma I tipo diabetas Adisono liga neoplazija: dauginė mieloma karcinomatozė tukliųjų ląstelių liga virškinamojo trakto ligos: bloga mityba malabsorbcija subtotalinė gastrektomija kepenų funkcijos nepakankamumas C, D 3 vitaminų stoka reumatinės ligos vaistai: antikoaguliantai chemoterapija gliukokortikoidai vaistai nuo traukulių litis alkoholis įvairios: osteogenesis imperfecta imobilizacija plaučių ligos homocistinurija Gošė liga Anemija Kaip minėta, kaulo formavimasis viršūnę pasiekia jaunystėje. Jį lemia paveldimumas, taip pat svarbu fizinis aktyvumas, raumenų jėga, mityba, hormonai. Pagrindinis genetinis veiksnys tai D 3 vitamino aktyviosios formos 1,25-DHCC receptoriaus genas. Kai pasiekiama maksimali griaučių masė, su kiekvienu rezorbcijos ir formacijos ciklu išryškėja nedidelė pastarosios stoka, ir rekonstrukcijos etapas nevyksta iki galo. Su amžiumi kasmet netenkama ~0,7% kaulo. Tai reiškinys, panašus į laipsnišką žilimą. Patogenezė iki galo nėra aiški, bet tai kaulo rezorbcijos ir formavimosi pusiausvyros sutrikimo rezultatas. Pirminės osteoporozės priežastys: kaulų metabolizmui svarbūs su amžiumi susiję pokyčiai (sintezės silpnėjimas, kt.); sumažėjęs fizinis aktyvumas skatina kaulo netektį; tai ir imobilizacijos ar galūnių paralyžiaus, taip pat gravitacijos, t. y. Žemės traukos, nebuvimo (tai ištinka kosmonautus) padarinys; kalcio stoka maiste greito kaulo augimo tarpsniu; pomenopauzinės osteoporozės priežastis yra nuo hormonų priklausoma pagreitėjusi kaulų masės netektis. Pomenopauzinė ir senatvinė osteoporozė pažeidža visus griaučius. Nuo osteoporozinių kaulų lūžių kenčia 1 iš 2 moterų, lyginant su 1 iš 40 vyrų. Manoma, kad čia svarbiausias vaidmuo tenka estrogenų stokai. Estrogenų ir kaulų 228
230 Kaulinio audinio medžiagų apykaita... masės ryšiui turi įtakos citokinai. Sumažėjus estrogenų kiekiui, padidėja interleukino-1 sekrecija iš monocitų. Interleukinas yra vienas stipriausių osteoklastų aktyvumą skatinančių veiksnių. Kompensacinis osteoblastų aktyvumo padidėjimas nepasiekia reikiamo greičio, todėl vystosi vadinamoji greitoji osteoporozė. Klinikinė eiga. Klinikiniai požymiai priklauso nuo to, kurie kaulai pažeidžiami. Labai skausmingi yra stuburo slankstelių lūžiai. Dėl šlaunikaulio galvos, dubens ar stuburo lūžių gali būti įvairių komplikacijų, pavyzdžiui, embolizacija, pneumonija. Rentgenologiškai osteoporozė nustatoma tada, kai netenkama 30 40% kaulų masės. Jei ji nekomplikuotos formos, tai kalcio, fosforo, šarminės fosfatazės kiekiai kraujyje gali ir nepakisti. Taigi osteoporozę diagnozuoti sunku, nes: ji ilgai būna besimptomė (kol neatsiranda kaulų lūžių); ją sunku diferencijuoti nuo kitų ligų, kai per mažai kaulo ; nėra specifinių jautrių metodų kaulų masės sumažėjimui nustatyti. Esant osteoporozei, paprastai padidėja kalcio ir hidroksiprolino ekskrecija; kiti kalcio ir fosforo apykaitos rodikliai dažniausiai yra normalūs. Jei osteoporozė vystosi dėl nejudros (imobilizacija, paralyžius), kalcio ir fosforo kiekis plazmoje padidėja. Diagnostikai svarbus yra kaulų tankio matavimas. Vienintelis biocheminis kaulo formavimosi žymuo yra osteoblastų gaminamas osteokalcinas, kurio kiekį galima išmatuoti kraujyje. Kaulo medžiagų apykaita, jos sutrikimų vystymosi mechanizmai šiuo metu yra ypač intensyviai tiriami, ieškoma naujų diagnostikos metodų, gydymo būdų, kuriami nauji vaistai, bandoma koreguoti tokių pacientų mitybą ir gyvenseną. Taigi atsiranda viltis ir galimybė šį procesą valdyti. Kaulo medžiagų sudėties ir apykaitos tyrimas Kaulo medžiagų apykaita tiriama įvairiais metodais in vitro ir in vivo. Šiuo metu, be rentgenologinio, biopsinio kaulo tyrimo, taikomi radiografinio vaizdo tyrimai, kuriais galima išmatuoti kaulo tankį (fotonų absorbciometrija, kiekybinė kompiuterinė tomografija), atliekami sudėtingi kinetiniai kaulo sudėties tyrimai naudojant radioaktyviąsias medžiagas. Didėja biocheminių kaulų žymenų tyrimo kraujo serume, šlapime svarba. Kaulų medžiagų apykaitą apibūdina du priešingų krypčių procesai: osteoblastų atliekamas naujo kaulo formavimas ir osteoklastų senojo kaulo ardymas (rezorbcija). Abu procesai yra labai susiję ir laike, ir erdvėje. Invaziniai tyrimo metodai. Jie suteikia daug informacijos, bet jų taikymas yra ribotas, pavyzdžiui, histomorfometrija. Klubinės skiauterės srities histomorfometrija teikia daug informacijos apie ląsteles, tarpląstelinį audinį, tačiau duomenys apsiriboja tik nedidele kaulo tyrimo vieta ir ne visada atspindi kauluose išplitusius procesus. Kalcio kinetikos tyrimais įvertinama kaulo medžiagų apykaita po menopauzės. Bet kalcio ekskrecijos greitis gali būti išmatuotas netiksliai. 229
231 25 lentelė. Biocheminiai kaulo medžiagų apykaitos žymenys I. Kaulo formavimosi žymenys (tiriamoji medžiaga kraujo serumas): bendroji ir kaului specifinė šarminė fosfatazė, osteokalcinas, I tipo prokolageno karboksigalo ir aminogalo peptidai. II. Kaulo rezorbcijos žymenys: tartratui atspari rūgščioji fosfatazė (tiriamoji medžiaga kraujo plazma arba serumas), I tipo kolageno karboksigalo ir aminogalo telopeptidai (tiriamoji medžiaga kraujo plazma arba serumas), kalcis (tiriamoji medžiaga šlapimas), piridinolino ir deoksipiridinolino (DPD) ekskrecija su šlapimu, hidroksiprolinas (tiriamoji medžiaga šlapimas), hidroksilizino glikozidai (tiriamoji medžiaga šlapimas). Žymėtųjų bifosfanatų sulaikymo organizme tyrimas atspindi kaulo medžiagų apykaitą ir formavimąsi. Jis nėra labai tikslus. Kaulo tarpląstelinės medžiagos formavimosi ir jos irimo greitį galima įvertinti tiriant kaulą formuojančių ar jį rezorbuojančių ląstelių fermentų aktyvumą, pavyzdžiui, šarminės ir rūgščiosios fosfatazių aktyvumą, ar matuojant kaulo tarpląstelinės medžiagos komponentų išsiskyrimą į kraujo tėkmę formuojantis ar rezorbuojantis kaului (25 lentelė). Šie žymenys gali rodyti kaulo formavimąsi ar rezorbavimą. Kadangi abu procesai glaudžiai susiję, diagnozuojant ligą šių procesų rodiklius interpretuoti nelengva. Biocheminiai kaulo formavimosi žymenys Kraujo serumo šarminė fosfatazė. Šarminės fosfatazės yra kepenyse, kauluose, žarnų sienoje, placentoje, bet didžiausią šio fermento aktyvumo dalį sudaro kepenų ir kaulų izofermentai. Kaulų šarminė fosfatazė yra osteoblastų membranų fermentas, kurio išsiskyrimo į kraują mechanizmas dar neaiškus. Bendras šarminės fosfatazės aktyvumas kraujo serume yra dažniausiai matuojamas rodiklis, kuriuo galima įvertinti kaulo formavimąsi, bet šis tyrimo būdas yra nelabai jautrus ir specifiškas. Fermento aktyvumas didėja su amžiumi ir ypač moterims po menopauzės. Būtina atsižvelgti į tai, kad bendrasis šarminės fosfatazės aktyvumas gali padidėti vartojant daug vaistų, veikiančių kepenis. Todėl gerokai informatyvesnis yra kaului specifinio šarminės fosfatazės izofermento nustatymas (elektroforeze). Tyrimo kokybė pagerėja naudojant monokloninius antikūnus, atpažįstančius kaului specifinį izofermentą. Kraujo serumo osteokalcinas itin specifiškas kaulų medžiagų apykaitos žymuo. Jis dar vadinamas kaulo Gla baltymu. Pirminei šio baltymo struktūrai būdingos trys g karboksiglutamo (Gla) rūgšties liekanos, kurios reikalingos kalciui ir hidroksiapatitams sujungti. Tai nedidelės molekulinės masės (5800 Da) nekolageninis baltymas, būdingas kaulo audiniui ir dentinui, ir sudaro apie 3% visų kaulų baltymų. Jį gamina osteoblastai ir išskiria į tarpląstelinę erdvę. Manoma, kad osteokalcinas yra chemo- 230
232 Kaulinio audinio medžiagų apykaita... taksinė osteoklastams ir osteoblastams medžiaga. Formuojantis užpildui, osteokalcino sintezė suintensyvėja. Ji rodo visiškai diferencijuotų nesidalijančių osteoblastų aktyvumą. Osteokalciną tiesiogiai veikia kalcitoninas, paratiroidinis hormonas, D 3 vitaminas, kurie būtini kaulo mineralizacijai. Dalis naujai susintetinto osteokalcino patenka į kraujo apytaką ir gali būti išmatuota, pvz., radioimuniniu metodu. Kraujyje osteokalcino gyvavimo puslaikis yra trumpas, jis greitai šalinamas per inkstus. Serumo osteokalcino kiekis koreliuoja su kaulų augimu: didėja dėl įvairių būklių (pvz., pirminės ir antrinės hiperparatirozės, hipertirozės, Pedžeto ligos, akromegalijos) suintensyvėjus kaulo apykaitai ar mažėja esant hipoparatirozei, hipotirozei, gydant gliukokortikoidais. Tai specifinis osteoblastų žymuo, atspindintis kaulo formavimąsi. I tipo prokolageno N ir C galo propeptidai. Baigiant formuotis I tipo kolagenui tarpląstelinėje erdvėje, dar iki fibrilių susidarymo, nuo jo N ir C galo atskeliami propeptidai, atitinkamai aminogalo ir karboksigalo propeptidai, kurie cirkuliuoja kraujyje. Pastarojo molekulinė masė yra didesnė ir jis kraujo serume yra išmatuojamas radioimuniniu metodu. I tipo prokolageno karboksigalo propeptidas atspindi kaulo formavimąsi, nes šio tipo kolagenas yra gausiausia tarpląstelinės kaulo organinės medžiagos sudedamoji (jo yra ir odoje). Po menopauzės jų kiekis padidėja ir koreliuoja su kaulo netekimo greičiu, išmatuotu densitometru. Biocheminiai kaulo rezorbcijos žymenys Kraujo plazmos tartratui atspari rūgščioji fosfatazė. Rūgščioji fosfatazė tai lizosomų fermentas, randamas kauluose, prostatoje, trombocituose, eritrocituose, blužnyje. Kaulo rūgščioji fosfatazė yra atspari tartrato poveikiui, o prostatos rūgščiąją fosfatazę tartratas slopina. Kraujo plazmos tartratui atspari rūgščioji fosfatazė yra gaminama osteoklastuose. Kraujo plazmoje jos daugėja dėl kaulo metabolinių ligų, kai intensyvėja kaulo medžiagų apykaita, slankstelių osteoporozė. Ateityje, naudojant monokloninius antikūnus, šio fermento nustatymas gali tapti vertingu osteoklastų aktyvumo ir osteoporozės pradžios rodikliu. I tipo kolageno N ir C galo telopeptidai. Vykstant I tipo kolageno proteolizei (atsinaujinant kaulo užpildui) nuo molekulės C ir N galo yra atskeliami karboksipeptidai ir aminotelopeptidai, kurių kiekis kraujo serume gali būti išmatuotas. Jis atspindi kaulinio audinio rezorbcijos intensyvumą. Piridinolino ir deoksipiridinolino (DPD) ekskrecija su šlapimu. Piridinolinas ir deoksipiridinolinas, arba atitinkamai hidroksilizilpiridinolinas ir lizilpiridinolinas, yra piridino dariniai iš lizino ar hidroksilizino radikalų, susijungusių kryžminiais (skersiniais) ryšiais. Bręstančiame kolagene, t. y. po jo sintezės, dėl hidrofobinių ir elektrostatinių jėgų tarp kolgeno fibrilių formuojasi kryžminės (piridino) jungtys. 231
233 Šis procesas yra audiniui specifinis ir priklauso nuo piridino junginių tipo, kitų veiksnių. Piridino darinys piridinolinas randamas kremzlės, kaulo, sausgyslių kolagene, o deoksipiridinolino (DPD) daugiausia yra kaulo ir dentino kolagene (kaulo organiniame užpilde DPD yra daugiau negu piridinolino). Kaulo rezorbcijos metu deoksipiridinolinas atsipalaiduoja, patenka į kraują ir skiriasi su šlapimu. Taigi matuojant kaulinio audinio irimo produktus galima susidaryti vaizdą apie kaulo medžiagų apykaitą. Hidroksiprolino tyrimas šlapime po nakties badavimo. Sustiprėjus kaulo rezorbcijai, padidėja hidroksiprolino ekskrecija su šlapimu, kaip ir esant kitos etiologijos kolageno apykaitos intensyvėjimui. Hidroksiprolinas atspindi kaulo rezorbciją, nes kolagenas yra vienintelis žinduolių baltymas, turintis ypač daug šios aminorūgšties. Laisvasis hidroksiprolinas, kuris atsipalaiduoja yrant kolagenui, negali būti vėl panaudotas kolageno sintezei. Taigi biologiniuose skysčiuose esantis endogeninis hidroksiprolinas yra įvairių tipų kolageno irimo produktas. Apie pusė žmogaus kolageno yra kauluose, kur jo apykaita yra intensyvesnė negu minkštuosiuose audiniuose, taigi hidroksiprolino ekskrecija su šlapimu yra kaulo rezorbcijos žymuo. Kuo ji intensyvesnė, tuo daugiau hidroksiprolino šalinama su šlapimu. Iki 40% hidroksiprolino šlapime yra kilusio iš komplemento komponento C1q, nes jame yra daug šios aminorūgšties. Šlapimo hidroksiprolino kiekio ryšys su kolageno apykaita yra sudėtingas. Hidroksiprolinas biologiniuose skysčiuose (kraujyje) yra skirtingų formų. Apie 90% hidroksiprolino, atsipalaidavusio suirus audinių kolagenui, ypač rezorbuojantis kaulams, yra laisvojo, jis cirkuliuoja kraujyje, filtruojamas ir beveik visas reabsorbuojamas inkstų kanalėliuose. Po to kepenyse visiškai oksiduojamas ir susidaro CO 2 bei NH 3 (iš jų sintetinamas šlapalas). Apie 10% hidroksiprolino cirkuliuoja susijungusio su peptidais; jis taip pat yra filtruojamas ir išskiriamas su šlapimu. Taigi bendras hidroksiprolino kiekis šlapime atspindi tik apie 10% bendro kolageno katabolizmo. Hidroksiprolinas šlapime yra trijų formų: 1) laisvasis; 2) mažai hidroksiprolino turinčių dializuojamų peptidų formos: juose hidroksiprolinas sudaro apie 90% viso su šlapimu šalinamo kiekio; 3) įeinantis į nedializuojamų peptidų sudėtį. Paprastai šlapime matuojamas bendras hidroksiprolino kiekis. Tai nedidelio jautrumo kaulų rezorbcijos žymuo. Hidroksilizino glikozidai šlapime. Hidroksilizinas yra kita aminorūgštis, būdinga kolagenui. Kaip ir hidroksiprolinas, hidroksilizinas nėra naudojamas kartotinei kolageno sintezei. Nors jo yra mažiau negu hidroksiprolino, tai svarbus kolageno irimo žymuo. Hidroksilizino ekskrecija didėja su amžiumi. Nustatomas sudėtingu didelio slėgio skysčių chromatografijos metodu. Manoma, kad jo tiriamoji svarba didės. 232
234 Kaulinio audinio medžiagų apykaita... Kalcio tyrimas šlapime po nakties badavimo. Po nakties badavimo rytiniame šlapime išmatuotas kalcio kiekis vienas pigiausiai nustatomų kaulo rezorbcijos žymenų. Jis atspindi kaulo rezorbcijos suintensyvėjimą, bet yra mažo jautrumo. Būtina žinoti, kad šis rodiklis taip pat atspindi inkstų ir kalcio kiekį reguliuojančių hormonų, estrogenų poveikį kalcio apykaitai. Api b e n d r i n i m a s Kaulas yra vienas iš jungiamojo audinio tipų, kuris unikalus tuo, kad jame kaupiamos mineralinės medžiagos. Kaulą sudaro mineralinis ir organinis užpildas (tarpląstelinė medžiaga), ląstelės ir vanduo. Svarbiausia neorganinė kaulo medžiaga yra kalcio hidroksiapatitas, kuris kaupiasi naujo kaulo formavimosi vietose. Kaulo užpildo mineralizacija sudėtingas ir dar ne iki galo atskleistas biocheminis procesas. Nemineralizuotas kaulas vadinamas osteoidu. Svarbiausi kaulo tarpląstelinės medžiagos baltymai yra kolagenas ir osteokalcinas; pastarasis yra specifinis kaulo mineralizacijos baltymas. Kaulą formuojanti ląstelė yra osteoblastas, o ląstelė, atsakinga už kaulo rezorbciją, yra osteoklastas. Kai žmogus auga, griaučiai didėja ir yra modeliuojami; tai vadinama kaulo formavimusi. Susiformavęs kaulas yra ardomas ir vėl atnaujinamas, t. y. kaulas rekonstruojamas. Kaulų apykaitą apibūdina du priešingų krypčių procesai: osteoblastai formuoja naują kaulą, o osteoklastai ardo (rezorbuoja) senąjį. Abu procesai yra labai susiję ir laike, ir erdvėje. Viena dažniausių kaulų metabolinių ligų yra osteoporozė tai griaučių porėtumas dėl sumažėjusios kaulo masės. Osteoporozė yra pagrindinė senų žmonių sergamumo ir mirtingumo priežastis. Nors su amžiumi ir vyrų, ir moterų kaulų masė vis mažėja, moterų po menopauzės šis procesas yra daug greitesnis. Kaulo masės netekimą, dėl kurio vystosi antrinė osteoporozė, skatina rūkymas, imobilizacija, gliukokortikoidų vartojimas. Vienas specifiškiausių kaulų žymenų yra osteokalcinas, kurį gamina osteoblastai. Laboratoriniai tyrimai Osteokalcinas (kaulo Gla baltymas) Tiriamoji medžiaga. Serumas. Rekomenduojama reikšmė. 3,1 13,7 mg/l. Diagnostinė vertė. Pedžeto liga, inkstų osteodistrofija, pirminė ir antrinė hipertirozė, metastazinė kaulų liga, lėtinis inkstų nepakankamumas, kai kurie osteoporozės atvejai, greitas paauglių augimas. 233
235 Pirminė biliarinė cirozė, nėštumas, augimo hormono stoka. Papildoma informacija. Padidėjęs osteokalcino kiekis atspindi naujų osteoblastų sintezę (ne kaulų rezorbciją). Taigi osteokalcinas yra jautrus ir neinvazyvus kaulų apykaitos žymuo. Osteoklastams vykdant rezorbciją, osteokalcinas yra fragmentuojamas ir išsiskiria į kraują. Fragmentai šalinami per inkstus ir šlapime randami kaip γ karboksiglutamo rūgšties (Gla) metabolitai. Mažiau negu 1% Gla susidaro iš intaktinio (pirminio) osteokalcino, 10% iš osteokalcino, išsiskyrusio rezorbuojantis kaulams. Serumo osteokalcinas kinta lygiagrečiai su šarminės fosfatazės aktyvumu. Tyrimas svarbus vertinant gydymo efektyvumą. Esant osteoporozei, osteokalcino koncentracija gali ir padidėti, ir būti normali. Serume koncentracija mažėja po naujagimystės tarpsnio, bet smarkiai padidėja paauglystėje greitai augant organizmui. V: kalcitriolis, estrogenai, vaistai nuo traukulių. V: gliukokortikoidai. Deoksipiridinolinas (DPD) Tiriamoji medžiaga. Šlapimas. Rekomenduotina reikšmė: moterų 3,0 7,4 nmol DPD/mmol kreatinino; vyrų 3,0 5,4 nmol DPD/mmol kreatinino. Diagnostinė vertė. Padidėjusio osteoklastų aktyvumo ir kaulo demineralizacijos žymuo. Papildoma informacija. Apie 90% kaulinio audinio organinio užpildo sudaro I tipo kolagenas. Tai trimatės struktūros baltymas. Šią struktūrą stabilizuoja kryžminės (skersinės) piridino jungtys tai piridinolinas ir deoksipiridinolinas (DPD). DPD susidaro po fermentinio liziloksidazės poveikio lizinui. Kaulo rezorbcijos metu atsipalaiduoja DPD, patenka į kraują ir skiriasi su šlapimu. Taigi matuojant kaulinio audinio irimo produktus galima susidaryti vaizdą apie kaulo medžiagų apykaitą. Paprastai DPD ekskrecija išreiškiama pagal kreatinino koncentraciją šlapime. 234
236 MAGNIO, GELEŽIES IR VARIO APYKAITA, JOS SUTRIKIMŲ LABORATORINĖ DIAGNOSTIKA Ma g n i s Magnio jonų ląstelėse yra apie 10 kartų daugiau negu už jų ribų; Iš ląstelinių katijonų daugiau nei Mg 2+ yra kalio. Magnis reikalingas aktyvuoti apie 300 fermentų (svarbiausias yra (Na + + K + )-ATF-azė), nuo jo priklauso tokie biocheminiai procesai kaip glikolizė, oksidacija, kalio ir kalcio, apskritai medžiagų pernaša per membraną. Elektrinės ląstelių membranų savybės priklauso nuo neląstelinio magnio koncentracijos. Gilinantis į magnio apykaitą ir jos svarbą, būtina neužmiršti magnio, kalio ir kalcio jonų tarpusavio sąveikos. Magnis yra augalų pigmento chlorofilo sudedamoji dalis, todėl žalios daržovės yra svarbus jo šaltinis; taip pat jo yra augaliniuose dribsniuose ir mėsoje. Vidutiniškai per dieną suvartojama apie 15 mmol (300 mg) magnio. Vaikams ir nėščiosioms jo reikia daugiau. Apie 30% su maistu patekusio magnio absorbuojama iš virškinamojo trakto ir pasiskirsto po audinius: apie 55 60% šio kiekio kauluose, o likusi dalis minkštuosiuose audiniuose (ypač griaučių raumenyse). Kraujyje yra ~1% organizmo magnio. Trečdalis kraujyje esančio magnio yra susijungęs su baltymais (daugiausia albuminais), o kitus du trečdalius magnio sudaro laisvieji magnio jonai (65 84%). Raumenų ląstelėje magnis funkcionuoja kaip kalcio antagonistas. Su šlapimu per parą pasišalina 2,5 8,5 mmol magnio. Magnis dalyvauja parathormono sekrecijoje ir todėl ryški hipomagnezemija gali būti hipoparatirozės priežastis. Rekomenduojamos magnio koncentracijos kraujo serume ribos yra 0,65 1,05 mmol/l. Vertikalioje kūno padėtyje magnio padaugėja apie 4%. Netinkamas vaistų (pvz., magnio sulfato) dozavimas ar antacidiniai vaistai padidina magnio kiekį serume. Esant kraujyje 0,15 0,50 mmol/l magnio, kai kalcio koncentracija ir ph yra normalūs, gali atsirasti tetanija. Kraujo plazmoje magnio kiekis gali išlikti normalus, net jei išeikvojama iki 20% bendro organizmo magnio kiekio. Riebalų rūgštys, per didelis fosfatų kiekis maiste sutrikdo magnio absorbciją. Hipermagnezemija yra reta, tačiau gali būti esant inkstų nepakankamumui. Hipermagnezemija sustiprina hiperkalemijos poveikį širdžiai. Sunkios formos hipermagnezemijos poveikis: 2,50 5,00 mmol/l sulėtėja širdies laidumo sistemos darbą; 5,00 6,50 mmol/l dingsta giliųjų sausgyslių refleksai; 7,50 mmol/l vystosi 235
237 kvėpavimo paralyžius, galima generalizuota anestezija; >12,5 mmol/l širdis sustoja esant raumens diastolei. Hipomagnezemija paprastai susijusi su magnio stoka. Jos požymiai labai panašūs į hipokalcemijos: sutrikusi nervų ir raumenų funkcija, kuriai būdinga tetanija, padidėjęs dirglumas, drebulys, traukuliai, raumenų silpnumas. Magnio stokos organizme priežastis bloga mityba. Simptominė magnio stoka gali išryškėti esant: nepakankamai mitybai sutrikus jo absorbcijai, vemiant, viduriuojant; osmosinei diurezei, pavyzdžiui, sergant cukriniu diabetu; ilgai gydant diuretikais, ypač jei su maistu gaunamas tik ribinis magnio kiekis; gydant citotoksiniais vaistais, kurie sutrikdo magnio reabsorbciją inkstų kanalėliuose; gydant imunosupresiniais vaistais (ciklosporinais). Kartotinai nustačius mažesnę negu 0,7 mmol/l magnio koncentraciją kraujo serume, daroma išvada apie ląstelinę magnio stoką ir reikalingą gydymą. Tačiau ląstelinė stoka galima ir esant plazmoje pakankamai magnio. Kaip minėta, magnis silpnina raumenų susitraukimą ir kraujagyslių tonusą slopindamas kalcio poreikį širdies raumens ląstelėse ir kraujagyslių miocituose, taigi magnis veikia kaip natūralus kalcio blokatorius. Tai ir lemia magnio svarbą širdies aritmijų genezei. Diagnozuojant širdies ir kraujagyslių ligas labai svarbu ištirti magnio kiekį kraujyje, kai yra širdies aritmijos, elektrokardiogramos pokyčių QT tarpo pailgėjimas. Šiuos simptomus lemia magnio stoka, kuri gali būti susijusi su hipokalcemija ir hipokalemija. Hipomagnezemija gali sutrikdyti paratiroidinio hormono sekreciją ir veikimą. Magnio nepakankamumo simptomų nebūna, kol magnio kiekis kraujo plazmoje nepasidaro mažesnis negu 0,50 mmol/l. Labai trūkstant magnio, atsiranda silpnumas, irzlumas, tetanija, elektrokardiogramos pokyčiai, kliedėjimas, traukuliai. Api b e n d r i n i m a s Magnio stoka galima esant blogai mitybai, netenkant jo per inkstus ar virškinamąjį traktą. Magnio stoka gali sukelti komplikacijų sergant virškinamojo trakto ligomis, po chirurginių intervencijų ar vartojant nefrotoksiškus vaistus, diuretikus, sergant cukriniu diabetu. Nustačius mažą magnio koncentraciją serume, galima didelė jo stoka, o maža magnio stoka kraujyje gali būti ir esant normaliam jo kiekiui organizme. Paprastai po širdies operacijų ar miokardo infarkto skiriama magnio preparatų, kad nebūtų aritmijų. 236
238 Magnio, geležies ir vario apykaita... Laboratoriniai tyrimai Magnis (Mg) Tiriamoji medžiaga. Serumas. Rekomenduojama reikšmė. 0,65 1,05 mmol/l. Diagnostinė vertė. Dehidratacija, inkstų nepakankamumas (ūminis ar lėtinis), nekontroliuojamas cukrinis diabetas (retai), antinksčių žievės funkcijos nepakankamumas, Adisono liga, audinių trauma, hipotirozė, raudonoji vilkligė, dauginė mieloma. Nepakankamas vartojimas ir (ar) absorbcija iš žarnyno (malabsorbcijos sindromas, kai maiste mažai baltymų ir kalorijų), ūminis pankreatitas, hipoparatirozė, lėtinis alkoholizmas, baltoji karštigė, padidėjus Mg poreikiui, didelis organizmo skysčių netekimas, lėtinis glomerulonefritas, sutrikęs Mg sulaikymas inkstuose (pvz., hiperkalcemija esant hiperparatirozei), hiperaldosteronizmas, diabetinė acidozė, intensyvi laktacija, nepakankama antidiurezinio hormono sekrecija, nėštumas (antras ir trečias trečdalis); kai kurie hipomagnezemijos atvejai yra idiopatiniai. Tetanija atsiranda, kai magnio kiekis 0,15 0,50 mmol/l, esant normaliai kalcio koncentracijai ir ph. Papildoma informacija. Serume Mg kiekis gali išlikti normalus net jei bendras organizmo Mg kiekis išeikvojamas iki 20%. Riebalų rūgštys, per didelis fosfatų kiekis maiste sutrikdo Mg absorbciją. Hipomagnezemija gali sutrikdyti parathormono sekreciją ir jo veiklą. Nepakankamumo simptomai neišryškėja, kol serume magnio kiekis pasidaro mažesnis kaip 0,5 mmol/l. Ryškiai stokai būdingas silpnumas, irzlumas, tetanija, elektrokardiogramos pokyčiai, kliedėjimas, traukuliai. Vertikalioje kūno padėtyje Mg padaugėja 4%. Netinkamas vaistų (pvz., magnio sulfato) dozavimas ar antacidiniai vaistai padidina magnio kiekį serume. Hipermagnezemija sustiprina hiperkalemijos poveikį širdžiai. Sunkios formos hipermagnezemijos poveikis: 2,50 5,00 mmol/l: sulėtina širdies laidumo sistemos darbą; 5,00 6,50 mmol/l: dingsta giliųjų sausgyslių refleksai; 7,50 mmol/l: vystosi kvėpavimo paralyžius; galima generalizuota anestezija; >12,50 mmol/l: širdis sustoja esant raumens diastolei. Apie 65 70% Mg yra jonizuoto, o 35% serume esančio Mg yra susijungusio su baltymais. Koncentracija smegenų skystyje ir eritrocituose analogiška kiekiui serume. V: aspirinas (ilgas vartojimas), litis, magnio produktai, progesteronas, triamterenas, D vitaminas (lėtinis inkstų nepakankamumas). V: aldosteronas, aminoglikozidai, amonio chloridas, amfotericinas B, citratas (kraujo perpylimas), ciklosporinas, digoksinas, diuretikai (pvz., etakrino rūgštis, furozemidas, tiazidai), etanolis, gliukagonas, insulinas (didelės dozės ištikus diabetinei komai), kalcio druskos, geriamieji kontracepikai, vidurius laisvinantys vaistai (ilgalaikis vartojimas). Ge l e ž i s Geležies apykaita. Žmogaus organizmui geležis (Fe) yra labai svarbus elementas, nes yra hemo nebaltyminės hemoglobino dalies jonas. Hemoglobinas perneša deguonį iš plaučių į audinius, todėl sutrikus hemo sintezei vystysis anemija, o audiniuose hipoksija. Hemas yra ir raumenų mioglobino sudedamoji dalis. Citochromai ir kiti ląsteliniai fermentai taip pat turi hemą, tačiau jų sintezė gali sutrikti tik esant labai ryškiai geležies stokai. 237
239 Organizme yra apie mmol (3 3,5 g) geležies. 3/4 jos yra hemo pavidalu, o kita dalis, susijungusi su baltymu feritinu ir hemosiderinu, daugiausia yra kepenyse, blužnyje ir kaulų čiulpuose kaip atsargos. Feritino molekulėje jos pirmtako apoferitino, kurio molekulinė masė yra daltonų, sluoksnis dengia šerdinę dalį, kurioje yra Fe +3 atomų. Geležiai atsipalaiduojant iš feritino molekulės vyksta nefermentinė Fe +3 redukcija į Fe +2. Tai hemoglobino ir kitų hemą turinčių junginių gamybai greitai naudojamas geležies šaltinis. Kai organizme trūksta apoferitino geležiai surišti, pastaroji įsotina audinių feritiną (audiniuose taip pat randama mažų geležies oksido kristalų). Hemosiderinas yra kita geležies kaupimo forma tai agreguotas ir iš dalies deproteinizuotas feritinas. Jis yra netirpus vandenyje, todėl geležis iš jo atsipalaiduoja lėtai. Apie 25% geležies atsargų organizme aptinkama feritino ir hemosiderino pavidalu. Mažiau negu 1% visos organizmo geležies yra kraujo plazmoje, kur ji yra susijungusi su geležį pernešančiu baltymu transferinu apotransferino ir Fe +3 kompleksu. Transferinas yra β 1 globulinams priklausantis kepenyse sintetinamas baltymas, kurio molekulinė masė yra daltonų ir gyvavimo puslaikis 10 dienų. Jo koncentracija kraujo serume yra 2 3,6 g/l. Kiekviena šio baltymo molekulė suriša du Fe 3+ su rūgščiojo karbonato anijonu. Kraujo plazmoje geležies koncentracija įvairuoja pagal žmogaus amžių ir lytį. Sveikų suaugusių vyrų serume jos yra 9,5 29,9 µmol/l, moterų 8,8 27,0 µmol/l. Su maistu per dieną gaunama apie 0,35 mmol (iki 20 mg) geležies (19 pav.). Kadangi organizme geležis yra labai efektyviai išsaugoma, tai virškinamajame trakte pakanka kasdien absorbuoti 6 12% su maistu patekusios geležies. Augimo ir nėš- Geležies suvartojimas apie 20 mg per dieną (0,35 mmol per dieną) 5 10% (1 2 mg) Absorbuojama Apie 90% šalinama Eritrocituose apie 75% Feritino pavidalu apie 20% Mioglobino pavidalu apie 5% Geležies netekimas su pleiskanomis, per mėnesines 19 pav. Geležies pusiausvyra organizme tumo metu geležies poreikis padidėja, tada ir absorbcija išauga nuo 1,3 mg iki 4 mg per dieną. Nemažai veiksnių gali sumažinti geležies koncentraciją plazmoje, kad ir koks būtų jos kiekis organizme. Tai ūminė reakcija į infekciją, traumą ar piktybinį procesą. Geležies apykaitos sutrikimų laboratorinė diagnostika. Geležies apykaitos sutrikimai nustatomi įvairiais tyrimais. 238
240 Magnio, geležies ir vario apykaita Serumo geležies koncentracijos nustatymas. Tai geležis, kuri yra prisijungusi prie transferino. Šio tyrimo galimybės ribotos, jis tinkamiausias geležies pertekliaus ar apsinuodijimo geležimi diagnostikai. 2. Geležies sujungimo bendroji geba (angl. total iron binding capacity TIBC) tai netiesioginis transferino koncentracijos matas, nors transferino kiekį galima nustatyti ir tiesiogiai. Normaliai 1/3 (30%) transferino yra įsotintas geležimi. Kai jo sumažėja iki 15%, atsiranda geležies stoka. Didelis įsotinimo procentas yra jautriausias geležies pertekliaus rodiklis. Geležies sujungimo laisvoji geba (angl. unsaturated iron binding capacity UIBS) atspindi transferino geležies atsargą ir yra apskaičiuojama iš TIBC atėmus serumo geležies koncentraciją. Kaip ir serumo geležies, transferino taip pat sumažėja esant ūminei reakcijai. Vartojant mažai baltymų, transferino sintezė kepenyse ir jo koncentracija kraujo serume sumažėja. 3. Serumo feritino koncentracija. Sveikų asmenų kraujyje feritino koncentracija yra daugiau negu 12 µg/l (vyrų µg/l, moterų µg/l) ji proporcinga geležies atsargų dydžiui, todėl yra geriausias geležies atsargų rodiklis. Ūminės reakcijos (į infekciją, pažaidą ar piktybinį procesą) metu feritino koncentracija didėja ir tuomet geležies stoką nustatyti sunku. Geležies stoka. Dėl geležies stokos išsivysčiusi anemija yra viena dažniausių ligų, atsirandančių trūkstant organizme vienos iš maisto sudedamųjų dalių. Šia liga pasaulyje serga milijonai žmonių, ji sutrikdo žmogaus sveikatą ir sumažina darbingumą. Pagrindinės geležies stokos priežastys yra lėtinis kraujavimas ir nepakankamas organizmo aprūpinimas geležimi, t. y. prasta mityba. Dvivalentės geležies įsisavinimą sumažina kai kurios maisto sudedamosios dalys, kaip fitano rūgštis ir skaidulingos medžiagos, pagerina C vitaminas. Geležies stoka taip pat galima esant celiakijai ir kitoms virškinimo sistemos organų ligoms, kai sutrinka medžiagų absorbcija iš žarnyno. Visais geležies stokos atvejais svarbu nustatyti priežastį, ypač piktybinį procesą, žarnyno parazitus ar kitą virškinamojo trakto patologiją, kuri sukelia lėtinę kraujo netektį. Geležies stoka gali išsivystyti nėštumo metu dėl padidėjusio jos poreikio vaisiui. Geležies stokos anemijos eigą sudaro trys etapai: 1. Geležies atsargų išnaudojimas, kai nėra funkcinių sutrikimų. Ši būklė patvirtinama, kai serumo feritino koncentracija yra mažesnė negu 12 µg/l. 2. Sutrikdyta eritropoezė. Hemoglobino koncentracija normali, bet eritrocituose yra sumažėjęs protoporfirino IX kiekis. Transferino sintezė padidėja, o įsotinimo procentas sumažėja. Kai įsotinimas sumažėja daugiau kaip 15%, sutrinka darbingumas. 3. Geležies stokos anemija. Nustatoma maža hemoglobino koncentracija, išryškėja mikrocitinė hipochrominė anemija. Kaulų čiulpuose yra mažai dažymu 239
241 aptinkamos geležies. Tik vėlesnėse stadijose serumo geležies koncentracija yra maža. Geležies perteklius. Geležies iš organizmo šalinimo vieninteliai būdai yra paviršinio sluoksnio ląstelių ir slaptas kraujo netekimas, todėl gydant geležies preparatais visada yra geležies pertekliaus tikimybė. Geležies perteklius organizme gali susidaryti ir kartotinai perpilant kraujo. Kitos būklės, susijusios su geležies pertekliumi, yra hemochromatozė ir apsinuodijimas geležimi. Hemochromatozė ( bronzinis diabetas). Tai dažna paveldima liga, kuriai būdinga padidėjusi geležies absorbcija ir jos kaupimasis (dėl netirpaus hemosiderino daugėjimo) parenchiminiuose organuose, daugiausia kepenyse, inkstuose, blužnyje. Dėl to vystosi fibrozė ir organų veiklos nepakankamumas. Kliniškai tai išryškėja įvairiai pagal geležies kiekį maiste, alkoholio, kitų kepenis pažeidžiančių medžiagų vartojimą. Moterys serga rečiau negu vyrai, nes jas apsaugo fiziologinis kraujo netekimas per mėnesines ir nėštumas. Bendrasis geležies kiekis organizme gali padidėti dešimtis kartų. Ligos klinika lėtinis nuovargis, rečiau odos pigmentacija, cukrinis diabetas, sutrikusi lytinių liaukų funkcija, kepenų cirozė ir hepatoma. Kraujo plazmoje geležies kiekis padidėja, transferinas būna beveik visiškai įsotintas geležimi. Serume feritino kiekis viršija 500 µg/l. Apsinuodijimas geležimi. Geležies preparatų, pavyzdžiui, geležies tablečių, kad ir atsitiktinis vartojimas, vaikams gali būti pavojingas gyvybei ir sukelti pykinimą, vėmimą, pilvo skausmus, viduriavimą, vėmimą krauju. Sunkesniais atvejais krinta kraujospūdis, pažeidžiamos kepenys, vystosi koma. Serume geležies kiekis padidėja, transferino įsotinimas ja gali viršyti 70%. Api b e n d r i n i m a s Geležies stoką dažniausiai sukelia geležies netekimas ir mažas jos kiekis maiste. Mikrocitinė hipochrominė anemija, kai kaulų čiulpai nenusidažo būdingais geležiai dažikliais, yra geriausias geležies stokos diagnostikos požymis. Serumo feritino koncentracija yra patikimas geležies stokos organizme biocheminis rodiklis. Geležies perteklius gali išsivystyti kartotinai perpilant kraujo. Geležies perteklius nustatomas, kai geležies koncentracija, transferino įsotinimas ja ir serumo feritino kiekis yra padidėję. 240
242 Magnio, geležies ir vario apykaita... Laboratoriniai tyrimai Feritinas Tiriamoji medžiaga. Serumas. Rekomenduojama reikšmė (µg/l): naujagimių ; 1 mėn. amžiaus ; 2 5 mėn. amžiaus ; 6 mėn. 15 m. amžiaus 7 140; suaugusiųjų: vyrų ; moterų Diagnostinė vertė. Organizmo patiriama geležies perkrova (pvz., hemochromatozė, kai kurios kepenų ligos). Badavimas ar išsekimas, ūminė leukemija, uždegiminės ligos (pvz., plaučių infekcija, osteomielitas, lėtinės šlapimo takų infekcijos, reumatoidinis artritas, sisteminė raudonoji vilkligė, nudegimai), ūminės ir lėtinės kepenų ligos (pvz., alkoholinė ir uždegiminė kepenų liga), ūminė mieloblastinė ir limfoblastinė leukemija, Hodžkino liga, krūties vėžys. Feritino padaugėjimas esant uždegiminėms būklėms (ūminės uždegimo fazės atsakas) gali maskuoti diagnostiškai mažą rezultatą. Geležies stoka. Papildoma informacija. Feritinas susidaro mononuklearinėje fagocitinėje sistemoje. Jis susideda iš baltyminio apvalkalo apoferitino ir šerdyje įvairuojančio kiekio geležies, esančios geležies hidroksido ar fosfato kompleksų pavidalu. Plazmos feritinas turi 20 25% geležies. Jos koncentracija yra geras geležies atsargų matas. Geležies prisijungimui prie feritino būtina jos oksidacija: Fe 2+ Fe 3+. V: etanolis (alkoholikai), geležies druskos, geriamieji kontraceptikai. V: eritropoetinas. Geležis (Fe) Tiriamoji medžiaga. Serumas. Rekomenduojama reikšmė. Vyrų 9,5 29,9 µmol/l, moterų 8,8 27,0 µmol/l. Diagnostinė vertė. B 12 vitamino stokos anemija, aplazinė ir hemolizinė anemija; hemochromatozė; ūminė leukemija; apsinuodijimas švinu; ūminis hepatitas; B 12 vitamino stoka; talasemija, geležies perteklius gydant; kartotiniai kraujo perpylimai; ūminis apsinuodijimas geležimi (vaikai); nefritas. Geležies stokos anemija; B 12 vitamino stokos anemijos remisija; ūminės ir lėtinės infekcijos; vėžys; nefrozė; hipotirozė; būklė po operacijos. Papildoma informacija. Geležies sulfatas yra nereta vaikų apsinuodijimo geležimi priežastis. Būdingas pilvo skausmas, vėmimas, viduriavimas su krauju, cianozė, mieguistumas, traukuliai. Fe tyrimas pacientams po kraujo perpylimo turi būti atliekamas praėjus kelioms dienoms po procedūros. Naujagimių geležies kiekis sumažėja po kelių valandų užgimus. V: chloramfenikolis, estrogenai, metotreksatas, geriamieji kontraceptikai, švinas. V: alopurinolis, anaboliniai steroidai, aspirinas (didelės dozės), kortizonas, kortikotropinas, metforminas. Geležies sujungimo bendroji geba (angl. TIBS) Tiriamoji medžiaga. Serumas. Rekomenduojama reikšmė. 44,8 80,6 µmol/l. Diagnostinė vertė. Hipochrominė anemija, ūminis hepatitas, paskutiniai nėštumo mėnesiai. Anemija (ne geležies stokos), lėtinės infekcijos, hemochromatozė, cirozė, neoplazinės inkstų ligos. 241
243 Papildoma informacija. GSBG pokyčiai koreliuoja su transferino kiekio serume kitimu, bet ryšys nėra tiesinis ir visai nutrūksta sergant ligomis, kurios sutrikdo transferino sujungimo gebą bei kitų geležį sujungiančių baltymų funkcijas. Geležies sujungimo laisvoji geba (angl. UIBS) Tiriamoji medžiaga. Serumas. Rekomenduojama reikšmė µmol/l. Papildoma informacija. Atspindi transferino geležies sujungimo gebą. Transferinas Tiriamoji medžiaga. Serumas. Rekomenduojama reikšmė. 2 3,6 g/l. Diagnostinė vertė. Estrogenai (nėštumas, geriamieji kontraceptikai), geležies stoka (padidėja net keliais mėnesiais anksčiau negu išsivysto anemija). Paveldima atransferinemija (retai), bet kuri būklė, susijusi su uždegimu ir nekroze; piktybinis procesas, ypač apatinėse žarnyno dalyse; bloga mityba, nefrozinis sindromas; būklės, kai padidėja onkotinis slėgis (dauginė mieloma, kepenų ligos). Kraujo plazmoje transferino mažėja, kai organizmas patiria geležies perkrovas (pvz., dažni kraujo perpylimai, paveldimoji hemochromatozė). Tyrimui indikacijos yra anemijų diferencinė diagnostika. Geležies stokos ar pertekliaus būkles geriausiai atspindi geležies kiekio, transferino ir feritino tyrimai. Papildoma informacija. Transferinas yra pagrindinis geležį nešantis baltymas. Normaliai homeostazei reikia nedidelio transferino kiekio. Nedidelis neįsotinto geležimi transferino kiekis yra svarbus žymuo, rodantis infekcijas bei geležies atsargas organizme naudojančių organizmų invaziją. 1 mg transferino sujungia 1,25 µg geležies. Taigi transferino kiekis 3,0 g/l atitinka bendrą geležies sujungimo gebos rodiklį 3,75 g/l. Smegenų skystyje transferinas yra be sialo grupės, t. y. τ (tau) baltymas (β 2 transferinas). Šią formą galima aptikti tiriant elektroforeze ir imunofiksacija su antikūnais prieš transferiną. τ (tau) baltymas svarbus nustatant rinorėją, otorėją, nes jis rodo smegenų skysčio nutekėjimą pro kaukolės lūžių vietas ar po operacijos. Šis baltymas yra gausaus alkoholio vartojimo žymuo. V: estrogenai, geriamieji kontraceptikai. V: kortikotropinas, gliukokortikoidai, testosteronas. Va r i s Vario apykaita. Varis (Cu) yra svarbus elementas, įeinantis į didelės grupės metalofermentų sudėtį: citochromoksidazės, superoksiddismutazės, urikazės, dopaminhidroksilazės, tirozinazės, ceruloplazmino; varis dalyvauja ir vitaminų, hormonų, baltymų, angliavandenių apykaitoje, imuniniuose procesuose. Nemažai patologinių būklių yra susijusių su vario turinčių fermentų stoka: jungiamojo audinio užpildo kryžminių jungčių defektai, pigmentacijos nebuvimas, ataksija, sutrikusi katecholaminų apykaita. Dar viena svarbi vario funkcija kraujodaros: gerina geležies pernešimą į kaulų čiulpus, taigi lemia hemoglobino sintezę, o vario stoka sutrikdo geležies absorbciją iš žarnyno. Varis veikia panašiai kaip insulinas stiprina priekinės hipofizės aktyvumą. 242
244 Magnio, geležies ir vario apykaita... Vario kraujo plazmoje būna laisvojo (10%) ir susijungusio su α 2 globulininiu baltymu ceruloplazmino pavidalu. Ceruloplazminas pasižymi feroksidaziniu aktyvumu, t. y. oksiduoja Fe 2+ į Fe 3+ prieš pastarajam susijungiant su plazmos transferinu. Apie 50% su maistu patekusio į organizmą vario (25 μmol, 1,5 mg) yra absorbuojama skrandyje ir plonojoje žarnoje, daugiausia dvylikapirštėje; jis jungiasi su albuminu ir yra nešamas į kepenis, kur kaupiamas, iki bus panaudotas. Iš kepenų varis išsiskiria ceruloplazmino pavidalu (jame yra 90 95% organizme esančio vario). Vario yra visuose metaboliškai aktyviuose audiniuose, daugiausia kepenyse ir inkstuose, taip pat širdies, griaučių raumenyse, kauliniame audinyje. Varis šalinamas su išmatomis: neabsorbuotas žarnyne, taip pat išsiskyręs per tulžies pūslę ir kaip žarnų sekretas. Vario apykaita tiriama nustatant vario koncentraciją kraujo serume (rekomenduojama norma 11,0 24,4 μmol/l ) ir šlapime (normaliai šalinama 1 μmol/l), taip pat ceruloplazmino koncentraciją kraujo serume (rekomenduojama norma 0,2 0,6 g/l). Klinikinė reikšmė. Vario stoka galima prieš laiką gimusiems naujagimiams, nes jo atsargos kepenyse pradeda kauptis trečią nėštumo trečdalį. Suaugusiesiems vario stoka gali išsivystyti po žarnyno operacijų (pašalinus dalį plonosios žarnos), maitinant parenteraliu būdu. Svarbiausi vario stokos simptomai yra šie: neutropenija ir hipochrominė anemija, osteoporozė ir kaulų bei sąnarių funkcijos sutrikimai, sumažėjusi odos pigmentacija, vėlesnėse stadijose nervų sistemos pažeidimo požymiai. Apsinuodijimas variu galimas į virškinamąjį traktą patekus vario turinčių medžiagų, pavyzdžiui, vario druskų (vario sulfato), ar neatsargiai elgiantis su vario turinčiais fungicidais. Apsinuodijus prasideda pykinimas, vėmimas, skausmas pakrūtinyje, viduriavimas; vėliau galima hemolizė, kepenų nekrozė, kraujavimas iš virškinamojo trakto, inkstų kanalėlių pažeidimas ir visi iš to išplaukiantys padariniai, traukuliai, koma. Vario apykaitos sutrikimai Hiperkupremija ir hiperceruloplazminemija susijusios su tirotoksikoze, kepenų ligomis (hepatitu, kepenų ciroze, mechanine gelta), anemija, infekcinėmis ligomis, nėštumu, priešmenstruaciniu laikotarpiu, sergant vėžiu, leukemija. Ceruloplazminas yra uždegimo ūminės fazės reaktantas. Hipokupremija ir hipoceruloplazminemija išsivysto susilpnėjus skydliaukės funkcijai dėl lėtinio apsinuodijimo cheminėmis medžiagomis (anilino dažais, gyvsidabriu, švinu), esant nefroziniam sindromui, naujagimiams, turintiems paveldimą vario apykaitos defektą Vilsono ligą (hepatolentikulinę degeneraciją). Vilsono liga tai paveldima vario apykaitos liga, kurios klinika išryškėja 6 20 metų individams, o dažnis yra apie 1: Manoma, kad priežastis yra defektyvus genas, koduojantis baltymą, kuris šalina varį su tulžimi ir reabsorbuoja inkstuose. 243
245 Sergant šia liga, kepenyse, smegenyse, inkstuose, ragenoje kaupiasi varis ir jo padidėjęs kiekis šalinamas su šlapimu. Plazmoje sumažėja vario, ceruloplazmino koncentracija, nes sutrinka vario sąveika su šiuo baltymu ir vario šalinimas su tulžimi. Ligai būdingas nervų sistemos pažeidimas, kepenų cirozė, o ragenoje Kaizerio Fleišerio (Kayser Fleischer) žiedas (žalsvai rudos spalvos sankaupos). Diagnozė patvirtinama atlikus kepenų biopsiją ir nustačius jose padidėjusį vario kiekį. Apie ceruloplazminą detaliau rašoma skyriuje Žmogaus kraujo plazmos baltymai, jų tyrimas, rezultatų klinikinis interpretavimas. Api b e n d r i n i m a s Bendroje populiacijoje vario stoka gali būti širdies ir kraujagyslių ligų rizikos veiksnys. Įrodyta, kad maiste stingant vario ir vartojant daugiau angliavandenių, vystosi hipercholesterolemija. Vario stoką galima nustatyti matuojant vario koncentraciją kraujyje. Detaliau būtina ištirti, kai suaugusiųjų organizme vario koncentracija serume yra <10 μmol/l, o naujagimių <5 μmol/l. Paveldimas vario apykaitos sutrikimas sukelia Vilsono ligą. Laboratoriniai tyrimai Varis (Cu) Tiriamoji medžiaga. Serumas. Rekomenduojama reikšmė. 11,0 24,4 µmol/l. Diagnostinė vertė. Su amžiumi, infekcijos, uždegimas, nėštumas, leukemija, biliarinė cirozė, vidurių šiltinė, Hodžkino liga, plaučių tuberkuliozė, pelagra, dauguma anemijų, talasemijos, reumatinė karštinė, ūminis miokado infarktas, smegenų infarktas, ankilozuojantis spondilitas, reumatoidinis artritas, hipotirozė ir hipertirozė, kolageno ligos, sisteminė raudonoji vilkligė, inkstų dializės ir kraujo perpylimo naujagimiams komplikacijos, trauma ir piktybiniai virškinamojo trakto, plaučių, kaulų, krūties, gimdos kaklelio ir kraujodaros sistemos navikai. Vilsono liga, virškinamojo trakto ligos, cistinė fibrozė, nefrozinis sindromas, AKTH ar prednizolono sukelta leukemijos remisija, kai kurios geležies stokos anemijos, nudegimai, lėtinė koronarinė širdies liga, baltymų stoka maiste. Gydant estrogenais (ir nėštumo metu) labai suintensyvėja ceruloplazmino sintezė kepenyse. Dėl to plazmoje vario kiekis gali padvigubėti. Plazmoje ceruloplazmino taip pat daugėja vartojant geriamųjų kontraceptikų, vaistų nuo epilepsijos (karbamazepino, fenobarbitalio). Papildoma informacija % plazmoje esančio vario įeina į ceruplazmino sudėtį. Pastarasis veikia kaip vario oksidazė. Vario absorbcija sutrinka esant difuzinei plonosios žarnos ligai, per daug vartojant konkuruojančių cinko ir kadmio jonų. Vario stoka galima ilgai parenteriniu būdu maitinant mažai metalų jonų turinčiu maistu, gydant cinku ar vario chelatais (pvz., penicilaminu). Vario stokos klinikiniai požymiai yra neutropenija, anemija (nereguoja į gydymą geležimi), osteoporozė, kaulų ir (ar) sąnarių anomalijos, sumažėjusi odos pigmentacija, neurologinė ir 244
246 Magnio, geležies ir vario apykaita... širdies pažeidimo simptomatika. Genetiškai nulemtos vario apykaitos ligos yra šios: Vilsono liga (hepatolentikulinė degeneracija), vario kaupimosi liga; retas Menkeso plieninių plaukų sindromas; naujagimių vario stokos liga. Vario smegenų skystyje padaugėja įvykus smegenų infarktui, sinoviniame skystyje sergant reumatoidiniu artritu. Apsinuodyti variu galima suvalgius maisto, užteršto fungicidais, taip pat jei įdėta gimdos spiralė, turinti vario. Būdingi požymiai: pykinimas, vėmimas, galvos skausmas, viduriavimas, pilvo skausmai. Palaipsniui pažeidžiamos kepenys, vystosi gelta, hemolizinis šokas. Sergant Vilsono liga, vario ir ceruloplazmino serume mažėja dėl sulėtėjusios ceruplazmino sintezės kepenyse, o vario šalinimas su šlapimu ir vario kiekis kepenyse didėja Tiriamoji medžiaga. Paros šlapimas. Rekomenduojama reikšmė. 1 µmol/l. Diagnostinė vertė. Vilsono liga, lėtinis aktyvusis hepatitas, biliarinė cirozė, reumatoidinis artritas, proteinurija. Baltymų stoka maiste. Papildoma informacija. Nustatymas šlapime vertingas Vilsono ligos diagnostikai ir gydymo efektyvumo vertinimui. 245
247 LIPOPROTEINAI, JŲ SUDĖTIS, APYKAITA IR SUTRIKIMŲ LABORATORINĖ DIAGNOSTIKA Lipidai, l i p o p r o t e i n a i ir li g o s Koronarinė širdies liga (KŠL) yra pagrindinė darbingo amžiaus žmonių invalidumo ir mirties priežastis ne tik Lietuvoje, bet ir kitose išsivysčiusiose šalyse. Širdies ir kraujagyslių ligos yra dažnesnės negu bet kurios kitos, tarp jų ir vėžys. Jau seniai nustatytas ryšys tarp cholesterolio kiekio kraujyje ir širdies bei kraujagyslių ligų. Kuo daugiau cholesterolio kraujyje, tuo didesnė tikimybė išsivystyti KŠL, o sumažėjus cholesterolio kiekiui 1%, miokardo infarkto tikimybė sumažėja 2%. Kraujyje cholesterolio bei triacilglicerolių (trigliceridų) padaugėja dėl įvairių priežasčių. Kai kurios jų yra pirminės dėl genetinių lipidų ir lipoproteinų apykaitos defektų, kitos yra antrinės, kai ši apykaita sutrinka dėl kitų priežasčių ar ligų. Dažniausios jų yra cukrinis diabetas, hipotirozė, nefrozinis sindromas, alkoholizmas, sisteminė raudonoji vilkligė, kontraceptinių vaistų vartojimas ir kt. Vakarietiška gyvensena, susijusi su nutukimu ir gyvūninių riebalų gausaus maisto vartojimu, yra viena dažniausių padidėjusio lipidų ir lipoproteinų kiekio kraujyje priežasčių. Genetinės priežastys taip pat neretos. Maždaug 1 žmogus iš 500 turi genų defektą, lemiantį šeiminę hipercholesterolemiją, kurios klinikoje vyrauja aterosklerozė ir jos komplikacijos (stenokardija, miokardo infarktas, staigi mirtis). Dar dažnesnės yra poligeninės, t. y. genetinių ir aplinkos veiksnių sukeltos, hiperlipidemijoss. Lipoproteinų nomenklatūra ir klasifikacija Nors kraujyje dažniausiai matuojamos lipidų triacilglicerolių ir cholesterolio koncentracijos, nei triacilgliceroliai, nei cholesterolis, nei kiti lipidai (pvz., riebalų rūgštys) netirpsta vandenyje, o su krauju gali būti nešamos tik vandenyje tirpios medžiagos. Tokia tirpi šių lipidų forma yra lipoproteinai. Juos sudaro riebalai triacilgliceroliai, cholesterolis ir jo esteriai, fosfolipidai, riebaluose tirpūs vitaminai bei specifiniai baltymai (20 pav.). Kraujo plazmos lipoproteinų klasifikacijos pagrindas yra jų elektroforezinis judrumas ir flotacijos greitis ultracentrifuguojant. Lipoproteinų frakcijų, išskirtų trimis pagrindiniais metodais, sinonimai pateikiami 26 lentelėje. 246
248 Lipoproteinai, jų sudėtis, apykaita... Fosfolipidai Cholesterolis Cholesterolio esteriai Triacilgliceroliai Baltymai 20 pav. Lipoproteino dalelės sandaros schema 26 lentelė. Lipoproteinų, išskirtų trimis metodais, sinonimai Elektroforezė β lipoproteinai (β LP) Pre-β lipoproteinai (pre-β LP) α lipoproteinai (α LP) Preparacinis ultracentrifugavimas Mažo tankio lipoproteinai (MTL) Labai mažo tankio lipoproteinai (LMTL) Didelio tankio lipoproteinai (DTL)! Analizinis ultracentrifugavimas S f yra iki 20 S f yra F 1,20 yra iki 9 S f flotacijos greitis Svedbergo vienetais (10-13 cm/s/din/g). Šis greitis priklauso nuo tirpalo tankio, kuris lygus 1,063 g/ml. Dalelės, kurios yra lengvesnės už terpę, flotuoja ultracentrifugos gravitacijos lauke. Juo didesnė S f reikšmė, juo didesnis flotacijos greitis. Be to, flotacijos greitis proporcingas mažesniam dalelių tankiui, didesniam lipidų kiekiui dalelėje, didesniam dalelės skersmeniui. Dydis F rodo flotacijos greitį, kai nustatytas dalelių tankis. Lipoproteinams būdinga lipidų ir baltymų įvairovė. Į jų sudėtį įeina skirtingų baltymų. Lipoproteinų baltymai vadinami apolipoproteinais, arba apoproteinais (sutrumpintai apo). Svarbiausi lipidiniai komponentai yra triacilgliceroliai, laisvasis cholesterolis ir jo esteriai, fosfolipidai. Mažesniais kiekiais randama laisvųjų riebalų rūgščių, monoglicerolių ir diglicerolių. Lipidų ir baltymų ryšio ypatybė yra ta, kad lipidai gana lengvai ekstrahuojami lipidų tirpikliais. Baltyminė ir lipidinė dalys keičiasi ir sąveikauja tarp skirtingų lipoproteinų. Plazmos lipoproteinų sudėtis ir jų funkcijos apibūdinamos 27 lentelėje. Pabrėžtina, kad lipidinė net ir vienos klasės lipoproteinų sudėtis kinta, pavyzdžiui, priklausomai nuo mitybos ypatybių. Be to, kiekvienoje lipoproteinų klasėje galima išskirti poklasius arba frakcijas, besiskiriančias dalelių dydžiu, elektroforeziniu judrumu, dedamųjų dalių kiekiu. Kraujo plazmos lipoproteinai tai globulinės dalelės, kurių kiekvienoje galima išskirti šerdinę dalį ir paviršinį sluoksnį. Pagal lipoproteinų struktūros modelį, ne- 247
249 27 lentelė. Žmogaus kraujo plazmos lipoproteinų sudėtis ir funkcijos Rodikliai Chilomikronai LMTL MTL DTL Sudėtis: baltymai, % lipidai, % 0, , Pagrindinis lipidas Triacilgliceroliai Triacilgliceroliai Cholesterolis Cholesterolis, fosfolipidai Kilmė Žarnynas Kepenys ir žarnynas LMTL apykaitos kraujyje produktas Kepenys ir žarnynas Funkcijos Egzogeninių triacilglicerolių pernaša Endogeninių triacilglicerolių pernaša Cholesterolio pernaša į periferinius audinius Cholesterolio pernaša iš periferinių audinių į kepenis poliniai lipidai triacilgliceroliai ir cholesterolio esteriai yra susitelkę dalelės šerdyje, o baltymai, fosfolipidai ir laisvasis cholesterolis sudaro dalelės paviršinį sluoksnį. Šio paviršinio sluoksnio storis yra apie Å, kas atitinka pusę fosfolipidinio dvisluoksnio, būdingo ląstelės membranai. Taigi lipoproteino dalelės paviršiuje yra ne du, o vienas fosfolipidų sluoksnis. Tarp baltymų ir lipidų esti netvirti vandeniliniai ryšiai bei elektrostatinė sąveika. Naujai sintetinami ir sekretuojami (pirminiai, arba natyviniai) lipoproteinai sudėtimi ir struktūra skiriasi nuo kraujyje cirkuliuojančių lipoproteinų. Pagrindiniai kraujo plazmos lipidai ir jų funkcijos Nors padidėjęs dviejų pagrindinių lipidų, t. y. cholesterolio ir triacilglicerolių, kiekis kraujyje yra susijęs su širdies ir kraujagyslių ligomis, šie lipidai yra labai svarbūs ir būtini žmogaus organizmui. Kraujo plazmos lipidai sudaro didelę grupę biologinių medžiagų, kurioms būdingesnis fizinių negu struktūrinių savybių bendrumas. Lipidai skirstomi į nepolinius ir polinius. Pirmieji triacilgliceroliai ir cholesterolio esteriai, kurie sudaro kraujo plazmos lipoproteinų dalelės šerdį. Pastarąją nuo vandeninės aplinkos skiria polinių lipidų, t. y. fosfolipidų ir laisvojo cholesterolio, bei specifinių baltymų apolipoproteinų sluoksnis. Triacilgliceroliai (trigliceridai, TG) yra glicerolio ir trijų riebalų rūgščių esteriai. Tai pagrindinis riebalų rūgščių šaltinis organizme. Jie sudaro didžiausią dalį tų lipidų, kurie vadinami riebalais. Iš laisvųjų riebalų rūgščių raumeniniame audinyje (ypač širdyje) susidaro daug energijos. Ramybės būklės griaučių raumenims jos teikia maždaug 50% energijos. Polinesočiosios riebalų rūgštys yra labai svarbios organizmui, nes įeina į membranos fosfolipidų sudėtį; kai kurios yra prostaglandinų pirmtakai ir yra įvairių organizmo lipidų sudedamoji dalis. Žmogaus organizmo riebaluose vyrauja oleino ir palmitino rūgštys. Dvi polinesočiosios riebalų rūgštys linolo ir α linoleno žmogaus organizme nesintetinamos, todėl jų būtina gauti su maistu (daug yra aliejuose). 248
250 Lipoproteinai, jų sudėtis, apykaita... Su maistu į organizmą patekusius triacilglicerolius virškinamajame trakte hidrolizuoja lipazės. Šiame procese susidarę monogliceroliai, riebalų rūgštys ir glicerolis yra rezorbuojami micelių pavidalu. Žarnų gleivinės epitelio ląstelėse iš rezorbuotų hidrolizės produktų resintetinami triacilgliceroliai. Jie sekretuojami iš ląstelių chilomikronų pavidalu. Triacilglicerolių sintezės greitis žarnų epitelio ląstelėse priklauso nuo rezorbuotuose trigliceriduose esančių riebalų rūgščių kiekio. Per parą į organizmą su maistu vidutiniškai patenka apie g riebalų (galima iki 300 g). Organizme triacilgliceroliai sintetinami kepenų, riebalinio audinio, raumenų, plonosios žarnos gleivinės ląstelių endoplazminiame tinkle. Į kepenis riebalų rūgštis iš riebalinio audinio atneša albuminai. Be to, čia patenka ir dalis riebalų rūgščių, susidariusių hidrolizuojant chilomikronų likučiuose (remnantuose) esančius triacilglicerolius. Šios riebalų rūgštys sudaro maždaug 1/3 visų riebalų rūgščių, patenkančių į kepenis. Jei su maistu vartojama daug angliavandenių, tai dalis jų kepenyse paverčiama riebalų rūgštimis (riebaliniame audinyje triacilgliceroliai sudaro 60 85% jų masės). Chilomikronuose ir labai mažo tankio lipoproteinuose esančius triacilglicerolius hidrolizuoja kraujagyslių endotelio paviršiaus lipoproteinlipazė. Po hidrolizės pasigaminusios riebalų rūgštys audiniuose sunaudojamos (oksiduojamos arba iš jų yra sintetinami ir kaupiami triacilgliceroliai). Dalis riebalų rūgščių, sudariusių kompleksus su albuminais, cirkuliuoja kraujyje. Triacilgliceroliai kepenyse gali būti kaupiami (iki 4%), hidrolizuojami; pagrindinė jų dalis įeina į daug triacilglicerolių turinčius labai mažo tankio lipoproteinus (LMTL), kurie išskiriami į kraują. Taigi kraujyje maisto kilmės (egzogeniniai) triacilgliceroliai yra chilomikronų, o organizme sintetinti (endogeniniai) labai mažo tankio lipoproteinų pavidalo. Laboratoriniu tyrimu nustatomas skirtingų triacilglicerolių mišinys. Cholesterolis yra vienas pagrindinių kraujo plazmos lipoproteinų komponentų. Tai riebaluose tirpus steroidinis alkoholis, randamas gyvūninės kilmės riebaluose. Suaugusio žmogaus organizme jo yra apie 150 g. Ypač gausu smegenyse, kepenyse, inkstuose. Kraujyje apie 70% cholesterolio yra esterifikuota su riebalų rūgštimis. Tyrimais šios abi cholesterolio formos nustatomos kartu kaip bendrasis cholesterolis. Audiniuose laisvojo cholesterolio yra daugiau, nes tai veiklioji jo forma; kaupiami yra jo esteriai. Cholesterolis yra visų lipoproteinų, ląstelių membranų komponentas; jis yra tulžies rūgščių, steroidinių hormonų (antinksčių, lytinių), D 3 vitamino pirmtakas. Cholesterolio gauname su maistu (egzocholesterolis), be to, jo sintetinama visose ląstelėse, daugiausia kepenų. Su maistu į mūsų organizmą per parą patenka iki 700 mg cholesterolio, rezorbuojama 1/3 šio kiekio. Kai su maistu į organizmą patenka labai mažai cholesterolio, kepenys jo per parą sugeba susintetinti apie 1 g. Šio kiekio 80% paverčiama tulžies rūgštimis, likusi dalis pašalinama su tulžimi, per odą. Paprastai apie 2/3 organizme esančio cholesterolio sudaro sintetintas cholesterolis. Su maistu gautus cholesterolio esterius žarnyne hidrolizuoja kasos cholestero- 249
251 lesterazė. Susidaręs laisvasis cholesterolis pereina žarnų epitelio ląstelių membraną. Ląstelėse dalis jo reesterifikuojama ir kartu su triacilgliceroliais bei dalimi laisvojo cholesterolio sekretuojama chilomikronų pavidalu. Cholesterolio į ląstelę patenka iš kraujo plazmoje cirkuliuojančių lipoproteinų arba, kaip minėta, jis yra sintetinamos ląstelėje. Dėl blogo tirpumo vandenyje cholesterolis kraujyje yra pernešamas susijungęs su apolipoproteinais, daugiausia mažo tankio lipoproteinų pavidalu, taip pat kaip didelio tankio ir labai mažo tankio lipoproteinų sudedamoji dalis. Dauguma lipoproteinų (svarbiausia, didelio tankio lipoproteinų) cholesterolio esterių susidaro veikiant fermentui lecitincholesterolaciltransferazei (LCAT). Vienas didžiausių biochemijos laimėjimų tiriant cholesterolio apykaitą atrastas sudėtingas būdas, kuriuo žinduolių organizmo ląstelės sintetina cholesterolį iš acetilkofermento A (acetil-koa) (21 pav.). Acetil-KoA yra bendras produktas, gaunamas iš angliavandenių, riebalų ir baltymų. Ląstelių cholesterolis slopina fermento 3-hidroksi-3-metilgliutaril-koenzimo A (HMG-KoA) reduktazės aktyvumą. Minėtasis fermentas katalizuoja reakciją, kurioje tarpinis produktas HMG-KoA virsta mevalonatu. Jo susidarymu baigiasi pirmasis cholesterolio sintezės etapas. Šiam cholesterolio sintezės ląstelėje reguliavimui labai svarbūs mažo tankio lipoproteinai ir specifiniai ląstelių receptoriai. HMG-KoA reduktazė Acetil- HMG Farnezil- KoA KoA Mevalonatas pirofosfatas Skvalenas Cholesterolis 21 pav. Cholesterolio biosintezės schema Tačiau žmogaus organizme nėra fermentų, kurie katabolizuotų cholesterolį, todėl iš ląstelės jis šalinamas nepakitęs keliais būdais: 1) ląstelė nuolat netenka membranos paviršiaus cholesterolio, kuris pasyviai pereina į kraujo plazmos didelio tankio lipoproteinus; 2) cholesterolis iš kepenų ir žarnų epitelio ląstelių aktyviai išskiriamas su lipoproteinais; 3) cholesterolis paverčiamas kitomis medžiagomis, pavyzdžiui, tulžies rūgštimis kepenyse ar steroidiniais hormonais endokrininėse liaukose, arba jo perteklius yra tiesiog šalinamas iš kepenų su tulžimi. Jei šalinimo procesas sutrinka, tai besikaupiantis cholesterolis pradeda slopinti ląstelės procesus: sumažina dujų difuziją per membraną, fermentų ir receptorių aktyvumą, dėl to ląstelė sensta ir žūva. Dauguma ląstelių neturi oksidacinių cholesterolį transformuojančių sistemų, todėl jose pagrindinis cholesterolio šalinimo būdas yra jo pernaša su lipoproteinais į kepenis ir su tulžimi į žarnyną. Choelsterolio esteriai ląstelėje sintetinami veikiant mikrosomų fermentui acil-koa-cholesterolaciltransferazei (ACAT), kuri iš acil-koa perneša ir prijungia riebalų rūgštį prie cholesterolio 3-hidroksilo grupės. 250
252 Lipoproteinai, jų sudėtis, apykaita... Fosfolipidai yra paviršinio lipoproteinų sluoksnio komponentai. Be glicerolio ir riebalų rūgščių, juose yra fosforo rūgšties ir poliškumo savybę turinčios medžiagos likučių. Jais gali būti azotinės bazės etanolaminas ar cholinas, aminorūgštys serinas ar treoninas bei polialkoholio inozitolio difosfatas ir kt. (pagrindinis jų sintezės tarpinis produktas, kaip ir triacilglicerolių, yra fosfatido rūgštis). Fosfolipidų sintezė vyksta visuose audiniuose, bet intensyviausiai kepenyse ir žarnyne. Iš čia fosfolipidai patenka į kraują. Fosfolipidų ypač gausu nervinėse ląstelėse, jie sudaro neuronų mielininį apvalkalą. Fosfolipidai įeina į ląstelių membranos ir jos organelių sudėtį. Jie sudaro pagrindinę membranos lipidinę dalį, dalyvauja hormonų pernašos procese. Svarbesni fosfolipidai, turintys reikšmės lipoproteinų apykaitai, yra fosfatidilcholinai (lecitinai) ir sfingomielinai. Hiperlipidemijos etiopatogenezei fosfolipidai yra nelabai svarbūs. Pagrindiniai lipoproteinų apykaitos fermentai Lipoproteinlipazė. Lipolizė tai sudėtingas procesas, veikiantis visus triacilglicerolių turinčius lipoproteinus. Triacilglicerollipazės pagal kilmę yra dvejopos: hepatinė (kepenų) ir ekstrahepatinė. Pastaroji dažniausiai ir vadinama lipoproteinlipaze. Ji esti dviejų formų: viena, išskirta iš širdies audinio, yra aktyvi tuomet, kai esti normali triacilglicerolių koncentracija kraujyje, kita, išskirta iš riebalinio audinio, yra aktyvi tuomet, kai kraujo plazmoje triacilglicerolių koncentracija yra didelė, pavyzdžiui, riebiai pavalgius. Dėl tokio pasiskirstymo riebalų rūgštys yra įsisavinamos net tuomet, kai triacilglicerolių yra labai nedaug, o tai svarbu tokiam organui kaip širdis. Hormonai, kurie veikia riebalinio audinio lipazių aktyvumą, veikia ir lipoproteinlipazės aktyvumą, tik priešinga kryptimi. Katecholaminai didina ląstelinių lipazių aktyvumą (dėl to riebalų rūgštys intensyviau atpalaiduojamos iš riebalinio audinio) ir slopina lipoproteinlipazę. Insulinas veikia atvirkščiai, t. y. aktyvina lipoproteinlipazes ir slopina audinių lipazės aktyvumą, kartu lipolizę riebaliniame audinyje. Lipoproteinlipazės esti kapiliarų endotelinių ląstelių paviršiuje ir jų aktyvumas kraujo plazmoje paprastai nenustatomas. Tačiau po intraveninės heparino injekcijos lipolizė smarkiai skatinama, nes atsipalaiduoja tos lipoproteinlipazės, kurios neaktyvios formos kaupiamos ląstelėse. Tai poheparininis lipolizinis aktyvumas, nes dėl heparino poveikio intensyviai hidrolizuojami įvairūs lipidai: triacilgliceroliai, diacilgliceroliai ir monoacilgliceroliai, fosfolipidai. Po riebalų hidrolizės balzgana kraujo plazma nuskaidrėja. Dėl to heparinas ir vadinamas plazmos nuskaidrinimo veiksniu. Lipoproteinlipazės aktyviai veikia tik triacilglicerolius, esančius lipoproteinuose, taigi jų substratas yra chilomikronai ir labai mažo tankio lipoproteinai. Be heparino, šį fermentą aktyvina į lipoproteino dalelės sudėtį įeinantis baltymas apoproteinas C-II. Kitas baltymas apoproteinas C-I šio fermento aktyvumą slopina. 251
253 Kepenų (hepatinė) triacilglicerollipazė veikia tuos triacilglicerolius, kurie su lipoproteinais nešami į kepenis. Lecitincholesterolaciltransferazė (LCAT) tai kitas fermentas, randamas kraujo plazmoje ir veikiantis lipidinę lipoproteinų dalį. Jis sintetinamas kepenyse, išskiriamas į kraujo plazmą ir daugiausia veikia pirminius (natyvinius) disko formos didelio tankio lipoproteinus, kurie yra geresnis substratas LCAT negu kraujyje cirkuliuojantys sferiniai didelio tankio lipoproteinai. Tai paaiškinama nedideliu cholesterolio esterių kiekiu pirminiuose DTL. Minėtasis fermentas perneša acilo grupę (riebalų rūgštį) nuo lecitino molekulės antrosios padėties prie laisvojo cholesterolio, t. y. esterifikuoja jo 3β-OH grupę. Taip susidaro cholesterolio esteris ir lizolecitinas. Tad naujai sekretuoti, turintys mažai esterių pirminiai didelio tankio lipoproteinai yra geresnis substratas fermentui negu plazmoje cirkuliuojantys sferiniai DTL. Pakitus lipoproteino lipidinei daliai, pakinta ir apoproteinai, todėl šiuos fermentus (lipoproteinlipzę ir LCAT) reikėtų vadinti lipoproteinus metabolizuojančiomis sistemomis, o ne paprastais fermentais. Ap o l i p o p r o t e i n a i, jų fu n k c i j o s Apolipoproteinai sudaro lipoproteinų molekulės baltyminę dalį ir dar vadinami apoproteinais (sutrumpintai apo). Jie žymimi abėcėlės raidėmis: A, B, C, D, E. Apolipoproteinai, įeinantys į didelio tankio lipoproteinų (DTL) sudėtį, žymimi raide A, į mažo tankio lipoproteinų (MTL) raide B, o į labai mažo tankio lipoproteinų (LMTL) raide C. Tačiau paaiškėjo, kad į kiekvieną lipoproteinų klasę įeina ne vienas, o keletas apolipoproteinų, pavyzdžiui, apo B yra ne tik MTL, bet ir LMTL, o apo C yra ir LMTL, ir DTL. Apolipoproteinai, būdami lipoproteino dalelės baltyminiai komponentai, atlieka nemažai svarbių funkcijų. Apolipoproteinai A (apo A-I ir apo A-II) yra pagrindiniai DTL baltymai. Apo A-I aktyvuoja fermentą lecitincholesterolaciltransferazę (LCAT), o pastaroji skatina laisvojo cholesterolio esterifikaciją didelio tankio lipoproteinų dalelėje ir ją galutinai suformuoja. Apolipoproteinas B tai vienintelis apolipoproteinas, kuris, kaip ir membranų baltymai, netirpsta vandeniniuose tirpaluose. Į šio baltymo sudėtį įeina apie 5 6% angliavandenių. Daugiausia jo randama MTL, mažiau chilomikronuose ir LMTL, kur atitinkamai sudaro 98%, 20% ir 40% jų baltymų masės. Skiriamos dvi apo B formos: tai sintetinamas kepenyse apo B-100, kuris yra svarbiausias MTL baltymas (mažiau jo yra LMTL dalelėje); kita baltymo forma yra apo B-48, kuris sintetinamas žarnų epitelyje ir jo daugiausiai yra chilomikronuose. Apo B yra atsakingumas už lipoproteino dalelės sąveiką su specifiniais ląstelių receptoriais. Apolipoproteinai C tai mažos molekulinės masės kraujo plazmos baltymų grupė. Jie yra sintetinami kepenyse ir yra svarbūs lipoproteinų, turinčių daug triacilgli- 252
254 Lipoproteinai, jų sudėtis, apykaita... cerolių, apykaitai. Apo C-II yra būtinas lipoproteinlipazei aktyvinti. Apo C-I taip pat aktyvina šią lipazę, taip pat kitą fermentą LCAT. Apo C-III yra lipoproteinlipazės inhibitorius. Apolipoproteinas E tai glikoproteinas, kuriame gausu aminorūgšties arginino. Yra žinomos šešios apo E izoformos: E2/E2, E2/E3, E2/E4, E3/E3, E3/E4 ir E4/E4. Apo E jungimasis prie MTL receptoriaus yra labai svarbus šalinant iš kraujo daug apo E turinčius lipoproteinus (chilomikronus, LMTL, TTL). Apo E2 nesijungia su MTL receptoriais; todėl LMTL ir lipoproteinų likučiai iš kraujo cirkuliacijos šalinami lėtai ir tokiu būdu aktyvina MTL receptorius kepenyse. Apo E4 veikia priešingai. Apo E sudaro 13% LMTL baltymų masės. Daug mažiau jo randama DTL. Apo E sudaro didelę tarpinio tankio lipoproteinų baltymų dalį. Kepenyse susintetinti apo E į kraują patenka kartu su pirminėmis disko formos DTL dalelėmis. Cholesterolio esterifikacijos metu šis baltymas atsiduria LMTL paviršiuje ir, manoma, slopina lipoproteinlipazės ir LCAT aktyvumą. Be to, ląstelių specifiniai receptoriai atpažįsta lipoproteinus, turinčius apo E. Taigi šis baltymas svarbus jį turinčių lipoproteinų metabolizmui. Lipoproteinai ir jų apykaita Kraujo plazmos lipoproteinai organizme nuolat kinta ardomi ir pakeičiami naujomis susintetintomis dalelėmis. Taigi tam tikros klasės lipoproteinų koncentracija kraujo plazmoje tai pusiausvyros būklė tarp jų sintezės ir skilimo greičių. Kasdien vidutiniškai su maistu gaunama apie 90 g riebalų ir apie 700 mg cholesterolio. Riebalai sudaro apie 30% visos su maistu gaunamos energijos. Jie virškinami plonojoje žarnoje. Tokiu būdu susidarę monoacilgliceroliai ir riebalų rūgštys, veikiamos tulžies rūgščių, yra absorbuojami plonosios žarnos gleivinės ląstelių, kuriose vyksta triacilglicerolių resintezė. Po resintezės triacilgliceroliai, taip pat cholesterolis, fosfolipidai ir specifiniai apolipoproteinai (svarbiausias apo B-48, taip pat apo A grupės baltymai) suformuoja dalelę micelę, vadinamą chilomikronu. Chilomikronai tai dalelės, aptinkamos limfoje ir kraujo plazmoje riebiai pavalgus. Tokia limfa ar plazma yra drumsta, pieno spalvos. Palaikius ją valandų, chilomikronai išplaukia ir sudaro grietinėlės konsistencijos sluoksnį. Chilomikronuose yra ypač daug triacilglicerolių: jie sudaro apie 90%; chilomikronuose cholesterolis sudaro apie 3% šios dalelės masės. Iš viso chilomikronuose yra apie 5 g cholesterolio ir tik 300 mg šio kiekio gaunama su maistu. Kita cholesterolio dalis patenka iš tulžies cholesterolio enterohepatinės cirkuliacijos (1 1,5 g) ir žarnyno ląstelių (čia jis sintetinamas). Chilomikronai yra išskiriami į limfinę sistemą, po to patenka į kraują. Ten jie prisijungia apo C-II ir apo E, cholesterolio ir jo esterių, fosfolipidų ir toliau kraujas juos neša į kepenis (22 pav.). Pakeliui chilomikronų triacilgliceroliai greit pašalinami 253
255 TG>CE TG>CE 22 pav. Su maistu gautų riebalų apykaita iš cirkuliacijos, nes jų gyvavimo puslaikis yra trumpesnis nei 1 valanda. Taigi chilomikronų apykaita yra labai greita ir 8 12 valandų nevalgiusio (po nakties badavimo) žmogaus kraujo plazmoje chilomikronų neturi būti. Badaujant jų nerandama. Triacilglicerolių skaidymas yra laipsniškas procesas, per kurų susidaro laisvųjų riebalų rūgščių. Šios oksiduojasi audiniuose (raumenyse, inkstuose, pieno liaukose ir kt.) ir iš jų gaminama energija. Šis procesas vyksta dviem etapais: 1) triacilglicerolius hidrolizuoja lipoproteinlipazė; 2) likusi chilomikronų dalis pašalinima iš kraujotakos. Vykstant pirmajam procesui chilomikronai mažėja, netenka daugumos triacilglicerolių ir tampa vadinamaisiais chilomikronų likučiais (remnantais), kurie į kepenis patenka juos atpažinus ir sąveikaujant su apo E receptoriais; ten jie galutinai katabolizuojami. Kita lipoproteinų rūšis, gausi triacilglicerolių, sintetintų organizme (daugiausia kepenyse), yra labai mažo tankio lipoproteinai, arba pre-β lipoproteinai, sutrumpintai LMTL (23 pav.). Jie perneša daugiausia endogeninės (nemaistinės) kilmės triacilglicerolius. Svarbiausi šios dalelės baltymai yra apo B-100 ir apo C, taip pat apo E. Šių lipoproteinų daugiau pasigamina, kai į kepenis atnešama daugiau riebalų rūgščių ar esant angliavandenių pertekliui. Elektriniame lauke jie juda prieš β globulinus, todėl vadinami pre-β lipoproteinais. Nevalgiusių žmonių LMTL neša 7 10% viso kraujo plazmos cholesterolio ir apie pusę triacilglicerolių kiekio. Pastarieji nešami į jų kaupimo riebaliniame audinyje ir panaudojimo vietas (širdį, raumenis, pieno liaukas). Sveikų žmonių kraujo plazmoje LMTL koncentracija yra mg/100 ml. Kaip ir chilomikronus, labai mažo tankio lipoproteinus kraujyje veikia fermentas, sukibęs su kraujagyslių (svarbiausia kapiliarų) endotelinių ląstelių paviršiumi. Tai lipoproteinlipazė. Jos veikiami lipoproteinuose esantys triacilgliceroliai yra hidrolizuojami: susidariusios laisvosios riebalų rūgštys oksiduojamos audiniuose (gaminama energija) arba su albuminais keliauja į kepenis. Fermentą aktyvina chilomi- 254
256 Lipoproteinai, jų sudėtis, apykaita pav. Lipoproteinų apykaitos schema: CE cholestesterolio esteriai; TG triacilgliceroliai; LMTL labai mažo tankio lipoproteinai; TTL tarpinio tankio lipoproteinai; MTL mažo tankio lipoproteinai; DTL didelio tankio lipoproteinai kronuose ir labai mažo tankio lipoptroteinuose esantis apolipoproteinas C-II, taip pat heparinas. Dėl to dalelės mažėja, o jų tankis didėja. Tai LMTL likučiai. Dalį jų iš kraujo paima ir toliau metabolizuoja kepenys. Likusi dalis, vykstant apykaitai ir keičiantis sudėtinėmis dalimis su kitais lipoproteinais, virsta tarpinio tankio lipoproteinais (TTL), kol pagaliau tokiose dalelėse lieka tik cholesterolis ir specifinis apolipoproteinas B-100. Tai jau kokybiškai nauja dalelė mažo tankio lipoproteinas, arba β lipoproteinas, sutrumpintai MTL; svarbiausias jo lipidas yra cholesterolis. Elektroforezės metu MTL juda su kraujo β globulinais. Taigi LMTL apykaita vyksta jiems sąveikaujant su lipoproteinlipaze ji hidrolizuoja triacilglicerolius; dėl to sumažėja šerdies tūris ir keičiasi lipoproteino sudėtis: jame mažėja triacilglicerolių ir gausėja cholesterolio esterių. Šių procesų metu (LMTL TTL MTL) susidarę MTL turi visą apo B kiekį iš LMTL (apo B kiekis MTL dalelėje yra toks pat, kaip ir LMTL dalelėje) ir didžiąją dalį cholesterolio esterių. Žmogaus kraujo plazmos MTL yra gausiausia lipoproteinų klasė jų koncentracija yra mg/100 ml. Įprastai žmogaus organizme MTL dalelės iš LMTL visiškai susiformuoja per 12 valandų. MTL neša 2/3 (apie 70%) viso kraujo plazmoje esančio cholesterolio. Padidėjęs MTL, kartu ir cholesterolio kiekis kraujo plazmoje koreliuoja su padidėjusia koronarinės širdies ligos rizika. Todėl šie lipoproteinai yra vadinami aterogeniniais. Pagrindinė MTL funkcija pernešti cholesterolį iš jo sintezės vietų kepenyse ir žarnų gleivinėje į jo suvartojimo (ar kaupimo) vietas periferiniuose audiniuose. MTL gyvavimo kraujyje puslaikis 2,5 dienos. Dauguma MTL į ląstelę patenka tada, 255
257 24 pav. Mažo tankio lipoproteinų atpažinimas, patekimas į ląstelę ir apykaita: HMG-KoA reduktazė cholesterolis, patekęs į ląstelę specifiniais receptoriais slopina šio fermento aktyvumą ir kartu cholesterolio sintezę; ACAT cholesterolis aktyvina šį fermentą (acetilcholesterolaciltransferazę) ir kartu skatina cholesterolio esterifikaciją; MTL receptoriai cholesterolis slopina MTL receptorių sintezę kai jų paviršiuje esantį baltymą apo B-100 atpažįsta specifiniai ląstelių paviršiaus receptoriai (24 pav.). Juos atrado ir ištyrė M. Braunas (Brown) ir J. Goldšteinas (Goldstein) 1970 m. (1985 m. jiems už šį atradimą paskirta Nobelio premija). MTL receptorius tai glikoproteinas. MTL receptorių skaičius ląstelėje priklauso nuo jos amžiaus, cholesterolio poreikio. Receptoriai yra dviejų rūšių: specifiniai ir nespecifiniai. Svarbiausią vaidmenį, sujungiant MTL, atlieka specifiniai MTL receptoriai, kurie atpažįsta tuos lipoproteinus, kuriuose yra apo B, t. y. LMTL ir MTL. Taigi šie lipoproteinai, kad galėtų susijungti su receptoriumi, konkuruoja tarp savęs. Tačiau receptorius specifiškesnis MTL, nes juose esanti apo B koncentracija bendroje baltymų masėje yra didesnė. Žmogaus fibroblastų vienos ląstelės receptoriai gali sujungti MTL molekulių. Geno, koduojančio MTL receptoriaus sintezę, mutacijų tyrimais nustatyta, kad MTL receptorius toje pačioje polipeptidų grandinėje turi dvi funkcines zonas: viena jų atsako už MTL sujungimą, kita būtina su receptoriumi susijungusio lipoproteino invaginacijai. Taigi, jeigu atpažinimas įvyko, MTL dalelė ir jos cholesterolis endocitozės būdu patenka į ląstelę ir joje atlieka nemažai svarbių reguliacinių funkcijų: 1) slopina reguliacinio cholesterolio sintezės fermento 3-hidroksi-3-metilgliutaril-koenzimo A (HMG-KoA) reduktazę; 2) aktyvina acil-koa-cholesterolaciltransferazę (ACAT) ir skatina patekusio cholesterolio 256
258 Lipoproteinai, jų sudėtis, apykaita... esterifikavimą (cholesterolio esteriai yra kaupiami); 3) slopina MTL receptorių biosintezę. Jeigu receptorių visai nėra ar jie nefunkcionalūs (taip būna sergant šeimine hipercholesterolemija), ar jei pakitęs pats apolipoproteinas B, tai atpažinimas neįvyksta. Tada cholesterolio turtinga mažo tankio lipoproteino dalelė nepatenka į ląstelę, o lieka cirkuliuoti kraujyje. Ląstelė, negaudama cholesterolio iš išorės, pradeda jį sintezuoti ir sekretuoti pati taip išsivysto hipercholesterolemija. MTL sąveika su receptoriumi gali būti įsotinta. Tuomet MTL į ląstelę patenka nuo apo B receptorių nepriklausomu būdu tai nespecifinė endocitozė. Šiuo būdu besikaupiančio cholesterolio kiekis ląstelėje nekontroliuojamas. Be to, šis cholesterolis neatlieka minėtųjų trijų pagrindinių funkcijų. Paprastai 2/3 MTL katabolizuojama specifiniu receptoriniu būdu ir 1/3 nuo apo B receptorių nepriklausomu būdu [dalyvauja vadinamieji valymo (angl. scavenger) receptoriai]. Homozigotų šeiminės hipercholesterolemijos atžvilgiu, kaip minėta, ląstelių receptorių funkcija esti sutrikusi ir visi MTL patenka į ląstelę nespecifiniu būdu. Lipoproteinas(a). Lipoproteinai yra antigenai. Jų specifiškumas priklauso nuo baltyminės dalies, o lipidai veikia labiau kaip haptenai. MTL sistemoje imunologiniais metodais nustatyta lipoproteino(a) sistema. Ji susijusi su lipoproteinuose esančiu specifiniu, daug sialo rūgšties turinčiu polipeptidu, vadinamuoju lipoproteinu(a) antigenu. Jo baltyminę dalį sudaro apo B ir specifinis Lp(a) apoproteinas. Lp(a) baltymas yra vadinamas apo(a) ir yra sujungtas su apo B-100 disulfidiniu tilteliu. Lp(a) lipoproteinas reaguoja su MTL antikūnais. Tiriant elektroforeze, jis migruoja kaip pre-β lipoproteinas, bet yra atipiškas, nes ultracentrifuguojant neiškyla (neflotuoja) kartu su LMTL. Apo(a) aminorūgščių seka turi ypatingą homologiją su plazmos zimogenu plazminogenu ir, pasirodo, tam tikromis aplinkybėmis gali būti susijusi su fibrinolize, t. y. Lp(a) gali sutrikdyti trombolizės procesą sąveikaudamas su plazminogeno receptoriais. Ši sistema paveldima kaip autosominis dominantinis požymis. Lp(a), kaip ir kiti lipoproteinai, turintys apo B, randami aterosklerozinėse plokštelėse. Rizika, susijusi su padidėjusiu Lp(a) kiekiu, matyt, dideliu mastu priklauso nuo kartu padidėjusio MTL kiekio. Didelio tankio lipoproteinai, arba a lipoproteinai, sutrumpintai DTL, yra svarbūs šalinant iš audinių cholesterolį ir mažinant jo kaupimąsi ant arterijų sienelių. Žmogaus kraujo plazmoje jų yra mg/100 ml. Moterų kraujo plazmoje DTL esti daugiau negu vyrų. DTL pirmtakai yra sintetinami parenchiminėse kepenų ir žarnų epitelio ląstelėse. Jie dar vadinami pirminiais (natyviniais) DTL 3 ir yra disko formos. Cirkuliuodami kraujyje jie keičiasi savo baltymais su kitais lipoproteinais ir atlieka savo svarbiausią funkciją iš ląstelių membranų paima laisvąjį cholesterolį, kuris yra puikus substratas fermentui LCAT, vyksta cholesterolio esterifikacija. Cholesterolio esteriai padidina dalelės šerdies tūrį, taigi susidaro sferinės formos tikrasis lipoproteinas DTL 2, kurio pagrindinis baltymas yra apo A. DTL 257
259 neša apie 25% viso plazmos cholesterolio. Keliaudama krauju į kepenis DTL dalelė dalį cholesterolio esterių atiduoda kitiems lipoproteinams (svarbiausia LMTL), o kepenyse atsipalaidavęs cholesterolis naudojamas tulžies rūgščių sintezei ar šalinamas su tulžimi. DTL gyvavimo puslaikis apie 5 dienos. Kuo daugiau didelio tankio lipoproteinų, tuo daugiau cholesterolio bus šalinama iš organizmo. Taigi šie lipoproteinai yra antiaterogeniniai. Lipidų ir li p o p r o t e i n ų ty r i m a s, ir jų kiekio kraujo serume vertinimo kriterijai Lipoproteinai yra nepatvarūs kompleksai: frakcionavimo metodais atskirti nuo kraujo plazmos baltymų ir mažų molekulių, jie greitai suyra. Klinikiniams tyrimams dažniausiai naudojamas kraujo serumas. Bendra taisyklė, kurios būtinai reikia laikytis tiriant kraujo serumo lipidus ir lipoproteinus, yra ta, kad pacientas valandų iki tyrimo turi būti nevalgęs (paprastai tiriama po nakties badavimo). Paprasčiausiu būdu lipoproteinus galima ištirti apžiūrint palaikytą per naktį šaldytuve (+4 C) kraujo serumą. Galimi šie variantai: 1) skaidrus serumas gali būti tiek esant normaliam lipidų ir lipoproteinų kiekiui, tiek hipercholesterolemijai, kai padaugėja mažo tankio lipoproteinų; 2) didelis drumstumas visame mėginyje rodo endogeninę hipertriacilglicerolemiją dėl padidėjusios labai mažo tankio lipoproteinų koncentracijos ar esant patologiniams lipoproteinams; 3) grietinėlės konsistencijos sluoksnis virš drumsto serumo tai požymis, rodantis, kad padaugėjo ir chilomikronų, ir labai mažo tankio lipoproteinų; 4) grietinėlės tirštumo sluoksnis virš skaidraus likusio serumo yra hiperchilomikronemijos požymis. Šis tyrimo metodas, nors yra subjektyvus ir nestandartizuotas, bet gana informatyvus, nustačius cholesterolio ir triacilglicerolių koncentraciją serume. Cholesterolio ir triacilglicerolių kiekis kraujo serume dažniausiai nustatomas fermentiniais metodais. Rekomenduojama bendrojo cholesterolio reikšmė yra <5,2 mmol/l. Galimi sezoniniai cholesterolio kiekio svyravimai: didesnė koncentracija rudenį ir žiemą, mažesnė pavasarį ir vasarą. Cholesterolio koncentracijai turi įtakos ir šie veiksniai: kūno padėtis imant kraują, neseniai suvalgytas maistas, emocinis stresas, mėnesinių ciklas. Rizika susirgti išemine širdies liga yra nedidelė, jei bendrojo cholesterolio kiekis kraujo serume yra 5,2 6,5 mmol/l (taigi pageidaujama, kad jis būtų ne didesnis kaip 5,2 mmol/l). Jei bendrojo cholesterolio kiekis yra 6,5 7,8 mmol/l tai jau hipercholesterolemija ir rizika yra padidėjusi, o jei viršija 7,8 mmol/l tokia hipercholesterolemija sukelia didelę pagreitėjusios aterosklerozės riziką. Taigi dažniausia cholesterolio tyrimo indikacija yra aterosklerozės rizikos nustatymas bei atsako gydant lipidų kiekį mažinančiais vaistais įvertinimas. Iš visų biocheminių žymenų bendrojo cholesterolio padaugėjimas kraujyje yra svarbiausias ate- 258
260 Lipoproteinai, jų sudėtis, apykaita... rosklerozės rizikos veiksnys, ką patvirtina ir faktas, kad koronarinė širdies liga (KŠL) yra labai reta populiacijose, kuriose kraujo serumo cholesterolio kiekis labai mažas, nepaisant esamų kitų rizikos veiksnių. Taip pat daugeliu epidemiologinių tyrimų buvo įrodytas ryšys tarp padidėjusios koronarinės širdies ligos rizikos ir cholesterolio pagausėjimo kraujyje. Sumažinus cholesterolio kiekį 1%, šios ligos rizika sumažėja 1,5 3%. Pagrindiniai triacilglicerolių tyrimo laboratorinėje praktikoje tikslai yra šie: nustatyti hipertriaciliglicerolemiją; nustatyti koronarinės širdies ligos riziką, susijusią su padidėjusia triacilglicerolių koncentracija; įvertinti gydymo lipidų kiekį mažinančiais vaistais efektyvumą; apskaičiuoti mažo tankio lipoproteinų cholesterolio koncentraciją Fridevaldo (W. T. Friedewald) formule. Rekomenduojama vidutinė triacilglicerolių koncentracija yra 1,8 mmol/l (neturi viršyti 2,3 mmol/l). Moterų, vartojančių geriamuosius kontraceptikus, TG kiekis serume yra 0,23 0,45 mmol/l didesnis negu nevartojančiųjų. Padidėjus TG kiekiui iki 11,0 mmol/l ir daugiau, pankreatito rizika labai išauga. Asmens kūno padėtis imant kraują yra labai svarbi. Keičiant padėtį iš gulimos į vertikalią, kraujo plazmos tūris sumažėja 12%. Todėl keičiasi kai kurių kraujo sudedamųjų dalių, taip pat triacilglicerolių koncentracija. Nors koronarinės širdies ligos rizikos ryšys su triacilglicerolių koncentracija kraujo serume nėra toks glaudus kaip su cholesteroliu, kai kuriais tyrimais nustatyta tiesioginė koreliacija tarp padidėjusio triacilglicerolių kiekio ir KŠL rizikos, ypač sergančiųjų cukriniu diabetu. Kol kas dar neaišku, ar triacilgliceroliai yra nepriklausomas rizikos veiksnys, nes kiti nepriklausomi rizikos faktoriai, kaip antai DTL cholesterolio kiekio sumažėjimas, dažnai susiję su triacilglicerolių koncentracijos padidėjimu. Tikslesnę tarptautinę hiperlipoproteinemijų klasifikaciją pateikė D. Fredriksonas (žr. 28 lentelę). Ji pagrįsta papildomais tyrimo metodais: mažo ir didelio tankio lipoproteinuose esančio cholesterolio kiekiu, lipoproteinų elektroforezinio tyrimo ir kitais duomenimis. Epidemiologiniai tyrimai parodė atvirkštinį ryšį tarp DTL cholesterolio kiekio ir KŠL: asmenys, turintys mažesnį DTL cholesterolio kiekį, yra linkę dažniau sirgti KŠL; ir priešingai asmenims, turintiems didelę DTL cholesterolio koncentraciją, retai išryškėja KŠL simptomai. Kaskart DTL cholesterolio kiekiui sumažėjus 0,13 mmol/l, KŠL rizika padidėja 25%. Sveikų vyrų kraujo serume DTL cholesterolio koncentracija neturi būti mažesnė kaip 0,91, o moterų 1,2 mmol/l. Faktas, kad moterų iki menopauzės DTL cholesterolio koncentracija yra didesnė, o KŠL rizika mažesnė nei vyrų, patvirtina apsaugi- 259
261 nį DTL cholesterolio vaidmenį. Be to, po menopauzės mažėjant DTL cholesterolio koncentracijai, rizika sirgti KŠL reikšmingai padidėja. Vienas mechanizmų, paaiškinančių apsauginį DTL vaidmenį nuo aterosklerozės, yra cholesterolio grąžinimas į kepenis. Kita svarbi šio rodiklio taikymo sritis įvertinant KŠL riziką tai DTL cholesterolio ir MTL ar bendrojo cholesterolio kiekio santykio skaičiavimas. Dažnai MTL cholesterolis yra apskaičiuojamas Fridevaldo formule: MTL cholesterolis (mmol/l) = bendrasis cholesterolis (DTL cholesterolis + TG/2,22); čia TG/2,22 atspindi LMTL cholesterolio kiekį mmol/l (jei dydžiai reiškiami mg/100 ml, tai TG/5). Formulė tinka, kai triacilglicerolių koncentracija neviršija 4,54 mmol/l. Svarbiausias šio MTL cholesterolio kiekio nustatymo pranašumas yra jo paprastumas: reikia nustatyti tik bendrojo cholesterolio, DTL cholesterolio ir triacilglicerolių kiekius. Pateiktąja formule apskaičiuoti MTL cholesterolio kiekį galima, jei: paciento TG koncentracija yra mažesnė už 4,5 mmol/l, nėra chilomikronų, nėra β-lmtl (flotuojančių β lipoproteinų, kurie būdingi III tipo hiperlipoproteinemijai). Ėminys, neatitinkantis šių sąlygų, turi būti siunčiamas į laboratoriją, kad būtų tiesiogiai nustatytas MTL cholesterolio kiekis. MTL cholesterolio reikšmė aterosklerozės išsivystymui yra gerai ištirta. Daugelyje šalių atlikti tyrimai patvirtina lemiamą padidėjusios MTL cholesterolio koncentracijos vaidmenį ankstyvam aterosklerozės išsivystymui ir progresavimui. Tačiau, nepaisant MTL cholesterolio tyrimų reikšmės nustatant polinkį sirgti KŠL, tenka pripažinti, kad KŠL yra poligeninė ir daugiaveiksnė liga ir kad MTL cholesterolis yra vienas veiksnių, lemiančių KŠL riziką. Pažymėtina, kad MTL cholesterolio koncentracija yra linkusi mažėti įvykus miokardo infarktui, todėl tyrimas turi būti atliktas per 24 valandas (dėl metabolinės būklės nestabilumo) arba praėjus 4 6 savaitėms, kad lipidų koncentracija stabilizuotųsi. Rekomenduojama MTL cholesterolio koncentracijos vertė yra 2,6 3,5 mmol/l. Bendrojo cholesterolio ir triacilglicerolių kiekiai turi būti nustatomi kiekvienam asmeniui, kuriam yra įtariama koronarinė širdies liga, miokardo infarktas ar periferinių kraujagyslių ligos. Be to, bendrasis cholesterolis turi būti nustatomas asmenims, kurių šeimos nariai sirgo minėtomis ligomis, ir tiems, kurie turi kitų rizikos veiksnių. Kitas žingsnis turėtų būti išplėstinis lipidų ir lipoproteinų būklę atspindinčių laboratorinių rodiklių nustatymas, apimantis bendrojo cholesterolio, triacilglicerolių, DTL cholesterolio ir MTL cholesterolio kiekių nustatymą ir lipoproteinų fenotipavimą. 260
262 Lipoproteinai, jų sudėtis, apykaita lentelė. Lipidų tyrimo rekomenduojamos reikšmės (aterosklerozės diagnostikai ir pirminei prevencijai) Tiriamas lipidas (mmol/l) Pageidaujama koncentracija Saikingas padidėjimas (rizikos ribos) Smarkus padidėjimas (vidutinė rizika ) Kritinis padidėjimas (didelė rizika) Cholesterolis (bendrasis) <5,2 (<5) 5,2 6,5 >6,5 >7,8 MTL cholesterolis <3,4 (<3) 3,4 4,1 >4,1 >4,9 DTL cholesterolis >0,91 (>1) (vyrų) >1,2 (>1) moterų) Triacilgliceroliai <2,3 (< 2) 2,3 4,5 >4,1 >11,3 Lipoproteinų fenotipavimas elektroforezės metodu yra kokybinis lipoproteinų tyrimas, kartu nustatant triacilglicerolių, bendrojo cholesterolio, MTL cholesterolio, DTL cholesterolio koncentracijas (28 lentelė). Antrinės profilaktikos algoritmas po miokardo infarkto remiasi kraujo serumo MTL cholesterolio koncentracija. MTL cholesterolio koncentracija, kurios reikia siekti gydant ligonius, pesirgusius mokardo infarktą ar turinčius didelę KŠL riziką, yra <2,6 mmol/l. Apie lipoproteinų apykaitos sutrikimus galima spręsti ir remiantis kiekybiniu apolipoproteinų kiekio kraujyje matavimu. Diagnostiškai svarbu išryškinti apolipoproteino B, kaip aterogeninio žymens (jo yra daugiausia mažo tankio lipoproteinuose), ir apolipoproteino A-I, kurio yra daugiausia antiaterogeninių savybių turinčiuose DTL, santykį. Rizikos veiksnys yra didelis apolipoproteino B kiekis, net jei cholesterolio koncentracija kraujo serume normali. Nustatyta, kad su amžiumi apolipopoproteino B kiekis didėja, kaip ir bendrojo bei MTL cholesterolio koncentracija, be to, vyrų jis didesnis negu moterų. Remiantis santykinai mažu, daugiausia jaunų ir apyjaunių žmonių (20 50 metų amžiaus) skaičiumi, imunologiniais metodais nustatyta, kad vidutinė apo B reikšmė yra lygi 0,8 0,9 g/l (vyrų ji svyruoja 0,55 1,40, moterų 0,55 1,25 g/l). Nustatyta terapinė apo B riba yra 1,25 g/l. Epidemiologiniais tyrimais nustatytas stiprus ryšys tarp kraujo plazmos apolipoproteino B kiekio ir koronarinių kraujagyslių aterosklerozės. Dažniausiai tiriant ir sveikus, ir sergančius KŠL, apo B pasirodė esąs geresnis aterosklerozės žymuo nei įvairūs kraujo plazmos lipidai. Visai neseniai atliktose studijose, gydant sergančius KŠL pacientus ir turinčius padidėjusį apo B kiekį, nustatyta, kad, sumažinus šio apoproteino kiekį, sumažėja su KŠL susiję įvykiai, taip pat regresuoja aterosklerozė. Taigi apo B atitinka visus reikalavimus, būtinus įrodant priežastinę jo reikšmę aterosklerozei, ir jo nustatymas ypač naudingas tais atvejais, kai yra normali lipidų koncentracija. 261
263 Apolipoproteino A-I (apo A-I) nustatymas nėra informatyvesnis už DTL cholesterolio nustatymą, o esami sandartizavimo sunkumai sumažina šio apoproteino klinikinę svarbą. Taigi apo A-I kol kas lieka potencialus, bet ne priežastinis aterosklerozės rizikos veiksnys. Suaugusiųjų apo A-I koncentracija vidutiniškai yra tokia: vyrų 1,1 2,05 g/l, moterų 1,25 2,15 g/l. Širdies ligų rizikai įvertinti skaičiuojamas apo A-I/apo B santykis. Sveikų vyrų jis yra 0,35 1,0, moterų 0,30 0,9. Aplipoproteino E (apo E) kiekio (koncentracija kraujo serume yra mg/l) ir ypač jo polimorfizmo nustatymas yra labai svarbus šeiminės disbetalipoproteinemijos (III tipas) diagnostikai. Apolipoproteino E2/E2 homozigotiškumas, įvertintas izoelektrinio fokusavimo metodu, yra galutinis šios ligos įrodymas. Apo E tipo nustatymas taip pat gali būti vertingas gydant hiperlipoproteinemijas. Asmenys, turintys E2 fenotipą, kur kas sėkmingiau gydomi cholesterolio sintezės reguliacinio fermento 3-hidroksi-3-metilgliutaril-KoA reduktazės inhibitoriais, palyginti su apo E4 fenotipo asmenimis. Lipoproteinas(a) (Lp(a)) tai lipoproteinas, kurio sveikų asmenų kraujyje dažniausiai yra mažai, tačiau jo kiekis plazmoje koreliuoja su KŠL rizika. Populiacijoje aptinkamos šešios apo (a) izoformos, todėl Lp(a) gali būti polinkio sirgti KŠL genetinis žymuo. Su amžiumi Lp(a) kiekis nekinta. Jo kiekio neveikia dieta ar kiti lipidus mažinantys vaistai, išskyrus nikotino rūgštį. Gydymas estrogenais sumažina Lp(a) kiekį. Didesnė kaip 0,3 g/l Lp(a) koncentracija du kartus padidina riziką sirgti koronarine širdies liga ir 5 kartus ši rizika padidėja, jei yra padidėjusi ir MTL cholesterolio koncentracija. Lp(a) reikšmė neturi viršyti 0,3 g/l. Norint tiksliai identifikuoti pirminį genetinį defektą, tai yra nustatyti konkrečias geno mutacijas, ir taikyti genų terapijos metodus, naudojami molekuliniai diagnostikos metodai. Dislipoproteinemijos Lipoproteinų apykaitos sutrikimus galima suskirstyti į dvi dideles grupes: 1) lipoproteinų sintezės ir sekrecijos sutrikimai (hipolipoproteinemijos), kuriems priklauso, pavyzdžiui, abetalipoproteinemija, Tanžero (Tangier) liga; 2) lipoproteinų katabolizmo sutrikimai (hiperlipoproteinamijos). Lipoproteinų, kartu ir lipidų kiekis kraujyje gali padidėti dėl suintensyvėjusios jų sintezės, kai maiste daug cholesterolio, gyvūninių riebalų ir (arba) esant genetinėms priežastims, sutrikdančioms normalią lipidų ar lipoproteinų apykaitą. Taigi pagal etiologiją dislipoproteinemijos (DLP) gali būti pirminės ir antrinės. Antrinės dislipoproteinemijos atspindi lipoproteinų sutrikimus dėl kitų ligų, pavyzdžiui, hipotirozės, cukrinio diabeto, nefrozinio sindromo ir kt. Sėkmingai gydant ligonį nuo pagrindinės ligos, išnyksta ar sumažėja ir DLP simptomai. Pirminių dislipoproteinemijų priežastis tai genetinis lipidų ar 262
264 Lipoproteinai, jų sudėtis, apykaita... lipoproteinų apykaitos defektas arba aplinkos veiksnių poveikis jų apykaitai per dar ne iki galo žinomus mechanizmus. Įvairiose šalyse atliktų tyrimų duomenimis, dislipoproteinemija (hiperlipoproteinemija ar hiperlipidemija) lemia aterosklerozinį kraujagyslių pažeidimą. Kai šios apykaitos sutrikimas labai ryškus, aterosklerozė pasireiškia jaunesniame amžiuje. Kartu reikia įvertinti ir tokius išeminės širdies ligos rizikos veiksnius kaip vyriškoji lytis, šeimos polinkis sirgti širdies ir kraujagyslių ligomis, rūkymas, hipertenzija, mažas antiaterogeninių didelio tankio lipoproteinų kiekis, cukrinis diabetas, nutukimas. Riziką padidina ir nepakankamas fizinis aktyvumas, kai kurie socialiniai ir fiziologiniai veiksniai. Cholesterolio ir triacilglicerolių kiekio kraujyje tyrimu remiamasi nustatant tolesnę gydymo taktiką ir klasifikuojant lipoproteinų apykaitos sutrikimus. Hiperlipoproteinemija (hiperlipidemija) tai padidėjęs vienos ar kelių klasių lipoproteinų (lipidų) kiekis kraujyje. Dislipoproteinemijos terminas apima didesnę šių sutrikimų įvairovę, t. y. ne tik lipoproteinų kiekio padidėjimą, bet ir jų sumažėjimą. Pavyzdžiui, antiaterogeninių didelio tankio lipoproteinų kiekio sumažėjimas yra toks pat rizikos veiksnys, kaip ir aterogeninių mažo tankio lipoproteinų kiekio padidėjimas. Dislipoproteinemijos pagal paprastą klasifikaciją yra skirstomos į hipercholesterolemiją, mišriąją hiperlipoproteinemiją (hiperlipidemiją) ir hipertriacilglicerolemiją. Norint nustatyti vieną šių sutrikimų, būtina žinoti bendrojo cholesterolio ir triacilglicerolių kiekį kraujo serume. Pirminės dislipoproteinemijos (hiperlipoproteinemijos), arba šeiminės hiperlipoproteinemijos (HLP), yra vienos dažniausių medžiagų apykaitos ligų: šeiminės hipercholestrolemijos dažnumas populiacijose yra 1 iš 500, šeiminės hipertriacilglicerolemijos 0,2 0,3%, mišriosios hiperlipidemijos 0,3 0,5%. Kartu šios būklės diagnozuojamos apie 20% pasveikusiųjų po miokardo infarkto grupėje, o bendroje populiacijoje 1 iš 160 individų turi vieno šių defektų geną. Skaičiuojant ir poligeninius lipoproteinų apykaitos sutrikimus, dažnis siekia 5 iš 100. Lietuvoje 1987 metų ir vėlesnių tyrimų duomenimis (Z. Kučinskienė ir bendraautoriai), metų kaimo vyrų aterogeninių hiperlipoproteinemijų dažnis sudarė 18,4%, moterų 13,3%, dažnis tarp miesto vyrų ir moterų atitinkamai 19,9% ir 14,2% metų miesto vyrų, sergančių išemine širdies liga, hiperlipoproteinemijų dažnis siekė 30,6%, o neturinčių KŠL požymių 17,1%; moterų atitinkamai 25,9% ir 13,7%. Pagal PSO 1970 m. patvirtintą D. Fredriksono (Fredrickson) klasifikaciją, pirminės hiperlipoproteinemijos skirstomos į penkis tipus: I tipas hiperchilomikronemija, IIa tipas hipercholesterolemija, IIb tipas mišrioji hiperlipidemija, III tipas disbetalipoproteinemija, IV tipas hipertriacilglicerolemija, V tipas sunki hipertriacilglicerolemija. Kadangi šiuo metu žinoma daugelio HLP pirminės priežastys, kurių gali 263
265 29 lentelė. Hiperlipoproteinemijos būklės D. Fredriksono klasifikacija I tipas IIa tipas IIb tipas III tipas IV tipas V tipas Lipoproteinas ir lipidas, kurių kiekis padidėja Egzogeninė hiperlipidemija chilomikronai Hipercholesterolemija mažo tankio lipoproteinai Mišrioji hiperlipidemija mažo ir labai mažo tankio lipoproteinai Remnantinė hiperlipidemija β-lmtl Endogeninė hiperlipidemija labai mažo tankio lipoproteinai Mišrioji hiperlipidemija chilomikronai, labai mažo tankio lipoproteinai Pirminiai sutrikimai Šeiminė lipoproteinlipazės (LPL) stoka LPL kofaktoriaus stoka Šeiminė hipercholesterolemija Poligeninė hipercholesterolemija Šeiminė dauginė hiperlipoproteinemija Šeiminė disbetalipoproteinemija Šeiminė hipertriacilglicerolemija Sporadinė hipertriacilglicerolemija Šeiminė sunki hipertriacilglicerolemija Antriniai sutrikimai Disglobulinemija Sisteminė raudonoji vilkligė Nefrozinis sindromas Hipotirozė Disglobulinemija Kušingo sindromas Hepatoma Nefrozinis sindromas Hipotirozė Disglobulinemija Kušingo sindromas Vartojant gliukokortikoidų Stresas Hipotirozė Sisteminė raudonoji vilkligė Cukrinis diabetas Glikogenozės I tipas Lipodistrofijos Disglobulinemija Uremija Nefrozinis sindromas Alkoholizmas Vartojant estrogenų Vartojant gliukokortikoidų Stresas būti ne viena, o kelios, tai skirtingiems hiperlipoproteinemijų tipams priskiriama keletas klinikinių variantų (29 lentelėje apibendrinti pirminiai sutrikimai). I tipo hiperlipoproteinemija. Galimos dvi jos priežastys, kurios lemia du pirminius sutrikimus. Šeiminė lipoproteinlipazės stokos liga (sinonimai: Biurgerio Griucės sindromas, šeiminė chilomikronemija) tai reta liga, išsivystanti dėl fermento lipoproteinlipazės stokos. Dėl to kraujyje susikaupia daug maistinės kilmės triacilglicerolių. Todėl šia liga sergančių žmonių kraujo plazmoje, net kai jie 12 valandų badauja, nustatoma didelė chilomikronų koncentracija. Tiriant sergančiųjų šeimas, įrodyta, kad ši reta geno mutacija perduodama autosominiu recesyviniu būdu. Liga išryškėja jau pirmomis gyvenimo savaitėmis. Vaikui būna pilvo skausmų priepuoliai, pilvas esti didelis. Atsiranda odos ir burnos gleivinės ksantominis bėrimas. Ksantomos tai gelsvos papulės, kurios dažniausiai išsidėsto kūno raukšlėse. Čiuopiant ligoniui pilvą nustatomos padidėjusios kepenys, blužnis, o tiriant akių dugną tinklainės lipemija. Ypač būdinga tokių ligonių kraujo ir plazmos spalva. Kraujas būna pomidorų sriubos su grietine spalvos, o plazma grietinėlės konsis- 264
266 Lipoproteinai, jų sudėtis, apykaita... tencijos ir spalvos. Pastovėjusi ji susisluoksniuoja: viršutinis sluoksnis būna baltas, po juo matyti skaidri plazma. Tai rodo, kad LMTL koncentracija beveik nepadidėjusi. Cholesterolio kiekis gali būti normalus, nors triacilglicerolių koncentracija kraujo serume siekia 28,2 33,8 mmol/l. Kelias dienas maitinamo riebalų neturinčiais maisto produktais vaiko būklė itin pagerėja: nebeskauda pilvo, sumažėja kepenys, blužnis. Tokių vaikų augimas ir vystymasis dažniausiai nesutrinka. Paprastai liga diagnozuojama vaikams iki 10 metų, bet kartais ji nustatoma ir suaugusiesiems. Vienas pavojingiausių simptomų ūminis pankreatitas. Neretai dėl ūmaus pilvo simptomų tokiems ligoniams gali būti atlikta laparotomija. Galutinė diagnozė turėtų remtis fermento aktyvumo nustatymu kraujo plazmoje, įdėjus heparino. Diagnozė neabejotina, jei šeimoje nustatomas kitas lipoproteinlipazės stokos atvejis. Tėvų lipoproteinų apykaita gali būti normali, bet dažniausiai vienam iš jų yra nedidelė hiperlipidemija. Teko konsultuoti ir nustatyti šio tipo hiperlipoproteinemiją trejų metų berniukui, kuriam buvo įtarta kraujo liga dėl padidėjusių kepenų ir blužnies. Apžiūrint berniuką buvo matoma išlikusi odos pigmentacija po ksantominio bėrimo, oda suglebusi dėl blogai išsivysčiusio poodinio riebalinio sluoksnio. Berniuko kraujo serumo triacilglicerolių koncentracija siekė 11,44 mmol/l, cholesterolio kiekis normalus; lipoproteinų elektroforezinis tyrimas išryškino chilomikronų susikaupimą (tiriant elektroforeze jie lieka starto linijoje). Motinos kraujyje lipidų kiekis buvo normalus, o tėvo kraujyje hipertriacilglicerolemija. Gydoma dieta, kurioje riebalų kiekis apribotas iki g per dieną. Apie 5 g suvartojamų riebalų turėtų būti augaliniai, nes tuomet išvengiama riebalų rūgščių stokos. Su maistu ligoniai turi gauti pakankamai vitaminų. Tai ypač svarbu vaikams. Lipoproteinlipazės kofaktoriaus stokos liga išsivysto dėl lipoproteinlipazės aktyvatoriaus apoproteino C-II nepakankamumo. Tokių ligonių kraujo plazma, net ir įdėjus heparino, nesugeba hidrolizuoti chilomikronų bei LMTL nešamų triacilglicerolių. Ligos klinikos simptomai tokie pat, kaip ir sergant šeiminės lipoproteinlipazės stoka. IIa tipo hiperlipoproteinemija. Šioje grupėje skiriami du klinikiniai ligos variantai, kurių etiologija skiriasi. Tai šeiminė hipercholesterolemija ir poligeninė hipercholesterolemija. Šeiminė hipercholestrolemija išryškėja ankstyvąja ateroskleroze ir jos komplikacijomis. Maždaug 50% suaugusių ligonių yra būdingos ksantomos (cholesterolio sankaupos) sausgyslėse, Achilo sausgyslės sustorėjimas, arcus cornea, ksanteliazmos (gelsvi riebalų susikaupimo židiniai akių vokuose). Šios ligos paveldėjimas yra autosominis dominantinis; visi I eilės giminės turi 50% tikimybę paveldėti šį defektą. Kadangi hipercholesterolemija susergama jau vaikystėje, tai nustačius šį sutrikimą galima gydyti dar iki išsivystant aterosklerozei. Šeiminė hipercholesterolemija yra pavyzdys ne tik dažnos ir sėkmingai gydomos, bet ir visapusiškai ištirtos ligos. 265
267 Šios ligos tyrimais buvo išskirtas mažo tankio lipoproteinų receptorius, nustatytas ir smulkiai ištirtas jį koduojantis genas. Mažo tankio lipoproteinų receptoriaus genas yra 19 chromosomoje. Jis yra 45 kb ilgio ir sudarytas iš 18 egzonų (25 pav.). Daugiau negu 135 homozigotinių pacientų tyrimais buvo nustatyta nemažai šio geno mutacijų. Įvairios mutacijos MTL receptoriaus gene gali būti sugrupuotos į keturias funkcines klases. Dėl pirmos klasės ir dažniausiai pasitaikančios mutacijos yra nebesintetinami receptoriai. Dėl antros klasės mutacijų MTL receptorius sintetinamas, bet nevyksta jo pernaša iš sintezės vietos endoplazminio tinklo į Goldžio kompleksą, kur jis modifikuojamas. Dėl trečios klasės mutacijų susintetintas receptorius pasiekia ląstelės paviršių, bet nesąveikauja su mažo tankio lipoproteinais; įvykus ketvirtos retos, bet labai įdomios klasės mutacijoms, receptorius lokalizuojasi nenormalioje (neįprastoje) ląstelės membranos paviršiaus vietoje ir nevyksta surištųjų MTL endocitozė. 25 paveiksle parodytos dažnesnės mutacijos, būdingos kai kurioms etninėms grupėms. 25 pav. MTL receptoriaus geno struktūra ir nustatytos mutacijos Taigi šeiminė hipercholesterolemija yra heterogeninė patologija, nes ją sukelia įvairios mutacijos. Dėl šių mutacijų MTL paviršiuje esantis apolipoproteinas B neatpažįstamas ir (ar) endocitozė nevyksta, taigi toks lipoproteinas ir jame esantis cholesterolis nepatenka į ląstelę ir joje neatlieka minėtų funkcijų. Kadangi į ląsteles nepatenka cholesterolio (su MTL), jose pačiose yra aktyvinama jo sintezė (cholesterolio sintezė neslopinama). Ląstelių cholesterolis patenka į kraują. Dėl to kraujyje gerokai padaugėja mažo tankio lipoproteinų ir bendrojo cholesterolio koncentracija. Paprastai heterozigotų kraujo plazmoje bendrojo ir MTL cholesterolio koncentracija yra 2 kartus didesnė negu to paties amžiaus sveikų žmonių vidurkis, o homozigotų ji 2 3 kartus didesnė negu heterozigotų ir apie 6 kartus negu sveikų žmonių. Triacilglicerolių koncentracija paprastai normali, kartais ji nedaug padidėjusi. Padidėjus cholesterolio koncentracijai kraujyje, jis kaupiasi ir kūno audiniuose, ypač sausgyslėse (ksantomos), ir ant arterijų sienelių (ateromos). Cholesterolio kaupimąsi skatina ir vietiniai veiksniai trauma, nejudrumas ir kt. Būdingiausios yra sausgys- 266
268 Lipoproteinai, jų sudėtis, apykaita... lių (ypač Achilo ir rankos tiesiamųjų raumenų) ksantomos, tuberozinės ksantomos alkūnėse, subperiostinės ksantomos žemiau kelio ir virš alkūninės ataugos. Ksantomose yra laisvojo ir esterifikuotojo cholestetolio, bet laisvojo cholesterolio daugiau negu kraujo plazmoje. Heterozigotoms ypač būdingos ksanteliazmos (plokščios vokų ksantomos). Tačiau ksanteliazmų gali būti ir visiškai sveikame organizme, kai lipidų kiekis kraujyje yra normalus. Šiuo atveju ksanteliazmos perduodamos kaip genetinis požymis. Plokščios oranžinės ksantomos galūnių odoje, ypač tarpupirščiuose, yra būdingos tik homozigotoms ir daug retesnės (15 20%) heterozigotoms. Homozigotoms ksantomos išsivysto pirmaisiais, o heterozigotoms dvidešimtaisiais gyvenimo metais. Arcus cornea tai žiedo formos lipidų kaupimosi zonos ragenoje, tinklainėje, skleroje ir kitose akies dalyse. Šis simptomas pasitaiko 10% heterozigotų iki 30 metų amžiaus ir 50% vyresniems kaip 30 metų, taip pat gali būti ir sveikiems žmonėms. Stenokardija, miokardo infarktas ir staigi mirtis tai trys pagrindiniai nustatomos koronarinės širdies ligos padariniai, pasitaikantys 5 20 metų homozigotoms; jie būdingos šio tipo hiperlipoproteinemijai. Ateromos aortos vožtuvuose yra aortos stenozės priežastis, dėl kurios išsivysto širdies ydos. 50% homozigotų būdinga reumato klinika: pažeistų sąnarių poliartritas, karščiavimas, leukocitozė. Vaikai, sergantys šia liga, paprastai yra mažesnio ūgio negu kiti sveiki šeimos nariai. Būdingas dar vienas šeiminės hipercholesterolemijos požymis tai jos asociacija su hipertrichoze. Šeiminę hipercholesterolemiją galima diagnozuoti prenataliniu laikotarpiu. Todėl šeimoms, kuriose yra dominantinis hipercholesterolemijos paveldėjimas, būtina genetinė konsultacija. Išmatavus MTL cholesterolio kiekį virkštelės kraujyje, homozigotinę būklę galima diagnozuoti ką tik gimusiam naujagimiui. Šią ligą teko diagnozuoti ne vienam vaikui, kurio šeimos anamnezė buvo sudėtinga, t. y. ir kitiems suaugusiems šeimos nariams nustatyta hiperlipoproteinemija. Teko konsultuoti 8 metų berniuką dėl oranžinės spalvos tuberozinės ksantomos abiejų kelių srityse ir plokščios ksantomos abiejų rankų pirmajame tarpupirštyje. Buvo planuojama jas šalinti. Kraujo serumo tyrimu buvo nustatyta, kad bendrojo cholesterolio koncentracija viršija 10 mmol/l, MTL cholesterolio 8,8 mmol/l, o DTL cholesterolio bei triacilglicerolių kiekis normalus. Iš šeimos anamnezės paaiškėjo, kad motinai būna skausmų širdies plote, jos pačios motinai jau buvo pašalinti tulžies pūslės akmenys, diagnozuota hipertonija; tėvas jau buvo miręs nuo miokardo infarkto, o abiem tėvo tėvams buvo padidėjęs kraujospūdis, skausmai širdies plote. Miokardo infarkto tikimybė vyrams heterozigotoms iki 60 metų amžiaus sudaro 85%, sveikiems šio amžiaus vyrams apie 15%. Moterims ši rizika yra mažesnė: heterozigotoms iki 60 metų amžiaus koronarinės širdies ligos tikimybė yra 50%, sveikoms 10%. Homozigotoms skirtumas tarp lyčių nebūdingas. Poligeninė hipercholesterolemija. Iš 20 žmonių, turinčių hipercholesterolemiją (nesant antrinių priežasčių), vienas bus heterozigota šeiminės hipercholestero- 267
269 lemijos atžvilgiu, trys turės IIb tipo hiperlipidemiją, 16 poligeninę hipercholesterolemiją. Jos priežastis yra ne vieno geno mutacija, o daugelio genetinių ir aplinkos veiksnių sąveika, kuri sutrikdo MTL apykaitą. Priežastys, sutrikdančios cholesterolio apykaitą sergant poligenine hipercholesterolemija, gali būti įvairios, pavyzdžiui, genetinis fermentų, dalyvaujančių tulžies rūgščių ir cholesterolio sintezėje, defektas, MTL susidarymo ar katabolizmo pažaidos. Ligonių, sergančių poligenine hipercholesterolemija, ir ligonių, sergančių šeimine hipercholesterolemija, lipidų bei lipoproteinų tyrimo duomenys nesiskiria. Diferencinei diagnostikai galima naudoti šiuos kriterijus: 1) šeimų tyrimą sergančiųjų poligenine hipercholesterolemija tik 10% pirmos eilės giminių bus randama hiperlipidemija, o sergančiųjų šeimine hipercholesterolemija apie 50%; 2) poligeninės hipercholesterolemijos tipui ksantomos nebūdingos. IIb tipo hiperlipoproteinemija (šeiminė mišrioji hiperlipidemija). Ir IIa tipo, ir IIb tipo hiperlipoproteinemija yra viena dažniausių hiperlipoproteinemijos formų. Bendroje populiacijoje pastarosios dažnis yra apie 0,3 0,5%. Pagrindinis šios ligos žymuo tai MTL ar LMTL, dažniausiai abiejų klasių lipoproteinų padaugėjimas kraujo plazmoje. Tos pačios šeimos vienų narių lipoproteinai gali būti būdingi IIa, kitų IV ar IIb tipo ligai. 10% žmonių iki 60 metų amžiaus, pasveikusių po miokardo infarkto, yra iš šeimų, kurių nariams būdingi dauginiai lipoproteinų apykaitos defektai. Tačiau šis tipas skiriasi nuo IIa ir IV tipo hiperlipoproteinemijos: nors lipidų kiekis plazmoje ir padidėjęs, jis mažesnis negu sergant IIa ir IV tipų hiperlipoproteinemija; 2) būdingas šeimos narių sergamumas: 1/3 probando giminių serga IIa tipo hiperlipoproteinemija, 1/3 IV tipo ir apie 1/3 tiek hipercholesterolemija, tiek hipertriacilglicerolemija (IIb tipas); 3) probandų receptorių MTL aktyvumas yra normalus, tad ir padidėjusio cholesterolio kiekio priežastis skiriasi nuo šeiminės hipercholesterolemijos priežasties. Šiam tipui būdinga padidėjusi apoproteino B sekrecija ir tai, matyt, lemia LMTL, kartu ir MTL hiperprodukciją. IIb tipo hiperlipoproteinemijos paveldėjimas yra autosominis dominantinis, bet vieno geno mutacija kol kas galutinai nepatvirtinta. Sergantiesiems šeimine mišriąja hiperlipidemija būdingas nutukimas, hiperinsulinemija, priešlaikinė koronarinė širdies liga. Ksantomų nebūna. Liga visiškai išryškėja apie gyvenimo metus. Hipertriacilglicerolemija paprastai išsivysto vėliau negu hipercholesterolemija. Pastovėjusi kraujo plazma dažniausiai truputį drumsta, joje nėra chilomikronų sluoksnio. Paprastai MTL cholesterolio koncentracija yra didesnė kaip 5,07 mmol/l, LMTL triacilglicerolių 1,25 mmol/l. Tririant elektroforeze matyti β lipoproteinų ir pre-β lipoproteinų juostos. III tipo hiperlipoproteinemija (šeiminė disbetalipoproteinemija). Sergant šia liga, labai mažo ir tarpinio tankio lipoproteinų zonoje atsiranda neįprastų lipoproteinų, kurie tiriant elektroforeze esti nelabai judrūs. Šie lipoproteinai buvo pavadinti flotuojančiais β lipoproteinais arba β-lmtl. Kadangi β lipoproteinų ir pre-β 268
270 Lipoproteinai, jų sudėtis, apykaita... lipoproteinų juostos atliekant elektroforezę blogai atsiskiria, tai ir sindromas dar vadinamas plataus β liga. β-lmtl nuo normalių LMTL dalelių skiriasi didesniu cholesterolio esterių ir mažesniu triacilglicerolių kiekiu, jose neproporcingai didelis arginino turinčių baltymų kiekis: daug apo E-II ir mažai apo E-III, sumažėjęs bendrasis apo E kiekis, todėl šie lipoproteinai, tiriant elektroforeze, nenormaliai migruoja, o liga dar vadinama disbetalipoproteinemija. Su pakitusiu apo E kaip tik ir susijęs LMTL katabolizmo defektas. Pažymėtina, kad sergant III tipo dislipoproteinemija, būna labai mažas antiaterogeninių DTL kiekis kraujo plazmoje. Ligos klinika paprastai išryškėja suaugusiesiems. Ji dažnai susijusi su nutukimu, kartais hipotiroze. Ligą galima įtarti, kai randama būdingų ksantomų delnų ir pirštų raukšlėse (xanthoma striata palmaris), tuberozinės ksantomos alkūnių, kelių, taip pat ksantomos tiesiamųjų raumenų sausgyslių ir kitose mechaninio dirginimo vietose, sėdmenų srityje. Ligoniams, sergantiems šia liga, būdinga priešlaikinė gana piktybinės eigos aterosklerozė, ypač šlaunies arterijos ir jos šakų. Kraujo plazma paprastai esti drumsta su plonu grietinėlės tirštumo sluoksniu tai nenormalios sudėties (patologiniai) lipoproteinai. Triacilglicerolių ir cholesterolio koncentracija, taip pat apo E kiekis esti padidėję. Plazmos cholesterolio ir triacilglicerolių santykis svyruoja nuo 0,3 iki 2,0. Tiriant elektroforeze dėl nenormalios sudėties randami neįprastai migruojantys lipoproteinai tai β-lmtl: agarozės gelyje jie juda greičiau negu MTL, todėl MTL ir LMTL juostos neatsiskyrusios (matyti vientisa juosta). IV tipo hiperlipoproteinemija. Šioje pirminių hiperlipoproteinemijų grupėje skiriami du klinikiniai jų tipai: šeiminė hipertriacilglicerolemija ir sporadinė hipertriacilglicerolemija. Šeiminė hipertriacilglicerolemija yra antra pagal dažnį pirminių hiperlipoproteinemijų forma. Šis triacilglicerolių apykaitos defektas paveldimas kaip autosominis dominantinis požymis, išryškėjantis padidėjusia kraujo plazmos LMTL ir triacilglicerolių koncentracija. Be hipertriacilglicerolemijos, šiems ligoniams būdingas nutukimas, audinių atsparumas insulinui, gliukozės netoleravimas, padidėjęs kraujospūdis ir šlapimo rūgšties kiekis kraujyje. Tačiau tai nepastovūs simptomai ir etiologiškai jie nesusiję su ligos priežastimi. Kartais ligoniams būna ksantominis bėrimas, bet daugumai ksantomos nebūdingos. Kai ligoniai, sergantys šeimine hipertriacilglicerolemija, badauja, jų kraujo plazmos triacilglicerolių kiekis nesunormalėja. Tuo ši liga skiriasi nuo negenetinių antrinių hipertriacilglicerolemijų. Ištirta, kad šiems ligoniams rizika susirgti miokardo infarktu yra du kartus didesnė negu sveikiems asmenims. Sergantiems šeimine hipertriacilglicerolemija būdinga drumsta kraujo plazma. Cholesterolio koncentracija joje yra normali, retai padidėjusi, o triacilglicerolių kiekis smarkiai padidėja (viršutinė normos riba 2,26 mmol/l). Sporadinė hipertriacilglicerolemija. Be pirminės hipertriacilglicerolemijos, kuri dažnai nustatoma keletui šeimos narių, galima endogeninė hipertriacilglice- 269
271 rolemija, nustatoma pavieniams asmenims. Tai sporadinė hipertriacilglicerolemija. Kliniškai tokių ligonių negalima atskirti nuo sergančiųjų šeimine hipertriacilglicerolemija. Šias formas diferencijuoti padeda šeimų tyrimas. Sporadinė hipertriacilglicerolemija sudaro 1/4 hipertriacilglicerolemijų, o kita dalis tenka šeiminei hipertriacilglicerolemijai ir IIb tipo hiperlipidemijai. V tipo hiperlipoproteinemija (sunki šeiminės hipertriacilglicerolemijos forma). Kai kuriose šeimose dominantiniu būdu paveldėta hipertriacilglicerolemija (IV tipo) genetiškai skiriasi nuo kitos šeiminės hipertriacilglicerolemijos formos. Ligoniams rytą, nevalgiusiems valandų, paėmus kraujo ir jį ištyrus, randamas gerokai padidėjęs LMTL ir chilomikronų kiekis. Kraujo plazmos triacilglicerolių koncentracija siekia 11 mmol/l ir daugiau. Ligos simptomai panašūs į šeiminės lipoproteinlipazės stokos sindromą. Liga išryškėja paaugliams ar suaugusiems individams pilvo skausmų priepuoliais. Todėl neretai diagnozuojamas pankreatitas. Prieš skausmų pradžią išryškėja hiperlipidemija, ksantominis bėrimas, hepatosplenomegalija, tinklainės lipemija. Tačiau šis hiperlipoproteinemijos tipas skiriasi nuo pirmojo tipo, nes sutrinka ne tik chilomikronų, bet ir LMTL apykaita. Daugumai ligonių gliukozės tolerancija yra sutrikusi. Ligą nustatyti padeda būdingas stovinčios plazmos vaizdas: viršuje išsiskiria chilomikronų sluoksnis, o po juo esantis yra drumstas dėl padidėjusio LMTL kiekio. Tiriant elektroforeze, išryškėja plati pre-β lipoproteinų juosta, neretai siekianti ir starto liniją. Tai rodo esant chilomikronų. MTL ir DTL kiekiai gali nepakisti. Taigi pirminės hiperlipoproteinemijos sudaro grupę heterogeninių ligų, kurių būdingiausias bruožas yra padidėjęs cholesterolio ir (ar) triacilglicerolių kiekis kraujo plazmoje. Tokie simptomai dažnai išryškėja tam tikrose šeimose, bet gali būti ir pavienių atvejų. Minėtųjų hiperlipoproteinemijų įvairovė tai vieno geno defekto arba kelių genų, esančių skirtingose chromosomose ar jų regionuose, sąveikos rezultatas. Nešeiminės hiperlipoproteinemijos dažniausiai yra antrinės. Jos išsivysto veikiant tokiems veiksniams kaip maistas, alkoholis, estrogenų vartojimas, ligos (pavyzdžiui, cukrinis diabetas, nefrozė, hipotirozė ir kt.). Dislipoproteinemijos ir aterosklerozė Aterosklerozė (gr. atherosclerosis: athere košelė, scleros standus, kietas) tai lėtinė liga, pažeidžianti arterijas. Sustorėjusios arterijų sienelės elastingumas ir spindis mažėja, sutrinka audinių ir organų kraujotaka. Arterijų sienelę sudaro trys sluoksniai (26 pav.): vidinis (intima) iš endotelio ląstelių; vidurinis (media) iš lygiųjų raumenų ląstelių ir jungiamojo audinio komponentų; išorinis (adventicia) iš jungiamojo ir riebalinio audinių. Pro arterijų endotelio ląstelių tarpus laisvai praeina didelio tankio lipoproteinai, o chilomikronai ir labai mažo tankio lipoproteinai neįveikia endotelio barjero. Mažo tankio lipopro- 270
272 Lipoproteinai, jų sudėtis, apykaita... a) pradinis pažeidimas b) plokštelės formavimasis c) antrinio trombo susidarymas ir organizuota plokštelė 26 pav. Aterosklerozinio pažeidimo vystymosi schema teinai gali pereiti endotelio ląstelių sluoksnį, bet per gilesnius sluoksnius skverbiasi lėtai (dėl savo dydžio, kiekio ar modifikacijos). Kai mažo tankio lipoproteinų kiekis neviršija rekomenduojamų normos ribų, tai patekusius į subendotelinį tarpą juos katabolizuoja lygiųjų raumenų ląstelės, makrofagai jau aprašytu receptoriniu būdu. Esant net ir mažiausiam endotelio ląstelių pažeidimui (pavyzdžiui, dėl hipertenzijos, sukeltos angiotenzino, padaugėjus katecholaminų dėl streso, nikotino sukeltų hipokseminių būklių, dėl lipidų peroksidacijos padidėjus kraujyje modifikuotųjų lipoproteinų, paveikus virusui ar antigeno ir antikūno kompleksui), ląstelių pralaidumas padidėja ir atsidaro vartai, pro kuriuos laisvai patenka tikrosios aterogeninės medžiagos, pavyzdžiui, mažo tankio lipoproteinai (27 pav.). Šis procesas ypač spartėja, kai MTL kiekis yra padidėjęs ir jie ilgesnį laiką cirkuliuoja kraujyje vyksta jų modifikacija: cheminis acetilinimas ar dažniausiai oksidacija 271
273 Neląstelinis užpildas Trombas Oksiduoti MTL Makrofagas Lygiųjų raumenų ląstelė 3 Putotoji ląstelė Negyvybingas audinys Aterosklerozinės plokštelės plyšimas ir trombo formavimasis Infiltracija MTL. MTL oksidacija Monocitų chemotaksis. Monocitų transformacija į makrofagus. Makrofagas, prisirijęs oksiduotų MTL, virsta putotąja ląstele. Riebalinės dėmės susidarymas Lygiųjų raumenų ląstelių chemotaksis. Lygiųjų raumenų ląstelių proliferacija. Aterosklerozinės plokštelės susidarymas Ląstelių žūtis, jų turinio išėjimas Aterosklerozinės plokštelės plyšimas, trombo formavimasis ir klinikos pasireiškimas (miokardo infarktas) 27 pav. Aterosklerozės vystymosi ir progresavimo schema 272
274 Lipoproteinai, jų sudėtis, apykaita... (žr. skyriuje Laisvaradikalė oksidacija, antioksidacinė gynyba ir ligos ). Tada šie lipoproteinai tampa stipriais chemotaksiniais agentais cirkuliuojantiems monocitams. Tuo aterosklerozė savo vystimosi pradžioje yra panaši į uždegiminį procesą ir dėl to kraujyje padaugėja uždegimo žymenų (pvz., CRB). Jei oksiduotų mažo tankio lipoproteinų yra daug, tai jie užpildo subendotelinį tarpą ir į ląsteles pradeda skverbtis ne tik normaliu receptoriniu būdu, bet kaip šiukšles juos ryja makrofagais virtę kraujo monocitai. Pastarieji tiesiog prisisotina cholesterolio. Tokią įvykių eigą galima pavaizduoti schema: didelis MTL kiekis kraujo plazmoje intimos infiltracija MTL oksiduoti MTL+makrofagai putotosios ląstelės lipidinė dėmė. Taip kraujagyslėse formuojasi riebalinės (geltonosios) dėmės. Proliferuojant ir diferencijuojantis lygiųjų raumenų ląstelėms (dėl dirginimo), daugėjant kolageno, riebalinės dėmės virsta ateromomis, kurios augdamos ir susiaurina kraujagyslės spindį. Šis procesas išsivysto žymiai jaunesnio amžiaus žmonėms, jei yra genetinis lipoproteinų apykaitos sutrikimas, pavyzdžiui, molekulinis apoproteinų sintezės ar receptorių defektas. Dislipoproteinemijos gydymo principai: 1) nustačius dislipoproteinemiją, be gydymo skyrimo, būtina šalinti (gydyti) kitus su ja susijusius rizikos veiksnius (hipertenzija, rūkymas, nutukimas, stresas ir kt., kurie skatina aterosklerozės progresavimą); 2) reikia išsiaiškinti, ar dispipoproteinemija yra pirminė ar antrinė; dažniausios būklės (ligos), susijusios su hiperlipidemija, yra cukrinis diabetas, hipotirozė, nefrozinis sindromas, alkoholio ar kai kurių vaistų ilgalaikis vartojimas; 3) visų dislipoproteinemijų (svarbiausia hiperlipoproteinemijų) gydymas pradedamas dietos rekomendacijomis; tik daliai pacientų būtina derinti dietą su vaistais; šį sprendimą turėtų lemti paciento aterosklerozės komplikacijų rizika, taip pat amžius, širdies ir kraujagyslių būklė; 4) po kai kurių procedūrų ir operacijų atsiranda lipidų nusėdimui palankių vietų (pavyzdžiui, vainikinės arterijos po angioplastikos). Po operacijos šiems ligoniams taip pat būtina nustatyti lipoproteinus ir sutrikimus koreguoti. Dieta yra labai svarbi gydant tiek pirmines, tiek antrines dislipoproteinemijas. Vienas svarbiausių labai mažo tankio lipoproteinų (LMTL) susidarymo veiksnių yra su maistu gaunamas kalorijų kiekis. Kai kepenys gauna daugiau riebalų rūgščių ar angliavandenių, negu gali oksiduoti, suintensyvėja triacilglicerolių sintezė ir LMTL susidarymas kepenyse. Sumažinus maisto kaloringumą, sumažės ir LMTL. Tačiau nerekomenduojama per daug sumažinti maisto kaloringumo, nes tai didina riebalų rūgščių mobilizaciją. Triacilglicerolių katabolizmą skatina atsparumo insulinui mažinimas. Dėl to sumažėja kūno masė. Nutukusiems žmonėms fizinis aktyvumas mažina LMTL ir MTL 273
275 kiekį net tuomet, kai patenkančių į organizmą kalorijų kiekis nesikeičia. Kepenyse triacilglicerolių sintezė mažėja, nes daugiau riebalų rūgščių ir gliukozės oksiduojama kepenyse. Rūkymas didina cholesterolio ir triacilglicerolių koncentraciją kraujo plazmoje, nes nikotinas skatina lipolizę riebaliniame audinyje; iš jo patekusios į kepenis riebalų rūgštys yra esterifikuojamos ir triacilglicerolių pavidalu patenka į LMTL. Be to, rūkymas, netgi pasyvus, skatina lipidų peroksidaciją. Alkoholis skatina triacilglicerolių sintezę kepenyse, todėl jo kiekį būtina riboti (be to, alkoholis teikia tam tikrą kalorijų kiekį). Padidėjusį MTL kiekį beveik visiems žmonėms galima sumažinti skiriant dietas, kuriose apribotas cholesterolio ir gyvūninių riebalų kiekis. Taigi dislipoproteinemijų gydymą reikia pradėti skiriant subalansuotą mažesnio kaloringumo dietą. Hipocholesteroleminį poveikį turi nesirezorbuojantys polisacharidai, pavyzdžiui, obuolių pektinas, nes jis suriša tulžies rūgštis. Dislipoproteinemijos vaistais gydomos tuomet, kai nuo dietos ligonio sveikata negerėja arba pagerėja per mažai. Šiuo metu žinomus hipolipideminius vaistus galima suskirstyti į tokias grupes: 1) nikotino rūgštis ir jos preparatai; 2) tulžies rūgščių rišikliai; 3) fibratų grupės preparatai; 4) cholesterolio sintezės inhibitoriai; 5) antioksidatoriai; 6) mononesočiųjų riebalų rūgščių preparatai. Nikotino rūgštis yra PP vitaminas, nuo seno vartojamas kaip triacilglicerolių ir cholesterolio kiekį mažinantis preparatas. Nikotino rūgštis slopina lipolizę riebaliniame audinyje, todėl mažiau laisvųjų riebalų rūgščių patenka į kepenis. Dėl to jose sumažėja triacilglicerolių sintezė, apo B pernaša ir jungimasis prie LMTL. Sumažėjus LMTL susidarymui ir sekrecijai, sumažėja ir MTL koncentracija. Dėl jos poveikio ne tik sumažėja apo B turinčių lipoproteinų koncentracija (LMTL ir MTL), bet ir padidėja DTL ir juose esančio cholesterolio kiekis. Vartojant po nedaug nikotino rūgšties (kaip vitaminą), cholesterolio serume nesumažėja. Taigi, kai nikotino rūgštis vartojama kaip cholesterolio ar triacilglicerolių kiekį mažinantis preparatas, ji yra vaistas ir skiriamas gydytojo. Dažniausiai nikotino rūgštis yra pirmučiausias vaistas gydant mišriąsias dislipoproteinemijas, nes dėl jos poveikio kraujo serume mažėja ir triacilglicerolių, ir cholesterolio, o daugėja DTL cholesterolio. Tulžies rūgščių rišikliai. Dažniausiai vartojami cholestiraminas ir kolestipolis. Tai sintetinės dervos, kurios virškinamajame trakte suriša tulžies rūgštis, sutrikdo absorbciją plonojoje žarnoje (t. y. jų enterohepatinę cirkuliaciją) ir skatina ekskreciją su išmatomis. Daugiau pašalinus tulžies rūgščių, intensyvėja jų naujų molekulių sintezė iš cholesterolio (ji paspartėja apie 10 kartų). Dėl to sumažėja cholesterolio atsargos kepenyse, kartu ir MTL cholesterolio kiekis kraujyje (iš pradžių cholesterolio sintezė ir sekrecija iš kepenų suintensyvėja ir MTL bei cholesterolio kiekis gali truputį padidėti). Be to, veikiant šiems vaistams, suaktyvėja MTL receptorių sintezė hepatocituose, nes skatinama MTL receptoriaus geno transkripcija. Dėl to daugiau 274
276 Lipoproteinai, jų sudėtis, apykaita... MTL, kartu ir cholesterolio bus šalinama iš kraujo. Taigi tulžies rūgščių rišikliai yra efektyvūs mažinant MTL cholesterolio koncentraciją, kartu ir koronarinės širdies ligos riziką. Dėl šių vaistų poveikio šiek tiek padidėja DTL cholesterolio koncentracija ir tai yra gerai, tačiau paspartėja ir triacilglicerolių sintezė bei LMTL susidarymas, todėl didelė hipertriacilglicerolemija yra kontraindikacija tulžies surišiklių skyrimui (gali išsivystyti ūminis pankreatitas). Fibratų grupės preparatai gerokai sumažina triacilglicerolių kiekį pacientams, kurių kraujo serume hipertriacilglicerolemija, taip pat MTL cholesterolio kiekį. Šie vaistai suaktyvina lipoproteinlipazę ir dėl to chilomikronų bei LMTL triacilglicerolių katabolizmą, taip pat sutrikdo LMTL susidarymą kepenyse. Be to, šie vaistai didina MTL receptorių aktyvumą. Tai vieni efektyviausių preparatų, kurie mažina triacilglicerolių kiekį kraujyje ir yra vartojami ūminio pankreatito profilaktikai (tuomet triacilglicerolių koncentracija gali būti didesnė nei 11,3 mmol/l). Cholesterolio sintezės inhibitoriai tai efektyviausiai cholesterolio kiekį mažinantys ir mažiausiai šalutinių reiškinių sukeliantys vaistai. Jie yra konkurentiniai 3-hidroksi-3-metilgliutarilkofermento A (HMG-KoA) reduktazės inhibitoriai, gaunami iš pelėsių Aspergillus. Šie vaistai sutrikdo cholesterolio sintezę, tačiau visiškai jos neblokuoja, ir cholesterolio stoka organizme neišsivysto. Be to, dėl jų poveikio padaugėja MTL receptorių. Labiausiai sumažėja MTL cholesterolio, o DTL cholesterolio kiekis padidėja. Taigi tik supratus MTL receptoriaus veikimą, buvo galima sukurti efektyvius vaistus nuo sunkios pirminės hipercholesterolemijos. Tik atskleidus MTL receptoriaus geno struktūrą ir jį susintetinus, prasidėjo ir genų terapijos bandymai. Tuo tikslu atliekant kepenų punkciją ar dalinį kepenų šalinimą paimti hepatocitai yra auginami audinių kultūroje, paskui normalus MTL receptoriaus genas įterpiamas į kepenų ląsteles. Po šios genetinės inžinerijos procedūros hepatocitai su MTL receptorių koduojančiu genu vėl grąžinami į paciento vartų venos kraujotaką. Kitas genų terapijos būdas remiasi dirbtinės liposomos sukūrimu, kuri būtų hepatocitų atpažįstama. Tokios struktūros šerdyje yra MTL receptorių koduojanti DNR, o jos išoriniame sluoksnyje yra baltymas, kurį atpažįsta hepatocitas. DNR, pasiekusi hepatocitų branduolį, koduos MTL receptorių. Taigi šios molekulinės patologijos esmės atskleidimas akivaizdžiai rodo dviejų mokslų medicinos ir genetikos glaudų ryšį. Api b e n d r i n i m a s Su krauju gali būti pernešamos tik vandenyje tirpios medžiagos. Tokia tirpi lipidų forma yra lipoproteinai. Kraujo plazmos lipoproteinai tai micelės, kuriose nepoliniai lipidai triacilgliceroliai ir cholesterolio esteriai yra dalelės šerdis, o baltymai (apolipoproteinai), fosfolipidai ir laisvasis cholesterolis sudaro dalelės paviršių. 275
277 Chilomikronai tai dalelės, esančios limfoje ir kraujo plazmoje riebiai pavalgius (kraujo plazma balzgana). Badaujant jų nerandama. Labai mažo tankio lipoproteinai perneša daugiausia endogeninės (nemaistinės) kilmės triacilglicerolius; jų daugiau pasigamina, kai į kepenis iš riebalinio audinio patenka daugiau riebalų rūgščių ar esant angliavandenių pertekliui. Mažo tankio lipoproteinai tai gausiausia žmogaus kraujo plazmos lipoproteinų klasė; jų funkcija cholesterolio pernaša iš jo sintezės vietų (kepenų ir žarnų gleivinės ląstelių) į jo sunaudojimo vietas periferiniuose audiniuose. Padidėjęs mažo tankio lipoproteinų, kartu ir cholesterolio kiekis kraujo plazmoje koreliuoja su padidėjusia išeminės širdies ligos rizika. Todėl šie lipoproteinai yra vadinami aterogeniniais. Didelio tankio lipoproteinai yra svarbūs šalinant iš audinių cholesterolį, kartu mažinant jo kaupimąsi ant arterijų sienelių. Taigi šie lipoproteinai yra antiaterogeniniai. Tiriant kraujo plazmos lipidus ir lipoproteinus, privalu, kad asmuo valandų iki tyrimo būtų nevalgęs (paprastai tiriama po nakties badavimo). Hiperlipoproteinemija (hiperlipidemija) tai padidėjęs vienos ar kelių klasių lipoproteinų (lipidų) kiekis kraujyje; dislipoproteinemijos terminas apima ne tik lipoproteinų kiekio padidėjimą, bet ir galimą jų sumažėjimą. I tipo hiperlipoproteinemija (chilomikronemija nevalgius) gali būti pirminė dėl šeiminės lipoproteinlipazės stokos (ši forma beveik visada išryškėja vaikystėje) ar antrinė, sergant cukriniu diabetu, sistemine raudonąja vilklige, esant disgamaglobulinemijai. Sergant I tipo hiperlipoproteinemija (HLP), cholesterolio koncentracija normali ar šiek tiek padidėjusi, triacilglicerolių koncentracija gerokai padidėjusi (>11,3 mmol/l), jie yra egzogeninės kilmės, cholesterolio ir triacilglicerolių santykis yra 1:5 1:10, elektroforegramoje būdinga išryškėjusi chilomikronų juosta, ėminiui pastovėjus per naktį 4 o C temperatūroje, chilomikronai iškyla į paviršių ir sudaro grietinėlės tirštumo sluoksnį virš skaidraus infranatanto. IIa tipo hiperlipoproteinemija (hipercholesterolemija) gali būti pirminė esant šeiminei hipercholesterolemijai (išryškėja vaikystėje), šeiminei mišriajai hiperlipidemijai, poligeninei hipercholesterolemijai, ar antrinė sergant hipotiroze, nefroziniu sindromu, esant disgamaglobulinemijai. Kliniškai išryškėja ankstyvąja koronarine širdies liga. Šeiminėms formoms būdingos ksantomos sausgyslių srityje, ksantelazmos, balzganas žiedas ragenoje (arcus cornea). Sergant IIa tipo hiperlipoproteinemija, cholesterolio koncentracija padidėjusi (>6,5 mmol/l), triacilglicerolių koncentracija normali, MTL cholesterolio koncentracija padidėjusi (>4,1 mmol/l), elektroforegramoje išryškėjusi β lipoproteinų juosta, pastovėjęs per naktį 4 C temperatūroje ėminys išlieka skaidrus, galimas geltonai oranžinis serumo atspalvis. IIb tipo hiperlipoproteinemijos (mišriosios hiperlipidemijos) klinika ryškesnė negu IIa tipo; ksantomos būna rečiau. Ligoniai dažniau nutukę, jie netoleruoja gliukozės. Sergant IIb tipo hiperlipoproteinemija, cholesterolio koncentracija padidėjusi (>6,5 mmol/l), triacilglicerolių (endogeninės kilmės) koncentracija padidėjusi (>2,3 mmol/l), MTL cholesterolio koncentracija padidėjusi (>4,1 mmol/l), 276
278 Lipoproteinai, jų sudėtis, apykaita... elektroforegramoje išryškėjusios β lipoproteinų ir pre-β lipoproteinų juostos, pastovėjęs per naktį 4 C temperatūroje ėminys tampa šiek tiek drumstas. III tipo hiperlipoproteinemija (disbetalipoproteinemija), kai kraujyje atsiranda patologinių lipoproteinų, gali būti pirminė dėl apo E defekto ar antrinė, sergant sunkia cukrinio diabeto forma, hipotiroze, esant disgamaglobulinemijai, vartojant alkoholį. Kliniškai išryškėja ankstyvąja kraujagyslių liga: smegenų ir periferinių kraujagyslių pažeidimas toks pat dažnas, kaip ir vainikinių arterijų. Šeiminei formai būdingas ksantominis bėrimas: tuberozinės ksantomos ir ksantomos delnų linijose (xanthoma striata palmaris). Sergant III tipo hiperlipoproteinemija, cholesterolio koncentracija padidėjusi (>6,5 mmol/l), triacilglicerolių koncentracija padidėjusi (>2,3 mmol/l), MTL cholesterolio koncentracija normali ar šiek tiek padidėjusi, elektroforegramoje atsiranda plati β juosta, pastovėjęs per naktį 4 C temperatūroje ėminys susidrumsčia, o paviršiuje susidaro plonas grietinėlės tirštumo sluoksnis (ne visada). Diagnozė patikslinama nustačius apo E2/2 fenotipą ar (retai) apo E stoką. Šeiminė forma dažnai išryškėja tik suaugusiems individams. Lipoproteinų elektroforezinis tyrimas būtinas III HLP tipui nustatyti. IV tipo hiperlipoproteinemija gali būti pirminė esant monogeninei endogeninei hipertriacilglicerolemijai, šeiminei mišriajai hiperlipidemijai, sporadinei hipertriacilglicerolemijai, ar antrinė esant negydytam cukriniam diabetui, disgamaglobulinemijai, sergant nefroziniu sindromu, lėtiniu inkstų nepakankamumu, vartojant alkoholį. Kliniškai išryškėja ankstyvąja koronarine širdies liga, periferinių kraujagyslių liga. Tokiems ligoniams yra sutrikusi gliukozės tolerancija, būdinga hiperurikemija, hipertenzija, nutukimas; ksantomos retos. Sergant IV tipo hiperlipoproteinemija, cholesterolio koncentracija normali ar šiek tiek padidėjusi, triacilglicerolių (endogeninės kilmės) koncentracija padidėjusi, MTL cholesterolio koncentracija normali, elektroforegramoje išryškėjusi pre-β lipoproteinų juosta, pastovėjęs per naktį 4 C temperatūroje bandinys susidrumsčia. V tipo hiperlipoproteinemija (chilomikronemija nevalgius) gali būti pirminė esant šeiminei monogeninei hipertriacilglicerolemijai ir apo CII stokai, ar antrinė esant negydytam cukriniam diabetui ar sunkiai jo formai, disgamaglobulinemijai, sergant nefroziniu sindromu, lėtiniu inkstų nepakankamumu, vartojant alkoholį. Kliniškai išryškėja požymiai, būdingi I tipui; taip pat tokių ligonių gliukozės tolerancija sutrikusi, būdinga hiperurikemija, ankstyva koronarinė širdies liga. Sergant V tipo hiperlipoproteinemija, cholesterolio koncentracija normali ar padidėjusi, triacilglicerolių koncentracija smarkiai padidėjusi (>11,3 mmol/l), MTL cholesterolio koncentracija normali, elektroforegramoje išryškėjusi chilomikronų ir pre-β lipoproteinų juosta, ėminiui pastovėjus per naktį 4 C temperatūroje, chilomikronai iškyla į paviršių ir sudaro grietinėlės tirštumo drumsto serumo sluoksnį. Išaiškinus MTL receptoriaus geno struktūrą buvo sukurta naujų hiperlipoproteinemijų diagnostikos ir gydymo metodų. 277
279 Laboratoriniai tyrimai Apolipoproteinas A-I (Apo A-I) Tiriamoji medžiaga. Serumas. Rekomenduojama reikšmė. Vyrų 1,1 2,05 g/l, moterų 1,25 2,15 g/l. Diagnostinė vertė. Šeiminė hiper-α lipoproteinemija, svorio mažėjimas. A-β lipoproteinemija, lipoproteinlipazės kofaktoriaus (apo C-II) stoka, įvairios hipo-α lipoproteinemijų formos, hipertriacilglicerolemija, priešlaikinė koronarinė širdies liga, kepenų ląstelių funkcijos sutrikimai, cholestazė, nefrozinis sindromas, lėtinis inkstų nepakankamumas, didelis angliavandenių ar polinesočiųjų riebalų rūgščių kiekis maiste, rūkymas. Papildoma informacija. V: estrogenai, etanolis (nedidelės dozės), fibratai (klofibratas, gemfibrozilas), karbamazepinas, lovastatinas, nikotino rūgšties dariniai, geriamieji kontraceptikai, fenobarbitalis, pravastatinas, simvastatinas, nutukusių asmenų svorio mažėjimas ir fizinis aktyvumas. V: androgenai, β adrenoblokatoriai, diuretikai, probukolis, progestinai, rūkymas; didelis angliavandenių ar nesočiųjų riebalų rūgščių kiekis maiste. Apolipoproteinas B (Apo B) Tiriamoji medžiaga. Serumas. Rekomenduojama reikšmė. Vyrų 0,55 1,40 g/l, moterų 0,55 1,25 g/l. Diagnostinė vertė. Hiperlipoproteinemija: IIa, IIb, IV ir V tipai, hiperapo-β lipoproteinemija (normalus MTL cholesterolio ir padidėjęs MTL apo B kiekis), priešlaikinė koronarinė širdies liga, cukrinis diabetas, hipotirozė, nefrozinis sindromas, inkstų nepakankamumas, kepenų ligos, Kušingo sindromas, disglobulinemija, porfirija, nėštumas, nervinė anoreksija, infantilinė hiperkalcemija, sfingolipodistrofijos, Vernerio sindromas, emocinis stresas. α lipoproteinų stoka (Tanžero liga), heterozigotinė hipo-β lipoproteinemija, lecitincholesterol-aciltransferazės stoka, I tipo hiperlipoproteinemija, lipoproteinlipazės kofaktoriaus (apo C-II) stoka, hipertirozė, malabsorbcija, lėtinė anemija, sunkus kepenų ląstelių funkcijos sutrikimas, Rejė sindromas, uždegiminė sąnarių liga, lėtinė plaučių liga, mielominė liga, svorio mažėjimas. Apolipoproteino B nerandama sergant abetalipoproteinemija ir homozigotine hipo-β lipoproteinemija. Papildoma informacija. Diferencijuojant (atrenkant) ligonius, sergančius išemine širdies liga, apo B kiekio matavimas ir jo santykis su apo A-I yra informatyvesni rodikliai negu lipidų ar lipoproteinų cholesterolio kiekio matavimai. Dažniausiai apolipoproteinų kiekio nustatymas yra kaip papildomas tyrimas su lipoproteinų cholesterolio kiekio matavimais. V: androgenai (anaboliniai steroidai), β adrenoblokatoriai, ciklosporinas, diuretikai, gliukokortikoidai, katecholaminai, piknaudžiavimas alkoholiu, progestinai; didelis sočiųjų riebalų rūgščių ir cholesterolio kiekis maiste. V: cholestiraminas, estrogenai (moterys po menopauzės), fibratai (klofibratas, gemfibrozilis), HMG-KoA reduktazės inhibitoriai (lovastatinas, pravastatinas, simvastatinas), kolestipolis, neomicinas, nikotino rūgšties preparatai, probukolis, tiroksinas; didelis nesočiųjų riebalų rūgščių ir mažas cholesterolio kiekis maiste. bendrasis Cholesterolis Tiriamoji medžiaga. Serumas. Rekomenduojama reikšmė. <5,2 mmol/l. Diagnostinė vertė. Šeiminė ar poligeninė hiperlipoproteinemija (IIa ir IIb tipai), šeiminė disbetalipoproteinemija (III tipas), šeiminė mišrioji hiperlipidemija, I, IV, V tipų hiperlipoteinemija, hiper-α lipoproteinemija (nedidelis padidėjimas), antrinė hiperlipoproteinemija sergant kepenų ligomis, esant intrahepatinei ir ekstrahepatinei cholestazei, glomerulonefritui, nefro- 278
280 Lipoproteinai, jų sudėtis, apykaita... ziniam sindromui, lėtiniam inkstų nepakankamumui, kasos, prostatos piktybiniam navikui, hipotirozei, išeminei širdies ligai, podagrai, nėštumui, cukriniam diabetui, alkoholizmui, analbuminemijai, disglobulinemijai (paraproteinemijai ar padidėjus α globulinų sergant sistemine raudonąja vilklige), glikogeno kaupimo ligoms (I, III, VI tipai), Vernerio sindromui, nervinei anoreksijai, idiopatinei hiperkalcemijai, ūminei interminuojančiai porfirijai, izoliuotai augimo hormono stokai. α lipoproteinų stoka (Tanžero liga), hipolipoproteinemija ir abetalipoproteinemija, hepatocitų nekrozė, kepenų piktybinis navikas, hipertirozė, malabsorbcija, nepakankama mityba, megaloblastinė anemija, sunki ūminė liga, platus nudegimas, lėtinė obstrukcinė plaučių liga, protinis atsilikimas, reumatoidinis artritas, žarnų limfangiektazija. Prieš pradedant gydyti cholesterolio kiekį mažinančiais vaistais, būtina išsiaiškinti ir atmesti antrines priežastis. Papildoma informacija. Naudojant EDTA plazmą reikšmės yra 3% mažesnės dėl osmosinio vandens pasiskirstymo tarp ląstelių ir plazmos. Laikant ėminį kambario temperatūroje, gali pasikeisti laisvojo ir esterifikuotojo cholesterolio santykis (norma yra atitinkamai 25 35% ir 65 75%) dėl serumo lecitincholesterolaciltransferazės (LCAT) veikimo, bet tai nepakeičia bendrojo cholesterolio koncentracijos. Šiuolaikiniai fermentiniai metodai beveik visai pakeitė klasikinę Libermano Burchardo reakciją. Fermentinis metodas padidino specifiškumą, nors cholesteroloksidazė reaguoja ir su 3β hidroksicholesteroliais, kurių nedidelis kiekis yra serume (pvz., pregnenolonas, dehidroepiandrosteronas). Galimi sezoniniai cholesterolio kiekio svyravimai: didesnė koncentracija rudenį ir žiemą, mažesnė pavasarį ir vasarą. Kiti veiksniai, turintys įtakos cholesterolio koncentracijai: kūno padėtis imant kraują, neseniai suvalgytas maistas, emocinis stresas, mėnesinių ciklas. Cholesterolio kiekio matavimą reikėtų pakartoti praėjus 3 mėnesiams po miokardo infarkto. Ch: askorbo rūgštis, bilirubinas, hemolizė, β hidroksicholesteroliai. V: androgenai, chenodeoksicholio rūgštis, ciklosporinas, diuretikai (nedidelis poveikis), ergokalciferolis (didelė dozė), gliukokortikoidai, katecholaminai, levadopa; didelis sočiųjų riebalų rūgščių ir cholesterolio kiekis maiste. V: aminosalicilo rūgštis, asparaginazė, cholestiraminas, estrogenai, fibratai (klofibratas, gemfibrozilis), HMG-KoA reduktazės inhibitoriai (lovastatinas, pravastatinas, simvastatinas), interferonas, klonidinas, kolestipolis, nikotino rūgšties preparatai, neomicinas, probukolis, tiroksinas; mažas cholesterolio ir didelis polinesočiųjų riebalų rūgščių kiekis maiste. Didelio tankio lipoproteinų cholesterolis (DTL Ch) Tiriamoji medžiaga. Serumas. Rekomenduojama reikšmė. Vyrų > 0,91 mmol/l, moterų > 1,2 mmol/l. Diagnostinė vertė. Šeiminė hiper-α lipoproteinemija. Antrinis DTL Ch padidėjimas galimas sergant: pirmine biliarine ciroze, lėtiniu hepatitu, alkoholizmu, esant kitos kilmės lėtinei intoksikacijai. Abetalipoproteinemija, lipoproteinlipazės kofaktoriaus (apo C-II) stoka, įvairios hipo-α lipoproteinemijų formos ( žuvies akių liga, šeiminė cholesterolaciltransferazės stoka), įvairios hipertriacilglicerolemijos formos. Antrinis DTL Ch sumažėjimas galimas sergant nekontroliuojamu cukriniu diabetu, priešlaikine koronarine širdies liga, esant hepatocitų pažeidimui, cholestazei, nefroziniam sindromui, lėtiniam inkstų nepakankamumui. Papildoma informacija. Epidemiologiniai tyrimai rodo neigiamą DTL Ch kiekio koreliaciją su koronarinės širdies ligos (KŠL) dažniu bei paplitimu. DTL Ch kiekio matavimas svarbus nustatant KŠL riziką. Su kiekvienu DTL Ch kiekio sumažėjimu 0,13 mmol/l KŠL rizika išauga 25%. Kita svarbi šio rodiklio taikymo sritis vertinant KŠL riziką yra santykio DTL Ch su MTL Ch ar bendrojo cholesterolio kiekiu skaičiavimas. V: karbamazepinas, cimetidinas, estrogenai, etanolis (mažai), fibratai (pvz., gemfibrozilis), 279
281 lovastatinas, pravastatinas, simvastatinas, nikotino rūgštis, fenobarbitalis, nutukusių asmenų svorio mažėjimas, fiziniai pratimai. Ch: Mn 2+ naudojimas precipitacijai, po to cholesterolio koncentraciją matuojant fermentiniu metodu ir šiam tikslui naudojant fosfatinį buferinį tirpalą; hiperlipidemija. V: androgenai; β adrenoblokatoriai (ypač nekardioselektyvūs), diuretikai, interferonas, interleukinas, progestinai, rūkymas, gausus angliavandenių bei polinesočiųjų riebalų rūgščių kiekis maiste. Lipoproteinas(a) [Lp(a)] Tiriamoji medžiaga. Serumas. Rekomenduojama reikšmė. <0,3 g/l. Diagnostinė vertė. Priešlaikinė koronarinė širdies liga, smegenų kraujagyslių stenozė, nekontroliuojamas cukrinis diabetas, sunki hipotirozė. Papildoma informacija. Lp(a) kiekis su amžiumi nekinta. Didelė koncentracija (>0,3 g/l) yra susijusi su padidėjusia rizika koronarinei širdies ligai išsivystyti ankstyvame amžiuje. Lp(a) paveldėjimo genetiniai veiksniai sudaro arti 100%, todėl Lp(a) yra svarbus ankstyvas koronarinės širdies ligos rizikos žymuo. Nuo Lp(a) priklauso mažiau negu 15% bendrojo serumo cholesterolio kiekio, todėl asmenys, turintys padidėjusią pastarojo koncentraciją, gali turėti ir didelį Lp(a) kiekį. Kadangi plazminogeno seka yra 95% homologiška su apo(a), kuris yra pagrindinis Lp(a) baltymas, antikūnai, naudojami imuninei reakcijai, neturi kryžmiškai reaguoti su plazminogenu. V: insulino stoka. V: estrogenai, neomicinas, žuvų taukai (omega-3 riebalų rūgštys). Mažo tankio lipoproteinų cholesterolis (MTL Ch) Tiriamoji medžiaga. Serumas. Rekomenduojama reikšmė. 2,6 3,5 mmol/l. Diagnostinė vertė. Pirminė (šeiminė ar poligeninė) hiperlipoproteinenija IIa ir IIb tipų; ksantomos, arcus cornea, priešlaikinė koronarinė širdies liga. Antrinis MTL Ch padidėjimas būdingas sergant hipotiroze, nefroziniu sindromu, disglobulinemija, kepenų ligomis, porfirija, cukriniu diabetu, lėtiniu inkstų nepakankamumu, Kušingo sindromu, nervine anoreksija, esant nėštumui. Hipo-β lipoproteinemija ir abetalipoproteinemija, α lipoproteinų stoka (Tanžero liga), lecitincholesterolaciltransferazės stoka, I tipo hiperlipoproteinemija, lipoproteinlipazės kofaktoriaus (apo C-II) stoka. Antrinis MTL Ch sumažėjimas būdingas sergant hipertiroze, lėtine anemija, mielomine liga, plaučių liga, uždegimine sąnarių liga, sutrikus kepenų funkcijai, ištikus ūminiam stresui (pvz., liga, nudegimai). Papildoma informacija % cholesterolio kraujyje įeina mažo tankio lipoproteinų sudėtį. Dažniausiai taikomas yra MTL Ch kiekio apskaičiavimas Fridevaldo formule: MTL Ch (mmol/l) = Bendrasis cholesterolis ; (čia TG/2,22 atspindi LMTL cholesterolio kiekį mmol/l, o jei dydžiai reiškiami mg/100 ml, tai TG/5). Formulė tinka, kai triacilglicerolių (TG) koncentracija neviršija 4,54 mmol/l. Tikslesnis yra tiesioginis MTL Ch nustatymo metodas. Nustatytas tiesioginis ryšys tarp koronarinės širdies ligos dažnio ir MTL Ch kiekio. V: androgenai, β adrenoblokatoriai, chenodeoksicholio rūgštis, ciklosporinas, diuretikai, gliukokortikoidai, katecholaminai, progestinai; didelis sočiųjų riebalų ir cholesterolio kiekis maiste. V: aminosalicilo rūgštis, cholestiraminas, estrogenai, fibratai (pvz., klofibratas, gemfibrozilis), HMG-KoA reduktazės inhibitoriai (pvz., lovastatinas, pravastatinas, simvastatinas), interferonas, interleukinas, kolestipolis, neomicinas, nikotino rūgšties preparatai, prazosinas, tiroksinas; mažai sočiųjų riebalų ir cholesterolio turintis maistas, daug nesočiųjų riebalų turintis maistas. 280
282 Lipoproteinai, jų sudėtis, apykaita... Triacilgliceroliai (trigliceridai, TG) Tiriamoji medžiaga. Serumas. Rekomenduojama reikšmė. 1,8 mmol/l. Moterų, vartojančių geriamuosius kontraceptikus, TG kiekis serume yra 0,23 0,45 mmol/l didesnis negu nevartojančių. Kai TG kiekis > 11,0 mmol/l, yra didelė pankreatito rizika. Diagnostinė vertė. Hiperlipoproteinemijos I, IIb, IV ir V tipų dėl šeiminės ar sporadinės endogeninės hipertriacilglicerolemijos, šeiminės lipoproteinlipazės ar jos kofaktorius (apo C-II) stokos. Antrinis triacilglicerolių kiekio padidėjimas dėl šių pirminių patologinių būklių: nutukimas, sutrikusi gliukozės tolerancija, virusinis hepatitas, alkoholizmas, kepenų cirozė, ekstrahepatinė biliarinė obstrukcija, ūminis ir lėtinis pankreatitas, nefrozinis sindromas, lėtinis inkstų nepakankamumas, pirminė hipertenzija, ūminis miokardo infarktas, išeminė širdies liga, smegenų trombozė, hipotirozė, cukrinis diabetas, podagra, nėštumas, glikogeno kaupimo ligos (I, III, VI tipai), Dauno sindromas, kvėpavimo sutrikimo sindromas, nervinė anoreksija, idiopatinė hiperkalcemija, ūminė protarpinė porfirija, stresas. Hipo-β lipoproteinemija ir abetalipoproteinemija. Antrinis triacilglicerolių kiekio sumažėjimas dėl šių pirminių priežasčių: lėtinė obstrukcinė plaučių liga, smegenų infarktas, hipertirozė, laktozurija, bloga mityba, malabsorbcijos sindromas, galutinės parenchiminių kepenų ligų stadijos. Papildoma informacija. Svarbi paciento padėtis kraujo ėmimo metu, nes keičia kai kurių kraujo dedamųjų dalių, taip pat triacilglicerolių kiekį dėl to, kad plazmos tūris sumažėja 12% keičiant gulimą padėtį į stovimąją. Triacilglicerolių kiekis šiek tiek mažesnis plazmoje negu serume. V: β adrenoblokatoriai, cholestiraminas, ciklosporinas, diuretikai, estrogenai, etanolis, interferonas, katecholaminai, gliukokortikoidai, etanolis, per didelis kalorijų kiekis maiste, daug angliavandenių turintis maistas. Ch: askorbo rūgštis, laisvasis glicerolis. V: askorbo rūgštis (didelės dozės), aminosalicilo rūgštis, chenodeoksicholio rūgštis, fibratai, heparinas, nikotino rūgšties preparatai, omega-3 riebalų rūgštys (žuvų taukai), progestinai. 281
283 LAISVARADIKALĖ OKSIDACIJA, ANTIOKSIDACINĖ GYNYBA IR LIGOS Laisvieji radikalai ir jų susidarymas žmogaus organizme Prieš 2 milijardus metų Žemės atmosferoje ėmė kauptis deguonis tai lėmė aerobinių organizmų atsiradimą. Aerobai prisitaikė gyventi esant ore apie 21% deguonies. Tačiau deguonis yra dviašmenis kardas : būdamas aerobinio gyvenimo pagrindas, jis kartu yra ir toksiškas. Iš jo susidaro reaktyviojo deguonies atmainos (joms tenka apie 5% viso organizmo deguonies). Žmogaus organizmas nuolat gamina laisvuosius radikalus, kuriuos padaro nekenksmingus veikianti antioksidacinė sistema. Vykstant evoliucijai, kai kurios ląstelės išmoko panaudoti laisvuosius radikalus, pavyzdžiui, fagocitozei. Kai kurie laisvieji radikalai organizmui yra naudingi, jeigu jų susidaro ne per daug. Kai jų kiekis viršija antioksidacinės apsaugos galimybes, kyla oksidacinis stresas. Įrodytas šio streso poveikis daugelio žmogaus ligų patogenezei, pradedant glomerulonefritu, ateroskleroze, vėžiu, autoimuninėmis ligomis ir baigiant AIDS. Taigi dėl laisvųjų radikalų sukeltų reakcijų žmogus gali susirgti vėžiu ar gali būti skatinamas šios ligos progresavimas. Laisvųjų radikalų perteklius rūkoriams gali padidinti riziką susirgti plaučių vėžiu (rūkymas sukelia stiprų oksidacinį stresą plaučių audinyje), o sergantiems opiniu kolitu žarnų vėžiu. Dėl laisvųjų radikalų poveikio susidarę lipidų peroksidai kaupiasi aterosklerozinėse plokštelėse, traumos ar hipoksijos pažeistame smegenų audinyje ir kituose audiniuose (pavyzdžiui, apsinuodijus anglies tetrachloridu). Trumpam prisiminkime laisvųjų radikalų susidarymo mechanizmą. Atomą sudaro branduolys (turintis protonų ir neutronų) ir aplink jį skriejantys elektronai. Elektronai yra poriniai, ir kiekviena jų pora skrieja savo orbita aplink branduolį. Iš poros išmušus vieną elektroną ir susidaro laisvasis radikalas. Taigi laisvasis radikalas tai bet kurios medžiagos, kuri turi vieną ar daugiau neporinių elektronų, egzistavimo forma. Pavyzdžiui, molekulės gali būti laisvieji radikalai, jei vienas ar keli atomai turi nesuporintą elektroną (28 pav.). Tokios molekulės pavyzdys yra ir azoto oksido laisvasis radikalas, kuris yra ne kas kita, o endotelį atpalaiduojantis veiksnys. Kai susitinka du laisvieji radikalai, jų nesuporinti elektronai gali suformuoti porą, ir radikalai prarandami. 282
284 Laisvaradikalė oksidacija, antioksidacinė gynyba ir ligos 1. Radikalai gali jungtis su beradikalėmis molekulėmis susidarant naujam radikalui 2. Radikalai gali atiduoti nesuporintą elektroną neradikalui ir pastarasis gali tapti radikalu 3. Kai susitinka du radikalai, grandininė reakcija sustoja 28 pav. Laisvųjų radikalų susidarymas Laisvieji radikalai yra aktyvesni negu jų neradikalinės formos. Dauguma fiziologinėmis sąlygomis susidarančių molekulių neturi nesuporintų elektronų. Tačiau vykstant audinių kvėpavimui ar fagozitozei, organizme susidaro laisvųjų radikalų. Jie gali reaguoti su beradikalėmis molekulėmis. Taip susidaro nauji radikalai. Taigi vyksta grandininė reakcija. Žmogaus organizme susidaro keletas rūšių laisvųjų radikalų. Kraujagysles išklojančios endotelio ląstelės, reaguodamos į dirgiklius, pavyzdžiui, acetilcholiną, bradikininą, atsako azoto oksido radikalo NO sekrecija. Ši medžiaga atpalaiduoja kraujagyslių sienelėje esančias lygiųjų raumenų ląsteles, dėl to išsiplečia kraujagyslės, krinta kraujospūdis. Daug reaktyvesnis, palyginti su NO, yra hidroksilo radikalas OH. Paveikto, pavyzdžiui, γ spinduliais, vandens molekulė skyla ir susidaro protonas (H + ) bei OH - su neporiniu elektronu, t. y. OH radikalas. OH gali atakuoti daugelį molekulių, esančių žmogaus organizmo ląstelėse, pradėdamas grandinines laisvųjų radikalų reakcijas. Dėl gamtoje esančios natūralios (foninės) jonizuojančiosios spinduliuotės, žmogaus organizme nuolatos susidaro nedidelis hidroksilo radikalų kiekis. Organizmo antioksidacinė sistema su tuo kiekiu susidoroja. Tačiau vartojant maisto produktus, apdorotus spinduliuote, pavyzdžiui, maisto sterilizacijai, organizme laisvųjų radikalų kiekis padidėja. Prisijungusi elektroną deguonies molekulė sudaro dar vieną reaktyviojo deguonies atmainą superoksido radikalą O 2 - (O 2 O 2 - ). Jis ne toks reaktyvus kaip hidroksilo radikalas. Reaguodamas su azoto oksido radikalu sudaro beradikalį produktą. Taigi superoksido radikalas, jeigu pasigamina arti kraujagyslių endotelio ląs- 283
285 29 pav. Fagocito reakcija telių ar jose, gali pašalinti kraujagysles plečiantį (vazodilatacinį) NO poveikį, t. y. superoksido radikalas šiuo atveju veikia kaip vazokonstriktorius. Tai vienas fiziologinio kraujagyslių raumenų tonuso reguliavimo mechanizmų, o pati reakcija rodo, kaip skirtingai gali veikti laisvieji radikalai. Limfocitai ir fibroblastai nuolat gamina nedidelį kiekį O 2 - kaip augimo stimuliatorių. Žmogaus organizme esančių fagocitinių ląstelių (neutrofilų, eozinofilų, monocitų, makrofagų) funkcija yra sunaikinti svetimą medžiagą ar organizmą, pavyzdžiui, bakterijas, virusus (29 pav.). Kai fagocitas kontaktuoja su nepageidaujama medžiaga, jo membranoje esanti NADFH-oksidazė yra aktyvinama ir ima gamintis daug superoksido radikalo. Šis radikalas dalyvauja kitose reakcijose, kurių produktai (irgi radikalai) sunaikina bakterijas. Gerai, kai fagocitai gamina laisvuosius radikalus kovai su svetimais organizmais. Tačiau kartais laisvieji radikalai gali padaryti žalos ir patiems fagocitams, ir aplinkiniams audiniams. Sergant kai kuriomis ligomis, jų žala gali būti didesnė nei nauda. Pavyzdžiui, sergant reumatoidiniu artritu, aplinkiniuose sąnarių audiniuose randama daug suaktyvintų fagocitų. Juose gaminamo superoksido radikalo perteklius kaip tik ir pažeidžia sąnarių audinius vystosi sąnarių uždegimas. Sergant opiniu kolitu, laisvųjų radikalų perteklius pažeistų žarnų audinio fagocituose padidina storosios žarnos vėžio riziką. Kartais dėl suaugusiųjų kvėpavimo sutrikimo sindromo per didelė suaktyvintų neutrofilų infiltracija gali labai pažeisti plaučių audinį. Nuo laisvųjų radikalų ląstelėje nėra apsaugota nė viena medžiaga. Jie gali sukelti: DNR fragmentaciją (inicijuojama kancerogenezė), baltymų fragmentaciją (atsiranda autoimuninės reakcijos), lipidų peroksidaciją (vystosi aterosklerozė). angliavandenių fragmentaciją. Lipidai l a i s v ų j ų ra d i k a l ų poveikio su b s t r a t a i Vienas laisvųjų radikalų taikinių yra ląstelių membranų lipidai, tiksliau juose esančios nesočiosios riebalų rūgštys. Dauguma riebalų rūgščių žmogaus organizme nėra laisvos. Jos įeina į lipidų triacilglicerolių, fosfolipidų, cholesterolio esterių sudėtį. Nemažai į fosfolipidų sudėtį įeinančių riebalų rūgščių yra polinesočiosios. 284
286 Laisvaradikalė oksidacija, antioksidacinė gynyba ir ligos 1) Membranų baltymų atakavimas 2) Cholesterolio oksidacija 3) Dviejų peroksido radikalų reakcija susidarant vinetiniam labai reaktyviam deguoniui ( O 2 ) 4) Reakcija su antioksidatoriais Todėl 37 C temperatūroje membranos yra skystos. Ši savybė svarbi membranų komponentų judrumui, pralaidumui ir lemia su membrana susijusių baltymų funkcijas. Kita vertus, polinesočiosios riebalų rūgštys yra ypač jautrios laisvųjų radikalų atakai, o oksiduotos (peroksiduotos) rūgštys skatina aterosklerozę (30 pav.). Lipidų peroksidai yra žalingi ir pažeidžia organizmo ląsteles. Šie radikalai gali: reaguoti su membranų baltymų aminorūgščių liekanomis ir taip pažeisti baltymų funkcijas, pavyzdžiui, fermentų, hormonų receptorių ar mažo tankio lipoproteinų receptorių; oksiduoti membranų cholesterolį; aterosklerozės vystymuisi yra svarbus ne tiek pats cholesterolis, kiek jo oksiduoti produktai; ištraukti vandenilio atomą iš polinesočiųjų riebalų rūgščių grandinių ir taip tęsti grandininę laisvųjų radikalų reakciją, kurios metu gaminasi peroksidai; taigi viena reakcija gali turėti grandininį poveikį peroksiduojant daugybę riebalų rūgščių grandinių; reaguoti tarpusavyje, jei membranoje susiduria du peroksido radikalai; reaguoti su antioksidatoriais. Antioksidacinė gynyba 30 pav. Lipidų peroksidacijos mechanizmas Organizmo ląstelės turi antioksidacinę sistemą, kuri kontroliuoja laisvųjų radikalų susidarymą ir nuo jų apsaugo DNR, baltymus ir riebalus. Ši gynyba yra dviejų rūšių: 285
287 pirminė ir antrinė. Pirminės antioksidacinės gynybos funkcija yra sustabdyti laisvųjų radikalų susidarymą ar padaryti juos nekenksmingus. Antrinė antioksidacinė gynyba tai įvairūs oksidacijos pažeistų biomolekulių taisymo mechanizmai (30 lentelė). Žmogaus ląstelių mitochondrijos turi fermentą superoksiddismutazę (SOD), kuri reaktyvųjį superoksido radikalą paverčia ne tokiu aktyviu vandenilio peroksidu (jis nėra radikalas) (31 pav.). 30 lentelė. Organizmo gynyba prieš laisvųjų radikalų sukeliamą oksidacinį pažeidimą Antioksidatoriai Superoksiddismutazė Glutationperoksidazė ir katalazė E vitaminas ir β karotenas Šlapimo rūgštis ir C vitaminas Mechanizmas Superoksido radikalą paverčia vandenilio peroksidu Vandenilio peroksidą verčia nekenksminga vandens molekule ir molekuliniu deguonimi Reaguoja su laisvaisiais radikalais ir sustabdo ląstelinių struktūrų pažeidimą; yra tirpūs riebaluose ir taip gali apsaugoti membranas Reaguoja su laisvaisiais radikalais citoplazmoje Taisymo sistemos Proteinazės (endopeptidazės) Proteazės Fosfolipazės Egzonukleazės ir endonukleazės Mechanizmas Atskelia oksiduotus baltymus Skaido proteinazių veiklos produktus Atskelia pažeistas oksiduotų lipidų dalis membranose taip, kad kiti fermentai galėtų ištaisyti pažeistus segmentus Iškerpa pažeistus DNR segmentus 1. Reaktyvųjų deguonies atmainų susidarymas ir neutralizavimas G glutationas Se selenas 2. a tokoferolio reakcija su peroksido radikalais 3. Augalinės kilmės medžiagos: b karotenas, likopenas, flavonoidai 31 pav. Svarbiausieji antioksidatoriai ir jų veikimas 286
288 Laisvaradikalė oksidacija, antioksidacinė gynyba ir ligos Toliau H 2 O 2 neutralizuoja glutationperoksidazė (esant glutationo) arba katalazė. Maiste turi būti seleno, nes glutationperoksidazė organizme yra vienintelis fermentas, kurio aktyvumui būtinas selenas. Glutationperoksidazė neutralizuoja vandenilio peroksidą naudodama redukuotąjį glutationą (jis virsta oksiduotuoju glutationu). O katalazė greit suskaido vandenilio peroksidą į vandenį ir deguonį. Nesuskilęs H 2 O 2 taip pat sąveikauja su Fe 2+ ar Cu 2+ (jie atiduoda elektroną), ir ląstelėje pasigamina hidroksilo radikalas. Antioksidacinės gynybos funkcija yra palaikyti minimalų laisvųjų metalų jonų kiekį. Geležis nešama kraujo plazmoje transferino pavidalu, todėl ji neskatina lipidų peroksidacijos. Varis įeina į kraujo plazmos baltymo ceruloplazmino sudėtį. Tačiau organizmo ląstelės turi paimti metalų jonų iš pernašos baltymų, todėl tarp pernašos formos ir galutinės lokalizacijos ląstelėje geležies ir vario jonai gali būti laisvi ir skatinti laisvųjų radikalų reakcijas. Ląstelėse šių metalų jonų stengiamasi palaikyti kiek galima mažiau, pavyzdžiui, jų perteklių sujungti su ląsteliniais sankaupų baltymais (feritinu). Yrant ląstelėms, šie metalų jonai atsipalaiduoja į aplinką ir gali skatinti laisvųjų radikalų reakcijas. Membranoms ir kraujo plazmos lipoproteinams apsaugoti nuo peroksidacijos svarbus vaidmuo tenka lipiduose tirpiems antioksidatoriams. Svarbiausias iš jų yra α tokoferolis. Tai vienas gausiausių E vitamino komponentų. Kiti antioksidatoriai (C vitaminas, glutationas, šlapimo rūgštis, transferinas, ceruloplazminas ir fermentai superoksiddismutazė, katalazė, glutationperoksidazė) veikia vandeninėje aplinkoje. α tokoferolio molekulėje funkciškai svarbiausia yra hidroksilo grupė, kurios vandenilio atomas yra lengvai atiduodamas. Lipidų peroksidacijos metu pasigaminę peroksido radikalai reaguoja su α tokoferoliu ir susidaro nereaktyvus tokoferolio radikalas: tokoferolis OH + lipidaio 2 lipidaio 2 H + tokoferolis-o. α tokoferolis ar kiti β, γ tokoferoliai, neutralizuodami peroksido radikalus, apsaugo nuo galimo tolesnio jų poveikio baltymams ar polinesočiųjų riebalų rūgščių grandinėms ir sustabdo grandininę laisvųjų radikalų reakciją. α tokoferoliui reaguojant su peroksido radikalais, pasigaminęs α tokoferolio radikalas (tokoferilas ) vėl virsta aktyviuoju α tokoferoliu dalyvaujant redukuotajai askorbo rūgščiai (C vitaminui). α tokoferolis yra svarbiausias lipiduose tirpus antioksidatorius žmogaus organizme, bet ne vienintelis. Kiti antioksidatoriai tai β karotenas, likopenas, kiti tokoferoliai, flavonoidai. Kaip ir α tokoferolis, šios medžiagos yra augalinės kilmės. Joms reaguojant su laisvaisiais radikalais, susidaro antioksidatorių radikalai, kurie vėl tampa aktyvūs po reakcijos su redukuotąja askorbo rūgštimi. Taigi veikdami kartu C ir E vitaminai slopina lipidų peroksidaciją. Tačiau C vitaminas peroksidaciją gali ir skatinti, jei terpėje yra geležies jonų. Jis redukuoja Fe 3+ į Fe 2+, o ši, vėl atidavusi e, virsta Fe 3+ ir taip skatina reaktyviųjų deguonies radikalų susidarymą. 287
289 Oksidacinis stresas ir ligos Antioksidacinė gynyba žmogaus organizme vyksta tokiu greičiu, kokiu gaminasi laisvieji radikalai. Laisvųjų radikalų susidarymo intensyvumas ar substratų šiai atakai daugėjimas gali sukelti oksidacinį stresą. Oksidacinis stresas gali ištikti suirus natūraliesiems antioksadatoriams ar nekaloringame dietiniame maiste esant mažai α tokoferolio, kitų antioksidatorių. Oksidacinio streso priežastis yra nepalankūs aplinkos veiksniai stresas, rūkymas. Dėl tabako dūmų poveikio ne tik suskyla C ir E vitaminai, bet ir aktyvinami fagocitai plaučiuose, superoksido radikalo gamyba juose. Nustatyta, kad išemijos metu slopinama natūralių biologinių antioksidatorių sintezė. Laisvieji radikalai pažeidžia ne tik lipidus, bet ir DNR, baltymus, ir tai gali būti net svarbesnė pažeidimo grandis negu lipidų peroksidacija. Šis poveikis priklauso ir nuo to, koks audinys ar ląstelė pažeidžiama, kas sukelia stresą. Be abejo, laisvieji radikalai nėra tiesioginė daugelio ligų priežastis, nors jų svarba didelė. Ligos priežastis dažniausiai yra kita ar kelių veiksnių sukelta, o oksidacinis stresas yra antrinis reiškinys. Pavyzdžiui, aktyvinti fagocitai gamina superoksido radikalą. Tam tikros vietos infiltracija jais ir pačių fagocitų aktyvinimas gali sukelti vietinį oksidacinį stresą. Antai reumatoidinis artritas yra susijęs su oksidaciniu audinių pažeidimu, nes juose daug suaktyvintų fagocitų. Tačiau neabejojama, kad oksidacinis stresas lemia aterosklerozės išsivystymą ir centrinės nervų sistemos pažeidimą, yra svarbiausias senėjimo proceso, imuninės sistemos silpnėjimo ir kai kurių ligų (vėžio, aterosklerozės, Alzhaimerio ar Parkinsono ligos) vystymosi veiksnys. Aterosklerozė yra daugelio priežasčių nulemtas procesas. Tačiau neabejotina, kad šiam procesui ypač svarbus endotelinių ląstelių pažeidimas. Monocitai prilimpa prie funkciškai pažeisto endotelio, patenka į intimą, kur virsta makrofagais. Suaktyvinti monocitai ir makrofagai gamina superoksido radikalus. Kaip atsakas į juos proliferuoja lygiųjų raumenų ląstelės ir limfocitai. Būdingas ląstelių tipas, nustatomas esant ateroskleroziniam pažeidimui, yra lipidų prisirijusi putotoji ląstelė. Mažo tankio lipoproteinai, pereinantys kraujagyslių sienelę, aterosklerozinio pažeidimo vietoje yra peroksiduojami. Šiame procese dalyvauja ir lipoksigenazė, esanti pažeistose endotelio ląstelėse. Be to, metalų jonai, atsipalaidavę iš pažeistų ląstelių, gali atiduoti elektroną vandenilio peroksidui, susidariusiam iš suaktyvintų monocitų ir makrofagų gaminamo superoksido radikalo. Fentono reakcijoje susidaro OH ir prasideda grandininė laisvaradikalė reakcija. Lipoproteinai, kurių lipidai buvo paveikti laisvųjų radikalų, tampa lyg ir svetimi organizmui ir turi būti šalinami. Peroksiduotieji mažo tankio lipoproteinai atpažįstami specialiųjų makrofagų receptorių, vadinamųjų receptorių valytojų ir greitai praryjami. Tokia putotoji ląstelė lieka subendoteliniame tarpe ir pradeda formuoti darinį ateromą. 288
290 Laisvaradikalė oksidacija, antioksidacinė gynyba ir ligos Galvos ir nugaros smegenys yra ypač jautrios oksidaciniam stresui dėl šių priežasčių: membranų lipiduose daug polinesočiųjų riebalų rūgščių; antioksidacinės sistemos poveikis smegenims yra nedidelis; kai kuriose smegenų srityse daug ląstelinės geležies jonų, kurie greitai atsipalaiduoja pažeidus ląsteles; smegenų skystyje, kitaip nei kraujo plazmoje, yra mažai transferino, ir šis nebesujungia atsipalaidavusių geležies jonų; nervų sistemoje yra daug adrenalino, noradrenalino, dopamino, kurie reaguoja su deguonimi ir susidaro superoksido radikalas O 2 (dvivalenčiai geležies jonai šią reakciją paskatina). Taigi išeminis ar trauminis smegenų pažeidimas gali lemti greitesnę laisvųjų radikalų reakciją. Ji plinta ir pažeidžia aplinkinius audinius audinys homogenizuojamas, t. y. suardomas ląstelių vientisumas. Laisvųjų radikalų ir antioksidatorių tyrimas Laisvuosius radikalus išmatuoti sunku, nes jų gyvavimo puslaikis yra labai trumpas, o koncentracija labai maža. Laisvieji radikalai gali būti matuojami tiesioginiu spektroskopiniu elektronų apsukų rezonanso metodu. Tačiau šis tyrimo metodas yra sudėtingas ir jį naudoja tik mokslininkai. Reakcijoms įvertinti ir jų metu susidariusių produktų kiekiams nustatyti gali būti taikomi šie metodai: laisvuosius radikalus generuojančių fermentų aktyvumo matavimas; antioksidatorių koncentracijos nustatymas; laisvaradikalių reakcijų produktų, pavyzdžiui, peroksidų, kiekio nustatymas; oksiduotų mažo tankio lipoproteinų koncentracijos kraujo serume vieno svarbiausių ikiklinikinės aterosklerozės žymenų matavimas. Api b e n d r i n i m a s Laisvasis radikalas tai bet kurios medžiagos, kuri turi vieną ar daugiau nesuporintų elektronų, egzistavimo forma. Laisvieji radikalai yra aktyvesni negu jų beradikalės formos. Laisvųjų radikalų susidarymas ir jų sukeltos reakcijos organizme yra neišvengiamos, o kai kurios jų ir naudingos. Laisvieji radikalai gali sukelti DNR fragmentaciją (inicijuojama kancerogenezė), baltymų fragmentaciją (atsiranda autoimuninės reakcijos), lipidų peroksidaciją (vystosi aterosklerozė). Kad organizme būtų palaikoma pusiausvyra tarp laisvųjų radikalų sukeltų oksidacijos reakcijų, veikia antioksidacinė gynyba. Kai laisvųjų radikalų kiekis viršija antioksidacinės apsaugos galimybes, kyla oksidacinis stresas. 289
291 KRAUJO PLAZMOS KREŠĖJIMO IR FIBRINOLIZĖS SISTEMA, JOS SUTRIKIMŲ LABORATORINĖ DIAGNOSTIKA Įv a d a s Hemostazė tai subalansuotos kraujo, endotelinių ląstelių, kraujo plazmos baltymų ir mažos molekulinės masės medžiagų sąveikos rezultatas. Normali hemostazė reiškia, kad nėra kraujavimo ir trombozės (32 pav.). Kraujo plazmos krešėjimas (koaguliacija) yra vienas kraujavimo stabdymo (hemostazės) sistemos elementų. Hemostazėje dalyvauja: audiniai, kraujagyslės sienelė, trombocitai, kraujo plazmos krešėjimo faktoriai, fibrinolizės sistema. 32 pav. Krešėjimo faktorių koncentracijos ryšys su trombozės ar kraujavimo rizika Kraujo krešėjimo reakcijos ir krešulio susidarymas Norint lokalizuoti sutrikimą nustatant specifinį faktorių ar faktorius, kurie yra pažeisti, reikia žinoti chemines kraujo krešėjimo reakcijas, pradedant kraujavimo priežasties atskleidimu ir baigiant galutiniu krešulio susidarymo supratimu. Kraujo krešėjimo procesą sudaro keletas etapų. Pirmasis, kuriame dalyvauja trombocitai, kaujagyslės sienelė ir kai kurie plazmos baltymai, vadinamas pirmine 290
292 Kraujo plazmos krešėjimo ir fibrinolizės sistema... Kraujagyslės sienelė Trombocitai Plazmos krešėjimo faktoriai Plazmos fibrinolizės faktoriai 33 pav. Hemostazės sisemos komponentai hemostaze (33 pav.). Ji prasideda iš karto po pažeidimo. Šiame etape svarbūs subendoteliniai jungiamojo audinio elementai kolagenas, pamatinė membrana ir kt. Kraujagyslė susitraukia, trombocitai jungiasi (adhezija) prie minėtų subendotelinių struktūrų, po to agreguoja, išskirdami medžiagas (ADF, ATF, serotoniną, tromboksaną A 2 ), kurios skatina agregaciją (31 lentelė). Fibrino susidarymo etapas: šį procesą katalizuoja kaskada veikiantys krešėjimo veiksniai, jis vadinamas antrine hemostaze. 31 lentelė. Hemostazės etapai po pažeidimo laiko atžvilgiu Pirminė hemostazė Antrinė hemostazė Fibrinolizė Vazokonstrikcija (tuoj po pažeidimo) Trombocitų adhezija (sekundės) Trombocitų agregavimas (3 5 minutės) Krešėjimo faktorių aktyvinimas Fibrino susidarymas (5 10 minučių) Fibrinolizės aktyvinimas (minutės) Krešulio lizė (48 72 val.) Hemostazės mechanizme dalyvauja daug faktorių, kurių dauguma yra baltymai (32 lentelė). Krešėjimo faktoriai žymimi romėniškais skaitmenimis ta tvarka, kaip jie buvo atrasti. Prie skaičiaus raidė a žymi aktyviąją baltymo (faktoriaus) formą, o raidė f fragmentuotąją. Audinių faktorius dar žinomas kaip III faktorius, o kalcio jonai kaip IV faktorius. VI faktorius yra ne kas kita kaip aktyvioji V faktoriaus forma. 32 lentelė. Kraujo plazmos krešėjimo baltymai Baltymas ir jo molekulinė masė (daltonais) I faktorius II faktorius (III) faktorius Sinonimas Baltymo rūšis Funkcija ir kelias Fibrinogenas Protrombinas Audinių faktorius (audinių tromboplastinas) Struktūrinis krešulio baltymas Susidarant krešuliui, virsta fibrinu; bendras kelias Nuo K vitamino priklausomas Aktyvina I, V, VIII, XIII, profermentas (serino C baltymą ir trombocitus; proteinazė) bendras kelias 291
293 32 lentelės tęsinys Baltymas ir jo molekulinė masė Sinonimas Baltymo rūšis Funkcija ir kelias (daltonais) (IV) faktorius Kalcio jonai (Ca 2+ ) V faktorius (VI faktorius) VII faktorius VIII faktorius IX faktorius X faktorius XI faktorius Proakcelerinas Aktyvioji V faktoriaus forma Prokonvertinas Antihemofilinis baltymas (antihemofilinis globulinas A) Kristmaso (Christmas) faktorius (antihemofilinis globulinas B) Stiuarto Prauerio (Stuart Prower) faktorius Plazmos tromboplastino pirmtakas Į ceruloplazminą panašus jungiamasis baltymas Nuo K vitamino priklausomas profermentas (serino proteinazė) Į ceruloplazminą panašus jungiamasis baltymas Nuo K vitamino priklausantis profermentas (serino proteinazė) Nuo K vitamino priklausomas profermentas (serino proteinazė) Profermentas serino proteinazė Palaiko Xa pradėtą II aktyvinimą; bendras kelias Aktyvina IX ir X; išorinis kelias Palaiko IXa pradėtą X aktyvinimą; vidinis kelias Aktyvina X; vidinis kelias Aktyvina II; bendras kelias Aktyvina XII ir prekalikreiną; vidinis kelias XII faktorius XIII faktorius fon Vilebrando (von Willebrand) faktorius Prekalikreinas Didelės mol. masės kininogenas Fibronektinas Antitrombinas III Heparino kofaktorius II C baltymas S baltymas Hagemano faktorius Fibriną stabilizuojantis faktorius Su VIII faktoriumi susijęs antigenas Didysis antitrombinas Mažasis antitrombinas Profermentas serino proteinazė Profermentas transglutaminazė Struktūrinis baltymas Profermentas serino proteinazė Aktyvina XI ir prekalikreiną; vidinis kelias Sudaro skersinius ryšius tarp fibrino molekulių (gijų) ir kitų baltymų; bendras kelias Skatina trombocitų adheziją; sujungia VIII faktorių Aktyvina XII ir prekalikreiną, skaldo didelės molekulinės masės kininogeną; vidinis kelias Jungiamasis baltymas Dalyvauja XII, XI ir prekalikreino aktyvinimo procese; vidinis kelias Struktūrinis baltymas Skatina ląstelių adheziją Serpinas (serino proteinazių inhibitorius) Serpinas Nuo K vitamino priklausomas profermentas (serino proteinazė) Nuo K vitamino priklausomas jungiamasis baltymas Slopina XIIa, Xa ir kitas proteazes, heparino kofaktorius Slopina IIa; heparino ir dermatansulfato kofaktorius Inaktyvina Va ir VIIIa faktorius C baltymo kofaktorius 292
294 Kraujo plazmos krešėjimo ir fibrinolizės sistema... Kraujo plazmos krešėjimo faktoriai (baltymai) yra sintetinami kepenyse. II, VII, IX ir X faktorių, taip pat C bei S baltymų sintezei (karboksilinimo reakcijai) būtinas K vitaminas. Pagal krešėjimo pirminę teoriją (ją suformulavo Morawitz as 1904 m.) kraujo plazmos krešėjimo reakcijos aktyvinamos pažeidus audinius ir iš jų atsipalaidavus tromboplastinui. Pastarasis kartu su kalcio jonais neaktyvų protrombiną verčia aktyviu fermentu trombinu, o trombinas fibrinogeną verčia fibrinu: Protrombinas (II faktorius) Tromboplastinas (III faktorius) Kalcio jonai (IV faktorius) Trombinas Fibrinogenas (I faktorius) Fibrinas Atradus vis naujus baltymus, dalyvaujančius krešėjimo reakcijose, ši schema buvo išplėsta ir suformuluota kraujo plazmos krešėjimo kaskados teorija (D. Macfarlane, E. Davie, 1964). Ji remiasi tokiais principais: visi krešėjimo faktoriai kraujo plazmoje yra neaktyvūs; krešėjimo kaskada gali prasidėti ir vykti dviem keliais: vidiniu ir išoriniu; aktyvūs krešėjimo faktoriai turi fermentinį aktyvumą ir jie aktyvina kitus faktorius tam tikra seka, t. y. kaskada. Kraujo plazmos krešėjimo kaskada Kraujo plazmos krešėjimo kaskadą (34 pav.) pagal ją sukėlusias priežastis ir baltymų aktyvinimą būtų galima suskirstyti į: vidinį kelią (jis aktyvinamas, kai specialūs baltymai kontaktuoja su pažeistos kraujagyslės subendotelinėmis struktūromis); išorinį kelią (kai pažeistas endotelis atpalaiduoja audinių veiksnį); bendrą abiem keliams būdą. Inicijavimo reakcijos. Krešėjimo sistemą inicijuoja XII (Hagemano) faktorius ir (ar) VII faktorius. Kol kas nėra aiškūs šių faktorių aktyvinimo veiksniai in vivo. Pasigaminęs aktyvintasis XII faktorius (XIIa) dalyvauja teigiamo grįžtamojo ryšio grandinėje, kartu į šį procesą įtraukdamas prekalikreiną ir didelės molekulinės masės kininogeną taip pagaminama daugiau XIIa faktoriaus. Pradiniam aktyvinimui ir šių reakcijų greičiui svarbūs yra neigiamą krūvį turintys paviršiai. Kraujagyslės pažeidimas kaip tik ir sukuria tokį paviršių. Aktyvintasis XII fraktorius (XIIa) taip pat kontaktuoja su tokiu paviršiumi bei su didelės molekulinės masės kininogenu, kuris suaktyvina XI faktorių. Trūkstant prekalikreino, pagaminama mažiau XIIa ir XI faktorių. 293
295 Didelės mol. masės kininogenas Prekalikreinas Didelės mol. masės kininogenas VIDINIS KELIAS IŠORINIS KELIAS XII VII Trombinas IXa Xa XIIa XIIa VII a XI Audinių faktorius Ca ++ XIa IX Trombocitai Ca ++ Audinių faktorius Ca ++ IXa X Trombocitai Ca ++ VIII VIIIa Xa Trombocitai Protrombinas Ca ++ Va V Trombinas Fibrinogenas XIII Tirpūs fibrino monomerai Ca ++ Polimerizuoto fibrino krešulys XIIIa Kovalentiškai kryžminėmis jungtimis sutvirtintas fibrino krešulys 34 pav. Kraujo plazmos krešėjimo schema Proteoliziškai veikiant XIIa, Xa, IXa faktoriams ar trombinui, VII faktorius tampa fermentiškai aktyvus. Tarpinės reakcijos. Aktyvintasis VIIa faktorius yra galinga serino proteinazė, kuri aktyvina IX ar X faktorius, kartu veikiant lipoproteinui, vadinamajam audinių faktoriui, ir jonizuotajam kalciui. Audinių faktorius yra gaminamas audiniuose. IX faktorių gali taip pat aktyvinti XIa faktorius. Šiai reakcijai nebūtinas audinių faktorius lipoproteinas, bet jai būtini neigiamo krūvio fosfolipidai bei jonizuotasis kalcis. In vivo trombocitai ir yra šių fosfolipidų šaltinis. Ramybės būklės trombocitų paviršiuje šių fosfolipidų kiekis yra ribotas, bet jiems aktyvinantis hemostazės metu fosfatidilserinas ir fosfatidiletanolaminas iš citoplazminio membranos paviršiaus 294
296 Kraujo plazmos krešėjimo ir fibrinolizės sistema... pereina į išorinį membranos paviršių ir tokiu būdu susidaro optimalus paviršius, skatinantis krešėjimą aktyvinančias reakcijas. Laboratorijoje fosfolipidų ekstraktas (dalinis tromboplastinas) neturinčioje trombocitų plazmoje pakeičia trombocitų fosfolipidus ir taip dėl XIa poveikio suaktyvinamas IX faktorius. X faktorius gali būti aktyvintas tiesiogiai veikiant VIIa bei dalyvaujant audinių faktoriui ir kalcio jonams. Netiesiogiai jį gali suaktyvinti VIIa faktorius, nes VIIa (audinių) faktoriui aktyvinant IX faktorių, XIa faktorius sudaro kompleksą su fosfolipidais ir suaktyvintu VIII faktoriumi, kuris veikiant kalcio jonams aktyvina X faktorių. VIII faktorius yra svarbiausia molekulė hemostazėje, ir jo paveldima stoka yra žinoma kaip hemofilija A (VIII:C faktoriaus stoka). Trombinas nutraukia VIII faktoriaus peptidines jungtis ir taip susidaro jo aktyvioji forma. Xa faktoriaus susidarymas netiesioginiu keliu gali vykti tokiu pat ar didesniu greičiu negu X aktyvinimas veikiant VIIa (audinių) faktoriui (klasikinis išorinis kelias). Be to, šis kelias gali būti toks svarbus, kaip ir IX faktoriaus aktyvinimas veikiant XIa /fosfolipidams ir po to X faktoriaus aktyvinimas veikiant IXa faktoriui/fosfolipidams, VIIIa faktoriui (klasikinis vidinis kelias). Tuo iš dalies aiškinamas faktas, kad vykstant vidinio kelio reakcijoms kontaktinių faktorių stoka dažniausiai nėra susijusi su polinkiu kraujuoti, o VIII ir IX faktorių stoka yra susijusi su polinkiu gausiai kraujuoti. Taip pat žinoma, kad pastovus lėtas X faktoriaus aktyvinimas gali palaikyti mažą krešėjimo faktorių aktyvumą, o audinių faktorių atsipalaidavimas iš pažeisto audinio staigiai suaktyvina krešėjimo sistemą. Susidaręs Xa faktorius aktyvina profermentą protrombiną (II faktorių). In vivo ši reakcija vyksta trombocitų paviršiuje, kur aktyvintasis V faktorius (iš plazmos ar trombocitų), dalyvaujant kalcio jonams, suformuoja receptorių Xa faktoriui; taip susidariusi protrombinazė katalizuoja protrombino virtimą aktyviuoju fermentu trombinu. Krešulio susidarymas. Trombino susidarymas yra kertinis hemostazės proceso įvykis. Trombinas nuo α ir β fibrinogeno grandinių atskelia po du peptidus ir susidaro fibrino monomerai: Trombinas Fibrinogenas (iš 6 polipeptidinių grandinių) (αa) 2, (βb) 2 γ 2 2A 2B α 2 β 2 γ 2 (fibrino monomerai) Veikiant XIIIa faktoriui (transglutaminazei) tarp monomerų susidaro skersiniai ryšiai, paskui ir krešulys. Trombinas taip pat yra galingas trombocitų aktyvinimo fiziologinis stimulas. Dėl trombino proteolizinio poveikio VIII ir V faktoriams pasigamina šių molekulių aktyviosios formos, kurios savo ruožtu aktyvina X faktorių ir protrombiną. 295
297 Fibrino susidarymas yra galutinis taškas, kuris vertinamas atliekant visus krešėjimo laiko tyrimus: aktyvintojo dalinio tromboplastino laiko (ADTL), protrombino aktyvumo (PA), protrombino komplekso aktyvumo (SPA) ir kitus. Šis krešulys iš pradžių yra netvirtas ir jį palaiko elektrostatinės sąveikos jėgos tarp gretimų fibrino monomero molekulių. Galutinai krešulys stabilizuojasi formuojantis kovalentinėms lizino ir glutamino jungtims tarp gretimų fibrino molekulių γ grandinių, taip pat tarp gretimų α grandinių per XIIIa faktorių (fibrino stabilizavimo faktorius). XIII faktorius yra aktyvinamas proteoliziškai veikiant trombinui, esant kalcio jonams, taip pat pats fibrinogenas yra šios reakcijos kofaktorius. XIIIa faktorius prie fibrininio krešulio prijungia fiziologinį fibrinolizės inhibitorių α 2 antiplazmino inhibitorių, todėl krešulys yra ne toks jautrus tirpdančiam plazmino poveikiui. Jei formuojantis krešuliui veikia trombocitų kontraktilinis baltymas trombosteninas, tai krešulys susitraukia (vyksta krešulio kontrakcija). Krešėjimo slopinimas. Krešėjimo proceso reguliavimas, sprendžiant iš daugybės jame dalyvaujančių įvairių faktorių ir kofaktorių, yra ypač sudėtingas. Krešėjimo proceso slopinimą (inhibiciją) taip pat sudaro daug grandininių reakcijų ir jos taip pat susijusios su audinių pažeidimu. III antitrombinas priklauso serpinų šeimai serino proteinazių inhibitoriams, kuriems taip pat priskiriamas α 1 antitripsinas, α 2 antiplazminas, heparino II kofaktorius ir plazminogeno aktyvatoriaus inhibitorius. III antitrombinas yra fiziologinis trombino ir IXa faktoriaus inhibitorius. Taip pat nustatytas jo inhibuojantis poveikis prieš XIIa, XIa ir IXa faktorius. III antitrombinas ir trombinas santykiu 1:1 sudaro kompleksą, kuris yra fermentiškai neaktyvus. Tokį kompleksą galima aptikti naudojant specifinius antikūnus. Vartojant hepariną antikoaguliantinis III antitrombino aktyvumas labai padidėja (nuo mažos molekulinės masės heparino poveikio reakcija paspartėja per 2000 kartų), ir tai, manoma, yra pirminis heparino antikoaguliantinis poveikis. Kitas, kur kas silpnesnis trombino inhibitorius, yra heparino II kofaktorius. Su jo paveldima stoka susijęs polinkis išsivystyti trombozėms. Trombino aktyvumą taip pat slopina α 2 makroglobulinas. Nurodoma, kad kraujo cirkuliacijoje III antitrombinas inaktyvina 75% susidariusio trombino, o kitą dalį 25% inaktyvina α 2 makroglobulinas ir heparino II kofaktorius. C baltymas yra natūralus krešėjimo inhibitorius. Jo sintezė priklauso nuo K vitamino [K vitaminas yra reikalingas karboksilazei, dalyvaujančiai II, VII, IX, X faktorių (profermentų) posintetinės modifikacijos procese]. Kraujyje C baltymas yra neaktyvus profermento formos; jį aktyvina trombinas, kai aplinkoje yra kofaktoriaus trombomodulino; pastarasis yra susijęs su endotelio ląstlėmis. Aktyvus C baltymas proteoliziškai skaido aktyviuosius V ir VIII faktorius ir juos inaktyvina. Inhibicinį C baltymo aktyvumą reguliuoja šios proteazės prisijungimas prie aktyvinto C baltymo inhibitoriaus. 296
298 Kraujo plazmos krešėjimo ir fibrinolizės sistema... Papildomas, nuo K vitamino priklausomas natūralusis antikoaguliantas S baltymas veikia kaip krešėjimo faktorių inaktyvinimo veiksnys, kai C baltymas aktyvus. S baltymas, prisijungęs prie fosfolipidų, paskatina aktyviojo C baltymo sukeltą Va faktoriaus inaktyvaciją. Tokia sąveika in vivo vyksta trombocitų, kraujo ar endotelinių ląstelių paviršiuje. Heterozigotų C baltymo aktyvumas yra 50% normalaus ir dėl to šiems individams gali išsivystyti trombozės. C baltymo antigeną galima išmatuoti imunologiniu metodu. Kraujo plazmos fibrinolizės sistema Krešulio susidarymas sustabdo kraujavimą iš pažeistos kraujagyslės, tačiau galų gale krešulį reikia pašalinti, jei norima atnaujinti kraujotaką. Krešulį ištirpdo fibrinolizės sistema. Fermentas plazminas suskaido fibrino peptidinius ryšius. Šis fermentas ne tik hidrolizuoja krešulį (fibrinolizė), bet ir fibrinogeną (fibrinogenolizė) ir susidaro fibrino ir fibrinogeno degradacijos (skaldymo) produktai įvyksta krešulio lizė. Krešėjimo faktorių aktyvinimas yra susijęs su neaktyviojo profermento plazminogeno virtimu aktyviuoju fermentu plazminu. Šiame procese svarbiausi yra XIIa faktorius, kalikreinas, didelės molekulinės masės kininogenas. Audinių plazminogeno aktyvatorius (t-pa) gaminasi audiniuose. Jo aktyvumą padidina prisijungimas prie fibrino. Rekombinantinis žmogaus t-pa šiuo metu naudojamas kaip trombolizinis preparatas. Urokinazė yra plazminogeno aktyvatorius, randamas žmogaus šlapime. Išgryninta urokinazė naudojama trombolizinei terapijai. Streptokinazė yra bakterijų baltymas, turintis plazminogeno aktyvatoriaus (urokinazės) aktyvumą ir naudojamas trombolizinėje terapijoje. Kaip minėta, plazminas hidrolizuoja ne tik krešulį (fibrinolizė), bet ir fibrinogeną (fibrinogenolizė). Dėl proteolizės pirmiausia susidaro dar galintis krešėti X fragmentas, o procesui tęsiantis jau nekrešantys Y ir D fragmentai. Y fragmentas, kurį sudaro D ir E dalys, pats skyla į šias dalis. Galutinės proteolizės kompleksai yra įvairūs, tačiau būdingiausi yra sudaryti iš dviejų D ir vienos E dalių. Tai D dimerai tipiniai fibrino degradacijos (skaidymo) produktai ir atspindi antrinę (reakcinę) hiperfibrinolizę. Nustatyta, kad plazminas slopina trombino sukeltą trombocitų agregaciją. Pagaliau patys susidarę fibrino ir fibrinogeno degradacijos produktai (FDP) turi antikoaguliamąjį poveikį: slopina fibrino polimerizaciją ir kai kurių krešėjimo fermentų aktyvumą, svarbiausia trombino. Taigi fibrino ir fibrinogeno degradacijos produktai yra pirminės hiperfibrinolizės ir padidėjusios kraujavimo rizikos žymenys. Pabrėžtina, kad FDP tyrimas nepadeda atskirti fibrinogeno fragmentų nuo fibrino fragmentų. Plazminą inaktyvina baltymas α 2 antiplazminas, kuris sudaro kompleksus su plazminu. Todėl tokių kompleksų nustatymas gali būti fibrinolizės in vivo indikatorius. 297
299 Kr a u j o pl a z m o s kre š ė j i m o si s t e m o s laboratoriniai tyrimai Hemostazės sutrikimai klinikoje gali pasireikšti kraujavimu arba tromboze. Kraujo plazmos krešėjimo sistemos sutrikimų priežastimi yra nepakankamas faktorių (baltymų) aktyvumas. Jis gali būti įgimtas (retai) ar įgytas. Laboratoriniai tyrimai yra svarbiausi diagnozuojant įvairius hemostazės sutrikimus, taip pat ir vertinant gydymo sėkmę. Kraujo plazmos krešėjimo sistemos tyrimus galima suskirstyti taip: 1) atrankiniai tyrimai: protrombino aktyvumo (laiko) (PA, angl. prothrombin time, PT) protrombino komplekso aktyvumo (SPA), aktyvintojo dalinio tromboplastino laikas (ADTL); 2) individualių faktorių tyrimai (jų aktyvumo ir/ar koncentracijos, pvz., fibrinogeno); 3) aktyvacijos žymenų tyrimai: D dimerų, 4) inhibitorių tyrimai: antitrombinas III, C baltymo, S baltymo. Fibrinolizės sistemai vertinti yra taip pat nustatomi faktoriai: plazminogenas, audinių plazminogeno aktyvatorius (t-pa), fibrinolizės žymenys fibrino ir fibrinogeno degradacijos produktai (FDP), fibrinolizės inhibitoriai plazminogeno aktyvatoriaus inhibitorius (PAI) bei kiti. Klinikoje dažnai, be protrombino aktyvumo reikšmės, naudojamas apskaičiuotas tarptautinis sunormintas santykis TNS (angl. INR): tai protrombino santykis, gautas tuomet, kai laboratorijoje naudojamas tromboplastinas yra kalibruojamas pagal originalų PSO tromboplastino referentinį preparatą. Šiuo atveju antikoaguliacijos laipsnis yra išreiškiamas vienodai ir priklauso nuo laboratorijose naudojamų reagentų jautrumo, bet nepriklauso nuo tyrimo metodo. Krešėjimo faktorių stoka Įgimta krešėjimo faktorių stoka yra reta būklė (išskyrus fon Vilebrando faktoriaus stoką) (33 lentelė). Nedidelė krešėjimo faktorių stoka, kuri siekia 30% normalaus aktyvumo ir net mažesnė, paprastai nesusijusi savaiminiu kraujavimu. Tačiau esant ir kitiems rizikos veiksniams, pavyzdžiui, trombocitopenijai, būklė gali tapti pavojinga, ypač jei numatomos chirurginės intervencijos. Todėl būtina įsigilinti į anamnezę, nustatyti trombocitų skaičių, įvertinti jų funkciją, krešėjimo faktorių aktyvu- 298
300 Kraujo plazmos krešėjimo ir fibrinolizės sistema... mą. (Apie afibrinogenemiją detaliau skyriuje Žmogaus kraujo plazmos baltymai, jų tyrimas, rezultatų klinikinis interpretavimas ). 33 lentelė. Krešėjimo faktorių stoka ir jos klinika Faktoriaus stoka fon Vilebrando faktorius Minimalus aktyvumas (išskyrus chirurgiją) Klinikinis didelės faktorių stokos pasireiškimas Tyrimai >10% Kraujavimas ADTL, standartizuotas kraujavimo laikas Fibrinogenas 0,4 0,5 g/l Nedidelis kraujavimas ar trombozė PA, SPA, ADTL II faktorius 20 30% Kraujavimas PA, SPA, ADTL V faktorius 10 15% Kraujavimas PA, SPA, ADTL V ir VIII faktoriai (mišrioji stoka) 10 15% Kraujavimas ADTL, PA, SPA VII faktorius 10 15% Nedidelis kraujavimas, norma ar trombozė PA, SPA VIII faktorius >10% Kraujavimas ADTL IX faktorius >10% Kraujavimas ADTL X faktorius 10 15% Kraujavimas PA, SPA, ADTL XI faktorius 30% Kraujavimas ADTL XII faktorius Trombozė? ADTL Krešėjimo faktorių stoka dažniausiai yra gydoma šviežiai šaldyta (ar liofilizuota) plazma, išgrynintu donorų plazmos koncentratu ar rekombinantinės kilmės preparatais, plazmos frakcija, kurioje gausu nuo K vitamino priklausomų krešėjimo faktorių. Pavojinga gydymo koncentratais komplikacija yra autoantikūnų ( inhibitorių ) susiformavimas, kurie slopina atitinkamą krešėjimo faktorių. Įgyta krešėjimo faktorių ir jų inhibitorių stoka gali būti nustatoma sergantiesiems kepenų ligomis (dauguma krešėjimo faktorių gaminami kepenyse), vėžiu, esant septicemijai, traumai, nudegimui. Pavojinga gyvybei būklė yra diseminuotos intravazalinės koaguliacijos sindromas (DIK) tai sunaudojimo koagulopatija, kuri neretai išsivysto sergant kepenų ligomis, vėžiu, esant septicemijai. Ligos klinika vienu metu kraujavimas ir trombozė dėl krešėjimo pusiausvyros sutrikimo. Būdingi tokios būklės laboratoriniai požymiai yra šie: krešėjimo ir fibrinolizės faktorių bei jų inhibitorių sunaudojimas, sumažėjęs trombocitų skaičius, fibrinogeno kiekis, krešėjimo aktyvavimo žymenų padaugėjimas, pavyzdžiui, tirpaus fibrino, fibrino ir fibrinogeno degradacijos (skaldymo) produktų. 5 10% ligonių, kurie serga sistemine raudonąja vilklige, imuninėmis ligomis ar vartoja kai kuriuos vaistus, organizme pasigamina antikūnų, žinomų kaip lupus antikūnai, arba antikoaguliantai (LA). Šie inhibitoriai dažniausiai yra IgG ar IgA antikūnai, kurie yra nukreipti prieš fosfolipidinius krešėjimo faktorių aktyvacijos 299
301 komponentus. LA buvimas dažniausiai nėra susijęs su kraujavimo sutrikimais, nes šie antikūnai nebūtinai reaguoja su krešėjimo faktoriais. Dažniausiai toks sutrikimas įtariamas, kai yra pailgėjęs aktyvintojo dalinio tromboplastino laikas. LA yra susijęs su padidėjusia venų ir arterijų trombozės rizika. Api b e n d r i n i m a s Hemostazė tai subalansuota kraujo, endotelio ląstelių, kraujo plazmos baltymų ir mažos molekulinės masės medžiagų sąveika. Pirminė hemostazė tai procesas, kuriame dalyvauja trombocitai, kaujagyslės sienelė ir kai kurie plazmos baltymai. Fibrino susidarymo etapas, kurį katalizuoja kaskados principu veikiantys krešėjimo faktoriai, vadinamas antrine hemostaze. Kraujo plazmos krešėjimo kaskadą pagal ją sukėlusias priežastis ir baltymų aktyvaciją būtų galima suskirstyti į: vidinį kelią: IX faktoriaus aktyvinimas veikiant XIa/fosfolipidams ir po to X faktoriaus aktyvinimas veikiant IXa faktoriui/fosfolipidams, VIIIa faktoriui, išorinį kelią: X faktoriaus aktyvinimas veikiant VIIa/audinių faktoriui ir bendrą abiem keliams būdą. Fibrino susidarymas yra galutinis taškas, kuris vertinamas atliekant visus krešėjimo laiko tyrimus (ADTL, PA, SPA, kt.). Krešulį ištirpdo fibrinolizės sistema fermentas plazminas suskaido fibrine peptidinius ryšius, susidaro fibrino ir fibrinogeno degradavimo produktai (FDP) ir fibrino degradavimo produktai (D dimerai) įvyksta krešulio lizė. Pavojinga gyvybei būklė yra diseminuotos intravazalinės koaguliacijos sindromo (DIK) išsivystymas tai sunaudojimo koagulopatija, kuri gali išsivystyti po chirurginių intervencijų, taip pat sergant kepenų ligomis, vėžiu, esant septicemijai. Lupus antikūnai (antikoaguliantai) yra IgG ar IgA antikūnai, kurie yra nukreipti prieš fosfolipidinius krešėjimo faktorių aktyvacijos komponentus. Jų buvimas yra susijęs su padidėjusia venų ir arterijų trombozės rizika. Laboratoriniai tyrimai Aktyvintojo dalinio tromboplastino laikas (ADTL, angl. activated partial thromboplastin time, APTT) Tiriamoji medžiaga. Kraujas (Na citratas). Rekomenduojama reikšmė s. Patikslinta reikšmė priklauso nuo analizatoriaus tipo ir yra nustatoma kiekvienoje laboratorijoje atskirai. Diagnostinė vertė. VIII, IX, X, XI ar XII faktorių, taip pat kininogeno, prekalikreino, fibrinogeno, V ar II faktorių stoka, aukščiau išvardytų veiksnių inhibitoriai, DIK sindromas, lupus 300
302 Kraujo plazmos krešėjimo ir fibrinolizės sistema... antikoagulianto buvimas, nefrakcionuotojo heparino naudojimas antikoaguliacijai, tiesioginio poveikio antikoaguliantai. ADTL dažniausiai nustatomas parenkant ir kontroliuojant heparino dozę. Papildoma informacija. Tyrimą aktyvina kaolinas, celitas. ADTL dažniausiai nenormalus, kai bet kuris faktorius sumažėja <30 40% normalaus dydžio. Traumuojanti venos punkcija gali užkrėsti ėminį audinių tromboplastinu ir sutrumpinti ADTL. Plazmos užšaldymas mažina ADTL jautrumą lupus antikoagulianto poveikiui ir esamai XII, XI faktorių, kininogeno, prekalikreino stokai. Plazmos bandinio atšaldymas (žemiau kaip 36,8 o C), blogai centrifuguota plazma (su trombocitų likučiais), centrifugavimas praėjus daugiau nei 1 val. po kraujo paėmimo, taip pat didelė VIII:C faktoriaus ar (ir) fibrinogeno koncentracija trumpina ADTL. Nėsčiųjų organizme ADTL reikšmės būna mažesnės dėl dažnai padidėjusios fibrinogeno koncentracijos. Neteisingas kraujo paėmimas heparino terapijos metu (imant kraują iš heparino kateterio), maža fibrinogeno koncentracija (aktyvumas), maža VIII faktoriaus koncentracija ilgina ADTL. Esant AT-III stokai, ADTL vangiai ar visai nereaguoja į gydymą nefrakcionuotuoju heparinu. Heparinas, lipemija (lipemijos poveikis ADTL reikšmėms nustatomas optinės detekcijos metodu ir priklauso nuo analizatoriaus). V: chlorpromazinas, valproatai rūgštis. Antitrombinas III (AT-III) Tiriamoji medžiaga. Plazma (citratas). Rekomenduojama reikšmė %. Diagnostinė vertė. Ūminis hepatitas, mechaninė gelta, inkstų transplantatas, uždegimas, mėnesinės, K vitamino stoka, heparino indukuotoji trombocitopenija (HIT). Įgimtoji stoka, kepenų transplantatas, dalinė hepatektomija, DIK sindromas, nefrozinis sindromas, kepenų cirozė, vėžys, lėtinis kepenų nepakankamumas, ilgalaikis gydymas nefrakcionuotuoju heparinu. Papildoma informacija. Sumažėjus antitrombino III, yra polinkis trombozei; ši būklė lemia blogą atsaką gydant heparinu. Imunologiniais metodais matuojamas antitrombino III kiekis, bet ne funkcija (aktyvumas). Kiekis neturi įtakos įprastiniams krešėjimo tyrimams. V: anaboliniai steroidai, gemfibrozilis, varfarinas. V: gydymas heparinu, asparaginazė, estrogenai, geriamieji kontraceptikai. C baltymas Tiriamoji medžiaga. Plazma (citratas). Rekomenduojama reikšmė %. Diagnostinė vertė. Įgimta stoka: homozigotinė būklė, išryškėjanti naujagimių purpura fulminans ir (ar) išplitusia organų tromboze tuoj po gimimo. Įgyta stoka: kepenų ligos, gydymas geriamaisiais antikoaguliantais. Papildoma informacija. C baltymas yra nuo K vitamino priklausomas, sintetinamas kepenyse. Jis cirkuliuoja kaip neaktyvus zimogenas, kurį aktyvina trombinas, kai gaminasi proteolizinis fermentas C a baltymas. Pastarasis suskaido aktyviuosius krešėjimo V ir VIII faktorius. Trombomodulinas, endotelių ląstelių membranų receptorius, dalyvauja aktyvinant C baltymą in vivo. Trombinas, prisijungęs prie trombomodulino, iš karto aktyvina C baltymą; o laisvasis trombinas pirmiausia fibrinogeną verčia fibrinu. V: geriamieji kontraceptikai. 301
303 S baltymas Tiriamoji medžiaga. Plazma (citratas). Rekomenduojama reikšmė % (pagal analizatorių). Diagnostinė vertė. Įgimta stoka: sumažėja S baltymo aktyvumas ir laisvojo S baltymo antigeno kiekis; bendrojo S baltymo antigeno kiekis gali būti sumažėjęs, normalus ar padidėjęs. Padidėjus S baltymo surišimui, sumažėja biologiškai aktyvaus laisvojo S baltymo kiekis. Taip gali atsitikti sergant kepenų ligoms, gydant antikoaguliantais, esant uždegimo sindromui. Papildoma informacija. S baltymas yra nuo K vitamino priklausomas, sintetinamas kepenyse. Kaip bendro veikimo faktorius, jis didina antikoaguliantinį aktyvintojo C baltymo veikimą. Sveiko žmogaus plazmoje S baltymas yra dviejų formų: laisvasis ( 40%) ir surištasis (60%). Tik laisvajam S baltymui yra būdingas biologinis aktyvumas, o surištasis yra funkciškai neaktyvus. D dimerai (fibrino irimo produktai) Tiriamoji medžiaga. Plazma (citratas). Rekomenduojama reikšmė. <250 µg/l. Diagnostinė vertė. Antrinė fibrinolizė; gydomoji trombolizė naudojant audinių plazminogeno aktyvatorius; trombozinės komplikacijos: giliųjų venų trombozė, plaučių embolija, arterinė tromboembolija, DIK sindromas; nėštumas (paskutiniai trys mėnesiai ir ypač po gimdymo); piktybiniai navikai; chirurginė intervencija. Įtariant trombogenizaciją, D dimerų aptikimas labai aiškiai rodo neigiamą klinikinę diagnozę. Pakankamai jautriu metodu neradus D dimerų plazmoje, venų trombozės diagnozės įtarimas gali būti atmetamas 99,8% atvejų. Teigiamos reikšmės nebūtinai patvirtintų trombozės įtarimą, nes D dimerai atsiranda plazmoje ir nesant trombozės: paskutinius tris nėštumo mėnesius, pirmą parą po chirurginės intervencijos, po trombolizinės terapijos. Norint patvirtinti trombozės įtarimą, svarbu matuoti D dimerų augimo dinamiką ir lygį. Papildoma informacija. Šiuo tyrimu nustatomi fibrino irimo produktai D dimerai. Fibrinogenas ir fibrinogeno irimo produktai nereaguoja su antikūnais, naudojamais D dimerams aptikti. Teigiamas rezultatas gali padėti nustatyti besivystantį DIK sindromą, kitas kraujagyslių trombozes. II faktorius (protrombinas) Tiriamoji medžiaga. Plazma (citratinė). Rekomenduojama reikšmė %. Diagnostinė vertė. Įgimta stoka. Įgyta: retai pacientams, turintiems lupus antikoaguliantą, sergantiesiems kepenų ligomis, esant K vitamino stokai. Papildoma informacija. Tyrimas remiasi plazmos savybe pakeisti specifinės faktoriaus neturinčios plazmos protrombino laiką. Rezultatai išreikškiami normalios plazmos aktyvumo procentais. V: estrogenai, oraliniai kontraceptikai. V: anaboliniai steroidai, androgenai, antibiotikai, geriamieji antikoaguliantai. Ch: heparinas, lupus antikoaguliantas. V faktorius Tiriamoji medžiaga. Plazma (citratinė) Rekomenduojama reikšmė %. Diagnostinė vertė. Įgimta stoka. Įgyta: DIK sindromas, kepenų ligos, V faktoriaus inhibitoriai. 302
304 Kraujo plazmos krešėjimo ir fibrinolizės sistema... Papildoma informacija. Tyrimas remiasi paciento plazmos savybe pakeisti specifinės faktoriaus neturinčios plazmos protrombino laiką. V: estrogenai, geriamieji kontraceptikai. V: anaboliniai steroidai, androgenai, antibiotikai, geriamieji antikoaguliantai. Ch: heparinas, lupus antikoaguliantas. VIII faktorius (antihemofilinis faktorius) Tiriamoji medžiaga. Plazma (citratas). Rekomenduojama reikšmė %. Diagnostinė vertė. Hemofilija A, fon Vilebrando liga, specifiniai antikūnai prieš VIII faktorių, DIK sindromas (gali būti ir padidėjęs). Hepatocitų funkcijos sutrikimai, inkstų nepakankamumas. Papildoma informacija. VIII veiksnys yra ūminės uždegimo fazės baltymas. Gali padidėti 2 3 kartus po intensyvių fizinių pratimų; labai padidėja paskutinius tris nėštumo mėnesius. IX faktorius (Christmas faktorius) Tiriamoji medžiaga. Plazma (citratas). Rekomenduojama reikšmė %. Diagnostinė vertė. B hemofilija (Christmas liga). Įgytos priežastys: kepenų ligos, K vitamino stoka, Gošė liga, nefrozinis sindromas. Fibrino ir fibrinogeno degradacijos produktai (FDP) Tiriamoji medžiaga. Serumas. Rekomenduojama reikšmė. <5 mg/l. Diagnostinė vertė. Miokardo infarktas, trombozė, embolai plaučiuose, pirminė ir antrinė fibrinolizė, trombolizinė terapija, kitos DIK sindromo priežastys. Padidėja ne taip ryškiai sergant piktybinėmis, kepenų ligomis, esant infekcijoms. Papildoma informacija. Remiantis vien FDP tyrimu negalima diferencijuoti pirminės fibrinolizės nuo antrinės, taip pat fibrinogeno fragmentų nuo fibrino fragmentų. FDP koncentraciją didina fiziniai pratimai, stresas. Traumuojanti venos punkcija, ilgesnis venos užspaudimas ar grubus mėgintuvėlio kratymas gali duoti klaidingai teigiamą rezultatą. V: plazminogeno aktyvatoriai. Esant padidėjusiam reumatoidinio faktoriaus kiekiui, galimas klaidingai teigiamas rezultatas. Heparinas ir disfibrinogenemija taip pat gali duoti klaidingai teigiamą rezultatą. Fibrinogenas Tiriamoji medžiaga. Plazma (citratas) Rekomenduojama reikšmė. 2,0 4,0 g/l. Diagnostinė vertė. Fibrinogenas yra jautrus ūminės uždegimo fazės baltymas, kurio koncentracija, esant uždegimui ar audinių nekrozei, padidėja kelis kartus. Padidėjimą galima aptikti pirmomis 24 val. po insulto. Vartojant estrogenus, nėštumo metu kiekis gali padidėti. Padidėjusi koncentracija dėl koronarinės širdies ligos bei smegenų kraujagyslių ligų yra nepriklausomas rizikos veiksnys. Sutrikusi sintezė kepenyse, DIK sindromas. Disfibrinogenemija: aprašyti keli paveldimi fibrinogeno struktūros variantai. Dauguma jų nėra susiję su klinikinėmis problemomis. Fibrinogeno nebuvimas (afibrinogenemija) yra reta paveldima liga. Papildoma informacija. Fibrinogenas yra svarbiausias baltymas, veikiantis eritrocitų nusėdimo greitį. 303
305 Kraujavimo laikas (standartizuotas) Tiriamoji medžiaga. Matuojamas laikas, kai po dūrio į odą nustoja kraujuoti. Rekomenduojama reikšmė: naujagimių 0,8 1,7 min., vaikų 3 15 metų 1,3 9 min., suaugusiųjų 2,0 8,0 min. Diagnostinė vertė. Trombocitopenija, fon Vilebrando liga, uremija, kai kurios jungiamojo audinio ligos, paveldima telangiektazija, kepenų ligos. Papildoma informacija. Kraujavimo laikas yra atrankinis tyrimas, norint nustatyti trombocitų funkcijos sutrikimus ir kraujagyslių sienelės vientisumo pažeidimus. Kraujavimo laikas esant krešėjimo sutrikimams dažniausiai yra normalus. Tyrimas svarbus fon Vilebrando ligos diferencinei diagnostikai nuo lengvos hemofilijos formos. Šiuo tyrimu galima numatyti gausaus kraujavimo galimybę atliekant procedūrą. V: alopurinolis, aminokaprono rūgštis (didelės dozės), ampicilinas, aspirinas, dekstranas, diltiazemo hidrochloridas, etanolis, halotanas, heparinas, karbenicilinas, nifedipinas, nesteroidiniai vaistai nuo uždegimo (pvz., fenilbutazonas, ibuprofenas, indometacinas, ketoprofenas, naproksenas, piroksikamas), G penicilinas, propranololis, streptodornazė, streptokinazė, tiklopidinas, urokinazė, valproatai. V: eritropoetinas. Lupus antikoaguliantas (LA) Tiriamoji medžiaga. Plazma (citratas). Rekomenduojama reikšmė. 34,4 40,4 sek. (kokybinis nustatymas: neigiamas rezultatas krešėjimo laikas normalus, teigiamas rezultatas krešėjimo laikas gerokai pailgėja). Diagnostinė vertė. Lupus antikoaguliantas randamas sergant daugeliu ligų, pirmiausia autoimuninėmis; netekus vaisiaus; retais atvejais esant infekcijai, vartojant vaistų ar visiškai sveikiems asmenims. LA yra nustatomas pailgėjus ADTL ir atlikus atrankinį ADTL-LA tyrimą. Patikslinta LA koncentracija įvertinama specialiais tyrimais. Papildoma informacija. Lupus antikoaguliantai yra įvairūs imunoglobulinai (dažniausiai IgG), kurie sutrikdo nuo fosfolipidų priklausomas krešėjimo reakcijas. Šie antikūnai nebūtinai reaguoja su krešėjimo faktoriais jie veikia prieš anijoninius fosfolipidus. LA buvimas dažniausiai nėra susijęs su kraujavimo sutrikimais, nebent kartu yra trombocitopenija ar antikūnų prieš protrombiną. LA yra susijęs su padidėjusia venų ir arterijų trombozės rizika (priežastys ne iki galo žinomos). Klaidingai teigiami rezultatai galimi dėl specifinių krešėjimo faktorių inhibitorių, krešėjimo faktorių stokos ar geriamųjų antikoaguliantų vartojimo. Protrombino akt y vumas kviko protrombino l aikas, kuriuo įvertinamas II, V, VII, X faktorių aktyvumas (PA) Tiriamoji medžiaga. Plazma (Na citratas). Rekomenduojama reikšmė %. Terapinės ribos gydant geriamaisiais antikoaguliantais 15 30%, o TNS (INR) 2,0 4,5. Diagnostinė vertė. Tyrimas naudojamas: 1) kaip atrankinis, įtarus kraujo krešėjimo sutrikimą dėl vieno ar kelių audinių krešėjimo faktorių (II, V, VII, X) aktyvumo stokos; 2) parenkant dozę ir kontroliuojant gydymą K vitamino antagonistais (kumarino grupės preparatais). Šiuo atveju dėl tikslesnio oralinių antikoaguliantų poveikio įvertinimo būtina lygiagrečiai atlikti ir ADTL tyrimą, nes V faktorius nepriklauso nuo K vitamino ir jo matavimas sumažina tyrimo tikslumą; 3) K vitamino stokos ir kepenų ligų diagnostikai bei jų gydymo kontrolei; 4) ikioperacinei ligonių atrankai dėl galimų krešėjimo sutrikimų. Kepenų ligos; K vitamino stoka ar gydymas jo antagonistais (kumarino grupės preparatais); intravazalinis krešėjimas (DIK sindromas); paveldima faktorių II (protrombinas), V, VII ir X 304
306 Kraujo plazmos krešėjimo ir fibrinolizės sistema... stoka; afibrinogenemija, hipofibrinogenemija (fibrinogeno kiekis <0,6 g/l), disfibrinogenemija; cirkuliuojantys antikoaguliantai (pvz., lupus antikoaguliantas). Sergnt A ir B formų hemofilija, aktyvumas dažniausiai yra normalus. Papildoma informacija. Protrombino aktyvumas vertinamas kaip normos procentas ir apskaičiuojamas naudojant kalibracinę plazmą ar pagal referentinės plazmos kreivę. Protrombino aktyvumas mažėja, kai II, V, VII ir X faktoriai plazmoje sumažėja iki <40% normalaus jų lygio. Be protrombino aktyvumo reikšmės, naudojamas apskaičiuotas tarptautinis sunormintas santykis TNS (angl. INR): tai protrombino santykis, gautas tuomet, kai laboratorijoje naudojamas tromboplastinas yra kalibruojamas pagal originalų PSO tromboplastino referentinį preparatą. ISI* Paciento PA TNS = Normalus vidutinis PA * ISI Tarptautinis tromboplastino jautrumo koeficientas (angl. International sensitivity index of thromboplastin). Šiuo atveju antikoaguliacijos laipsnis yra išreiškiamas vienodai ir priklauso tik nuo laboratorijose naudojamų reagentų jautrumo (ISI), bet nepriklauso nuo tyrimo metodo. V: alkoholis (dažnas piktnaudžiavimas), aspirinas (mažos dozės), merkaptopurinas, geriamieji kontraceptikai. Su oraliniais antikoaguliantais gali reaguoti ir susilpninti jų poveikį šie vaistai: barbitūratai, cholestiraminas (sutrikdo absorbciją), etanolis, grizeofulvinas, chloruotieji anglies insekticidai, karbamazepinas, gliukokortikoidai, rifampinas. V: aminosalicilo rūgštis, anaboliniai steroidai, antistreptazė, asparaginazė, aspirinas (didelės dozės), cefalosporinai, chinidinas, chininas, cholestiraminas (retai), ciklofosfamidas, etanolis (didelės dozės, alkoholizmas), halotanas, heparinas (su koncentracija susijęs poveikis), α-2b interferonas, karbenicilinas, nikotino rūgštis, geriamieji antikoaguliantai, tiazidai, vidurius laisvinantys vaistai. Šie vaistai gali turėti papildomą poveikį, kartu vartojant geriamuosius antikoaguliantus. Kiti vaistai gali turėti poveikį šiems antikoaguliantams ir jų veikimą sustiprinti: alopurinolis, amiodaronas, chloralhidratas (pradinis poveikis), chloramfenikolis (slopina apykaitą), cimetidinas, eritromicinas, etakrino rūgštis, fenilbutazonas, gliukagonas, klofibratas, metronidazolis, sulfonamidai, tamoksifenas, tiroksinas. Protrombino komplekso aktyvumas, kuriuo įvertinamas protrombino II, VII, X faktorių komplekso aktyvumas protrombino prokonvertino metodu (SPA) Tiriamoji medžiaga. Plazma (Na citratas). Rekomenduojama reikšmė. Normos intervalas nevartojant geriamųjų antikoaguliantų >70%. Terapinės ribos gydant geriamasiais antikoaguliantais 15 26%, o TNS (INR) 2,0 4,5. Diagnostinė vertė. Tyrimas naudojamas: 1) kaip atrankinis, įtarus kraujo krešėjimo sutrikimą dėl vieno ar kelių protrombino komplekso faktorių (II, VII, X) aktyvumo stokos; 2) specializuotasis tyrimas parenkant dozę ir kontroliuojant gydymą K vitamino antagonistais (kumarino grupės preparatais, pvz., orfarinu, varfarinu). Vien šio tyrimo pakanka valdyti gydymą netiesioginiais antikoaguliantais, nes nustatomi jautriausiai į K vitaminą reaguojantys krešėjimo faktoriai (II, VII, X). Papildomai ADTL tyrimo atlikti nebūtina; 3) K vitamino stokos ir kepenų ligų diagnostikai bei jų gydymo eigos kontrolei; 4) ikioperacinei ligonių atrankai dėl galimų krešėjimo sutrikimų. Kepenų ligos; K vitamino stoka ar gydymas jo antagonistais (kumarino grupės preparatais); intravazalinis krešėjimas (DIK sindromas); paveldima II (protrombinas), VII ir X faktorių stoka; afibrinogenemija, hipofibrinogenemija (fibrinogeno kiekis <0,6 g/l), disfibrinogenemija; cirkuliuojantys antikoaguliantai (pvz., lupus antikoaguliantas). Sergant A ir B formų hemofilija, aktyvumas dažniausiai yra normalus. 305
307 Papildoma informacija. Protrombino aktyvumas vertinamas normos dydžio procentu ir apskaičiuojamas naudojant kalibracinę plazmą ar pagal referentinės plazmos kreivę. Protrombino aktyvumas mažėja, kai II, VII ir X faktoriai plazmoje sudaro <40% normalaus jų lygio. Be protrombino aktyvumo reikšmės, naudojamas apskaičiuotas tarptautinis sunormintas santykis TNS (aprašyta pirmiau Protrombino aktyvumas Kviko protrombino laikas, kuriuo įvertinamas II, V, VII, X faktorių aktyvumas ). V: alkoholis (dažnas piktnaudžiavimas), aspirinas (mažos dozės), merkaptopurinas, geriamieji kontraceptikai. Su geriamaisiais antikoaguliantais galintys reaguoti ir susilpninti jų poveikį vaistai: barbitūratai, cholestiraminas (sutrikdo absorbciją), etanolis, grizeofulvinas, chloruotieji anglies insekticidai, karbamazepinas, gliukokortikoidai, rifampinas. V: aminosalicilo rūgštis, anaboliniai steroidai, antistreptazė, asparaginazė, aspirinas (didelės dozės), cefalosporinai, chinidinas, chininas, cholestiraminas (retai), ciklofosfamidas, etanolis (didelės dozės, alkoholizmas), halotanas, heparinas (su koncentracija susijęs poveikis), α-2b interferonas, karbenicilinas, nikotino rūgštis, geriamieji antikoaguliantai, tiazidai, vidurius laisvinantys vaistai. Šie vaistai gali turėti papildomą poveikį vartojant geriamųjų antikoaguliantų. Šių antikoaguliantų veikimą gali sustiprinti kiti vaistai: alopurinolis, amiodaronas, chloralhidratas (pradinis poveikis), chloramfenikolis (slopina apykaitą), cimetidinas, eritromicinas, etakrino rūgštis, fenilbutazonas, gliukagonas, klofibratas, metronidazolis, sulfonamidai, tamoksifenas, tiroksinas. 306
308 ŠIRDIES IR KRAUJAGYSLIŲ LIGŲ LABORATORINĖ DIAGNOSTIKA Širdies ir kraujagyslių ligų rizikos veiksnių tyrimai Gydytojas ligonio gydymą pradeda nuo anamnezės, objektyvios apžiūros. Šiandien gydytojas, paskyręs įvairius laboratorinius tyrimus, turi galimybę gauti įvairių pokyčių sergančiame organizme skaitinę išraišką, įvertinti tų pokyčių dydį, kitimo tendencijas. Šiame skyriuje apžvelgiami dažniausiai širdies ligų diagnostikai taikomi laboratoriniai tyrimai. Rizikos veiksnys yra kintamas dydis, kuris atspindi statistinį ryšį su vėlesniu ligos išryškėjimu, nebūtinai būdamas ligos priežastis. Šiandien pripažinti širdies ir kraujagyslių ligų rizikos veiksnių tyrimai apima šių rodiklių nustatymą: lipidų ir lipoproteinų apykaitos rodikliai: cholesterolis (bendrasis), triacilgliceroliai, DTL cholesterolis, MTL cholesterolis, lipoproteinų fenotipavimas, Lp(a), apo B, apo A-I, apo E; homocisteinas, fibrinogenas, magnis, mikroalbuminas, šlapimo rūgštis, γ glutamiltransferazė. Laboratoriniams širdies ir kraujagyslių ligų rizikos veiksnių įvertinimo tyrimams būdingas nuoseklumas nuo paprasčiausių iki sudėtingų. 34 lentelėje pateikiami laboratoriniai tyrimai lipidų apykaitos sutrikimams diagnozuoti. 307
309 34 lentelė. Lipidų apykaitos sutrikimų diagnostiniai tyrimai Pagrindinė programa Išplėsta programa Specialieji tyrimai Cholesterolis Triacilgliceroliai MTL cholesterolis DTL cholesterolis Lipoproteinų fenotipavimas (lipoproteinų elektroforezė) Lp(a) Apo AI Apo B Apo E Receptorių tyrimas Lipolizės fermentų nustatymas MTL oksidacijos ir antioksidacinės būklės tyrimas Detaliai lipidų ir lipoproteinų apykaitos, magnio bei kai kurie kiti šiame skyriuje minimi tyrimai, jų vertinimo kriterijai aptarti atitinkamuose skyriuose. Homocisteinas yra nepriklausomas širdies ir kraujagyslių ligų rizikos veiksnys. Homocisteinas yra sieros turinti aminorūgštis, kuri pirmą kartą buvo nustatyta protiškai atsilikusių vaikų šlapime (homocistinurija). Tokių ligonių kraujyje randama didelė homocisteino koncentracija. Dažniausia genetinė sunkios hiperhomocisteinemijos priežastis cistationino β sintazės stoka. Šiems ligoniams vystosi ankstyvoji aterosklerozė, arterijų ir venų trombozė (35 pav.). Homocisteinas Homocisteino tiolaktonas Homocistinas MTL MTL ir homocisteino tiolaktono junginiai Putotosios ląstelės Endotelio disfunkcija Reakcinio deguonies rūšys Lipidų peroksidacija Lygiųjų raumenų ląstelių proliferacija MTL oksidacija Aterosklerozė 35 pav. Homocisteino apykaita ir poveikis aterosklerozei 308
310 Širdies ir kraujagyslių ligų laboratorinė diagnostika Hiperhomocisteinemijos sukelti kraujagyslių pažeidimo mechanizmai yra šie: pažeidžiamos endotelio lastelės, suaktyvėja mažo tankio lipoproteinų oksidacija, padidėja tromboksano sukelta trombocitų agregacija, slopinama trombomodulino ir aktyvinama C baltymo ekspresija, stiprėja lipoproteino(a) ir fibrino jungimasis, aktyvinama lygiųjų raumenų proliferacija, kaupiamas kolagenas. Daugiausiai homocisteino katabolizuojama inkstuose ir tik nedidelė dalis šalinama su šlapimu kaip homocistinas (homocisteinas labai nestabilus ir savaime oksiduojasi į homocistiną). Hiperhomocisteinemiją skatina folio rūgšties stoka. Rekomenduojama homocisteino koncentracija yra 5,0 10,0 µmol/l. Nedidelė hiperhomocisteinemija nustatoma, kai homocisteino koncentracija yra µmol/l, vidutinė µmol/l, ir ryški, kai koncentracija viršija 100 µmol/l. Homocisteino koncentraciją reikėtų vertinti atsižvelgiant į ligonio amžių: asmenų iki 30 metų normali homocisteino koncentracija yra 4,5 8 µmol/l, vyresnių nei 60 metų apie 11,0 12,0 µmol/l. Mikroalbuminurija. Mikroalbuminas priskiriamas širdies ir kraujagyslių ligų rizikos veiksniams. Kliniškai sveikų, taip pat jaunų ir vyresnio amžiaus asmenų, kuriems nustatyta hipertenzija ir kurie gydomi dėl padidėjusio kraujospūdžio, klinikiniai tyrimai atskleidė ryšį tarp mikroalbuminurijos ir tokių širdies bei kraujagyslių ligų rizikos veiksnių kaip antsvoris, hipertenzija, rūkymas, piktnaudžiavimas alkoholiu, padidėjęs sistolinis kraujospūdis ir atsparumas insulinui. Kol kas iki galo neaišku, ar mikroalbuminurija yra ankstyvasis glomerulinės nefropatijos požymis, padidėjusio inkstų perfuzinio spaudimo padarinys, ar sutrikusios endotelio funkcijos rodiklis. Anksti aptikta mikroalbuminurija gali padėti nustatyti nefropatiją. Mažinant kraujospūdį ir geriau kontroliuojant gliukozės koncentraciją kraujyje, galima sustabdyti nefropatijos vystymąsi. Prisimintina, kad mikroalbuminas nerodo albumino rūšių, bet tik labai mažą šalinamo albumino kiekį. γ glutamiltransferazė. Nustatyta γ glutamiltransferazės asociacija su sergamumu ir mirtingumu nuo širdies ir kraujagyslių ligų, ypač miokardo infarkto, nepriklausomai nuo kepenų ligų ar alkoholio vartojimo. Šis fermentas atlieka svarbų vaidmenį vystantis oksidaciniam stresui (prooksidatoriaus vaidmuo susidarant aterosklerozinei plokštelei). Stiprus serumo γ glutamiltransferazės ir C reaktyviojo baltymo ryšys rodo esminį oksidacinio streso vaidmenį lėtinio uždegimo vystymosi procese. Esant padidėjusiai šio fermento koncentracijai, būtina vengti alkoholio, hepatotoksinių vaistų, taip pat kavos, rekomenduojama mažinti kūno svorį, nerūkyti. 309
311 Detaliaus apie širdies ir kraujagyslių ligų rizikos veiksnius fibrinogeną, magnį bei šlapimo rūgštį rašoma kituose knygos skyriuose. Miokardo pažeidimą rodantys tyrimai aptariami nagrinėjant miokardo infarkto laboratorinę diagnostiką. Širdies ne p a k a n k a m u m o nu s t a t y m a s iš B t i p o natriurezinio pe p t i d o ty r i m ų Širdis, be savo pagrindinės mechaninės funkcijos, veikia ir kaip endokrininė liauka: joje sintetinama ir išskiriama nemažai baltymų, kurie reguliuoja druskų ir skysčių homeostazę. Tai širdies hormonai, arba natriureziniai peptidai: atrialinis, arba prieširdžių (ANP), ir smegenų (BNP) (35 lentelė). Kraujagyslių endotelio ląstelės išsiskiria C tipo natriurezinį peptidą (CNP). 35 lentelė. A ir B tipų natriurezinių peptidų savybės Savybė ANP BNP Sintezės vieta Prieširdžių miokardas Skilvelių miokardas Baltymo molekulės ilgis 28 aminorūgštys 32 aminorūgštys Gyvavimo plazmoje puslaikis 3 minutės 21 minutė Atsipalaidavimą skatina Prieširdžių sienelių tempimas (prieširdžių išsiplėtimas) Skilvelių sienelių tempimas (skilvelių išsiplėtimas) Šis atradimas buvo padarytas prieš 40 metų, kai elektroninės mikroskopijos būdu prieširdžių miocituose buvo rasta sekrecinių granulių, kurios struktūriškai buvo labai panašios į peptidinius hormonus gaminančių ląstelių granules. Šiuo metu žinoma, kad BNP sintetinamas daugiausia širdyje, todėl pavadinimas smegenų natriurezinis peptidas dažniausiai yra keičiamas sąvoka B tipo natriurezinis peptidas. Veikiant šiems hormonams: skatinamas natrio išsiskyrimas su šlapimu (natriurezė) dėl to sumažėja širdies apkrova; skatinamas šlapimo išsiskyrimas (diurezė) dėl to atpalaiduojami kraujagyslių lygieji raumenys (vazodilatacija ir hipotenzinis poveikis); slopinama renino angiotenzino aldosterono sistema; slopinama trombocitų aktyvacija, reguliuojamas krešėjimas ir fibrinolizė; slopinama simpatinė nervų sistema. A ir B tipo natriurezinius peptidus koduoja skirtingi genai ir jie sintetinami širdies miocituose prohormonų pavidalu: proanp ir probnp. B tipo natriurezinio peptido prohormoną (probnp) sudaro 108 aminorūgštys, proanp 126. Pastarųjų pirmtakai yra sudaryti: preprobnp iš 134 aminorūgščių, preproanp 310
312 Širdies ir kraujagyslių ligų laboratorinė diagnostika iš 151. Sekrecijos metu prohormonai skyla į biologiškai aktyvius peptidus: ANP (jį sudaro 28 aminorūgštys) ir BNP (jį sudaro 32 aminorūgštys), ir jų N galo atitikmenis: NT-proANP bei NT-proBNP (pastarąjį sudaro iki 76 aminorūgščių) (36 lentelė). 36 lentelė. BNP ir NT-proBNP savybės Savybė BNP NT-proBNP Molekulinė masė 3,5 kilodaltono 8,5 kilodaltono Hormoninis aktyvumas Taip Ne Gyvavimo puslaikis 20 minučių 120 minučių Didėja senstant Patvirtintos ribinės reikšmės diagnozuoti širdies nepakankamumą 100 pg/ml <75 metų: 125 ng/l >75 metų: 450 ng/l Prohormonų sintezė spartėja esant mechaninei širdies apkrovai, tūrio perkrovai ir neurohumoralinei širdies stimuliacijai. Dėl to daugiau į kraują bus išskiriama ANP ir BNP bei jų N galo peptidų. Nors BNP ir NT-proBNP sekretuojami ekvimoliniais kiekiais, kraujo plazmoje jų santykis nėra 1:1, nes BNP gyvavimo pusperiodis yra trumpesnis negu NT-proBNP. Išsiskyrę į kraujo tėkmę BNP ir ANP jungiasi prie inkstų ląstelių specifinių natriurezinių peptidų receptorių ir pradeda fiziologiškai veikti membranų pralaidumą aktyvindami guanilatciklazę. Kraujyje natriurezinius peptidus suardo endopeptidazės. Klinikinėje praktikoje B natriurezinis peptidas gali būti nustatomas ligonių, sergančių širdies nepakankamumu, atrankai. Šis rodiklis pasižymi ypač geru prognoziniu specifiškumu (t. y. kuo rezultatas didesnis, tuo prognozė blogesnė). BNP padidėja: ligoniams, sergantiems simptominiu ir asimptominiu širdies nepakankamumu, esant kairiojo skilvelio hipertrofijai; sergant hipertonine liga (ne visada); padidėjus slėgiui prieširdžiuose; ištikus miokardo infarktui kuo didesnė koncentracija ir kuo ilgiau rodiklis išlieka padidėjęs, tuo blogesnė prognozė ir didesnis mirtingumas; esant inkstų nepakankamumui (ne visada); esant kitoms patologinėms būklėms: vožtuvų stenozei, tachikardijai, padidėjusiam centriniam veniniam slėgiui. Šio rodiklio dydis koreliuoja su kairiojo skilvelio hipertrofija bei širdies sienelės storiu. BNP mažėja sėkmingai gydant ligą tai geras terapinis atsakas. 311
313 Ty r i m a i, kuriais nu s t a t o m a s uždegimo aktyvumas Veiksniai, kurie pažeidžia audinius, sukelia uždegiminį atsaką. Iš pradžių vyksta vietinė uždegiminė reakcija, paskui atsiranda sisteminių apykaitinių pokyčių, apibūdinamų kaip ūminės uždegimo fazės atsakas. Atsako į pažeidimą, pavyzdžiui, infekciją, audinių nekrozę, traumą, teorija šiuo metu yra vienas svarbiausių aterosklerozės patogenezę aiškinančių mechanizmų. Ja remiantis sėkmingai taikomas koronarinės širdies ligos gydymas uždegiminį atsaką modifikuojančiais vaistais. Todėl svarbu anksti nustatyti uždegimo ir jo aktyvumo žymenis. Detaliau uždegimo laboratoriniai žymenys ir jų vertinimo kriterijai aptariami skyriuje Žmogaus kraujo plazmos baltymai, jų tyrimas ir rezultatų klinikinis interpretavimas. Šiame skyriuje pabrėžiama tik jų svarba širdies ir kraujagyslių ligų diagnostikai. Uždegimą rodo šie laboratoriniai tyrimai: leukocitų skaičius ir jų diferencinis skaičiavimas; eritrocitų nusėdimo greitis; kraujo serumo baltymų elektroforezinis tyrimas įvertinant α 1 ir α 2 globulinų pokyčius; C reaktyviojo baltymo ar serumo amiloido koncentracija; fibrinogeno koncentracija; interleukino-6 bei navikų nekrozės faktoriaus koncentracija. Leukocitų skaičius ir jų diferencinis skaičiavimas. Audinių nekrozei įvykus miokardo infarktui ir steriliam uždegimui būdinga tik nedidelė granulocitozė. Ūminei bakterinei infekcijai būdinga leukocitozė, o daugiau nei 80% ląstelių yra granulocitai. Būdingas nuokrypis į kairę ir kartais tai gali būti vienintelis požymis. Dėl virusinės infekcijos leukocitų skaičius gali būti normalus, nedaug padidėjęs ar sumažėjęs, dažniau limfocitozė. Lėtiniam uždegimui būdingas normalus ar kiek padidėjęs leukocitų skaičius, neretai monocitozė. Rekomenduojamas suaugusiųjų leukocitų skaičius yra 4,0 9, /l. Eritrocitų nusėdimo greitis (ENG). Kilus uždegimo reakcijai, kraujyje daugėja α globulinų, ūminės uždegimo fazės baltymų, fibrinogeno. Šie veiksniai skatina eritrocitų agregaciją ir jie greičiau nusėda. Eritrocitų nusėdimo greičio tyrimas svarbus ligų prognozei: nustatyta, kad jauni, metų amžiaus, žmonės, kuriems nuolat padidėjęs eritrocitų nusėdimo greitis, turi apie 5 kartus didesnę riziką susirgti kuria nors liga. Didžiausia yra miokardo infarkto rizika. Eritrocitų nusėdimo greitis, kaip atsakas į uždegimą, pradeda didėti po pažeidimo praėjus 24 valandoms. Normaliai vaikų iki 17 metų ENG matuojamas Vestergreno (Westergren) metodu, yra <10 mmhg, metų vyrų <10, moterų <12 mm/val., metų 312
314 Širdies ir kraujagyslių ligų laboratorinė diagnostika vyrų <12, moterų <19 mm/val., vyresnių kaip 60 metų vyrų <14, moterų <20 mmhg. ENG tuo didesnis, kuo būklė sunkesnė. Tyrimas vertingas nustatant ligos aktyvumą ir vertinant gydymo veiksmingumą. Detaliau apie baltymų elektroforezinį tyrimą ir α 1 bei α 2 globulinų pokyčius, C reaktyvųjį baltymą, serumo amiloidą A, fibrinogeną, interleukiną-6 ir navikų nekrozės α faktorių kaip uždegimo aktyvumo sergant širdies ir kraujagyslių ligomis žymenis rašoma skyriuje Žmogaus kraujo plazmos baltymai, jų tyrimas ir rezultatų klinikinė interpretacija. Kraujo krešėjimo sutrikimų tyrimai Šiems tyrimams priskiriami: trombocitų skaičiaus ir jų funkcijos tyrimas, kraujo krešėjimo kaskados ir fibrinolizės sistemos rodikliai: protrombino aktyvumas (Kviko protrombino laikas), kuriuo įvertinamas II, V, VII, X faktorių aktyvumas (PA); protrombino komplekso aktyvumas, kuriuo įvertinamas protrombino II, VII, X faktorių komplekso aktyvumas protrombino prokonvertino metodu, pavyzdžiui, SPA; aktyvintasis dalinis tromboplastino laikas; individualių krešėjimo faktorių nustatymas: fibrinogenas, fibrino ir fibrinogeno degradacijos (irimo) produktai ir D dimerai, C baltymas ir jo kofaktorius S baltymas. Trombocitai yra labai svarbi kraujo krešėjimo sistemos dalis. Fiziologinėmis sąlygomis trombocitai prie pažeistos kraujagyslės sienelės nelimpa. Pažeistoje kraujagyslėje trombocitai prilimpa prie subendotelio (adhezija), formuoja agregatus (agregacija) ir aktyvina kraujo krešėjimo kaskadą. Trombocitų prilipimas prie subendotelio struktūrų juos aktyvina. Be to, trombocitų aktyvaciją inicijuoja adrenalinas, trombinas, kolagenas, tromboksanas, trombocitų aktyvinimo faktorius. Trombocitų aktyvacija yra susijusi su jų formos pasikeitimu: jie išleidžia pseudopodijas, išryškėja organelės, aktyvinasi sekrecinė reakcija. Aktyvinti trombocitai išskiria plazminogeno aktyvatoriaus inhibitorių-1 (PAI-1) ir taip slopina fibrinolizę krešulio zonoje. Iš aktyvintų trombocitų granulių į aplinką sekretuojamas ADF, ATF, serotoninas, fibrinogenas, fon Vilebrando faktorius, didelės molekulinės masės kininogenas, V faktorius, augimo faktoriai. Vienas jų iš trombocitų išsiskyręs augimo faktorius (angl. platelet derived growth factor, PDGF) skatina lygiųjų raumenų proliferaciją, ląstelių migraciją, o sykiu uždegimą, aterosklerozės progresavimą ir komplikacijų vystymąsi. Po sekrecijos trombocitai ištuštėja, tampa degranuliuoti. Trombocitų sekrecija ir pirmiausia ADF sekrecija skatina jų agregaciją. Svarbiausias agregacijos momen- 313
315 tas yra fibrinogeno prisijungimas prie trombocitų paviršiaus glikoproteino GPIIb/ IIIa komplekso. Fibrinogeno molekulė lyg tiltas sujungia du trombocitus. Tokiais tilteliais gali būti fon Vilebrando faktorius, fibronektinas. Terapiškai trombocitų funkciją labiausiai pažeidžia aspirinas: jis slopina trombocitų agregaciją. Taigi ne tik trombocitų skaičiaus, bet ir jų funkcinio aktyvumo tyrimas nustatant jų granuliacijos laipsnį ir pirmiau tekste minėtąsias individualias medžiagas, gali duoti daug informacijos apie hemostazės sistemos būklę. Rekomenduojamas suaugusiųjų trombocitų skaičius yra /l. Trombocitų daugėja fizinio aktyvumo metu, esant streso reakcijai ar dėl katecholaminų poveikio. Gydymas heparinu lemia imuninių procesų sukeltą trombocitopeniją, dėl to galimos tromboembolinės komplikacijos, pavyzdžiui, stambiųjų kraujagyslių, smegenų veninių a¹čių trombozė. Vertinant trombocitų funkciją: atliekami agregacijos ir agliutinacijos tyrimai (trombocitų aglomeratus galima nustatyti įvairiais metodais); skaičiuojami trombocitai prieš ir po stimuliacijos; tyrimą galima atlikti kraujo tėkmės citometriniu metodu, kuris yra labai jautrus ir juo galima nustatyti net ir silpną trombocitų agregaciją; tiriami adhezijos receptoriai; nustatoma ir įvertinama trombocitų granulių sudėtis. Kiti kraujo krešėjimo sutrikimų tyrimai, naudojami širdies ligų diagnostikai, jų vertinimo kriterijai detaliai aprašyti knygos skyriuje Kraujo plazmos krešėjimo ir fibrinolizės, jų sutrikimų laboratorinė diagnostika. Širdies ir kr a u j a g y s l i ų li g ų diferencinės diagnostikos tyrimai Katecholaminai tai adrenalinas ir noradrenalinas. Katecholaminai yra sintetinami smegenyse, antinksčių šerdyje, chromafininiame audinyje ir simpatinių nervų galūnėlėse. Katecholaminai skatina α (α 1, α 2 ) ir β (β 1, β 2, β 3 ) adrenerginius receptorius. Noradrenalinas didina periferinį pasipriešinimą dėl vazokonstrikcijos, dėl to kyla ir sistolinis, ir diastolinis kraujospūdis. Padidėjus kraujospūdžiui, didėja širdies susitraukimų dažnis. Adrenalinas skatina širdies susitraukimus ir didina išvaromo kraujo tūrį (angl. cardiac output), dėl to didėja sistolinis kraujospūdis, bet nepakinta (ar net mažėja) diastolinis kraujospūdis. Be to, adrenalinas, ne taip kaip noradrenalinas, yra labai svarbus medžiagų apykaitai: slopina insulino ir skatina gliukagono sekreciją. Dėl jo poveikio mažėja gliukozės poreikis periferiniuose audiniuose, skatinama glikogenolizė ir gliukoneogenzė. Tai sukelia hiperglikemiją. Negana to, adrenalinas aktyvina audinių lipazę ir kraujyje didėja riebalų rūgščių 314
316 Širdies ir kraujagyslių ligų laboratorinė diagnostika koncentracija. Taigi katecholaminų nustatymas yra svarbus širdies ir kraujagyslių ligų diagnostikai. Rekomenduojama reikšmė kraujo plazmoje: adrenalino iki 100 ng/l, noradrenalino iki 600 ng/l. Šlapime adrenalino kiekis turi būti iki 20 µg/24 val., noradrenalino iki 104 µg/24 val. Fizinis aktyvumas, stresas, rūkymas, skausmas fiziologiškai didina katecholaminų kiekį. Jų kraujyje daugėja ligoniui stovint, dėl įvairių stresinių situacijų, taip pat dėl streso atliekant venos punkciją. Idealiu atveju kraujas imamas rytą po 30 min. poilsio ligoniui gulint. Nustatyti plazmos noradrenaliną svarbu ortostatinės hipotenzijos diagnostikai šiais atvejais noradrenalino koncentracija nepadidėja. Jei noradrenalino koncentracija nepadidėja pereinat iš gulimos padėties į stovimą, galima įtarti simpatinės nervų sistemos sutrikimą. Jei įmanoma, prieš tiriant katecholaminų kiekį šlapime, ligonis savaitę laiko turi nevartoti vaistų. Katecholaminų ekskrecija naktį yra daug mažesnė. Adrenalino ir noradrenalino ekskrecija didėja esant mėnesinių ciklo geltonkūnio fazei, o ovuliacijos metu sumažėja iki minimumo. Panašiai kinta ir vanilmigdolų rūgšties kiekis. Reninas tai fermentas, priklausantis renino angiotenzino aldosterono sistemai ir yra gaminamas inkstuose bei antinksčiuose. Ši sistema reikalinga natrio ir neląstelinių skysčių tūrio, kalio homeostazei bei arterinio kraujospūdžio reguliavimui. Reninas didina aldosterono sekreciją per angiotenziną II. Padidėjęs natrio vartojimas lygiagrečiai yra susijęs su renino ir aldosterono sekrecijos sumažėjimu, o sumažėjęs natrio vartojimas padidina minėtų medžiagų sekreciją. Renino aktyvumą ypač rekomenduojama tirti diagnozuojant piktybinę hipertenziją ir endokrininių ligų (hiperaldosteronizmo, reniną gaminančių navikų, izoliuotos mineralkortikoidų stokos) diferencinei diagnostikai. Rekomenduojama renino reikšmė kraujo plazmoje, esant ramybės būklei, 0,5 1,9 ng/ml, po krūvio 1,9 6,0 ng/ml. Renino kiekio reikšmės priklauso nuo metodo, Na + ar K + kiekių, vandens apykaitos būklės, kūno padėties. Pavyzdžiui, mažai druskos turinti dieta, vertikali kūno padėtis ir diuretikai didina renino kiekį. Su amžiumi ir vyrų, ir moterų renino aktyvumas mažėja, bet moterų yra šiek tiek mažesnis. Moterų renino koncentracija yra maža per folikulinę fazę, prieš pat ovuliaciją kyla ir kiekis išlieka didelis esant liuteininei fazei. Nėščių moterų renino kiekis yra padidėjęs. Tyrimas naudingas vertinant gydymą mineralkortikoidais. Šiame skyriuje minimi tyrimai (pvz., kalio nustatymas) detaliau aprašyti kituose atitinkamuose knygos skyriuose. 315
317 Api b e n d r i n i m a s Hiperlipoproteinemijų fenotipavimui plačiai naudojama Fredriksono klasifikacija. Dažniausios antrinės hiperlipidemijos priežastys yra hipotirozė, cukrinis diabetas kepenų ligos ir alkoholis. Homocisteinas yra nepriklausomas širdies ir kraujagyslių ligų rizikos veiksnys. Kai yra širdies aritmija ir elektrokardiogramos pokyčių, rekomenduojama ištirti magnio kiekį kraujyje. Esama ryšio tarp mikroalbuminurijos ir širdies bei kraujagyslių ligų rizikos veiksnių antsvorio, hipertenzijos, rūkymo, piktnaudžiavimo alkoholiu, padidėjusio sistolinio kraujospūdžio ir audinių atsparumo insulinui. Atsako į pažeidimą, pavyzdžiui, infekciją, audinių nekrozę, traumą, teorija šiuo metu yra vienas iš svarbiausių aterosklerozės patogenezę aiškinančių mechanizmų. Todėl labai svarbu anksti nustatyti uždegimą ir jo aktyvumo žymenis. Fiziologinėmis sąlygomis trombocitai prie pažeistos kraujagyslės sienelės nelimpa. Ją pažeidus, trombocitai prilimpa prie subendotelio, formuoja agregatus ir aktyvina kraujo krešėjimo kaskadą. Biocheminiai tyrimai yra svarbūs nustatant inkstų, endokrininių liaukų ligas, kurios gali būti hipertenzijos priežastis, taip pat vertinant antihipertenzinio gydymo veiksmingumą. Homocisteinas Tiriamoji medžiaga. Serumas. Rekomenduojama reikšmė. 5,0 12,0 µmol/l; vyresniems kaip 60 m. asmenims 5,0 20,0 µmol/l. Diagnostinė vertė. Nepriklausomas širdies kraujagyslių ligų rizikos veiksnys. Papildoma informacija. Hiperhomocisteinemijos sukelti kraujagyslių pažeidimo mechanizmai yra šie: pažeidžiamos endotelio lastelės, suaktyvėja mažo tankio lipoproteinų oksidacija, padidėja tromboksano sukelta trombocitų agregacija, slopinama trombomodulino ir aktyvinama C baltymo ekspresija, stiprėja lipoproteino(a) ir fibrino jungimasis, aktyvinama lygiųjų raumenų proliferacija, kaupiamas kolagenas. Daugiausia homocisteino katabolizuojama inkstuose ir tik nedidelė dalis šalinama su šlapimu homocistino formos (homocisteinas labai nestabilus ir savaime oksiduojasi į homocistiną). Hiperhomocisteinemijos vystymąsi skatina folio rūgšties stoka. Reninas Laboratoriniai tyrimai Tiriamoji medžiaga. Plazma (EDTA). Rekomenduojama reikšmė. Esant ramybė būklei 0,5 1,9 mg/l, po krūvio 1,9 6,0 mg/l. Diagnostinė vertė. Kartu esant antriniam aldosteronizmui: Hipertenzinės būklės: piktybinė ar labai sunki hipertenzija, vienos pusės inksto liga su piktybine ar sunkia hipertenzija, inkstų parenchimos ligos, reniną sekretuojantys navikai, oralinių kontraceptikų sukelta hipertenzija, feochromacitoma. Normotenzinės būklės (su edema): kepenų cirozė, hepatitas, nefrozė, įgimta širdies liga. Hipokaleminės normotenzinės būklės: jukstaglomerulinių ląstelių hiperplazija (Barterio sindro- 316
318 Širdies ir kraujagyslių ligų laboratorinė diagnostika mas), kitos neoplazijos, kurių metu netenkama Na + ar K +. Alimentiniai sutrikimai netenkant elektrolitų. Be antrinio aldosteronizmo: Antinksčių žievės nepakankamumas, kalio išeikvojimas (alimentinis). Su antinksčių žievės liga: Hipertenzinės būklės: pirminis aldosteronizmas dėl antinksčių adenomos, pseudopirminis ar idiopatinis aldosteronizmas (dažniausiai abipusė antinksčių žievės hiperplazija), gliukokortikoidais užslopinamas aldosteronizmas, antinksčių vėžys, gaminantis mineralkortikoidų perteklių, antinksčių fermentų stoka, dėl kurios išryškėja padėjusi kitų mineralkortikoidų sekrecija. Be antinksčių žievės ligos: Hipertenzinės būklės: pirminė hipertenzija su mažu renino kiekiu; kai kuriems ligoniams, sergantiems inkstų parenchiminėmis ligomis; pseudohiperaldosteronizmas t. y. Lidlio (Liddle) sindromas, mineralkortikoidų vartojimas. Normotenzinės būklės: inkstų parenchiminės ligos, autonominės nervų sistemos sutrikimai su ortostatinė hipotenzija, vaistų sukelta adrenerginė blokada, hiperkalemija. Papildoma informacija. Renino kiekio reikšmės priklauso nuo metodo, Na + ar K + kiekių, vandens apykaitos būklės, kūno padėties. Pvz., mažai druskos turinti dieta, vertikali kūno padėtis ir diuretikai didina renino kiekį. Su amžiumi ir vyrų, ir moterų renino aktyvumas mažėja, bet moterų yra kiek mažesnis. Moterų renino koncentracija yra maža per folikulinę fazę, prieš pat ovuliaciją kyla ir kiekis išlieka didelis esant liuteininei fazei. Nėštumo metu renino kiekis yra padidėjęs. Tyrimas naudingas vertinant gydymą mineralkortikoidais. V: chlorpropamidas, enalaprilis, estrogenai, hidralazinas, kaptoprilis, lizinoprilis, nifedipinas, (jauniems), nitroprusidas, geriamieji kontraceptikai, kalį išsaugantys diuretikai (spironolaktonas, triamterenas), tiazidiniai diuretikai. V: β adrenoblokatoriai, angiotenzinas (į veną), aspirinas, deoksikortikosteronas, indometacinas, kalio preparatai, metildopa, rezerpinas, saldymedžio ekstraktas. 317
319 HORMONŲ KLINIKINĖ BIOCHEMIJA IR JŲ NUSTATYMO REIKŠMĖ Bendrosios žinios apie hormonus Hormonus gaminančios liaukos yra vadinamos endokrininėmis liaukomis. Žodis hormonas kilęs iš graikų kalbos ir reiškia sukelti, išjudinti, užvesti. Hormonai tai biocheminiai reguliatoriai, cheminės medžiagos, kurios perduoda savo informaciją kaip signalą į tam tikrą ląstelę taikinį; šios ląstelės paviršiuje ar viduje yra specifiniai receptoriai, prie kurių hormonai prisijungia ir taip perduoda informaciją. Jungiantis hormonams prie receptorių, prasideda procesai, kuriuos lemia hormonų cheminė prigimtis, taip pat ląstelės, kuriai perduodama informacija, tipas. Dėl hormonų poveikio gali keistis jonų ir kitų medžiagų pernaša per membraną ir dėl to modifikuotis genomo transkripcija, baltymai, suaktyvėti fermentai. Visų hormonų fiziologinio gyvavimo kraujyje puslaikis yra trumpas, dažniausiai mažesnis nei 1 valanda. Taigi hormonai, kad atliktų savo funkciją palaikydami normalią fiziologinę organizmo būklę, taip pat dėl to, kad jie dažnai veikia per sintezės ir sekrecijos grįžtamojo ryšio reguliacijos mechanizmą, turi būti nuolat sintetinami, sekretuojami, veikti greitai ir greitai būti inaktyvinami. Tačiau hormonų sekrecijos greitis kinta. Pavyzdžiui, antinksčių šerdies hormonai sekretuojami tam tikru paros ritmu, o gonadotropinai sudėtingu cikliniu ritmu. Kiti hormonai gaminami kaip atsakas į dirgiklį, pavyzdžiui, insulinas į gliukozės kiekį kraujyje, aldosteronas į natrio jonų koncentraciją. Taigi skiriami dviejų rūšių hormonai: 1) adaptaciniai, kurie reaguoja į aplinkos veiksnius, ir 2) homeostaziniai, kurie reaguoja į vidinės terpės pokyčius. Be pripažintos hormonų reikšmės, ląstelėse vykstančias reakcijas veikia ir kitos prigimties medžiagos, esančios biologiniuose skysčiuose ir audiniuose. Tai polipeptidai, kurie slopina ląstelių proliferaciją ir yra specifiniai organui taikiniui, pavyzdžiui, odoje esantys polipeptidai slopina odos ląstelių proliferaciją, bet jie nėra rūšiai specifiški. Šios rūšies inhibitoriai vadinami chalonais (iš graikų k. žodžio slopinti ). Tačiau chalonai, kaip ir kininai bei prostaglandinai, nors veikia ląstelėse vykstančius procesus, gali būti gaminami ir neendokrininių liaukų. Kai kurie hormonai, pavyzdžiui, sekretuojami skrandžio ir žarnyno gleivinėje, taip pat nesintetinami pripažintuose hormonus gaminančiuose organuose endokrininėse liaukose. Endokrininėmis ligomis susergama dėl hormonų hipersekrecijos ar hiposekrecijos. 318
320 Hormonų klinikinė biochemija ir jų nustatymo reikšmė En d o k r i n i n ė s li a u k o s, jų ga m i n a m ų ho r m o n ų st r u k t ū r a, f u n k c i j o s, s e k re c i j o s r e g u l i a v i m a s, veikimo me c h a n i z m a s ir nustatymas Hormonų struktūra. Žinduolių hormonai pagal cheminę prigimtį gali būti sugrupuoti į tris pagrindinius tipus: I grupė tai baltymai ir polipeptidai. Dauguma hormonų priklauso šiai grupei. Jie gali būti nedidelės moekulės, pavyzdžiui, tirotropiną atpalaiduojantį hormoną sudaro vos 3 aminorūgštys, arba didelės molekulės, pavyzdžiui, hipofizės gonadotropinai yra didelės glikoproteinų molekulės; II grupė tai aminorūgščių dariniai, pavyzdžiui, adrenalinas, skydliaukės hormonai; III grupė steroidai. Jų visų sintezės pirmtakas yra cholesterolis. Pagrindinės endokrininės liaukos, jų gaminamų hormonų prigimtis ir savybės yra pateikiamos 37 lentelėje, o pagrindinės liaukos, gaminančios steroidinius hormonus, 38 lentelėje. 37 lentelė. Pagrindinių endokrininių liaukų gaminamų hormonų prigimtis ir savybės Endokrininė liauka Antinksčių šerdis Hipofizės priekinė dalis adenohipofizė Pagrindinė veikimo Hormonas vieta Adrenalinas (epinefrinas) Širdies raumuo, lygieji raumenys, arteriolės Noradrenalinas (norepinefrinas) Prolaktinas (PRL); yra ir placentoje Adrenokortikotropinas (AKTH) arba kortikotropinas; yra ir placentoje Kepenys ir raumenys Riebalinis audinys Arteriolės Riebalinis audinys Pieno liauka Geltonkūnis Antinksčių žievė Veikiamas procesas ar reiškinys Pulso greitis ir kraujospūdis; lygiųjų raumenų susitraukimas Glikogenolizė Lipidų atpalaidavimas (lipolizė) Susitraukimas, padidėjęs periferinis pasipriešinimas Lipolizė Proliferacija ir pieno sekrecijos skatinimas Geltonkūnio proliferacija ir progesterono sekrecijos stimuliavimas Antinksčių žievės steroidinių hormonų (kortizolio) sintezė ir (ar) sekrecija Tirotropinas, arba skydliaukę stimuliuojantis hormonas (TSH) Riebalinis audinys Skydliaukė Riebalinis audinys Lipolizė Skydliaukės hormonų gamyba ir sekrecija Lipolizė 319
321 37 lentelės tęsinys Endokrininė liauka Hormonas Somatotropinas (STH), arba augimo hormonas (AH); yra ir placentoje Liutropinas, arba liuteinizuojantis (intersticines ląsteles stimuliuojantis) hormonas (LH, ILSH) Folitropinas, arba folikulus stimuliuojantis hormonas (FSH) β lipotropinas Pagrindinė veikimo vieta Bendras veikimas Kiaušidės Sėklidės Kiaušidės Sėklidės Veikiamas procesas ar reiškinys Kaulų ir raumenų augimas; anabolinis poveikis kalcio jonų, fosfatų ir azoto apykaitai, angliavandenių ir riebalų apykaitai, raumenų ir širdies glikogeno kiekio padidėjimas Liuteinizacija, progesterono sekrecija Intersticinio audinio vystymasis, androgenų sekrecija Folikulų vystymasis; estrogenų sekrecija ir ovuliacija (kartu su LH) Kanalėlių vystymasis; spermatogenezė β melanocitus stimuliuojančio hormono (β-msh) bei endorfinų pirmtakas β endorfinas Smegenys Endogeninis opiatas; padidina skausmo slenkstį Hipofizės užpakalinė dalis neurohipofizė Oksitocinas Vazopresinas, arba antidiurezinis hormonas (ADH) Lygieji raumenys, ypač gimdos Pieno liauka, laikotarpis po gimdymo Arteriolės Kontrakcija, gimdymas Pieno išskyrimas Didina kraujospūdį Inkstų kanalėliai H 2 O reabsorbcija Koherinas Žarnų raumenys Peristaltikos ritmiškumo reguliavimas Hipofizės tarpinė dalis α melanocitus stimuliuojantis hormonas (α-msh) Odos melanoforų ląstelės Pigmento pasiskirstymas, odos patamsėjimas Inkstai Reninas Reguliuoja kraujospūdį Eritropoetinas Kaulų čiulpai Skatina eritropoezę Kankorėžinė liauka Melatotinas Pogumburis Slopina gonadotropinio ir augimo hormonų sekreciją; sukelia mieguistumą Serotoninas, arba 5- hidroksitriptaminas Širdies ir kraujagyslių, kvėpavimo, virški nimo sistemos, smegenys Neurotransmiteris; skatina ar slopina lygiųjų raumenų, nervų veiklą Kasa β ląstelės insulinas Bendras veikimas Angliavandenių panaudojimas ląstelėje; baltymų sintezės stimuliacija 320
322 Hormonų klinikinė biochemija ir jų nustatymo reikšmė 37 lentelės tęsinys Endokrininė liauka Hormonas Pagrindinė veikimo Veikiamas procesas vieta ar reiškinys Riebalinis audinys Lipogenezė α ląstelės gliukagonas Kepenys Glikogenolizė Riebalinis audinys Lipolizė Somatostatinas Kasa; adenohipofizė Gliukagono ir somatotropino sekrecijos slopinimas Kasos polipeptidai Kepenys Sustiprėjusi glikogenolizė Kiaušidės, geltonkūnis, Relaksinas Gaktinė sąvarža, Raumenų tonusas placenta gimda Kiaušidės, sėklidės Inhibinas Pogumburis FSH sekrecijos reguliavimas Placenta Žmogaus chorioninis gonadotropinas, estrogenas, progesteronas Kaip ir hipofizės gonadotropinas: LH ir FSH Veikia panašiai kaip adenhipofizės hormonai, bet neidentiškai Prieskydinės liaukos Parathormonas Griaučiai, inkstai, virškinamasis traktas Kalcio jonų ir fosfatų apykaita; didina kalcio kiekį kraujyje ir šalina fosfatus su šlapimu Kalcitoninas Griaučiai Kalcio jonų ir fosfatų apykaita, mažina kalcio kiekį kraujyje Skydliaukė Tiroksinas ir T 4 Bendras veikimas Augimas ir brendimas, Trijodtironinas T 3 medžiagų apykaitos greitis, deguonies panaudojimas audiniuose Kalcitoninas Griaučiai Kalcio jonų ir fosfatų apykaita; mažina kalcio kiekį kraujyje Smegenys Užkrūčio liauka (thymus) Virškinamasis traktas Endorfinai: β endorfinas, enkefalinas Timozinas (vienas iš kelių aktyviųjų užkrūčio liaukos hormonų) Limfoidinės ląstelės Tai endogeniniai peptidai, kurie jungiasi prie morfino receptorių Limfocitopoezės skatinimas; imunologiškai atsakingų limfocitų subrendimo skatinimas; ląstelinis imunitetas Gastrinas Skrandis Rūgšties sekrecija Somatostatinas Kasa, adenohipofizė Gliukagono ir somatropino sekrecijos slopinimas Sekretinas Kasa Kasos sulčių sekrecija Cholecistokininas Kasa Virškinimo fermentų sekrecija Tulžies pūslė Susitraukimas ir išsituštinimas Motilinas Virškinamasis traktas Skatina virškinamojo trakto judesius Skrandžio veiklą slopinantis polipeptidas Virškinamasis traktas Slopina skrandžio sekreciją ir judesius; skatina insulino sekreciją Bombezinas Virškinamasis traktas Skatina įvairių hormonų, kasos fermentų išsiskyrimą, lygiųjų raumenų susitraukimą 321
323 38 lentelė. Endokrininės liaukos, gaminančios steroidinius hormonus Endokrininė liauka Antinksčių žievė Hormonas Antinksčių žievės steroidai (adrenokortikosteroidai) Aldosteronas Pagrindinė veikimo vieta Bendras poveikis Veikiamas procesas ar reiškinys Elektrolitų ir vandens apykaita Kortikosteronas Kortizolis Baltymų, angliavandenių ir riebalų apykaita; homeostazės Antinksčių androgenai palaikymas; uždegimas, imunitetas ir atsparumas infekcijai; padidėjęs jautrumas Geltonkūnis Progesteronas Gimda Pasiruošimas kiaušinėlio implantacijai; nėštumo palaikymas Pieno liaukos Alveolinės sistemos vystymasis Kiaušidės Estronas ir estradiolis Antriniai lyties organai Brendimas ir normali ciklinė lytinė funkcija Pieno liaukos Kanalėlių sistemos išsivystymas Bendras poveikis Antrinių lytinių požymių formavimasis Placenta Estrogenai Kaip ir kiaušidžių hormonai Kaip ir kiaušidžių hormonai Progesteronas Kaip ir geltonojo kūno hormonai Kaip ir geltonojo kūno hormonai Sėklidės Testosteronas ir androgenai Antriniai lyties organai Brendimas ir normali lytinė funkcija Bendras poveikis Antrinių lytinių požymių vystymasis Sėklinės pūslelės (prostata) Prostaglandinai (sintezė vyksta ne tik endokrininėse liaukose) Lygieji raumenys: riebalinis audinys, trombocitai, smegenys, virškinimo traktas Kraujospūdis, lygiųjų raumenų susitraukimas, lipidų apykaita, trombocitų agregacija, jaudrumas, sekrecija Polipeptidiniai hormonai dažnai yra sintetinami atitinkamose liaukose didesnių molekulių prohormonų pavidalu. Kai kuriais atvejais baltymai, didesni už prohormonus, yra pirminis ribosomų produktas ir vadinami preprohormonais. Kaip ir daugelis virškinamojo trakto proteolizinių fermentų, biologiškai aktyvių baltymų pirmtako sintezė žinoma nuo seno: neaktyvios prohidrolazių formos zimogenai apsaugo ląsteles nuo žalingo hidrolizinio jų poveikio. Tačiau hormonai šio žalingo poveikio neturi, jie yra veikliųjų hormonų kaupimo forma. Prohormonai yra biologiškai aktyvūs, nors mažiau negu prohormonų proteolizės produktas hormonas, pavyzdžiui, proinsulinas. Dėl endokrininių liaukų 322
324 Hormonų klinikinė biochemija ir jų nustatymo reikšmė nenormalios proliferacijos, pavyzdžiui, esant kasos adenomai, gaminamas prohormono perteklius ir padidėjęs jo kiekis aptinkamas kraujyje. Jautriais metodais (pavyzdžiui, radioimuniniu) bus aptinkamas labai didelis hormono kiekis, ir rezultatas bus klaidingas, nes galima kryžminė reakcija tarp prohormono ir atitinkamo hormono. Hormonų sekrecija ir jos reguliavimas. Hormonų sekreciją veikia nemažai veiksnių: skatinančios ar slopinančios sekreciją medžiagos, pavyzdžiui, pogumburio peptidai; hormonų sintezę apgrąžos principu reguliuoja organų ar ląstelių taikinių medžiagų apykaitos produktai; hormonai sekretuojami tam tikru ritmu: galima pulsinė sekrecija, cirkadinis ritmas; pavyzdžiui, adrenokortikotropinis, tirotropinis hormonai sekretuojami skirtingu ritmu dieną ir naktį; stresas gali padidinti hormonų sintezę ir sekreciją, pavyzdžiui, adrenokortikotropinio hormono; kiti hormonai ar vaistai gali keisti normalų endokrininių liaukų atsaką. Priekinės posmegeninės liaukos dalies (adenohipofizės) hormonai atpalaiduoja nemažai kitų endokrininių liaukų hormonų ir reguliuoja jų sintezės ir sekrecijos greitį. Taip pat kai kurie mažos molekulinės masės polipeptidai, sekretuojami pogumburyje (hipotalame), valdo adenohipofizės hormonų sekreciją (39 lentelė). 39 lentelė. Pogumburio reguliaciniai hormonai Pogumburio hormonai Adrenokortikotropiną atpalaiduojantis hormonas Augimo hormoną atpalaiduojantis hormonas Augimo hormoną inhibuojantis hormonas, arba somatostatinas Gonadotropinus atpalaiduojantis hormonas (arba liutropiną išskiriantis hormonas) Melanocitus reguliuojantys hormonai: stimuliuojantis hormonas, inhibuojantis hormonas, arba melanostatinas Prolaktiną atpalaiduojantys hormonai: stimuliuojantis hormonas; inhibuojantis hormonas Tirotropiną atpalaiduojantis hormonas Veikiamas hormonas Skatina adrenokortikotropinio hormono ir β lipotropino išsiskyrimą Skatina augimo hormono atsipalaidavimą Slopina augimo, tirotropinio hormonų, insulino, sekretino, gliukagono išsiskyrimą Skatina liuteinizuojančio (liutropino) ir folikulus stimuliuojančio (folitropino) hormonų asipalaidavimą Skatina ar slopina melanocitus stimuliuojančio hormono (melanotropino) atsipalaidavimą Skatina ar slopina prolaktino išsiskyrimą Skatina tirotropinio hormono (tirotropino) išsiskyrimą Dėl nervinių ir cheminių stimuliatorių poveikio iš pogumburio išsiskiriančios medžiagos (žr. 39 lentelę) priskiriamos reguliaciniams polipeptidams tai va- 323
325 dinamieji atpalaidavimo (angl. releasing) faktoriai. Kadangi šie reguliaciniai polipeptidai yra sekretuojami tiesiai į kraują ir nešami į jų poveikio audinį taikinį, t. y. adenohipofizę, juos galima vadinti ir priskirti reguliaciniams hormonams. Pogumburio, taip pat posmegeninės liaukos (hipofizės) hormonų sekrecijos greitis, kuriuos veikia pirmieji, yra kontroliuojami teigiamo ir neigiamo grįžtamojo ryšio mechanizmų. Nervinių poveikių įvairovė organizme ir jo aplinkoje gali didinti ar mažinti pogumburio ir posmegeninės liaukos sistemos sekrecinį aktyvumą. Specifinių adenohipofizės hormonų koncentracija kraujyje grįžtamuoju ryšiu gali teigiamai ar neigiamai veikti pogumburį. Mažesnės negu normalios tam tikrų hormonų koncentracijos kraujyje skatins pogumburio hormonų sekrecinį aktyvumą, o didesnės negu normalios mažins šį aktyvumą. Toks veikimas būdingas ir hormonų sekrecinio aktyvumo reguliavimui per adenohipofizę. Adenohipofizės hormonų sekreciją reguliuoja per kraują tirpūs pogumburio hormonai, t. y. pastaruosius kraujas nuneša į adenohipofizę; neurohipofizės hormonai, sintetinti pogumburyje, migruoja kaip granulės nervinėmis skaidulomis ir kaupiasi nervų galūnėlėse neurohipofizėje, o iš ten išskiriami priklausomai nuo nervinio dirgiklio. Hormonų veikimo mechanizmas. Hormonų specifiškumas tam tikroms ląstelėms taikiniams yra susijęs su specifinių receptorių buvimu ląstelėse. Hormonas yra baltymas ar polipeptidas, ar aminorūgšties darinys, o receptorius yra ląstelės membranos sudedamoji dalis. Veikiant šiems hormonams, ląstelės atsakas susiformuoja, kai jie prisijungia prie ląstelės membranos. Ląstelės membranos receptoriai yra glikoproteinai, o receptorių specifiškumą ir lemia angliavandeninis komponentas. Prisijungimas prie receptoriaus skatina vieno ar kelių jonų (Ca 2+, Na + ar K + ) pernašą per membraną ir aktyvina su membrana susijungusią adenilatciklazę; dėl to padidėja ląstelinė ciklinio adenozinmonofosfato (camf) koncentracija. Hormonų veiklą ir ląstelės medžiagų apykaitą camf veikia kaip antrinis ar tretinis tarpininkas: Pirminis tarpininkas Antrinis tarpininkas Liauka Ląstelė taikinys Poveikis (hormonas) (camf) medžiagų apykaitai camf dalyvauja fosforilinant baltymus. Šį procesą taip pat katalizuoja proteinkinazės. Ribosomų baltymų fosforilinimas veikia sintetinamo baltymo prigimtį ir kiekį. Nustatyta ne tik ląstelių membranų receptorių sistema, bet ir specifinės surišimo zonos branduolyje. Taigi egzistuoja du ląsteliniai baltyminės, polipeptidinės ar aminorūgšties prigimties hormoną veikiantys mechanizmai: vienas jų generuoja antrinį tarpininką membranoje, o šis veikia tam tikras branduolio zonas. 324
326 Hormonų klinikinė biochemija ir jų nustatymo reikšmė Steroidiniai hormonai taip pat funkcionuoja veikdami specifinių baltymų sintezės greitį. Steroidiniai hormonai patenka į jų ląstelių taikinių citoplazmą ir dėl stiprios traukos prisijungia prie specifinių citoplazmos baltymų. Pastarieji nešami į ląstelės branduolį ir ten prisijungia prie chromatino (DNR). Šį procesą gali modifikuoti chromosominiai nehistoniniai baltymai. Pakeisdami DNR šabloną, prieinamą transkripcijai, šie steroidiniai kompleksai veikia specifinės irnr sintezę taigi genomo lygmeniu. Jei steroidinių hormonų koncentracija ląstelėje padidėja, sintetinama nauja ar papildoma irnr, kuri indukuoja baltymo gamybą (arba padidėja jau egzistuojančio baltymo sintezės greitis). Taigi abi pagrindinės hormonų klasės veikia baltymų sintezės greitį ląstelėse taikiniuose. Pagrindinis dviejų hormonų klasių veikimo mechanizmo skirtumas yra tas, kad baltyminės, polipeptidinės ir aminorūgšties kilmės hormonai veikia potranskripcinius procesus ląstelėje, o steroidiniai hormonai genomo transkripciją. Kraujo plazmoje hormonai, pavyzdžiui, steroidiniai ar skydliaukės, prisijungia prie specifinių hormonus sujungiančių baltymų glikoproteinų. Biologiškai aktyvus yra neprisijungęs, arba laisvasis, hormonas. Taigi diagnozei svarbu išmatuoti laisvojo arba prisijungusio prie baltymų hormono koncentraciją. Endokrininės ligos tai ligos dėl hormonų hipersekrecijos ar hiposekrecijos. Hormonų nustatymas. Iki laboratorinių nustatymo metodų atsiradimo hormonai buvo tiriami pagal biologinį atsaką į hormoną. Radioimuniniai metodai padarė tikrą revoliuciją endokrinologijos moksle. Panaudojus monokloninius antikūnus buvo sukurti daug jautresni ir specifiniai hormonų nustatymo metodai. Kadangi biologiniu aktyvumu pasižymi laisvosios hormonų formos, todėl diagnozei svarbu nustatyti ne tik bendrąjį hormonų kiekį, bet ir laisvą ar sujungtą jų formą. Šiame skyriuje detaliau aptarsime dažniausiai klinikinėse laboratorijose nustatomus hormonus. Api b e n d r i n i m a s Endokrinologija yra mokslas apie hormonus biocheminius organizme vykstančių procesų reguliatorius, kurie yra išskiriami į kraują ir veikia atokiose organizmo vietose. Hormonų fiziologinio gyvavimo kraujyje puslaikis yra trumpas, dažniausiai mažesnis kaip 1 valanda. Taigi jie turi būti nuolat sintetinami, sekretuojami, veikti greitai ir greitai būti inaktyvinami. Polipeptidiniai hormonai dažnai yra sintetinami didesnių molekulių prohormonų pavidalu. Baltymai, didesni už prohormonus, yra pirminis ribosomų produktas ir vadinami preprohormonais. Posmegeninės liaukos (hipofizės) hormonai reguliuoja kitų hormonų sekrecijos greitį. Taip pat mažos molekulinės masės polipeptidai, sekretuojami pogumburyje (hipotalame), valdo adenohipofizės hormonų sekreciją. 325
327 Hormonų specifiškumas tam tikroms ląstelėms taikiniams yra susiję su specifinių receptorių buvimu ląstelėse. Ir baltyminiai, ir steroidiniai hormonai veikia baltymų sintezės greitį ląstelėse taikiniuose. Pagrindinis dviejų hormonų klasių veikimo mechanizmo skirtumas yra tas, kad baltyminės, polipeptidinės ir aminorūgšties kilmės hormonai veikia potranskripcinius procesus ląstelėje, o steroidiniai hormonai genomo transkripciją. Biologiškai aktyvus yra su baltymais nesusijungęs, t. y. laisvasis, hormonas. Posmegeninė liauka ir joje sintetinami hormonai Posmegeninė liauka, arba hipofizė (hypophysis), tai sudėtinga sekrecinių ląstelių, kraujagyslių ir nervinio audinio struktūra kaukolės pamato kaulinėje duobėje. Palyginti su svarba visoms organizmo funkcijoms, ši liauka yra labai mažas organas, sveriantis apie 0,5 g. Apie 75% šios liaukos sudaro priekinė dalis, kuri vadinama adenohipofize, o kitą neurohipofizė ir užpakalinė hipofizės dalis. Šios liaukos veiklą reguliuoja pogumburyje (hypothalamus) gaminami hormonai abi šias struktūras jungia gausus kraujagyslių ir nervinio audinio tinklas. Klinikoje yra nustatyti navikai, sekretuojantys kiekvieną iš adenohipofizės hormonų. Tirotropiną (angl. thyroid stimulating hormone, TSH) ir gonadotropinus sekretuojantys navikai yra reti, o augimo hormoną (somatotropiną, STH) ir adrenokortikotropiną (AKTH) dažnesni. Dažniausios yra prolaktiną sekretuojančios adenomos (prolaktinomos). Augimo reguliavimas, sutrikimai ir akromegalija. Vaikų augimui būdingi trys augimo etapai: pirmaisiais ir antraisiais gyvenimo metais vaikas auga greitai; vėliau, iki 9 metų, vaikas auga nuolat šį augimo etapą reguliuoja augimo hormonas; jei jo sintetinama nepakankamai, augimas atsilieka, ir vaikas bus mažaūgis; trečiasis augimo etapas paauglystė, kai augimą reguliuoja lytiniai hormonai, taip pat augimo hormonas. Pastarasis nėra vienintelis hormonas, reguliuojantis augimą; jį veikia ir kiti tiroksinas, kortizolis, lytiniai hormonai bei parakrininiai augimo veiksniai (somatomedinai, į insuliną panašūs augimo faktoriai, kt.). Somatomedinai tai grupė mažos molekulinės masės peptidų, kurie stuktūriškai yra panašūs į proinsuliną ir insuliną ir veikia panašiai kaip augimo hormonas ir insulinas. Somatomedinų veikimas pagrįstas signalo perdavimu ląstelėms per specifinius receptorius. Neretai jų svarba reguliuojant augimą tampa didesnė negu paties augimo hormono. Tai įvyksta sutrikus grįžtamojo slopinimo reguliacijai. Somatomedinų grupei priklauso somatomedinai A, B, C (pastarasis tai yra tas pats į insuliną panašus augimo faktorius-1, angl. insuline-like growth factor, IGF-1), į insuliną panašus augimo faktorius-2, kiti. Šių peptidų sintezę ir sekreciją reguliuoja įvairūs veiksniai (svarbiausias jų mityba), o kraujyje jie yra sujungti su jų pernašos baltymais (angl. insulin growth factor binding protein, IGFBP). Pastarųjų yra keletas formų (svarbiau- 326
328 Hormonų klinikinė biochemija ir jų nustatymo reikšmė sias IGFBP-3). Šių baltymų veikimo reguliacija mažiau priklauso nuo mitybos veiksnių ir todėl juos nustatyti yra svarbu vertinant vaikų augimo sutrikimus. Rekomenduojama somatomedino C koncentracija kraujo plazmoje (serume) įvairuoja pagal amžių (lytinį subrendimą) ir, pavyzdžiui, 0 4 metų vaikų yra µg/l, metų suaugusiųjų µg/l, metų µg/l; į insuliną panašius augimo faktorius sujungiančio baltymo-3 koncentracija taip pat kinta su amžiumi: vaikų iki 1 metų µg/l, metų µg/l, metų µg/l, o metų µg/l. Augimo hormono nepakankamumas yra reta fizinio augimo sutrikimo priežastis. Vienų, mažo ūgio, vaikų kiti požymiai gali būti normalūs, o kitų išvaizda gali būti nenormali. Mažą ūgį gali lemti įvairios priežastys: abiejų tėvų žemaūgiškumas, paveldimos (achondroplazija) ar lėtinės ligos (inkstų, virškinamojo trakto, kvėpavimo), nepakankama mityba, sutrikusi hormonų reguliacija. Augimo hormono stoka neretai susijusi su hipotiroze ir antinksčių nepakankamumu. Augimo hormono perteklius sukelia itin greitą augimą vadinamąjį gigantizmą. Būklė yra reta, o dažniausia jos priežastis posmegeninės liaukos navikas. Akromegalija suaugusiesiems išsivysto padidėjus augimo hormono sekrecijai ir pradėjus kaulėti epifizei. Dažniausia priežastis posmegeninės liaukos adenoma. Tokiems ligoniams būdingi stambūs veido bruožai, atsikišęs apatinis žandikaulis, sustorėję minkštieji audiniai (storos lūpos), būdingas prakaitavimas, sutrikusi gliukozės tolerancija ar jau išsivystęs cukrinis diabetas. Kraujyje yra padidėjusi augimo hormono koncentracija. Kitos nenormalaus ūgio priežastys: įgimta antinksčių hiperplazija, hipertirozė, paveldimos ligos, pavydžiui, Kleinfelterio sindromas (47 chromosomų kariotipas, XXY). Hiperprolaktinemija, kuri gali sukelti nevaisingumą, diagnozuojama ir vyrams, ir moterims. Moterims anksti išryškėja amenorėja, o vyrams simptomų gali ilgai nebūti; klinika atsiranda, kai prolaktinoma padidėja ir pradeda spausti regos nervą. Hiperprolaktinemijos priežastys gali būti stresas (vien venos punkcija kai kuriems asmenims padidina prolaktino kiekį kraujyje), vaistai (pvz., estrogenai), pirminė hipotirozė, kitos hipofizės ligos. Vazopresinas (antidiurezinis hormonas, ADH) ir oksitocinas sintetinami pogumburio neuronuose; po to nervų skaidulomis jie keliauja į užpakalinę posmegeninės liaukos dalį ir ten kaupiasi. ADH sekreciją skatina padidėjęs plazmos osmoliališkumas (per pogumburyje esančius osmoreceptorius), kraujo tūrio sumažėjimas (per širdies baroreceptorius), taip pat stresas. Oksitocinas atpalaiduojamas, kai žindoma krūtimi arba gimdant susitraukia gimda. Hipofizės hormonų hipofunkcija yra reta. Ją gali sukelti navikas, infarktas, trauma, įgimtas neišsivystymas, infekcija. Klinika priklauso nuo ligonio amžiaus: jei pra- 327
329 sideda naujagimystės tarpsniu būdingas mažas ūgis, sutrikęs vystymasis; moterims atsiranda amenorėja ar nevaisingumas, vyrams sumažėja lytinis potraukis, neišsivysto antriniai lytiniai požymiai, senyviems asmenims simptomai yra susiję su AKTH ar TSH stoka (hipoglikemija, hipotermija). Api b e n d r i n i m a s Nustatyti adenohipofizės navikai, sintetinantys ir sekretuojantys visus jos hormonus. Hiperprolaktinemija yra dažniausias adenohipofizės hormonų sintezės ir sekrecijos sutrikimas. Augimo hormono stoka yra reta vaikų mažo ūgio priežastis. Gigantizmas dažniausiai yra susijęs su vaikystėje padidėjusia augimo hormono sekrecija, posmegeninės liaukos naviku. Suaugusiųjų akromegalijos priežastis yra padidėjusi augimo hormono sekrecija. Laboratoriniai tyrimai Adrenokortikotropinas (adrenokortikotropinis hormonas, AKTH) Tiriamoji medžiaga. Plazma (EDTA). AKTH koncentracija greitai kinta, todėl paimtą kraują būtina laikyti lede. Rekomenduojama reikšmė. 46 ng/l. Diagnostinė vertė. Adisono liga; įgimtoji antinksčių hiperplazija; nuo hipofizės priklausomas Kušingo sindromas; ektopinis AKTH gaminantis navikas. Antrinis antinksčių nepakankamumas, antinksčių vėžys, adenoma; hipofizės funkcijos nepakankamumas. Papildoma informacija. AKTH nestabilus kraujyje, todėl svarbu tinkamai ruošti ėminį. Nėštumas, lytinis ciklas, stresas didina sekreciją. Būdingi paros ritmo svyravimai: didžiausia sekrecija yra 6 8 val. ryte, mažiausia val. Periodiškumas prarandamas esant hiperkorticizmui, išskyrus retus antinksčių navikus. Palyginimui kraujo būtina imti tuo pačiu paros metu, geriau anksti ryte. Kušingo sindromo diagnostikai rekomenduojama papildomai kraujo imti vakare. V: amfetaminai, hipoglikemija, insulinas, levadopa, pirogenai, vazopresinas. V: deksametazonas, kiti gliukokortikoidai, heparinizuotoji plazma. Žmogaus Augimo hormonas (žah, angl. hgh, arba somatotropinis hormonas, STH) Tiriamoji medžiaga. Serumas. Rekomenduojama reikšmė: vyrų <2,4 miu/l (<1 ng/ml), moterų <24 miu/l (<10 ng/ml). Diagnostinė vertė. Hipofizinis gigantizmas, akromegalija, nykštukinis ūgis dėl augimo hormonų receptorių defekto, ektopinė augimo hormono sekrecija (skrandžio, plaučių navikai), inkstų nepakankamumas, cirozė, bloga mityba, stresas, fiziniai pratimai, badavimas (ilgiau trunkantis), nekontroliuojamas cukrinis diabetas, nervinė anoreksija. Hipofizinis nykštukinis ūgis, hipofizės hipofunkcija, antinksčių žievės hiperfunkcija. 328
330 Hormonų klinikinė biochemija ir jų nustatymo reikšmė Papildoma informacija. Augimo hormono sekrecija yra epizodinė, pulsinė. Didžiausias kiekis sekretuojamas gilaus miego metu. Esant akromegalijai ir gigantizmui, ritmiškumas prarandamas. Tyrimas svarbus vertinant akromegalijos gydymą. Išsivysčius nutukimui, sumažėjęs augimo hormono išsiskyrimas ir sutrikinka šio hormono atsakas į insuliną, miegą, fizinį aktyvumą. Su amžiumi augimo hormono sekrecija mažėja kaip atsakas į natūralius veiksnius. V: β adrenoblokatoriai, amfetaminai, estrogenai, gliukagonas, insulinas, klonidinas, kortikotropinas, levadopa, nikotino rūgštis (į veną), oraliniai kontraceptikai, vazopresinas. V: gliukozė, fenotiazinai, gliukokortikoidai, probukolis. Folitropinas (folikulus stimuliuojantis hormonas, FSH) Tiriamoji medžiaga. Serumas. Rekomenduojama reikšmė (U/l): vyrų 0,7 11,1 moterų: folikulinė fazė 2,8 11,3 folikulinė fazė 2 3 dienų 3,0 14,4 ovuliacijos fazė 5,8 21 geltonkūnio fazė 1,2 9,0 pomenopauzė 21,7 153 vartojant kontraceptikus 4,9 Diagnostinė vertė. Pirminis lytinių liaukų nepakankamumas, kiaušidžių ar sėklidžių agenezė, Kleinfelterio sindromas, kastracija, alkoholizmas, menopauzė, orchitas, gonadotropinius hormonus sekretuojanis hipofizės navikas. Priekinės hipofizės dalies hipofunkcija, pogumburio funkcijos sutrikimai, nėštumas, nervinė anoreksija, policistinė kiaušidžių liga, hemochromatozė, sunki liga, hiperprolaktinemija. Hipogonadizmo priežastis, jei folitropino ir liutropino kiekiai mažesni, negu turėtų būti to amžiaus asmeniui, greičiausiai yra sutrikusi pogumburio ar hipofizės veikla. Didesni šių hormonų kiekiai rodo pirminį lytinių liaukų defektą. Papildoma informacija. Mėnesinių ciklo viduryje ši hormono sekrecijos viršūnė yra mažesnė ir trunka trumpiau negu liutropino. Dėl epizodinės, cirkadinės ir ciklinės lytines liaukas stimuliuojančių hormonų sekrecijos jų nustatymą reikia kartoti daug kartų ar naudoti supiltus kelis ėminius. Vyrų hormonų kiekis įvairuoja mažiau. V: cimetidinas, digitalis, levadopa. V: estrogenai (priklauso nuo dozės ir trukmės: didelės dozės mažina, o mažos gali didinti), fenotiazinai, gonadotropinus atpalaiduojančių hormonų analogai (nuolatinis vartojimas), gliukokortikoidai, geriamieji kontraceptikai. Liutropinas (liuteinizuojantis hormonas, LH) Tiriamoji medžiaga. Serumas. Rekomenduojama reikšmė (U/l): vyrų 0,8 7,6 moterų: folikulinė fazė 1,1 11,6 folikulinė fazė 2 3 dienų 3,0 14,4 ovuliacijos fazė geltonkūnio fazė 14,7 premenstruacinė fazė ±8 d. 12 pomenopauzė 11,3 39,8 vartojant kontraceptikus 8,0 Diagnostinė vertė. Pirminė lytinių liaukų disfunkcija, kiaušidžių policistozė, pomenopauzė, hipofizės adenoma (retai). 329
331 Hipofizės ar hipotalamo srities pažaida, izoliuota lytinių hormonų stoka, nervinė anoreksija, izoliuota LH stoka, stiprus stresas, bloga mityba, sunki liga. Uždelsta LH ir FSH sintezės pradžia lytinio brendimo metu ir jų išsiskyrimas yra būdingi vėluojančiojo konstitucinio augimo ir lytinio brendimo sindromo požymiai. Papildoma informacija. Fiziologinę lytinių hormonų sekrecijos įvairovę apibūdina epizodinė sekrecija, įvairavimas per parą, ciklinė sekrecija. Lytinio brendimo metu cirkuliuojančių lytinių hormonų kiekis yra didesnis miegant negu aktyviu paros metu. Epizodiniai LH sekrecijos įvairavimai yra didesni negu FSH. Todėl sumaišytų kelių kraujo ėminių tyrimas yra patikimesnis ir informatyvesnis negu pavienis kraujo tyrimas. LH ir žchg (žmogaus chorioninio gonadotropino) β subvienetai pasižymi didele homologija. LH gali kryžmiškai reaguoti su žchg, todėl LH matavimas netikslus nėščiosioms, gimdyvėms ar esant žchg sekretuojančiam navikui. V: vaistai nuo traukulių, spironolaktonas. V: digoksinas, gonadotropinus išskiriančio hormono analogai, oraliniai kontraceptikai, progesteronas. Estrogenų poveikis priklauso nuo dozės ir vartojimo trukmės: didelės dozės mažina, o mažos didina LH kiekį. Poveikis trunka tik kelias dienas. Prolaktinas (PRL) Tiriamoji medžiaga. Serumas. Rekomenduojama reikšmė: ng/ml mu/l vyrų 2, moterų: visas ciklas 4, folikulinė fazė 4, ovuliacijos fazė 6, geltonkūnio fazė 4, Diagnostinė vertė. Prolaktiną išskiriantis hipofizės navikas (makroadenoma); mikroadenoma; 3/4 pacientų esant amenorėjai ir (ar) galaktorėjai; hipotalamo ir hipofizės ligos (pvz., sarkoidozė, granulomatozė, kraniofaringioma, metastazinis vėžys, tuščio turkabalnio sindromas); pirminė hipotirozė, nervinė anoreksija, policistinės kiaušidės, insktų nepakankamumas, insulino sukelta hipoglikemija, antinksčių nepakankamumas, chirurginė procedūra (hipofizės srityje). Hipofizės apopleksija, pvz., Šyhano (Sheehan) sindromas). Papildoma informacija. Fiziologinis padidėjimas būdingas vaisiui ir naujagimiui. Suaugusiesiems padaugėja miegant (viršūnė anksti ryte), esant stresui, mankštinantis. Moterims padidėja nėštumo metu, po sueities, maitinant. Prolaktino tyrimas svarbus nustatant, ar buvo visiškai pašalinta hipofizė. V: antihistamininiai, antipsichoziniai (pvz., haloperidolis, fenotiazinas, pimozidas), argininas, alus, estrogenai, histamino antagonistai (cimetidinas), monoaminooksidazės inhibitoriai, opijatai, geriamieji kontraceptikai, rezerpinas, tricikliai antidepresantai, verapamilis. V: dopaminas, levadopa, klonidinas, skalsės alkaloidai (bromokriptinas). Tirotropinas (skydliaukę stimuliuojantis hormonas, angl. TSH) Tiriamoji medžiaga. Serumas. Rekomenduojama reikšmė (mu/l): vaikų: 1 metų 0,4 8,6 5 metų 0,64 6,0 10 metų 0,36 5,5 12 metų 0,36 5,4 suaugusiųjų 0,4 4,0 Diagnostinė vertė. Pirminė hipotirozė (nuo 3 iki 100 kartų daugiau už normą), Hašimoto tiroiditas, esant hipotirozės klinikai; daliai ligonių, kuriems yra Hašimoto tiroiditas ir eutirozės 330
332 Hormonų klinikinė biochemija ir jų nustatymo reikšmė klinika; ektopinė tirotropino sekrecija (plaučių, krūties navikai); poūmis tiroiditas (sveikimo fazė); ligos, nesusijusios su skydliauke (sveikimo fazė). Pirminė hipertirozė, antrinė hipotirozė (hipofizės), tretinė hipotirozė (pogumburio); hipertirozė, esant toksiniam daugiamazgiam gūžiui, autonominei skydliaukės hormono sekrecijai, gydant skydliaukės hormonu. Papildoma informacija. Paros ritmo svyravimai: viršūnė 2 4 val. ir mažiausias kiekis valandą. Gydant hipertirozę, tiroglobulino kiekis 4 6 savaites gali būti mažas ir kai pasiekta eutiroidinė būklė. Tirotropino pakilimo banga yra tik gimus, po 30 min., vėliau, 3-ią dieną, sumažėja ir pirmą gyvenimo savaitę pasiekia suaugusio žmogaus lygį. V: amiodaronas, fenotiazinai, haloperidolis, jodidai, litis, morfinas, geriamieji radiografiniai dažikliai, propiltiouracilis, tirotropiną atpalaiduojantis hormonas. V: dopaminas, heparinas į veną, karbamazepinas, gliukortikoidai, somatostatinas, trijodtironinas. Sk yd l i a u k ė, j o s si n t e t i n a m ų ho r m o n ų veikimas Skydliaukė sintetina ir sekretuoja hormonų tiroksino (T 4 ) ir trijodtironino (T 3 ) mišinį (kartu jie vadinami skydliaukės hormonu ). Jie veikia bendrą organizmo metabolinį aktyvumą ir jo greitį. Šių hormonų sintezė vyksta prijungiant jodą ir suporinant dvi tirozino molekules, po to jas prijungiant prie baltymo tiroglobulino. T 4 turi keturis jodo atomus, T 3 tris. Skydliaukė gamina ir kitą hormoną kalcitoniną polipeptidą, kuris reguliuoja kalcio apykakaitą. Kalcitoniną taip pat gamina prieskydinės liaukos ir užkrūčio liauka. Skydliaukėje esantis jodas įeina į tiroglobulino sudėtį. Tai glikoproteinas (molekulinė masė 660 kda), užpildantis skydliaukės folikulų ertmes. Tiroglobulino, kaip ir kitų skydliaukės baltymų, sintezę reguliuoja pogumburio ir posmegeninės liaukos sąveika (36 pav.). Pogumburis TRH + Adenohipofizė TSH + Skydliaukė: T 4, T 3 slopina ; + skatina T 4 tiroksinas; T 3 trijodtironinas; TRH tirotropiną atpalaiduojantis hormonas; TSH tirotropinas (skydliaukę stimuliuojantis hormonas) 36 pav. Skydliaukės funkcijos reguliacija 331
333 Pogumburio tirotropiną atpalaiduojantis hormonas (thyrotropin releasing hormone, TRH) veikia tirotropino (TSH) sekreciją adenohipofizėje. TSH reguliuoja tiroglobulino sintezę skatindamas rrnr ir irnr sintezę. Cirkuliuojantys kraujyje skydliaukės hormonai grįžtamai slopina pogumburio ir posmegeninės liaukos hormonų sekrecijos greitį. Šie greičiai kinta atvirkščiai nelygu, kokia skydliaukės hormonų koncentracija kraujyje. Antrasis pogumburio hormonas somatostatinas yra TSH sekrecijos inhibitorius. Taigi veikia dviguba tirotropino sekrecijos reguliacija, kuri vykdoma per teigiamo (tarpininkas yra tirotropiną atpalaiduojantis hormonas) ir neigiamo (tarpininkas yra somatostatinas) poveikio mechanizmus. Dar yra papildomų reguliacijos mechanizmų, pavyzdžiui, dėl pogumburio tirotropiną atpalaiduojančio hormono inaktyvinimo plazmos proteazėmis. Mažiau negu 3% viso tiroglobuline esančio jodo yra N 3 -monojod-l-histidine, bet jis neturi skydliaukės hormonams būdingo aktyvumo, ir yra skydliaukės hormono biosintezės šalutinis produktas. Monojodtirozinas ir dijodtirozinas taip pat nepasižymi biologiniu aktyvumu (40 lentelė). 40 lentelė. Skydliaukėje randamos jodo turinčios organinės medžiagos Junginys 3,5-dijodtirozinas Tiroksinas (T 4 ) 3,5,3 -trijodtironinas (T 3 ) (rt 3 ), 3,3,5-trijodtironinas (rt 3 ) 3,3 -dijodtironinas 3-monojodtirozinas Procentas viso jodo kiekio žmogaus skydliaukėje <1 < Biologinis aktyvumas, prilygintas tiroksinui Tik jodtironinams būdingas fiziologinis poveikis ir jie yra normaliai liaukos sekretuojami produktai. Jodinti tironinai yra tiroglobulino sudedamosios dalys. Skydliaukėje yra keturi jodinti tironinai, iš jų svarbiausi yra L tiroksinas ir L-3,5,3 -trijodtironinas. Apie 1% jų skydliaukėje yra laisvi. Jodo turinčių skydliaukės hormonų biosintezė ir sekrecija. Jodo apykaita skydliaukėje vyksta nuolat ir trimis etapais: jodo patekimu į liauką, jodo virtimu jodo turinčiu skydliaukės baltymu (tiroglobulinu), proteolizės ir skydliaukės hormonų sekrecija. Skydliaukė kaupia patekusį į organizmą jodą skydliaukės folikulų koloide. Liauka gali sukaupti jodo mažiausiai 25 kartus daugiau, palyginti su jo koncentracija plazmoje, ir greitai jį sujungia su organiniais junginiais. Normaliai skydliaukėje yra apie 10 µg laisvojo jodo, lyginant su 7500 µg organiškai sujungto jodo. Jodo kaupimosi skydliaukėje mechanizmas susijęs su K + ir Na + pernaša. Kitos liaukos, pavyzdžiui, seilių ir skrandžio gleivinės, taip pat kaupia jodą. Seilėse, skrandžio sultyse, pie- 332
334 Hormonų klinikinė biochemija ir jų nustatymo reikšmė ne jodo koncentracija gali kartų viršyti jo koncentraciją kraujyje, bet šios liaukos, priešingai negu skydliaukė, negali sukaupti didelių jodo atsargų, nesudaro tiroksino ar trijodtironino, nereaguoja į tirotropinio hormono veikimą. Tiroksino sintezę sudaro šios stadijos: tirozino liekanų jodinimas į monojodtiroziną, tolesnis monojodtirozino jodinimas į dijodtiroziną, dviejų dijodtirozino liekanų suporinimas susidarant tiroksinui arba vienos monojodtirozino ir vienos dijodtirozino liekanos susijungimas į trijodtironiną. Šių hormonų sintezę liaukoje katalizuoja skydliaukės peroksidazė. Tiroglobulinas neturi jokių hormoninių savybių. Jos atsiranda tik vykstant tiroglobulino proteolizei. Aplink šias ląsteles yra gausus kapiliarų tinklas, į kurį ir išskiriami hormonai. Tiroglobulino sintezė ir proteolizė vyksta nuolat. Kasdien normaliai žmogaus skydliaukė išskiria apie 70 µg tiroksino (T 4 ) ir apie 25 µg trijodtironino (T 3 ). Skydliaukės mikrosomose yra dehalogenazė, kuri atskiria jodą nuo monojodtirozinų ir dijodtirozinų. Išsiskyręs halogenas yra vėl panaudojamas. Sergant paveldimuoju šeiminiu gūžiu, dėl šio fermento stokos iš skydliaukės netenkama daug jodintų tirozinų. Tiroksino ir trijodtironino pernaša su krauju. Kraujas tiroksiną (99,95%) perneša prisijungusį prie trijų pernašos baltymų. Pagrindinis ir specifiškiausias yra tiroksiną sujungiantis globulinas (prijungia 70% T 4 ) tai glikoproteinas (molekulinė masė Da), kuris, tiriant elektroforeze, juda tarp α 1 ir α 2 globulinų. Albuminas prijungia apie 25% ir transtiretinas (anksčiau vadintas prealbuminu) apie 5% tiroksino. Tie patys baltymai sujungia per 99,95% T 3. Trijodtironinas taip pat gali būti perneštas junginyje su tiroksiną sujungiančiu globulinu, bet ryšio stiprumas sudaro tik 1/10 tiroksiną rišančiosios jėgos. Tai veikia ir hormono kiekį, ir iš dalies paaiškina didesnį biologinį trijodtironino aktyvumą. Tai atspindi ir didesnis tiroksino gyvavimo kraujyje puslaikis 6 7 dienos, palyginti su trijodtironino dviem dienomis. Tiroksinas ir trijodtironinas yra deamininami, dejodinami ir konjuguojami. Kepenys (po jų inkstai) yra svarbiausias organas, reguliuojantis tiroksino ir trijodtironino kiekį kraujyje, nes jose šie hormonai galutinai katabolizuojami. Apie 40% suleistos tiroksino dozės gali būti randama kepenyse po 1 mėnesio. Nedaug nepakitusių hormonų kartu su jodidais pasirodo tulžyje ir šlapime. Normaliai tiroksinas turi 85 90%, trijodtironinas apie 4 5% viso kraujyje esančio jodo. Nedaug jo yra dijodtirozine ir retai pasitaikančiame monojodtirozine. Kitas kiekis apie 5% yra neorganiniai jodo junginiai. Normali laisvojo tiroksino ir trijodtironino koncentracija plazmoje yra atitinkamai 2 ir 0,6 ng/100 ml (100 ir 2 nmol/l). 333
335 Skydliaukės hormonų veikimas. Dauguma ląstelių paima T 4 ir dejodina į biologiškai aktyvesnį T 3. T 4 gali virsti ir neaktyviu T 3 (angl. reverse rt 3 ). Pagrindinis biologinis skydliaukės hormonų veikimas susijęs su pirminiu poveikiu genų ekspresijos kontrolei. Hormonas greitai patenka į ląsteles (kepenų, raumenų) ir yra sujungiamas su branduolio chromatino baltymu, kuris skatina transkripciją. Dėl tiroksino poveikio padidėja baltymų sintezės greitis ir daugelio fermentinių sistemų aktyvumas. Be jo sujungimo branduolyje, yra rasti kiti du receptorių tipai: vienas mitochondrijų membranoje, kitas citozolio baltyme; pastarasis daug dažniau sujungia trijodtironiną negu tiroksiną. Susijungęs su branduolio baltymais hormonas veikia augimą, vystymąsi ir funkcijas, susijusias su ląstelės diferenciacija. Mitochondrinis hormoną sujungiantis baltymas yra susijęs su energijos apykaitos reguliavimu. Dėl tiroksino poveikio pakinta apie 100 fermentinių sistemų greitis, yra skatinamos reakcijos kiekviename organe ir audinyje: spartėja apykaita, greitėja augimas, O 2 sunaudojimas. Skydliaukės hormonai didina pagrindinę apykaitą, kuri susijusi su termogeneze. Skydliaukės hipofunkcija ir hiperfunkcija. Skydliaukės hipofunkciją rodo sulėtėję procesai organizme, svarbiausia pagrindinės energijos apykaitos, taip pat sumažėjusi kūno temperatūra. Ligos klinikai būdinga letargija ir nuovargis, ligoniai nepakenčia šalčio, jie priauga svorio, sausėja oda, sulėtėja raumenų atsipalaidavimas ir sausgyslių refleksai, taip pat išryškėja anemija, demencija, vidurių užkietėjimas, bradikardija, subfebrili temperatūra, kraujyje hipercholesterolemija. Jei hipotirozė yra jau gimus, tai išsivysto būklė, vadinama infantiline miksedema, arba kretinizmu. Suaugusiųjų ši būklė apibūdinama terminu miksedema. Hipofunkcinė skydliaukė blogai kaupia jodą ir ši savybė naudojama diagnostikai, t. y. matuojamas nesusijungusio su hormonu baltymo kiekis. Esant hipotirozei, cirkuliuojančio skydliaukės hormono koncentracija sudaro apie 1/4 normalaus jo kiekio. Įgimta hipotirozė būna 1 iš 4000 gimusių naujagimių (Vilniaus universiteto ligoninės Santariškių klinikų Medicininės genetikos centro duomenimis (V. Kučinskas), Lietuvoje 1 iš 4500). Anksti diagnozavus ligą, gydymui skiriami skydliaukės hormonai. Tokių naujagimių, vėliau ir kūdikių vystymasis nesutrinka. Laiku nepradėjus gydymo, išsivysto kretinizmas. Padidėjusi TSH koncentracija, nustatyta kraujo laše, yra diagnostinis pirminės (įgimtos) naujagimių hipotirozės požymis. Lietuvoje visuotinis naujagimių tikrinimas dėl įgimtos hipotirozės įdiegtas 1993 metais. Hipertirozė tai būklė, kai yra padidėjęs skydliaukės aktyvumas; tirotiksikozė tai būklė, kai audiniai yra veikiami per didelio skydliaukės hormonų kiekio 334
336 Hormonų klinikinė biochemija ir jų nustatymo reikšmė (pvz., gydant T 4 ). Hipertirozė būdinga sergant Greivso (seniau vadinta Bazedovo) liga, difuziniu toksiniu (egzoftalminiu) gūžiu, tiroiditu, taip pat vartojant jodo ar jodo turinčių vaistų (pvz., amiodaroną), skydliaukės hormonų. Esant hipertirozei, pagrindinė apykaita padidėja 30 60%, palyginti su norma. Klinikiniai hipertirozės požymiai yra ryškūs: ligoniams krinta svoris, nors apetitas geras, jie prakaituoja ir nepakelia karščio, jaučiamas silpnumas, sinusinė tachikardija ar prieširdžių virpėjimas, dirglumas, raumenų silpnumas, viduriavimas, gūžys ir išverstakumas (egzoftalmas); kraujo tyrimai rodo hipocholesterolemiją, hiperglikemiją, glikozuriją, sumažėjusią gliukozės toleranciją, neigiamą azoto balansą, padidėjusį jodo kaupimąsi skydliaukėje. Greivso liga yra dažniausia hipertirozės priežastis. Tai autoimuninė liga, kai susidaro antikūnų prieš TSH receptorius ir jie imituoja hipofizės hormono veikimą. Nepiktybinis skydliaukės padidėjimas gūžys vystosi dėl skydliaukės nesugebėjimo sekretuoti tinkamą aktyvių hormonų kiekį, kuris galėtų patenkinti periferinių audinių reikmes. Trūkstant hormonų kraujyje, sutrinka TSH reguliacija grįžtamuoju ryšiu, t. y. ji sustiprėja, dėl to yra stimuliuojamas liaukos augimas ir visų skydliaukėje vykstančių hormonų sintezės ir sekrecijos reakcijų greitis. Šie kompensaciniai mechanizmai palaiko normalų hormonų kiekį, bet tik didėjant liaukai. Jei hormono gamyba sutrinka dar labiau, tai išryškėja gūžys ir hipotirozė (gūžys nekompensuoja hipofunkcijos). Antitiroidinės medžiagos. Tai medžiagos, slopinančios skydliaukės funkciją, nes: 1) neleidžia hormonui atsipalaiduoti iš skydliaukės dėl grįžtamojo ryšio sutrikimo, pavyzdžiui, tiroksinas, kuris veikia hipofizės tirotropinio hormono sintezę ir sekreciją; 2) lėtina hormono sintezę, pavyzdžiui: tiocianatas ir kiti anijonai (jie slopina jodidų patekimą į skydliaukę), kalcio jonai (jie slopina skydliaukės peroksidazę ir taip blokuoja tiroglobulino tirozino liekanų jodinimą); hipotirozė išsivysto vartojant kobalto druskų eritropoezei skatinti; 3) slopina skydliaukės hormonų naudojimą tai struktūriniai skydliaukės hormono analogai. Api b e n d r i n i m a s Skydliaukė sintetina, sekretuoja ir kaupia skydliaukės hormonus T 4 ir T 3, kurie yra svarbūs normaliam organizmo vystymuisi ir medžiagų apykaitai. Skydliaukės hormonų sintezę ir sekreciją reguliuoja adenohipofizės tirotropinis hormonas. Dauguma T 4 ir T 3 plazmoje yra susijungę su baltymais ir tik nedidelė dalis yra laisvi. Biologiškai aktyvūs yra laisvieji hormonai. 335
337 TSH, skydliaukės hormonų ir tiroksiną sujungiančio globulino koncentracijų nustatymas yra svarbus skydliaukės ligų diagnotikai. Hipotiroze sergama dažnai ir pagrindinė jos priežastis yra skydliaukės destrukcija dėl autoimuninės ligos, chirurginių procedūrų ar gydymo radioaktyviosiomis medžiagomis. Pirminė hipotirozė diagnozuojama remiantis padidėjusia TSH koncentracija kraujyje. Autoimuninės skydliaukės ligų priežastys yra dažnos. Jų buvimas gali padėti gydytojui nustatyti kitas autoimunines ligas, kurios nebuvo diagnozuotos, pavyzdžiui, nuo insulino priklausomas diabetas, autoimuninė hipoparatirozė, pirminių lytinių liaukų nepakankamumas, autoimuninė antinksčių destrukcija ir Adisono liga bei kitos. Hipertirozė diagnozuojama remiantis sumažėjusia TSH ir padidėjusia T 4 koncentracija. Sudėtingesniais atvejais gali padėti T 3, laisvojo ir susijungusio su baltymu hormono koncentracijos matavimas. Laboratoriniai tyrimai Antikūnai prieš skydliaukės peroksidazę Tiriamoji medžiaga. Serumas. Rekomenduojama reikšmė. <35 ku/l. Diagnostinė vertė. Autoimuninė skydliaukės patologija (Hašimoto tiroiditas, idiopatinė miksedema, Greivso liga). Sergant neimuninėmis skydliaukės ligomis, antikūnų prieš skydliaukės peroksidazę radimo dažnis yra kaip ir sveikų asmenų populiacijoje. Papildoma informacija. Antikūnai prieš skydliaukės peroksidazę yra pagrindinis ir vienintelis autoantigeninis mikrosomų komponentas. Tyrimas jautresnis ir specifiškesnis negu antikūnų prieš tiroglobuliną. Antikūnai prieš tiroglobuliną Tiriamoji medžiaga. Serumas. Rekomenduojama reikšmė. <40 ku/l. Diagnostinė vertė. Teigiami titrai sergant Hašimoto tiroiditu, Greivso liga, skydliaukės vėžiu, idiopatine miksedema, B 12 vitamino stokos anemija, sistemine raudonąja vilklige. Nedidelis procentas sveikų asmenų gali turėti mažą antikūnų titrą be jokių ligos požymių (dažniau moterys ir senyvi žmonės). Silpnai teigiama reakcija galima dėl kitų autoimuninių, chromosominių ligų Ternerio (Turner) sindromo, Dauno sindromo. Radus antikūnų prieš tiroglobuliną bei mikrosomas, galima įtarti autoimuninę skydliaukės patologiją. Tiroglobulinas (Tg) Tiriamoji medžiaga. Serumas. Rekomenduojama reikšmė. 0,83 55 mg/l. Diagnostinė vertė. Negydytos skydliaukės folikulinis ir papilinis vėžys (ne medulinis), didelis procentas individų, kuriems yra hipertirozė (nėra koreliacijos tarp serumo Tg ir T 4 kiekio); poūmis tiroiditas, gerybinė adenoma. Sėkmingai gydant vėžį, Tg kiekis sumažėja iki normalaus ir kyla, kai po pradinio gydymo atsiranda metastazių. Kiekis didelis naujagimių serume, vėliau, per pirmus dvejus gyvenimo metus, mažėja. Tg tyrimas svarbus nustatant skydliaukės audinį naujagimiams, turintiems įgimtą hipotirozę. Papildoma informacija. V: autoantikūnai prieš tiroglobuliną. 336
338 Hormonų klinikinė biochemija ir jų nustatymo reikšmė bendrasis Tiroksinas (T 4 ) Tiriamoji medžiaga. Serumas. Rekomenduojama reikšmė nmol/l (4,5 12,5 µg/dl). Diagnostinė vertė. Hipertirozė, būklės, kai padaugėja tiroksiną sujungiančio globulino (pvz., nėštumas, genetinės padidėjimo priežastys, protarpinė porfirija, pirminė biliarinė cirozė), tirotoksikozė, kai kada ūminis tiroiditas, hepatitas (po 4 sav.), nutukimas, ūminė psichikos liga; T 4 gali būti padidėjęs pacientams su eutiroze dėl padidėjusio T 4 jungimosi su tiroksiną sujungiančiu prealbuminu ar esant T 4 autoantikūnų; šiais atvejais T 3 yra normalus. Hipotirozė, būklės kai sumažėja tiroksiną sujungiančio globulino (nefrozinis sindromas, lėtinės kepenų ligos, baltymų netekimas per virškinamąjį traktą, genetinės sumažėjimo priežastys, bloga mityba), hipofizės panhipofunkcija, fizinė įtampa. Sergant hipotiroze, bendrasis serumo T 4 mažėja anksčiau negu T 3. Padidėjęss T 4 ir laisvasis T 4, taikant pakeičiamąjį gydymą tiroksinu, nebūtinai rodo perdozavimą; normalus T 3 patvirtina eutiroidinę būklę. Papildoma informacija. T 4 tyrimas svarbus, kai tirotropino kiekis yra padidėjęs ar sumažėjęs. Pats bendrojo tiroksino nustatymas kliniškai nėra labai informatyvus. Naujagimių T 4 yra didesnis dėl padidėjusio tiroksiną sujungiančio globulino kiekio, laisvojo T 4 kiekis yra panašus į suaugusiųjų. Kiekis pirmomis valandomis po gimimo didėja ir vėliau mažėja iki 5 metų amžiaus. Berniukų T 4 lytinio brendimo metu mažėja. V: amiodaronas, amfetaminas, dekstrotiroksinas, estrogenai, heroinas, levadopa, metadonas, geriamieji kontraceptikai, propranololis, skydliaukės preparatai, tirotropinas. V: aminosalicilo rūgštis, androgenai, aspirinas, augimo hormonas, fenilbutazonas, furozemidas (didelės dozės), jodidai, gliukokortikoidai, kortikotropinas, litis, penicilinas, vaistai nuo traukulių, rezerpinas, rifampicinas, somatotropinas, trijodtironinas. laisvasis Tiroksinas (L-T 4 ) Tiriamoji medžiaga. Serumas. Rekomenduojama reikšmė. 10,3 24,5 pmol/l (0,8 1,9 ng/dl). Diagnostinė vertė. Hipertirozė; hipotirozė, gydoma tiroksinu. Hipotirozė, gydoma trijodtironinu; paskutiniai nėštumo mėnesiai. Laisvojo tiroksino kiekio svyravimai esant eutirozei galimi asmenims, sergantiems ūminėmis ar lėtinėmis ne skydliaukės ligomis. Papildoma informacija. Laisvasis tiroksinas sudaro 0,02 0,04% bendrojo tiroksino kiekio. V: amiodaronas, aspirinas, propranololis. V: metadonas, vaistai nuo traukulių (karbamazepinas), rifampicinas. Tiroksiną sujungiantis globulinas Tiriamoji medžiaga. Serumas. Rekomenduotina reikšmė nmol/l (13 39 µg/ml). Diagnostinė vertė. Infekcinis hepatitas, ūminė protarpinė porfirija, genetiškai nulemtas didelis kiekis, hipotirozė (kai kada), nėštumas. Sunkios ligos, chirurginis stresas, bloga mityba (ypač baltymų stoka), enteropatijos, netenkant baltymų, nefrozinis sindromas, aktyvioji akromegalija, kiaušidžių hipofunkcija, genetiškai nulemtas mažas kiekis. Papildoma informacija. Šis glikoproteinas yra pagrindinis T 3 ir T 4 hormonų nešiklis. Šių hormonų pusiausvyrą užtikrina prealbuminas. Kiekis mažėja su amžiumi, kartu mažėjant bendrojo ir laisvojo T 4 ir T 3. V: estrogenai, geriamieji kontraceptikai, tamoksifenas. V: anaboliniai steroidai, androgenai, gliukokortikoidai, kortikotropinas, propanololis. 337
339 bendrasis Trijodtironinas (T 3 ) Tiriamoji medžiaga. Serumas. Rekomenduojama reikšmė. 1,3 2,6 nmol/l ( ng/dl). Diagnostinė vertė. Hipertirozė, T 3 tirotoksikozė, gydoma hipertirozė, skydliaukės nepakankamumas, gūžys dėl jodo stokos, būklės, kai padidėja tiroksiną sujungiančio globulino kiekis, nėštumas. Hipotirozė, būklės, kai sumažėja tiroksiną sujungiančio globulino kiekis, ūminės ir lėtinės skydliaukės ligos. Esant ankstyvos stadijos ar nesunkiai pirminei hipotirozei, T 4 sumažėja daugiau negu T 3 (didelis T 3 /T 4 santykis). Papildoma informacija. Apie 80% kraujyje esančio trijodtironino yra susidariusio po T 4 monodejodinimo periferiniuose audiniuose. T 3 biologinėse sistemose yra 4 5 kartus aktyvesnis negu T 4. Serume T 3 kiekis yra apie 100 kartų mažesnis už T 4 koncentraciją. Kadangi T 3 greitai sumažėja (sureaguoja) dėl organizmo atsako į stresą ir kitus ne su skydliauke susijusius veiksnius, vien T 3 nustatymas nėra pakankamas tyrimas įvertinant skydliaukės būklę. V: estrogenai, didelis aukštis (kalnuose), heroinas, metadonas, geriamieji kontraceptikai. V: androgenai, cimetidinas, medžiagos cholecistografijai (per os), deksametazonas, jodidai, litis, vaistai nuo traukulių, propranololis, salicilatai (didelės dozės). Prieskydinėse liaukose sintetinami hormonai Prieskydinės liaukos gamina parathormoną ir kalcitoniną. Kartu su D vitaminu jie yra pagrindiniai kalcio ir fosfatų apykaitos reguliatoriai. Parathormonas sintetinamas ir sekretuojamas tik prieskydinėse liaukose, o kalcitoninas ir skydliaukėje bei užkrūčio liaukoje. Parathormonas Parathormonas (molekulinė masė 9500 Da) yra polipeptidas iš 84 aminorūgščių liekanų. Prieskydinėse liaukose jis egzistuoja kaip prohormonas (90 liekanų) ir savo struktūroje turi papildomą heksapeptidą. Žmogaus ir jaučio šis heksapeptidas yra identiškas. Prohormonas biologiškai neaktyvus, kol nepašalinamas jo heksapeptidas. Vykstant transliacijos procesui, prie prohormono dar prisijungia 25-ių aminorūgšties liekanų fragmentas, ir visas toks kompleksas vadinamas preproparathormonu tai prohormono pirmtakas biosintezės procese. Preprohormonas virsta prohormonu per 1 minutę. Prohormono virtimas hormonu trunka minučių. Šis laikas reikalingas prohormono pernašai iš šiurkštaus endoplazminio tinklo pro lygųjį endoplazminį tinklą į Goldžio kompleksą, kur prohormonas ir virsta hormonu, o pastarasis įvelkamas į sekrecines granules. Pagrindinės šio hormono veikimo vietos yra inkstai ir griaučiai, o svarbiausias parathormono reguliuojamas metabolitas yra kalcio jonai (Ca 2+ ) pastarieji yra vieninteliai, reguliuojantys šio hormono sekreciją. 338
340 Hormonų klinikinė biochemija ir jų nustatymo reikšmė Parathormono sekreciją reguliuoja kraujo serume esantis jonizuotojo kalcio kiekis, ir jų kiekis kinta atvirkščiai, pavyzdžiui, kalcio jonų kiekio padidėjimas serume sumažina hormono sekreciją. Cirkuliuojančio kraujyje žmogaus parathormono gyvavimo pusperiodis yra apie min., t. y. artimas kitų polipeptidinių hormonų (panašaus dydžio) gyvavimo trukmei. Parathormono veikimas. Audinių taikinių ląstelių membranose yra specifinių parathormonui receptorių. Hormono susijungimas su jais stimuliuoja membranoje esančią adenilatciklazę ir dėl to greitai didėja camf kiekis, ypač inkstų ir kaulų ląstelėse. Šis procesas yra susijęs su ląstelinių kalcio jonų persiskirstymu, pvz., mitochondrijose, endoplazminio tinklo vezikulėse. Mitozinis aktyvumas, kurį atspindi DNR sintezė, priklauso nuo Ca 2+. Tokiu būdu parathormonas veikia (reguliuoja) ląstelių proliferaciją bei imuninį atsaką ir, pavyzdžiui, pašalinus prieskydines liaukas, sutrikdoma antikūnų atsakomoji reakcija. Parathormonas greit prisijungia prie inkstų ląstelių receptorių, ir dėl to inkstų kanalėliuose greitai didėja Ca 2+ ir Mg 2+ reabsorbcija, K +, neorganinio fosforo (Pi) ir HCO 3 ekskrecija, mažėja H + ir NH 4 + ekskrecija. Dėl sumažėjusios Pi reabsorbcijos inkstų kanalėliuose išryškėja fosfaturija. Kraujo plazmoje daugėja Ca 2+ (pastarasis imamas iš kaulų pagrindinio kalcio šaltinio). Esant prieskydinių liaukų hiposekrecijai (pavyzdžiui, jas pašalinus), sumažėja fosfatų ekskrecija, jų kraujyje padaugėja, o Ca 2+ sumažėja. Parathormonas skatina inkstinę gliukoneogenezę iš aminorūgščių, laktato, glicerolio ir citratinio ciklo tarpinių produktų. Be to, parathormonas svarbus D 3 vitamino veikimui dėl pastarojo poveikio didėja Ca 2+ ir Pi absorbcija iš virškinamojo trakto. Parathormonas svarbus kaulo medžiagų apykaitai, nes slopina kolageno sintezę osteoblastuose, skatina osteoklastų vykdomą osteolizę, didina ląstelių pirmtakų brendimo virtimo osteoblastais ir osteoklastais greitį. Dėl to mažėja Ca 2+ rišamoji geba ir vyksta net ir gerai kalcifikuoto kaulo erozija. Ne toks tiesioginis, tačiau svarbus hormono veikimas mobilizuojant Ca 2+ iš kaulų. Parathormonas inkstuose stimuliuoja 1,25-dihidroksicholekalciferolio (D 3 vitamino) gamybą iš 25-hidroksicholekalciferolio ir taip skatina Ca 2+ mobilizaciją iš kaulų ir jo pernašą per žarnų sienelę. Dėl to didėja kaulo rezorbcija, atsipalaiduoja daugiau Ca 2+, kaulo užpildas netenka proteoglikanų (nes yra padidėjęs kolagenolizinis aktyvumas dėl kolageno sintezės osteoblastuose slopinimo). Kadangi dėl šių procesų kaulų ląstelėse kaupiasi izocitrinų bei pieno rūgštys, taip pat vandenilio jonai, gerėja kalcio jonų patekimas iš kaulų į kraują. Hipoparatirozė ir hiperparatirozė. Hipoparatirozė žmonėms pasitaiko retai ir priklauso nuo chirurginių skydliaukės ar prieskydinių liaukų procedūrų, o dar 339
341 rečiau nuo prieskydinių liaukų ligų. Negydant atsiranda hipokalcemija, traukuliai, tetanija ir ištinka mirtis. Hiperparatirozė išsivysto dėl šių liaukų hiperfunkcijos, dėl auglio ar hiperplazijos. Žmonėms, sergantiems sunkia pirmine hiperparatiroze, išryškėja osteitis fibroza cystica: būdinga [Ca 2+ ] kiekio padidėjimas ir [Pi] sumažėjimas kraujyje, ypač paspartėja Ca 2+ ekskrecija per inkstus. Neretai dėl to inkstuose susidaro akmenų ir vystosi antrinis inkstų veiklos nepakankamumas. Jei taip atsitinka, toliau Pi ir Ca 2+ ekskrecija mažėja, padidėja [Pi] kiekis serume, o [Ca 2+ ] kiekis sunormalėja. Bet, tęsiantis kaulų mineralinio audinio rezorbcijai, Ca 2+ ir Pi pasirodo ir išmatose. Dėl Ca 2+ netekimo išsivysto diseminuotoji cistinė kaulų dekalcifikacija, padidėja lūžimų pavojus. Apykaitos sutrikimas kauluose yra susijęs su serumo šarminės fosfatazės aktyvumo padidėjimu. Hiperparatirozės simptomai gali atsirasti asmenims, sergantiems lėtiniu inkstų nepakankamumu. Dėl inkstų ligos sulaikomi fosfatai mažina kalcio jonų koncentraciją plazmoje, skatina parathormono gamybą, dėl to ir liaukos hiperplaziją. Kalcitoninas Tai vienagrandis polipeptidas (molekulinė masė 3600 Da) iš 32 aminorūgščių liekanų. Nustatytos aštuonios skirtingos kalcitonino formos. Gyvavimo puslaikis 2 15 minučių (mažesnis už parathormono). Skirtingai nuo parathormono, kuriam tik 34 N galo aminorūgštys iš 84 yra būtinos biologiniam aktyvumui, visos 32 kalcitonino aminorūgštys yra būtinos jo biologiniam veikimui. Kaip ir parathormono, kalcitonino pasigamina vykstant didesnių pirmtakų hidrolizei. Kalcitonino sekrecija ir veikimo reguliavimas. Pirminė kalcitonino veikimo vieta yra kaulai, o per antrinius mechanizmus jis veikia inkstus. Kalcitonino poveikis sudaro 1/3 stimuliacinio parathormono poveikio adenilatciklazės aktyvumui inkstuose ir kauluose. Kalcitonino sekrecija nenutrūksta esant fiziologinei Ca 2+ koncentracijai kraujyje ir tiesiogiai priklauso nuo [Ca 2+ ] kraujyje. Gliukagonas (kasos hormonas), gastrinas (virškinamojo trakto hormonas) taip pat stimuliuoja kalcitonino sekreciją. Per didelis kalcio kiekis maiste skatina gliukagono sekreciją ir netiesiogiai kalcitonino išsiskyrimą. Svarbiausia kalcitonino funkcija yra neleisti išsivystyti hiperkalcemijai po valgio. Hormonas ją vykdo per kaulų rezorbcijos ir Ca 2+ pasišalinimo iš kaulų slopinimą. Taigi kalcitonino poveikis kaulams yra priešingas parathormono veikimui: kalcitoninas mažina kaulų rezorbciją ir jos lemiamą hipokalcemiją bei hipofosfatemiją, taip pat Ca 2+ ir hidroksiprolino ekskreciją su šlapimu. Padidėjusi fosfatų ekskrecija yra antrinė dėl [Ca 2+ ] pokyčių kraujyje. Nors kalcitonino poveikis kaulams yra priešingas parathormonui, tai nėra antiparathormonas. Du hormonai, matyt, veikia dviejų skirtingų tipų kaulų ląsteles, kurių vienos atsako į kalcitonino veikimą, kitos į parathormono (abu didina camf kiekį kaulų ląstelėse). 340
342 Hormonų klinikinė biochemija ir jų nustatymo reikšmė Laboratoriniais tyrimai Parathormonas (paratiroidinis hormonas, PTH) Tiriamoji medžiaga. Serumas, plazma. Rekomenduojama kartu tirti bendrojo kalcio, jonizuotojo kalcio ir fosforo kiekį. Rekomenduojama reikšmė (pmol/l): serume 1,2 7,3; plazmoje 1,7 9,2; intaktinio plazmoje 0,8 7,8. Diagnostinė vertė. Pirminė hiperparatirozė; antrinė hiperparatirozė (pvz., lėtinės inkstų ligos, paveldimas priklausomumas nuo D vitamino, D vitamino stoka), fluorozė, nugaros smegenų trauma, šeiminis skydliaukės medulinis vėžys, dauginė endokrininė neoplazija. Autoimuninė hipoparatirozė; chirurginė hipoparatirozė, susijusi su skydliaukės pašalinimu, sarkoidozė, neparatiroidinė hiperkalcemija, nesant inkstų nepakankamumo, hipertirozė, hipomagnezemija, laikinoji naujagimių hipokalcemija. Papildoma informacija. Normalus intaktinio parathormono (1 84 aminorūgštys) gyvavimo kraujotakoje puslaikis apie 5 min. Neaktyvieji C galo ir vidurinis fragmentai (53 84, ir aminorūgštys) sudaro apie 90% viso kraujotakoje esančio parathormono. Šie fragmentai šalinami per inkstus ir jų gyvavimo puslaikis 1 2 val. Aminoterminalinio fragmento (1 34 aminorūgštys) gyvavimo puslaikis 1 2 min. Jo koncentracija kraujyje labai maža. Tik intaktinis parathormonas (1 84) ir N galo fragmentas (1 34) pasižymi biologiniu aktyvumu. Be šalinimo per inkstus, intaktinis ir N galo parathormonas šalinami ir kitais būdais. Esant lėtiniam inkstų veiklos nepakankamumui, labai padidėja C galo ir vidurinio fragmentų kiekiai, net jei ir nėra prieskydinių liaukų ligos. Parathormonas nustatomas jau po gimimo ir jo palaipsniui daugėja. Būdingas cirkadinis ritmas: didžiausios reikšmės nustatomos val. ir vėliau nukrinta iki bazinio kiekio 8 val. ryte. Plazmoje jo koncentracija 5 10% mažesnė negu serume. Plazmos kalcio kiekiui sumažėjus iki 0,38 mmol/l, parathormono padaugėja 400%. V: fosfatai, kortikosteroidai, litis, vaistai nuo traukulių. V: cimetidinas, propranololis. Kalcitoninas Tiriamoji medžiaga. Serumas. Rekomenduojama reikšmė. 0,8<10 ng/l. Diagnostinė vertė. Skydliaukės medulinis vėžys; C ląstelių hiperplazija; kai kuriems ligoniams, sergantiems plaučių, krūties, kasos vėžiu, B 12 vitamino stokos anemija, pankreatitu, tiroiditu; esant lėtiniam inkstų nepakankamumui, pseudoparatirozei, alkoholinei cirozei. Gali padidėti nėštumo metu ir sergant gerybinėmis plaučių ligomis. Kalcitoniną ektopiškai gali gaminti įvairių lokalizacijų vėžinės ląstelės, ypač neuroendokrininės kilmės. Tyrimas svarbus vertinant atsaką į gydymą ir numatant ligos pasikartojimą (sergant skydliaukės meduliniu vėžiu); jis gali būti naudojamas sergančiųjų minėtąja vėžio forma šeimos narių atrankiniam tyrimui (20% šių vėžio formų būdinga šeimoms). Papildoma informacija. Kalcitoninas yra peptidinis hormonas, sudarytas iš 32 aminorūgščių grandinės, gaminamas skydliaukės perifolikulinės zonos C ląstelėse. Tai parathormono antagonistas: jis slopina osteoklastų aktyvumą kauluose ir mažina serumo kalcio kiekį. Kalcitonino mažėja su amžiumi, didėja nėštumo ir laktacijos metu. Serume koncentracija yra didesnė negu plazmoje. Kliniškai tyrimas yra vertingas kaip skydliaukės medulinio vėžio žymuo. V: kalcio infuzijos, adrenalinas, estrogenai, gliukagonas, pentagastrinas, geriamieji kontraceptikai. Lipemija ir hemolizė yra nepageidaujamos. 341
343 Kasos sintetinami hormonai Preproinsulinas Proinsulinas C peptidas ir insulinas 37 pav. Insulinas ir C peptidas Kasa yra mišrioji liauka. Jos endokrininė dalis Langerhanso salelių β (arba B) ląstelės, gaminčios insuliną, ir α (arba A) ląstelės, gaminančios gliukagoną. Be to, kasa dar gamina somatostatiną, kuris slopina adenohipofizės somatotropino sekreciją ir yra išskirtas iš kasos salelių D tipo ląstelių, ir kasos audinio F ląstelių citoplazminės granulės kasos polipeptidą. Insulinas tai nedidelės molekulinės masės globulininis polipeptidas (molekulinė masė = 5700 Da). Insulinas Langerhanso salelių b ląstelėse yra sintetinamas proinsulino pavidalu tai vienos grandinės iš aminorūgščių liekanų (priklausomai nuo rūšies) polipeptidas (žmogaus proinsulinas iš 86 aminorūgščių liekanų). Ta dalis, kuri yra pašalinama sekrecijos metu iš proinsulino grandinės, vadinama C peptidu. Proinsulino mrnr transliacijos produktas yra daltonų polipeptidas, kuris vadinamas preproinsulinu (37 pav.). Jis turi papildomas 23 aminorūgščių liekanas. Preinsulino ir proinsulino sintezė vyksta šiurkščiajame endoplazminiame tinkle. Molekulė erdvinę struktūrą, susidarant disulfidinėms jungtims, įgyja tuoj po sintezės. Susintetintas polipeptidas iš šiurkščiojo endoplazminio tinklo į Goldžio aparatą pernešamas vykstant energijos imliam procesui. Jame vyksta fermentinis proteolizinis proinsulino virtimas insulinu. Šį procesą katalizuoja į tripsiną panaši proteazė ir kitas fermentas, kurio specifiškumas panašus į B karboksipeptidazės. Goldžio aparate susiformuoja insulino įsotintos granulės, kurios patenka į citoplazmą ir toliau biochemiškai bręsta, t. y. proinsulinas pagaliau virsta insulinu. Insulinas ir C peptidas sekretuojami ekvimoliniais kiekiais ir aptinkami kraujyje. Sergant kasos b ląstelių adenoma, kraujo serume būna padidėję proinsulino ir insulino kiekiai. Normaliai proinsulino serume aptinkama labai nedaug. Insulino sekrecijos reguliavimas. Insulino sekrecijos greitis priklauso nuo gliukozės koncentracijos kraujyje. Kai gliukozės kiekis kraujyje padidėja, insulino sekrecija skatinama, o kai gliukozės sumažėja slopinama. Gliukozės reguliacinis veikimas susijęs su jau esamos irnr kiekiu, t. y. gliukozė veikia potranskripciniu lygmeniu. Tokie hormonai, kaip gliukagonas, sekretinas, cholecistokininas, somatotropinas ir prostaglandi- 342
344 Hormonų klinikinė biochemija ir jų nustatymo reikšmė nas E 1, didina salelių ląstelių adenilatciklazės aktyvumą ir taip moduliuoja insulino sekreciją. Ciklazės aktyvacija gali paspartinti gliukozės sukeliamą insulino sekreciją. Insulino sekrecija, veikiama gliukozės, priklauso nuo Ca 2+ : jis įeina į Langerhanso salelių ląsteles kartu su gliukoze; pastarųjų koncentracijos abipus membranos greitai susilygina ir salelių ląstelių viduje gliukozė fosforilinama į gliukozės-6-fosfatą tai gliukokinazės kepenyse katalizuojama reakcija; glikolizė labai paspartėja. Šie procesai yra susiję su salelių ląstelių fosfofruktokinazės aktyvumu. Taip susidaro pusiausvyra tarp glikolizės greičio, Ca 2+ patekimo į ląstelę ir insulino sintezės greičio. Priešingai, badaujant mažėja gliukozės koncentracija, slopinama jos apykaita ir ląstelių savybė sintetinti insuliną. Nors insulino sekrecijos greitis priklauso nuo Ca 2+ kiekio, hormono sintezė nuo jo neprikauso. Taip pat vaistai, stimuliuojantys insulino sekreciją, neskatina jo sintezės. Insulino sekrecijos tyrimų duomenimis, tai dvifazis procesas. Iš pradžių yra trumpas staigus sekrecijos suintensyvėjimas, vėliau pastovus lėtesnis sekrecijos didėjimas. Pradinei fazei reikalingas sukaupto insulino išsiskyrimas, antrajai fazei naujai sintetintas insulinas. Kiti fiziologiniai stimulai taip pat skatina insulino išsiskyrimą. Gliukagonas aktyvina adenilatciklazę kasos b ląstelių membranose; su maistu gauti baltymai taip pat skatina insulino sekreciją, kaip ir į veną sulašintos aminorūgštys (ypač L-argininas ir mažiau L-leucinas; arginino injekcijomis yra tiriama insulino gamyba kasoje). Somatotropinas taip pat skatina insulino sekreciją. Daugiau jo išsiskiria iš hipofizės vartojant baltymų ar arginino, leucino. Taigi tie patys dirgikliai, t. y. baltymų sintezės substratai, skatina baltymų sintezės reguliavimui svarbių hormonų išsiskyrimą. Insulino veikimas. Pirminės insulino veikimo ląstelės taikiniai yra raumenų, kepenų ir adipocitai. Tačiau jis veikia ir fibroblastus, limfocitus; sinergiškai su kitais hormonais kitus audinius, pvz., su prolaktinu pieno liaukos audinį. Receptoriai insulinui yra išsidėstę ląstelių taikinių paviršiuje. Tai glikoproteinas (molekulinė masė Da). Insulino prisijungimas prie adipocitų, kepenų, raumenų ir kitų ląstelių receptorių yra sotinantis procesas, priklausantis nuo laiko, temperatūros ir stereochemiškai yra ypač specifiškas insulinui. Proinsulino prisijungimo prie membranų stiprumas (afinitetas) sudaro 1/20 natyvinio insulino, taigi ir jo biologinis aktyvumas atitinkamai yra mažesnis. Insulino molekulės erdvinė struktūra yra labai svarbi kompleksui su receptoriumi susidaryti. Asmenų, kurių audiniai ypač atsparūs insulinui, kraujyje rasta specifinių antikūnų prieš ląstelių paviršiuje esančius receptorius insulinui. Insulino prisijungimas prie ląstelių taikinių receptorių yra procesas, didinantis baltymo sintezės greitį ir kaupimą, taip pat energijos išteklių sintezę ir kaupimą, pirmiausia glikogeno ir lipidų (41 lentelė). 343
345 41 lentelė. Insulino poveikis medžiagų apykaitai Metaboliniai procesai Insulino perteklius Insulino stoka Lipogenezė Baltymų sintezė Glikogeno sintezė Ketogenezė iš riebalų rūgščių Gliukoneogenezė iš aminorūgščių Glikogenolizė Lipolizė skatina; lėtina. Insulino stimuliuojama makromolekulių sintezė yra nepriklausoma nuo jo poveikio gliukozės panaudojimui. Beveik į visas ląsteles gliukozės patekimas priklauso nuo insulino, išskyrus smegenų, eritrocitų, kai kurias kepenų ląsteles, į kurias gliukozės patekimo insulinas nereguliuoja. Insulino poveikis angliavandenių apykaitai. Hiperglikemija ir gliukozurija dėl nepakankamo insulino aprūpinimo atspindi hormono svarbą gliukozės pernašai organizme ir panaudojimui audiniuose. Insulinas skatina angliavandenių, ypač gliukozės, patekimą į ląsteles, kur ji greitai fosforilinama. Dėl to sumažėja gliukozės koncentracija kraujyje, paspartėja ląstelinis heksozių fosfatų glikogeno ir glikolizės produktų susidarymas. Insulinas taip pat veikia gliukozės panaudojimą ląstelėse nepriklausomai nuo jos pernašos. Specifinė mikrosominė kepenų gliukokinazė yra aktyvinama insulino, taip pat glikogensintetazės dėl jų poveikio iš gliukozės-6-fosfato susidaro daugiau glikogeno, o insulinas slopina gliukoneogenezę, mažindamas fermentų, reikalingų gliukozės sintezei iš neangliavandenių (pvz., piruvato), aktyvumą. Poveikis baltymų ir nukleorūgščių sintezei. Insulinas greitai padidina aminorūgščių panaudojimą baltymų sintezei kepenyse ir kituose audiniuose. Paspartėja aminorūgščių pernaša per membraną į ląstelių vidų, didėja baltymų, dalyvaujančių pernašoje, sintezės greitis. Šį insulino poveikį gali slopinti baltymų sintezės inhibitoriai. Kitas insulino poveikis baltymų sintezei tai peptidinio ryšio susidarymo stimuliavimas. Insulinas skatina RNR ir DNR sintezę, kartu proliferaciją, reikalingą augimo ir diferenciacijos procesams. Poveikis lipidų apykaitai. Insulinas netiesiogiai skatina lipogenezę iš angliavandenių kepenyse ir kituose audiniuose, mažo tankio lipoproteinų, fosfolipidų sintezę. Gliukozės anglies atomai verčiami riebalų rūgštimis ir triacilgliceroliais, o riebalų rūgščių išsiskyrimas iš audinių yra slopinamas. Dėl to didėja riebalų atsargos. Lipolizę slopinantį insulino veikimą lemia camf kiekio sumažėjimas. 344
346 Hormonų klinikinė biochemija ir jų nustatymo reikšmė Insulino stoka. Trūkstant insulino, susergama cukriniu diabetu (diabetes mellitus). Sutrikus gliukozės panaudojimui energijos poreikis kompensuojamas suintensyvėjusia lipidų ir baltymų apykaita (žr. 10 pav.). Taip pat intensyvėja gliukoneogenezė iš aminorūgščių, dėl to padidėja azoto darinių ekskrecija su šlapimu, o baltymų sintezė slopinama, nes aminorūgštys silpniau jungiasi į baltymus. Dauguma gliukozės, susidariusios gliukoneogenezės būdu, išskiriama su šlapimu, nes trūksta insulino. Susidaro mažiau piruvato, reikalingo oksaloacetato sintezei. Tada daugiau acetil-koa susidaro iš riebalų. Dėl suintensyvėjusios riebalų mobilizacijos iš atsargų atsiranda lipemija ji skatina kepenų suriebėjimą. Padidėja ketoninų medžiagų sintezė; kai ji viršija sunaudojimą, išsivysto ketozė. Insulino stoka gali išsivystyti dėl kelių priežasčių: 1. Nepakankama insulino sintezė ją sukelia kasos audinio degeneracija, kuri gali būti pirminė ir antrinė (pastaroji dėl nuolatinės insulino hipersekrecijos, užsitęsus hiperglikemijai). Kadangi insulino sekrecija priklauso nuo gliukozės kiekio kraujyje, veiksniai, didinantys gliukozės kiekį, skatins insulino sekreciją. Hiperglikemija gali būti dėl suintensyvėjusios gliukoneogenezės, dėl padidėjusios AKTH ar kortikosteroidų sekrecijos, pavyzdžiui, esant navikui. Hipofizės somatotropinas irgi gali padidinti gliukozės kiekį, o užsitęsus šio hormono sekrecijai, gali atsirasti antriniai destrukciniai kasos salelių b ląstelių pokyčiai. 2. Pagreitėjęs insulino skaidymas. Insulino aktyvumas krinta dėl jo proteolizės (pvz., tripsino poveikio, todėl jį reikia vartoti parenteraliai arba per os liposomų pavidalu). Veikiant karboksipeptidazei, atskeliamas B grandinės C galo alaninas, tačiau tai mažai keičia hormono aktyvumą; atskilus A grandinės C galo asparaginui, aktyvumas prarandamas. Žmogui į kraują suleisto insulino gyvavimo puslaikis 40 min., nes kepenų ir kitų audinių fermentai jį inaktyvina. Šiame procese svarbiausi du fermentai: glutationinsulintranshidrogenazė nutraukia disulfidines jungtis atsiskiria insulino A ir B grandinės, o tada jas veikia proteazė insulinazė. 3. Insulino antagonistų ir inhibitorių poveikis. Skiriami du insulino antagonistų tipai, dėl kurių išsivysto funkcinis insulino nepakankamumas. Vienas jų gydymo insulinu padarinys. Sergančiųjų diabetu ir gydytų ne žmogaus insulinu kraujyje atsiranda antikūnų, kurie suriša insuliną. Jų randama kraujo plazmos β ir γ globulinų frakcijose. Dėl to kai kuriems diabeto ligoniams būdingas silpnesnis atsakas į suleistą insuliną. Antigeninis insulino aktyvumas taip pat paaiškina atsparumą jaučio insulinui (jį ilgiau vartojant). Kitas antagonistų tipas, mažinantis insulino efektyvumą (tiek endogeninio, tiek egzogeninio) ir randamas sergančiųjų diabetu kraujyje, yra susijęs su antikūnų prieš insulino receptorius susidarymu. 345
347 Hiperinsulinizmas. Esant salelių ląstelių navikams, didėja insulino sintezė ir sekrecija išsivysto hiperinsulinizmas. Jam būdinga hipoglikemija ne tik dėl padidėjusio gliukozės patekimo į ląsteles, bet ir dėl sumažėjusio substratų, reikalingų gliukoneogenezei (pvz., aminorūgščių), patekimo į kepenis; greitas gliukozės kiekio sumažėjimas aktyvina vegetacinę nervų sistemą ir skatina adrenalino išsiskyrimą. Dėl to ligonis prakaituoja, jį krečia šaltis, jaučia nuovargį, alkį, silpnumą. Užsitęsus hipoglikemijai, sumažėja gliukozės patekimas į smegenis, dėl to atsiranda nervų sistemos pažeidimo simptomų. Gliukagoną sekretuoja kasos salelių a ląstelės. Dėl jo poveikio kraujyje didėja gliukozės koncentracija (skatina glikogenolizę kepenyse). Taigi insulinas ir gliukagonas veikia reakcijas priešingomis kryptimis. Toks ryšys yra ir tarp parathormono bei kalcitonino prieskydinių liaukų hormonų. Kiekviena hormonų pora turi dvigubą grįžtamuoju ryšiu veikiantį reguliavimo mechanizmą, kai viena pora reguliuoja gliukozės homeostazę (kasa), o kita kalcio ir fosfatų apykaitą (prieskydinės liaukos). Somatostatinas. Pirmiausia somatostatinas buvo išskirtas iš pogumburio. Jis turi slopinamąjį poveikį adenohipofizės somatotropino sekrecijai. Somatostatinas taip pat gaminamas kitose vietose: skrandžio ir žarnų gleivinėje ir kasoje joje somatostinas sintetinamas salelių D ląstelėse. Adenohipofizės somatotropinas skatina insulino ir gliukagono sekreciją, o kasos somatostatinas yra šių kasos hormonų išsiskyrimo inhibitorius. Taip pat jis slopina gastrino ir sekretino sekreciją. Laboratoriniai tyrimai Insulinas Tiriamoji medžiaga. Serumas. Rekomenduojama reikšmė pmol/l (6 29,1 µu/ml). Diagnostinė vertė. Insulinoma (kasos salelių navikas), nuo insulino nepriklausomas (II tipo) cukrinis diabetas, kepenų ligos, akromegalija, Kušingo sindromas, šeiminis fruktozės ir galaktozės netoleravimas, nutukimas, slaptas insulino ar geriamųjų hipoglikeminių medžiagų vartojimas. Nuo insulino priklausomas cukrinis diabetas (I tipo), hipofizės hipofunkcija. Papildoma informacija. Klinikine prasme insulino kiekio matavimas nėra labai vertingas rodiklis, išskyrus badavimo hipoglikemijos diagnostiką. Esant badavimo hipoglikemijai ir didelei serumo insulino koncentracijai, galima įtarti insulinomą. V: aminorūgštys, chlorpropamidas, fruktozė, gliukagonas, gliukozė, augimo hormonas, levadopa (gydant parkinsonizmą), nikotino rūgštis (didelės dozės), geriamieji kontraceptikai, pankreoziminas (į veną), fentolaminas (infuzijos), prednizolonas, chinidinas, sekretinas (į veną), spironolaktonas, sacharozė, tolazamidas, tolbutamidas. V: β adrenoblokatoriai (pvz., propranololis), asparaginazė, bezafibratas, kalcitoninas, chlorpropamidas (kai didelė pradinė koncentracija), cimetidinas, klofibratas, etakrino rūgštis, etanolis, eteris, furozemidas, metforminas, nifedipinas, fenforminas, fenobarbitalis, fenitoinas, tiazidiniai diuretikai. 346
348 Hormonų klinikinė biochemija ir jų nustatymo reikšmė C peptidas Tiriamoji medžiaga. Serumas. Rekomenduotina reikšmė pmol/l (1,1 5 ng/ml). Diagnostinė vertė. Insulinoma, kasos ar β ląstelių transplantacija, geriamųjų hipoglikeminių vaistų vartojimas, inkstų nepakankamumas, nuo insulino nepriklausomas (II tipo) cukrinis diabetas. Hipoglikemija vartojant insuliną, radikalus kasos pašalinimas, nuo insulino priklausomas (I tipo) cukrinis diabetas. Kitos indikacijos: vertinant β ląstelių funkciją ir endogeninę insulino sekreciją skiriant egzogeninio insulino ar kai cirkuliuojantys antikūnai prieš insuliną trukdo nustatyti insuliną. C peptido tyrimas prieš ir po stimuliacijos gliukagonu gali padėti įvertinti cukrinio diabeto gydymą insulinu. Papildoma informacija. Nustatyta stipri koreliacija tarp insulino ir C peptido kiekių serume. C peptidas yra biologiškai neaktyvus. Insulinas nesukelia kryžminės reakcijos nustatant C peptidą, o proinsulinas gali reaguoti; tačiau jis sudaro <1% C peptido kiekio. Serume molinis C peptido ir insulino santykis yra >5 dėl ilgesnio C peptido gyvavimo puslaikio, palyginti su insulinu (atitinkamai 20 min. ir 5 10 min.). Be to, didžiausias insulino kiekis metabolizuojamas kepenyse, o C peptido didžiausias kiekis suskaidomas inkstuose ir iš dalies šalinamas su šlapimu. V: geriamieji kontraceptikai. Antinksčių sintetinami hormonai Kiekvieną antinkstį sudaro šerdis, išsivysčiusi iš nervinio audinio (tai simpatinės nervų sistemo dalis) ir žievė, kilusi iš liaukinio audinio. Šių dviejų antinksčių dalių hormonai skiriasi savo veikimu, tačiau šerdies hormonai gali veikti žievės sekrecinį aktyvumą per pogumburio ir posmegeninės liaukos reguliavimą, o žievės hormonai veikia kai kurių šerdies hormonų sintezės greitį. Katecholaminai antinksčių šerdies hormonai Iš antinksčių šerdies yra išskirti du hormonai adrenalinas ir noradrenalinas (epinefrinas ir norepinefrinas). Žmogaus organizme noradrenalinas sudaro apie 10% viso antinksčių šerdies hormonų kiekio. Katecholaminų sintezė: Tirozinas Dihidroksifenilalaninas (dopa) Dihidroksifeniletilaminas (Dopaminas) Noradrenalinas Adrenalinas Pirmuoju etapu fenilalaninas kepenyse hidroksilinamas į tiroziną. Sergant fenilketonurija, dėl fermento fenilalaninhidroksilazės stokos kraujo plazmoje adrenalino koncentracija yra maža. Tirozino oksidaciją į 3,4-dihidroksifenilalaniną (dopa) katalizuoja tirozinhidroksilazė. Šios reakcijos greitį reguliuoja nuo camf priklausoma proteinkinazė (fermentas fosforilinamas ar defosforilinamas). Tai greitį ribojantis 347
349 šių hormonų sintezės etapas. Tirozinhidroksilazės yra smegenyse, simpatinėje nervų sistemoje, o antinksčių žievėje jos yra labai nedaug. Aromatinių L aminorūgščių dekarboksilazė, randama inkstuose, kepenyse, antinksčių šerdyje, katalizuoja dopa dekarboksilinimą į 3,4-dihidroksifeniletilaminą (dopaminą). Šio fermento aktyvumui reikalingas kofaktorius piridoksalfosfatas. Dopaminas verčiamas norepinefrinu dalyvaujant dopamin-β-hidroksilazei, kurios sudėtyje yra Ca 2+, o kofaktorius yra askorbo rūgštis ar kita redukuojančioji medžiaga. Galutinis adrenalino susidarymo etapas tai metilinimo reakcija katalizuojant feniletanolamin-n-metiltransferazei. Fermentą slopina reakcijos produktas adrenalinas. Slopinimas vyksta jau esant normaliai antinksčių šerdyje hormono koncentracijai. Adrenalino ir noradrenalino apykaita. Nors žmogaus antinksčių šerdis turi nuo 3 iki 10 kartų daugiau adrenalino negu noradrenalino, vidutinė adrenalino koncentracija plazmoje yra <100 ng/l, noradrenalino <600 ng/l, dopamino <100 ng/l. Su šlapimu per 24 val. išsiskiria <20 µg adrenalino, <104 µg noradrenalino ir <600 µg dopamino. Abu hormonai yra greitai metabolizuojami (daugiausia kepenyse) ir inaktyvinami trimis būdais, vykstant metilinimo reakcijai, oksidaciniam deamininimui (katalizuoja monoaminooksidazė) ir konjugacijai. Adrenalinas daugiausia inaktyvinamas vykstant metilinimo reakcijai; susidarę jo metabolitai išskiriami su šlapimu: tai 3-metoksi-4-hidroksimigdolo rūgštis, 3-metoksiadrenalinas (metanefrinas) ir 3-metoksi-4-hidroksifenilglikolis. Su šlapimu, tačiau po mažiau, taip pat šalinami noradrenalinas ir adrenalinas. Kai kurie šių metabolitų randami šlapime ir tulžyje kaip laisvi junginiai ar kaip sulfatai bei gliukoziduronidai; galimas ir jų acetilinimas. Adrenalino ir noradrenalino veikimas. Antinksčių šerdies hormonai veikia daugelį organizmo funkcijų, o veikimo mechanizmas susijęs su adenilatciklazės stimuliacija audiniuose taikiniuose (42 lentelė). 42 lentelė. Katecholaminų veikimas Audinys Kepenys Griaučių raumenys Širdis Seilių liauka Gimda Pagrindinis poveikis Suintensyvėjusi glikogenolizė, gliukoneogenezė Suintensyvėjusi glikogenolizė Sustiprėjęs inotropinis poveikis Suintensyvėjusi amilazės sekrecija Sustiprėjusi relaksacija Dėl adrenalino poveikio ląstelėse taikiniuose didėja ląstelinio camf kiekis, aktyvinama proteinkinazės vykdoma reakcija, kuri katalizuoja specifinių baltymų fosforilinimą citoplazmoje, endoplazminiame tinkle ir membranoje; suaktyvintos proteinkinazės translokacija į branduolį skatina chromosominių baltymų fosforilinimą, o tai aktyvina RNR polimerazės transkripciją. 348
350 Hormonų klinikinė biochemija ir jų nustatymo reikšmė! Poveikis lipidų apykaitai. Katecholaminai skatina lipolizę, didina laisvųjų riebalų rūgščių kiekį kraujyje dėl padėjusio laisvųjų riebalų rūgščių išsiskyrimo iš riebalinio audinio. Kartu padidėja ir O 2 sunaudojimas. Esant feochromocitomai dėl antinksčių šerdies hiperfunkcijos laisvųjų riebalų rūgščių koncentracija kraujyje gali viršyti normą kelis šimtus kartų. Poveikis širdžiai ir griaučių raumenims. Adrenalinas, suleistas į veną, padidina kraujospūdį dėl arteriolių vazokonstrikcijos, dėl to padažnėja širdies plakimas ir pulsas, širdies darbo našumas. Nedidelėmis dozėmis adrenalinas greičiau išplečia, negu sutraukia, griaučių raumenų kraujagysles, taip pat koronarines bei vidaus organų kraujagysles dėl to padidėja kraujo priplūdimas. Adrenalinas skirtingai veikia lygiuosius raumenis: jis atpalaiduoja virškinamojo trakto, gimdos, bronchų raumenis, o sutraukia skrandžio prievarčio, klubinės ir aklosios žarnos raukus. Noradrenalinas lygiuosius raumenis veikia silpniau negu adrenalinas, neatpalaiduoja bronchų raumenų, padidina sistolinį bei diastolinį kraujospūdį dėl padidėjusio periferinio pasipriešinimo, tačiau menkai pagerina širdies darbą (43 lentelė). 43 lentelė. Adrenalino ir noradrenalino intraveninių infuzijų poveikio palyginimas Indeksas Adrenalinas Noradrenalinas Širdies susitraukimų dažnis Širdies darbo našumas Sistolinis kraujospūdis Diastolinis kraujospūdis Bendras periferinis pasipriešinimas O 2 sunaudojimas Gliukozės kiekis kraujyje Laktatų kiekis kraujyje Neesterifikuotų riebalų rūgščių kiekis kraujyje Poveikis centrinei nervų sistemai Poveikis eozinofilų skaičiaus mažėjimui + padidėja; sumažėja; 0 nekinta ,0, , ,+ 0,+ 0, Antinksčių šerdies hiperfunkcija. Žmogaus antinksčių šerdies hiperfunkcija išsivysto dėl chromafininio audinio naviko, vadinamo feochromocitoma. Esant šiam navikui būdinga hipertenzija, padidėjęs pagrindinės apykaitos greitis, gliukozurija. Adrenalino ir noradrenalino kiekis plazmoje padidėja daugiau negu 500 kartų, taip pat laisvųjų riebalų rūgščių kiekis plazmoje, o šlapime padaugėja šių hormonų ir jų metabolitų. Jei navikas yra ekstramedulinis, tai noradrenalinas sudaro 90% viso šerdies hormonų kiekio, o jei medulinis tai abiejų hormonų kiekis yra vienodas. 349
351 Antinksčių žievės hormonai Antinksčių žievės hormonų sintezė, jos reguliavimas. Antinksčių žievėje mikroskopiškai yra skiriamos trys zonos (tarp jų aiškių ribų nėra), kurių ląstelėse sintetinami skirtingi hormonai: 1) išorinė kamuolinė zona (zona glomerulosa) gamina mineralkortikoidą aldosteroną; 2) pluoštinė zona (zona fasciculata) gamina gliukokortikoidus, kurių pagrindinis yra kortizolis, mažiau gaminama kortikosterono ir 11-deoksikortikosterono; 3) tinklinė zona (zona reticularis) gamina lytinius hormonus, svarbiausi antinksčių androgenai: androstenedionas ir dehidroepiandrosteronas, ir labai nedaug estrogenų bei progesterono. Pagal veikimą antinksčių žievės hormonai skirstomi į tris grupes: 1) veikiantys angliavandenių, baltymų ir riebalų apykaitą tai gliukokortikoidai; 2) veikiantys vandens ir mineralinių medžiagų apykaitą tai mineralkortikoidai; 3) lytiniai hormonai, analogiški lytinių liaukų hormonams. Pirmųjų dviejų grupių hormonai vadinami kortikosteroidais, nes jie specifiški tik antinksčių žievei. Žmogaus antinksčių žievė per parą normaliai išskiria apie mg kortizolio, 2 4 mg kortikosterono ir µg aldosterono (kortizolis ir kortikosteronas sudaro apie 60% visų žievėje sintetinamų hormonų). Acetatas Cholesterolis Pregnenolonas 17aOH Pregnenolonas Dehidroepiandrosteronas (DHEA) Progesteronas 17aOH Progesteronas Androstenedionas 11-deoksikortikosteronas 11-deoksikortizolis Kortikosteronas Kortizolis 18-hidroksikortikosteronas Aldosteronas 38 pav. Antinksčių žievės hormonų sintezė 350
352 Hormonų klinikinė biochemija ir jų nustatymo reikšmė Cholesterolis yra žievės steroidinių hormonų pirmtakas (38 pav.), ir jiems yra būdinga 17 anglies atomų turinti ciklopentanoperhidrofenantreno ciklinė struktūra. Cholesterolio koncentracija antinksčiuose yra antroje vietoje po nervinio audinio ir beveik visas jis yra esterifikuotas. Antinksčių žievėje yra daug MTL receptorių ir tai labai pagerina cholesterolio patekimą į ląsteles. Antinksčiuose taip pat yra didžiausia organizme askorbo rūgšties koncentracija: ji reikalinga NADF redukcijai, nes vykstant hormonų sintezei jis oksiduojasi. Steroidų sintezėje dalyvauja keturių rūšių fermentai: 1) hidoksilazės: jos vandenilį (H) pakeičia hidroksilo (OH) grupe ir yra specifiškos kiekvienam steroidui; joms būtini bendrai veikiantys veiksniai NADF ir molekulinis deguonis, vadinasi, reakcija vyksta tik aerobinėmis sąlygomis; 2) dehidrogenazės jos katalizuoja vandenilio pernešimą, t. y. oksidacijos ir redukcijos reakcijas; 3) desmolazės jos atskelia šonines grandines; pavyzdžiui, dalyvaujant 20,22-desmolazei, cholesterolis verčiamas pregnenolonu; 4) izomerazės jos katalizuoja dvigubųjų jungčių perkėlimą; pavyzdžiui, tokiu būdu pregnenolonas virsta progesteronu. Antinksčių žievės steroidinių hormonų sintezė prasideda adrenokortikotropiniam hormonui aktyvinant adenilatciklazę pasigamina camf; ši aktyvina glikogenofosforilazę. Susidaręs gliukozės-6-fosfatas pasuka fosfogliukonato susidarymo keliu ir gaminamas hidroksilinimo reakcijoms reikalingas NADFH 2. Taigi AKTH veikia per camf aktyvaciją, o camf per kai kuriuos fermentus skatina gliukozės-6- fosfato susidarymą iš glikogeno. Veikiant adrenokortikotropiniam hormonui aktyvinama cholesterolesterazė, dėl kurios poveikio cholesterolio esteriai hidrolizuojami į aktyvią cholesterolio formą laisvąjį cholesterolį ir riebalų rūgštis. Minėtoji desmolazė cholesterolį verčia 21 anglies (C) atomą turinčiu pregnenolonu, kuris, veikiamas kitų fermentų, verčiamas progesteronu. Toliau veikiant hidroksilazėms (17α-hidroksilazei arba (ir) 21βhidroksilazei), vyksta oksidacijos reakcija ir susidaro hidroksilo grupės prie C-21, C-17 ir C-11 anglies atomų. Pasigaminęs produktas hormonas priklauso nuo to, kuriose antinksčių žievės ląstelėse vyksta reakcija, ir fermento specifiškumo. Nors kortizolis yra svarbiausias gliukokortikoidas, šį aktyvumą turi ir mineralkortikoidų apykaitos kelyje pasigaminęs kortikosteronas. Svarbiausias mineralkortikoidas yra aldosteronas (žr. 38 pav.). Sekrecinį antinksčių žievės aktyvumą skatina AKTH, ypač veikdamas kortikosterono ir kortizolio gamybą, o aldosterono sekrecija mažiau priklauso nuo hipofizės. Kortikosterono ir kortizolio sekrecijos reguliavimą veikiant AKTH kontroliuoja pogumburio paraventrikulinio branduolio neuronų sekretuojamas adrenokortikotropinį hormoną atpalaiduojantis hormonas (39 pav.). Paros ritmas (didžiausia sekrecija yra 4 8 val. ryte, o dienos metu sumažėja), taip pat nemažai nespecifinių streso dirgiklių, kurie veikia nervinį aktyvumą, didina antinksčių steroidinių hormonų 351
353 Paros ritmas Stresas: fizinis emocinis cheminis (pvz., hipoglikemija) + Pogumburis Kortikotropiną atpalaiduojantis hormonas + Posmegeninė liauka AKTH + Antinksčių žievė Kortizolis + slopina skatina 39 pav. Pogumburio, posmegeninės liaukos ir antinksčių žievės sąveikos reguliacija: AKTH adrenokortikotropinis hormonas (adrenokortikotropinas) kiekį kraujyje. Pastarieji, veikdami pogumburį, grįžtamojo ryšio slopinimo principu reguliuoja savo sekrecijos greitį (šis greitis yra atvirkščiai proporcingas antinksčių žievės hormonų kiekiui). Pavyzdžiui, chirurginė trauma, pirogenai, hipoglikemija, kraujavimas gali staigiai padidinti AKTH ir kartu kortizolio sekreciją. Antinksčių kamuolinėje zonoje vyksta aldosterono sintezė, kuri nepriklauso nuo kitų žievės hormonų sintezės. Mineralkortikoidų sintezės kelias skiriasi nuo gliukokortikoidų kelio, nes čia nedalyvauja fermentas 17α-hidroksilazė (kamuolinėse ląstelėse šio fermento nėra); galutiniame sintezės etape, vykstant hidroksilinimo reakcijai, susidaro aldosteronas. Jo sekrecijos reguliavimas yra sudėtingesnis už kortizolio ir kortikosterono sekreciją, nes jai turi įtakos daug veiksnių: AKTH, augimo hormonas, renino ir angiotenzino sistema, plazmos Na + ir K + koncentracijos (aldosterono sekrecija kinta atvirkščiai, negu [Na + ]). Pirminis renino, kuris yra proteolizinis fermentas, sekrecijos dirgiklis yra sumažėjusi perfuzija jukstaglomeruliniame aparate ir neigiamas natrio balansas. Veikiant dirgikliui, reninas hidrolizuoja substratą angiotenzinogeną į angiotenziną I, o pastarasis greit paverčiamas angiotenzinu II, kuris yra galingas vazokonstriktorius ir skatina aldosterono gamybą. Renino injekcijos didina aldosterono sekreciją ir K + kiekį plazmoje. Antinksčių tinklinėje zonoje, kaip jau minėta, gaminami ir sekretuojami androgenai, progesteronas ir estrogenai, kurie gaminami ir lytinėse liaukose. Tai steroidai, 352
354 Hormonų klinikinė biochemija ir jų nustatymo reikšmė kurie turi 17 ar 18 anglies atomų ir hidroksilo grupę 17 padėtyje. C-17 junginiai, kurie turi nesotųjį A ciklą, yra estrogenai, o C-18 steroidai, kurie neturi šio ciklo, yra androgenai. Androgenams priklauso androstenedionas, testosteronas (tai aktyviausias androgenas), dehidroepiandrosteronas (DHEA, pastarojo susintetinama daugiausia) bei 11β-hidroksiandrostenedionas. Ta DHEA dalis, kuri nėra panaudojama androstenediono sintezei, kepenyse ar antinksčiuose yra verčiama dehidroepiandrosterono sulfatu (DHEAS), kuris nėra aktyvus hormonas, tačiau, netekęs sulfo grupės, vėl tampa aktyvus. Iš androstenediono ir moterų, ir vyrų antinksčiuose, taip pat periferiniuose audiniuose (daugiausia riebaliniame audinyje, kepenyse, odoje) sintetinamas testosteronas. Iš antinksčių žievės androgenų sintetinami moteriškieji lytiniai hormonai estrogenai. Ir moterų, ir vyrų periferiniuose audiniuose, taip pat moterų kiaušidėse ir pieno liaukose iš DHEA sintetinamas moteriškasis lytinis hormonas β estradiolis; pastarasis moterų organizme taip pat gaminamas iš antinksčių žievės testosterono. Moterų periferiniuose audiniuose iš androstenediono gaminamas estronas. Antinksčiuose gaminamų estrogenų (estrono) bei progesterono kiekiai praktiškai yra menki. Trūkstant AKTH, kuris skatina pluoštinę bei tinklinę zonas, pastarosios atrofuoja, o kamuolinė zona, kurią labiausiai veikia renino ir angiotenzino sistema, išlieka. Padaugėjus AKTH, didėja lipazės aktyvumas, dėl to antinksčių žievėje riebalų kiekis sumažėja. Tada periferiniuose audiniuose skatinama triacilglicerolių hidrolizė, padidėja riebalų rūgščių išsiskyrimas į kraują, vystosi transportinė hiperlipidemija. Antinksčių steroidinių hormonų pernaša su krauju ir inaktyvinimas. Apie 90% kraujyje esančio kortizolio yra susijungusio su kraujo baltymais, o likęs yra laisvas. Didžiausia kortizolio dalis kraujyje yra prisijungusi prie specifinio α 1 globulino transkortino (kortikosteroidus sujungiančio globulino), kuris turi vieną kortizolį sujungiančią vietą. Šis baltymas taip pat sujungia kortikosteroną. Tokiame junginyje kraujyje esantis hormonas yra paruoštas veiklai, be to, jis nėra inaktyvinamas kepenyse jį konjuguojant, taip pat tokios formos nėra šalinamas su šlapimu. Nedaug jo yra prisijungusio prie albumino. Kortikosteroidai, esantys junginyje su transkortinu, yra neaktyvūs. Aldosteroną perneša albuminai ir tik po labai nedaug transkortinas. Transkortinas gaminasi kepenyse (koncentracija sumažėja dėl kepenų ligų, nefrozės, o padidėja veikiant skydliaukės hormonams, estrogenams). Svarbiausia steroidinių hormonų katabolizmo vieta yra kepenys; silpna metabolinė transformacija taip pat galima inkstuose bei virškinamajame trakte. Antinksčių žievės hormonų metabolitai susidaro vykstant redukcijos, oksidacijos, konjugacijos (dažniausiai su gliukorono ar sieros rūgštimis) ir kitoms reakcijoms. Taip per biochemines reakcijas prarandamas biologinis hormonų aktyvumas. Gliukokortikoidai po redukcijos reakcijos virsta dihidrodariniais ir tetrahidrodariniais, kurie konjuguojami su gliukurono (daugiausia) ar sieros rūgštimis ir pašali- 353
355 nami su tulžimi į žarnyną, po to su šlapimu (apie 70%), išmatomis (apie 20%), per odą (10%). Kortizolis po oksidacijos virsta kortizonu. Šis ir kiti 95% kortizolio metabolitų yra, kaip minėta, konjuguojami ir ekskretuojami. Su šlapimu išsiskiria apie 1% nepakitusio kortizolio. Aldosteronas yra redukuojamas, po to jungiasi su gliukurono rūgštimi ir didžiausia susidariusio tetrahidroaldosterono gliukuronido dalis išskiriama pro inkstus. Dalis metabolitų, kurie išskiriami su tulžimi, gali būti reabsorbuojami iš žarnyno į vartų venos sistemą. Šalinamų kortikosteroidų kiekį rodo 17-hidroksikortikosteroidų tyrimas šlapime. Šiuo tyrimu įvertinama 11-deoksikortizolio, kortizolio ir jo metabolito kortizono šalinimas. Pagrindinė androgenų metabolinės transformacijos vieta taip pat yra kepenys. Veikiant fermentui 5α-reduktazei, testosteronas yra metabolizuojamas į kitą biologiškai aktyvų androgeną dehidrotestosteroną. Dehidroepiandrosteronas (DHEA) kepenyse bei inkstuose yra konjuguojamas su sieros rūgštimi ir šalinamas su šlapimu. Moterų kraujyje jo koncentracija yra 0,9 11,7, vyrų 2,2 15,2 mmol/l. Kiti testosterono metabolitai yra androsteronas, etiocholanolonas, taip pat jų konjugavimo su gliukurono ar sieros rūgštimis produktai. Šie konjugatai, šalinami su tulžimi, šlapimu, yra tirpūs vandenyje ir biologiškai neaktyvūs. Kitos rūšies androgenų transformacija gali irgi vykti kepenyse, taip pat antinksčiuose, sėklidėse, prostatoje. Dauguma su šlapimu šalinamų androgenų metabolitų yra 17-ketosteroidai ir jų nustatytas kiekis yra svarbus steroidinių hormonų apykaitos rodiklis. 17-ketosteroidai. Kadangi nemažai testosterono metabolitų šlapime turi keto grupę prie 17 anglies atomo, tai šios medžiagos priskiriamos 17-ketosteroidams, ir jų koncentracija šlapime yra svarbus endogeninės androgeninių hormonų gamybos rodiklis. Moterų organizme steroidus, turinčius C-17 padėtyje keto grupę, sekretuoja antinksčiai. Vyrų antinksčiai gamina du trečdalius šių medžiagų, o kitą dalį sėklidės. Taigi kai kurie testosterono metabolitai, sudarantys didelę frakciją plazmoje ir šlapime, neturi 17-keto grupės, pavyzdžiui, dihidrotestosteronas ir epitestosteronas, ir jie nebus išmatuoti kaip 17-ketosteroidai, o androsteronas ir dehidroepiandrosteronas bus išmatuoti kaip 17-ketosteroidai, kaip ir etiocholanolonas, nors pastarasis nepasižymi androgeninėmis savybėmis. Estrogenai, nors ir turi keto grupę C-17 padėtyje, nebus išmatuoti kaip 17-ketosteroidai, nes ekstrakcijos metu pašalinami. 17-ketosteroidų tyrimo metodai yra paremti jų reakcija su m-dinitrobenzenu šarminiame tirpale, susidarant purpurinei spalvai. 17-ketosteroidų ekskrecija per dieną rodo steroidų, sekretuojamų tiek lytinėse liaukose, tiek antinksčiuose, metabolizmą. Sveikos suaugusios moters 17-ketosteroidų ekskrecija per dieną yra 4 17 mg ir sudaro 2/3 vyrų organizme išskiriamo kiekio (6 28 mg) tai antinksčių žievės kortikosteroidų (androgenų ir gliukokortikoidų) metabolitai. Vyrų 17-ketosteroidų 1/3 yra sėklidžių androgenų, 2/3 antinksčių androgenų ir gliukokortikoidų kilmės. Iki subrendimo 17-ketosteroidų ekskrecija sudaro 1/3 suaugusiųjų lygio. 354
356 Hormonų klinikinė biochemija ir jų nustatymo reikšmė Tie 17-ketosteroidai, kurie yra gauti iš antinksčių žievės hormonų, paprastai turi hidroksilo ar keto grupių, t. y. deguonies atomą ties 11 anglies atomu, ir vadinami 11-oksi-17-ketosteroidais. Santykinė 11-deoksi-17-ketosteroidų ir 11-oksi-17-ketosteroidų koncentracija šlapime leidžia nustatyti santykinio sekrecinio sėklidžių ir antinksčių žievės aktyvumo (atitinkamai) indeksą. Antinksčių šimte mililitrų veninio kraujo yra apie 240 µg kortizolio ir 80 µg korti kosterono. Kortizolio sekrecija yra cirkadinė ir kiekis periferiniame kraujyje svyruoja: 8 10 val. yra didžiausias ir siekia 5 25 µg/100 ml, o apie 20 val. ji yra 2 12 µg/100 ml. Kepenų ligos sutrikdo aktyvių antinksčių steroidinių hormonų apykaitą jų kiekis gali smarkiai padidėti. Antinksčių žievės hormonų poveikis ir reikšmė. Antinksčių žievės hormonai išsiskiria plačiu biocheminiu ir fiziologiniu veikimu, ir dėl jų nepakankamumo sutrinka įvairių organų veikla (43 lentelė). Kortizolis (kaip svarbiausias gliukokortikoidas): skatina baltymų katabolizmą; veikia gliukoneogenezę: didėja gliukozės koncentracija kraujyje bei glikogeno kepenyse, intensyvėja glikogenolizė kepenyse, mažėja gliukozės panaudojimas; slopina glikozaminoglikanų (mukopolisacharidų) sintezę; veikia riebalų sintezę ir pasiskirstymą; veikia ląsteles ir audinius: išryškėja priešuždegiminis, imunosupresinis, antialerginis veikimas; būdinga limfopenija dėl limfinio audinio irimo, eozinopenija, o eritropoezė skatinama; keičiasi ląstelių membranų pralaidumas (ypač mažėja jų pralaidumas vandeniui); skrandyje didėja druskos rūgšties ir pepsino sekrecija. Aldosteronas (kaip svarbiausias mineralkortikoidas) reguliuoja elektrolitų apykaitą: organizme sulaiko natrio jonus bei vandenį; skatina kalio jonų išsiskyrimą; didina kraujospūdį. Androgenai (kaip svarbiausi lytiniai hormonai): anaboliškai veikia baltymų apykaitą ir taip skatina augimą ir brendimą, ypač kaulų ir raumenų. Kortizolis veikia visas minėtas funkcijas, šiek tiek mažiau tik elektrolitų ir vandens apykaitą. Aldosteronas pirmiausiai veikia vandens ir elektrolitų apykaitą, o kitas funkcijas jis aktyvina silpniau, jo aktyvumas sudaro iki 1/3 kortizolio aktyvumo. Kortikosteronas veikia visas funkcijas, bet silpniau negu du pirmiau minėtieji steroidai (44 lentelė). 355
357 43 lentelė. Antinksčių žievės veiklos nepakankamumo sukeliami pokyčiai Pakitimo prigimtis Kraujo serume sumažėja [Na + ], [Cl - ] ir padaugėja [K + ] Hemokoncentracija Acidozė Hipoglikemija badaujant Padidėjęs šlapalo kiekis kraujyje Limfocitozė Eozinofilija Anemija Pakitimo esmė Sutrikusi inkstų funkcija, kurią rodo sutrikusi Na + ir Cl - reabsorbcija kanalėliuose Vandens netekimas per inkstus, kartu netenkant ir elektrolitų Sutrikęs Na + K + H + keitimosi inkstuose mechanizmas Sumažėjęs glikogeno kiekis kepenyse badaujant, sumažėjusi gliukoneogenezė ir padidėjęs angliavandenių naudojimas Inkstų funkcijos sutrikimas Susilpnėjęs limfocitolizinis 11-oksikortikosteroidų veikimas kartu su limfinio audinio proliferacija Nežinoma Susilpnėjusi eritropoetinio audinio stimuliacija; skrandžio hiposekrecija Sumažėjęs azoto kiekis šlapime badaujant Sumažėjęs glikogeno kiekis kepenyse badaujant Baltymų apykaitos sutrikimai Angliavandenių apykaitos sutrikimai Susilpnėjęs antianabolinis antinksčių žievės steroidų poveikis Susilpnėjusi gliukogenazė ir gliukoneogenezė Padidėjęs jautrumas insulinui Susilpnėjusi gliukogenezė ir gliukoneogenezė Sutrikusi angliavandenių absorbcija iš virškinamojo trakto Sutrikusi riebalų mobilizacija iš sankaupų Lipidų apykaitos sutrikimai Išplitę pažeidimai Sustiprėjęs uždegimo atsakas ir padidėjusio jautrumo reakcijos Tai gali būti sutrikusios K + apykaitos padarinys, nes angliavandenių perėjimas į ląstelę vyksta kartu K + šalinimu iš ląstelių (dėl antinksčių žievės nepakankamumo ląstelės netenka K + ) 44 lentelė. Kai kurių steroidų aktyvumas, palyginti su kortizonu Steroidas Na + sulaikantysis aktyvumas Glikogeninis aktyvumas Priešuždegiminis aktyvumas Kortizonas Kortizolis Deoksikortikosteronas Aldosteronas 1 1, , ,
358 Hormonų klinikinė biochemija ir jų nustatymo reikšmė Poveikis angliavandenių apykaitai. Vartojant kortizolį, po kelių valandų padidėja gliukozės atsipalaidavimas iš kepenų; skatinama glikogenezė ir gliukoneogenezė iš aminorūgščių, glikogeno kaupimasis kepenyse; sumažėja periferinis gliukozės panaudojimas. Šiuos pokyčius, veikiant koritkosteroidams, lemia padidėjęs kepenų gliukozės-6-fosfatazės aktyvumas. Padidėja ir specifinių aminotransferazių aktyvumas kepenyse, taip pat piruvatkarboksilazės, glikogensintetazės aktyvumas, o šie fermentai skatina glikogeno sintezę ir jo kaupimąsi kepenyse. Sumažėja aminorūgščių panaudojimas baltymų sintezei, dėl to spartėja gliukoneogenezė. Kortizolis sumažina gliukozės panaudojimą periferiniuose audiniuose raumenyse, riebaliniame, limfiniame. Dėl jo poveikio silpnėja proteoglikanų sintezė jungiamajame audinyje. Dėl heksokinazės aktyvumo slopinimo, pavyzdžiui, badaujant, padaugėja glikogeno kepenyse ir gliukozės kraujyje. Ilgiau vartojant kortizolį, gali būti nustatomas diabetinis gliukozės toleravimo kreivės tipas, gliukozurija ir cukrinis diabetas dėl kasos salelių ląstelių degeneracijos ir išsekimo. Priešingai, adrenektomija padidina jautrumą insulinui. Dėl to sumažėja insulino poreikis, greitai išsivysto hipoglikemija badaujant. Trūkstant kortikosteroidų, raumenyse nepalaikoma pastovi glikogeno koncentracija, dėl to susilpnėja raumenų darbas. Poveikis baltymų ir nukleorūgščių apykaitai. Kortizolis indukuoja specifinių baltymų sintezę kepenyse, bet slopina jų sintezę raumenyse, limfiniame ir kituose audiniuose (dėl sumažėjusios aminorūgščių pernašos). Kadangi šiuose audiniuose baltymai ýra nuolat, tai minkštieji audiniai nyksta, vystosi osteoporozė. Taigi nors kepenyse baltymų sintezė spartėja, ji yra nepakankama kituose audiniuose, ir aminorūgščių koncentracija plazmoje padidėja. Aminorūgščių irimas ir suintensyvėjusi šlapalo sintezė lemia neigiamą azoto balansą. Kortizolio poveikis baltymų sintezei kepenyse yra tiesioginis, t. y. hormonas skatina aminorūgščių jungimąsi į baltymus. Hormonas skatina RNR sintezę kepenyse, o periferiniuose audiniuose, ypač limfiniame ir raumenyse, ją slopina. Poveikis riebalų apykaitai. Vartojant steroidinius hormonus, skatinama periferinė lipogenezė dėl padidėjusios insulino sekrecijos (pastarasis hormonas stimuliuoja lipogenezę). Dėl netiesioginio poveikio intensyvėja lipolizė, ir šis riebalus mobilizuojantis veikimas rodo, kad gliukozės panaudojimas slopinamas. Taigi hormonas, kaip ir veikdamas baltymų sintezę, riebalų apykaitą kepenyse ir periferiniuose audiniuose veikia priešingai. Dėl to kepenyse suintensyvėja triacilglicerolių sintezė (lipogenezė). Poveikis elektrolitų ir vandens apykaitai. Nustatyta, kad jei maiste trūksta druskos, aldosterono išsiskyrimas padidėja 3 5 kartus, o jei daug natrio pateks į organizmą, tai aldosterono sekrecija gali visai nevykti. Kalio stoka, net esant normaliai natrio koncentracijai, sumažina aldosterono išsiskyrimą, o kalio vartojimas 357
359 skatina. Kitas aldosterono sekreciją reguliuojantis veiksnys yra vartojamų skysčių kiekis: padaugėjus neląstelinio skysčio, sumažėja aldosterono sekrecija, ir atvirkščiai. Šį veikimą reguliuoja kraujagyslių ir audinių tūrio receptoriai. Kortikosteroidai reguliuoja [Na + ] ir [K + ] neląsteliniame skystyse. Dėl aldosterono ir deoksikortikosterono poveikio didėja Na +, Cl ir HCO 3 reabsorbcija distaliniuose inkstų kanalėliuose, prakaito, seilių liaukose, žarnyno gleivinėje. Todėl padidėja neląstelinio Na + koncentracija, skysčio tūris ir [HCO 3 ], o sumažėja [K + ] ir [Cl ] serume. Natrio jonų sulaikymas lemia ląstelių kalio jonų keitimąsi su tarpląsteliniais natrio jonais ir kalio jonų ekskreciją. Na + mobilizuojami iš jungiamojo audinio. Padidėjus tarpląsteliniam tūriui, didėja kraujospūdis. Dėl [K + ] serume mažėjimo, veikiant kortikosteroidams, išryškėja jų toksinis poveikis širdies raumeniui ir EKG pokyčiai. Padidėjus neląstelinio [Na + ], mažėja smegenų audinio jautrumas. Vartojant kortikosteroidus, didėja Ca 2+ išsiskyrimas su šlapimu (Ca 2+ šalinamas iš kaulo dėl susilpnėjusios baltymų sintezės). Susilpnėjus kaulinio audinio sintezei, vystosi osteoporozė, o Ca 2+, užuot kaupęsi osteoide, šalinamas su šlapimu. Dėl kortikosteroidų stokos sutrinka normali Na + reabsorbcija inkstų kanalėliuose, dėl to didėja Na +, Cl ir H 2 O ekskrecija, mažėja plazmos tūris, Na + patenka į audinius. K + koncentracija serume ir audiniuose padidėja dėl sumažėjusios jo ekskrecijos. Sumažėjęs neląstelinio skysčio tūris, hemokoncentracija, padidėjęs kraujo klampumas lemia susilpnėjusį širdies darbą, vystosi hipotenzija. Negydant antinksčių žievės nepakankamumo, išsivysto metabolinė acidozė. Ji pagal kilmę yra dvejopa: inkstų kilmės (reninė) ir ne inkstų (ekstrareninė): inkstuose sutrinka H + ir NH 4 + sekrecija ir dėl to padidėja rūgštingumas; inkstų atsakas į šį pokytį yra nepakankamas ir šlapimo rūgštingumas atitinkamai nepadidėja; didėjant [K + ] serume, rūgštieji karbonatai keliauja į ląsteles, o H + iš ląstelių į tarpląstelinį skystį ir dėl to vystosi acidozė. Esant antinksčių nepakankamui ir netenkant Na +, atsiranda ir kitų nepageidaujamų požymių. Pavyzdžiui, sumažėjus neląstelinio Na +, didėja smegenų nervinio audinio jaudrumas. Atsiranda Adisono ligai būdingi elektroencefalogramos pokyčiai. Hiperkalemija yra žalinga širdies raumeniui, dėl to pakinta elektrokardiograma, širdis gali sustoti per diastolę. Dėl antinksčių nepakankamumo pro inkstus netenkama daug skysčių, mažėja plazmos tūris, krinta kraujospūdis, mažėja kraujotaka inkstuose ir vystosi inkstų nepakankamumas. Dėl to kraujyje didėja šlapalo, fosforo, kalcio bei kalio jonų, koncentracija. Į organizmą patekęs vanduo yra sulaikomas, o kai jo patenka daug, galima intoksikacija vandeniu. Poveikis kraujodarai. Vartojant kortikosteroidų (kitų nei aldosteronas), kraujyje mažėja limfocitų ir eozinofilų, skatinama eritropoezė. Limfopenija priklauso nuo hormonų poveikio limfoidiniam audiniui, kuris nyksta, tai šių hormonų po- 358
360 Hormonų klinikinė biochemija ir jų nustatymo reikšmė veikio imuninei sistemai padarinys. Esant antinksčių žievės hipofunkcijai, vystosi limfoidinio audinio hipertrofija ir limfocitozė. Kortikosteroidai, stimuliuodami kaulų čiulpus, skatina eritropoezę. Poveikis virškinamojo trakto funkcijai. Kortikosteroidai skatina druskos rūgšties ir pepsinogeno sekreciją skrandžio gleivinėje ir tripsinogeno kasoje. Dėl šio poveikio, ilgai gydant šiais hormonais, virškinamajame trakte gali atsirasti opų. Poveikis uždegimui ir alergijai. Kortizolis ir kai kurie sintetiniai steroidai slopina uždegimo atsaką, sukeltą fizinių, cheminių ar bakterinių veiksnių dėl arachido rūgšties atsipalaidavimo iš fosfoglicerolių slopinimo; dėl to sutrinka uždegiminių prostaglandinų susidarymas. Antinksčių žievės hormonai slopina polimorfonuklearinių leukocitų patekimą į uždegiminį audinį. Jie mažina hidroksiprolino ekskreciją su šlapimu ir kolageno sintezę toks yra šių hormonų poveikis jungiamajam audiniui; ilgai vietiškai naudojant šiuos steroidus, atrofuojasi oda. Kortizoliu ypač veiksmingai šalinamos padidėjusio jautrumo būklės, pavyzdžiui, anafilaksinis šokas. Dėl šios priežasties juo gydomas ūminis uždegimas, alerginės akių, odos ligos. Antinksčių žievės hormonai ir atsparumas žalingiems veiksniams. Trūkstant antinksčių žievės hormonų, organizmas, veikiamas žalingų veiksnių, nepajėgia palaikyti pastovios homeostazės. Todėl, esant antinksčių veiklos nepakankamumui ir kartu, pavyzdžiui, prisidėjus infekcijai, patyrus fizinę traumą, kraujuojant ar dėl žalingų cheminių veiksnių gali ištikti mirtis. Padėti gali tik kortikosteroidai. Antinksčių žievės hipofunkcija. Pirminis ūminis antinksčių žievės nepakankamumas (Adisono liga) yra reta būklė, kuri, jei nediagnozuojama, baigiasi mirtimi. Seniau pagrindinė antinksčių žievės destrukcijos priežastis buvo tuberkuliozė; dabar ją dažniau sukelia yra autominuninės ligos. Ši būklė gali išsivystyti ir dėl vėžio metastazių, sepsio, kitų ligų. Antrinio (sumažėjus adrenokortikotropinio hormono sekrecijai) ir tretinio (sumažėjusi kortikotropiną atpalaiduojančio hormono sekrecija) antinksčių žievės veiklos nepakankamumo priežastys yra patologiniai pogumburio ir posmegeninės liaukos procesai: tai infekcijos, augliai, kraujotakos sutrikimas. Antinksčių žievės veiklos nepakankamumui būdinga letargija, anoreksija, rankų, burnos pigmentacija, pilvo skausmai, svorio kritimas, hipotenzija. Kraujo tyrimai rodo hiponatremiją, hiperkalemiją, hiperuremiją. Antinksčių žievės hiperfunkcija. Antinkščių žievės hiperfunkcija dažniausiai išsivysto sergant antinksčių žievės ląstelių navikais, ilgą laiką vartojant steroidinius vaistus nuo kitų ligų. Antinkščių žievės hiperfunkcijos klinika ir padariniai priklauso nuo sekretuojamo dominuojančio hormono prigimties. Jei pagrindinis gaminamas steroidas yra kortizolis, išsivysto Kušingo sindromas ir atsiranda pokyčiai, būdingi šio hormono hipersekrecijai: centrinis nutukimas, hipertenzija, hipokalemija, 359
361 metabolinė alakalozė, angliavandenių netoleravimas ir hiperglikemija, reprodukcinės sistemos sutrikimas, nervų ir psichikos pažeidimas. Jei pagrindinis gaminamas hormonas yra aldosteronas (pirminis aldosteronizmas), organizme yra sulaikomi Na + ir H 2 O, atsiranda edemos ir hipertenzija, vystosi širdies veiklos nepakankamumas, o dėl mažo kalio kiekio serume didelis silpnumas. Androgeninių hormonų hipersekrecijos klinika priklauso nuo ligonio amžiaus ir lyties. Suaugusios moterys išvaizda tampa panašios į vyrus būklė vadinama adrenaliniu virilizmu: būdinga žemas balsas, nutrūksta mėnesinės, nyksta krūtys, ant veido, krūtinės, galūnių gali pradėti augti plaukai. Suaugusiems vyrams padidėja plaukuotumas, varpa, lytinis potraukis. Jei auglys išsivysto vaikams, jie subręsta per anksti. Trejų penkerių metų berniukai atrodo kaip suaugę: padidėja varpa, krūtinės, gaktos, veido plaukuotumas, anksti atsiranda lytinis potraukis, tokie vaikai greitai auga, jų raumenys neįprastai išsivystę. Mergaitėms padidėja krūtys, plaukuotumas gaktos srityje, subręsta gimda, prasideda mėnesinės. Aldosterono perteklius gali būti pirminis kliniškai išryškėja pirminiu hiperaldosteronizmu (Kono liga), ir antrinis išsivysto sergant inkstų, širdies ir kepenų ligomis. Pirminio hiperaldosteronizmo priežastis dažniausiai yra antinksčių žievės adenoma. Jai būdingi simptomai yra polidipsija, poliurija, nervų ir raumenų veiklos sutrikimas (raumenų silpnumas, parestezijos, tetanija), hipertenzija. Įtarti tokią būklę galima asmenims, kurių kraujyje yra sumažėjusi kalio koncentracija. Api b e n d r i n i m a s Steroidiniai hormonai, pasižymintys kortizolio veikimu, žinomi kaip gliukokortikoidai. Jie stipriai veikia medžiagų apykaitą ir kaip imunosupresantai. Steroidiniai hormonai, pasižymintys aldosterono veikimu, vadinami mineralkortikoidais. Jie skatina natrio reabsorbciją inkstų kanalėliuose. Antinksčių žievės funkcijos nepakankamumas yra reta gyvybei pavojinga būklė. Autoimuninės ligos ar navikai yra dažna antinksčių žievės pažeidimo, nesugebėjimo sintetinti kortizolį ir aldosteroną priežastis. Pirminis aldosterono perteklius yra reta būklė, kurios dažniausia priežastis yra adenoma (Kono sindromas). 360
362 Hormonų klinikinė biochemija ir jų nustatymo reikšmė Laboratoriniai tyrimai Aldosteronas Tiriamoji medžiaga. Plazma (EDTA, arba heparinas). Rekomenduojama reikšmė (ng/l): naujagimių , vaikų nuo 1 mėn. iki 2 metų , vaikų nuo 3 16 metų , suaugusiųjų: gulint 8 172, sėdint Diagnostinė vertė. Pirminis aldosteronizmas dėl aldosteroną sekretuojančios adenomos (Kono sindromas); tariamasis pirminis aldosteronizmas (abipusė antinksčių hiperplazija). Antrinis aldosteronizmas: piktnaudžiaujant diuretikais, vidurius laisvinančiais vaistais, esant širdies nepakankamumui, kepenų cirozei ir ascitui, nefroziniam sindromui, idiopatinei ciklinei edemai, hipovolemijai dėl kraujavimo ir transudacijos, inkstų jukstaglomerulinei hiperplazijai, kai kartu netenkama kalio ir sulėtėja augimas, reniną gaminančiai inkstų hemangiopericitomai, piktybinei inkstinei hiperplazijai, nėštumui, stresui dėl karščio, vidurinei ir vėlyvajai liuteininei mėnesinių ciklo fazei, po 10 dienų badavimo, sergant lėtine obstrukcine plaučių liga. Be hipertenzijos: Adisono liga, izoliuotoji aldosterono stoka, hipoaldosteronizmo sindromas dėl renino stokos. Su hipertenzija: perteklinė deoksikortikosterono, kortikosterono ar 18-hidroksideoksikortikosterono sekrecija; Ternerio sindromas (25% atvejų); cukrinis diabetas; ūminis apsinuodijimas alkoholiu (ypač esant pagirioms). Papildoma informacija. Normali sekrecija priklauso nuo daugelio veiksnių: renino ir angiotenzino sistemos, kalio, AKTH, magnio, natrio koncentracijos. Plazmoje aldosterono mažėja su amžiumi. V: angiotenzinas, estrogenai, kalis, kilpiniai diuretikai (pvz., furozemidas), natrio ribojimas, geriamieji kontraceptikai, spironolaktonas, tiazidiniai diuretikai, vidurius laisvinantys vaistai (piktnaudžiavimas). V: angiotenziną konvertuojančio fermento inhibitoriai (pvz., enalaprilis, kaptoprilis), deoksikortikosteronas. Estradiolis (E 2 ) Tiriamoji medžiaga. Serumas. Rekomenduojama reikšmė: pmol/l pg/ml vyrų moterų: folikulinė fazė folikulinė fazė 2 3 dienų preovuliacinė fazė geltonkūnio fazė pomenopauzė vartojant kontraceptikus Diagnostinė vertė. Feminizacija (vaikų amžiuje), estrogenus gaminantys navikai, ginekomastija, kepenų cirozė, hipertirozė. Pirminis ir antrinis hipogonadizmas. Papildoma informacija. Estradiolis yra aktyviausias iš endogeninių estrogenų. Tyrimas svarbus diagnozuojant mėnesinių ciklo sutrikimus, moterų lytinį brendimą, ginekomastijos ar feminizacijos būkles dėl estrogenus gaminančių navikų, vaisingumo problemas, vertinant gydymo efektyvumą. Estradiolio kiekis gerokai padidėja ką tik gimusiam kūdikiui, per pirmąją gyvenimo savaitę grei- 361
363 tai sumažėja. Mergaičių lytinio brendimo metu kiekis pamažu didėja. Normalaus ovuliacinio ciklo metu estradiolio sekrecija yra dvifazė: viršūnė būna ciklo viduryje ir esant liuteininei fazei. Vyrų estradiolio kiekis didėja brendimo metu dėl periferinio testosterono perdirbimo. V: geriamieji kontraceptikai (slopina fiziologinį pakilimą). 17-hidroksikortikosteroidai (17-OHKS) Tiriamoji medžiaga. Paros šlapimas. Rekomenduojama reikšmė. 7,23 15,17 µmol/ 24 val. Diagnostinė vertė. Kušingo sindromas, stresas, nutukimas, nėštumas, sunki hipertenzija, akromegalija, tirotoksikozė, gydymas hidrokortizonu. Adisono liga, įgimtoji antinksčių hiperplazija (adrenogenitalinis sindromas), hipofizės hipofunkcija, hipotirozė, prednizonas, deksametazonas. Papildoma informacija. Bet kuri ūminė liga padidina 17-OHKS ekskreciją su šlapimu. Ekskrecija yra proporcinga kūno masei ir didesnė nutukusių asmenų negu liesų. Šį anksčiau vertingą tyrimą dabar beveik jau pakeitė kortizolio nustatymas kraujyje ir šlapime. V: AKTH, gonadotropinai, hidrokortizonas, kortizono acetatas. Ch: chloralhidratas, chorpropamazinas, digitalio glikozidai, eritromicinas, fenotiazinai, fruktozė, jodidai, ketoprofenas, meprobamatas, meticilinas, oleandomicinas, spironolaktonas. V: estrogenai, gliukokortikoidai, morfinas, geriamieji kontraceptikai Ch: karbamazepinas, rezerpinas (didelės dozės), tiazidai. 17-hidroksiprogesteronas (17-OHP) Tiriamoji medžiaga. Serumas (plazma). Rekomenduojama reikšmė (µg/l): vyrų 0,59 3,44 moterų: folikulinė fazė 0,11 1,08 geltonkūnio fazė 0,95 5,0 nėščiųjų: I trimestrą 2,50 9,78 II trimestrą 3,40 8,50 III trimestrą 4,53 18,86 Diagnostinė vertė. Įgimta antinksčių hiperplazija dėl 21-hidroksilazės stokos, 11-β hidroksilazės stoka; kai kurie antinksčių ir kiaušidžių navikai. Vyrai pseudohermafroditai (17α-hidroksilazės stoka); Adisono liga. Papildoma informacija. 17-OHP sekrecija pasižymi cirkadiniu ritmu (didžiausia sekrecija ryte). Pakilimas liuteininės fazės metu atspindi geltonkūnio aktyvumą. Labai padidėja prieš dieną iki liuteinizuojančio hormono sekrecijos viršūnės, po kurios eina kita viršūnė, sutampanti su liuteinizuojančio hormono viršūne ciklo viduryje. Po šios fazės šiek tiek sumažėja, paskui pakyla, koreliuoja su estradiolio ir progesterono svyravimais. Didžiausias kiekis randamas asmenims, turintiems 21-hidroksilazės stoką. Padidėjusi bazinė ir po stimuliacijos AKTH serumo 17-OHP koncentracija padeda nustatyti klasikinę ir neklasikinę 21-hidroksilazės stokos formas ir jos nešiklius, įvertinti įgimtos antinksčių hiperplazijos gydymo gliukokortikoidais veiksmingumą. Katecholaminai: adrenalinas ir noradrenalinas Tiriamoji medžiaga. Plazma (EDTA). Rekomenduojama reikšmė. Adrenalino <100 ng/l, noradrenalino <600 ng/l. Tiriamoji medžiaga. Paros šlapimas. Konservuoti 20 ml HCl (6 mol/l), šaldyti. Rekomenduotina reikšmė. Adrenalino <20 µg/24 val., noradrenalino <104 µg/24 val. Diagnostinė vertė. Feochromocitomai būdingas didesnis noradrenalino negu adrenalino kiekis plazmoje. Kai kuriems ligoniams su šapimu gali išsiskirti apie µg/24 val. nor- 362
364 Hormonų klinikinė biochemija ir jų nustatymo reikšmė adrenalino ir >750 µg/24 val. adrenalino. Vyraujantis noradrenalino padidėjimas rodo, kad feochromocitoma yra kilusi iš antinksčių šerdies. Neuroblastoma, ganglioneuroblastoma, ganglioneuroma (didelė dopamino, noradrenalino ir jų metabolitų koncentracija); paraganglioma, miokardo infarktas, stresas, hipotirozė, diabetinė acidozė, ilgai trunkanti maniakinė depresinė būklė. Autonominė neuropatija (pvz., dėl cukrinio diabeto, parkinsonizmo). Papildoma informacija. Fizinis aktyvumas, stresas, rūkymas, skausmas fiziologiškai didina katecholaminų kiekį. Jų kraujyje daugėja pacientui esant vertikalioje padėtyje, įvairiomis stresinėmis aplinkybėmis, taip pat dėl streso venos punkcijos metu. Idealiu atveju kraujas imamas ryte po 30 min. poilsio gulinčiam ligoniui. Plazmos noradrenalino nustatymas svarbus ortostatinės hipotenzijos diagnostikai noradrenalino koncentracija nepadidėja. Noradrenalino koncentracijai nepadidėjus keičiant gulimą padėtį į stovimą, rodo simpatinės nervų sistemos sutrikimą. Jei įmanoma, likus savaitei iki katecholaminų tyrimo šlapime reikia nutraukti vaistų vartojimą. Katecholaminų ekskrecija naktį yra daug mažesnė. Adrenalino ir noradrenalino ekskrecija didėja mėnesinių ciklo liuteininės fazės metu, o per ovuliaciją nukrinta iki minimumo. Panašiai kinta ir vanilmigdolų rūgšties kiekis. 17-ketosteroidai (17-KS) Tiriamoji medžiaga. Paros šlapimas. Rekomenduojama reikšmė (µmol/24 val.): 1 4 metų <7; 5 metų: berniukų 8,67, mergaičių 6,93 10 metų: berniukų 27,74, mergaičių 24,8 15 metų: berniukų 8,14, mergaičių 31, metų: vyrų 35 78, moterų metų: vyrų 28 35, moterų metų: vyrų 10 17, moterų Vyrų paros šlapime vidutiniškai yra mg 17-ketosteroidų, moterų 5 8 mg; 2 4 metų vaikų šių hormonų paros ekskrecija sudaro 1/10 dalį suaugusiųjų dydžio. Diagnostinė vertė. Kušingo liga, ektopinis AKTH gaminantis navikas, antinksčių navikai (17-ketosteroidų kiekis didesnis esant antinksčių vėžiui, palyginti su antinksčių adenoma), įgimtos antinksčių hiperplazijos virilizuojanti forma. Sėklidžių navikai, intenersticinių ląstelių navikai, kiaušidžių geltonkūnio navikai (androgeniniai). Adisono liga, hipofizės panhipofunkcija, antrinis moterų hipogonadizmas (hipofizinis, ne kiaušidžių), hipotirozė, nefrozė, pirminis vyrų hipogonadizmas (Kleinfelterio sindromas, kastracija). Papildoma informacija. Stiprus stresas padidina17-ks kiekį. Ekskrecija didėja lytinio brendimo metu, vėliau pasiekia maksimumą ir nuo metų amžiaus vis mažėja. Tyrimas nėra jautrus vertinant endogeninę androgenų gamybą, nes testosteronas ir dihidrotestosteronas šioje reakcijoje nematuojami. Dehidroepiandrosterono sulfatas (DHEA-S) kraujyje šiuo metu keičia 17-KS tyrimą ir yra antinksčių androgenų gamybos žymuo. V: gonadotropinai, kortikotropinas, testosteronas. Ch: cefalosporinai, eritromicinas, penicilinas, spironolaktonas. bendrasis Kortizolis Tiriamoji medžiaga. Serumas. Rekomenduojama reikšmė: ryte (iki pietų) nmol/l, po pietų nmol/l; ryte (iki pietų) 5 25 µg/dl, po pietų 2,5 12,5 µg/dl (1/2 rytinės reikšmės). 363
365 Diagnostinė vertė. Kušingo (hipofizės) sindromas, antinksčių adenoma, vėžys. Ektopinis adrenokortikotropinio hormono sekrecijos sindromas. Adisono liga, įgimta antinksčių hiperplazija (adrenogenitalinis sindromas), hipofizės hipofunkcija (būtini funkciniai mėginiai). Papildoma informacija. Padidėjusi sekrecija nustatoma esant hipoglikemijai, stresui, eterio narkozei, nėštumui, nutukimui, depresijai, hipertirozei. Sumažėjusi sekrecija būdinga hipotirozei, cirozei, hepatitui. Tačiau dėl šioms būklėms būdingo sutrikusio šalinimo kortizolio kiekis gali būti normalus. Kortizolio sekrecija su amžiumi nekinta. Nėštumo metu palengva didėja (dėl kortizolį sujungiančio globulino kiekio didėjimo); vėlyvuoju nėštumo laikotarpiu gali padidėti 2,5 karto. Būdingas paros ritmas: 20 val. kiekis sudaro 50% kiekio, nustatomo 8 val. ryte. Esant Kušingo sindromui šie paros svyravimai dažniausiai išnyksta. V: estrogenai, etanolis, hidrokortizonas, interferonas (γ), kortikotropinas, kortizono acetatas, geriamieji kontraceptikai, gausus rūkymas, vazopresinas. V: betametazonas, deoksimetazonas, deksametazonas, ličio karbonatas, metilprednizolonas, morfinas. Lytinius hormonus sujungiantis globulinas (LHSG, angl. SHBG) Tiriamoji medžiaga. Serumas. Rekomenduojama reikšmė. Vyrų nmol/l, moterų nmol/l. Diagnostinė vertė. Hipertirozė, estrogenų perteklius, gydymas skydliaukės hormonu, nervinė anoreksija, nėštumas, kepenų cirozė. Hipotirozė, testosterono perteklius, hirsutizmas, nutukimas, policistinių kiaušidžių sindromas. Papildoma informacija. Lytiniai hormonai testosteronas ir estrogenai yra sujungiami kraujyje cirkuliuojančio lytinius hormonus sujungiančio globulino. Bendrojo cirkuliuojančių androgenų ar estrogenų kiekio įvairavimas priklauso nuo steroidinių hormonų gamybos pokyčių, lytinius hormonus sujungiančio globulino koncentracijos kitimo ar gebėjimo sujungti. LHSG kiekis abiejų lyčių individuose didėja su amžiumi. Prieš menopauzę gimdžiusios moterys turi didesnį kiekį negu negimdžiusios. Taip pat ištekėjusios moterys turi didesnę koncentraciją negu netekėjusios. Esant gausiam moterų plaukuotumui, LHSG koncentracija gali būti maža ir dėl to padidėja androgenų frakcija, nors bendrasis androgenų kiekis padidėjęs nedaug. Vyrų, sergančių Kleinfelterio sindromu, LHSG koncentracija gali būti normali. V: vaistai nuo traukulių. V: testosteronas. Testosteronas Tiriamoji medžiaga. Serumas. Rekomenduojama reikšmė: nmol/l ng/dl vyrų: m. 9,1 55, m. 6,3 26, moterų: iki menopauzės <2,7 <80 po menopauzės <2,1 <6,2 Diagnostinė vertė. Idiopatinis ankstyvas lytinis subrendimas ir antinksčių hiperplazija berniukams (reikšmės kaip suaugusių vyrų), antinksčių žievės navikai, lytinius hormonus gaminantys ne lytinių liaukų navikai, trofoblasto ligos nėštumo metu, idiopatinis hirsutizmas, virilizuojantys kiaušidžių navikai, virilizuojanti liuteoma. Dauno sindromas, uremija, miopatinė distrofija, kepenų veiklos nepakankamumas, kriptorchizmas, pirminis ir antrinis lytinių liaukų neišsivystymas, vėluojantis berniukų brendimas. 364
366 Hormonų klinikinė biochemija ir jų nustatymo reikšmė Papildoma informacija. Matuojamas bendrasis cirkuliuojančio testosterono kiekis (laisvojo ir susijungusio su baltymais). Berniukams serumo testosterono kiekis staigiai pakyla lytinio brendimo metu. Suaugusiesiems testosterono daugiausia yra anksti ryte, vakare sumažėja 25%. Kiekis padidėja po fizinių pratimų ir sumažėja po imobilizacijos ir gliukozės apkrovos. Po 50 metų amžiaus nuolat mažėja. Moterų testosterono koncentracija mažesnė negu vyrų ir kinta cikliškai: ciklo viduryje 1 2 dienas padidėja. V: barbitūratai, estrogenai, gonadotropinas (vyrams), geriamieji kontraceptikai, vaistai nuo traukulių. V: androgenai, deksametazonas, dietilstilbestrolis, digitalis, digoksinas (vyrams), etanolis (vyrams alkoholikams), gliukokortikoidai, gliukozė, gonadotropiną atpalaiduojančio hormono analogai, halotanas, metopropolis, spironolaktonas, tetraciklinas. Lytinės liaukos ir jų sintetinami hormonai Androgenai (gr. andros vyras) ir estrogenai (gr. oistros aistra) tai hormonai, atsakingi už antrinių lytinių požymių išsivystymą. Jie yra sintetinami ir sekretuojami sėklidėse ir kiaušidėse. Be to, estrogenų randama sėklidėse ir antinksčiuose, androgenų kiaušidėse ir antinksčiuose, jie rodo bendrą sėklidžių, kiaušidžių ir antinksčių žievės kilmę ir vystymąsi embriogenezės metu. Sėklidės. Vyriškieji lytiniai hormonai Vyriškųjų lytinių hormonų struktūra, sintezė ir reguliavimas. Androgenai, kuriuos gamina antinksčiai ir vyrų lytinės liaukos, priklauso 19 anglies atomų (C-19) turintiems steroidams. Biologiškai aktyviems androgenams priklauso testosteronas, dihidrotestosteronas (jie aktyviausi), androstandiolis bei androstenedionas (pastarųjų dviejų koncentracija kraujo plazmoje beveik neišmatuojama). Testosteronas yra svarbiausias kraujyje randamas androgenas. Vyrų organizme testosteronas gaminamas sėklidžių Leidigo ląstelėse. Vykstant apykaitai ir veikiant fermentui 5α-reduktazei, kuri randama prostatoje, odoje (ypač dengiančioje lytines liaukas), sėklidžių pūslelėse, testosteronas yra verčiamas dihidrotestosteronu tai taip pat aktyvusis androgenas. Raumenyse aktyvusis androgenas yra testosteronas. Androstandiolis gaminamas iš testosterono periferiniuose audiniuose arba gali susidaryti iš plazmos dehidroepiandrosterono. Androstenedionas ir dehidroepiandrosteronas yra svarbūs kaip testosterono prehormonai. Androgeninio aktyvumo, kaip jau minėta, turi ir junginiai, sintetinami antinksčiuose. Moterų organizme 50% kraujyje cirkuliuojančio testosterono yra kilęs iš androstenediono, transformuoto periferiniuose audiniuose, o kita dalis susidaro kiaušidėse ir antinksčiuose. Pregnenolonas yra pagrindinis visų steroidinių hormonų pirmtakas. Svarbiausias pregnenolono transformavimosi kelias yra jo virtimas 7-hidroksipregnenolonu, po to dehidroepiandrosteronu (DHEA) ir galiausiai androstenedionu ir testosteronu. 365
367 Galimas ir kitas kelias, kai pregnenolonas virsta progesteronu ir tada jau androstenedionu. Pastarojo transformacija į testosteroną yra grįžtamoji reakcija. Sėklidėse visos reakcijos vyksta testosterono gamybos ir sekrecijos linkme, o kiaušidėse pagrindinis gaminamas hormonas yra androstenedionas. Testosterono sekreciją Leidigo ląstelėse kontroliuoja pogumburio posmegeninės liaukos sėklidžių ašies hormonai. Pogumburio gonadotropinį hormoną atpalaiduojantis hormonas skatina liuteinizuojančio hormono (LH) sekreciją, o pastarasis hormonas testosterono sekreciją. Šį poveikį skatina ir folikulus stimuliuojantis hormonas (FSH), nes dėl pastarojo poveikio ląstelių paviršiuje daugėja LH receptorių. Didėjanti testosterono koncentracija savo ruožtu slopina LH sekreciją. Metabolinė androgenų transformacija. Patekęs į kraują testosteronas prisijungia prie plazmos baltymų svarbiausias yra lytinius hormonus sujungiantis globulinas, kuris vyrų organizme perneša apie 60 70% testosterono; apie 30 40% testosterono laisvai prisijungia prie albumino. Apie 2 3% testosterono kraujyje yra laisvo tai jo aktyvioji forma. Pagrindinė androgenų metabolinės transformacijos vieta yra kepenys. Dauguma su šlapimu šalinamų androgenų metabolitų yra 17-ketosteroidai. Detaliau apie tai knygos skyriuje Antinksčių žievės hormonai. Androgenų veikimas ir jo sutrikimai. Androgenų veikimas yra svarbus ir lyties, ir kitų organų funkcijai. Testosteronas yra vyraujantis androgenas smegenyse, posmegeninėje liaukoje, sėklidėse (jam veikiant gaminami spermatozoidai), inkstuose, o dehidrotestosteronas svarbiausias androgenas odoje, prostatoje, sėklinėse pūslelėse (antsėklidyje). Smegenyse yra specifiniai receptoriai testosteronui ir fermentinės sistemos, verčiančios šį hormoną moteriškuoju lytiniu hormonu estradioliu. Dėl androgenų poveikio organizme sulaikomas azotas ir veikiama kalcio apykaita; indukuojama baltymų sintezė audinių taikinių ląstelėse, ypač raumenų, kaulų, inkstų, gerklų, ir taip skatinamas jauno organizmo audinių augimas. Šį poveikį minėtųjų audinių ląstelėse atspindi suintensyvėjusi branduolinės DNR ir RNR sintezė, RNR pernaša į citoplazmą ir spefinių ribosominių baltymų sintezė, suintensyvėjusi fosfolipidų sintezė plazmos ir endoplazminio tinklo membranose. Androgenai specifiškai veikia plaukų augimą tam tikrose vietose jie tampa ilgesni, šiurkštesni, tamsesni. Dėl androgenų poveikio formuojasi antriniai lytiniai požymiai: vystosi lyties organai, keičiasi balso tembras, odos struktūra, plaukų augimas, elgesys, atsiranda lytinis potraukis. Suaugusiame organizme šie hormonai veikia kaip steroidinių hormonų sekrecijos reguliatoriai pogumburio lygmeniu: pogumburis posmegeninė liauka lytinės liaukos, t. y. gonadotropinus atpalaiduojantis hormonas skatina posmegeninės liaukos priekinėje dalyje liuteinizuojančio ir folikulus stimuliuojančio hormonų sintezę ir sekreciją, o šie lytinių hormonų sekreciją ir reprodukcinę funkciją. Leidigo 366
368 Hormonų klinikinė biochemija ir jų nustatymo reikšmė ląstelių funkciją ir testosterono sekreciją labiau veikia liuteinizuojantis hormonas, o folikulus stimuliuojantis hormonas Sertolio ląstelių funkciją. Jose gaminasi inhibinas, kuris mažina FSH sekreciją veikdamas tiesiogiai posmegeninę liauką ir per pogumburio reguliacinius hormonus. Jaunų vyrų testosterono sekrecijai būdingas cirkadinis ritmas: didžiausia sekrecija yra ryte bundant, o su amžiumi tai išnyksta. Adrenopauzės metu labiau mažėja DHEA, palyginti su testosterono sekrecija. Esant neišsivysčiusiems vyriškiesiems lytiniams organams (hipogonadizmas), sutrinka spermos, sumažėja testosterono gamyba. Taip gali atsitikti esant pirminei šio hormono stokai (hipergonadotropinis hipogonadizmas) arba dėl pogumburio ar posmegeninės liaukos defektų (hipogonadotropinis hipogonadizmas); pastaruoju atveju trūksta gonadotropinų ar tik LH. Pirminio hipogonadizmo priežastys gali būti įgimti defektai (Kleinfelterio sindromas, sėklidžių agenezė) ar įgytos priežastys (infekcijos, pažeidžiančios sėklides, pvz., tymai, trauma, spinduliuotės poveikis, citotoksiniai vaistai). Antrinis hipogonadizmas gali išsivystyti, pavyzdžiui, dėl posmegeninės liaukos navikų. Androgenų svarba augimui ir vystymuisi yra akivaizdi po kastracijos. Kastracija iki subrendimo sutrikdo antrinių lytinių požymių vystymąsi, sulėtėja ilgųjų kaulų epifizių kaulėjimas (osifikacija), dėl to didėja ūgis, apatinės galūnės neproporcingai pailgėja, vystosi nutukimas, o riebalai pasiskirsto būdingai moterų organizmui. Neišsivysto gerklos ir balsas išlieka aukštas. Nors plaukų galvoje gali būti daug, jie neauga veido srityje ir ant kūno. Varpa lieka infantiliška, neišsivysto lytinio potraukio jausmas. Sumažėja raumenų jėga. Jei kastracija yra po lytinio subrendimo, požymiai vystosi panašūs, kaip ir iki lytinio subrendimo, bet jie ne tokie ryškūs. Suintensyvėjęs plaukų augimas yra vadinamas hirsutizmu ir priklauso nuo nekoordinuotosios testosterono ir jo pirmtako androstendiono sekrecijos. Galimas nuo androgenų priklausomas ir nuo androgenų nepriklausomas plaukuotumas, kuris nustatomas pagal plaukų pasiskirstymą ant kūno. Nuo androgenų priklausomas plaukuotumas ribojasi plaukų augimu smakro, viršutinės lūpos, krūtinės ir kitose androgenams jautriose vietose, o nuo androgenų nepriklausomam plaukuotumui būdingas plaukų augimas minėtose vietose, taip pat kaktos, pilvo, rankų, kojų srityse. Tokiems asmenims reikia matuoti laisvojo testosterono kiekį kraujyje jis, esant nuo androgenų priklausomam plaukuotumui, dažniausiai yra padidėjęs. Laisvojo testosterono koncentracija su jo biologiniu aktyvumu koreliuoja geriau negu bendrojo testosterono kiekis. Kiaušidės. Moteriškieji lytiniai hormonai Estrogenų struktūra, sintezė ir reguliavimas. Kiaušidžių folikulai sekretuoja tris estrogeniškai aktyviausius junginius: β estradiolį (E 2 ) (pasižymi didžiausiu aktyvumu moters organizme iki menopauzės), estroną (E 1 ) (jo daugiausia moters or- 367
369 ganizme po menopauzės) ir estriolį (E 3 ). Pastarieji du hormonai yra estradiolio apykaitos produktai. Visi jie yra steroidai, turintys 18 anglies atomų, A ciklą su trimis nesočiosiomis dvigubosiomis jungtimis: b Daugumą estrogenų gamina ir sekretuoja kiaušidės (estradiolis sintetinamas tik kiaušidėse), geltonkūnis ir nėštumo metu placenta. Vyro organizme sėklidės sintetina 1/3 viso estradiolio ir dar mažiau estrono. Kita dalis estradiolio pasigamina periferiniuose organuose iš testosterono ir estrono. Kiaušidės yra pagrindinis nenėščios moters estrogenų gamybos organas (nėštumo metu tokiu organu tampa placenta); jose taip pat sintetinami progestinai ir androgenai, tačiau estradiolis ir progesteronas yra jų pirminiai produktai. Kiaušidėse pagrindinis sintetinamas hormonas yra estradiolis, o placentoje daugiausia pagaminama estriolio. Pagrindinis estrogenų gamybos pirmtakas yra testosteronas: kiaušidėse yra aktyvi fermentinė aromatazių sistema, kuri skatina androgenų virtimą estrogenais. Periferiniuose audiniuose estrogenai gaminami iš antinksčių žievėje sintetinamo androstenediono: ir moters, ir vyro organizme apie 1% jo paverčiama estronu. Menopauzės metu, kai kiaušidės nustoja gaminti estrogenus, pastarasis sintezės kelias tampa svarbiausias. Pažymėtina, kad pagrindinis periferinis organas, kuriame androgenai transformuojami į estrogenus, yra riebalinis audinys, todėl nutukusių moterų organizme estrono kiekis padidėja. OH HO b Metabolinė estrogenų transformacija. Kraujyje didžioji estradiolio dalis yra konjuguota su lytinius hormonus sujungiančiu globulinu, nedaug jo yra prisijungusio prie albumino ir apie 2 3% yra laisvo, t. y. aktyvaus, o didžioji dalis estrono yra susijungusi su albuminu. Įvairiuose audiniuose odoje, riebaliniame audinyje, gimdoje, eritrocituose yra fermentų, metabolizuojančių estrogenus, tačiau kepenys yra pagrindinis estrogenų transformavimo ir inaktyvinimo organas. Estrogenai ir jų metabolitai, kurie gaminasi 368
370 Hormonų klinikinė biochemija ir jų nustatymo reikšmė vykstant hidroksilinimo, oksidacijos, redukcijos bei metilinimo reakcijoms ir galutinai juos konjuguojant su gliukurono ar sieros rūgštimis, yra šalinimi su tulžimi, per inkstus su šlapimu. Pastebėtina, kad šie metabolitai, jeigu vartojami per os, yra estrogeniškai aktyvūs. Sergant hipertiroze, paspartėja estradiolio hidroksilinimas; ypač padaugėja metabolito 2-hidroksiestrono, jis tampa pagrindiniu estrogenų metabolitu. Estrogenų sintezę ir sekreciją kiaušidėse reguliuoja pogumburio gonadotropinius hormonus išskiriantis hormonas, kuris reguliuoja posmegeninės liaukos FSH ir LH sekreciją. Estradiolis grįžtamuoju ryšiu reguliuoja ir pogumburio, ir adenohipofizės funkcijas. Estrogenų funkcijos ir jų sutrikimai. Nors estrogenai daro įtaką beveik visų audinių veiklai, pagrindinė jų funkcija yra moterų reprodukcinės sistemos augimo ir subrendimo stimuliavimas ir reprodukcinių galimybių palaikymas, t. y. jie skatina folikulų augimą, gimdos gleivinės vystymąsi bei moteriškųjų antrinių lytinių požymių formavimąsi: pažastų ir lyties organų plaukuotumo vystymąsi, kūno formų kitimus, ilgųjų kaulų epifizių užakimą. Jie taip pat reguliuoja mėnesinių ciklą ir palaiko nėštumą. Kiaušidžių ciklo metu estrogenai skatina makšties epitelio proliferaciją, padidėjusią gimdos kaklelio liaukučių sekreciją, gimdos gleivinės proliferaciją, nėštumo metu pieno liaukų augimą. Audiniuose taikiniuose yra specifinių receptorių β estradioliui: gimdoje, makštyje, pieno liaukose, adenohipofizėje, pogumburyje. Estronas kur kas silpniau veikia reprodukcinius audinius. Kaip ir androgenai, estrogenai, patekę į ląsteles taikinius, susijungia su specifiniu citoplazminiu receptoriumi baltymu ir nunešami į jų branduolį. Hormono ir receptoriaus kompleksas su chromatino nehistoniniais baltymais skatina naujos irnr, koduojančios specifinius baltymus, sintezę. Todėl, estrogenams patekus į organizmą, padidėja RNR polimerazės aktyvumas, RNR ir baltymų sintezė audinyje taikinyje. Estrogenų poveikis lipidų apykaitai yra vėlesnis negu baltymų ir nukleorūgščių sintezei, bet audringesnis. Estrogenai skatina glicerofosfolipidų apykaitą gimdos gleivinėje. Lipoproteinų apykaita ir estrogenų poveikis jai yra plačiai tyrinėtas. Paaiškėjo, kad koronarine širdies liga dažnesniau serga vyrai, o vartojančio estrogenus vyro organizme lipidų kiekis sumažėja, ypač esant hiperlipidemijai. Estrogenai yra svarbūs normaliai kaulų mineralinių medžiagų apykaitai. Ilgai vartojant estrogenus, kraujyje didėja [Ca 2+ ] ir [Pi], skatinama ilgųjų kaulų kalcifikacija ir hiperosifikacija, todėl kaulų ertmės gali išnykti, o kraujyje išsivysto kalcio stoka. Tuo pat metu netenkama Ca 2+ iš dubens kaulų, juose atsiranda cistų. Po menopauzės moterims išsivysto osteoporozė. Iki lytinio brendimo estrogenų koncentracija organizme yra maža, bet bręstant ji labai padidėja ir estrogenai pradeda funkcionuoti cikliškai. Po menopauzės estrogenų koncentracija sumažėja, nors gonadotropinų koncentracija yra didelė. 369
371 Kiaušidės yra susijusios su dviem cikliniais reiškiniais, kurių metu moters organizme vyksta struktūriniai, funkciniai ir cheminiai pakitimai: tai mėnesinių ciklas, kai galima reprodukcija, ir reprodukcinis ciklas. Sutrikus moteriškųjų lytinių hormonų sintezei ir sekrecijai, išsivysto amenorėja ar oligomenorėja, atsiranda vyrams būdingas kūno plaukuotumas (dažniausiai sergant kiaušidžių policistine liga), virilizmo požymių: padidėja testosterono koncentracija kraujyje, padidėja klitoris, atrofuojasi krūtys, būdingas žemas balsas. Estrogenų reikšmė šiems procesams išryškėja pašalinus kiaušides. Jei kastracija yra iki subrendimo, tai mėnesinių neatsiranda ir lyties organai lieka infantiliški: nepadidėja dubuo, nesivysto pieno liaukos, menkas pažastų ir lyties organų plaukuotumas. Dėl kastracijos po subrendimo nutrūksta mėnesinių ciklas, sunyksta gimdos, makšties gleivinė, kiaušintakiai, pieno liaukos. Išnyksta antriniai lytiniai požymiai, vystosi osteoporozė. Mėnesinių ciklo hormoninis reguliavimas yra susijęs su pogumburio, posmegeninės liaukos ir kiaušidžių sintetinamų hormonų sąveika. Paprastai mėnesinių ciklo pradžia yra laikoma pirmoji menstruacinio kraujavimo diena. Ciklą sudaro trys fazės. Folikulinė fazė tai pirmosios 14 dienų iš 28 dienų ciklo. Jos metu folikulai gamina mažai estrogenų. Dėl sumažėjusio neigiamo grįžtamojo ryšio poveikio pogumburio posmegeninės liaukos ašiai padidėja FSH (ypač) bei LH sekrecija. Tai skatina folikulų augimą. Progesterono koncentracija šios fazės metu yra maža. Pradėjus didėti estradiolio koncentracijai, vėl reaguoja pogumburio ir posmegeninės liaukos centrai ir didėja gonadotropinus atpalaiduojančio hormono sekrecija. Kai padidėja estradiolio, LH (ypač) ir FSH kiekis, prasideda ovuliacijos fazė. Ji yra mėnesinių ciklo viduryje ir trunka apie 48 valandas. Ši fazė baigiasi ovuliacija. Paskutinė yra geltonkūnio fazė, kai plyšęs folikulas vystosi į geltonkūnį, kuris sekretuoja progesteroną bei estradiolį ir jų kiekis padidėja veikiama šių hormonų, gimdos gleivinė pasirengia kiaušinėlio implantacijai. Tada LH ir FSH kiekis pradeda mažėti. Geltonkūnio hormonai Progesterono sintezė, apykaita ir funkcijos. Progesteroną gamina geltonasis kūnas (corpus luteum) (nenėščios moters organizme), taip pat placenta (nėštumo metu) ir antinksčiai: ir vyrų, ir moterų antinksčių žievė sintetina progesteroną. Geltonkūnyje, kaip ir antinksčiuose, progesterono sintezė prasideda acetato virtimu cholesteroliu ir po to 19 anglies atomų turinčiu steroidu pregnenolonu. Jo sintezę ir sekreciją reguliuoja liuteinizuojantis hormonas. Iš progesterono per testosteroną gali susidaryti estronas ir estradiolis. Kraujyje progesteronas, kaip ir kortizolis, jungiasi prie kortikosteroidus sujungiančio globulino. Nėštumo metu šio baltymo kiekis kraujyje padidėja. Sujungtas 370
372 Hormonų klinikinė biochemija ir jų nustatymo reikšmė su baltymu progesteronas yra neaktyvus. Be to, progesteronas gali prisijungti ir prie plazmos α 1 rūgščiojo glikoproteino. Laisvasis progesteronas sudaro apie 2 10% bendrojo jo kiekio kraujyje ir šis kiekis esti pastovus per visą normalų mėnesinių ciklą. Svarbiausias progesterono metabolitas yra pregnandiolis. Jis susidaro kepenyse iš progesterono, vykstant redukcijos reakcijai, ir po to konjuguojamas su gliukurono ar sieros rūgštimi ir šalinamas su šlapimu. Pregnandiolio nustatymo šlapime svarba padidėja derinant jo kiekį su moters fiziologine būkle ir atspindi endogeninę progesterono gamybą. Folikulinėje mėnesinių ciklo fazėje progesterono kiekis kraujo plazmoje yra <1 ng/ml. Po ovuliacijos jį intensyviai pradeda sekretuoti geltonkūnis ir per 4 7 dienas jo koncentracija išauga iki ng/ml. Tokia ji išlieka dar 4 6 dienas, vėliau staigiai (maždaug per 24 val.) nukrinta iki bazinio lygio, t. y. iki mėnesinių pradžios. Progesterono koncentracijos pokyčiai atspindi geltonkūnio aktyvumo svyravimus, todėl jo nustatymu kraujyje patvirtinima ovuliacijos klinika ir įvertinama normali nenėščios moters geltonkūnio veikla. Neįvykus ovuliacijai, geltonkūnis nesusidaro ir plazmos progesterono koncentracija nepakinta. Nėštumo metu progesteroną gamina placenta. Jo koncentracija pamažu kyla per visą nėštumą (progesterono sekrecija palaiko nėštumą) ir prieš gimdymą pasiekia 400 ng/ml. Hormonas veikia gimdos gleivinę, paruoštą estrogenų, skatindamas sekrecinį aktyvumą, būtiną kiaušinėlio implantacijai. Progesteronas taip pat skatina pieno liaukų augimą ir palaiko gimdą ramybės būklės. Šią funkciją jis atlieka slopindamas oksitocino išsikyrimą. Vartojamas progesteronas 5 25-ą normalaus mėnesinių ciklo parą slopina ovuliaciją; tuo pagrįstas sintetinių progestinų, geriamųjų kontraceptikų, vartojimas. Labai didelėmis dozėmis progesteronas skatina druskų ir vandens susilaikymą ir tuo jis primena kai kurių antinksčių žievės hormonų veikimą, nes slopina imunitetą. Kaip ir androgenams bei estrogenams, ląstelės taikiniai progesteronui turi specifinį citoplazminį receptorių. Pirminis progesteronas, kaip ir testosteronas bei estradiolis, veikia genų transkripcijos lygmeniu. Šią transkripciją lemia steroido ir receptoriaus (baltymo) komplekso prisijungimas prie ląstelės taikinio chromatino ir jo moduliacija per specifinį fosforilinimo procesą. Relaksinas. Geltonkūnis gamina kitą hormoną relaksiną. Šis pasižymi savybe atpalaiduoti gaktikaulio simfizę. Tai polipeptidas (molekulinė masė 6000 Da), sudarytas iš dviejų grandinių, turinčių 22 ir 32 aminorūgščių liekanas, sujungtas disulfidiniais tilteliais. Relaksinas taip pat sintetinamas kiaušidėse, gimdoje. Jis parengia gimdymui lytinius takus: dėl jo poveikio suminkštėja ir išsiplečia gimdos kaklelis, slopinamas gimdos susitraukimas, atpalaiduojama gaktikaulio simfizė ir kiti dubens sąnariai. 371
373 Api b e n d r i n i m a s Androgenai ir estrogenai tai hormonai, atsakingi už antrinių lytinių požymių vystymąsi. Jie yra sintetinami ir sekretuojami sėklidėse ir kiaušidėse. Be to, estrogenų randama sėklidėse ir antinksčiuose, androgenų kiaušidėse ir antinksčiuose. Biologiškai aktyviems androgenams priklauso testosteronas, dihidrotestosteronas (jie aktyviausi), androstandiolis bei androstenedionas. Vyrų organizme testosteronas yra svarbiausias kraujyje randamas androgenas. Moterų organizme 50% kraujyje cirkuliuojančio testosterono yra kilusio iš androstenediono, o kita dalis susidaro kiaušidėse ir antinksčiuose. Kraujyje testosteronas prisijungia prie plazmos baltymų svarbiausias yra lytinius hormonus sujungiantis globulinas; apie 2 3% testosterono kraujyje yra laisvo tai jo aktyvioji forma. Pagrindinė androgenų metabolinės transformacijos vieta yra kepenys. Dauguma su šlapimu šalinamų androgenų metabolitų yra 17-ketosteroidai. Kiaušidžių folikulai sekretuoja tris estrogeniškai aktyviausius junginius: β estradiolį (pasižymi didžiausiu aktyvumu moters organizme iki menopauzės), estroną (jo daugiausia moters organizme po menopauzės) ir estriolį. Daugumą estrogenų gamina ir sekretuoja kiaušidės, geltonkūnis ir nėštumo metu placenta. Vyro organizme sėklidės sintetina 1/3 viso estradiolio ir dar mažiau estrono. Pagrindinis estrogenų gamybos pirmtakas yra testosteronas. Kraujyje didžioji estradiolio dalis sudaro junginį su lytinius hormonus sujungiančiu globulinu, apie 2 3% yra laisvo, t. y. aktyvaus. Kepenys yra pagrindinis estrogenų transformavimo ir inaktyvinimo organas. Pagrindinė estrogenų funkcija yra moterų reprodukcinės sistemos augimo ir brendimo skatinimas, reprodukcinių galimybių palaikymas. Pregnenolonas yra pagrindinis visų steroidinių hormonų pirmtakas. Progesteroną gamina geltonkūnis (nenėščios moters organizme), taip pat placenta (nėštumo metu) ir antinksčiai; jo sintezė prasideda acetato virtimu cholesteroliu. Geltonkūnis gamina ir relaksiną, kuris parengia gimdymui lytinius takus. Laboratoriniai tyrimai Progesteronas Tiriamoji medžiaga. Serumas. Rekomenduojama reikšmė: nmol/l ng/ml vyrų: 0,86 2,9 0,27 0,9 moterų: folikulinė fazė 3,6 1,13 folikulinė fazė 5 11 d. 3,1 0,98 ovuliacijos fazė 1,5 5,5 0,48 1,72 geltonkūnio fazė ,95 21 geltonkūnio fazė 7 8 d pomenopauzė 3,2 1,0 vartojant kontraceptikus 1,1 2,9 0,34 0,92 372
374 Hormonų klinikinė biochemija ir jų nustatymo reikšmė nėščiųjų: I nėštumo trečdalis 29, ,3 33,2 II nėštumo trečdalis 93, ,5 50 III nėštumo trečdalis ,1 160 Diagnostinė vertė. Įgimtoji antinksčių hiperplazija dėl 21-hidrolizės, 17 α-hidroksilazės ir 11 β-hidroksilazės stokos; lipoidinis kiaušidžių navikas, tekaliuteininė cista, nėštumas su pūsline išvisa, kiaušidžių chorioepitelioma. Gresiantis persileidimas, pirminis ir antrinis hipogonadizmas, trumpos liuteininės fazės sindromas. Papildoma informacija. Diagnostinė šio tyrimo vertė tai galimybė nustatyti ovuliaciją ir geltonkūnio funkciją. Reikalinga serija tyrimų per mėnesinių ciklą. Kiekis gerokai išauga liuteininėje fazėje, maksimumą pasiekia 5 10 dieną po liuteinizuojančio hormono viršūnės ciklo viduryje. Nėščiųjų progesterono kiekis nuolat didėja 9 32 savaitę (padidėja kartų). Jei nėštumas dvivaisis, progesterono kiekis didesnis, negu kai vaisius vienas. Tyrimas svarbus vertinant gydymo progesteronu ir kitais vaistais efektyvumą, taip pat ankstyvo persileidimo riziką. V: etinilestradiolis, geriamieji kontraceptikai. Kitų vyriškųjų ir moteriškųjų lytinių hormonų tyrimas aprašytas skyrelyje Antinksčių žievės hormonai. 373
375 MOLEKULINIAI NAVIKŲ ŽYMENYS IR JŲ NAUDOJIMAS LIGŲ DIAGNOSTIKAI Vė ž i o bi o l o g i j a ir pa p l i t i m a s Pasaulio sveikatos organizacijos duomenimis, kas penktos mirties priežastis yra vėžys. Europos ir įvairių šalių nacionalinės statistikos duomenimis, mirtingumo nuo vėžio ir kitų piktybinių navikų dažnis yra apie 25%. Tai antra po širdies ir kraujagyslių ligų mirties priežastis. Mirtingumas nuo vėžio, pradedant šio amžiaus pradžia, labai išaugo: 1909 m. jis buvo apie 4% mirčių priežastis, o 1990 m. apie 20%. Tokį padažnėjimą galima paaiškinti pailgėjusia gyvenimo trukme (vėžys dažnesnė vyresnio amžiaus žmonių liga, pavyzdžiui, vėžiu apie 10 kartų dažniau serga 70 metų amžiaus asmenys, palyginti su 25 metų žmonių populiacija). Įvairių lokalizacijų vėžio paplitimas skiriasi. Tačiau vyrų prostatos, plaučių (bronchų), storosios žarnos vėžys ir moterų krūties, storosios žarnos vėžys yra labiausiai paplitęs. Dažnėja moterų bronchų vėžys. Taip pat tarp abiejų lyčių dažnėja piktybinė odos melanoma, nors dėl geros diagnostikos mirtingumas nuo jos nedidėja. Vėžys tai ląstelių nenormalaus vystymosi ir dauginimosi liga. Kai šie procesai pradeda nepaklusti biologiniams reguliavimo mechanizmams, atsiranda piktybinė neoplazinė, t. y. vėžinė, ląstelė (karcinoma, gr. karkinos vėžys). Biologinių procesų, susijusių su ląstelės ciklu, angiogeneze ir apoptoze, taip pat patologinių neoplazinės transformacijos, naviko progresavimo ir metastazavimo procesų supratimas gali padėti atrasti navikų žymenis, juos pritaikyti vėžio diagnostikai ir gydymui. Ląs t e l i ų au g i m o r e g u l i a v i m a s, neoplazija ir hiperplazija Su ląstelių augimu ir vystymusi susiję du procesai: proliferacija ir diferenciacija. Abu jie yra reguliuojami vaisiui vystantis ir lemia ląstelių formą, dydį, taip pat ląstelių ir audinių bei organų funkciją. Ląstelių proliferaciją ir jų skaičiaus didėjimą valdo mechanizmai, reguliuojantys ląstelių ciklą ir apoptozę. Normalių ląstelių transformavimasis į navikines yra svarbiausia nekontroliuojamo jų augimo išdava. Vėžinės ląstelės pabėga nuo šių kontrolės mechanizmų ir tampa pavojingos šeimininko organizmui. 374
376 Molekuliniai navikų žymenys ir jų naudojimas ligų diagnostikai Ląstelių proliferacijos ir mirties pusiausvyros kontrolė lemia ląstelių skaičių ar jų populiacijų homeostazę. Ląstelėse veikia natūrali save savinaikos sistema, t. y. užprogramuotoji, arba fiziologinė, ląstelės žūtis apoptozė. Šis kontrolės mechanizmas įgalina augančio ir besivystančio organizmo audinių remodeliavimą, taip šalinamas ląstelių perteklius, netinkamu būdu išsivysčiusios ar genetiškai pažeistos ląstelės. Reikia skirti apoptozę nuo nekrozės, kuri irgi susijusi su ląstelių žūtimi. Tačiau nekrozė vyksta po ląstelės traumos ar kitokios pažaidos, kai ji greitai išburksta ir suyra. Vystantis nekrozei, pažeidžiamas ląstelės vientisumas, išsilaisvina jos turinys ir dėl to prasideda uždegiminis atsakas. Apoptozė nėra susijusi su uždegimu, tai reguliuojamas procesas. Dauguma suaugusiųjų audinių yra galutinės diferenciacijos stadijos. Tuo būdu baigia formuotis organai, kurie įgyja tam tikrą pastovų tūrį, formą, funkciją ir darnų augimo greitį. Suaugusio organizmo audiniai išsivysto per daugelį diferenciacijos etapų iš trijų pirminių gemalinių lapelių (sluoksnių): endodermos (vidinio, arba pirminio žarnų vamzdžio), ektodermos (atokiausio išorinio sluoksnio) ir mezodermos (vidurinio gemalinio lapelio). Galutinėje diferenciacijos stadijoje atsiradusi nauja augimo užuomazga reiškia hiperplaziją arba neoplaziją, o dėl to gali padaugėti arba atsirasti tam tikrų medžiagų. Svarbiausias šių dviejų panašių procesų skirtumas yra susijęs su augimo kontrole. Hiperplazija yra susijusi su organo ar audinio ląstelių skaičiaus didėjimu, dėl to padidėja organo masė. Nors vykstant hiperplazijai daugėja mitoziškai besidalijančių ląstelių ir intensyvėja DNR sintezė, tai yra kontroliuojamas procesas. Vystantis neoplazijai (gr. neoplasia audinio auglys, paprastai piktybinis), šie procesai tampa nekontroliuojami, tai nereguliuojama patologinė hiperplazija. Hiperplazijos metu navikų žymenų padaugėja laikinai, o esant neoplazijai tai ilgalaikis požymis (jei negydoma). Taigi nevaldoma proliferacija yra esminis visų neoplazinių ląstelių požymis, nepriklausantis nuo to, ar navikas gerybinis, ar piktybinis. Navikų augimo greitis atitinka diferenciacijos laipsnį piktybiniai navikai auga greičiau negu gerybiniai. Normalios ir vėžinės ląstelės skirtumai Dar 1956 m. O. Varburgas (Warburg) nustatė, kad glikolizės greitis vėžinėje ląstelėje yra daug didesnis negu sveikoje ląstelėje, kartu labai išauga ir šios medžiagų apykaitos fermentų aktyvumas. Todėl glikolizės fermentų aktyvumo padidėjimas gali būti vėžio žymuo. Tačiau šis padidėjimas nėra specifinis tik vėžinėms ląstelėms jis gali atspindėti reikšti ir nevėžinių ląstelių proliferacijos greitį. Vėžinės ląstelės nuo normalių skiriasi ir kitais požymiais: tokios ląstelės praranda savybę diferencijuotis, padidėja jų skverbimasis į aplinkinius audinius, mažėja jautrumas vaistams. Viena iš priežasčių yra nekontroliuojamas augimas. Taigi, kai 375
377 Sveika (normali) ląstelė Sutrikusi vystymosi reguliacija Vėžinė ląstelė Greita ląstelių proliferacija Dediferenciacija Padidėja normalių Karcinoembrioniniai baltymai, molekulių kiekis ektopiniai žymenys 40 pav. Vėžinės ląstelės požymiai sutrinka vienas iš dviejų ląstelės augimą (vystymąsi) reguliuojančių procesų diferenciacija ar proliferacija, yra rizika, kad normali ląstelė virs vėžine (40 pav.). Nekontroliuojama ląstelių proliferacija susijusi su nenormalios audinio masės susidarymu, ir tai yra navikas. Šiuo atveju padaugės įvairių molekulių, kaip fermentai, plazmos baltymai, hormonai ir metabolitai, kurios normaliai randamos kraujyje ir dėl to gali būti vertinamos kaip mažo specifiškumo navikų žymenys. Vėžinės ląstelės nuo normalių skiriasi ir savo paviršiaus komponentais, nes joms būdinga kontaktinė inhibicija. Proliferacijos greitis normalios ląstelės ir gerybinio naviko ląstelės skiriasi mažai. Tačiau gerybiniam navikui toliau vystantis ir tampant piktybiniu (pvz., vėžys), šie skirtumai darosi vis ryškesni. Be greitos proliferacijos, būdinga ir dediferenciacija. Vykstant šiam procesui, paprastai pradedami gaminti nauji produktai, kaip karcinoembrioniniai baltymai ar ektopinės molekulės, t. y. vėl pasirodo medžiagos, būdingos vaisiaus organizmui, kurios suaugusiame sveikame audinyje išnyksta. Tai rodo tolesnę naviko vystymosi stadiją, sutrikusį augimo reguliavimą ir blogą prognozę. Vis aiškėja, kad vėžys yra genetinė liga. Ląstelės genetinių komponentų pokyčiai lemia jos skirtingas savybes ir funkcijas. Svarbiausi požymiai, kurie skiria normalią ląstelę nuo vėžinės, atsiranda dėl įvairių ląstelės genetinio plano pakitimų, pavyzdžiui, onkogenų mutacijos ar nenormalaus jų raiškos reguliavimo, onkogeninės DNR sekos pokyčių. Proonkogenai, normaliose ląstelėse pažeisti ar dėl įvairių priežasčių nefiziologiškai aktyvinti, transformuojasi į onkogenus, o normali ląstelė virsta piktybine. Onkogenai gali indukuoti augimo faktorių ar jų receptorių ir DNR sujungiančių baltymų, kurie veikia genų ekspresiją ar dalyvauja ląstelės kontrolės mechanizme, gamybą. Žinomi šie proonkogenų transformavomosi į onkogenus aktyvinimo mechanizmai: 376
378 Molekuliniai navikų žymenys ir jų naudojimas ligų diagnostikai taškinės mutacijos, sustiprinančios genų produktų funkciją, proonkogenų amplifikacija, aktyvuotojo reguliacinio geno persikėlimas į proonkogeno kaimynystę, virusinio geno įsiterpimas. Vieno onkogeno aktyvavimo paprastai nepakanka, kad susifomuotų navikas šiame procese dalyvauja keletas veiksnių. Vėžys gali išsivystyti ir tais atvejais, kai savo funkciją praranda navikų slopinimo (stabdymo) genai. Pastarieji svarbūs ląstelių proliferacijai reguliuoti. Jų funkcijos praradimas skatina proliferaciją ar sutrikdo ląstelių diferenciaciją. Sukuriama vis daugiau tokių pažeistų genų ar jų gaminamų produktų aptikimo metodų. Gerybiniai ir piktybiniai navikai Piktybiniai navikai (navikas = auglys), kurie savo ląstelių kilme yra epiteliniai ir išsivysto iš bet kurio iš trijų gemalinių lapelių, yra vadinami vėžiu. Tai terminas, kuris savo pirmine reikšme buvo vartojamas apibūdinti uždegimo sukeltam patinimui. Normalios ląstelės transformavimasis (virsmas) į piktybinę susideda iš kelių etapų ir trunka mėnesius, metus (kartais 10, 20 metų). Pavyzdžiui, leukemijos dažnis padidėjo praėjus 5 metams po atominės bombos sprogimo Hirošimoje. Dauguma navikų pereina gerybinio naviko stadiją ir toliau progresuoja į piktybinį, o negydomi jie metastazuoja. Naviko vystymuisi nebūdinga viena priežastis. Karcinogenezė (piktybinis neoplazinis procesas vėžys) vystosi keliomis stadijomis, kurias savo ruožtu lemia veiksniai, priklausantys nuo individo genetinės struktūros, aplinkos veiksnių ir (ar) gyvensenos. Navikų susidarymą lemiantys veiksniai yra šie: 1. Biologiniai veiksniai: genetiniai, navikų virusai, pavyzdžiui, žmogaus papilomos, B hepatito, Epšteino Bar (Epstein Barr), žmogaus imunodeficito (ŽIV) virusai ir kt. 2. Cheminiai veiksniai vadinamieji karcinogenai: neorganinės medžiagos, metalai, jų druskos, asbestas, aromatiniai angliavandeniliai, pavyzdžiui, benzpirenas, azoto junginiai, pavyzdžiui, esantys tabako dūmuose, organinės natūralios medžiagos, pavyzdžiui, aflatoksinai iš pelėsinio grybo Aspergillus, esančio maiste. 3. Mityba (pavyzdžiui, rizika didėja kai trūksta A, C, E vitaminų, seleno, skaidulinių medžiagų). 377
379 4. Fizikiniai veiksniai: spinduliuotė: ultravioletiniai, gama spinduliai ar rentgeno spinduliai, mechaninis dirginimas, nudegimas. 5. Su amžiumi susiję veiksniai: dažnėja transkripcijos ir transliacijos klaidų. 6. Imuninės sistemos defektai. 7. Fiziologiniai veiksniai. Gerybinės stadijos navikas išlieka savo pirminėje vietoje ir, jį pašalinus, pacientas išgydomas. Todėl ankstyvoji gerybinių navikų diagnostika yra labai svarbi vėžio profilaktikai. Gerybiniai navikai yra geros diferenciacijos, juos sudaro ląstelės, panašios į pirminio audinio subrendusias normalias ląsteles. Todėl, matuojant tradicinius navikų žymenis, sunku atskirti normalias ir gerybinio auglio ląsteles. Piktybiniai navikai yra sudaryti iš įvairios diferenciacijos ląstelių: nuo gerai diferencijuojamų iki vyraujančių nediferencijuojamų. Tokios ląstelės yra praradusios savo specializaciją, t. y. piktybinių navikų ląstelės praranda proliferacijos ir diferencijacijos kontrolę. Į savo pirminę diferenciacijos stadiją sugrįžusios ląstelės pradeda gaminti tokias medžiagas kaip karcinoembrioniniai baltymai, kurių randama vaisiaus audiniuose. Vėžio progresavimas ir metastazavimas Vystydamasis vėžys paprastai pereina šias stadijas: carcinoma in situ, mikroinvazinis vėžys, invazinis vėžys, išplitimas į sritinius limfinius mazgus, ir paskutinė metastazuojantis į tolimus (atokius) organus, dažniausiai kepenis, plaučius, smegenis, kaulus, vėžys. Tolesnį vėžinės ląstelės vystymąsi lemia jos proliferacinis aktyvumas, kurį gali apibūdinti tokie prognoziniai žymenys kaip DNR kiekis, augimo baltymai, jų receptoriai, onkogenai ar jų produktai. Dauguma mirčių nuo vėžio yra susijusios su metastazine liga. Kaip jau minėta, dauginiai genetiniai pokyčiai yra svarbiausia sutrikusio reguliavimo priežastis, sukelianti nekontroliuojamą proliferaciją. Tačiau, kad navikas įgautų savybę plisti, būtini papildomi genetiniai pažeidimai. Jie gali būti susiję su onkogenų aktyvinimu, negatyvių efektorių praradimu (slopinimo genai), navikinių ląstelių prisitvirtinimu prie šeimininko ląstelinio ar neląstelinio užpildo, pamatinės membranos proteolize ir kitais. Tie proliferacijos, invazijos ir metastazavimo veiksniai yra nepriklausomi vienas nuo kito ir yra su metastazavimo procesu susiję žymenys. 378
380 Molekuliniai navikų žymenys ir jų naudojimas ligų diagnostikai Navikų augimas ir metastazavimas priklauso nuo angiogenezės intensyvumo, t. y. navikas turi nuolat skatinti naujų kapiliarų augimą, kad augtų ir jis pats. Šiam tikslui navikas sintetina angiogenezės stimuliatorius; taip gali atsitikti ir sumažėjus angiogenezę slopinančių veiksnių gamybai. Taigi įvertinus angiogenezės aktyvumą, galima anksti diagnozuoti naviką. Vė ž i o di a g n o s t i k o s, k l i n i k o s, gydymo bei ligos prognozės ypatybės Diagnozuoti ankstyvosios stadijos vėžį yra sunku, nes dažnai šioje stadijoje simptomų dar nėra ir pacientas laiku nesikreipia į gydytoją. Dėl to dauguma diagnostinių procedūrų ankstyvajai vėžio diagnostikai netinka: pavyzdžiui, anamnezė, fizinis, rentgeninis ištyrimas ar bendras kraujo tyrimas. Šiais metodais naviką galima aptikti jau 1 2 cm dydžio, o tada jį sudaro jau daugiau kaip 1 milijardas ląstelių. Galimi vėžio simptomai yra susiję su obstrukcija, padidėjusiu spaudimu į normalius audinius ar jų destrukcija. Atsižvelgiant į ligos etapą, t. y. naviko tipą, išplitimą, masę ir ligonio būklę, galimi įvairūs gydymo būdai ir jų deriniai: chirurginis, spindulinė terapija, chemoterapija, gydymas hormonais, imunoterapija. Gydymo būdo parinkimui įtakos turi ir prognozė tai ligos eigos ir išgyvenamumo įvertinimas. Pavyzdžiui, bloga ligos prognozė reiškia, kad tolesnė chemoterapija, jei ji blogai toleruojama ir pacientui sukelia stresą, neindikuojama. Ligos prognozei svarbu žinoti naviko masę, ląstelių diferenciacijos laipsnį, proliferacijos greitį, ar įtraukti limfmazgiai, ar yra metastazių. Jau seniai bandoma rasti žymenų, iš kurių būtų galima kiek įmanoma anksčiau aptikti navikinę ląstelę. Na v i k ų žy m e n y s: b e n d r y b ė s Apibrėžimas. Terminu naviko žymuo apibrėžiama didelė grupė medžiagų, kurias gamina piktybinė ląstelė ar kaip atsaką į neoplaziją (piktybinį darinį ar procesą) gerybinė ląstelė ir kurias galima išmatuoti organizmo skysčiuose ir audiniuose (taip pat įlietuose į parafiną) turint tikslą: 1) nustatyti piktybinį procesą, 2) identifikuoti piktybinį naviką, kad būtų įvertinta ligos prognozė ir parinktas tinkamiausias gydymas, 3) įvertinti gydymo veiksmingumą. Navikų žymenų gali būti randama ląstelių citoplazmoje ar branduolyje, jie gali būti susiję su ląstelės paviršiaus membrana ar cirkuliuoti kraujyje, o jų atsiradimas ir koncentracijos kitimas tam tikra prasme yra susijęs su piktybinio auglio geneze ir augimu. Taigi idealiu atveju naviko žymuo turi būti išmatuojamas kraujyje tik po to, kai normali ląstelė transformavosi į piktybinę. 379
381 Navikų žymenų paieška jau turi savo istoriją metais buvo nustatytas pirmasis žymuo Bens-Džonso baltymas. Tai imunoglobulinų lengvosios grandinės, kurios perteklingai gaminasi sergant mielomine liga. Ypač daug navikų žymenų įvardyta paskutiniais dešimtmečiais: tai fermentai, izofermentai, glikoproteinai, metabolitai, hormonai, ląstelių ir branduolių membranų receptoriai, adhezijos molekulės, citokinai, onkogenai, navikų slopinimo genai, angiogenezės ir metastazavimo veiksniai. Navikų žymenų kriterijai. Idealaus naviko žymens požymiai: didelis specifiškumas, t. y. jo neaptinkama esant gerybiniam augliui ar sveikame organizme (100% specifiškumas reiškia, kad juo remiantis nustatysime visus asmenis, turinčius specifinį naviko tipą ir jo nerasime sergančiųjų gerybiniu naviku organizme); didelis jautrumas, t. y. jį galima aptikti labai anksti, kai yra dar tik kelios vėžinės ląstelės (100% jautrumas reiškia, kad jis turi būti nustatomas visiems šio naviko tipą turintiems asmenims); būti organui specifinis; koreliuoti su naviko išsivystymo laipsniu ir mase (dauguma šiuo metu žinomų navikų žymenų koreliuoja su naviko išsivystymo laipsniu, t. y. žymens koncentracija didėja augant masei); koreliuoti su ligos prognoze; būti patikimai nustatomas. Vertinant tyrimo jautrumą ir specifiškumą, reikia žinoti kai kuriuos terminus. Specifiškumas tai galimybė tyrimu atskirti nesergančius vėžiu asmenis nuo sergančiųjų (pripažinti sveikus asmenis sveikais), t. y. sveikų ar turinčių gerybinį naviką asmenų procentas, kuriems tyrimo rezultatas yra teisingai neigiamas. 100% specifiškumas reiškia, kad nėra klaidingai teigiamų rezultatų ir žymenį galima taikyti pacientų atrankai populiacijoje. Specifiškumas = tikrai neigiamų rezultatų skaičius tikrai neigiamų rezultatų skaičius + klaidingai teigiamų 100% rezultatų skaičius Jautrumas tai gebėjimas tyrimu aptikti sergančius vėžiu pacientus (atpažinti ligą kaip tikrai esančią), t. y. tyrimo rezultatų, kurie esant navikui yra teisingai teigiami, procentas. 100% jautrumas reiškia, kad nėra klaidingai neigiamų rezultatų ir žymenį galima taikyti vėžio diagnostikai, juo remiantis vertinti gydymo veiksmingumą, toliau tirti pacientus. Jautrumas = tikrai teigiamų rezultatų skaičius tikrai teigiamų rezultatų skaičius + klaidingai neigiamų 100% rezultatų skaičius 380
382 Molekuliniai navikų žymenys ir jų naudojimas ligų diagnostikai Jautrumas ir specifiškumas yra atvirkščiai susiję ir matuojami pagal viršutinę rekomenduojamą tam tikro naviko žymens normos ribą (ribinę reikšmę, angl. cut off value). Dažniausiai ribinė reikšmė yra ties 95% riba tų žymens reikšmių, kurios nustatomos tiriamojoje žinomų sergančiųjų vėžiu populiacijoje. Ribinė reikšmė tai naviko žymens koncentracija, kuria remiantis sveiki asmenys skiriami nuo sergančiųjų. Žymenų, pasižyminčių 100% specifiškumu (kai jis nenustatomas sveikiems ar turintiems gerybinį naviką asmenims) ir 100% jautrumu (visada nustatomas ankstyvosios vystymosi stadijos navikas, t. y. nėra klaidingai neigiamų rezultatų) beveik nėra. Klinikinė navikų žymenų reikšmė ir panaudojimas Pacientų atranka. Pripažinta, kad jei pirminiu naviko nustatymu metastazių nerandama, tai yra didelė tikimybė tokį pacientą išgydyti. Todėl ankstyvoji diagnostika ar pacientų atranka dar iki ligos simptomų atsiradimo yra labai svarbi. Dažniausiai navikų žymenų koncentracija padidėja prieš kelis mėnesius iki simptomų atsiradimo. Be to, navikų žymenų kraujyje nustatymas yra neinvazyvus, palyginti nebrangus, vienu metu galima ištirti daug asmenų. Tačiau dauguma šiuo metu žinomų navikų žymenų reikiamu jautrumu ar specifiškumu neišsiskiria, kad juos būtų galima naudoti pacientų atrankinei patikrai. Pavyzdžiui, padidėjusi karcinoembrioninio antigeno (CEA) koncentracija nustatoma sergant ir kitais, ne tik storosios ir tiesiosios žarnos, navikais, taip pat kitomis ligomis bei sveikiems individams. Todėl šiuo metu navikų žymenys beveik nenaudojami neturinčių ligos simptomų asmenų atrankai, nes šiais atvejais tyrimo specifiškumas ir jautrumas yra labai mažas. Ir priešingai, navikų žymenys naudojami tam tikrų asmenų grupių atrankai (pvz., esant rizikos veiksniams) ar atrankai asmenų, kurie turi ligos simptomų, pavyzdžiui, α fetoproteinas (AFP) kepenų cirozės ir pirminio kepenų vėžio rizikos diferenciacijai; kalcitoninas esant šeiminei skydliaukės C ląstelių vėžio rizikai. Pirminė diagnostika. Daugelis šiuo metu tiriamų navikų žymenų negali padėti atskirti piktybinės ligos nuo gerybinio naviko, nes jų jautrumas ir specifiškumas yra nepakankamas. Tačiau šie tyrimai papildo kitus diagnostikos metodus, be to, taip tobulinami ir patys metodai. Pirminei diagnostikai gali būti naudojami β žmogaus chorioninis gonotropinas (β-hcg), α fetoproteinas, kalcitoninas. Vėžio lokalizacijos nustatymas. Navikų žymenimis gali būti nustatoma proceso lokalizacija, t. y. jie yra organui specifiniai, pavyzdžiui, prostatos specifinio antigeno (PSA) ar prostatos rūgščiosios fosfatazės (PRA) padidėjimas rodo prostatos ligą, tiroglobulinas yra specifinis skydliaukės žymuo. Ligos etapo (pažeidimo laipsnio) nustatymas. Kai kurie navikų žymenys yra susiję su proceso išsivystymo laipsniu, t. y. su piktybinių ląstelių mase ir metastazė- 381
383 mis. Pavyzdžiui, padidėjęs karcinoembrioninis antigeno kiekis sergant storosios žarnos vėžiu, atsinaujinęs tiroglobulino koncentracijos padidėjimas po tiroidektomijos rodo ligos progresavimą. Prognozė. Kai kurie žymenys turi svarbią prognozinę vertę. Didelė ar didėjanti karcinoembrioninio antigeno koncentracija rodo blogą prognozę. Ligos prognozė vertinama iš žymens koncentracijos prieš ir po gydymo. Paciento gydymo efektyvumo vertinimas ir tolesnė stebėsena. Tai viena svarbiausių navikų žymenų nustatymo indikacijų. Gydymo metu galima tirti tris navikų žymenų kiekio kitimo priežastis: žymens kiekio sumažėjimas iki rekomenduojamos normos rodo pagijimą ar viso naviko pašalinimą, ar remisiją; naviko žymens pastovi patologinė koncentracija po menko ir trumpalaikio jos sumažėjimo ar naujas padidėjimas po jos sumažėjimo rodo, kad yra likusių vėžinių ląstelių ar jau išplitusios metastazės; atsinaujinęs naviko žymens kiekio padidėjimas po jo normalizavimosi gydant rodo atsinaujinusią ligą. Bendro pobūdžio pastabos dėl navikų žymenų taikymo: 1. Naviko žymens kitimų kinetika yra svarbesnė negu individualios jo reikšmės; koncentracijos padidėjimas, net jei ir neviršija rekomenduojamų normos ribų, yra svarbus žymuo. 2. Naviko žymens kiekio kartotinis nustatymas yra svarbus diferencijuojant piktybinį auglį nuo gerybinio, kai gali būti tik trumpalaikis (nepastovus) žymens koncentracijos padidėjimas ar kiekis, nedaug viršijantis rekomenduojamą normą. 3. Naviko žymens kiekio teigiamas kartotinis tyrimo rezultatas gali padėti išsiaiškinti jo tipą, lokalizavimąsi ir metastazes, pavyzdžiui, greitas karcinoembrioninio antigeno koncentracijos didėjimas po operacijos (>4ng/ml/6 mėn.) rodo galimas metastazes kauluose, kepenyse, o lėtas didėjimas (<2 4 ng/ml/ 6 mėn.) dažniau metastazavimą į smegenis ar minkštuosius audinius. 4. Naviko žymenų kiekio nustatymas priklauso nuo naviko bei metastazių antigenų heterogeniškumo, t. y. galimos ir tokios metastazės, kurios nustoja gaminti (išskirti) naviko antigenus, nes prarado antigeniškumą. 5. Naviko žymens kiekis kraujo serume priklauso nuo jo gamybos, sekrecijos, naviko aprūpinimo krauju ir žymens šalinimo. Šalutinis poveikis navikų žymenims. Šis poveikis žymeniui galimas pačiame organizme (in vivo), pavyzdžiui: naviko žymens kiekis gali padidėti sutrikus jo šalinimui dėl inkstų, kepenų veiklos nepakankamumo, esant cholestazei; nespecifinis poveikis naviko žymenų kiekiui pasitaiko intensyvaus gydymo pradžioje, kai ýra daug ląstelių; 382
384 Molekuliniai navikų žymenys ir jų naudojimas ligų diagnostikai žymenų kiekio gali svyruoti sutrikus kraujotakai navike; po tyrimo per rectum padidėja prostatos specifinio antigeno, prostatos rūgščiosios fosfatazės kiekis, taigi netirti prieš imant kraujo tyrimui; vaistų poveikis, pavyzdžiui, antiandrogeninis gydymas, sergant prostatos vėžiu, slopina prostatos specifinio antigeno gamybą. Tiriamosios medžiagos ėmimo (in vitro) poveikis, pavyzdžiui: jei normaliai naviko žymuo sekretuojamas ir skiriasi su prakaitu, seilėmis ir kitais organizmo skysčiais, tai galima užteršti ėminį ir gauti klaidingai padidėjusį žymens kiekį; ėminio laikymo sąlygos: dažnai naviko žymuo nustatomas ne tik kraujo serume, bet ir eritrocituose, plazminėse ląstelėse, trombocituose, taigi jų kiekis kraujyje gali padidėti palikus kraują stovėti ilgesnį laiką (60 90 min.) iki centrifugavimo; žymens stabilumas: kiekvienas vėžio žymuo turi savo biologinį gyvavimo laiką, t. y. per tam tikrą laiką jis suyra, pavyzdžiui, prostatos specifinio antigeno gyvavimo puslaikis yra 2 4 dienos, α fetoproteino, karcinoembrioninio antigeno 2 8 dienos, žmogaus chorioninio gonotropino β grandinės 1 diena, o prostatos rūgščioji fosfatazė suyra per kelias valandas, jei serumas laikomas kambario temperatūroje. Navikų žymenų klasifikacija Navikų žymenis galima klasifikuoti įvairiai. Pagal biocheminę prigimtį skiriami hormonai, pavyzdžiui, žmogaus chorioninis gonadotropinas, kurį sekretuoja choriokacinoma; fermentai, pavyzdžiui, prostatos rūgščioji fosfatazė, kurią gamina prostatos vėžinė ląstelė; navikų antigenai, pavyzdžiui, chorioembrioninis antigenas. Pagal kitą klasifikaciją navikų žymenys gali būti suskirstyti į du tipus: ląsteliniai ir humoraliniai. Ląsteliniai navikų žymenys. Piktybinė ląstelė pasižymi nekontroliuojamu augimu, taigi bet kuri medžiaga, kuri yra susijusi su ląstelės ciklo, apoptozės, angiogenezės ar metastazavimo reguliavimu, gali būti naviko žymuo metais T. Kaspersonas (Casperson) kiekybinės vaizdo citometrijos metodu naviko ląstelėse nustatė padidėjusį nukleorūgščių kiekį, ir nuo tada tėkmės citometrija tapo svarbiausiu tokių žymenų tyrimo metodu. Tokiems žymenims priklauso leukemijų žymenys, hormonų ir augimo veiksnių receptoriai, molekulinių genetinių pokyčių žymenys. Humoraliniai navikų žymenys. Tai medžiagos ir molekulės, kaip ląstelės apykaitos ir jos aktyvumo išraiška, kurių aptinkama koncentracija viršija kraujo serume, šlapime ir organizmo skysčiuose fiziologinėmis sąlygomis randamą kiekį. Jas gami- 383
385 na ir sekretuoja navikinis audinys arba jų išsiskiria audiniui yrant, ar susiformuoja kaip organizmo atsakas į naviką. Tai fermentai, baltymai, metabolitai, hormonai. Šių medžiagų fiziologinė funkcija yra gerai žinoma, jos svarbios normaliai medžiagų apykaitai, dėl to jų randama ir sveikų asmenų kraujyje. Padidėjęs šių medžiagų kiekis randamas sergant ir piktybiniais, ir nepiktybiniais navikais, t. y. nėra specifinis vėžiui. Tačiau padidėjusi tokių medžiagų koncentracija sergančiųjų vėžiu kraujyje gali būti susijusi su piktybiniu ląstelių daugėjimu. Normaliai ląstelei transformuojantis į piktybinę, kai kurie baltymai, kurie normaliame ląstelės vystymosi procese nedalyvavo, navikinėje ląstelėje gali būti reaktyvuoti. Gerybinių navikų gaminami žymenys paprastai ląstelei yra specifiški, susiję su normaliais ląstelės produktais, bet randami padaugėję. Kai gerybinis navikas progresuoja ir tampa agresyvus, ląstelių kontrolė susilpnėja dar labiau ir pradeda gamintis baltymai, kurie randami tik vaisiaus vystymosi stadijoje, pavyzdžiui, karcinoembrioniniai baltymai. Kai kurie šių žymenų yra susiję su naviku, bet navikui nespecifiški. Da ž n i a u s i a i tiriami na v i k ų žy m e n y s ir jų taikymas klinikinėje praktikoje Karcinoembrioninis antigenas (CEA). Pirmą kartą karcinoembrioninį antigeną aprašė P. Goldas ir S. O. Freedmanas 1965 metais. Tai glikoproteinas, kurio molekulinė masė apie daltonų ir kuris yra sudarytas iš 40% baltymų ir 60% angliavandenių. Tai vienas antigenų, gaminamas gleives sekretuojančių liaukų epitelinėse besivystančio embriono ir vaisiaus ląstelėse. Po gimimo šio baltymo sintezė yra slopinama, ir suaugusiųjų organizme CEA koncentracija yra labai maža. Su CEA susijusius antigenus koduoja genų šeima, esanti 19 chromosomos ilgajame petyje (19q ). Vienas iš jos genų grupės koduojamų baltymų ir yra karcinoembrioninis antigenas. Manoma, kad CEA, susijungęs su ląstelių membrana, naudojamas tarpląstelinio atpažinimo mechanizmuose. Taip pat šiam baltymui priskiriamas imunitetą slopinantis poveikis. CEA gyvavimo kraujyje puslaikis 2 8 dienos. CEA pirmą kartą identifikuotas embriono storosios žarnos audinyje. Mažas šio baltymo kiekis aptinkamas normaliame žarnų audinyje (gleivinėje), egzokrininėje kasos dalyje, seilių liaukose, kepenyse, prostatoje, gimdos kaklelyje. Didžiausia koncentracija yra nustatyta vaisiaus virškinamajame trakte ir kasoje, taip pat pacientų, sergančių virškinamojo trakto, kasos, krūties, plaučių, skydliaukės, šlapimo ir lytinių takų vėžiu, kraujo serume. CEA koncentracija gali kiek padidėti sergant gerybinėmis ligomis: žarnų uždegimu, kepenų ciroze, pankreatitu, pneumonija. Rūkalių kraujyje ir nesant piktybinio proceso CEA koncentracija yra didesnė, palyginti su nerūkančiųjų. Svarbiausia CEA nustatymo indikacija yra gydymo efektyvumo vertinimas ir pacientų, sergančių virškinamojo trakto, kasos, krūties, plaučių, skydliaukės, šlapimo 384
386 Molekuliniai navikų žymenys ir jų naudojimas ligų diagnostikai ir lytinių takų vėžiu, stebėsena vertinant ligos progresavimą. CEA koncentracija koreliuoja su naviko išsivystymo laipsniu. Po naviko pašalinimo operacijos CEA kiekis per 6 8 savaites sumažėja iki normalaus. Naujas CEA didėjimas rodo piktybinio proceso pasikartojimą ar metastazes. Laipsniškas didėjimas (2 4 ng/ml per 6 mėn.) dažniau pasikartoja toje pačioje vietoje, o greitas didėjimas dažniau rodo metastazavimą. Anksti nustačius šį vėžį ir gydant, išgyvenamumas yra apie 90%. Tačiau dažniausiai ši liga diagnozuojama jau tada, kai išplinta, ir tuomet gydymas tampa sudėtingas. CEA nerekomenduojama nustatyti atrankiniam storosios ir tiesiosios žarnos vėžio tyrimui. Taip pat nerekomenduojama tirti iš karto po operacijos, nes jos metu į kraują išsiskiria didelis šių molekulių kiekis ir tai gali klaidinti vertinant gydymą. CEA tyrimas smegenų skystyje gali padėti patikimai nustatyti piktybinę meningiomą, nors nerasta koreliacijos tarp CEA sintezės greičio ir naviko ląstelių masės smegenų skystyje. CEA koncentracija sveikų nerūkančiųjų kraujo serume yra <2,5 mg/l (moterims) ir <3,4 mg/l (vyrams); rūkalių atitinkamai <4,9 ir <6,2 mg/l. α fetoproteinas (AFP). Tai glikoproteinas, sudarytas iš vienos polipeptidinės grandinės, turinčios 590 aminorūgščių liekanų. Jo molekulinė masė apie daltonų. Angliavandeninė dalis sudaro 2,5% tai sialo rūgšties liekana metais C. G. Bergstrandas ir B. Czaras aptiko α fetoproteiną vaisiaus serume, o 1963 metais G. I. Abelevas aprašė jį kaip su naviku susijusį baltymą. AFP sintetinamas vaisiaus kepenyse, vaisiaus trynio maiše ir sekretuojamas į serumą. Didžiausia sekrecija yra 13-ą nėštumo savaitę, vėliau nuosekliai mažėja. α fetoproteino fizikocheminės savybės ir 39% aminorūgščių sekõs yra panašūs į žmogaus albumino. Todėl manoma, kad šis baltymas atlieka tokių molekulių kaip estrogenai, riebalų rūgštys nešiklio funkciją. Taip pat nustatytas imunosupresinis poveikis nėštumo metu: α fetoproteinas apsaugo vaisiaus organizmą nuo motinos estrogenų veiklos, taip pat nuo audinių atmetimo ir yra vėliau atsirandančio albumino pakaitalas. Gyvavimo kraujyje puslaikis 2 8 dienos. Normaliai šį baltymą galima nustatyti vaisiaus kepenyse ir trynio maiše. Suaugusių sveikų asmenų organizme jo yra tik pėdsakai. AFP koncentracija smarkiai padidėja sergant pirminiu kepenų ląstelių vėžiu (hepatoma), kuris dažniausiai išsivysto po kepenų cirozės ar lėtinio hepatito. Šis žymuo gali būti naudojamas atrankiniams pirminio kepenų vėžio tyrimams, siekiant anksti diagnozuoti ligą. Padidėjęs AFP kiekis randamas daugiau kaip 90% hepatoma sergančių pacientų. Nurodoma AFP koncentracija tokiais atvejais yra didesnė kaip 1000 ng/ml, kartais siekia ir net ng/ml. AFP koncentracija taip pat padidėja esant embrioniniams, pavyzdžiui, trynio maišo, navikams. Nustatyta tiesioginė koreliacija tarp AFP kiekio serume ir ligos 385
387 išsivystymo laipsnio sergant pirminiu kepenų ląstelių vėžiu ir ne iš sėklidžių kilusiu sėklidžių vėžiu. Pažymėtina, kad grynosios seminomos, disgerminomos ir diferencijuotosios teratomos dažniausiai yra AFP neigiamos, o trynio maišo navikas visada yra AFP teigiamas. Embrioninių navikų diagnostikai lygiagrečiai su AFP turi būti tiriama ir žmogaus chorioninio gonadotropino (žchg) koncentracija, nes gydant gali kisti žymens tipas. Didelė AFP koncentracija rodo didelę naviko masę ir blogą ligos prognozę. Po operacinio naviko pašalinimo AFP ir (ar) žchg koncentracijos augimas rodo ligos progresavimą, kuris nustatomas prieš keletą mėnesių iki kitų galimų diagnostinių procedūrų. Taigi šis radinys gerokai paankstina gydymą. Padidėjusi AFP koncentracija randama ir esant kitos lokalizacijos navikams: skrandžio, storosios žarnos, tulžies pūslės ir takų, kasos, bei metastazėms į kepenis. Diferencijuojant pirminį kepenų vėžį ir jo metastazes į kepenis bei kitos lokalizacijos navikus, gali padėti α fetoproteino tyrimas kartu su karcinoembrioninio antigeno nustatymu: mažas AFP kiekis, esant didelei CEA koncentracijai, būdingesnis metastazėms kepenyse. α fetoproteino gali padaugėti sergant gerybinėmis ligomis: hepatitu, kepenų ciroze, Krono liga, polipoze. AFP nustatymas nėštumo metu padeda vaisiaus nervinio vamzdžio nesuaugimo defektų diagnostikai. Kitoms vaisiaus ligoms, pavyzdžiui, inkstų anomalijos, omfalocelė, taip pat būdingas AFP padidėjimas motinos kraujyje. Sumažėjęs AFP kiekis motinos kraujo serume gali būti rastas esant Dauno sindromui, savaiminiam persileidimui, pūslinei išvisai. Sveikų vyrų ir nenėščių moterų kraujo serume α fetoproteino koncentracija paprastai yra 0,56 2,64 ku/l. Žmogaus chorioninis gonadotropinas (žchg). Tai sialoglikoproteinas, kurio molekulinė masė yra apie daltonų. Baltymo struktūra primena liutropino, folitropino ir tirotropino struktūrą. Šie hormonai savo molekulėje turi 7 25% angliavandenių, prisijungusių N glikozidiniu ryšiu, ir yra sudaryti iš dviejų grandinių: α ir β, susijungusių nekovanlentiniu ryšiu. α grandinės yra identiškos, o β grandinės skiriasi. žchg-β grandinė tai sialoglikoproteinas, sudarytas iš 180 aminorūgščių. žchg ir LH-β grandinėje pirmosios 150 aminorūgštys yra 80% homologiškos; žchg-β grandinėje yra papildomas peptidas C gale, sudarytas iš 30 aminorūgščių. Šie β grandinės skirtumai ir lemia biologines savybes ir hormonų specifiškumą. žchg-β grandinės biologinis gyvavimo puslaikis yra valandos. Sveikų nėščių moterų serume galima rasti įvairių formų žchg: intaktinį (sudaro 92 98%), tik α grandinę (iki 7%), tik β grandinę (iki 3%) ir iš dalies suskaidytą, pavyzdžiui, įkirptasis žchg ar β grandinės fragmentai. Nėštumo pradžioje moterų šlapime daugiausia yra β grandinės fragmentų (~50%), mažiau intaktinio (~35%) ir įkirptojo (~10%) žchg. 386
388 Molekuliniai navikų žymenys ir jų naudojimas ligų diagnostikai Nėštumo pradžioje žchg yra sintetinamas besivystančio blastocito trofoblastinėse ląstelėse, o vėliau, nuo 3-ios savaitės pabaigos, placentos sincitiotrofoblastinėse ląstelėse. žchg yra atsakingas už geltonkūnio palaikymą ir taip užtikrina progesterono ir estrogenų sintezę, būtiną gimdos gleivinės proliferacijai. Vyrų organizme žchg gamina trofoblastinės ląstelės. žchg tyrimas atliekamas ankstyvam nėštumui (6 8 dienos po pastojimo), nėštumo laikui nustatyti bei stebėsenai. žchg koncentraciją rekomenduojama tirti rizikos grupių moteris, įtarus ektopinį nėštumą ar jei iš anamnezės žinomas ektopinis nėštumas, gresiantis persileidimas ar pūslinė išvisa. Tai gali padėti anksti aptikti piktybinį trofoblastinį naviką. Esant placentos trofoblastiniam navikui, žchg koncentracija smarkiai padidėja. Kaip navikų žymuo žchg tiriamas gemalo navikų (sėklidžių ir kiaušidžių) diagnostikai ir jų stebėsenai. Ištirta, kad esant navikams aptinkama didelė žchg laisvosios β grandinės koncentracija, todėl rekomenduojama tirti ne bendrojo žchg, bet jo laisvosios β grandinės koncentraciją. Pažymėtina, kad grynosios choriokarcinomos visada yra žchg teigiamos ir AFP neigiamos, o trynio maišo navikai AFP teigiami ir žchg neigiami. žchg ir AFP reikia tikrinti pirmus dvejus metus po gydymo, nes daugumai ligonių kaip tik tuo metu liga atsinaujina. Esant trofoblastiniam ir gemalo navikui, žchg koncentracija koreliuoja su naviko išsivystymo laipsniu, mase ir ligos prognoze. Sveikų vyrų kraujyje žchg kiekis yra <1,1 U/l, nenėščių sveikų moterų <2,7 U/l; nėščių moterų jis priklauso nuo nėštumo laiko. Navikų mucininiai žymenys: CA 15-3, CA 19-9, CA 50, CA 125. Šios glikoproteinų šeimos vėžio navikų žymenys turi didelę molinę masę. Oligosacharidinės grandinės yra prisijungusios prie polipeptidinės grandinės. Dauguma monokloninių antikūnų, kuriais aptinkami audinių mucinai, veikia prieš molekulių baltymines šerdis. Tačiau kai kurie antikūnai atpažįsta angliavandeninius epitopus. Navikinių ląstelių membranų paviršiaus angliavandeniuose yra daugiau glikanų, ir tai lemia sumažėjusią ląstelių adheziją, padidėjusį jų invazyvumą ir metastazinį potencialą. Naviko žymuo vėžio antigenas 15-3 (CA 15-3). Tai didelės molekulinės masės į muciną panašus antigenas, kuris atsipalaiduoja iš krūties vėžio ląstelių ir kai kurių epitelinių ląstelių į kraują, kitus organizmo skysčius. Normaliai šio antigeno yra tik pėdsakai (neturi viršyti 40 ku/l), jo funkcija nežinoma. Svarbiausia žymens tyrimo indikacija tai sergančiųjų krūties vėžiu tikrinimas, gydymo efektyvumo verinimas, taip pat jis naudojamas įtarus ligos atsinaujinimą ar ieškant krūties vėžio metastazių. Padidėjęs CA 15-3 kiekis randamas ir sergant bronchų, kiaušidžių, kasos, storosios žarnos vėžiu. CA 15-3 kiekis gali padidėti sergant kepenų ciroze, hepatitu, taip pat kiaušidžių, plaučių ir krūties ligomis. 387
389 Naviko žymuo angliavandeninis antigenas 19-9 (CA 19-9). Tai oligosacharidas, kuris audiniuose įsijungia į glikoproteinų sudėtį (monosialogangliozidas), o serume esti prisijungęs prie baltymų, yra didelės molinės masės mucinas (molekulinė masė daugiau kaip 1 milijonas daltonų). CA 19-9 buvo išskirtas iš storosios žarnos vėžinių ląstelių. Šis antigenas taip pat yra susijęs su Liuiso (Lewis) kraujo grupės antigenu. CA 19-9 antigenas yra randamas vaisiaus skrandžio, plonosios ir storosios žarnos epitelyje, kepenyse, kasoje. Jis yra daugelio mukozinių ląstelių ir jų sekrecijos produktų komponentas. Tačiau suaugusiųjų organizme jo tik pėdsakai nustatomi kasoje, kepenyse, tulžies pūslėje ir plaučiuose. CA 19-9 yra pirminis kasos vėžio žymuo. Nustatyta koreliacija tarp šio antigeno koncentracijos serume ir naviko dydžio. Taip pat jis naudojamas su CEA kaip antrinis žymuo esant tulžies pūslės, storosios žarnos bei skrandžio vėžiui, metastazėms kepenyse (labai didelė CA 19-9 koncentracija būdingesnė hematogeninės kilmės metastazėms). CA 19-9 padidėjimas nustatytas sergant šiomis gerybinėmis ligomis: ūminiu hepatitu, lėtiniu aktyviuoju hepatitu, tulžies pūslės ir takų ligomis, pankreatitu, cistine fibroze, reumatu. Šio antigeno gyvavimo puslaikis apie 7 val. (ląstelių kultūroje). Sveikų asmenų kraujyje CA 19-9 kiekis yra < 37 ku/l. Naviko žymuo angliavandeninis antigenas 50 (CA 50). Tai tiesioginis CA 19-9 pirmtakas: CA 19-9 iš CA 50 pasigamina prisijungiant fukozei: Oligosacharidas + N acetilneuramino rūgštis Oligosacharidas + Fukozė CA 50 CA 19-9 Antikūnai prieš CA 50 buvo gauti imunizuojant storosios žarnos vėžio ląsteles. Šio žymens klinikinis pritaikymas yra toks, kaip ir žymens CA 19-9, t. y. naudojamas sergant storosios žarnos, kasos vėžiu. Jų derinys nėra pranašesnis nei naudojamų pavieniui. CA 50 kiekio padidėjimas taip pat nustatomas sergant plaučių, gimdos, prostatos, rečiau krūties, šlapimo, lyties organų vėžiu. Sveikų asmenų kraujyje CA 50 koncentracija įvairuoja atsižvelgiant į metodą: <16 ku/l arba <23 ku/l. Naviko žymuo vėžio antigenas 125 (CA 125). Tai didelės molekulinės masės glikoproteinas, kurio molekulinė masė yra apie daltonų, o angliavandeniai sudaro apie 25% procentus. CA 125 kraujyje yra susijungęs su kitais glikoproteinais, todėl bendra molekulinė masė viršija 1 milijoną daltonų. CA 125 yra identifikuojamas pagal jo reakciją su monokloniniu antikūnu OC 125. Šis antikūnas buvo gautas hibridinant pelės mielomos ląsteles su pelės blužnies ląstelėmis, kurios buvo imunizuotos žmogaus serozinės cistadenomos ląs- 388
390 Molekuliniai navikų žymenys ir jų naudojimas ligų diagnostikai telių linija OVCA 433. Monokloninis antikūnas OC 125 reaguoja su pasikartojančiomis CA 125 antigeno determinantėmis. Biologinis gyvavimo kraujyje puslaikis 2 6 dienos. CA 125 randamas vaisiaus epiteliniuose dariniuose, taip pat serozinėse kiaušidžių vėžio ląstelėse ir serozinės adenokarcinomos audinyje. CA 125 kiekis kraujyje padidėja sergant gimdos kaklelio vėžiu, taip pat storosios žarnos, krūties ir plaučių vėžiu. Taigi CA 125 nustatymas yra svarbus diferencijuojant gerybinį kiaušidžių naviką nuo piktybinio. CA 125 koncentracija koreliuoja su naviko mase. Dažniausiai juo nustatomas gydymo efektyvumas ir atliekama pacientų, sergančių kiaušidžių vėžiu, stebėsena. CA 125 rekomenduojama tirti ankstyvajai kiaušidžių vėžio diagnostikai moterims, kurių šeimose yra sergančiųjų krūties ar kiaušidžių vėžiu, jei randamos genų BRCA 1, BRCA 2 mutacijos. CA 125 kiekis gali padidėti sergant gerybinėmis ginekologinėmis ligomis, endometrioze, krūties ligomis, kepenų ciroze, pankreatitu, granulomatoze. Taip pat šio antigeno gali laikinai padaugėti normalaus nėštumo ir mėnesinių metu. CA 125 svarbu nustatyti prieš antrinės apžiūros operacijas, kai reikia įsitikinti, ar yra visiška proceso remisija. Jei CA 125 koncentracija išlieka padidėjusi arba jei po sumažėjimo ji vėl padidėja, tai rodo, kad navikas (ar jo dalis) liko ir tuomet apžiūros operacija neturi prasmės. Tačiau jei CA 125 kiekis ir nepadidėja, vis dėlto galimos naviko liekanos ir tada indikuojama apžiūros operacija. Sveikų asmenų kraujyje CA 125 kiekis turi būti mažesnė negu 21 ku/l. Audinių polipeptidinis antigenas (APA, angl. tissue polypeptide antigen, TPA). Tai antigenas, susijęs su citoskeleto baltymais metais B. Björklundas šį antigeną išskyrė iš žmogaus vaisiaus ir placentos proliferuojančių (vėžio) ląstelių. Tai polipeptidas, kurio molekulinė masė yra daltonų; jis yra keratino komponentas (keratinų irimo produktas). Audinių polipeptidinis antigenas nėra specifinis tam tikro naviko požymis, o daugiau proliferacijos žymuo. Padidėjęs APA kiekis randamas ligonių, sergančių įvairios lokalizacijos vėžiu, kraujyje: plaučių, krūties kepenų, kasos, storosios ir tiesiosios žarnos, skrandžio, prostatos, šlapimo pūslės, kiaušidžių, skydliaukės, galvos ir kaklo. Taigi APA nėra specifiškas tam tikram audiniui ar organui. Pašalinus piktybinį auglį, šio žymens koncentracija sunormalėja per 14 dienų. Pooperacinis APA kiekio didėjimas ar mažėjimas yra labai susijęs (asocijacija siekia 90%) su ligos pasikartojimu ar jos regresija. Jo gali padaugėti ir sergant gerybinėmis (uždegiminėmis) plaučių, virškinamojo trakto, šlapimo ir lyties organų, krūties, galvos ir kaklo ligomis. Sveikų asmenų kraujyje jo kiekis neturi būti didesnis nei 83 U/l. Audinių polipeptidinis specifinis antigenas (APSA, angl. tissue polypeptide specific antigen, TPS). Tai antigenas, atpažįstantis APA M3 epitopą. Taigi APSA yra 389
391 specifinė APA dalis. Ji atspindi proliferacinį vėžinio proceso aktyvumą. APSA yra sintetinamas vėlyvosiose S ir G2 ląstelių ciklo fazėse ir susijęs su vėžinio proceso kaita. Navikas auga ne visą laiką. Nedidelio augimo ar neaugimo tarpsnį keičia proliferacija. Periodiškai matuojant APSA koncentraciją sergančiųjų vėžiu kraujyje, galima gauti informacijos apie naviko augimo aktyvumą gydymo metu, t. y. įvertinti, ar gydymas sėkmingas. Šis žymuo nėra specifiškas, tačiau suteikia daugiau informacijos apie piktybinio proceso eigą ir gydymo veiksmingumą, palyginti su kitais, kad ir specifinis, žymenimis. Normaliai APSA koncentracija yra <83 U/l. Prostatai specifinis antigenas (PSA). Tai glikoproteinas, kurio molekulinė masė daltonų. Pagal veikimą tai serinoproteazė, gaminama prostatos epitelinėse ląstelėse ir išskiriama į spermą. Fermentas ardo fibronektiną ir taip skystina spermą; taigi jo funkcija yra neleisti spermos skysčiui sukrešėti. Aktyvioji fermento forma susidaro, kai nedidelis peptidas atsiskiria nuo neaktyvaus pirmtako, fermentas inaktyvinamas, kai susidaro jo kompleksas su įvairiais proteazių inhibitoriais, svarbiausia α 1 antichimotripsinu. Šį glikoproteiną pirmą kartą (1979) išskyrė T. Wangas su bendradarbiais iš žmogaus prostatos ekstrakto. Moterų aplink šlapimkanalį esančios (parauretralinės) liaukos atitinka prostatos rudimentus, ir jose taip pat susidaro, nors labai mažas, PSA kiekis. PSA aptinkamas ir normalioje, ir patologiškai pakitusioje prostatoje, taip pat jo padaugėja sergant piktybinėmis ir gerybinėmis prostatos ligomis. Taigi PSA yra organui, bet ne navikui specifinis žymuo. PSA komplekso su α 1 antichimotripsinu forma ( Da) yra vyraujanti kraujo serume ir sudaro 60 90% viso PSA kiekio. Be to, kraujyje dar cirkuliuoja Da laisvasis PSA, kuris sudaro 10 40% viso PSA kiekio. Ši forma neturi fermentinio aktyvumo ir nesudaro komplekso su proteazių inhibitoriais. Biologinis gyvavimo puslaikis kraujo serume 2,5 dienos metais H. Lilja iškėlė hipotezę, kad PSA komplekso santykis su laisvuoju PSA gali būti svarbus diferencijuojant prostatos vėžį nuo gerybinės prostatos hiperplazijos: nustatyta, kad serumo PSA komplekso kiekis gerokai didesnis negydytų prostatos vėžiu sergančių ligonių kraujyje negu sergančiųjų gerybinėmis prostatos ligomis, ir priešingai laisvojo PSA daug mažiau rasta negydytų prostatos vėžiu sergančių ligonių kraujyje, palyginti su sergančiųjų gerybinėmis prostatos ligomis. Taigi bendrojo PSA koncentracija kraujyje dažniausiai yra padidėjusi sergant prostatos vėžiu. Tačiau nemažai daliai pacientų šis padidėjimas neviršija rekomenduojamos normos (4 mg/l), o sergant daugeliu gerybinių prostatos ligų, bendrojo PSA kiekis tą ribą viršija. Kaip tik tada ir pravartu nustatyti laisvojo PSA santykį su bendruoju PSA: šis santykis yra labai padidėjęs sergant gerybinėmis prostatos ligomis ir smarkiai sumažėjęs sergant prostatos vėžiu. 390
392 Molekuliniai navikų žymenys ir jų naudojimas ligų diagnostikai Dėl didelio jautrumo šis tyrimas gali būti naudojamas pirminei prostatos vėžio diagnostikai, ir PSA nustatymas rekomenduojamas ne tik rizikos grupių atrankai, bet ir vyrams per 50 metų amžiaus. Taip pat PSA koncentracija tiriama vertinant gydymo veiksmingumą ir stebint ligonius, kuriems buvo nustatytas prostatos vėžys. PSA koncentracijos padidėjimas labai anksti rodo naviko augimą prieš 6 mėnesius iki aptinkant naviką kitais diagnostikos metodais. Esant pirminio nežinomos lokalizacijos naviko metastazėms į kaulus, PSA nustatymas gali būti svarbus diagnostikai ir leidžia nustatyti prostatos vėžio diagnozę. Taip pat PSA tyrimas svarbus prognozei. PSA padidėja ir sergant gerybinėmis prostatos ligomis: ūminiu prostatitu, gerybine prostatos hiperplazija. Prostatai specifinis antigenas yra jautresnis žymuo negu prostatos rūgščioji fosfatazė (PRF), bet PSA dažniau ir labiau padidėja sergant ne tik piktybinėmis, bet ir gerybinėmis prostatos ligomis. Jeigu imamas tas pats specifiškumo atskaitos taškas (95%), tai PSA jautrumas yra 70%, o PRF 30%. 45 lentelėje pateikiamas prostatai specifinio antigeno ir prostatos rūgščiosios fosfatazės (PRF) koncentracijų padidėjimo lygis sergant gerybine prostatos hiperplazija (GPH) ir esant įvairioms prostatos vėžio stadijoms. 45 lentelė. PSA ir PRF kitimas sergant gerybinėmis ir piktybinėmis prostatos ligomis Būklė PSA padidėjimas, % PRF padidėjimas, % GPH Prostatos vėžys: A stadijos B stadijos C stadijos D stadijos Rekomenduojama bendrojo prostatai specifinio antigeno koncentracija kraujyje 3,2 mg/l (0 4 mg/l), laisvojo 0,42 mg/l. Įvairios manipuliacijos (prostatos biopsija, tyrimas pro tiesiąją žarną) turi įtakos PSA koncentracijai. Kad būtų išvengta klaidingai padidėjusių rezultatų, tarp tokių procedūrų ir kraujo ėmimo turi praeiti 1 2 savaitės. Prostatai specifinio antigeno gamybą slopina gydymas antiandrogenais. Prostatos rūgščioji fosfatazė (PRF, angl. prostatic acid phosphatase, PAP). Tai glikoproteinas, kurio molekulinė masė daltonų. Fermentas gaminamas prostatos epitelio lizosomose ir išskiriamas į prostatos sekretą. Prostatos rūgščioji fosfatazė yra antrasis izofermentas iš penkių izofermentų. Izofermentus taip pat gamina trombocitai, eritrocitai, retikuloendotelinės sistemos ląstelės (kepenyse, blužnyje), kaulų čiulpai ir prostata. Pusė bendrojo vyrų rūgščiosios fosfatazės aktyvumo priklauso nuo prostatos izofermento, o kita nuo kepenų, trombocitų, eritrocitų. 391
393 Šio fermento randama moterų parauretrinėse liaukose. Prostatos rūgščioji fosfatazė katalizuoja fosforo rūgšties monoesterių hidrolizę spermoje, kai ph yra 4,5 ir 6,0. Biologinio gyvavimo puslaikis 1,1 2,6 valandos. Tai organui, bet ne navikui specifinis žymuo. Kaip ir prostatai specifinis antigenas, prostatos rūgščioji fosfatazė imunohistologiškai randama sveikoje ir pažeistoje prostatoje. Kadangi ankstyvosiose prostatos ligų stadijose prostatos rūgščiosios fosfatazės nepadaugėja, tyrimas nerekomenduojamas atrankai. Jis vertingas ligos (prostatos vėžio) stebėsenai ir gydymo efektyvumo vertinimui. PRF koncentracija didėja augant naviko masei. Prostatos rūgščioji fosfatazė yra mažesnio jautrumo žymuo, palyginti su prostatai specifiniu antigenu. 80% asmenų, kuriems nustatytas metastazinis prostatos vėžys, šios fosfatazės padaugėjimas buvo susijęs su ligos stadija. Padidėjęs PRF kiekis, nors ne toks didelis kaip PSA, nustatomas sergant gerybinėmis prostatos ligomis: prostatitu ir gerybine prostatos hiperplazija, jos aktyvumas gali padidėti po tyrimo pro tiesiąją žarną. PAP yra labai jautri temperatūrai, todėl paimtą kraują reikia tirti tuoj pat, o serumą laikyti šaldytuve. Gydymas antiandrogenais prostatos rūgščiosios fosfatazės gamybos neslopina, o prostatai specifinio antigeno gamybą slopina. Sveikų asmenų kraujyje PRF koncentracija yra 4 U/l. β 2 mikroglobulinas (β 2 M). β 2 mikroglobulinas yra sudarytas iš vienos polipeptidinės grandinės, kurios molekulinė masė daltonų. Šis baltymas formuoja žmogaus leukocitų antigeno (ŽLA) lengvąją grandinę ir dėl to yra randamas beveik visų ląstelių, turinčių branduolį, paviršiuje. Ypač daug jo yra limfocitų paviršiuje. β 2 M taip pat yra aptinkamas visuose organizmo skysčiuose. Šis baltymas svarbus formuojant imuninį atsaką. Gyvavimo kraujyje puslaikis nuo 20 minučių iki 2,1 valandos. Pirmą kartą β 2 mikroglobulinas buvo išskirtas iš paciento, sergančio inkstų kanalėlių proteinurija, šlapimo. Po filtracijos inkstų glomeruluose 99,8% šio baltymo yra reabsorbuojama proksimaliniuose kanalėliuose. Todėl sutrikus glomerulų filtracijai β 2 M kiekis didėja kraujo serume, o sutrikus kanalėlių funkcijai (sergant glomerulų ir kanalėlių nefropatija), jis didėja šlapime. Kaip navikų žymens, β 2 mikroglobulino koncentracija yra prognozinis piktybinių limfinės sistemos ligų (mielominės ligos) rodiklis: ligoniai, kuriems β 2 M kiekis padidėjęs, gyvena trumpiau, negu tie, kuriems nustatomos normalios reikšmės (išgyvenamumas yra atitinkamai 1,5 ir 5,3 metų). Taip pat šis žymuo naudojamas gydymo efektyvumui vertinti, lėtine limfocitine leukemija sergančių ligonių stebėsenai, ligos prognozei. Padidėjęs β 2 M kiekis smegenų skystyje reiškia, kad į procesą įtraukta centrinė nervų sistema. Dar viena taikymo sritis AIDS sergančių ir sutrikusios imuninės sistemos ligonių stebėsena. 392
394 Molekuliniai navikų žymenys ir jų naudojimas ligų diagnostikai Sveikų asmenų kraujyje β 2 mikroglobulino koncentracija yra 0,7 1,8 mg/l. Interpretuojant rezultatus, būtina įvertinti inkstų funkciją. Be to, β 2 M molekulės stabilumas priklauso ir nuo ph, ir tai reikia žinoti tiriant jį šlapime. Feritinas. Tai didelės molekulinės masės baltymas, turintis geležies; jo molekulinė masė apie Da. Geležies įsotintoje molekulėje geležis sudaro daugiau negu 20% molekulės masės. Tai normalus žmogaus serumo ir eritrocitų bei hepatocitų komponentas ir svarbiausia jo funkcija yra geležies kaupimas. Feritino nustatymu remiasi diferencinė anemijų diagnostika. Klinikiniai tyrimai įrodė, kad pacientų, sergančių piktybinėmis ligomis, kaip leukemija, Hodžkino liga, krūties, kiaušidžių vėžys, ausų, nosies ir gerklės lokalizacijų vėžys, kraujyje feritino koncentracija yra padidėjusi. Feritinas gali padėti diagnozuoti ligą, įvertinti jos eigą, prognozę, atsaką į gydymą, ligos pasikartojimą (recidyvą). Esant kraujo išsiliejimui po voratinkliniu dangalu (subarachnoidinė hemoragija) likvore feritino koncentracija labai padidėja. Centrinės nervų sistemos hemoragijoms atskirti nuo jatrogeninio kraujavimo reikia nustatyti eritrocitų skaičių ir feritino koncentracijos smegenų skystyje (likvore) santykį. Normaliai feritino kiekis vyrų kraujo serume yra μg/l, moterų μg/l, likvore 3 10 μg/l. Žmogaus tiroglobulinas (žtg). Tai glikoproteinas, kurio molekulinė masė daltonų. Šis baltymas yra gaminamas skydliaukės ląstelių endoplazminiame tinkle ir po to nusėda jų folikuluose, kuriuose ir kaupiamas skydliaukės hormonas. Normaliai kraujyje tiroglobulino kiekis esti nedidelis. Padidėjusi tiroglobulino koncentracija nustatoma sergant ne tik hipertiroze, bet ir negydytu skydliaukės folikuliniu ir papiliniu (ne meduliniu) vėžiu. Svarbiausia indikacija atlikti šį tyrimą yra skydliaukės vėžiu sergančių ligonių stebėsena po tiroidektomijos. Pašalinus skydliaukę ar gydant radioaktyviuoju jodu ( 131 J), besilaikanti padidėjusi tiroglobulino koncentracija ar vėl didėjantis jo kiekis, jei buvo sumažėjęs, rodo lokalų recidyvą ar tolimąsias metastazes. 10% skydliaukės vėžio atvejų susidaro autoantikūnai prieš tiroglobuliną, todėl galima nustatyti klaidingai mažą žtg kiekį. Šis hormonas taip pat tiriamas gydant ligonius, sergančius tiroiditu, gerybine adenoma, kitomis skydliaukės ligomis, taip pat šių ligonių stebėsenai. Rekomenduojamas kiekis kraujo serume 0,83 55 mg/l. Kalcitoninas. Tai peptidinis hormonas, sudarytas iš 32 aminorūgščių grandinės, gaminamas skydliaukės parafolikulinės zonos C ląstelėse. Jis yra parathormono antagonistas: slopina osteoklastų aktyvumą kauluose ir mažina serumo kalcio kiekį. Kalcitonino mažėja su amžiumi, daugėja nėštumo ir laktacijos metu. Kalcitonino tyrimas yra vertingas skydliaukės šerdinės dalies ar C ląstelių (medulinio) vėžio žymuo ir yra svarbus vertinant atsaką į gydymą ir numatant ligos pasikartojimą. Apie 20% C ląstelių vėžio atvejų būdingas šeiminis kaupimasis, todėl 393
395 46 lentelė. Dažniausiai nustatomi pakitę navikų žymenys ir vėžio lokalizacija Vėžys Storosios žarnos Žymenys CEA AFP β žchg CA 15-3 CA 19-9 CA 50 CA 125 APA PSA/LPSA PRF žtg Kal Kasos + + Kepenų (pirminis kepenų vėžys) + Krūties + Kiaušidės + + Prostatos + + kalcitonino kiekio matavimą galima taikyti atrankiniam kraujo giminių tyrimui. Be to, kalcitonino koncentracija padidėja sergant plaučių, kasos vėžiu, B 12 vitamino stokos anemija, pankreatitu, tiroiditu, alkohololine kepenų ciroze. Rekomenduojama reikšmė serume iki 10 ng/l (serume koncentracija yra didesnė negu plazmoje). 46 lentelėje apibendrintas navikų žymenų padidėjimas, esant įvairiai vėžio lokalizacijai. Choriokarcinoma + Šlapimo pūslės + Skydliaukės folikulinis vėžys + Skydliaukės C ląstelių vėžys + Api b e n d r i n i m a s Vėžiu vadinami piktybiniai, pagal ląstelių kilmę epiteliniai navikai. Karcinogenezė (piktybinis neoplazinis procesas vėžys) vystosi stadijomis, kurias savo ruožtu lemia veiksniai, priklausantys nuo individo genetinės struktūros, aplinkos ir (ar) gyvensenos. Vėžinėms ląstelėms būdingi trys piktybiškumo požymiai: jų nereguliuoja ląstelių augimą reguliuojanti sistema, jos infiltruoja aplinkinius audinius (priešingai negu gerybiniai navikai), jos sudaro metastazes, plisdamos limfogeniniu ar hematogeniniu būdu. Šie požymiai atsiranda pakitus ląstelės DNR dėl tiesioginių mutacijų ar netiesiogiai šiuos požymius lemia pakitusi baltymų sintezę reguliuojančių genų raiška. 394
396 Molekuliniai navikų žymenys ir jų naudojimas ligų diagnostikai Terminu naviko žymuo apibrėžiama didelė grupė medžiagų, kurias gamina piktybinė ląstelė ar kaip atsaką į neoplaziją gerybinė ląstelė ir kurias galima išmatuoti organizmo skysčiuose bei audiniuose. Navikų žymenų tyrimo tikslai: pacientų atrankai, pirminei diagnostikai, vėžio lokalizacijai nustatyti, ligos stadijai (pažeidimo laipsniui) nustatyti, prognozei įvertinti, gydymo efektyvumui įvertinti ir pacientams stebėti. Naviko žymens kitimų kinetika yra svarbesnė negu individualios jo reikšmės, o koncentracijos padidėjimas, net ir neviršijantis rekomenduojamų normų, yra svarbus. Laboratoriniai tyrimai α fetoproteinas (AFP) Tiriamoji medžiaga. Serumas. Rekomenduojama reikšmė. Sveikų vyrų ir moterų 0,56 2,64 ku/l. Diagnostinė vertė. 100% atvejų, esant metastazinei hepatoceliulinei karcinomai; 50% atvejų, esant neembrioninių ląstelių sėklidžių vėžiui; nedideliam procentui pacientų, esant kitų organų vėžiui (kasos, skrandžio, storosios žarnos, plaučių), 5 10% pacientų, sergančių hepatitu ar ciroze, alkoholine kepenų liga, embrioninių ląstelių vėžiu. Esant kepenų vėžiui, AFP kiekis yra daug didesnis negu sėklidžių vėžiu. Jei motinos kraujyje jo kiekis yra didesnis negu du kartus, būtinas ultragarsinis ištyrimas, kad būtų galima patikslinti nėštumo laiką, nustatyti daugiavaisį nėštumą, vaisiaus mirtį, apsigimimus (pvz., anencefaliją). Padidėjęs AFP kiekis motinos serume ir amniono skystyje yra susijęs su nervinio vamzdžio apsigimimais (pvz., anencefalija, nugaros smegenų išvarža), omfalocele, stemplės ir dvylikapirštės žarnos atrezija, Mekelio sindromu, vaisiaus kepenų nekroze dėl virusinės infekcijos ar kitų priežasčių. Motinos kraujyje: Dauno sindromas (21 chromosomos trisomija), vaisiaus mirtis, savaiminis abortas, 18 chromosomos trisomija, pernešiotas nėštumas. Papildoma informacija. AFP yra glikoproteinas, sintetinamas vaisiaus kepenyse, virškinamajame trakte ir trynio maiše. Po gimimo AFP kiekis mažėja ir po pirmų gyvenimo metų randami tik pėdsakai. Šiek tiek gali padidėti esant kepenų regeneraciniams procesams. AFP kiekio matavimas svarbus įvertinant kepenų vėžio gydymo veiksmingumą. Serumo AFP kiekis koreliuoja su naviko dydžiu, esant sėklidžių ir kiaušidžių embrioninei piktybinei teratoblastomai. Vaisiaus AFP patenka ir į motinos kraujotaką. Motinos kraujyje maksimali reikšmė yra 30-ą nėštumo savaitę, vėliau greitai mažėja ir ą nėštumo savaitę sudaro < 2% maksimalios reikšmės. Chorioninis gonadotropinas (žchg, angl. hcg) Tiriamoji medžiaga. Serumas. Rekomenduojama reikšmė (U/l): vyrų: <1,1 moterų: <2,7 395
397 nėščiųjų: 1,3 2 sav sav sav sav sav sav sav sav sav sav Diagnostinė vertė. Ankstyvojo nėštumo diagnostika (6 8 dienos po pastojimo) ir nėštumo laiko nustatymas. Tyrimu gali būti aptinkami ektopiniai audiniai, produkuojantys žchg. Papildoma informacija. Žmogaus chorioninis gonadotropinas yra sudarytas iš dviejų nekovalentiškai susijungusių α ir β glikoproteinų grandinių. Sveikų nėščių moterų serume žchg yra įvairių formų: intaktinis (92 98%), α grandinė (iki 7%), β grandinė (iki 3%) ir iš dalies suskaidytas (pvz., įkirptasis žchg ar β grandinės fragmentai). Pačioje nėštumo pradžioje moterų šlapime daugiausia yra β grandinės fragmentų ( 50%), mažiau intaktinio ( 35%) ir įkirptojo ( 10%) žchg. Reakcija yra jautri intaktiniam žchg ir beveik neduoda kryžminės reakcijos su liuteinizuojančiu hormonu. Būtini kartotiniai tyrimai, ypač įtariant patologinį nėštumą. Jei nėštumas normalus, ŽChG greitai didėja, o jei nėštumas ektopinis ar įvyko savaiminis abortas, žchg koncentracija didėja lėčiau ar mažėja Tiriamoji medžiaga. Šlapimas. Tirti šviežią. Rekomenduojama reikšmė. Reakcija neigiama. Diagnostinė vertė. Nėštumas nustatomas 8 14 dieną po pirmųjų neįvykusių mėnesinių. Papildoma informacija. Atrankinis tyrimas nėštumui nustatyti ant plokštelės yra greitas, bet ne toks jautrus kaip mėgintuvėlyje. Kryžminė reakcija su LH (pvz., menopauzė ar LH maksimumas ciklo viduryje) gali duoti klaidingai teigiamą rezultatą. Chorioninio gonadotropino β grandinė (βžchg, angl. βhcg) Tiriamoji medžiaga. Serumas. Rekomenduojama reikšmė. Vyrų, nenėščių ir po menopauzės moterų 0,1 mg/l. Diagnostinė vertė. Choriokarcinoma, pūslinė išvisa, netrofoblastinis vėžys, ypač kiaušidžių ir sėklidžių gemalo ląstelių navikai. Esant pastariesiems, padidėja ir βžchg, ir α fetoproteino koncentracija. βžchg didėjimas ir mažėjimas rodo ligos eigą. Padidėję kiekiai leidžia nustatyti diagnozę. Ligai atsinaujinus, gali būti padidėjęs tik vienas minėtųjų žymenų. Gydant koncentracija mažėja ir tai yra geros prognozės ženklas. Padidėjimas būdingas trofoblastiniams navikams (100% atvejų), sėklidžių negemaliniams navikams (70% atvejų) ir seminomai (10% atvejų). Padidėjimas taip pat nustatomas nuo pirmos nėštumo savaitės, o II III mėnesį pasiekia maksimumą; vėliau nuosekliai mažėja. Gresiantis persileidimas, ektopinis nėštumas. Papildoma informacija. βžchg tai sialoglikoproteinas iš 180 aminorūgščių. Pirmosios 150 aminorūgščių yra 80% homologinės su liuteinizuojančiuoju hormonu. Sintetinamas besivystančios blastocistos trofoblastinėse ląstelėse, vėliau sincitiotrofoblasto ląstelėse. Biologinio gyvavimo puslaikis val. Gali didėti sergant gerybinėmis ligomis, kurioms būdinga pagreitėjusi ląstelių proliferacija. 396
398 Molekuliniai navikų žymenys ir jų naudojimas ligų diagnostikai Kalcitoninas Tiriamoji medžiaga. Serumas. Rekomenduojama reikšmė. 0,8<10 ng/l. Diagnostinė vertė. Skydliaukės medulinis vėžys; C ląstelių hiperplazija; kai kuriems pacientams, sergantiems plaučių, krūties, kasos vėžiu, B 12 vitamino stokos anemija, pankreatitu, tiroiditu; esant lėtiniam inkstų nepakankamumui, pseudoparatirozei, alkoholinei cirozei. Padidėti gali nėščiosioms ir sergant plaučių gerybinėmis ligomis. Kalcitoniną ektopiškai gali gaminti įvairių lokalizacijų vėžinės ląstelės, ypač neuroendokrininės kilmės. Tyrimas svarbus vertinant atsaką į gydymą ir numatant ligos (skydliaukės medulinio vėžio) pasikartojimą; gali būti naudojamas sergančiųjų minėta vėžio forma šeimos narių atrankiniam tyrimui (20% šio vėžio atvejų yra šeiminių). Papildoma informacija. Kalcitoninas yra peptidinis hormonas iš 32 aminorūgščių grandinės, gaminamas skydliaukės perifolikulinės zonos C ląstelėse. Tai parathormono antagonistas: jis slopina osteoklastų aktyvumą kauluose ir mažina serumo kalcio kiekį. Kalcitonino mažėja su amžiumi, didėja nėštumo ir laktacijos metu. Serume koncentracija yra didesnė negu plazmoje. Kliniškai tyrimas yra vertingas kaip skydliaukės medulinio vėžio žymuo. V: kalcio infuzijos, adrenalinas, estrogenai, gliukagonas, pentagastrinas, geriamieji kontraceptikai. Lipemija ir hemolizė nepageidaujamos. Karcinoembrioninis antigenas (angl. CEA) Tiriamoji medžiaga. Serumas. Rekomenduojama reikšmė. Nerūkančių moterų 2,5, vyrų 3,4 mg/l, rūkalių moterų 4,9, vyrų 6,2 mg/l. Diagnostinė vertė. CEA daugiau yra rūkalių serume negu nerūkančių asmenų. Sergant piktybinėmis ligomis padidėjęs kiekis yra susijęs su ligos stadija ir išplitimo laipsniu. Padidėja dėl storosios žarnos, tiesiosios žarnos, plaučių, krūties, kepenų, kasos, prostatos, skrandžio ir kiaušidžių vėžio. Mažesnis padidėjimas nustatytas sergant gerybinėmis kepenų (hepatitas, cirozė), skrandžio ir žarnų ligomis (polipozė, opinis kolitas), gerybinėmis krūties ligomis, plaučių infekcija, emfizema, inkstų nepakankamumu. CEA svarbus metastazinio storosios žarnos ir vėlyvosios stadijos krūties vėžio stebėsenai. CEA yra geriausias neinvazinis būdas kontroliuoti storosios žarnos vėžio eigą. Laikas tarp CEA padidėjimo ir kliniškai dokumentuotos ligos gali siekti 36 mėnesius. CEA smegenų skystyje gali būti tiriamas pirminių ar metastazinių centrinės nervų sistemos navikų diagnostikai. Papildoma informacija. CEA yra su naviku susijęs onkofetalinis antigenas, randamas embriono ir vaisiaus audiniuose. Tai heterogenis glikoproteinas (mažiausiai 13 genetinių variantų). Molekulėje yra apie 800 aminorūgščių liekanų, didelis angliavandenių procentas (50 85%). Tiriant elektroforeze juda su β globulinais. Prostatos rūgščioji fosfatazė Tiriamoji medžiaga. Serumas. Rekomenduojama reikšmė. 4 U/l. Diagnostinė vertė. Prostatos vėžys (dažnai, bet ne visada, jau metastazavęs); Gošė liga, Nimano Piko liga; 1 2 dienos po prostatos biopsijos ar operacijos; po prostatos manualinio tyrimo, kateterizacijos; gerybinė prostatos hipertrofija; prostatitas; prostatos infarktas. 80% asmenų, sergančių metastaziniu prostatos vėžiu, padidėjimas koreliuoja su ligos stadija. Kadangi prostatos rūgščioji fosfatazė nepadidėja ankstyvosiose prostatos ligų stadijose, tyrimas nerekomenduojamas atrankai. Jis vertingas ligos stebėsenai. 397
399 Papildoma informacija. Rūgščioji fosfatazė yra lizosominis fermentas, glikoproteinas. Prostatos izofermentas yra prostatos epitelio lizosomose. Didžiausias bendrosios rūgštčiosios fosfatazės ir jos prostatos izofermento aktyvumas 1 g audinio yra prostatoje. Mažesnis aktyvumas ne prostatai specifinės rūgščiosios fosfatazės yra kepenyse, blužnyje, eritrocituose, trombocituose, kaulų čiulpuose. Pusę bendrojo vyrų rūgščiosios fosfatazės aktyvumo sudaro prostatos izofermentas, o kita aktyvumo dalis yra iš kepenų, trombocitų, eritrocitų. Lengvos formos hemolizė. Prostatai specifinis antigenas Tiriamoji medžiaga. Serumas. Rekomenduojama reikšmė. Vyrų (mg/l): m. <3,2; m. <1,5; m. <1,9. Diagnostinė vertė. Prostatos vėžys; 25% pacientų, turinčių gerybinę prostatos hiperplaziją. Mažėjimas po gydymo (chirurginio) rodo, kad navikas pašalintas. PSA rekomenduotinas lokaliojo ir sisteminio gydymo efektyvumui įvertinti. Papildoma informacija. Tai glikoproteinas, kuris funkcionuoja kaip kalikreinserinproteazė. PSA yra prostatos audiniui, bet ne protatos vėžiui specifinis antigenas. Jis yra vertingesnis negu rūgščioji fosfatazė, vertinant gydymo efektyvumą ir anksti aptinkant atsinaujinusį prostatos vėžį. PSA rekomenduojama tirti per 50 metų amžiaus vyrams atrankos tikslais. Tyrimas vertingas didelės rizikos vyrų stebėseną. PSA reikšmės didėja su amžiumi, būdingi svyravimai per dieną. Gulint reikšmės mažėja. Manualinis prostatos tyrimas ir kitos manipuliacijos prieš imant kraujo gali padidinti PSA reikšmes. Laisvojo prostatai specifinio antigeno kiekis metų vyrų neturi viršyti 0,42 mg/l. 398
400 NAUJAGIMIŲ, VAIKŲ IR SENYVŲ ŽMONIŲ KLINIKINĖS BIOCHEMIJOS YPATYBĖS Amžiaus įtaką laboratoriniams rodikliams lemia lytinio subrendimo laipsnis ir griaučių raumenų masė. Žmogaus gimimas ir perėjimas iš motinos įsčių į nepriklausomą būvį reikalauja daugelio biocheminių sistemų persitvarkymo. Šis tarpsnis trunka nuo kelių savaičių iki kelerių metų po gimimo. Gimimo metu plaučiai turi perimti iš placentos dujų apykaitos funkciją. Vaisiaus ir naujagimio ji visiškai skiriasi. Vaisiaus kraujyje yra fetalinio hemoglobino HbF, kuris pasižymi didele geba jungtis su deguonimi tai gerina jo perėjimą vaisiui iš motinos. Šio hemoglobino koncentracija vaisiaus kraujyje yra didesnė negu motinos, ir tai lemia, kad deguonies pernaša ir audinių oksigenacija yra efektyvesnė. Gimdymo metu vaisiaus organizmas patiria tam tikro laipsnio hipoksiją ir acidozę, kuri sunormalėja per 24 valandas. Su pirmu įkvėpimu plaučiai, jei yra subrendę, t. y. turi pakankamai surfaktanto, išsipučia, ir dujų apykaita greitai sunormalėja, t. y. po 2 padidėja, pco 2 sumažėja. Trūkstant surfaktanto, vystosi kvėpavimo nepakankamumo sindromas: alveolės negali išsipūsti, jos lieka subliūškusios (41 pav.). Dėl hipoventiliacijos vystosi respiracinė acidozė, o dėl hipoksemijos metabolinė acidozė. Kuo mažiau subrendęs naujagimis, tuo didesnė šio sindromo išsivystymo rizika. Naujagimio kepenys nėra visiškai subrendusios ir negali konjuguoti viso laisvojo bilirubino. Dėl to pirmąją gyvenimo savaitę vystosi naujagimių gelta. Ji ryškiausia Sveiko naujagimio alveolė Alveolė esant kvėpavimo sutrikimo sindromui iškvėpimas įkvėpimas atelektazė Išsitempusi alveolė įkvėpimo pabaigoje Alveolė normalaus iškvėpimo pabaigoje Kolapsinė alveolė, kai nėra surfaktanto 41 pav. Naujagimių respiracinio distreso sindromo schema 399
401 3 5-ą gyvenimo dieną, tačiau dažniausiai neviršija 85 μmol/l. Tai fiziologinė naujagimių gelta. Išnešiotų naujagimių gelta greitai praeina, o neišnešiotųjų ji gali būti ryški ir trukti ilgiau. Viena dažniausių jos priežasčių yra kraujo grupių nesutapimas ar galima infekcija. Dėl kraujo grupių nesutapimo daugėja nekonjuguotojo (laisvojo) bilirubino, kurį perneša albuminas. Kai albumino molekulė yra visiškai įsotinta bilirubino, jo perteklius patenka į ląsteles. Toks (laisvasis) bilirubinas pereina kraujo ir smegenų barjerą ir sąveikauja su baltymais smegenyse, sutrikdo oksidacijos ir redukcijos reakcijas dėl to jis yra neurotoksiškas. Encefalopatija, išsivysčiusi dėl laisvojo bilirubino koncentracijos didėjimo ir kaupimosi smegenyse (kernicterus), lemia sunkų smegenų pažeidimą, dėl to gali ištikri mirtis. Jei gelta trunka daugiau kaip 10 dienų po gimimo, tokį naujagimį reikia tirti ir nustatyti ligos priežastį. Gelta galima esant patologinėms būklėms galaktozurijai, įgimtai hipotirozei, cistinei fibrozei ar gliukozės-6-fosfatdehidrogenazės stokai. Jei naujagimių kraujyje randamas padidėjęs konjuguotojo bilirubino kiekis, tai priežastys yra visai kitos. Dažniausios jų yra naujagimių hepatitas, greičiausiai užsikrėtus nuo motinos gimstant, arba tulžies takų atrezija. Pagrindinis vaisiaus energijos šaltinis yra per placentą iš motinos organizmo gauta gliukozė. Jos perteklius kaupiamas kepenyse glikogeno pavidalu. Tačiau naujagimių kraujyje gliukozės koncentracija yra maža, nes dėl nesubrendusių antinksčių mažai yra atsargų glikogeno pavidalu. Naujagimių hipoglikemija nustatoma, kai gliukozės koncentracija kraujyje yra mažesnė negu 2 mmol/l. Į tai svarbu atkreipti dėmesį, kai naujagimiai yra per maži pagal apskaičiuotą jų amžių ar gimę prieš laiką, nes tuomet jie neturi glikogeno atsargų; tokie naujagimiai neretai yra cukriniu diabetu sergančių motinų ir dėl to vaisiaus organizme išsivysčiusios hiperinsulinemijos. Laisvosios riebalų rūgštys praeina placentą ir kaupiamos riebalinio audinio triacilgliceroliuose. Vaisiaus ir naujagimio kraujo baltymų apykaitos ypatybės detaliau aprašytos skyriuje Žmogaus kraujo plazmos baltymai, jų tyrimas, rezultatų klinikinis interpretavimas. Pirmomis gyvenimo dienomis naujagimių, ypač prieš laiką gimusių, kraujyje gali būti praeinanti, paprastai besimptomė hipokalcemija, nes naujagimio prieskydinės liaukos dar neadekvačiai reaguoja į hipokalcemiją. Tokia būklė dažnesnė motinų, sergančių diabetu, naujagimiams ar neišnešiotiems naujagimiams, taip pat gimusiems asfiksijos būsenos ar išsivysčius kvėpavimo sutrikimo sindromui. Naujagimių šlapalo koncentracija po gimimo mažėja, nes pradedami sintetinti nauji baltymai. Dėl šios priežasties ir aminorūgščių koncentracija kraujyje yra maža, tačiau jos gali būti šalinamos su šlapimu, nes dar nėra subrendę inkstų reabsorbcijos mechanizmai. Inkstų glomerulai susiformuoja 36-ą nėštumo savaitę. Tačiau dėl mažos kraujotakos vaisiaus inkstuose filtracija glomeruluose gimimo metu yra sumažėjusi. Todėl pirmąją gyvenimo savaitę kreatinino koncentracija serume yra padidėjusi, o vėliau, 400
402 Naujagimių, vaikų ir senyvų žmonių klinikinės biochemijos ypatybės per 4 savaites, mažėja ir išlieka nedidelė apie 5 metus. Bręstant kreatinino koncentracija pradeda didėti. Sveikas naujagimis su šlapimu išskiria gliukozę, aminorūgštis. Kol nesubrendę inkstų proksimaliniai kanalėliai, rūgščiųjų karbonatų ir gliukozės reabsorbcija yra susilpnėjusi, dėl to rūgščiųjų karbonatų koncentracija serume maža. Susilpnėjusi ir koncentravimo geba. Naujagimystės tarpsniu inkstų galimybės šalinti vandenį ir elektrolitus taip pat ribotos, todėl veninės skysčių injekcijos turi būti tiksliai apskaičiuotos. Naujagimio organizme vanduo sudaro apie 75% jo kūno masės (suaugusiųjų organizme 60%). Pirmą gyvenimo savaitę mažėja neląstelinio skysčio, todėl sumažėja kūno svoris (masė). Vienerių metų kūdikio organizme vanduo sudaro apie 60% ir jo 25% yra už ląstelių ribų. Naujagimio organizmas labai jautrus vandens netekimui, nes jo inkstų kanalėlių funkcija dar nėra subrendusi. Be to, jie dalies skysčių netenka per virškinamąjį traktą dėl viduriavimo. Nedidelė dehidratacija dėl viduriavimo gali būti gydoma duodant gerti gliukozės ir elektrolitų tirpalų. Jei vandens netekta daugiau, gali prireikti skysčių leisti į veną. Atsaką į gydymą būtina stebėti vertinant skysčių pusiausvyrą, šlapimo kiekį. Todėl vaikams skysčius reikia skirti atsižvelgiant į jų amžių ir kūno svorį. Gimimo metu virškinamajame trakte jau veikia disacharidazės (maltazė, laktazė), tačiau per pirmąsias 7 gyvenimo dienas laktozė gali būti absorbuojama ir nepakitusi bei skirtis su sveiko naujagimio šlapimu. Nors proteoliziniai fermentai yra aktyvūs, gali absorbuotis ir kai kurie nesuskaidyti baltymai. Po gimimo kraujo plazmoje baltymų koncentracija pamažu didėja ir suaugusiųjų rekomenduojamas normos ribas pasiekia apie 10 gyvenimo metus. Serumo šarminės fosfatazės aktyvumas kūdikystėje yra didelis, paskui mažėja, o pradėjus vaikui augti vėl ima didėti. Šio fermento aktyvumas koreliuoja su kaulų augimu ir lytiniu brendimu, t. y. su didžiausiu osteoblastų aktyvumu augant kaulams, o po subrendimo aktyvumas greitai sumažėja. Tiroksino koncentracija naujagimių kraujyje yra tokia, kaip ir nėščios moters kraujyje gerokai didesnė negu nenėščios moters kraujyje. Po gimimo kūdikio pomegeninė liauka pradeda sekretuoti tirotropiną, ir tiroksino koncentracija toliau didėja. Tai fiziologinė hipertirozė, kuri pradeda mažėti per pirmuosius gyvenimo metus. Ir berniukų, ir mergaičių kraujyje lytinių hormonų ir gonadotropinų koncentracija yra vienoda ir maža. Lytinis brendimas prasideda sumažėjus posmegeninės liaukos ir pogumburio jautrumui neigiamam lytinių hormonų grįžtamojo ryšio atsakui. Liutropino, folitropino ir lytinių hormonų kiekiai palaipsniui per daug metų pradeda didėti ir stabilizuojasi, kai lytiškai subręstama. Daugumos laboratorinių rodiklių koncentracija kraujyje yra pastovi visą laikotarpį nuo lytinio subrendimo iki moterų menopauzės ar vyrų andropauzės. 401
403 Su amžiumi ir senstant organizme vyksta nemažai funkcinių pokyčių. Net ir nesant ligos, silpnėja daugelio organų funkcija, tačiau dėl esančių funkcinių rezervų klinika neišryškėja. Gydytojui yra svarbu diferencijuoti biocheminius ir fiziologinius amžiaus nulemtus pokyčius nuo ligos požymių. Ne visada pakitęs biocheminis rodiklis yra ligos požymis. Vyresniame amžiuje kai kurios ligos yra dažnesnės, palyginti su jaunu amžiumi, be to, ir tų pačių ligų eiga gali skirtis. Senyvi žmonės dažniau serga ne viena, o keliomis ligomis, ir tai sunkina diagnozę. Pagyvenusių žmonių kai kurie laboratoriniai tyrimai gali būti kaip atrankiniai, kurie leidžia įtarti ligą, pavyzdžiui, šlapalo ir kreatinino koncentracijos padidėjimas inkstų ligą, kalcio, fosforo ir šarminės fosfatazės koncentracijų pokyčiai kaulų ligą, o kraujo ląstelinės sudėties (hematologinis) tyrimas gali padėti nustatyti kraujo ligą. Api b e n d r i n i m a s Kvėpavimo sutrikimo sindromo priežastis yra surfaktanto stoka, dėl to plaučių alveolės neišsipučia ir jų aeracija nevyksta. Palyginti su suaugusiaisiais, naujagimių organizme yra daugiau vandens ir neląstelinio skysčio. Inkstų funkcija subręsta tik po gimimo, taigi ji su amžiumi keičiasi. Pirmąją savaitę po gimimo išsivysto naujagimiams būdinga gelta. Hipoglikemija visada būdinga neišnešiotiesiems naujagimiams, prieš laiką gimusiesiems ir jei motina serga cukriniu diabetu. Naujagimių organizme K vitamino koncentracija yra maža, o jis būtinas posintetinės krešėjimo baltymų modifikacijos fermento karboksilazės aktyvumui. Todėl galima smegenų kraujavimo rizika. Ir berniukų, ir mergaičių kraujyje lytinių hormonų ir gonadotropinų koncentracija yra vienoda ir maža. Lytinio brendimo metu jų kiekiai didėja ir nusistovi lytiškai subrendus. Pagyvenusiems asmenims nustačius medžiagų apykaitos rodiklių pokyčius, svarbu nepamiršti, kad galima daugiau negu viena patologinė būklė. Jei žmogus senyvas, svarbu nustatyti, ar pakitęs tiriamasis žymuo yra dėl amžiaus, ar dėl ligos. Pagyvenę žmonės vartoja nemažai vaistų, kurie gali turėti įtakos laboratorinio tyrimo rezultatui. 402
404 Literatūra 1. Allan Gaw, Robert A. Cowan, Denis St. J. O Reilly, Michael J. Stewart, James Sheperd. Clinical Biochemistry. Churcill Livingstone Edinburgh London New York Sydney Tokyo, p. 2. Cardiac markers. Ed. H. B. Wu, Totowa New Jersy: Humana Press, p. 3. Clinical Chemistry (International Journal of Molecular and Laboratory Medicine). 2004; 50(9): , ; 2005; 51(12): ; 53(5): Marc A. Silver et al. Congestive Heart Failure. BNP Consensus Panel 2004: a Clinical Approach for the Diagnostic, Prognostic, Screening, Treatment Mmonitoring and Therapeutic Roles of Natriuretic Peptides in Cardiovascular Diseases, Suppl p. 5. Fundamentals of Clinical Chemistry. Ed. Norbert W. Tietz. Philadelphia London Toronto Mexico city Rio De Janeiro Sydney Tokyo Hong Kong: W. B. Saunders Company, p. ISBN Kolde H. J. Haemostasis: Physiology, Pathology, Diagnostics. Pentapharm Ltd., Basel, Switzerland, p. 7. Kučinskienė Z. Lipoproteinai. Vilnius: Mokslas, p. 8. Kučinskienė Z. Žmogaus kraujo plazmos baltymai, jų tyrimas, klinikinė interpretacija: mokomoji priemonė. Vilnius: VU l-kla, p. 9. Kučinskienė Z. Fermentai medicinoje, jų tyrimas, klinikinė interpretacija: mokomoji priemonė. Vilnius: VU l-kla, p. 10. Kučinskienė Z. Bilirubino apykaita, jos laboratoriniai rodikliai ir jų kitimas sergant geltomis: mokomoji priemonė. Vilnius: VU l-kla, p. 11. Kučinskienė Z. A. Laboratorinių tyrimų žinynas. Vilnius: UAB Vaistų žinios, p. 12. Laboratory Medicine Practice Guidelines: Laboratory Guidelines for Screening, Diagnosis and Monitoring of Hepatic Injury. Ed. Robert Dufour. National Academy of Clinical Biochemistry. Washington, DC, p. 13. Clinical Laboratory Diagnostics. Ed. Lothar Thomas. Frankfurt/Main: TH-Books Verlagsgesellschaft, p. 14. Praškevičius A., Ivanovienė L., Stasiūnienė N., Burneckienė J., Rodovičius H Biochemija. Kaunas, p. 15. Seminars in Clinical Biochemistry. Ed. Marek H.Dominiczak. University of Glasgow, p. 16. Vilniaus universiteto ligoninės Santariškių klinikų Laboratorinės diagnostikos centro tyrimai ir jų normos: metodinė priemonė Santariškių klinikų medikams, rezidentams ir studentams: 3-iasis leid. Rengė: B. Baliūnienė, V. Betingienė, J. Bytautienė, I. Bogušienė, A. Burneikaitė, A. Duobienė, Z. Kučinskienė, A. Lujienė, R. Malickaitė, D. Vitkus. Vilnius, p. 17. Clinical diagnosis and management by laboratory methods. Ed. John Bernard Henry. Philadelphia London Toronto Montreal Sydney Tokyo: W. B. Saunders Company, p. ISBN
405 Dalykinė rodyklė Acidozė 30, 35 42, 50, 51, 53 62, 64, 65, 75, 76, 78, 89, 91, 92, 143, 153, 158, 169, 177, 178, 211, 213, 217, 219, 237, 356, 358, 363, 399 Adrenalinas 36, 40, 41, 65, 122, 169, 181, 182, 219, 289, , 319, 341, , 362, 397 Adrenokortikotropinis hormonas, AKTH 25, 78, 36, 40, 87, 182, 319, 323, 328, 351, 352, 359, 364 Alaninaminotransferazė 141, 142, 146, 147, 152, 204, 207 Albuminas, -ai 33, 84, 85, 87, 94 97, 9 101, 107, 108, 110, 112, 115, 119, 120, 121, 123, 124, 143, 175, 181, , 195, 198, 199, 202, 203, 207, 213, 216, 217, 243, 249, 254, 333, 353, 366, 368, 385, 400 Aldosteronas 26, 28, 29, 33, 34, 62, 65, 80, 96, 237, 310, 315, 318, 322, Alkalozė 36, 37, 39, 40, 42, 50, 52 58, 60 65, 133, 200, 211, 213, 217, 219 α amilazė , , 177 Amoniakas 15, 51, 52, 59, 60, 64, 66 68, 72, 138, 139, 202, 206, 207 Analitė 13, Androgenai 36, 42, 73, 122, 126, 217, 219, , 302, 303, 320, 322, 337, 338, 350, , 360, 363, 371, 372 Angiotenzinas 29, 36, 39, 40, 80, 88, 271, 310, 315, 317, 352, 353, 361 Angiotenzinogenas 29, 80, 352 Antidiurezinis hormonas, ADH 25 27, 29, 30, 32 36, 42, 79, 80, 88, 237, 320, 327 Antikoaguliantas 13 16, 72, 78, 124, 145, 228, 297, Antikūnai 99, 106, 107, 109, 121, , 160, 162, 166, 170, 180, 206, 230, 242, 257, 280, 296, , , 339, 343, , 393 Antioksidatoriai 285, 289 α 1 antitripsinas 95, 97, 101, 102, 112, 115, , 125, 131, 143, 208, 296 Apolipoproteinai 247, 248, 250, , 261, 262, 266, 275, 278 Aspartataminotransferazė 141, 146, 147, 153, 154, 160, 204, 207 Ateroma 104, 266, 267, 273 Aterosklerozė 70, 75, 77, 78, 120, 159, 171, 246, 258, , 265, 269, , 284, 285, 288, 289, 308, 312, 313, 316 Audinių polipeptidinis antigenas 389 Augimo hormonas 41, 73, 169, 178, 183, 184, 213, 217, 219, 224, 234, 279, 320, 323, , 337, 340, 346, 352 Azotinės medžiagos 66, 68 72, 79 Baltymų elektroforezė 15, 95, 110, 118, 119, 123, 206, 230, 242 Bens-Džonso baltymas 118, 121, 129, 380 Bilirubinas 94, 96, 100, 101, 103, 120, 149, 181, , 202, 205, 208, 209, 219, 279, 399, 400 Biliverdinas 187, 188, 197 Biliverdinreduktazė 187 Buferinės sistemos 44, 46, 47, 49, 50, 53, 54, 56, 59, 60, 95 C peptidas , 342, 347 C reaktyvusis baltymas, CRB 95, 98, 101, 103, 104, 115, 116, 119, 121, 124, 125, 309, 312, 313 Ceruloplazminas 95, 97, 99, 102, 108, 112, 115, 124, 126, 131, 203, 205, 208, , 287, 292 Chilomikronai 125, 140, , 260, 264, 265, 268, 270, Chloridai 22, 26, 28, 41 43, 52, 58, 80, 177, 217,
406 Dalykinė rodyklė Cholesterolis 97, 98, 132, 139, 195, 203, 212, , 284, 285, 307, 308, 350, 351, 370, 372 Cistatinas C 83, 86 Citochromai 103, 185, 187, 191, 203, 237 D vitaminas 87, 97, 145, 157, 212, 213, , 237, 238, 241 Dehidratacija 22, 24, 26, 31, 32, 36, 39, 42, 62, 68, 70, 72, 87, 114, 122, 177, 216, 401 Delta hiperbilirubinemija 195 Deoksipiridinolinas , 234 Didelio tankio lipoproteinai, DTL 97, 104, 121, 145, 154, 171, 247, 248, 252, 253, , 267, 269, 274, 275, 279, 307, 308 1,25-dihidroksicholekalciferolis 80, 92, , 226, 339 Dislipoproteinemija 262, 263, 269, 273, 274, 276 Disproteinemijos 107, 108, 114 Elektrolitai 21 26, 30, 38, 43, 62, 80, 81, 88, 92, 100, 161, 177, 207, 317, 322, , 401 Ergosterolis 212 Eritrocitų nusėdimo greitis, ENG 14, 118, 119, 125, 206, 303, 312 Eritropoetinas 80, 92, 98, 241, 304, 320, 356 Estrogenai 36, 42, 78, 88, 112, , 130, 131, 152, 154, 158, 173, 183, 217, 219, 223, 225, 226, 228, 233, 241, 242, 262, 264, 270, , , , 327, 329, 338, 350, 352, 353, 361, 364, , 385, 397 Ėminys 13 15, 17, 53, , 125, 129, 157, , 260, 276, 277, 279, 301, 328, 383 Feritinas , 287, 393 Fermentų aktyvumas 52, 77, 104, 109, 122, 130, , , , 187, 194, 204, 209, 230, 289, 297, 375 α fetoproteinas 97, 102, 206, 209, 381, 383, 385, 386, 395, 396 Fibrinas 15, 98, 105, 116, 140, , 309, 313, 316 Fibrinogenas 15, 94 96, 98, 105, 107, 109, 115, 116, 119, 124, 206, 291, , 307, 310, Fibrinolizė 257, 290, 291, , 302, 303, 313, 314 Fosfatai 15, 16, 22, 49, 51, 80, 89, 92, 177, , , 235, 237, 320, 321, 338, 340, 346 Fosforas 92, 93, 145, 181, , 214, , 222, 224, 227, 229, 339, 341, 358, 402 Fruktozaminas 175, 176, 181 Geležis 13, 95, 97, 98, 102, 103, 109, 124, 126, , 207, 208, 235, , 244, 287, 289, 293 Gelta 100, 112, 147, 150, 152, 153, 156, 157, 185, 188, 190, , 201, 208, 243, 245, 301, 399, 400, 402 Glikogenfosforilazė 162, 164 Glikozilintas hemoglobinas 14, 175, 181 Gliukagonas 169, 176, 178, , 184, 217, 237, 305, 306, 314, 321, 323, 329, 340, , 346, 347, 397 Gliukokortikoidai 39, 42, 62, 65, 73, 78, 79, 88, 103, 122, 125, 126, 131, 143, 152, 173, 179, , 188, 219, 223, 225, 228, 231, 234, 242, 264, , 305, 317, 328, 337, , 360, 365 Gliukozė 15, 64, 81, 87 89, 132, 138, , , 269, 270, 274, 276, 277, 281, 309, 314, 318, 327, 335, , 357, 365, 400 Gliukozurija 89, 169, 172, 174, 176, 344, 349, 357 Globulinai 15, 29, 74, , 107, , 119, 202, 206, 238, 243, 255, 292, 312, 313, 333, 345 Glomerulų filtracijos greitis, GFG 33, 36, 81 87, 90, 91 g glutamiltransferazė 145, 154, 195, 205, 206, 209 H aptoglobinas 94, 95, 97, 99, , 112, 115, 116, 121, 123, 125, 126, 130, 131,
407 Hemas 103, 185, 187, 203, 237 Hemolizė 15, 16, 38 40, 70, 102, 110, 112, 122, , 131, 134, 150, 151, , 186, 192, 194, 196, 199, 200, 218, 243, 279, 341, 397, 398 Hemopeksinas 94, 95, 98, 103, 124 Hemosiderinas 202, 208, 238, 240 Hemostazė 290, 291, 294, 295, 298, 300, 314 Hidroksilizinas Hidroksiprolinas 229, 230, 232, 240, hidroksicholekalciferolis 92, , 339 Hiperazotemija 69, 70, 72 Hiperchloremija 42 Hiperglikemija 24, 31, 36, 40, 122, 169, , 176, , 184, 314, 335, 344, 345, 360 Hiperkalemija 38 40, 57, 59, 88, 91, 93, 235, 237, 317, 358, 359 Hiperlipidemija 77, 78, 122, 169, 171, , 251, , 268, 270, 273, , 316, 353, 369 Hiperlipoproteinemija 75, 112, 123, 170, 259, , 316 Hipernatremija 30 32, 34 36, 42 Hiperprolaktinemija Hiperproteinemija 110, 122 Hiperuremija 24, 359 Hiperurikemija 74 78, 89, 170, 277 Hipochloremija 41, 43 Hipoglikemija 168, 172, , 182, 184, 207, 328, 330, 346, 347, 352, 356, 357, 364, 400, 402 Hipokalemija 37 40, 59, 60, 88, 108, 219, 236, 359 Hiponatremija 30, 32 36, 359 Hipoproteinemija 36, 108, 110, 112, 114, 120 Homocisteinas , 316 Imunoglobulinai 94, 95, 99, 102, 106, 107, 113, , 124, , 143, 148, 154, 203, 206, 304, 380 Imunoglobulinų grandinės 102, 106, 119, 129, 380 Indikanas 66, 79, 200, 206 Insulinas 27, 37, 40, 98, 122, , , , , 222, 237, 242, 251, 269, 273, 280, 309, 314, 316, , , , 357 Interleukinas 103, , 115, 125, 131, 152, 222, 225, 226, 229, 280, 312, 313 Intersticinis skystis 21, 23, 28 Izofermentai 104, 136, 137, 141, 142, , , , 160, , , 230, 380, 391, 398 Jodas , 393 K alcio fosfatas 89, 92, 222, 224 Kalcio hidroksiapatitas 210, 211, 222, 233 Kalcis 16, 24, 58, 60, 61, 80, 92, 100, 103, 140, 141, 157, 177, 203, , 233, 291, , 320, , 358, 366, 393, 402 Kalcitoninas 36, 41, , 211, 217, 225, 226, 231, 321, 331, 338, 340, 341, 346, 381, 393, 394, 397 Kalcitriolis 212, 226, 234 Kalis 15, 16, 22 24, 28, 37 39, 42, 52, 57, 58, 63 65, 67, 81, 88, 91, 93, 140, 177, 203, 235, 315, 317, Karboanhidrazė 44, 47, 49, 51, 57, Karcinoembrioninis antigenas, CEA 381, 382, 384, 386, 397 Katecholaminai 178, 183, 184, 242, 251, 271, , 314, 315, , 362, 363 Ketoacidozė 26, 32, 40, 41, 58, 76, 78, 143, 152, 169, , 184, 218 Ketonai 175, 202, ketosteroidai 354, 355, 363, 366, 372 Klirensas 68, 69, 71, 73, 81, 82, 86, 87, 220 Kolagenas 113, , 227, , 244, 273, 291, 309, 313, 316, 339, 359 Komplemento komponentai 95, 98, 99, , 106, 112, 115, 116, 125, 129, 130, 232 Kortizolis 25, 31, 97, 178, 179, 319, 322, 326, , 363, 364,
408 Dalykinė rodyklė Kraujagyslių skystis 21 Kraujo dujos 17, 177 Kreatinas 66, 68, 69, 72, 79, 148, 202 Kreatinfosfatas 68, 69, 72, 82, 83, 148 Kreatinfosfokinazė 104, 137, 140, 148, 149, 154, 155, 160, 161, Kreatininas 19, 33, 66, 68 73, 77, 79, 81 83, 86, 87, 90, 91, 93, 177, 217, 220, 234, 400, 401 Krešėjimas 13 16, 94, 95, 105, 106, 109, 130, 140, 206, 209, 210, , 310, , 402 Krešėjimo faktorius(-iai) 25, 95, 106, 116, , 304, 305, 313 Ksantoma , 276, 277, 280 Labai mažo tankio lipoproteinai, LMTL 104, 171, , 260, Laisvieji radikalai 208, Laktatas 15, 57, 58, 64, 75, 76, 149, 156, 160, 161, 177, 339, 349 Laktatdehidrogenazė 15, 16, 137, 140, 142, 149, 150, 155, 156, 160, 161, , 204 Ląstelinis skystis 21, 22, 30, 38, 39, 45, 57 Lecitincholesterolaciltransferazė, LCAT 250, 252, 278, 279 Leukocitai 40, 57, 62, 78, 105, 122, 130, 312, 359 Lipazė 143, 144, 156, 157, 249, 251, 253, 353 Lipoproteinas (a) 257, 262, 280, Lipoproteinlipazė 140, 157, 249, 251, , 264, 265, 270, 276, 279 M gradientas 15, 117, 118 Magnis 24, 89, 95, 155, 157, 158, 177, 214, , 222, , 307, 308, 310, 316, 361 α 2 makroglobulinas 95, 98, 101, 123, 126, 129, 130, 296 Mažo tankio lipoproteinai, MTL 98, 104, 121, 145, 246, 257, , , 280, 308 Mėgintuvėlis(-iai) 13 16, 38, 172 Mikroalbuminurija 85 87, 171, 175, 176, 309, 316 α 1 mikroglobulinas 85, 89 β 2 mikroglobulinas 85, 89, 98, 130, 392 Mioglobinas 136, , 185, 187, 191, 237, 238 Miokardo infarktas 38, 85, , 125, 142, 145, , , 176, 181, 182, 207, 236, 246, 260, 263, , 279, 303, , 363 Mononuklearinė fagocitinė sistema 102, 186, 187, 202, 205 MTL receptorius 253, 256, 257, 266, 274, 275, 277, 351 Natrio kalio siurblys 26, 29 Natris 22 26, 28 36, 41, 49, 51, 52, 58, 67, 80, 88, 91, 93, 140, 177, 203, 222, 310, 315, 318, 352, 355, Navikų mucininiai žymenys 387 Navikų nekrozės faktorius , 115, 225, 226, 312, 313 Neląstelinis skystis 21, 22, 26, 28 30, 32 35, 38, 39, 42, 47, 56, 58, 80, 90, 107, 210, 211, 315, 358, 401, 402 Noradrenalinas 79, 289, 314, 315, 319, , 362 O ksiduoti MTL 272, 273, 289 Oksitocinas 36, 320, 327, 371 Onkotinis slėgis 33, 94, 100, 119, 120, 203, 242 Osmolialinis plyšys 24, 31 Osmoliališkumas 22 26, 31, 32, 35, 36, 81, 88 91, 93, 327 Osmosas 23, 100 Osmosinis slėgis 23, 25, 28, 41, 89, 96, 100 Osteoblastai , , 233, 234, 239, 401 Osteocitai , 226 Osteoidas 222, 224, 227, 233, 358 Osteokalcinas 222, 223, , 233, 234 Osteoklastai 222, , 229, 231, 233, 234, 239, 341, 393,
409 Paraproteinai 100, 113, Paraproteinemijos 116, 117, 119, 279 Parathormonas 80, 92, , , 235, 237, 321, , 346, 393, 397 pco 2 17, 48 50, 53 65, 399 ph 37, 38, 45 64, 74, 81, 95, 96, 101, 118, 133, 137, 139, 143, 144, 146, 153, 182, 211, 217, 235, 392 po 2 17, 54, 63, 399 Podagra 74, 76 79, 219, 279, 281 Prieširdžių natriurezinis peptidas 28, 29, 310, 311 Progesteronas 36, 60, 97, 122, 131, 217, 237, , 330, , 362, 366, 368, 370, 373, 387 Prokolagenas 223, 230, 231 Prokonvertinas 206, 292, 305, 313 Prostatai specifinis antigenas, PSA 381, 383, , 398 Prostatos rūgščioji fosfatazė 146, 157, 231, 381, 383, 391, 392, 397 Proteinurija 83 87, 89, 90, , 144, 171, 245, 392 Protrombinas 97, 206, 291, 293, 295, 296, 298, , 313 Reabsorbcija 25, 28, 33, 41, 50 52, 68, 69, 74, 75, 80, 81, 87 89, 91, 92, 144, 197, 212, , 320, 339, 356, 360, 400 Relaksinas 321, 371, 372 Reninas 29, 39, 80, 87, 88, 101, 140, 310, , 320, 352, 353, 361 Riebalai 21, 57, 64, 108, 112, 112, 169, 177, 203, 246, 248, 253, 254, 265, 320, 322, 345, 350, 355, 357, 367 Riebalų rūgštis sujungiantis baltymas 160, 162 Riebalų rūgštys 94, 96, 997, 100, 139, 142, 162, 176, 188, 235, , 265, 273, 274, 276, , , 314, 344, 345, 351, 385, 400 Rūgščioji fosfatazė 140, 142, 146, , 231, 381, 391, 397 Rūgščių ir šarmų pusiausvyra 28, 37, 44, 46 48, 50, 52 56, 61, 63, 81, 92, 207, 213, 218 α 1 rūgštusis glikoproteinas 95, 101, 115, 116, 123, 124, 126, 131 nėra Rūgštusis karbonatas 22, 30, 46 51, 53 65, 81, 92, 93, 177, 215, 217, 220, 238, 258, 401 Serumo amiloidas , 115, 121, 157, 312, 313 Somatostatinas 182, 321, 323, 331, 332, 342, 346 Sterkobilinogenas 186, 191, 192, Superoksiddismutazė 242, 284, 286, 287 Šarminė fosfatazė 141, 142, 144, 145, 154, 157, 158, 195, 199, 205, 206, 208, 209, 222, 229, 230, 234, 340, 402 Šlapalas 24, 26, 27, 31 33, 35, 36, 52, 64, 66 73, 81 83, 87, 90, 91, 93, 132, 138, 139, 151, 169, 177, 201, 202, 207, 232, , 400 Šlapimo rūgštis 66, 71, 74 79, 81, 89, 139, 269, 286, 287, 307 T arpląstelinis skystis 21, 33, 39, 45, 52, 358 Testosteronas 40, 123, 226, 242, 322, 353, 354, , Tiroksinas 16, 73, 87, 96, 97, 182, 224, 226, , 305, 306, 321, , 401 Tirotropinas 319, 323, 326, , 335, 337, 401 Tokoferolis 286, 288 Transferinas 94, 95, 98, 99, 103, 112, 124, 187, , 242, 287, 289 Triacilgliceroliai 181, , , , , 284, 307, 308, 344, 353, 357, 400 Trijodtironinas 97, 321, , 337, 338 Trombocitai 15, 40, 70, 97, 98, 105, 106, 131, 140, 146, 151, 156, 157, 222, 231, 271, , 304, 309, 310, 313, 314, 316, 322, 391, 398 Troponinas
410 Dalykinė rodyklė Tulžies pigmentai 185, 188, 192, Tulžies rūgštys 120, 143, 195, 203, 249, 250, 253, 258, 268, 274, 275 Uremija 57, 70 72, 90, 166, 171, 177, 181, 364 Urobilinogenas 186, 191, 192, Urosterkobilinogenas 186, 191, 192, 198, 199 Ūminės fazės baltymai 95, 97, 98, , 108, , , 131, 303, 312 Vanduo 16, 21 37, 41, 42, 45 48, 52, 53, 68, 73, 77, 80, 84, 88, 91, 94, 100, 110, 114, 177, 190, 203, 221, 233, 275, 279, 283, 317, 322, , 371, 401 Varis 95, 102, 124, 203, 205, 207, 208, 235, , 287 Vazopresinas 36, 320, , 364 Vidinis α tripsino inhibitorius 98, 101 Ž mogaus chorioninis gonadotropinas 321, 330, 381, 383, 386, 387, 395,
411 410
412 Zita Aušrelė Kučinskienė KLINIKINĖS BIOCHEMIJOS ir LABORATORINĖS DIAGNOSTIKOS PAGRINDAI Viršelio dailininkė Audronė Uzielaitė Redaktorės Danutė Griniūtė ir Jolanta Storpirštienė Maketavo Nijolė Bukantienė Išleido Vilniaus universiteto leidykla Universiteto g. 1, LT Vilnius El. paštas: Spausdino AB Aušra Vytauto pr. 23, LT Kaunas
413 Rytis Stanikūnas, Laimonas Puišys, Aldona Radzevičienė, Henrikas Vaitkevičius. Spalvų porų patrauklumo vertinimo ypatumai 125
Slide 1
 RACIONALUS VAISTŲ VARTOJIMAS Med. Dr. Romualdas Basevičius INDIVIDUALIOS LIGONIO SĄLYGOS: VIDINĖS: Amžius Lytis Gretutiniai susirgimai IŠORINĖS: Vaistų dozės Vaistų skaičius Vartojimo laikas Darbo ir mitybos
RACIONALUS VAISTŲ VARTOJIMAS Med. Dr. Romualdas Basevičius INDIVIDUALIOS LIGONIO SĄLYGOS: VIDINĖS: Amžius Lytis Gretutiniai susirgimai IŠORINĖS: Vaistų dozės Vaistų skaičius Vartojimo laikas Darbo ir mitybos
Maisto lipidų pernaša ir jos sutrikimai. Audinių lipoproteinlipazės. Alimentinė lipemija. Akvilė Gaupšaitė Igr.
 Maisto lipidų pernaša ir jos sutrikimai. Audinių lipoproteinlipazės. Alimentinė lipemija. Akvilė Gaupšaitė Igr. Lipidai žmogaus organizme Maisto lipidai: o 1. Daugiausia trigliceridų (TAG) ~90 % o 2. Fosfolipidai;
Maisto lipidų pernaša ir jos sutrikimai. Audinių lipoproteinlipazės. Alimentinė lipemija. Akvilė Gaupšaitė Igr. Lipidai žmogaus organizme Maisto lipidai: o 1. Daugiausia trigliceridų (TAG) ~90 % o 2. Fosfolipidai;
Prezentacja programu PowerPoint
 TIENS KALCIS KALCIS Kalcis yra gyvybiškai svarbus cheminis elementas, kuris palaiko tinkamą žmogaus organizmo funkcionavimą KALCIO VAIDMUO ŽMOGAUS ORGANIZME Kalcis reikalingas normaliai kaulų būklei palaikyti
TIENS KALCIS KALCIS Kalcis yra gyvybiškai svarbus cheminis elementas, kuris palaiko tinkamą žmogaus organizmo funkcionavimą KALCIO VAIDMUO ŽMOGAUS ORGANIZME Kalcis reikalingas normaliai kaulų būklei palaikyti
Microsoft PowerPoint - Presentation1
 Danutė Povilėnaitė Reumatologijos centras Vilnius 2012-12-05 Įvadas Amiloidozės tai baltymų struktūros pokyčių ligos, kai įprastas tirpus baltymas virsta nenormaliu netirpiu fibriliniu baltymu, kuris deponuojasi
Danutė Povilėnaitė Reumatologijos centras Vilnius 2012-12-05 Įvadas Amiloidozės tai baltymų struktūros pokyčių ligos, kai įprastas tirpus baltymas virsta nenormaliu netirpiu fibriliniu baltymu, kuris deponuojasi
VETERINARINIO VAISTO APRAŠAS
 VETERINARINIO VAISTO APRAŠAS 1. VETERINARINIO VAISTO PAVADINIMAS Colvasone 2 mg/ml, injekcinis tirpalas 2. KOKYBINĖ IR KIEKYBINĖ SUDĖTIS 1 ml yra: veikliosios medžiagos: deksametazono (natrio fosfato)
VETERINARINIO VAISTO APRAŠAS 1. VETERINARINIO VAISTO PAVADINIMAS Colvasone 2 mg/ml, injekcinis tirpalas 2. KOKYBINĖ IR KIEKYBINĖ SUDĖTIS 1 ml yra: veikliosios medžiagos: deksametazono (natrio fosfato)
Senebactum PIL_Kaunas
 Pakuotės lapelis: informacija vartotojui Senebactum 100 mg/ml odos tirpalas Joduotas povidonas Atidžiai perskaitykite visą šį lapelį, prieš pradėdami vartoti šį vaistą, nes jame pateikiama Jums svarbi
Pakuotės lapelis: informacija vartotojui Senebactum 100 mg/ml odos tirpalas Joduotas povidonas Atidžiai perskaitykite visą šį lapelį, prieš pradėdami vartoti šį vaistą, nes jame pateikiama Jums svarbi
EGZAMINO PROGRAMOS MINIMALIUS REIKALAVIMUS ILIUSTRUOJANTYS PAVYZDŽIAI Egzamino programos minimalūs reikalavimai I. METODOLOGINIAI BIOLOGIJOS KLAUSIMAI
 EGZAMINO PROGRAMOS MINIMALIUS REIKALAVIMUS ILIUSTRUOJANTYS PAVYZDŽIAI Egzamino programos minimalūs reikalavimai I. METODOLOGINIAI BIOLOGIJOS KLAUSIMAI Minimalius reikalavimus iliustruojantys pavyzdžiai
EGZAMINO PROGRAMOS MINIMALIUS REIKALAVIMUS ILIUSTRUOJANTYS PAVYZDŽIAI Egzamino programos minimalūs reikalavimai I. METODOLOGINIAI BIOLOGIJOS KLAUSIMAI Minimalius reikalavimus iliustruojantys pavyzdžiai
Ibuprofen Art 31 CMDh agreement Annexes
 II priedas Mokslinės išvados ir pagrindas keisti rinkodaros leidimų sąlygas 355 Mokslinės išvados ir pagrindas keisti rinkodaros leidimų sąlygas Ibuprofenas yra nesteroidinis vaistas nuo uždegimo (NVNU),
II priedas Mokslinės išvados ir pagrindas keisti rinkodaros leidimų sąlygas 355 Mokslinės išvados ir pagrindas keisti rinkodaros leidimų sąlygas Ibuprofenas yra nesteroidinis vaistas nuo uždegimo (NVNU),
Microsoft Word - Document1
 PAKUOTĖS LAPELIS: INFORMACIJA VARTOTOJUI Betadine 100 mg/ml odos tirpalas Joduotas povidonas Atidžiai perskaitykite visą šį lapelį, nes jame pateikiama Jums svarbi informacija. Betadine galima įsigyti
PAKUOTĖS LAPELIS: INFORMACIJA VARTOTOJUI Betadine 100 mg/ml odos tirpalas Joduotas povidonas Atidžiai perskaitykite visą šį lapelį, nes jame pateikiama Jums svarbi informacija. Betadine galima įsigyti
Pakuotės lapelis: informacija vartotojui Berocca Plus šnypščiosios tabletės B grupės vitaminai, C vitaminas, kalcis, magnis, cinkas Atidžiai perskaity
 Pakuotės lapelis: informacija vartotojui Berocca Plus šnypščiosios tabletės B grupės vitaminai, C vitaminas, kalcis, magnis, cinkas Atidžiai perskaitykite visą šį lapelį, prieš pradėdami vartoti šį vaistą,
Pakuotės lapelis: informacija vartotojui Berocca Plus šnypščiosios tabletės B grupės vitaminai, C vitaminas, kalcis, magnis, cinkas Atidžiai perskaitykite visą šį lapelį, prieš pradėdami vartoti šį vaistą,
Meningokokinė infekcija klinika, diagnostika (Epideminis cerebrospinalinis meningitas) Doc. E. Broslavskis VU Infekcinių, krūtinės ligų, dermatovenero
 Meningokokinė infekcija klinika, diagnostika (Epideminis cerebrospinalinis meningitas) Doc. E. Broslavskis VU Infekcinių, krūtinės ligų, dermatovenerologijos ir alergologijos klinika 2012 gegužės 9 d.,
Meningokokinė infekcija klinika, diagnostika (Epideminis cerebrospinalinis meningitas) Doc. E. Broslavskis VU Infekcinių, krūtinės ligų, dermatovenerologijos ir alergologijos klinika 2012 gegužės 9 d.,
HOT-G II
 Heparino indukuotos trombocitopenijos (HIT) diagnostikos ir gydymo algoritmas Įvertinkite klinikinę HIT tikimybę, naudojantis 4T skale Atlikite antipf4/ heparino antikūnų titro tyrimą 1:4 ir, jei pastarasis
Heparino indukuotos trombocitopenijos (HIT) diagnostikos ir gydymo algoritmas Įvertinkite klinikinę HIT tikimybę, naudojantis 4T skale Atlikite antipf4/ heparino antikūnų titro tyrimą 1:4 ir, jei pastarasis
SIŪLOMO ĮRAŠYTI Į KOMPENSAVIMO SĄRAŠUS VAISTINIO PREPARATO FARMAKOEKONOMINĖS VERTĖS NUSTATYMO PROTOKOLAS (data) Vertinimas pirminis patiksl
 SIŪLOMO ĮRAŠYTI Į KOMPENSAVIMO SĄRAŠUS VAISTINIO PREPARATO FARMAKOEKONOMINĖS VERTĖS NUSTATYMO PROTOKOLAS 2017-11-27 (data) Vertinimas pirminis patikslintas Vilnius (sudarymo vieta) Paskutinio vertinimo
SIŪLOMO ĮRAŠYTI Į KOMPENSAVIMO SĄRAŠUS VAISTINIO PREPARATO FARMAKOEKONOMINĖS VERTĖS NUSTATYMO PROTOKOLAS 2017-11-27 (data) Vertinimas pirminis patikslintas Vilnius (sudarymo vieta) Paskutinio vertinimo
Vilniaus krašto 2019 m. mokymų planas Eil. Nr. Mokymų pradžios ir Registracijos vieta ir Grupės kodas Programos pavadinimas ir trukmė (val.) Mokymų vi
 1 12.8 Pacientų, turinčių limfotakos sutrikimų ir sergančių onkologinėmis ligomis, limfodrenažinis masažas (80 val.) 2019-08-19 2019-08-30 Eimantas Pocius, 9-10 V2019T12.8-2 13821 170 Eur 2 1.152 Saugus
1 12.8 Pacientų, turinčių limfotakos sutrikimų ir sergančių onkologinėmis ligomis, limfodrenažinis masažas (80 val.) 2019-08-19 2019-08-30 Eimantas Pocius, 9-10 V2019T12.8-2 13821 170 Eur 2 1.152 Saugus
CL2008L0100LT bi_cp 1..1
 2008L0100 LT 18.11.2008 000.001 1 Šis dokumentas yra skirtas tik informacijai, ir institucijos nėra teisiškai atsakingos už jo turinį B KOMISIJOS DIREKTYVA 2008/100/EB 2008 m. spalio 28 d. iš dalies keičianti
2008L0100 LT 18.11.2008 000.001 1 Šis dokumentas yra skirtas tik informacijai, ir institucijos nėra teisiškai atsakingos už jo turinį B KOMISIJOS DIREKTYVA 2008/100/EB 2008 m. spalio 28 d. iš dalies keičianti
TVIEŠOSIOS
 VIEŠOJI ĮSTAIGA PRIENŲ LIGONINĖ 2015 M. VEIKLOS ATASKAITA VšĮ Prienų ligoninės direktorė Jūratė Milaknienė PRIENAI 2016 LIGONINĖS MISIJA Teikti prieinamas, mokslu ir pažangiausiomis technologijomis pagrįstas,
VIEŠOJI ĮSTAIGA PRIENŲ LIGONINĖ 2015 M. VEIKLOS ATASKAITA VšĮ Prienų ligoninės direktorė Jūratė Milaknienė PRIENAI 2016 LIGONINĖS MISIJA Teikti prieinamas, mokslu ir pažangiausiomis technologijomis pagrįstas,
VETERINARINIO VAISTO APRAŠAS 1. VETERINARINIO VAISTO PAVADINIMAS ERGOGEN COMPLEX, injekcinis tirpalas 2. KOKYBINĖ IR KIEKYBINĖ SUDĖTIS 100 ml tirpalo
 VETERINARINIO VAISTO APRAŠAS 1. VETERINARINIO VAISTO PAVADINIMAS ERGOGEN COMPLEX, injekcinis tirpalas 2. KOKYBINĖ IR KIEKYBINĖ SUDĖTIS 100 ml tirpalo yra: veikliųjų medžiagų: L-histidino L-arginino 400
VETERINARINIO VAISTO APRAŠAS 1. VETERINARINIO VAISTO PAVADINIMAS ERGOGEN COMPLEX, injekcinis tirpalas 2. KOKYBINĖ IR KIEKYBINĖ SUDĖTIS 100 ml tirpalo yra: veikliųjų medžiagų: L-histidino L-arginino 400
2014 m. kovo 14 d. Komisijos reglamentas (ES) Nr. 274/2014, kuriuo taisoma Reglamento (ES) Nr. 432/2012 dėl tam tikrų leidžiamų vartoti teiginių apie
 LT 2014 3 20 Europos Sąjungos oficialusis leidinys L 83/1 II (Įstatymo galios neturintys teisės aktai) REGLAMENTAI KOMISIJOS REGLAMENTAS (ES) Nr. 274/2014 2014 m. kovo 14 d. kuriuo taisoma Reglamento (ES)
LT 2014 3 20 Europos Sąjungos oficialusis leidinys L 83/1 II (Įstatymo galios neturintys teisės aktai) REGLAMENTAI KOMISIJOS REGLAMENTAS (ES) Nr. 274/2014 2014 m. kovo 14 d. kuriuo taisoma Reglamento (ES)
ALYTAUS RAJONO SAVIVALDYBĖS VISUOMENĖS SVEIKATOS BIURAS ALYTAUS RAJONO MOKSLEIVIŲ SERGAMUMAS 2015 METŲ SAUSIO- BIRŽELIO MĖNESIŲ LAIKOTARPIU Parengė: A
 ALYTAUS RAJONO SAVIVALDYBĖS VISUOMENĖS SVEIKATOS BIURAS ALYTAUS RAJONO MOKSLEIVIŲ SERGAMUMAS 2015 METŲ SAUSIO- BIRŽELIO MĖNESIŲ LAIKOTARPIU Parengė: Alytaus rajono savivaldybės Visuomenės sveikatos biuro
ALYTAUS RAJONO SAVIVALDYBĖS VISUOMENĖS SVEIKATOS BIURAS ALYTAUS RAJONO MOKSLEIVIŲ SERGAMUMAS 2015 METŲ SAUSIO- BIRŽELIO MĖNESIŲ LAIKOTARPIU Parengė: Alytaus rajono savivaldybės Visuomenės sveikatos biuro
AKMENĖS RAJONO BENDROJO LAVINIMO MOKYKLŲ MOKINIŲ PROFILAKTINIŲ SVEIKATOS PATIKRINIMŲ DUOMENŲ ANALIZĖ 2016 M. Parengė: Akmenės rajono savivaldybės visu
 AKMENĖS RAJONO BENDROJO LAVINIMO MOKYKLŲ MOKINIŲ PROFILAKTINIŲ SVEIKATOS PATIKRINIMŲ DUOMENŲ ANALIZĖ 2016 M. Parengė: Akmenės rajono savivaldybės visuomenės sveikatos biuro visuomenės sveikatos stebėsenos
AKMENĖS RAJONO BENDROJO LAVINIMO MOKYKLŲ MOKINIŲ PROFILAKTINIŲ SVEIKATOS PATIKRINIMŲ DUOMENŲ ANALIZĖ 2016 M. Parengė: Akmenės rajono savivaldybės visuomenės sveikatos biuro visuomenės sveikatos stebėsenos
Kiekvienos įstaigos klaidingų atvejų skaičius (procentas) pagal kiekvieną specialųjį rodiklį
 2016 M. KLINIKINIO KODAVIMO STEBĖSENOS REZULTATŲ VERTINIMO ATASKAITOS priedas Kiekvienos įstaigos (procentas) pagal kiekvieną specialųjį rodiklį Respublikos lygmens ligoninė VšĮ Klaipėdos Jūrininkų ligoninė
2016 M. KLINIKINIO KODAVIMO STEBĖSENOS REZULTATŲ VERTINIMO ATASKAITOS priedas Kiekvienos įstaigos (procentas) pagal kiekvieną specialųjį rodiklį Respublikos lygmens ligoninė VšĮ Klaipėdos Jūrininkų ligoninė
Pakuotės lapelis: informacija vartotojui Kamiren XL 4 mg modifikuoto atpalaidavimo tabletės Doksazosinas Atidžiai perskaitykite visą šį lapelį, prieš
 Pakuotės lapelis: informacija vartotojui Kamiren XL 4 mg modifikuoto atpalaidavimo tabletės Doksazosinas Atidžiai perskaitykite visą šį lapelį, prieš pradėdami vartoti vaistą, nes jame pateikiama Jums
Pakuotės lapelis: informacija vartotojui Kamiren XL 4 mg modifikuoto atpalaidavimo tabletės Doksazosinas Atidžiai perskaitykite visą šį lapelį, prieš pradėdami vartoti vaistą, nes jame pateikiama Jums
65 m. amžiaus ir vyresnių asmenų sveikatos netolygumai Lietuvoje
 65 m. amžiaus ir vyresnių asmenų sveikatos netolygumai Lietuvoje Projekto vadovė: dr. Laura Nedzinskienė Atsakinga vykdytoja: Vaida Aguonytė, Jolanta Valentienė Tyrimo dalyvės: dr. Aušra Beržanskytė, Eimantė
65 m. amžiaus ir vyresnių asmenų sveikatos netolygumai Lietuvoje Projekto vadovė: dr. Laura Nedzinskienė Atsakinga vykdytoja: Vaida Aguonytė, Jolanta Valentienė Tyrimo dalyvės: dr. Aušra Beržanskytė, Eimantė
VAIKŲ, VARTOJANČIŲ NARKOTINES IR PSICHOTROPINES MEDŽIAGAS VARTOJIMO NUSTATYMO ORGANIZAVIMAS Atmintinė ugdymo įstaigų darbuotojams ir jose dirbantiems
 VAIKŲ, VARTOJANČIŲ NARKOTINES IR PSICHOTROPINES MEDŽIAGAS VARTOJIMO NUSTATYMO ORGANIZAVIMAS Atmintinė ugdymo įstaigų darbuotojams ir jose dirbantiems visuomenės sveikatos specialistams Vilnius, 2011 Atpažinti
VAIKŲ, VARTOJANČIŲ NARKOTINES IR PSICHOTROPINES MEDŽIAGAS VARTOJIMO NUSTATYMO ORGANIZAVIMAS Atmintinė ugdymo įstaigų darbuotojams ir jose dirbantiems visuomenės sveikatos specialistams Vilnius, 2011 Atpažinti
Kai kurie gyvūnai tokie primityvūs, kad jiems kraujotakos nereikia. Pvz., hidros kūno sandara tokia, kad visas ląsteles skalauja vanduo gaunamas O 2,
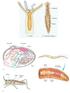 Kai kurie gyvūnai tokie primityvūs, kad jiems kraujotakos nereikia. Pvz., hidros kūno sandara tokia, kad visas ląsteles skalauja vanduo gaunamas O 2, visos jos turi priėjimą prie virškinamosios ertmės,
Kai kurie gyvūnai tokie primityvūs, kad jiems kraujotakos nereikia. Pvz., hidros kūno sandara tokia, kad visas ląsteles skalauja vanduo gaunamas O 2, visos jos turi priėjimą prie virškinamosios ertmės,
Helicobacter Test INFAI, C13-Urea
 I PRIEDAS PREPARATO CHARAKTERISTIKŲ SANTRAUKA 1 1. VAISTINIO PREPARATO PAVADINIMAS Helicobacter Test INFAI 75 mg milteliai geriamajam tirpalui 2. KOKYBINĖ IR KIEKYBINĖ SUDĖTIS Viename plačiakakliame inde
I PRIEDAS PREPARATO CHARAKTERISTIKŲ SANTRAUKA 1 1. VAISTINIO PREPARATO PAVADINIMAS Helicobacter Test INFAI 75 mg milteliai geriamajam tirpalui 2. KOKYBINĖ IR KIEKYBINĖ SUDĖTIS Viename plačiakakliame inde
SEPSIS: ankstyva diagnos2ka ir gydymas Parengė A. Bukauskas
 SEPSIS: ankstyva diagnos2ka ir gydymas Parengė A. Bukauskas 2011-07- 20 Planas AKTUALUMAS APIBRĖŽIMAS PATOFIZIOLOGIJA DIAGNOSTIKA GYDYMAS Aktualumas Pagrindinė ūmi būklė HOT centre (hematologinės ligos
SEPSIS: ankstyva diagnos2ka ir gydymas Parengė A. Bukauskas 2011-07- 20 Planas AKTUALUMAS APIBRĖŽIMAS PATOFIZIOLOGIJA DIAGNOSTIKA GYDYMAS Aktualumas Pagrindinė ūmi būklė HOT centre (hematologinės ligos
Januvia, INN-sitagliptin
 I PRIEDAS PREPARATO CHARAKTERISTIKŲ SANTRAUKA 1 1. VAISTINIO PREPARATO PAVADINIMAS Januvia 25 mg plėvele dengtos tabletės 2. KOKYBINĖ IR KIEKYBINĖ SUDĖTIS Kiekvienoje tabletėje yra sitagliptino fosfato
I PRIEDAS PREPARATO CHARAKTERISTIKŲ SANTRAUKA 1 1. VAISTINIO PREPARATO PAVADINIMAS Januvia 25 mg plėvele dengtos tabletės 2. KOKYBINĖ IR KIEKYBINĖ SUDĖTIS Kiekvienoje tabletėje yra sitagliptino fosfato
Microsoft Word - Utenos_raj_bio_2018_7-8kl..docx
 Utenos rajono mokinių biologijos olimpiada 2018 m. balandžio 19 d. UŽDUOTYS 7-8 klasei Mokinio Vardas, Pavardė... Klasė... Mokyklos pavadinimas... Mokytojo Vardas, Pavardė... Užduotis sudaro A, B ir C
Utenos rajono mokinių biologijos olimpiada 2018 m. balandžio 19 d. UŽDUOTYS 7-8 klasei Mokinio Vardas, Pavardė... Klasė... Mokyklos pavadinimas... Mokytojo Vardas, Pavardė... Užduotis sudaro A, B ir C
Pulmonologijos naujienos_is PDF.indd
 5 INTENSYVIOJI PULMONOLOGIJA III. Sergančiųjų ūminiu kvėpavimo nepakankamumu gydymas neinvazine plaučių ventiliacija Rolandas Zablockis Vilniaus universiteto Krūtinės ligų, imunologijos ir alergologijos
5 INTENSYVIOJI PULMONOLOGIJA III. Sergančiųjų ūminiu kvėpavimo nepakankamumu gydymas neinvazine plaučių ventiliacija Rolandas Zablockis Vilniaus universiteto Krūtinės ligų, imunologijos ir alergologijos
HOT-G II
 Hodžkino limfomos (HD) Klasifikatoriai Hodžkino limfomų klasifikatorius Nodulinė dominuojančių limfocitų Hodgkin limfoma WHO: 96593, TLK-10: C81.0 Klasikinė Hodgkin limfoma WHO: 96503, TLK-10: C81.9 Nodulinės
Hodžkino limfomos (HD) Klasifikatoriai Hodžkino limfomų klasifikatorius Nodulinė dominuojančių limfocitų Hodgkin limfoma WHO: 96593, TLK-10: C81.0 Klasikinė Hodgkin limfoma WHO: 96503, TLK-10: C81.9 Nodulinės
NAUJOVĖ Celiuliazė Beta gliukozidazė Individuali produkto koncepcija mažesniam klampumui ir geresniam substrato panaudojimui pasiekti Kitos gliukanazė
 NAUJOVĖ Celiuliazė Beta gliukozidazė Individuali produkto koncepcija mažesniam klampumui ir geresniam substrato panaudojimui pasiekti Kitos gliukanazės Ksilanazės Beta-ksilozidazė Arabinofuranozidazė Beta-galaktozidazė
NAUJOVĖ Celiuliazė Beta gliukozidazė Individuali produkto koncepcija mažesniam klampumui ir geresniam substrato panaudojimui pasiekti Kitos gliukanazės Ksilanazės Beta-ksilozidazė Arabinofuranozidazė Beta-galaktozidazė
VILNIAUS UNIVERSITETO ONKOLOGIJOS INSTITUTO VĖŽIO KONTROLĖS IR PROFILAKTIKOS CENTRAS VĖŽIO REGISTRAS Vėžys Lietuvoje 2010 metais ISSN
 VILNIAUS UNIVERSITETO ONKOLOGIJOS INSTITUTO VĖŽIO KONTROLĖS IR PROFILAKTIKOS CENTRAS VĖŽIO REGISTRAS Vėžys Lietuvoje 2010 metais ISSN 2029-6274 ISSN 2029-6274 Informacinį leidinį sudarė: Giedrė Smailytė
VILNIAUS UNIVERSITETO ONKOLOGIJOS INSTITUTO VĖŽIO KONTROLĖS IR PROFILAKTIKOS CENTRAS VĖŽIO REGISTRAS Vėžys Lietuvoje 2010 metais ISSN 2029-6274 ISSN 2029-6274 Informacinį leidinį sudarė: Giedrė Smailytė
1 023_028 antidotai
 PRIEŠNUODŽIŲ VARTOJIMAS Priešnuodis Amilnitritas Antibotulininis serumas Antitoksinis serumas Antitetaninis serumas Nuodingoji medžiaga Vandenilio sulfidas Indikacijos Aiški anamnez Sunkaus apsinuodijimo
PRIEŠNUODŽIŲ VARTOJIMAS Priešnuodis Amilnitritas Antibotulininis serumas Antitoksinis serumas Antitetaninis serumas Nuodingoji medžiaga Vandenilio sulfidas Indikacijos Aiški anamnez Sunkaus apsinuodijimo
DANTŲ ĖDUONIS IR PERIODONTO LIGOS Jau daugiau nei 200 metų ColgatePalmolive yra pasaulinis burnos priežiūros lyderis, siekiantis gerinti burnos sveika
 DANTŲ ĖDUONIS IR PERIODONTO LIGOS Jau daugiau nei 200 metų ColgatePalmolive yra pasaulinis burnos priežiūros lyderis, siekiantis gerinti burnos sveikatą visame pasaulyje. Įmonė gamina pastas ir rankinius
DANTŲ ĖDUONIS IR PERIODONTO LIGOS Jau daugiau nei 200 metų ColgatePalmolive yra pasaulinis burnos priežiūros lyderis, siekiantis gerinti burnos sveikatą visame pasaulyje. Įmonė gamina pastas ir rankinius
Microsoft Word - Ch-vert-1-09.doc
 PATVIRTINTA Nacionalinio egzaminų centro direktoriaus 009 m. birželio 6 d. įsakymu (..)-V-98 009 m. EMIJS VALSTYBINI BRANDS EGZAMIN UÞDUTIES VERTINIM INSTRUKIJA Kiekvienas I dalies klausimas vertinamas
PATVIRTINTA Nacionalinio egzaminų centro direktoriaus 009 m. birželio 6 d. įsakymu (..)-V-98 009 m. EMIJS VALSTYBINI BRANDS EGZAMIN UÞDUTIES VERTINIM INSTRUKIJA Kiekvienas I dalies klausimas vertinamas
JONIŠKIO RAJONO SAVIVALDYBĖS VISUOMENĖS SVEIKATOS BIURAS Savivaldybės biudžetinė įstaiga, Vilniaus g. 6, LT Joniškis, tel. (8 426) , faks.
 JONIŠKIO RAJONO SAVIVALDYBĖS VISUOMENĖS SVEIKATOS BIURAS Savivaldybės biudžetinė įstaiga, Vilniaus g. 6, LT-84147 Joniškis, tel. (8 426) 605 37, faks. (8 426) 605 36, el. p. joniskis.sveikata@gmail.com.
JONIŠKIO RAJONO SAVIVALDYBĖS VISUOMENĖS SVEIKATOS BIURAS Savivaldybės biudžetinė įstaiga, Vilniaus g. 6, LT-84147 Joniškis, tel. (8 426) 605 37, faks. (8 426) 605 36, el. p. joniskis.sveikata@gmail.com.
HIGIENOS INSTITUTAS HOSPITALINIŲ INFEKCIJŲ VALDYMO SVEIKATOS PRIEŽIŪROS ĮSTAIGOSE M. PROGRAMA HOSPITALINIŲ INFEKCIJŲ EPIDEMIOLOGINĖ PRIEŽIŪR
 HIGIENOS INSTITUTAS HOSPITALINIŲ INFEKCIJŲ VALDYMO SVEIKATOS PRIEŽIŪROS ĮSTAIGOSE 2007 2011 M. PROGRAMA HOSPITALINIŲ INFEKCIJŲ EPIDEMIOLOGINĖ PRIEŽIŪRA REANIMACIJOS - INTENSYVIOS TERAPIJOS SKYRIUOSE 2008
HIGIENOS INSTITUTAS HOSPITALINIŲ INFEKCIJŲ VALDYMO SVEIKATOS PRIEŽIŪROS ĮSTAIGOSE 2007 2011 M. PROGRAMA HOSPITALINIŲ INFEKCIJŲ EPIDEMIOLOGINĖ PRIEŽIŪRA REANIMACIJOS - INTENSYVIOS TERAPIJOS SKYRIUOSE 2008
Projektas
 Aplinkos apsaugos agentūrai ŪKIO SUBJEKTŲ APLINKOS MONITORINGO ATASKAITA 1. Informacija apie ūkio subjektą: 1.1. teisinis statusas: juridinis asmuo juridinio asmens struktūrinis padalinys (filialas, atstovybė)
Aplinkos apsaugos agentūrai ŪKIO SUBJEKTŲ APLINKOS MONITORINGO ATASKAITA 1. Informacija apie ūkio subjektą: 1.1. teisinis statusas: juridinis asmuo juridinio asmens struktūrinis padalinys (filialas, atstovybė)
VETERINARINIO VAISTO APRAŠAS 1. VETERINARINIO VAISTO PAVADINIMAS CANIGEN DHPPi/L liofilizatas ir suspensija injekcinei suspensijai ruošti šunims 2. KO
 VETERINARINIO VAISTO APRAŠAS 1. VETERINARINIO VAISTO PAVADINIMAS CANIGEN DHPPi/L liofilizatas ir suspensija injekcinei suspensijai ruošti šunims 2. KOKYBINĖ IR KIEKYBINĖ SUDĖTIS Vienoje 1 ml dozėje yra:
VETERINARINIO VAISTO APRAŠAS 1. VETERINARINIO VAISTO PAVADINIMAS CANIGEN DHPPi/L liofilizatas ir suspensija injekcinei suspensijai ruošti šunims 2. KOKYBINĖ IR KIEKYBINĖ SUDĖTIS Vienoje 1 ml dozėje yra:
VETERINARINIO VAISTO APRAŠAS 1. VETERINARINIO VAISTO PAVADINIMAS FLORKEM 300 mg/ml injekcinis tirpalas galvijams ir kiaulėms 2. KOKYBINĖ IR KIEKYBINĖ
 VETERINARINIO VAISTO APRAŠAS 1. VETERINARINIO VAISTO PAVADINIMAS FLORKEM 300 mg/ml injekcinis tirpalas galvijams ir kiaulėms 2. KOKYBINĖ IR KIEKYBINĖ SUDĖTIS Kiekviename ml yra: veikliosios medžiagos:
VETERINARINIO VAISTO APRAŠAS 1. VETERINARINIO VAISTO PAVADINIMAS FLORKEM 300 mg/ml injekcinis tirpalas galvijams ir kiaulėms 2. KOKYBINĖ IR KIEKYBINĖ SUDĖTIS Kiekviename ml yra: veikliosios medžiagos:
BYLOJE DĖL UAB „FARMAX BALTIC“ SIA LIETUVOS RESPUBLIKOS REKLAMOS ĮSTATYMO PAŽEIDIMO
 Išrašas VALSTYBINĖ VARTOTOJŲ TEISIŲ APSAUGOS TARNYBA VALSTYBINĖS VARTOTOJŲ TEISIŲ APSAUGOS TARNYBOS KOMISIJA NUTARIMAS BYLOJE DĖL UAB BIOKLINIKA LIETUVOS RESPUBLIKOS REKLAMOS ĮSTATYMO PAŽEIDIMO 2014-07-31
Išrašas VALSTYBINĖ VARTOTOJŲ TEISIŲ APSAUGOS TARNYBA VALSTYBINĖS VARTOTOJŲ TEISIŲ APSAUGOS TARNYBOS KOMISIJA NUTARIMAS BYLOJE DĖL UAB BIOKLINIKA LIETUVOS RESPUBLIKOS REKLAMOS ĮSTATYMO PAŽEIDIMO 2014-07-31
Avandia, INN-rosiglitazone
 I PRIEDAS PREPARATO CHARAKTERISTIKŲ SANTRAUKA 1 1. VAISTINIO PREPARATO PAVADINIMAS AVANDIA 2 mg plėvele dengtos tabletės 2. KOKYBINĖ IR KIEKYBINĖ SUDĖTIS Kiekvienoje tabletėje yra roziglitazono maleato
I PRIEDAS PREPARATO CHARAKTERISTIKŲ SANTRAUKA 1 1. VAISTINIO PREPARATO PAVADINIMAS AVANDIA 2 mg plėvele dengtos tabletės 2. KOKYBINĖ IR KIEKYBINĖ SUDĖTIS Kiekvienoje tabletėje yra roziglitazono maleato
Microsoft Word - Bio-MBE-analiz_2005.doc
 LIETUVOS RESPUBLIKOS ŠVIETIMO IR MOKSLO MINISTERIJA NACIONALINIS EGZAMINŲ CENTRAS 2005 M. BIOLOGIJOS MOKYKLINIO BRANDOS EGZAMINO REZULTATŲ KOKYBINĖ ANALIZĖ Jolanta Dzikavičiūtė, Danguolė Gižienė KOKYBINĖS
LIETUVOS RESPUBLIKOS ŠVIETIMO IR MOKSLO MINISTERIJA NACIONALINIS EGZAMINŲ CENTRAS 2005 M. BIOLOGIJOS MOKYKLINIO BRANDOS EGZAMINO REZULTATŲ KOKYBINĖ ANALIZĖ Jolanta Dzikavičiūtė, Danguolė Gižienė KOKYBINĖS
Alytaus regiono uždaryto Pagirmuonių sąvartyno aplinkos monitoringo 2017 m. ataskaita Ūkio subjektų aplinkos monitoringo nuostatų 4 priedas ALYTAUS RE
 Ūkio subjektų aplinkos monitoringo nuostatų 4 priedas ALYTAUS REGIONO UŽDARYTO PAGIRMUONIŲ SĄVARTYNO APLINKOS MONITORINGO 2017 M. ATASKAITA I BENDROJI DALIS 1. Informacija apie ūkio subjektą: 1.1. teisinis
Ūkio subjektų aplinkos monitoringo nuostatų 4 priedas ALYTAUS REGIONO UŽDARYTO PAGIRMUONIŲ SĄVARTYNO APLINKOS MONITORINGO 2017 M. ATASKAITA I BENDROJI DALIS 1. Informacija apie ūkio subjektą: 1.1. teisinis
[Version 7
 VETERINARINIO VAISTO APRAŠAS 1. VETERINARINIO VAISTO PAVADINIMAS STOMORGYL 20, tabletės 2. KOKYBINĖ IR KIEKYBINĖ SUDĖTIS Vienoje tabletėje yra: veikliųjų medžiagų: spiramicino metronidazolo 1 500 000 TV,
VETERINARINIO VAISTO APRAŠAS 1. VETERINARINIO VAISTO PAVADINIMAS STOMORGYL 20, tabletės 2. KOKYBINĖ IR KIEKYBINĖ SUDĖTIS Vienoje tabletėje yra: veikliųjų medžiagų: spiramicino metronidazolo 1 500 000 TV,
CTLA-4 BLOKADA PO ALOGENINĖS KKLT Skirmantė Bušeckaitė
 CTLA-4 BLOKADA PO ALOGENINĖS KKLT Skirmantė Bušeckaitė Intro Seniai žinoma, kad žmogaus imuninė sistema turi vidinį antinavikinį veikimo mechanizmą, o pagrindinis navikų progresijos mechanizmas yra galimybė
CTLA-4 BLOKADA PO ALOGENINĖS KKLT Skirmantė Bušeckaitė Intro Seniai žinoma, kad žmogaus imuninė sistema turi vidinį antinavikinį veikimo mechanizmą, o pagrindinis navikų progresijos mechanizmas yra galimybė
DĖL APLINKOS IR SVEIKATOS MOKSLO KOMITETO ĮSTEIGIMO
 LIETUVOS RESPUBLIKOS SVEIKATOS APSAUGOS MINISTRAS ĮSAKYMAS DĖL LIETUVOS RESPUBLIKOS SVEIKATOS APSAUGOS MINISTRO 011 M. KOVO D. ĮSAKYMO NR. V-199 DĖL LIETUVOS HIGIENOS NORMOS HN 80:011 ELEKTROMAGNETINIS
LIETUVOS RESPUBLIKOS SVEIKATOS APSAUGOS MINISTRAS ĮSAKYMAS DĖL LIETUVOS RESPUBLIKOS SVEIKATOS APSAUGOS MINISTRO 011 M. KOVO D. ĮSAKYMO NR. V-199 DĖL LIETUVOS HIGIENOS NORMOS HN 80:011 ELEKTROMAGNETINIS
NVSPL Analitė Automatinis hematologinis (kraujo) tyrimas Eritrocitų nusėdimo greitis (ENG) Kraujo grupės pagal ABO sistemą 1(21) NACIONALINĖS VISUOMEN
 Automatinis hematologinis (kraujo) tyrimas Eritrocitų nusėdimo greitis (ENG) Kraujo grupės pagal ABO sistemą 1(21) NACIONALINĖS VISUOMENĖS SVEIKATOS PRIEŽIŪROS LABORATORIJOS KLINIKINIŲ TYRIMŲ SKYRIAUS
Automatinis hematologinis (kraujo) tyrimas Eritrocitų nusėdimo greitis (ENG) Kraujo grupės pagal ABO sistemą 1(21) NACIONALINĖS VISUOMENĖS SVEIKATOS PRIEŽIŪROS LABORATORIJOS KLINIKINIŲ TYRIMŲ SKYRIAUS
Kantos Master - Draft Annex I at start of procedure
 II priedas Mokslinės išvados ir pagrindas keisti rinkodaros leidimų sąlygas 6 Mokslinės išvados Kantos Master ir susijusių pavadinimų (žr. I priedą) mokslinio vertinimo bendroji santrauka Bendroji informacija
II priedas Mokslinės išvados ir pagrindas keisti rinkodaros leidimų sąlygas 6 Mokslinės išvados Kantos Master ir susijusių pavadinimų (žr. I priedą) mokslinio vertinimo bendroji santrauka Bendroji informacija
VIEŠO NAUDOJIMO Aplinkos oro teršalų koncentracijos tyrimų, atliktų 2017 m. rugpjūčio d. Šiltnamių g. 23 Vilniaus mieste, naudojant mobiliąją la
 Aplinkos oro teršalų koncentracijos tyrimų, atliktų 2017 m. rugpjūčio 11 25 d. Šiltnamių g. 23 Vilniaus mieste, naudojant mobiliąją laboratoriją, rezultatų apžvalga Vilnius, 2017 m. Turinys Įžanga... 3
Aplinkos oro teršalų koncentracijos tyrimų, atliktų 2017 m. rugpjūčio 11 25 d. Šiltnamių g. 23 Vilniaus mieste, naudojant mobiliąją laboratoriją, rezultatų apžvalga Vilnius, 2017 m. Turinys Įžanga... 3
Microsoft Word - 8 Laboratorinis darbas.doc
 Laboratorinis darbas Nr. 8 MOP (metalo sido puslaidininkio) struktūrų tyrimas aukštadažniu -V charakteristikų metodu Darbo tikslas: 1. Nustatyti puslaidininkio laidumo tipą. 2. Nustatyti legiravimo priemaišų
Laboratorinis darbas Nr. 8 MOP (metalo sido puslaidininkio) struktūrų tyrimas aukštadažniu -V charakteristikų metodu Darbo tikslas: 1. Nustatyti puslaidininkio laidumo tipą. 2. Nustatyti legiravimo priemaišų
PULMONOLOGIJOS NAUJIENOS 2016 / Nr ŽIDINIŲ PLAUČIUOSE STEBĖJIMO PRINCIPAI Giedrė Cincilevičiūtė VšĮ Vilniaus universiteto ligoninės Santariškių
 PULMONOLOGIJOS NAUJIENOS 2016 / Nr. 5 66 ŽIDINIŲ PLAUČIUOSE STEBĖJIMO PRINCIPAI Giedrė Cincilevičiūtė VšĮ Vilniaus universiteto ligoninės Santariškių klinikų Pulmonologijos ir alergologijos centras Nėra
PULMONOLOGIJOS NAUJIENOS 2016 / Nr. 5 66 ŽIDINIŲ PLAUČIUOSE STEBĖJIMO PRINCIPAI Giedrė Cincilevičiūtė VšĮ Vilniaus universiteto ligoninės Santariškių klinikų Pulmonologijos ir alergologijos centras Nėra
Microsoft Word - Biseptyl
 VETERINARINIO VAISTO APRAŠAS 1. VETERINARINIO VAISTO PAVADINIMAS 2. KOKYBINö IR KIEKYBINö SUDöTIS 1 ml tirpalo yra: veikliųjų medžiagų: spektinomicino (sulfato) linkomicino (hidrochlorido) pagalbinių medžiagų:
VETERINARINIO VAISTO APRAŠAS 1. VETERINARINIO VAISTO PAVADINIMAS 2. KOKYBINö IR KIEKYBINö SUDöTIS 1 ml tirpalo yra: veikliųjų medžiagų: spektinomicino (sulfato) linkomicino (hidrochlorido) pagalbinių medžiagų:
VETERINARINIO VAISTO APRAŠAS 1. VETERINARINIO VAISTO PAVADINIMAS Prednisolonacetat 1 %, injekcinė suspensija galvijams, arkliams, šunims ir katėms 2.
 VETERINARINIO VAISTO APRAŠAS 1. VETERINARINIO VAISTO PAVADINIMAS Prednisolonacetat 1 %, injekcinė suspensija galvijams, arkliams, šunims ir katėms 2. KOKYBINĖ IR KIEKYBINĖ SUDĖTIS 1 ml suspensijos yra:
VETERINARINIO VAISTO APRAŠAS 1. VETERINARINIO VAISTO PAVADINIMAS Prednisolonacetat 1 %, injekcinė suspensija galvijams, arkliams, šunims ir katėms 2. KOKYBINĖ IR KIEKYBINĖ SUDĖTIS 1 ml suspensijos yra:
Microsoft Word - Liuminescencija_teorija
 2. BOLOGNŲ OBJEKTŲ LUMNESCENCJA. 2.1 Įvadas. Liuminescencijos reiškinys Daugelis fotofizikinių ir fotocheminių vyksmų yra šviesos sąveikos su bioobjektu pasekmės. Vienas iš pagrindinių šviesos emisijos
2. BOLOGNŲ OBJEKTŲ LUMNESCENCJA. 2.1 Įvadas. Liuminescencijos reiškinys Daugelis fotofizikinių ir fotocheminių vyksmų yra šviesos sąveikos su bioobjektu pasekmės. Vienas iš pagrindinių šviesos emisijos
PAKRUOJO RAJONO SAVIVALDYBĖS TARYBA SPRENDIMAS DĖL VIEŠOSIOS ĮSTAIGOS PAKRUOJO LIGONINĖS 2012 M. VADOVO VEIKLOS ATASKAITOS PATVIRTINIMO 2013 m. baland
 PAKRUOJO RAJONO SAVIVALDYBĖS TARYBA SPRENDIMAS DĖL VIEŠOSIOS ĮSTAIGOS PAKRUOJO LIGONINĖS 2012 M. VADOVO VEIKLOS ATASKAITOS PATVIRTINIMO 2013 m. balandžio 18 d. Nr. T-122 Pakruojis Vadovaudamasi Lietuvos
PAKRUOJO RAJONO SAVIVALDYBĖS TARYBA SPRENDIMAS DĖL VIEŠOSIOS ĮSTAIGOS PAKRUOJO LIGONINĖS 2012 M. VADOVO VEIKLOS ATASKAITOS PATVIRTINIMO 2013 m. balandžio 18 d. Nr. T-122 Pakruojis Vadovaudamasi Lietuvos
k
 KLINIKINIO KODAVIMO BIULETENIS 2016 m. balandis, Nr. 14. Šiame biuletenyje toliau aprašomi stacionare teikiamų aktyviojo gydymo ir transplantacijos paslaugų klinikinio kodavimo kokybės stebėsenos rodikliai.
KLINIKINIO KODAVIMO BIULETENIS 2016 m. balandis, Nr. 14. Šiame biuletenyje toliau aprašomi stacionare teikiamų aktyviojo gydymo ir transplantacijos paslaugų klinikinio kodavimo kokybės stebėsenos rodikliai.
KODĖL SVARBU VARTOTI VITAMINĄ D? Vitamino D trūkumas yra plačiai paplitęs reiškinys. Teigiama, kad žiemą šio vitamino nepakanka daugiau kaip 80 proc.
 KODĖL SVARBU VARTOTI VITAMINĄ D? Vitamino D trūkumas yra plačiai paplitęs reiškinys. Teigiama, kad žiemą šio vitamino nepakanka daugiau kaip 80 proc. mūsų planetos gyventojų. Lietuva ne išimtis saulėtų
KODĖL SVARBU VARTOTI VITAMINĄ D? Vitamino D trūkumas yra plačiai paplitęs reiškinys. Teigiama, kad žiemą šio vitamino nepakanka daugiau kaip 80 proc. mūsų planetos gyventojų. Lietuva ne išimtis saulėtų
Microsoft PowerPoint - Ernesto_epidemiolog_indik-UNODC
 Narkotinių ir psichotropinių medžiag iagų vartojimo ir narkomanijos paplitimo nustatymas, informacinių sistemų plėtra Pranešėjas: ERNESTAS JASAITIS Data: 2008 m. gegužės 30 d. NACIONALINĖS NARKOTIKŲ KONTROLĖS
Narkotinių ir psichotropinių medžiag iagų vartojimo ir narkomanijos paplitimo nustatymas, informacinių sistemų plėtra Pranešėjas: ERNESTAS JASAITIS Data: 2008 m. gegužės 30 d. NACIONALINĖS NARKOTIKŲ KONTROLĖS
1 Nuostatos „Saikingas alkoholio vartojimas yra kasdienio gyvenimo dalis” vertinimas
 Tyrimo rezultatai Parengė: Valstybinio psichikos sveikatos Priklausomybės ligų skyriaus Vyriausioji specialistė Lina Ignatavičiūtė 1 Turinys 1. Tiriamųjų tam tikrų alkoholinių gėrimų vartojimo dažnio vertinimas...
Tyrimo rezultatai Parengė: Valstybinio psichikos sveikatos Priklausomybės ligų skyriaus Vyriausioji specialistė Lina Ignatavičiūtė 1 Turinys 1. Tiriamųjų tam tikrų alkoholinių gėrimų vartojimo dažnio vertinimas...
SERGANČIŲJŲ CUKRINIU DIABETU MOKYMO PROGRAMA Skirta slaugytojams diabetologams 2015 PATVIRTINTA: LIETUVOS SLAUGYTOJŲ DIABETOLOGIŲ DRAUGIJOS LIETUVOS E
 SERGANČIŲJŲ CUKRINIU DIABETU MOKYMO PROGRAMA Skirta slaugytojams diabetologams 2015 PATVIRTINTA: LIETUVOS SLAUGYTOJŲ DIABETOLOGIŲ DRAUGIJOS LIETUVOS ENDOKRINOLOGŲ DRAUGIJOS Lietuvos endokrinologų draugija
SERGANČIŲJŲ CUKRINIU DIABETU MOKYMO PROGRAMA Skirta slaugytojams diabetologams 2015 PATVIRTINTA: LIETUVOS SLAUGYTOJŲ DIABETOLOGIŲ DRAUGIJOS LIETUVOS ENDOKRINOLOGŲ DRAUGIJOS Lietuvos endokrinologų draugija
MAITINKIS SVEIKAI, SUMAŽINK GRĖSMĘ SUSIRGTI VĖŽIU
 MAITINKIS SVEIKAI, SUMAŽINK GRĖSMĘ SUSIRGTI VĖŽIU Mūsų mityba gali padidinti vėžio išsivystymo grėsmę. Patikimų mokslinių įrodymų duomenimis apie 30 proc. vėžio atvejų išsivysčiusiose šalyse ir 20 proc.
MAITINKIS SVEIKAI, SUMAŽINK GRĖSMĘ SUSIRGTI VĖŽIU Mūsų mityba gali padidinti vėžio išsivystymo grėsmę. Patikimų mokslinių įrodymų duomenimis apie 30 proc. vėžio atvejų išsivysčiusiose šalyse ir 20 proc.
HC
 Hemoraginio cistito sukelto BK viruso po alogeninės kaulų čiulpų transplantacijos gydymas Roberta Petrauskaitė Aktualumas Daugiau kaip 80% suaugusiųjų - nustatoma serologiškai teigiamas BK virusas Latentinis
Hemoraginio cistito sukelto BK viruso po alogeninės kaulų čiulpų transplantacijos gydymas Roberta Petrauskaitė Aktualumas Daugiau kaip 80% suaugusiųjų - nustatoma serologiškai teigiamas BK virusas Latentinis
15. BIOCHEMINIAI TYRIMAI Kodas Paslaugos pavadinimas Kaina Kaina LT EUR Amoniako koncentracijos nustatymas 104,7 Lt 30,33 EUR Bendrojo bal
 15. BIOCHEMINIAI TYRIMAI Kodas Paslaugos pavadinimas Kaina Kaina LT EUR 15001 Amoniako koncentracijos nustatymas 104,7 Lt 30,33 EUR 15002 Bendrojo baltymo koncentracijos nustatymas 7,0 Lt 2,03 EUR 15003
15. BIOCHEMINIAI TYRIMAI Kodas Paslaugos pavadinimas Kaina Kaina LT EUR 15001 Amoniako koncentracijos nustatymas 104,7 Lt 30,33 EUR 15002 Bendrojo baltymo koncentracijos nustatymas 7,0 Lt 2,03 EUR 15003
EN
 LT LT LT EUROPOS BENDRIJŲ KOMISIJA Briuselis, 2008.6.27 COM(2008) 393 galutinis KOMISIJOS ATASKAITA EUROPOS PARLAMENTUI IR TARYBAI DĖL TARYBOS DIREKTYVOS 89/398/EEB DĖL VALSTYBIŲ NARIŲ ĮSTATYMŲ, SUSIJUSIŲ
LT LT LT EUROPOS BENDRIJŲ KOMISIJA Briuselis, 2008.6.27 COM(2008) 393 galutinis KOMISIJOS ATASKAITA EUROPOS PARLAMENTUI IR TARYBAI DĖL TARYBOS DIREKTYVOS 89/398/EEB DĖL VALSTYBIŲ NARIŲ ĮSTATYMŲ, SUSIJUSIŲ
IŠVADA DĖL KORUPCIJOS PASIREIŠKIMO TIKIMYBĖS NUSTATYMO VŠĮ VALSTYBĖS IR SAVIVALDYBIŲ TARNAUTOJŲ MOKYMO CENTRE DAINAVA Vadovaujantis Lietuvos Respublik
 IŠVADA DĖL KORUPCIJOS PASIREIŠKIMO TIKIMYBĖS NUSTATYMO VŠĮ VALSTYBĖS IR SAVIVALDYBIŲ TARNAUTOJŲ MOKYMO CENTRE DAINAVA Vadovaujantis Lietuvos Respublikos korupcijos prevencijos įstatymu (Žin., 2002, Nr.
IŠVADA DĖL KORUPCIJOS PASIREIŠKIMO TIKIMYBĖS NUSTATYMO VŠĮ VALSTYBĖS IR SAVIVALDYBIŲ TARNAUTOJŲ MOKYMO CENTRE DAINAVA Vadovaujantis Lietuvos Respublikos korupcijos prevencijos įstatymu (Žin., 2002, Nr.
VETERINARINIO VAISTO APRAŠAS 1. VETERINARINIO VAISTO PAVADINIMAS Folligon TV, liofilizatas ir skiediklis injekcinei suspensijai 2. KOKYBINĖ IR K
 VETERINARINIO VAISTO APRAŠAS 1. VETERINARINIO VAISTO PAVADINIMAS Folligon 1 000 TV, liofilizatas ir skiediklis injekcinei suspensijai 2. KOKYBINĖ IR KIEKYBINĖ SUDĖTIS 1 liofilizato buteliuke yra: veikliosios
VETERINARINIO VAISTO APRAŠAS 1. VETERINARINIO VAISTO PAVADINIMAS Folligon 1 000 TV, liofilizatas ir skiediklis injekcinei suspensijai 2. KOKYBINĖ IR KIEKYBINĖ SUDĖTIS 1 liofilizato buteliuke yra: veikliosios
Valstybės kontrolės rašto Nr. S-(10-1.8)-233 priedas Aukščiausioji audito institucija, jau daug metų skirdama ypatingą dėmesį vaiko teisių
 Valstybės kontrolės 2017-02-21 rašto Nr. S-(10-1.8)-233 priedas Aukščiausioji audito institucija, jau daug metų skirdama ypatingą dėmesį vaiko teisių apsaugai, yra atlikusi ne vieną auditą ir teikusi rekomendacijas
Valstybės kontrolės 2017-02-21 rašto Nr. S-(10-1.8)-233 priedas Aukščiausioji audito institucija, jau daug metų skirdama ypatingą dėmesį vaiko teisių apsaugai, yra atlikusi ne vieną auditą ir teikusi rekomendacijas
PATVIRTINTA Vilkaviškio rajono savivaldybės visuomenės sveikatos biuro direktoriaus 2017 m. kovo 1 d. įsakymu Nr. V-7 1 priedas Vilkaviškio Aušros gim
 PATVIRTINTA Vilkaviškio rajono savivaldybės visuomenės sveikatos biuro direktoriaus 2017 m. kovo 1 d. įsakymu Nr. V-7 1 priedas Vilkaviškio Aušros gimnazija (Ugdymo įstaigos pavadinimas) VISUOMENĖS SVEIKATOS
PATVIRTINTA Vilkaviškio rajono savivaldybės visuomenės sveikatos biuro direktoriaus 2017 m. kovo 1 d. įsakymu Nr. V-7 1 priedas Vilkaviškio Aušros gimnazija (Ugdymo įstaigos pavadinimas) VISUOMENĖS SVEIKATOS
Lithuanian translation of Induction of labour - Information for pregnant women, their partners and families Gimdymo sužadinimas Informacija nėščiosiom
 Lithuanian translation of Induction of labour - Information for pregnant women, their partners and families Gimdymo sužadinimas Informacija nėščiosioms, jų partneriams ir šeimoms Šiame lankstinuke rasite:
Lithuanian translation of Induction of labour - Information for pregnant women, their partners and families Gimdymo sužadinimas Informacija nėščiosioms, jų partneriams ir šeimoms Šiame lankstinuke rasite:
Šiaulių miesto bendrojo lavinimo mokyklų mokinių profilaktinių sveikatos patikrinimų duomenų analizė 2010 m. Vadovaujantis Lietuvos Respublikos Sveika
 Šiaulių miesto bendrojo lavinimo mokyklų mokinių profilaktinių sveikatos patikrinimų duomenų analizė 2010 m. Vadovaujantis Lietuvos Respublikos Sveikatos apsaugos ministro 2000 m. gegužės 31 d. įsakymu
Šiaulių miesto bendrojo lavinimo mokyklų mokinių profilaktinių sveikatos patikrinimų duomenų analizė 2010 m. Vadovaujantis Lietuvos Respublikos Sveikatos apsaugos ministro 2000 m. gegužės 31 d. įsakymu
VERSLO IR VADYBOS TECHNOLOGIJŲ PROGRAMA
 PATVIRTINTA Lietuvos Respublikos švietimo ir mokslo ministro 2007 m. rugsėjo 6 d. įsakymu Nr. ISAK-1790 VERSLO IR VADYBOS TECHNOLOGIJŲ BENDROJI PROGRAMA MOKINIAMS, BESIMOKANTIEMS PAGAL VIDURINIO UGDYMO
PATVIRTINTA Lietuvos Respublikos švietimo ir mokslo ministro 2007 m. rugsėjo 6 d. įsakymu Nr. ISAK-1790 VERSLO IR VADYBOS TECHNOLOGIJŲ BENDROJI PROGRAMA MOKINIAMS, BESIMOKANTIEMS PAGAL VIDURINIO UGDYMO
[Version 7, 08/ 2005]
![[Version 7, 08/ 2005] [Version 7, 08/ 2005]](/thumbs/101/150317338.jpg) VETERINARINIO VAISTO APRAŠAS 1. VETERINARINIO VAISTO PAVADINIMAS QUADRICAT, gyva liofilizuota ir inaktyvuota skysta vakcina 2. KOKYBINĖ IR KIEKYBINĖ SUDĖTIS Vienoje liofilizuotos vakcinos dozėje yra: gyvų
VETERINARINIO VAISTO APRAŠAS 1. VETERINARINIO VAISTO PAVADINIMAS QUADRICAT, gyva liofilizuota ir inaktyvuota skysta vakcina 2. KOKYBINĖ IR KIEKYBINĖ SUDĖTIS Vienoje liofilizuotos vakcinos dozėje yra: gyvų
(Microsoft Word - mokiniu sergamumo analiz\ )
 ŠIAULIŲ MIESTO BENDROJO LAVINIMO MOKYKLŲ MOKINIŲ PROFILAKTINIŲ SVEIKATOS PATIKRINIMŲ DUOMENŲ ANALIZö 212/13 M. Šiauliai, 212 Pagal mokyklų visuomen s sveikatos priežiūros specialisčių pateiktus duomenis
ŠIAULIŲ MIESTO BENDROJO LAVINIMO MOKYKLŲ MOKINIŲ PROFILAKTINIŲ SVEIKATOS PATIKRINIMŲ DUOMENŲ ANALIZö 212/13 M. Šiauliai, 212 Pagal mokyklų visuomen s sveikatos priežiūros specialisčių pateiktus duomenis
Slide 1
 Ar kanabinoidų preparatai pasižymi priešvėžiniu poveikiu: įrodymais pagrįstas vertinimas Kęstutis Sužiedėlis Nacionalinis vėžio institutas Vilniaus universitetas 2019-04-01 Kababinoidų klasifikacija; Pranešimo
Ar kanabinoidų preparatai pasižymi priešvėžiniu poveikiu: įrodymais pagrįstas vertinimas Kęstutis Sužiedėlis Nacionalinis vėžio institutas Vilniaus universitetas 2019-04-01 Kababinoidų klasifikacija; Pranešimo
Vorikonazolio koncentracijos stebėsena Roberta Petrauskaitė
 Vorikonazolio koncentracijos stebėsena Roberta Petrauskaitė Planas Ê Vaisto charakteristika Ê Vorikonazolio (VRC) terapinės dozės monitoravimo (TDM) multicentrinis tyrimas, nutrauktas anksčiau nei planuota
Vorikonazolio koncentracijos stebėsena Roberta Petrauskaitė Planas Ê Vaisto charakteristika Ê Vorikonazolio (VRC) terapinės dozės monitoravimo (TDM) multicentrinis tyrimas, nutrauktas anksčiau nei planuota
Hemlibra, INN-emicizumab
 I PRIEDAS PREPARATO CHARAKTERISTIKŲ SANTRAUKA 1 Vykdoma papildoma šio vaistinio preparato stebėsena. Tai padės greitai nustatyti naują saugumo informaciją. Sveikatos priežiūros specialistai turi pranešti
I PRIEDAS PREPARATO CHARAKTERISTIKŲ SANTRAUKA 1 Vykdoma papildoma šio vaistinio preparato stebėsena. Tai padės greitai nustatyti naują saugumo informaciją. Sveikatos priežiūros specialistai turi pranešti
Šiame sąsiuvinyje Jūs rasite keleto dalykų užduotis bei mokinio anketą
 Pagrindinės formulės Mechanika v v0 v = s/ t, a =, F = ma, F = mg, F Vg n = ρ sk, = Fs, N =, η = 100 %. t t v Šiluma m ρ =, Q = cm t, Q = λm, Q = Lm, Q = qm, η = 100 %. V Q Elektrodinamika q U l I =, I
Pagrindinės formulės Mechanika v v0 v = s/ t, a =, F = ma, F = mg, F Vg n = ρ sk, = Fs, N =, η = 100 %. t t v Šiluma m ρ =, Q = cm t, Q = λm, Q = Lm, Q = qm, η = 100 %. V Q Elektrodinamika q U l I =, I
Klaipėdos miesto suaugusiųjų žmonių gyvensenos ypatumai Dainora Bielskytė, visuomenės sveikatos specialistė, Klaipėdos miesto visuomenės sveikatos biu
 Klaipėdos miesto suaugusiųjų žmonių gyvensenos ypatumai Dainora Bielskytė, visuomenės sveikatos specialistė, Klaipėdos miesto visuomenės sveikatos biuras Tyrimo vykdytojas: UAB Eurotela Įvadas Daug įvairiausių
Klaipėdos miesto suaugusiųjų žmonių gyvensenos ypatumai Dainora Bielskytė, visuomenės sveikatos specialistė, Klaipėdos miesto visuomenės sveikatos biuras Tyrimo vykdytojas: UAB Eurotela Įvadas Daug įvairiausių
VETERINARINIO VAISTO APRAŠAS 1. VETERINARINIO VAISTO PAVADINIMAS Marbodex, ausų lašai, suspensija šunims 2. KOKYBINĖ IR KIEKYBINĖ SUDĖTIS 1 ml yra: ve
 VETERINARINIO VAISTO APRAŠAS 1. VETERINARINIO VAISTO PAVADINIMAS Marbodex, ausų lašai, suspensija šunims 2. KOKYBINĖ IR KIEKYBINĖ SUDĖTIS 1 ml yra: veikliųjų medžiagų: marbofloksacino klotrimazolo deksametazono
VETERINARINIO VAISTO APRAŠAS 1. VETERINARINIO VAISTO PAVADINIMAS Marbodex, ausų lašai, suspensija šunims 2. KOKYBINĖ IR KIEKYBINĖ SUDĖTIS 1 ml yra: veikliųjų medžiagų: marbofloksacino klotrimazolo deksametazono
Sveikatos rastingumo tyrimas-2012
 LIETUVOS RESPUBLIKOS SVEIKATOS APSAUGOS MINISTERIJA SVEIKATOS MOKYMO IR LIGŲ PREVENCIJOS CENTRAS VILNIAUS UNIVERSITETO MEDICINOS FAKULTETO VISUOMENĖS SVEIKATOS INSTITUTAS LIETUVOS GYVENTOJŲ SVEIKATOS RAŠTINGUMO
LIETUVOS RESPUBLIKOS SVEIKATOS APSAUGOS MINISTERIJA SVEIKATOS MOKYMO IR LIGŲ PREVENCIJOS CENTRAS VILNIAUS UNIVERSITETO MEDICINOS FAKULTETO VISUOMENĖS SVEIKATOS INSTITUTAS LIETUVOS GYVENTOJŲ SVEIKATOS RAŠTINGUMO
PATVIRTINTA Vyriausiojo gydytojo įsakymu Nr.55 LYGIŲ GALIMYBIŲ POLITIKOS ĮGYVENDINIMO IR VYKDYMO PRIEŽIŪROS TVARKA I SKYRIUS ĮVADAS 1. Vieš
 PATVIRTINTA Vyriausiojo gydytojo 2017-12-05 įsakymu Nr.55 LYGIŲ GALIMYBIŲ POLITIKOS ĮGYVENDINIMO IR VYKDYMO PRIEŽIŪROS TVARKA I SKYRIUS ĮVADAS 1. Viešosios įstaigos Klaipėdos sveikatos priežiūros centro
PATVIRTINTA Vyriausiojo gydytojo 2017-12-05 įsakymu Nr.55 LYGIŲ GALIMYBIŲ POLITIKOS ĮGYVENDINIMO IR VYKDYMO PRIEŽIŪROS TVARKA I SKYRIUS ĮVADAS 1. Viešosios įstaigos Klaipėdos sveikatos priežiūros centro
MOTYVUOTA IŠVADA DĖL KORUPCIJOS PASIREIŠKIMO TIKIMYBĖS Informuojame, kad vadovaujantis Lietuvos Respublikos korupcijos prevencijos įstatymu ir Korupci
 MOTYVUOTA IŠVADA DĖL KORUPCIJOS PASIREIŠKIMO TIKIMYBĖS Informuojame, kad vadovaujantis Lietuvos Respublikos korupcijos prevencijos įstatymu ir Korupcijos analizės atlikimo tvarka, patvirtinta Lietuvos
MOTYVUOTA IŠVADA DĖL KORUPCIJOS PASIREIŠKIMO TIKIMYBĖS Informuojame, kad vadovaujantis Lietuvos Respublikos korupcijos prevencijos įstatymu ir Korupcijos analizės atlikimo tvarka, patvirtinta Lietuvos
ŠIAULIŲ MUNICIPALINĖ APLINKOS TYRIMŲ LABORATORIJA Gegužių g. 94, Šiauliai. Įmonės kodas Tel. : +370 (41) ; el.p.:
 ŠIAULIŲ MUNICIPALINĖ APLINKOS TYRIMŲ LABORATORIJA Gegužių g. 94, 78365 Šiauliai. Įmonės kodas 145412194. Tel. : +370 (41) 51 41 44; el.p.: matl@splius.lt; www.matl.lt. ŠIAULIŲ MUNICIPALINIS PAVIRŠINIŲ
ŠIAULIŲ MUNICIPALINĖ APLINKOS TYRIMŲ LABORATORIJA Gegužių g. 94, 78365 Šiauliai. Įmonės kodas 145412194. Tel. : +370 (41) 51 41 44; el.p.: matl@splius.lt; www.matl.lt. ŠIAULIŲ MUNICIPALINIS PAVIRŠINIŲ
Microsoft Word - BIO-MBE- ST-AN_2005.doc
 LIETUVOS RESPULIKOS ŠVIETIMO IR MOKSLO MINISTERIJ NIONLINIS EGZMINŲ ENTRS 2 25 M. IOLOGIJOS MOKYKLINIO RNOS EGZMINO REZULTTŲ STTISTINĖ NLIZĖ 25 m. gegužės 2 d. biologijos mokyklinį brandos egzaminą laikė
LIETUVOS RESPULIKOS ŠVIETIMO IR MOKSLO MINISTERIJ NIONLINIS EGZMINŲ ENTRS 2 25 M. IOLOGIJOS MOKYKLINIO RNOS EGZMINO REZULTTŲ STTISTINĖ NLIZĖ 25 m. gegužės 2 d. biologijos mokyklinį brandos egzaminą laikė
red-BK_moduliai_ _Po redaktores
 P R O J E K T A S VP1-2.2-ŠMM-04-V-01-001 MOKYMOSI KRYPTIES PASIRINKIMO GALIMYBIŲ DIDINIMAS 14-19 METŲ MOKINIAMS, II ETAPAS: GILESNIS MOKYMOSI DIFERENCIJAVIMAS IR INDIVIDUALIZAVIMAS, SIEKIANT UGDYMO KOKYBĖS,
P R O J E K T A S VP1-2.2-ŠMM-04-V-01-001 MOKYMOSI KRYPTIES PASIRINKIMO GALIMYBIŲ DIDINIMAS 14-19 METŲ MOKINIAMS, II ETAPAS: GILESNIS MOKYMOSI DIFERENCIJAVIMAS IR INDIVIDUALIZAVIMAS, SIEKIANT UGDYMO KOKYBĖS,
VšĮ Radviliškio ligoninė
 PATVIRTINTA Viešosios įstaigos Radviliškio ligoninės direktoriaus 2006 m. spalio 20 d. įsakymu Nr. V-180 (Viešosios įstaigos Radviliškio ligoninės direktoriaus 2014 m. gruodžio 31 d. įsakymo Nr. V-272
PATVIRTINTA Viešosios įstaigos Radviliškio ligoninės direktoriaus 2006 m. spalio 20 d. įsakymu Nr. V-180 (Viešosios įstaigos Radviliškio ligoninės direktoriaus 2014 m. gruodžio 31 d. įsakymo Nr. V-272
PRITARTA Alytaus miesto savivaldybės tarybos 2011 m. d. sprendimu Nr. ALYTAUS MIESTO SAVIVALDYBĖS VISUOMENĖS SVEIKATOS STEBĖSENOS METŲ PROGR
 PRITARTA Alytaus miesto savivaldybės tarybos 2011 m. d. sprendimu Nr. ALYTAUS MIESTO SAVIVALDYBĖS VISUOMENĖS SVEIKATOS STEBĖSENOS 2009 2011 METŲ PROGRAMOS 2010 METŲ ATASKAITA I. ĮVADAS Alytaus miesto savivaldybės
PRITARTA Alytaus miesto savivaldybės tarybos 2011 m. d. sprendimu Nr. ALYTAUS MIESTO SAVIVALDYBĖS VISUOMENĖS SVEIKATOS STEBĖSENOS 2009 2011 METŲ PROGRAMOS 2010 METŲ ATASKAITA I. ĮVADAS Alytaus miesto savivaldybės
Alkoholis, jo poveikis paauglio organizmui ir elgesiui, vartojimo priežastys ir pasekmės Justinos Jurkšaitės (I e) nuotr.
 Alkoholis, jo poveikis paauglio organizmui ir elgesiui, vartojimo priežastys ir pasekmės Justinos Jurkšaitės (I e) nuotr. Paauglystė svarbus gyvenimo laikotarpis, kuris tęsiasi nuo fizinio lytinio brendimo
Alkoholis, jo poveikis paauglio organizmui ir elgesiui, vartojimo priežastys ir pasekmės Justinos Jurkšaitės (I e) nuotr. Paauglystė svarbus gyvenimo laikotarpis, kuris tęsiasi nuo fizinio lytinio brendimo
KANITERAPIN∏S PAGALBOS CENTRAS
 KANITERAPINĖS PAGALBOS CENTRAS PADEDAME SVEIKTI Kaniterapijos ištakos Kaniterapijos istorija rašoma nuo Antrojo pasaulinio karo metų. Kapralas Williamas Wynas karo lauke rado Jorkšyro terjerų kalaitę
KANITERAPINĖS PAGALBOS CENTRAS PADEDAME SVEIKTI Kaniterapijos ištakos Kaniterapijos istorija rašoma nuo Antrojo pasaulinio karo metų. Kapralas Williamas Wynas karo lauke rado Jorkšyro terjerų kalaitę
Nexa serija Stūmokliniai ir hidrauliniai dozavimo siurbliai su dviguba diafragma UAB Elega, Žalgirio , Vilnius, LT 08217, Lietuva, Tel:
 Nexa serija Stūmokliniai ir hidrauliniai dozavimo siurbliai su dviguba diafragma UAB Elega, Žalgirio 131-211, Vilnius, LT 08217, Lietuva, Tel: +370 5 2 715444; tel./faksas: +370 5 2 715445; mob. tel.:
Nexa serija Stūmokliniai ir hidrauliniai dozavimo siurbliai su dviguba diafragma UAB Elega, Žalgirio 131-211, Vilnius, LT 08217, Lietuva, Tel: +370 5 2 715444; tel./faksas: +370 5 2 715445; mob. tel.:
Microsoft PowerPoint - JPSPPM mokymai_2015_10_08_09_3 dalis_AS [Compatibility Mode]
![Microsoft PowerPoint - JPSPPM mokymai_2015_10_08_09_3 dalis_AS [Compatibility Mode] Microsoft PowerPoint - JPSPPM mokymai_2015_10_08_09_3 dalis_AS [Compatibility Mode]](/thumbs/88/116318474.jpg) Projektas JAUNIMUI PALANKIŲ SVEIKATOS PRIEŽIŪROS PASLAUGŲ TEIKIMO MODELIO SUKŪRIMAS Finansuojamas pagal 2009 2014 m. Norvegijos finansinio mechanizmo programą Nr. LT11 Visuomenės sveikatai skirtos iniciatyvos
Projektas JAUNIMUI PALANKIŲ SVEIKATOS PRIEŽIŪROS PASLAUGŲ TEIKIMO MODELIO SUKŪRIMAS Finansuojamas pagal 2009 2014 m. Norvegijos finansinio mechanizmo programą Nr. LT11 Visuomenės sveikatai skirtos iniciatyvos
2010 m. vakcinomis valdomu ligu epidemiologines situacijos apzvalga Lietuvoje
 VAKCINOMIS VALDOMŲ LIGŲ EIPIDEMIOLOGINĖS SITUACIJOS APŽVALGA LIETUVOJE 2010 metai UŽKREČIAMŲJŲ LIGŲ IR AIDS CENTRAS LIETUVOS RESPUBLIKOS SVEIKATOS APSAUGOS MINISTERIJA Vilnius 2011 Parengė Imunoprofilaktikos
VAKCINOMIS VALDOMŲ LIGŲ EIPIDEMIOLOGINĖS SITUACIJOS APŽVALGA LIETUVOJE 2010 metai UŽKREČIAMŲJŲ LIGŲ IR AIDS CENTRAS LIETUVOS RESPUBLIKOS SVEIKATOS APSAUGOS MINISTERIJA Vilnius 2011 Parengė Imunoprofilaktikos
PATVIRTINTA
 PATVIRTINTA Vilniaus kolegijos Verslo vadybos fakulteto dekano 2018 m. gruodžio 19 d. įsakymu Nr. V-100 VILNIAUS KOLEGIJA VERSLO VADYBOS FAKULTETAS PRAKTIKŲ ORGANIZAVIMO TVARKA I. BENDROSIOS NUOSTATOS
PATVIRTINTA Vilniaus kolegijos Verslo vadybos fakulteto dekano 2018 m. gruodžio 19 d. įsakymu Nr. V-100 VILNIAUS KOLEGIJA VERSLO VADYBOS FAKULTETAS PRAKTIKŲ ORGANIZAVIMO TVARKA I. BENDROSIOS NUOSTATOS
MES PAKEISIME JŪSŲ GYVENIMO KOKYBĘ ASV-P balansinis ventilis su 1.5 m impulsiniu vamzdeliu (G1/16 A) ir dreno čiaupu (G 3/4 A) Pastovus slėgio perkryt
 MES PAKEISIME JŪSŲ GYVENIMO KOKYBĘ ASV-P balansinis ventilis su 1.5 m impulsiniu vamzdeliu (G1/16 A) ir dreno čiaupu (G 3/4 A) Pastovus slėgio perkrytis 0.1 bar (10 kpa) ASV-PV balansinis ventilis su m
MES PAKEISIME JŪSŲ GYVENIMO KOKYBĘ ASV-P balansinis ventilis su 1.5 m impulsiniu vamzdeliu (G1/16 A) ir dreno čiaupu (G 3/4 A) Pastovus slėgio perkrytis 0.1 bar (10 kpa) ASV-PV balansinis ventilis su m
Lietuvos energetikos instituto
 LIETUVOS ENERGETIKOS INSTITUTO ŠILUMINIŲ ĮRENGIMŲ TYRIMO IR BANDYMŲ LABORATORIJA AKREDITAVIMO SRITIS (Lanksti sritis) 1(11) puslapis 1. Membraniniai dujų skaitikliai, kurių didžiausias debitas Q max 16
LIETUVOS ENERGETIKOS INSTITUTO ŠILUMINIŲ ĮRENGIMŲ TYRIMO IR BANDYMŲ LABORATORIJA AKREDITAVIMO SRITIS (Lanksti sritis) 1(11) puslapis 1. Membraniniai dujų skaitikliai, kurių didžiausias debitas Q max 16
Prezentacja programu PowerPoint
 TIENS DiCHO II kartos prietaisas vaisiams ir daržovėms valyti (ozonatorius) PROBLEMOS, KURIAS SUKELIA APLINKOS TARŠA PARAZITAI MIKROORGANIZMAI BAKTERIJOS Švieži vaisiai ir daržovės yra spalvingi ir skanūs,
TIENS DiCHO II kartos prietaisas vaisiams ir daržovėms valyti (ozonatorius) PROBLEMOS, KURIAS SUKELIA APLINKOS TARŠA PARAZITAI MIKROORGANIZMAI BAKTERIJOS Švieži vaisiai ir daržovės yra spalvingi ir skanūs,
Microsoft Word - svetainei.prof. mokymas..doc
 ir įsigyti paklausią specialybę Sveikatos statistiko mokymo programa Mokymo trukmė 4 sav., 160 val. Skirta asmenims, norintiems dirbti sveikatos statistikais įvairiose sveikatos priežiūros įstaigose. Sveikatos
ir įsigyti paklausią specialybę Sveikatos statistiko mokymo programa Mokymo trukmė 4 sav., 160 val. Skirta asmenims, norintiems dirbti sveikatos statistikais įvairiose sveikatos priežiūros įstaigose. Sveikatos
Ginčo byla Nr LIETUVOS BANKO PRIEŽIŪROS TARNYBOS FINANSINIŲ PASLAUGŲ IR RINKŲ PRIEŽIŪROS DEPARTAMENTO DIREKTORIUS SPRENDIMAS DĖL N. J. IR
 Ginčo byla Nr. 2016-00757 LIETUVOS BANKO PRIEŽIŪROS TARNYBOS FINANSINIŲ PASLAUGŲ IR RINKŲ PRIEŽIŪROS DEPARTAMENTO DIREKTORIUS SPRENDIMAS DĖL N. J. IR UAB PZU LIETUVA GYVYBĖS DRAUDIMAS GINČO NAGRINĖJIMO
Ginčo byla Nr. 2016-00757 LIETUVOS BANKO PRIEŽIŪROS TARNYBOS FINANSINIŲ PASLAUGŲ IR RINKŲ PRIEŽIŪROS DEPARTAMENTO DIREKTORIUS SPRENDIMAS DĖL N. J. IR UAB PZU LIETUVA GYVYBĖS DRAUDIMAS GINČO NAGRINĖJIMO
