VYTAUTO DIDŽIOJO UNIVERSITETAS IMUNOCHROMATOGRAFINIO TYRIMO METODO PATIKIMUMO ĮVERTINIMAS ATLIEKANT ŽMOGAUS IMUNODEFICITO VIRUSO ASPEKTŲ ANALIZĘ
|
|
|
- Povilas Urbonas
- prieš 3 metus
- Peržiūrų:
Transkriptas
1 VYTAUTO DIDŽIOJO UNIVERSITETAS GAMTOS MOKSLŲ FAKULTETAS BIOCHEMIJOS IR BIOTECHNOLOGIJŲ KATEDRA Eglė Balčiūnaitė IMUNOCHROMATOGRAFINIO TYRIMO METODO PATIKIMUMO ĮVERTINIMAS ATLIEKANT ŽMOGAUS IMUNODEFICITO VIRUSO ASPEKTŲ ANALIZĘ Magistro baigiamasis darbas Molekulinės biologijos ir biotechnologijos studijų programa, valstybinis kodas 621C71001 Molekulinė biologijos, biofizikos ir biochemijos studijų kryptis Vadovas (-ė) Doc. dr. Raimonda Matulionytė (Moksl. laipsnis, vardas, pavardė) (Parašas) (Data) Apginta GMF dekanas (Fakulteto/studijų instituto dekanas/direktorius) (Parašas) (Data) Kaunas, 2014
2 TURINYS SANTRAUKA... 3 SUMMARY...4 SANTRUMPŲ SĄRAŠAS...5 ĮVADAS LITERATŪROS APŽVALGA Žmogaus imunodeficito viruso raida Retrovirusų bendra charakteristika ŽIV viruso struktūra ŽIV viruso replikacija žmogaus organizme Žmogaus imunodeficito viruso klinika ŽIV diagnostika PSO testavimo strategija ŽIV infekcijos nustatymui TYRIMŲ METODIKOS Imunochromatografinis ŽIV tyrimas FIRST RESPONSE HIV CARD TEST rinkinio sudėtis FIRST RESPONSE HIV CARD TEST reagentų laikymas ir stabilumas Tyrime naudojamų mėginių surinkimas ir saugojimas Įspėjimai Tyrimo procedūra Tyrimo apribojimai Imunofermentinis ŽIV tyrimas GENSCREEN PLUS HIV Ag-Ab rinkinio sudėtis Reikalingos medžiagos, nepateiktos rinkinyje Reagentų paruošimas tyrimui Mėginių paėmimas ir naudojimas Įspėjimai Tyrimo procedūra Rezultatų apskaičiavimas ir interpretacija Tyrimo apribojimai ŽIV Western Blot tyrimas Rinkinio sudėtis Reikalingos medžiagos, nepateiktos rinkinyje Reagentų paruošimas tyrimui Reagentų laikymo sąlygos Įspėjimai Mėginių paėmimas ir naudojimas Tyrimo procedūra Tyrimo rezultatų įvertinimas Tyrimo apribojimai TIRIAMOJI DALIS Tiriamųjų imtis Tyrimo metodas Tyrimo eiga ir naudojamos priemonės Imunochromatografiniu tyrimo metodu atliktų ŽIV tyrimų analizė ir apibendrinimas...49 IŠVADOS...57 LITERATŪROS SĄRAŠAS
3 SANTRAUKA Baigiamojo darbo autorius: Pilnas baigiamojo darbo pavadinimas: Baigiamojo darbo vadovas: Baigiamojo darbo atlikimo vieta ir metai: Puslapių skaičius: Lentelių skaičius: Paveikslų skaičius: Eglė Balčiūnaitė Imunochromatografinio tyrimo metodo patikimumo įvertinimas atliekant Žmogaus imunodeficito viruso aspektų analizę Doc. dr. Raimonda Matulionytė Vytauto Didžioji universitetas, Gamtos mokslų fakultetas, Kaunas, Šio baigiamojo darbo tikslas įvertinti imunochromatografinio tyrimo metodo patikimumą, atliekant Žmogaus imunodeficito viruso aspektų analizę. Siekiant įvertinti imunochromatografinio tyrimo metodo patikimumą, ŽIV tyrimai buvo atliekami atrankiniu FIRST RESPONSE HIV CARD TEST testu, pagrįstu nagrinėjamu metodu. Tyrimas atliktas Infekcinių ligų ir tuberkuliozės ligoninės, VšĮ Vilniaus universiteto ligoninės Santariškių klinikų filialo laboratorijoje. ŽIV tyrimai atlikti visiems metų amžiaus pacientams, hospitalizuotiems į Infekcinių ligų ir tuberkuliozės ligoninės Žvėryno stacionarą, taip pat ambulatoriškai konsultuojamiems dėl nepatikslintos kilmės karščiavimo, bėrimo, limfadenopatijos, mononukleozinio sindromo, užsitęsusio arba besikartojančio viduriavimo bei virusinių hepatitų nuo iki Gauti teigiami mėginiai buvo siunčiami į Nacionalinę visuomenės sveikatos priežiūros laboratoriją, kurioje atlikti patvirtinamieji tyrimai dėl ŽIV. Ne visi teigiami mėginiai buvo patvirtinti, tačiau šio tyrimo metu buvo atskleista 14 naujų ŽIV atvejų per metus. Siekiant nustatyti gautų klaidingai teigiamų rezultatų susidarymo priežastį, buvo atrinkti pacientai, kuriems nebuvo patvirtinti atrankiniai ŽIV tyrimai. Išnagrinėjus pagrindines jų tuometines diagnozes, nustatyta kad daugiausiai klaidingai teigiamų rezultatų gaunama sergant šiomis infekcinėmis ligomis: rože, Epštein Baro sukelta mononukleoze ir hepatitu A. 3
4 SUMMARY Author of Master Thesis: Full title Master Thesis: Supervisor: Presented at: Number of pages: Number of tables: Number of picture: Eglė Balčiūnaitė The assessment of reliability of immunochromatographic method carrying out the analys of human immunodeficiency virus aspects Doc. dr. Raimonda Matulionytė Vytautas Magnus University, Faculty of biology, Kaunas, The main goal of this paper is to assess the reliability of the immunochromatographic method carrying out the analysis of human immunodeficiency virus aspects. In order to assess the reliability of immunochromatographic method, the HIV tests were performed using the selective FIRST RESPONSE CARD TEST HIV test, based on the method in question. The assay was carried out in the Laboratory of National Tuberculosis and Infectious disease hospital in Vilnius. The HIV tests were carried out from till to all patients aged years, who were hospitalized in the National Tuberculosis and Infectious disease hospital in Vilnius as well as to outpatient, who were consulted due to fever of unspecified origin, rash, lymphadenopathy, mononucleosis syndrome, prolonged or recurrent diarrhea and viral hepatitis. All positive samples were sent to National Public Health Surveillance Laboratory for final confirmation. Not all the samples were confirmed, but this assay revealed 14 new cases of HIV per year. In order to identify the reasons of false positive results, the patients, whose selective HIV tests were not approved, have been selected and after the examination of their diagnoses, it was found that the majority of false-positive results were received to patients with the following infections: rose, mononucleosis induced by Epstein - Barr virus and hepatitis A. 4
5 SANTRUMPŲ SĄRAŠAS AIDS - Įgytas imuninio nepakankamumo sindromas AT Atvirkštinė transkriptazė CDC Centers for Disease Control an Prevention (JAV ligų kontrolės ir prevencijos centras) cdnr Complementary DNA (komplementari DNR) CRF Corticotropin - releasing factor (kortikotropiną atpalaiduojantis faktorius) EIA Enzyme immunoassay (imunofermentinė analizė) ELISA - Enzyme-linked immunosorbent assay (imunofermentinė analizė) env Genomo dalis, koduojanti paviršinius baltymus gag Genomo dalis, koduojanti šerdinius ir struktūrinius baltymus HTLV-1 Human T-lymphotropic virus 1 (1 tipo žmogaus limfotropinis virusas) HTLV-2 - Human T-lymphotropic virus 2 (2 tipo žmogaus limfotropinis virusas) IL Interleukinas ILTL Infekcinių ligų ir tuberkuliozės ligoninė irnr Informacinė ribonukleino rūgštis LAV Lymphadenopathy associated virus (limfodenopatiją sukeliantis virusas) MMWR Morbidity and Mortality Weekly Report (sergamumo ir mirštamumo savaitraštis) NVSPL Nacionalinė visuomenės sveikatos priežiūros laboratorija pol Genomo dalis, koduojanti atvirkštinės transkriptazės, proteazės ir integrazės fermentų baltymus PSO Pasaulio sveikatos organizacija RNR Ribonukleino rūgštis SIV - Simian immunodeficiency virus (beždžionių imunodeficito virusas) SIVcpz - Chimpanzees Simian immunodeficiency virus (Centrinės Afrikos šimpanzių imunodeficito virusas SIVsm Sooty mangabeys Simian immunodeficiency virus (Cercocebus atys beždžionių imunodeficito virusas) ŽIV Žmogaus imunodeficito virusas 5
6 ĮVADAS Darbą atlikau Infekcinių ligų ir tuberkuliozės ligoninės, VšĮ Vilniaus universiteto ligoninės Santariškių klinikų filialo laboratorijoje. Šį darbą atlikau siekdama įvertinti Infekcinių ligų ir tuberkuliozės ligoninėje naudojamų atrankinių FIRST RESPONSE HIV CARD TEST testų, pagrįstų imunochromatografiniu tyrimo metodu, gautų teigiamų rezultatų patikimumą bei nustatyti susidariusių klaidingai teigiamų rezultatų priežastį. Atrankiniuose tyrimuose naudojami ŽIV testai pasižymi dideliu jautrumu ir yra naudojami siekiant nustatyti visus galimai infekuotus asmenis. Didelis tyrimo jautrumas gali nulemti klaidingai teigiamų rezultatų susidarymą, tačiau gauti neigiami rezultatai yra patikimi. Priešingai yra su didelio specifiškumo testais, kurie dėl ŽIV viruso kintamumo gali iššaukti klaidingai neigiamus rezultatus. Diagnostikoje naudojamų ŽIV testų jautrumas ir specifiškumas turėtų būti ypatingai aukštas tam, kad būtų išvengiama klaidingų rezultatų, tačiau praktiškai tai yra sunkiai pasiekiama. Dėl šios priežasties serologinis tyrimas dėl ŽIV susideda iš kelių etapų: pirmiausia, atliekami didelio jautrumo testai siekiant atrinkti visus galimai infekuotus tiriamuosius, po to, atrinkti ŽIV teigiami mėginiai kartojami atliekant didelio specifiškumo testus, kad būtų galutinai patvirtinami. Darbo tikslas: įvertinti imunochromatografinio tyrimo metodo patikimumą atliekant Žmogaus imunodeficito viruso aspektų analizę. Tikslui įgyvendinti buvo iškelti uždaviniai: 1. Išanalizuoti nuo iki atliktų atrankinių ŽIV tyrimų rezultatus atsižvelgiant į pacientų lytį ir amžių; 2. Išanalizuoti gautų teigiamų atrankinių ŽIV tyrimų rezultatų patikimumą; 3. Nustatyti nepatvirtintų teigiamų rezultatų susidarymo priežastį. 6
7 1. LITERATŪROS APŽVALGA 1.1 Žmogaus imunodeficito viruso raida Žmogaus imunodeficito virusas tai virusas, kuris sukelia nepagydomą, įgytą imuninio nepakankamumo sindromą. Pirmos žinios apie šią infekciją pasklido 1981 m. birželio 5 d., kai CDC savaitraštis MMWR pranešė apie 5 jaunų, anksčiau buvusių sveikų homoseksualių vyrų Pneumocystis jirovecii sukeltos pneumonijos atvejus Los Andžele. Jiems buvo diagnozuotos ir kitos oportunistinės infekcijos, rodančios imuninės sistemos pažeidimą, kuriomis normalų imunitetą turintys asmenys paprastai neserga. Praėjus vos kelioms dienoms po pranešimo į CDC pradėjo plūsti laiškai iš įvairių Jungtinių Amerikos Valstijų gydytojų, apibūdinantys panašius atvejus. Tarp pranešimų apie Pneumocystis jirovecii ir kitas oportunistines infekcijas homoseksualių vyrų tarpe, CDC taip pat gavo pranešimų apie retos ir neįprastai agresyvios vėžio formos Kapoši Sarkoma (angl. Kaposis sarkoma) atvejus tarp homoseksualių vyrų grupės Niujorko ir Kalifornijos miestuose, po kurių CDC įsteigė specialios paskirties darbo grupę Kapoši Sarkoma ir oportunistinių infekcijų rizikos faktoriams identifikuoti bei formuoti tokių atvejų apibrėžimą nacionalinei priežiūrai. Visuomenė buvo informuota apie homoseksualių vyrų tarpe lytiniu keliu plintantį virusą, sukeliantį imuninės sistemos nepakankamumą, ir skatinama imtis atsargumo priemonių, tačiau vėliau paaiškėjo ir kiti infekcijos perdavimo būdai. Nauju virusu užsikrėtė daug švirkščiamuosius narkotikus vartojančių narkomanų, todėl konstatuota, jog virusas plinta ir per kraują m. CDC pranešė apie pirmą imunodeficito atvejį po kraujo perpylimo. Per keletą metų tūkstančiai hemofilija sergančių žmonių užsikrėtė virusu kraujo perpylimo metu m. CDC pranešė apie dvi tokį imunodeficitą turinčias moteris: vienos partneris buvo biseksualus, kitos vartojo švirkščiamuosius narkotikus. [1, 2] Sutelkus dėmesį į infekcijos sukėlėjo paieškas, galiausiai 1983 m. dvi atskiros mokslininkų grupės, vadovaujamos R. Gallo (JAV) ir L. Montagnier (Prancūzija) tuo pačiu metu paskelbė atradę naują retrovirusą, kuris galimai lemia imunodeficito būklę. R. Gallo teigimu, naujas, iš AIDS sergančių pacientų išskirtas virusas, esą neįtikėtinai panašus į jo ankstesniuose tyrimuose, ieškant žmogaus leukozės sukėlėjo, išskirtą žmogaus T ląstelių limfotropinio viruso I ir II tipą. Jis manė, kad naujas virusas yra HTLV-I ir HTLV-II padermė ir pavadino jį HTLV-III. L. Montagnier ir jo mokslininkų grupė taip pat išskyrė šį naują virusą iš pacientų, turinčių klasikinius imunodeficito 7
8 simptomus. Jie įrodė, jog viruso šerdiniai baltymai imunologiškai skiriasi nuo kolegos atrastų HTLV baltymų ir pavadino jį limfadenopatiją sukeliančiu virusu. Nors tarp mokslininkų kilo ginčų, buvo nustatyta, jog rasti virusai yra identiški m. Virusologijos nomenklatūros komisija suteikė virusui Žmogaus imunodeficito viruso pavadinimą, o jo sukeliamą imunodeficitą pavadino AIDS. [2] Radus ligos sukėlėją, kilo daug klausimų apie viruso atsiradimą. Vieni manė, jog virusas atsirado stebuklingai, kaip bausmė nuo moralės normų nukrypusiems žmonėms, kiti jog virusas buvo kažkieno sukurtas genetinės modifikacijos pagalba. Tik neseniai atlikti genetiniai tyrimai parodė, kad viruso formavimosi raida buvo kur kas sudėtingesnė. Išanalizavus ŽIV genomą pastebėta, kad genų išsidėstymas yra labai panašus į kito retroviruso, kuris buvo išskirtas iš Centrinės Afrikos šimpanzių (Pan troglodytes) ir Cercocebus atys beždžionių. Tai Šimpanzių imunodeficito virusas ir Cercocebus atys beždžionių imunodeficito virusas, sukeliantis imuniteto nepakankamumo sindromą, panašų kaip AIDS žmonėms. Istoriniuose šaltiniuose minima, jog Centrinės Afrikos šiaurinėje dalyje šimpanzės buvo medžiojamos maistui, taigi yra didelė tikimybė, kad virusas per kraują pateko į medžiotojų organizmą. SIV evoliucija yra ypatingai greita dėl jo reprodukcijos būdo, kurio metu atvirkštinės transkriptazės pagalba virusas savo genetinę medžiagą įterpia į šeimininko genomą ir dauginasi kartu su infekuota ląstele. Tokio dauginimosi metu mutacijų dažnis yra didelis, taigi virusas gali greičiau prisitaikyti prie pakitusios aplinkos, ko pasekoje, galėjo tapti patogenišku ir žmogui. [3, 4] Arizonos universiteto mokslininkai, vedami M. Worobey (2009), ėmėsi nagrinėti viruso evoliucijos eigą. Jų nuomone, ŽIV ir visi kiti patogenai yra kintamos struktūros organizmai, sukeliantys infekcijas. Tai per ilgą laikotarpį evoliucijos eigoje susiformavę organizmai iš jų pirmtakinių populiacijų. Atsižvelgdami į turimus duomenis apie virusų genomų panašumą, jie iškėlė hipotezę, jog ŽIV-1 evoliucionavo iš SIVcpz, o ŽIV-2 iš SIVsm. Surinkus pavyzdžius ir atlikus tyrimą buvo pateiktas maksimaliai tikėtinas filogenetinis SIV/ŽIV env lokusų medis, atspindintis viruso evoliuciją. Rasta faktų, įrodančių, jog SIVcpz ir SIVsm virusai yra padermė, kilusi iš beždžionių imunodeficito viruso, egzistavusio dar prieš tūkstančius ar net dešimtis tūkstančių metų tai pradinė filogenetinio medžio šaka, pažymėta SIVcol. [3] 8
9 1 pav. Filogenetinis medis, nurodantis SIV evoliuciją į ŽIV, sudarytas remiantis env lokusu. SIVsm/HIV-2 giminystės linijos pavaizduotos žalia spalva, o artimiausi protėviai žalia žvaigžde. SIVcpz/HIV-1 giminystės linijos yra raudonos spalvos, o jų artimiausi protėviai pažymėti raudona žvaigžde. Visos kitos SIV giminystės linijos pavaizduotos mėlynai. Mėlynos žvaigždutės šakų susikirtimo vietose žymi sekų sutapimą didesnį kaip 80 %. [3] Sekant viruso vystymosi eigą, buvo rasta duomenų ir apie ankstesnes viruso nusineštas žmonių gyvybes. Virusas buvo aptiktas kraujo mėginyje, kuris nuo 1959 m. buvo saugomas Kongo Respublikos sostinės Kinšasos ligoninėje. Tai įrodė, kad virusas egzistavo dešimtmečius, kol galiausiai buvo atpažintas 1980 m. Ilgalaikį viruso egzistavimą taip pat įrodė 2008 m. Arizonos universitete M. Worobey atliktas tyrimas, kurio metu ŽIV RNR fragmentai buvo išskirti iš limfmazgio bioptato, saugomo nuo 1960 m. toje pačioje ligoninėje m. buvo užfiksuoti dar keli ligos atvejai, kol galiausiai 1980 m. prasidėjus tarptautinėm kelionėm, virusas išplito po JAV, Europą ir kitas pasaulio šalis. [5] 9
10 Pasaulinės sveikatos organizacijos duomenimis, beveik visose pasaulio šalyse yra užregistruota bent po vieną ŽIV infekcijos ar AIDS atvejį tai pirma ir vienintelė pandemija. Pasaulio istorijoje užkrečiamųjų ligų epidemijos nusinešdavo daugybę gyvybių, bet jos būdavo daugiau ar mažiau lokalizuotos, jų metu pasitaikydavo savaiminių pasveikimo atvejų. ŽIV infekcija apėmė visus kontinentus ir šalis, per visą laikotarpį nuo 1980 m. neįregistruotas nei vienas savaiminio pasveikimo atvejis. Pasaulyje šiuo metu yra mln. užsikrėtusiųjų, iš kurių apie pusę sudaro moterys. Maždaug 90 % infekuotų asmenų sudaro ekonomiškai silpnų šalių gyventojai, kadangi jose klesti skurdas, prasta sveikatos apsaugos sistema, riboti ligos prevencijos šaltiniai. Kiekvienais metais nuo šios infekcijos ir jos pasekmių miršta apie 3 mln. žmonių. Nuo 1981 m., kai buvo diagnozuotas pirmasis AIDS atvejis, iki 2010 m. jau mirė 30 mln. žmonių. [6, 7] Labai sparčiai ŽIV infekcija plinta Afrikos žemyne, kur pagrindinis užsikrėtimo kelias heteroseksualinis. Infekuoti šio žemyno gyventojai sudaro 2/3 viso pasaulio užsikrėtusiųjų. Kai kuriose Pietų Afrikos šalyse užsikrėtusiųjų yra iki % gyventojų. Kitas žemynas, kuriame sparčiai plinta infekcija, Azija. Čia vyraujantys viruso perdavimo būdai yra švirkščiamųjų narkotikų vartojimas ir komercinės seksualinės paslaugos. Staigus ir greitas plitimas Azijoje, epidemiologų nuomone, gali baigtis tuo, kad šiame žemyne užsikrėtusiųjų bus apie 25 %. Lotynų Amerikoje ir Karibų baseine vyraujantys užsikrėtimo būdai yra švirkščiamųjų narkotikų vartojimas ir homoseksualūs santykiai. [8] Iš Vakarų Europos šalių daugiausiai užsikrėtusiųjų yra Prancūzijoje, Italijoje ir Ispanijoje. Šiame regione vyraujantis užsikrėtimo būdas yra nesaugūs lytiniai santykiai. Centrinėje Europoje infekcija iš pradžių plito iš lėto (išskyrus Rumuniją) ir gerokai greičiau pradėjo plisti nuo m. Plitimo greitį paskatino švirkščiamųjų narkotikų vartojimas. Rytų Europoje ŽIV epidemijos šuolis stebimas m. Nuo 2000 m. aiškus epidemijos pagreitis stebimas Estijoje. Didelis užsikrėtusiųjų skaičius užregistruotas Latvijoje, Baltarusijoje, Rusijoje, ypač Kaliningrado, Peterburgo ir Maskvos regionuose, Ukrainoje. Pagrindinis užsikrėtimo būdas švirkščiamųjų narkotikų vartojimas (70-80 %), vidutinis užsikrėtusiųjų amžius metų. [8] Pirmas įvežtinis viruso atvejis Lietuvoje užfiksuotas 1989 m., kai į Kauno klinikas dėl sunkios sveikatos būklės kreipėsi jūreivis iš Klaipėdos. Įtarus, kad jis gali būti infekuotas ŽIV, paciento kraujas buvo nuvežtas į virusologijos laboratoriją Maskvoje, kur galutinai patvirtinta diagnozė. [9] m. Lietuvoje ŽIV infekcija pradėjo plisti tarp homoseksualių vyrų. Manoma, kad šie vyrai infekciją atsivežė iš svetimų šalių, kur dirbo ar kurį laiką gyveno. Lietuvos AIDS centro epidemiologinio tyrimo duomenimis, ŽIV infekcija tarp Lietuvos vyrų homoseksualų plinta 10
11 jau nuo m. Vėliau, m. viruso paplitimas buvo stebimas tolimųjų plaukiojimų jūreivių tarpe. Perdavimo būdas heteroseksualiniai santykiai, manoma, kad jūreiviai užsikrėtė naudodamiesi komercinio sekso paslaugomis Afrikos, Azijos ir Rusijos uostuose m. Lietuvoje pirmą kartą diagnozuotas ŽIV švirkščiamuosius narkotikus vartojančiam asmeniui (užsikrėtė Lenkijoje). Šioje rizikos grupėje infekcija Lietuvoje pradėjo sparčiai plisti, kol galiausiai m. tapo vyraujančiu infekcijos perdavimo būdu. [6] 2002 m. buvo užfiksuotas ŽIV protrūkis Alytaus griežtojo rėžimo pataisos kolonijoje, kur iš 2000 tiriamų nuteistųjų kraujo mėginių, buvo gauti 207 teigiami ŽIV rezultatai. Po mėnesio pakartotinai ištyrus kalinius, kuriems nebuvo diagnozuota ŽIV, paaiškėjo, jog iš 1813 mėginių nustatyti dar 78 teigiami rezultatai. Dar kartą po trijų mėnesių ištyrus 1481 neigiamus mėginius, buvo aptikta 15 naujų ŽIV atvejų. Ekspertų vertinimu, viena pagrindinių ŽIV plitimo Alytaus kolonijoje priežasčių buvo švirkščiamųjų narkotikų vartojimas, švirkštų ir adatų dalijimasis. To neneigė ir tuo metu apklausti kaliniai. [10] 2 pav. ŽIV ir AIDS atvejų skaičius Lietuvoje m. [11] 1.2 Retrovirusų bendra charakteristika Retrovirusai tai sferiniai, nm skersmens virusai, sudaryti iš ribonukleino rūgšties, apgaubtos kapside, ir paviršiaus darinio apvalkalo, sudaryto iš lipoproteinų ir glikoproteinų. Retrovirusai priskiriami Retroviridae šeimai, kurią sudaro trys pošeimiai: Oncovirinae (onkogeninių retrovirusų), kuriam priklauso HTLV-1 ir HTLV-2, Lentivirinae (neonkogeninių 11
12 retrovirusų), kuriam priklauso ŽIV virusas, ir Spumavirinae, kurį sudaro žmonėms nepatogeniški spumavirusai, sukeliantys ląstelių vakuolizaciją. [7] Retroviruso virionas turi dvi identiškas viengrandes RNR molekules, kurių ilgis svyruoja nuo 7 iki 10 kilobazių. Pagrindinės genomo sudedamosios dalys yra: grupei specifinius antigenus, polimerazę ir apvalkalą koduojantys genai. gag genas koduoja šerdinius ir struktūrinius baltymus, pol atvirkštinės transkriptazės, proteazės ir integrazės fermentų baltymus, env retrovirusų išorinio sluoksnio baltymus. Dvejose ypatingose viruso genomo srityse yra šeši papildomi genai, vadinami tat, rev, vif, vpr, vpu, ir nef. Jie reguliuoja viruso baltymų gamybą ir viruso dauginimąsi ląstelėse taikiniuose. [7] Abiejų viruso nukleokapside esančių vienagrandžių RNR molekulių 5` gale yra kepurė tai pirmasis RNR molekulę koduojantis nukleotidų subvienetas. RNR genomas sudarytas iš koduojančių ir nekoduojančių regionų. Koduojantys regionai atsakingi už baltymus, dalyvaujančius genų ekspresijoje, o nekoduojantys regionai svarbūs RNR replikacijoje. 5` galas turi tris regionus: R, U5 ir PBS. R regionas tai trumpos pasikartojančios sekos, aptinkamos abiejuose RNR genomo galuose, jos reguliuoja RNR transkripcijos iniciaciją ir poliadenilinimą. Daugumoje retrovirusų R regionas turi poliadenilinimo signalinę seką (AAUAAA). U5 regionas yra įsiterpęs tarp R ir PBS regionų, RNR genome jis yra unikalus. PBS tai dažniausiai 18 nukleotidų ilgio regionas, prasidedantis 5`TGG kodonu. Jis komplementarus trnr sekos 3` galui. PBS regionas yra trnr prisijungimo vieta, kuri funkcionuoja kaip pradmuo AT inicijuojant virusinės minus (-) DNR grandinės sintezę. Retroviruso RNR 3` gale taip pat yra 3 regionai: PPT, U3 ir R. PPT regionas yra purinais turtinga seka, sudaryta iš 7 18 nukleotidų. Jis lokalizuotas tiesiai prieš (5`) U3, kuris atvirkštinės transkripcijos metu suskyla ir prie jo prisijungia RNR pradmuo, sužadinantis DNR plius (+) grandinės sintėzę. U3 regionas sudarytas iš kelių šimtų (~ ) nukleotidų, įsiterpusių tarp PPT ir R regionų, tai unikali RNR seka. U3 regionas turi promotoriaus/enhanserio seką, kontroliuojančią virusinės RNR transkripciją nuo 5` galo. R galinės pasikartojančios sekos. RNR molekulė 3` gale turi Poli(A) uodegą tai homopolimeras, sudarytas iš adenilinės rūgšties liekanų. Poly(A) uodega viruso genomo nekoduoja, ji prisitvirtina pasibaigus transkripcijai ir suteikia molekulei stabilumo. gag, pol ir env genus koduojančios sekos įsiterpusios genomo viduryje. [12] 12
13 3. Retroviruso RNR genomo struktūra [13] Kad įvyktų sėkminga viruso replikacija, viengrandė RNR turi būti paverčiama dvigrande DNR molekule, kitu atveju ji negalės įsiterpti į ląstelės taikinio genomą. Šis procesas vyksta infekuotos ląstelės citozilyje ir susideda iš kelių etapų: 1. Retrovirusams specifinė ląstelinė trnr, veikdama kaip pradmuo, hibridizuojasi prie komplementarių viruso genomo sekų, vadinamų PBS; 2. DNR segmentas sintezuojamas nuo trnr pagal retroviruso genominės RNR seką; 3. Viruso R ir U5 regiono sekos 5` gale pašalinamos veikiant AT fermentui, vadinamam RNRaze H; 4. Naujai susidaręs pradmuo peršoka į viruso genomo 3` galą ir prisijungia prie jam komplementaraus RNR R regiono; 5. Prasideda DNR grandinės sintezė nuo 3` galo; 6. Nuo primos susintezuotos komplementarios DNR grandinės RNRazė H pašalina didžiąją dalį viruso RNR; 7. Antra DNR grandinė sintezuojama nuo virusinės RNR 5` 3` kryptimi; 8. Virusinės RNR likutis ir abi trnr molekulės pašalinamos paveikiant RNRaze H; 9. Antros DNR grandinės PBS regionas prisijungia prie pirmos DNR grandinės PBS regiono, jie yra komplementarūs tarpusavyje; 10. Susintetinama dvigrandė DNR, kuri yra pasiruošusi integruotis į ląstelės taikinio genomą. Tai atlikti padeda fermentas integrazė. [14] Procesas schematiškai pavaizduotas 4 paveiksle. 13
14 4 pav. Atvirkštinės transkripcijos mechanizmas [14] Visas šis procesas katalizuojamas AT, kuri atlieka DNR polimerazės ir RNazės H funkcijas. Retroviruso reprodukcijos ciklas. Virusas absorbuojasi prie ląstelės taikinio ir, tirpdydamas jos membraną, ten įterpia savo apvalkalą. Viruso genomui patekus į ląstelės citozolį, AT pradeda sintetinti minus (-) DNR nuo RNR. Plius (+) DNR grandinė perrašoma nuo minus (-) 14
15 DNR ir susidaro dvigrandė DNR molekulė. Toliau dvigrandė DNR pernešama į ląstelės branduolį, kur fermento integrazės pagalba yra įterpiama į ląstelės šeimininkės DNR. RNR polimerazė transkribuoja susidariusią DNR į plius (+) RNR, kuri naudojama palikuonių genomams sudaryti. Dalis plius (+) RNR transliuojama į poliproteinus, kurie vėliau suskaidomi į struktūrinius baltymus ir fermentus, kita dalis suskaidoma į trumpas informacinės RNR grandis, koduojančias apvalkalo reguliacinius ir kt. baltymus. Palikuonys iš ląstelės pasišalina pumpuruodami. Reprodukcijos ciklas vaizdžiai pateiktas 5 pav. [15] 5 pav. Retroviruso reprodukcijos ciklas [16] 1.3 ŽIV viruso struktūra ŽIV tai sferinės formos, 1/10,000 milimetrų diametro virusas, iš išorės apgaubtas dvigubu lipidų molekulių sluoksniu. Apvalkalą virusas pasisavina iš infekuotos ląstelės membranos, naujai susiformavusių viruso dalelių pumpuravimo metu. Į apvalkalą yra įsiterpę vidutiniškai 72 ŽIV env baltymų molekulės, kurios išsikiša arba kaip smaigas persmeigia viriono membraną. env sudaryta iš kepurės, kuri susideda iš trijų glikoproteino 120 molekulių, ir stiebo, savo sudėtyje turinčio tris glikoproteino 41 molekules. Baltymas gp41 persmeigia viruso apvalkalą ir veikia kaip atrama šios struktūros palaikyme. [17] Apvalkalo viduje yra kapsidė sudaryta iš 2000 p24 baltymų molekulių. Kapsidė apgaubia dvi viengrandes ŽIV RNR molekules, kurių kiekviena turi pilną viruso genų kopijų skaičių. ŽIV 15
16 turi tris pagrindines genomo sudedamąsias dalis (gag, pol ir env), saugančias informaciją apie viruso dalelių gamybai reikalingų struktūrinių baltymų ir fermentų sintezę. env genas koduoja paviršinius viruso baltymus, pvz. gp160, kuris paveiktas viruso fermentų suskaidomas į gp120 ir gp41 (env baltymų komponentus). Baltymai gp120 ir gp41 prisijungia prie ląstelės taikinio membranos paviršinių CD4 receptorių, taip padėdami virusui prasiskverbti ir infekuoti ląstelę virusine RNR. Kadangi viruso apvalkalo paviršiuje šių baltymų formuojami išsikišimai yra gausiai padengti angliavandeniais, juos sunkiai atpažįsta antikūnai. [17] Kiti viruso struktūriniai baltymai, koduojami gag geno, sudaro matricos, kapsidės ir nukleokapsidės baltymus. Kapsidės baltymas p24 formuoja kūgio formos dangalą aplink virusinę RNR, kuris infekcijos metu transportuoja RNR į ląstelės vidų. Šis dangalas suformuotas iš stabilių heksamerų, kurie išsidėsto kaip plytų siena formuodami vientisą kapsidę. Tuo tarpu nukleokapsidės baltymas suformuoja stabilų kompleksą su virusine RNR ir ją apsaugo. Viruso membranos vidinėje pusėje, t.y. tarp viruso šerdies ir apvalkalo, matricos baltymas p17 formuoja dangalą, kuris atlieka pagrindinį vaidmenį naujiems virusams pumpuruojant infekuotoje ląstelėje. Šie baltymai įgavę trimerinę formą jungiasi su membrana. [17, 18] ŽIV pol lokusas koduoja tris pagrindinius viruso replikacijai būtinus fermentus AT, integrazę ir proteazę, kurie yra viruso nukleokapsidėje. AT atsakinga už DNR kopijų sintezę virusinės RNR pagrindu. Ši struktūra pradžioje susintetina dvigrandę DNR RNR molekulę, nuo kurios pašalinusi RNR dalį galutinai užbaigia dvigrandės DNR spiralės sintezę. Tuomet fermentas integrazė įterpia viruso DNR į infekuotos ląstelės genomą, kur dauginama viruso genetinė medžiaga arba virusas gali egzistuoti nepastebimas dešimtmečius, dėl šios priežasties yra nepaprastai sunku su juo kovoti. Fermentas proteazė yra labai svarbus ŽIV dalelių brandinimui. Virusas gamina baltymus ilgų poliproteinų pavidalu, kurie vėliau turi būti suskaidomi į smulkesnes, tam tikras funkcijas atliekančias struktūra, tai atlieka proteazė. [18] ŽIV turi šešis reguliacinius genus (tat, rev, nef, vif, vpr ir vpu), kuriuose užkoduota informacija reikalinga baltymų, atsakingų už viruso gebą infekuoti ląstelę taikinį, sintetinančių naujas viruso kopijas ar sukeliančių ligą, sintezei. nef (neigiamo reguliavimo faktorius) geno koduojami baltymai infekuotoje ląstelėje sustabdo daugumos baltymų atsakingų už ląstelės gynybinius procesus sintezę, jis svarbus ŽIV efektyviam dauginimuisi ir infekcijos progresavimui į AIDS. vpu (virusinis baltymas U) genas koduoja baltymus, kurie padeda viruso dalelėms pasišalinti iš ląstelės pumpuravimo metu, sumažindami sąveiką tarp naujai susiformavusių apvalkalo baltymų ir ląstelės receptorių. Jis taip pat formuoja jonų kanalą viruso membranoje. Genas vif koduoja viruso užkrečiamumo baltymą. Jis atakuoja vieną iš ląstelės gynybinių baltymų (APOBEC3G), 16
17 sukeldamas ląstelės antivirusinio poveikio inaktyvaciją. Vpr (virusinis baltymas r) nukreipia viruso genomą į branduolį po ląstelės infekavimo. Baltymas P6 dalyvauja vpr geno įterpime į naujai susiformavusius virusus. rev tai virionų reguliatorius. Šio geno koduojamas baltymas, prisijungęs prie virusinės RNR, reguliuoja splaisingo ir virusinės RNR transportavimo procesus. tat geno koduojamas baltymas - transkripcijos transaktyvatorius, prisijungęs prie virusinės RNR ryškiai padidina sintetinamų baltymų kiekį. [17, 18] 6 pav. ŽIV viruso struktūra. ŽIV genomas susideda iš 3 pagrindinių genų koduojančių viruso fermentinius ir struktūrinius baltymus: gag (matricos ir kapsidės baltymus), pol (polimerazės, integrazės ir proteazės fermentus) ir env (apvalkalo baltymus). [19] ŽIV virusai klasifikuojami vadovaujantis filogenetinėmis nukleotidų sekų sąsajomis. Dabartinė klasifikacija susideda iš tipų, grupių, potipių, po- potipių ir rekombinantinių formų (7 pav.). Tarpusavyje mažiausiai giminingos viruso atmainos yra suskirstytos į tipus: ŽIV-1 ir ŽIV-2. ŽIV-1 tipas yra skirstomas į grupes: M, O ir N. Dažniausiai pasitaikanti ŽIV-1 tipo M grupės infekcija dar diferencijuojama į potipius (ŽIV-1 M grupės potipiai - A, B, C, D, F, G, H, J ir K). 17
18 Potipiai A ir F papildomai klasifikuojami į po- potipius A1, A2, A3, F1 ir F2. ŽIV-2 turi du pagrindinius potipius A ir B. Kai dvi ar kelios viruso atmainos, priklausančios ŽIV-1 tipui, infekuoja vieną individą ir pakeičia viruso genetinį materialą, jie traktuojami kaip rekombinantiniai virusai. Jei rekombinantinio viruso pilnas genomas buvo perduotas trims ar daugiau asmenų, tuomet jis vadinamas cirkuliuojančia rekombinantine forma. CRF dar žymima numeriu. Nuo 2007 m. liepos, kai buvo nustatyta pirmas CRF0, iki dabar jau yra atpažinta 34 CRF formos. Rekombinantiniai virusai, kurie buvo nustatyti anksčiau, tačiau nebuvo dokumentuota tolimesnių jų perdavimo atvejų, vadinami unikaliomis rekombinantinėmis formomis. Nukleotidų sekų skirtumai gali turėti įtakos viruso biologijai ir perdavimo būdui, pacientų išgyvenamumui, taip pat, padeda paaiškinti viruso geografinį pasiskirstymą bei ŽIV infekcijos epidemiologiją. Diagnostiniu požiūriu, sekų variacijos gali turėti didelę įtaką komercinių testų, skirtų nustatyti specifiniams viruso baltymams ar peptidams, reaktyvumui ir kryžminių reakcijų susidarymui. [19] 7 pav. ŽIV viruso klasifikacija. [19] 18
19 1.4 ŽIV viruso replikacija žmogaus organizme ŽIV replikacija vyksta taip pat, kaip ir kitų retrovirusų pošeimių, skiriasi tik procesiniai baltymai ir ląstelių taikinių populiacijos. ŽIV žmogaus organizme infekuoja T limfocitus turinčius CD4 receptorius ir juose dauginasi. Svarbiausi viruso taikiniai: CD4 (T) helperiai; monocitai, makrofagai; folikulinės dendritinės ląstelės ir mikroglijos ląstelės smegenyse; fibroblastinės ląstelės; žarnų epitelio ląstelės; kraujagyslių endotelio ląstelės ląstelės atsakingos už ląstelinį imunitetą. [7] ŽIV replikacija susideda iš kelių žingsnių. Virusui artėjant prie ląstelės taikinio, pvz., CD4 + T limfocito, apvalkalo paviršiuje esantys baltymų kompleksai traukia ląstelės membranos CD4 receptorių. ŽIV apvalkalo baltymų kompleksą sudaro ekstraląstelinis gp120 ir transmembraninis gp41 glikoproteinas. Kad virusas galėtų įsiskverbti į ląstelę, jo apvalkalo glikoproteinas gp120 turi prisitvirtinti prie ląstelės CD4 receptoriaus. Prisitvirtinus prie receptoriaus pakinta gp120 struktūra ir įvyksta sąveika su chemokino koreceptoriais CCR5 ar CXCR4, taip pat ekspresuojamais ląstelės paviršiuje. Koreceptorių sąveika iššaukia gp120 komformacinius pasikeitimus, dėl to gp41 išsitiesia ir įterpia savo hidrofobines determinantes į ląstelės membraną. Po to glikoproteinas gp41 vėl susiveja, taip traukdamas ląstelę prie viruso paviršiaus, kol galiausiai įvyksta membranų susiliejimas. ŽIV kapsidė patenka į ląstelės citoplazmą kur atsiveria išlaisvindama dvi viengrandes virusines RNR ir tris viruso replikacijai būtinus fermentus: AT, integrazę ir proteazę. AT inicijuoja viruso RNR atvirkštinę transkripciją. AT turi dvi katalitines sritis tai ribonukleazės H ir polimerazės aktyvieji centrai. Polimerazės aktyviajame centre viengrandė RNR transkribuojama į dvigrandę RNR DNR spiralę, kuriai patekus į ribonukleazės H sritį RNR dalis yra atskiriama. Viengrandė DNR grįžta į polimerazės aktyvųjį centrą kur jos pagrindu baigiama sintetinti dvigrandė viruso DNR. Toliau sąveikauja fermentas integrazė, kuris kiekviename DNR spiralės 3` gale nukerpa dalį nukleotidų suformuodamas du lipnius galus. Integrazės pagalba viruso DNR transportuojama į branduolį kur yra įterpiama į ląstelės genomą. Tuomet ląstelėje sužadinama provirusinės DNR transkripcija į irnr. Šį procesą kontroliuoja tat ir rev genai. irnr migruoja iš ląstelės branduolio į citoplazmą ir yra panaudojama kaip genominė viruso RNR, taip pat statybinių viruso baltymų sintezei. Dalis susintetintų baltymų yra sukarpomi proteazės į smulkesnius šerdinius baltymus, būtinus formuojant kapsidę. Šį procesą kontroliuoja baltymo gamybą reguliuojantys genai (tat, rev ir nef). Toliau vyksta viruso dalelių surinkimas ir RNR apgaubimas apvalkalu. Taip susidaro naujos dalelės, kurios pumpuruoja ant ląstelės paviršiaus, prieš išeidamos iš jos. [7, 16] 19
20 8 pav. ŽIV replikacija CD4 ląstelėje. 1. ŽIV ir ląstelės taikinio susijungimas; 2. ŽIV RNR, AT, integrazės ir kitų virusinių baltymų patekimas į ląstelę taikinį; 3. AT pagalba formuojama virusinė DNR; 4. Virusinė DNR transportuojama į branduolį ir įterpiama į ląstelės taikinio DNR; 5. Nauja virusinė RNR panaudojama kaip genominė RNR ir kaip virusinių baltymų sintetinimo šaltinis; 6. Nauja virusinė RNR ir baltymai juda link infekuotos ląstelės membranos, formuojamos naujos, nesubrendę ŽIV formos; 7. Paveikti proteazės virusai subrandinami ir palieka infekuotą ląstelę. [16] ŽIV replikuojasi milijonus kartų per dieną, pasidauginęs ląstelėje, ją suardo ir užkrečia kitas ląsteles. Palengva organizme mažėja T(CD4) limfocitų ir makrofagų, dėl to mažėja organizmo imuninis atsakas. T ląstelės, į kurias patenka ŽIV, nebeatpažįsta antigenų, nes sutrinka jų specifinių receptorių, esančių ant ląstelės, veikla. Dalis T(CD4) limfocitų suyra, dalis jungiasi į neaktyvius 20
21 limfocitų tinklus. Nykstant CD4 receptorius turinčioms ląstelėms, mažėja ir jų sintetinamų baltymų interleukinų nuo IL1 iki IL10 skaičius, interferonų, naviko nekrozės faktoriaus kiekis, CD8 kiekis, natūraliųjų žudikų kiekis, B ląsteles ir monocitus reguliuojančių medžiagų kiekis bei aktyvumas. B limfocitai, negaudami signalo pradeda sintetinti nespecifiškus antikūnus, silpnėja natūraliųjų žudikų bei makrofagų aktyvumas. Palengva visai išnyksta imuninė reakcija į svetimus antigenus. [7] Netekę imuninio atsparumo, ŽIV užsikrėtę žmonės tampa imlūs pirmuonių ir parazitų (pneumocistų, toksoplazmų), virusų (Herpesviridae šeimai), grybelių (baltojo balkšvagrybio, kriptokokų, paprastojo pelėsio) ir mikobakterijų sukeliamoms ligoms. Jie serga tuberkulioze, odos ir gleivinių pūsleline bei kitomis ligomis. Šios ir kitos oportunistinės ligos yra žmonių, užsikrėtusių ŽIV, mirties priežastys. [7] 1.5 Žmogaus imunodeficito viruso klinika ŽIV infekcija yra liga, kuriai nebūdingi kokie nors išskirtiniai požymiai ar sindromai, kaip daugeliui kitų infekcinių ligų. Užsikrėtus šios ligos sukėlėjais, patologinis procesas pereina keletą ligos stadijų, kurioms būdinga savotiška serologinių rodiklių dinamika. Šių stadijų klinika matyti 1 lentelėje. Dažniausiai ligonį ima varginti tik 4 ligos stadijoje atsiradę limfadenopatijos požymiai, išliekantys ilgiau kaip 3 mėnesius. Vėliau atsiranda vadinamųjų su AIDS liga susijusių kompleksų, kuriems esant taip pat nėra jokių ypatingų, tik šiai ligai būdingų požymių. Mažėjant CD4 ląstelių, didėjant imuninės sistemos nepakankamumui, pradedama sirgti įvairios kilmės ligomis arba vystosi piktybiniai navikai. Pasireiškia AIDS sindromas, kurio dažnis priklauso nuo CD4 ląstelių kiekio ir nuo ŽIV RNR kopijų skaičiaus. Oportunistines infekcijas sukelia įvairūs mikroorganizmai: bakterijos, virusai, grybeliai ir pirmuonys. [8] 1 lentelė Žmogaus imunodeficito viruso sukeliama klinika [7] Ligos stadija 1. Užsikrėtimo periodas 2. Inkubacijos periodas Vidutinė trukmė 3-24 savaitės Pagrindiniai simptomai Viruso gyvybinis ciklas žmogaus organizme val. Užkrėsti kitus infekuotas žmogus gali praėjus 1-3 paroms nuo užsikrėtimo. Jokių simptomų nėra. Laboratorinių tyrimų rezultatai neigiami. 21
22 Ligos stadija 3. Ūminis ligos periodas 4. Besimptomis periodas 4.1 Išplitusi limfadenopatija 4.2 Su AIDS susijęs ligų kompleksas Vidutinė Pagrindiniai simptomai trukmė 2-6 Karščiavimas, padidėję limfiniai mazgai, gerklės, raumenų, savaitės sąnarių skausmas, odos bėrimai (panašūs į gripo ar infekcinės mononukleozės simptomus). Laboratorinių tyrimų rezultatai teigiami tik praėjus 2 savaitėms nuo karščiavimo pradžios. 5-7 metai Jokių simptomų nėra. Laboratorinių tyrimų rezultatai teigiami. Apžiūrint ligonį, nustatoma kad padidėję bent dviejų grupių limfiniai mazgai, jie lieka padidėję ilgiau kaip 3mėn. Bendrieji intoksikacijos simptomai: Be priežasties arba pasikartojantis karščiavimas (daugiau kaip 38 C), trunkantis ilgiau kaip 3 mėnesius; Be priežasties krintantis svoris, kai per 3 mėnesius prarandama 7,5 kg arba 10 % svorio; Limfadenopatija (limfinių mazgų padidėjimas); Silpnumas, negalavimas; Viduriavimas be priežasties, trunkantis ilgiau kaip 1 mėnesį (daugiau kaip 2 kartus per dieną); Stiprus prakaitavimas naktį; Nespecifinės odos ir gleivinių ligos (piodermijos, karpos, opos, aknė ir kt.). Laboratoriniai tyrimų rezultatai teigiami. 5. Stipri ŽIV infekcija - AIDS 2-3 metai Imuninės sistemos nepakankamumas ir įvairios kilmės infekcinės (oportunistinės) ligos ir (arba) piktybiniai navikai. Laboratorinių tyrimų rezultatai teigiami, prieš mirtį gali būti neigiami. 22
23 1.6 ŽIV diagnostika ŽIV infekcija yra lėtinė virusinė infekcija. Tuo pačiu metu žmogaus organizme yra laisvai cirkuliuojančių virusinių dalelių bei virusų, integruotų į ląstelių genomą. Ar virusų yra organizme galima nustatyti pagal antikūnų imuninį atsaką į viruso antigenus. Pastarųjų metų laboratorinių tyrimų duomenimis, viruso dalelės ir virusais užkrėstos ląstelės žmogaus organizme gyvuoja labai trumpai, jos greitai suyra ir užkrečia kitas ląsteles, todėl absoliutus jų skaičius labai kinta. Sukurtos metodikos, padedančios tiesiogiai nustatyti, ar virusas yra organizme arba netiesiogiai nustatyti žmogaus imuninį atsaką į virusus. [7] Visiems laboratoriniams tyrimams taikomi vienodi reikalavimai: jie turi būti jautrūs, specifiški, pigūs ir techniškai lengvai atliekami. ŽIV galima nustatyti tiesioginiais ir netiesioginiais metodais. [7] Netiesioginiai tyrimo metodai: ŽIV antikūnų nustatymas kraujo serume (ELISA); ŽIV antikūnų nustatymo patvirtinimas Western Blot testu. Tiesioginiai tyrimo metodai: p24 antigeno nustatymas; ŽIV izoliavimas ląstelių kultūroje; ŽIV nuleorūgščių išskyrimas PGR metodu; Kiekybinis ŽIV kopijų skaičiavimas; ŽIV genotipinių ir fenotipinių savybių nustatymas. Labiausiai paplitęs metodas diagnozuoti ŽIV yra antikūnų nustatymas prieš ŽIV baltymus. Šiuo metu naudojamų komercinių testų, reaguojančių su kraujo serume esančiais antikūnais prieš ŽIV, jautrumas ir specifiškumas siekia 98 %. Testai gali būti pasirenkami pagal didesnį jautrumą arba specifiškumą, priklausomai nuo to kam bus naudojami tyrimo rezultatai. Didelio jautrumo testai naudojami pirminei atrankai siekiant nustatyti visus galimai infekuotus tiriamuosius, kartais gaunant klaidingai teigiamus neinfekuotų asmenų rezultatus. Šiuo testu gauti neigiami rezultatai yra patikimi, tačiau teigiami rezultatai gali būti ir klaidingi. Priešingai, ypač specifiškas testas gali iššaukti infekuoto asmens klaidingai neigiamą rezultatą, tačiau yra patikimas gavus teigiamą. [20] Diagnostikoje naudojamų testų jautrumas ir specifiškumas turi būti ypatingai aukštas tam, kad būtų išvengiama klaidingų rezultatų, tačiau tai sunkiai pasiekiama. Dėl šios priežasties serologinis tyrimas dėl ŽIV susideda iš kelių etapų: pirma atliekamas didelio jautrumo testas 23
24 siekiant atrinkti visus galimai infekuotus tiriamuosius, po to, atrinkti ŽIV teigiami mėginiai kartojami atliekant didelio specifiškumo testus, kad būtų galutinai patvirtinami. [20] Serologiniai tyrimai, skirti nustatyti ŽIV-1/2 tipo antikūnus, ar ŽIV-1/2 antikūnus ir ŽIV-1 p24 antigeną yra klasifikuojami į pirmaeilius (kartais įvardijamus kaip atrankinius testus) ir antraeilius bei trečiaeilius (kartais įvardijamus kaip papildomus arba patvirtinamuosius testus) testus. 2 lentelė ŽIV diagnostikoje naudojami tyrimai ir jų pritaikymas [21] Diagnostikos Metodas Panaudojimas pobūdis Greitieji diagnostiniai testai Imunochromatografinis Imunofiltracijos Aptinka ŽIV-1/2 antikūnų arba ŽIV-1/2 antikūnų ir ŽIV-1 p24 antigeną. Mėginys (kapiliarinis kraujas, veninis kraujas, serumas, plazma ar seilės) lašinamas į testo įtaisą sterilia pipete. Teigiami rezultatai išryškėja spalvinio ruožo, juostos ar taško pavidalu mėginio ir kontrolės regione. Kontrolė naudojama siekiant užtikrinti sėkmingą mėginio ir reagentų įvedimą. Imunochromatografinis tyrimas gali būti vertinamas per mažiau nei 30 min., imunofiltracinis per mažiau nei 5 min. Rezultatai vertinami vizualiai. Testams nereikia specialios laboratorinės įrangos. Paprastieji testai Imunologinis Agliutinacijos Latex agliutinacijos Įrangos nereikalaujantys tyrimai, nustatantys ŽIV-1/2 antikūnus arba ŽIV-1/2 antikūnus ir ŽIV-1 p24 anteginą. Šio tipo tyrimai skirti naudoti laboratorijoje arba patalpose kur yra tiksliai matuojančių pipečių ir šaldytuvas reagentų laikymui. Tyrimams netinka kapiliarinis kraujas bei seilės, reikia atlikti flebotomiją norint tinkamai surinkti pavyzdžius. Paprastieji testai ne tokie greiti, užtrunka nuo 30 min. iki 2 val. Rezultatai vertinami vizualiai. 24
25 Diagnostikos pobūdis Imunofer - mentinė analizė Metodas Panaudojimas EIA Laboratorinis metodas, skirtas aptikti ŽIV-1/2 antikūnams arba ŽIV-1/2 antikūnams ir ŽIV-1 p24 antigenui. Didelio našumo, per diena galima atlikti daugiau nei 40 tyrimų. Tyrimas reikalauja specialios technikos ir įgudusio specialisto, gebančio teisingai atlikti procedūrą. Serologiniai tyrimai kategorizuojami pagal kartas ir klasifikuojami pagal antigenų ir/ar konjugato naudojimą. Pirmos kartos EIA testuose kaip antigenas buvo naudojami viruso lizatai. Šis tyrimas jautrus tačiau žemo specifiškumo, dažnai iššaukia klaidingai teigiamus rezultatus. Antros kartos testuose naudojami sintetiniai peptidai, kurie yra jautresni ir specifiškesni. Trečios kartos testuose naudojami rekombinantiniai baltymai ir konjugatas su ženklintais antigenais, padidinantis jautrumą ir specifiškumą. Paskutinės 4 kartos testai aptinka ir ŽIV antigeną ir ŽIV antikūnus, tai dar jautresnis testai. Papildomi tyrimai Kombinuoti greitieji, paprastieji ir EIA (linijinė imunoanalizė) Gali būti naudojami kaip antraeiliai ir trečiaeiliai testai teigiamo rezultato patvirtinimui. Linijinės imunoanalizės pagrindą sudaro rekombinantiniai baltymai ir/ar sintetiniai peptidai, reaguojantys su antikūnais prieš ŽIV-1 ir/ar ŽIV-2. Plačiai naudojama ŽIV infekcijos patvirtinimui. Linijinė imunoanalizė papildė Western blot testą daugeliu aspektų, paskirtis panaši, tačiau ji dar papildomai suteikia informacijos apie serologinį aktyvumą. 25
26 Diagnostikos pobūdis Ketvirtos kartos tyrimai, skirti atlikti išskiriančiai ar kombinuotai ŽIV-1 antigeno ir ŽIV-1/2 antikūnų analizei Metodas Kombinuotas EIA Panaudojimas Šis tyrimas įgalina nustatyti ŽIV-1 p24 antigeną ir ŽIV-1/2 antikūnus ankstyvoje ligos stadijoje, įskaitant lango periodą. Kai kurie tyrimai geba identifikuoti ar reakcija vyko su antigenu ar su antikūnais. Kai šie išskiriantieji testai yra naudojami pirmaeilėje diagnostikoje, o gauti teigiami rezultatai stebimi pakartotinai atliekant antros ir trečios eilės tyrimus nustatančius tik antikūnus, reikėtų dėmesį skirti ir antigeno reaktyvumo nustatymui panaudojant alternatyvius testus. Tai gali būti atliekama pakartotinai paimant mėginį po 14 dienų ir tiriant serokonversiją arba persiuntus mėginį ŽIV-1 p24 antigeno ištyrimui į aukštesnio lygio laboratoriją. Cirkuliuojantis p24 antigenas pranyksta ankstyvoje ŽIV stadijoje. Molekulinė technologija Polimerazės grandininė reakcija (PGR), nukleorūgščių sekomis pagrįsta amplifikacija (NASBA), zondo hibridizacijos signalo amplifikacija Molekulinė analizė gali būti naudojama kokybiškai nustatant ŽIV infekciją arba kiekybiškai, stebint infekcijos progresavimą ar jautrumą antiretrovirusiniams vaistams. Molekulinės analizės metu aptinkamos viruso nukleorūgštys t.y. RNR ar DNR. Molekuliniai metodai dažniausiai taikomi kūdikių iki 18 mėn. amžiaus diagnostikoje, kadangi serologiniams rezultatams įtakos gali turėti motinos antikūnai, pasyviai perduodami vaisiui. Daugumoje tyrimų mažiausias aptinkamas nukleorūgščių kiekis yra 50vnt/ml tai labai jautrūs ir specifiški testai. 26
27 1.7 PSO testavimo strategija ŽIV infekcijos nustatymui PSO rekomenduojama ŽIV testavimo strategija aukšto paplitimo aplinkoje, t.y. kai ŽIV paplitimas testuojamoje populiacijoje viršija 5 %. Pirmiausia, visi mėginiai turi būti testuojami taikant pirmaeilės analizės tyrimus. Nereaktyvūs mėginiai (A-1) yra interpretuojami ir pranešami tiriamajam kaip neigiami. Pirmaeiliuose tyrimuose gauti reaktyvūs mėginiai (A+1) turi būti pakartotinai atliekami antraeilės analizės testu. Reaktyvūs mėginiai, gauti pirmaeilės ir antraeilės (A+1; A+2) analizės metu, pranešami tiriamajam kaip ŽIV teigiami. Šie asmenys turi būti nukreipiami pas specialistus, kad būtu paskirtas tinkamas gydymas ir priežiūra, jei nėra galimybės šių paslaugų suteikti testavimo vietoje. Mėginiai reaktyvūs pirmaeiliuose tyrimuose, tačiau gauti neigiami antraeiliuose (A+1; A-2) turi būti kartojami naudojant tą pati mėginį (serumą ar plazmą) tokiais pat dviem tyrimo metodais. Jei naudojamas kapiliarinis kraujas iš piršto, reikia pakartotinai paimti kraujo. Tyrimų kartojimas padeda nustatyti klaidingus rezultatus, susidariusius dėl techninių nesklandumų ar klaidų, kurias iššaukė testo komponentai. Jei nauji rezultatai sutampa (A+1; A+2 arba A-1; A-2), tuomet jie interpretuojami ir pranešami tiriamiesiems atitinkamai ar yra ŽIV teigiamas ar neigiamas. Jei tyrimų rezultatai tebėra priešingi (A+1; A-2), mėginys turi būti kartojamas atliekant tyrimą trečiaeilės analizės testu. Jei trečias tyrimas nėra reaktyvus (A+1; A-2 ;A-3), rezultatas interpretuojamas ir pranešamas tiriamajam, kaip ŽIV neigiamas. Gavus teigiamą trečios eilės ŽIV testą (A+1; A-2; A+3) jis pranešamas tiriamajam, kaip ŽIV, nedavęs tikslaus rezultato. Tiriamas asmuo kviečiamas atvykti po 14 dienų ir pakartoti tyrimą. [21] 27
28 9 pav. PSO testavimo strategija ŽIV infekcijos nustatymui aukšto paplitimo aplinkoje [21] Žemo ŽIV paplitimo aplinkoje PSO testavimo strategija yra labai panaši. Skiriasi tik tuo, kad atliekant ŽIV tyrimą antros eilės testais ir gavus abu rezultatus teigiamus (A+1; A+2), norint patvirtinti diagnozę reikia papildomai atlikti trečiaeilį testą. Jei trečias testas nėra reaktyvus (A+1; A+2; A-3), jis pranešamas tiriamajam kaip ŽIV, nedavęs tikslaus rezultato, tiriamas asmuo kviečiamas atvykti po 14 dienų ir pakartoti tyrimą. Antraeiliuose tyrimuose, gavus priešingus rezultatus (A+1; A-1), atsakymas interpretuojamas kaip ŽIV neigiamas. [21] 28
29 10 pav. PSO testavimo strategija ŽIV infekcijos nustatymui žemo paplitimo aplinkoje [21] Lietuva priskiriama žemo ŽIV paplitimo aplinkai, todėl laikosi 10 pav. pavaizduotos ŽIV testavimo strategijos. Pacientą tiriant pirmą kartą iš karto atliekami tyrimai ŽIV-1 ir ŽIV-2 antikūnams nustatyti. Gavus teigiamą rezultatą, tyrimas kartojamas antraeiliais ELISA testais. Jei antras testas gaunamas neigiamas, rezultatas pranešamas tiriamajam kaip ŽIV neigiamas. Gavus abu teigiamus rezultatus, atsakymas dar turi būti pagrindžiamas papildomai atliekant tyrimą Western blot metodu. 29
30 2. TYRIMŲ METODIKOS 2.1 Imunochromatografinis ŽIV tyrimas Atlikdama tiriamąją analizę pirmaeiliams atrankiniams ŽIV tyrimams, naudojau FIRST RESPONSE HIV CARD TEST testus. FIRST RESPONSE HIV CARD TEST yra imunochromatografiniu (greituoju) tyrimo metodu pagrįstas testas, skirtas kokybiškam visų izotipų (IgG, IgM, IgA) antikūnų, specifiškų ŽIV-1, įskaitant potipį O, bei ŽIV-2 nustatymui žmogaus kraujo serume, plazmoje ar kraujyje. [22] FIRST RESPONSE HIV CARD TEST testo pagrindą sudaro nitroceliuliozinė membrana, padengta rekombinantiniais ŽIV-1 antigenais (gp41, įskaitant subtipą O ir p24) atitinkančiais testo juostelės regioną, pažymėtą 1 ir rekombinantiniais ŽIV-2 antigenais (gp36) atitinkančiais regioną - 2. Testo įtaisas yra suskirstytas į tris dalis: C, 2 ir 1, kurios atitinka Kontrolinės linijos, ŽIV-2 ir ŽIV-1 pozicijas ant testo membranos. Testo rezultatų lange neišryškėja jokia linija (įskaitant ir kontrolės) kol nėra įvedamas mėginys. Mėginiui kartu su skiedikliu chromatografiškai judant nitroceliuliozine membrana prie mėginyje esančių ŽIV antikūnų pirmiausia prisijungia rekombinantiniai ŽIV-1/2 antigenai (gp41, p24 ir gp36) konjuguoti koloidinėmis aukso dalelėmis. Susidarę konjuguoto antigeno antikūno kompleksai toliau išilgai juda nitroceliuliozine membrana prisitvirtindami atitinkamoje vietoje, imobilizuotoje ŽIV-1 ar ŽIV-2 antigenais ir formuoja matomą liniją žyminčią antigeno antikūno konjuguoto antigeno kompleksą. Kontrolinė linija išryškėja nepriklausomai nuo to ar mėginys teigiamas ar neigiamas. Kontrolinė juostelė patvirtina testo rezultatų patikimumą. [22] FIRST RESPONSE HIV CARD TEST rinkinio sudėtis FIRST RESPONSE HIV CARD TEST rinkinys sudarytas iš: Testo įtaisai su lašintuvu ir drėgmės sugerėju; Testo skiediklis (karbonato buferio druskos tirpalas, kurio sudėtyje yra baltymų ir konservantų); Naudojimosi instrukcija; Alkoholiu suvilgyti tamponai; 30
31 Sterilūs lancetai. Rinkinio sudėtyje yra visi tyrimui atlikti būtini komponentai. [22] FIRST RESPONSE HIV CARD TEST reagentų laikymas ir stabilumas FIRST RESPONSE HIV CARD TEST testo įtaisai ir skiediklis turi būti laikomi 4 30 C temperatūroje. Negalima užsaldyti testo rinkinio ar jo komponentų. Testo skiediklis, nepriklausomai nuo to ar buvo atidarytas ar ne, yra stabilus iki galiojimo laiko pabaigos, kuris yra nurodytas ant etiketės, kai yra laikomas kambario temperatūroje 4-30 C. Testo įtaisas yra jautrus drėgmei ir karščiui. Prieš atidarant folijos maišelį, kuriame jis įpakuotas, reikia, kad testo įtaisas pasiektų kambario temperatūrą. Naudoti iš karto. Nenaudoti pasibaigus galiojimo laikui. [22] Šis tyrimas nereikalauja specialios laboratorinės įrangos ar ypatingų laikymo sąlygų, todėl gali būti atliekamas tiek laboratorijose, tiek paprastose patalpose Tyrime naudojamų mėginių surinkimas ir saugojimas Kapiliarinio kraujo: su alkoholiu suvilgytu tamponu nuvalomas piršto paviršius, kur ketinama imti kraują. Suspaudus piršto galą staigiu judesiu praduriamas odos sluoksnis steriliu lancetu. Surenkama 20 µ kraujo su rinkinyje esančia vienkartine pipete. Plazmos: kraujas, dūrimo į veną metu, surenkamas į vakutainerius kurių sudėtyje yra antikoaguliantų, tokių kaip EDTA, heparinas ar natrio citratas. Vakutaineriai centrifuguojami siekiant išgauti plazmą. Serumo: kraujas, dūrimo į veną metu, surenkamas į vakutainerius, kurių sudėtyje nėra antikoaguliantų. Paimtas ėminys laikomas 30 min. vertikaliai, vėliau centrifuguojamas min apsisukimų per minutę greičiu, kad susidarytų serumas. Tyrime naudojamų mėginių saugojimas. Kraujo mėginiai gali būti naudojami iš karto arba gali būti laikomi iki 3 dienų šaldytuve 2-8 C temperatūroje. Norint mėginius išlaikyti tinkamus tyrimui ilgiau nei tris dienas, rekomenduojama užšaldyti -20 C temperatūroje. Prieš tiriant reikia atšildyti iki kambario temperatūros. Serumo ar plazmos mėginiai, kurių sudėtyje yra nuosėdų gali iššaukti klaidingus rezultatus. Tokie mėginiai visada turi būti dar kartą centrifuguojami prieš naudojimą. 31
32 2.1.4 Įspėjimai 1) Tyrimo rezultatai bus patikimi tik laikantis Geros laboratorinės praktikos taisyklių; 2) Testo įtaisas, alkoholiu suvilgyti tamponai, lancetai ir mėginių pipetė yra vienkartinio naudojimo; 3) Tyrimas turi būti atliekamas griežtai laikantis procedūros nurodymų, smulkus nukrypimas gali iššaukti klaidingus rezultatus; 4) Testą reikia atlikti naudojant rinkinyje esantį skiediklį, kiti skiedikliai ar skysčiai iššaukia klaidingus rezultatus; 5) Negalima liesti atidaryto skiediklio buteliuko paviršiaus, tai gali jį užteršti; 6) Išvengti purslų ar aerozolio susidarymo; Tyrimo procedūra 1. FIRST RESPONSE HIV CARD TEST rinkinys prieš naudojimą turi pasiekti kambario temperatūrą; 2. Testo įtaisas kartu su pipete išimamas iš įpakavimo ir padedamas ant sauso plokščio paviršiaus; 3. Lėtai įlašinama 20 µl (du lašus) kraujo arba 10 µl (vieną lašą) serumo/plazmos į mėginio duobutę (S) naudojant pipetę. Panaudotą pipetę išmesti į biopavojaus atliekų konteinerį; 4. Įlašinama 35 µl (vienas lašas) skiediklio į mėginio duobutę (S); 5. Sekamas spalvos plėtimasis ir juostelių išryškėjimas rezultatų lange; 6. Testo rezultatai interpretuojami po 5 15 min. (Po rezultato išrašymo testo įtaisas išmetamas į biopavojaus atliekų konteinerį); 7. Negalima atsakymo interpretuoti vėliau nei per 15 min. [22] Tyrimo apribojimai 1) Antikoaguliantai, tokie kaip heparinas, EDTA ar citratas neturi įtakos testo rezultatų patikimumui; 2) Hemolizuoti mėginiai gali duoti raudoną foną rezultatų lange net ir pasibaigus analizės laikui; 32
33 3) Testas kartojamas jei tyrimo metu susidaro blanki rezultatų linija, ar jei kyla kokių nors įtarimų dėl rezultato patikimumo; 4) Klaidingai neigiami rezultatai gali susidaryti mėginyje esant labai dideliam antikūnų titrui, tokiu atveju testas kartojamas panaudojus didesnį mėginio skiedimą; 5) Teigiamas rezultatas nurodo ŽIV-1 ar ŽIV-2 viruso egzistavimą, AIDS diagnozė gali būti nustatoma tik atsižvelgiant į klinikinius požymius, jei asmuo atitinka ligų kontrolės centro nustatyto AIDS atvejo apibrėžimą. 6) Imunochomatografinis tyrimo metodas negali būti vienintelis rodiklis diagnozuojant AIDS, net jeigu tiriamo kraujo mėginyje yra antikūnų prieš ŽIV-1/ŽIV-2 virusus. Neigiami rezultatai tam tikru metu negali visiškai atmesti galimybės, jog tiriamas asmuo neinfekuotas ŽIV-1 ar ŽIV-2. Dėl ŽIV-1 ir ŽIV-2 virusų genetinės struktūros panašumo teigiamame mėginyje gali išryškėti juostelės ties ŽIV-1 ir ŽIV-2 testo regionais ir nurodyti mišrią infekciją. [22] 2.2 Imunofermentinis ŽIV tyrimas Antraeilis ŽIV tyrimas yra atliekamas su GENSCREEN PLUS HIV Ag-Ab rinkiniu, skirtu ŽIV infekcijos nustatymui kraujo serume ar plazmoje, identifikuojant antikūnus prieš ŽIV-1 ir ŽIV-2, bei ŽIV-1 antigeną. GENSCREEN PLUS HIV Ag-Ab rinkinio veikimas pagrįstas imunofermentinės analizės metodu, kai reakcijos eigoje susiformuoja imuninis kompleksas, vadinamasis sumuštinis su ŽIV antigenais ir įvairiais antikūnais, susijusiais su ŽIV-1 ir ŽIV-2 virusais. Rinkinio kietoji fazė yra padengta monokloniniais antikūnais prieš p24 ŽIV-1 antigeną bei išgrynintais antigenais: gp160 rekombinantiniu baltymu su sintetiniu funkciniu konservatyviu polipeptidu, kuris yra sudarytas iš įvairių viruso sekų, esančių labai konservatyviose ŽIV-1 O grupės kamieno sekos regionuose ir peptidų, imituojančių ŽIV-2 viruso apvalkalo baltymo imunodominantinį epitopą. Konjugatas susideda iš dviejų dalių: 1 - biotinintų polikloninių antikūnų prieš ŽIV antigenus, 2 - iš avidino ir ŽIV antigenų konjuguotų su peroksidaze (gp41 ir gp36 peptidai, imituojantys ŽIV-1 ir ŽIV-2 viruso apvalkalo glikoproteininius imunodominantinius epitopus ir tuo pačiu ŽIV-1 funkciniu konservatyviu polipeptidu, kuriuo yra padengta kietoji fazė). [23] Tyrimo reakciniai etapai: 1) Konjugatas 1 (biotininti monokloniniai antikūnai prieš p24 ŽIV-1 antigeną) yra įnešamas į mikroplokštelės šulinėlius; 33
34 2) Į šulinėlius įnešami tiriamieji kraujo serumo ar plazmos mėginiai bei kontrolės; Jei ŽIV antigenų yra mėginyje, jie jungsis su monokloniniais antikūnais, imobilizuotais kietojoje fazėje, ir konjugatu 1. ŽIV-1 ir/ar ŽIV-2 antikūnai (jei yra) jungsis su antigenais, imobilizuotais kietojoje fazėje. Konjugato 1 ir mėginio įnešimas patikrinamas pagal reakcijos mišinio spalvos pokytį (reakcijos mišinio spalva pakinta iš geltonos į mėlyną). 3) Po inkubacijos 37 C temperatūroje ir plovimo į šulinėlius įnešamas konjugatas 2; Avidinas reaguoja su biotinintais Ab-Ag-Ab kompleksais. Peroksidaze žymėti išgryninti ŽIV- 1 ir ŽIV-2 antigenai savo ruožtu sąveikauja su kietojoje fazėje surištais imunoglobulinais (IgG, IgM ar IgA antikūnais). 4) Po inkubacijos C temperatūroje nesusijungęs konjugatas 2 yra išplaunamas. Po inkubacijos su substratu kambario temperatūroje (18-30 C) imuniniuose kompleksuose surištas konjugatas nustatomas pagal reakcijos mišinio spalvos pokytį. 5) Reakcija stabdoma. Absorbcija matuojama spektrofotometru 450/ nm bangose. Pagal išmatuotas absorbcijos reikšmes nustatoma ar mėginyje yra ŽIV antigenų ar antikūnų prieš ŽIV-1 ir/ar ŽIV-2. [23] GENSCREEN PLUS HIV Ag-Ab rinkinio sudėtis 6 lentelė GENSCREEN PLUS HIV Ag-Ab rinkinio sudėtis [23] ETIKETĖ REAGENTAI KIEKIAI R1 Mikroplokštelė juostelių po 8 šulinėlius, dengti antikūnais prieš p24 ŽIV1 (pelės) ir išgrynintais ŽIV1 ir ŽIV2 antigenais R2 Koncentruotas plovimo tirpalas 10 x 1 buteliukas 2 buteliukai Tris NaCl buferis ph 7.4 (100 ml) (2 x 250 ml) Konservantas: Timerosalis 0.01% R3 Neigiama kontrolė 1 buteliukas 1 buteliukas Aukšta temperatūra inaktyvuota žmogaus plazma, (1 ml) (1 ml) neigiama pagal HBs antigeną, ŽIV antigeną, anti- 34
35 ŽIV1, anti-živ2 ir anti-hcv antikūnus. Konservantas: Natrio azidas < 0.1 R4 Ribinės vertės kontrolė Aukšta temperatūra inaktyvuota žmogaus plazma, 1 buteliukas (2,5 ml) 1 buteliukas (2,5 ml) teigiama pagal ŽIV antikūnus, neigiama pagal HBs antigenus ir anti-hcv antikūnus. Konservantas: Natrio azidas < 0.1% R5 ŽIV Ag Teigiama kontrolė Išgrynintas ŽIV1 antigenas, inaktyvuotas 1 buteliukas (1 ml) 1 buteliukas (1 ml) chaotropiniu agentu, sintetiniame skiedimo tirpale. Konservantas: ProClin % R6 Konjugatas 1 Biotininti polikloniniai antikūnai prieš p24 ŽIV1 1 buteliukas (10 ml) 2 buteliukai (2 x 10 ml) (avies), spalva geltona. Konservantas: ProClin % R7a Konjugatas 2 Liofilizuoti, peroksidaze žymėti avidinas ir ŽIV1 ir 1 buteliukas (12,5 ml) 2 buteliukai (2 x 30 ml) ŽIV2 antigenai. R7b Konjugato 2 Skiedimo tirpalas Nugriebto pieno tirpalas, spalva raudona. 1 buteliukas (12,5 ml) 2 buteliukai (2 x 30 ml) Konservantas: ProClin % R8 Peroksidazės substrato buferis Citrinos rūgšties ir natrio acetato tirpalas, ph 4.0, su 1 buteliukas (60 ml) 2 buteliukai (2 x 60 ml) H2O2 (0.015%) ir DMSO (4%) R9 Chromogenas Tetrametilbenzidino tirpalas (TMB) 1 buteliukas (5 ml) 2 buteliukai (2 x 5 ml) R10 Sustabdymo tirpalas (1N sieros rūgšties tirpalas) 1 buteliukas (28 ml) 3 buteliukai (3 x 28 ml) Lipni plėvelė mikroplokštelėms
36 2.2.2 Reikalingos medžiagos bet nepateiktos rinkinyje Distiliuotas vanduo; Natrio hipochloritas (buitinis baliklis) ir natrio bikarbonatas; Automatinės, pusiau automatinės, reguliuojamo ar fiksuoto tūrio pipetės 25 µl, 75 µl, 80 µl ir 100 µl; Graduoti cilindrai 25 ml; 100 ml; 1000 ml talpos; Biologiškai pavojingų atliekų konteineris; Vandens vonelė ar mikroplokštelių inkubatorius, 37 C ± 1 C; Rankinis, pusiau automatinis ar automatinis mikroplokštelių plovimo įrenginys; Mikroplokštelių analizatorius su 450nm ir nm filtrais; Sugeriamasis popierius. [23] Reagentų paruošimas tyrimui Prieš naudojimą reagentai sušildomi iki kambario temperatūros (18-30 C). 1) Paruošti naudojimui reagentai: Reagentas 1 (R1) : Mikroplokštelė Reagentas 3 (R3) : Neigiama kontrolė Reagentas 4 (R4) : Ribinės vertės kontrolė Reagentas 5 (R5) : ŽIV Ag teigiama kontrolė Reagentas 6 (R6) : Konjugatas 1 Reagentas 10 (R10) : Sustabdymo tirpalas 2) Ruošiami reagentai: Reagentas 2 (R2) : Plovimo tirpalas (10x koncentratas) Skiedimas 1:10, su distiliuotu vandeniu (gaunamas paruoštas plovimo tirpalas). Vienai 12 juostelių plokštelei reikia paruošti 800 ml šio tirpalo. Reagentas 7a (R7a) + Reagentas 7b (R7b) : Konjugato 2 darbinis tirpalas 36
37 Atsargiai stuktelėjus liofilizuoto konjugato 2 (R7a) buteliuką į stalą, kad ant kamštelio esanti medžiaga nukristų ant buteliuko dugno. Nuo Konjugato 2 Skiedimo tirpalo (R7b) buteliuko atsargiai nuimamas kamštelis ir visas turinys supilamas į liofilizuoto konjugato 2 (R7a) buteliuką. Uždėjus kamštelį reikia palaikyti 10 minučių, kartas nuo karto atsargiai pavartant buteliuką. Reagentas 8 (R8) + Reagentas 9 (R9) : Fermentinis ryškalo tirpalas Skiedimas 1:11, chromogeną (R9) su Substrato buferiu (R8) (pvz.: 1 ml reagento R9+10 ml reagento R8). Paruoštas reagentas stabilus 6 valandas tamsoje. [23] Mėginių paėmimas ir naudojimas Kraujo ėminiai imami įprastais metodais. Tyrimui naudojami neskiesti serumo ar plazmos mėginiai (su EDTA, heparinu, citratu ar ACD koaguliantais). Serumą ir plazmą nuo leukocitų - trombocitų sluoksnio ar nuo eritrocitų masės, reikia atskirti kaip galima greičiau, kad neįvyktų hemolizė. Stipri hemolizė gali paveikti tyrimo charakteristikas. Mėginiai su matomomis plaukiojančiomis dalelėmis prieš tyrimą turi būti nuskaidrinami centrifuguojant. Fibrino dalelės ar agregatai gali sąlygoti klaidingai teigiamus arba neigiamus rezultatus. [23] Mėginius galima laikyti +2-8 C temperatūroje iki 7 dienų. Jei mėginiai bus laikomi ilgiau, juos reikia užšaldyti -20 o C temperatūroje. Plazmos mėginiai turi būti greitai (per kelias minutes) atitirpinami vandens vonelėje 40 C temperatūroje (kad neišsėstų fibrinas). Dėl ŽIV Ag nestabilumo, mėginių negalima atitirpinti aukštesnėje nei 40 o C temperatūroje. Mėginių nerekomenduojama užšaldyti - atšildyti po kelis kartus. Daugiau nei 3 kartus užšaldytų - atšildytų mėginių tyrimui naudoti nebegalima. Jei mėginiai bus transportuojami, juos reikia supakuoti pagal atitinkamas mėginių transportavimo nuorodas. Pastaba: tyrimo rezultatų neįtakoja 90 g/l albuminas, 200 mg/l bilirubinas, lipeminių mėginių 36 g/l trigliceridų ekvivalentas, hemoliziuotų mėginių hemoglobinas (iki 20 mg/l). [23] Įspėjimai Tyrimo rezultatai bus patikimi tik laikantis Geros laboratorinės praktikos taisyklių; Kruopščiai paruošti reagentus, neužteršti jų; 37
38 Tyrimo negalima atlikti tose patalpose, kur yra reaktyvių garų (rūgščių, šarmų, aldehidų garų) ar dulkių, kurie gali paveikti konjugato fermentinį aktyvumą; Naudoti tik kruopščiai išplautus ir dejonizuotu vandeniu išskalautus stiklinius indus. Rekomenduojama naudoti vienkartines priemones; Neleisti mikroplokštelei išdžiūti tarp plovimo ir reagentų paskirstymo etapų; Fermentinė reakcija yra labai jautri metalams ar metalų jonams. Todėl į įvairius tirpalus, kuriuose yra konjugato ar substrato tirpalų, negalima įmerkti jokių metalinių komponentų; Ryškalo tirpalas (substrato buferis + chromogenas) turi būti rožinės spalvos. Jei praėjus kelioms minutėms po reagento paruošimo spalva pakinta, vadinasi reagento naudoti negalima, jį reikia pakeisti kitu tirpalu. Ryškalo tirpalo paruošimui rekomenduojama naudoti plastikinius vienkartinius indus. Galima naudoti ir stiklinius laboratorinius indus, prieš tai išplautus 1 N HCl rūgštimi, išskalautus distiliuotu vandeniu ir išdžiovintus. Šis reagentas turi būti laikomas tamsoje; Šulinėlių plovimas yra kritinis procedūros žingsnis: reikia laikytis nurodyto plovimo ciklų skaičiaus, patikrinti ar visi šulinėliai yra pilnai užpildomi ir nusiurbiami. Dėl netinkamo plovimo gali būti gauti netikslūs rezultatai; Nenaudoti tų pačių priemonių konjugato ir ryškalo tirpalo paskirstymui; Negalima keisti tyrimo procedūros. [23] Tyrimo procedūra Tyrimo rezultatų patvirtinimui kiekvienoje procedūroje reikia naudoti neigiamą, ribinės vertės ir ŽIV Ag teigiamą kontroles. Būtina laikytis Geros laboratorinės praktikos taisyklių, t.y.: 1. Sudaryti mėginių paskirstymo ir identifikacijos schemą; 2. Paruošti plovimo tirpalą; 3. Paruošti konjugato 2 darbinį tirpalą; 4. Dėklą ir juosteles išimti iš apsauginio maišelio; 5. Į mikrošulinėlius medžiagas įnešti tokia tvarka (siūloma paskirstymo schema): a. Į kiekvieną šulinėlį įnešama po 25 µl konjugato 1; b. Į šulinėlį A1 įnešama 75 µl neigiamos kontrolės; c. Į šulinėlius B, C1 ir D1 įnešama po 75 µl ribinės vertės kontrolės; 38
39 d. Į šulinėlį E1 įnešama 75 µl ŽIV Ag teigiamos kontrolės; e. Į šulinėlį F1 įnešama 75 µl mėginio Nr. 1; f. Į šulinėlį G1 įnešama 75 µl mėginio Nr. 2 ir t.t.; g. Po mėginių ir kontrolių paskirstymo reakcijos mišiniai sumaišomi mažiausiai 3 kartus 75 µl tūrio pipete įtraukiant ir išleidžiant reakcijos mišinius arba sukračius mikroplokštelę. Mėginio ir konjugato 1 įnešimą į šulinėlius galima patikrinti vizualiai: įnešus mėginio, konjugatas 1 iš geltonos spalvos pasikeičia į žaliai mėlyną. 6. Mikroplokštelė uždengiama lipnia plėvele ir gerai užspaudžiant kraštus; 7. Mikroplokštelė inkubuojama vandens vonelėje arba mikroplokštelių inkubatoriuje 37 C ± 1 C temperatūroje 1 val. ± 5 min.; 8. Išėmus mikroplokštelę iš termostato, nuo jos nuimama lipni plėvelė. Iš visų šulinėlių išsiurbiamas skystis ir išmetamas į biologiškai pavojingų atliekų konteinerį. Į kiekvieną šulinėlį pilama mažiausiai po 370 µl plovimo tirpalo. Šulinėlius su plovimo tirpalu reikia palaikyti mažiausiai 30 sekundžių. Skystis nusiurbiamas. Ši procedūra kartojama dar mažiausiai 2 kartus (mažiausiai 3 plovimo ciklai); 9. Šulinėliuose likusios skysčio turi būti mažiau nei 10 µl (jei reikia, apverskite plokštelę ant sugeriamojo popieriaus ir pilnai nusausinkite); 10. Naudojant automatinį mikroplokštelių plovimo įrenginį, reikia laikytis tokios pačios plovimo procedūros; 11. Į visus šulinėlius greitai įnešama po 100 µl konjugato 2. Prieš įnešimą konjugato tirpalas gerai sumaišomas; 12. Plokštelė uždengiama nauja lipnia plėvele ir inkubuojama 30 min. kambario temperatūroje (18-30 C); 13. Nuimama lipni plėvelė, nupilamas skystis iš šulinėlių ir plaunama mažiausiai 5 kartus, kaip nurodyta anksčiau; 14. Į kiekvieną šulinėlį greitai įnešama po 80 µl šviežiai paruošto ryškalo tirpalo ir inkubuojama kambario temperatūroje (18-30 C), tamsioje vietoje 30 ± 5 min. Šios inkubacijos metu plokštelės plėvele uždengti nereikia; 15. Ta pačia tvarka ir greičiu, kokiu buvo paskirstytas substrato tirpalas, į kiekvieną šulinėlį įnešamas sustabdymo tirpalas, po 100 µl. Reakcijos mišiniai sumaišomi; 16. Atsargiai nuvalius plokštelės apačią, mažiausiai po 4 minučių po sustabdymo tirpalo įnešimo ir daugiausiai per 30 minučių nuo reakcijos sustabdymo, plokštelių analizatoriumi matuojamas reakcijos mišinių optinis tankis 450/ nm ilgio bangose. [23] 39
40 2.2.7 Rezultatų apskaičiavimas ir interpretacija ŽIV antigenas ar antikūnai prieš ŽIV-1 ir/arba ŽIV-2 nustatomi palyginus išmatuotą kiekvieno mėginio absorbciją su ribine verte. 1) Apskaičiuojamas ribinės vertės kontrolinio serumo absorbcijos vidurkis (ODR4): 2) Apskaičiuojama ribinė vertė pagal santykį: 3) Tyrimo patvirtinimas: Neigiamos kontrolės absorbcijos reikšmė turi būti 70% mažesnė už ribinę vertę: Ribinės vertės kontrolės absorbcijos vidurkis turi būti didesnis už 0.35: ŽIV Ag teigiamos kontrolės OD turi būti didesnis už 0.50: 4) Rezultatų interpretavimas Mėginiai, kurių absorbcijos reikšmės yra mažesnės už ribinės vertės reikšmę, GENSCREEN PLUS ŽIV Ag-Ab teste yra laikomi neigiamais. Rezultatai, esantys šiek tiek žemiau ribinės vertės (C.O -10% < OD < C.O), turi būti atsargiai interpretuojami (yra tikslinga atlikti dar vieną to paties mėginio testą dvejais pakartojimais). Mėginiai, kurių absorbcijos reikšmės yra lygios arba didesnės už ribinės vertės reikšmę, laikomi preliminariai teigiamais. Norint pateikti galutinę rezultatų interpretaciją, šiuos mėginius reikia dar kartą ištirti dviem pakartojimais. Jei po pakartotinio tyrimo dviejų mėginio pakartojimų absorbcijos reikšmės yra mažesnės už ribinės vertės reikšmę ir preliminarūs pradiniai rezultatai neatsikartoja, tada mėginiai GENSCREEN PLUS HIV Ag-Ab testu yra pripažįstami neigiamais. Reakcijos gali neatsikartoti dėl: nepakankamo mikroplokštelių plovimo; neigiamų mėginių užkrėtimo aukštą antikūnų titrą turinčio serumo ar plazmos; 40
41 substrato tirpalo užteršimo oksiduojančiomis medžiagomis (chloru, metalo jonais ir pan.); sustabdymo tirpalo užkrėtimo. Jei po pakartotinio tyrimo vieno iš dviejų mėginio pakartojimų absorbcijos reikšmė yra lygi arba didesnė už ribinės vertės reikšmę, pradiniai rezultatai atsikartoja, tada mėginys GENSCREEN PLUS HIV Ag-Ab testu pripažįstamas teigiamu. [23] Tyrimo apribojimai Pirmosiose infekcijos stadijose gali būti neaptiktas labai žemas antikūnų ar antigeno titras, todėl neigiami rezultatai rodo, kad su GENSCREEN ŽIV Ag-Ab testu tirtas mėginys turi nenustatomą ŽIV antigeno ar anti-živ antikūnų titrą. Tačiau tokie rezultatai neatmeta galimybės, kad ŽIV-1/ŽIV-2 infekcijos nėra. ŽIV-1 (M grupė ir O grupė) ir ŽIV-2 kintamumas neatmeta galimybės gauti klaidingai neigiamus rezultatus. Nėra serologinių tiriamųjų metodų pilnai užtikrinančių, kad ŽIV viruso nėra. Labai jautrus ELISA metodas gali duoti klaidingai teigiamus rezultatus. [23] Norint patvirtinti reakcijos specifiškumą, kiekvienas teigiamas rezultatas turi būti patvirtintas atitinkamu metodu (specifiniu ŽIV Ag testu, pvz., Genetic System ŽIV Ag EIA, neutralizacijos metodu, siekiant įrodyti, kad ŽIV Ag tikrai yra arba Western blotu, siekiant įrodyti, kad tikrai yra ŽIV antikūnai). [24] Mėginių kaitinimas gali paveikti rezultatų kokybę. Deja, kolorimetrinis mėginių ir konjugato paskirstymo patikrinimas nenurodo tikslaus mėginių ir konjugato paskirstymo tūrio. Šiuo būdu galima tik nustatyti ar mėginiai, ryškalo tirpalas ir konjugatas buvo įnešti į šulinėlius. Visa tai susiję su naudojamos sistemos tikslumu. [23] 2.3 ŽIV Western Blot tyrimas Trečios eilės patvirtinamasis ŽIV tyrimas atliekamas komerciniu BIO-RAD firmos rinkiniu NEW LAV-BLOT I. Šis rinkinys skirtas ŽIV-1 antikūnų kraujo serume ar plazmoje nustatymui, naudojant imunoblotingo metodiką tam, kad patvirtinti teigiamą anti-živ-1 atsakymą ir tiksliai nustatyti viruso antigeninį specifiškumą. [25] Rinkinio veikimo principas. Testo veikimo principas pagrįstas netiesiogine imunofermentinės analizės technologija. Visi baltymai, iš kurių yra sudarytas ŽIV virusas, kartu su 41
42 vidine anti-živ IgG kontrole, yra padengti ant nitroceliuliozinio testo strypelio. Ruožas, atsakingas už vidinę kontrolę, lokalizuotas strypelio gale ir nėra kaip nors atitinkamai pažymėtas. Jis seka po P18 baltymo reakcijos vietos. P18 - tai mažiausios molekulinės masės ŽIV baltymas, esantis ant testo strypelio, ties juo baigiama mėginio analizė. Vidinė kontrolė leidžia užtikrinti, jog reakcija vyko pagal procedūrą ir gauti rezultatai yra patikimi. [24, 25] Nitroceliulioziniai strypeliai gaminami Western Blotting būdu. Į poliakrilamido gelį įnešus inaktyvuotų ŽIV-1 baltymų ir vykdant elektroforezę, jie paskirstomi gelyje pagal molekulinę masę, t.y. tam tikros molekulinės masės baltymai redukuojasi tam tikrais atstumais gelyje. Vėliau, naudojant elektrinį lauką, jie yra perkeliami ant nitroceliuliozinės membranos pagrindo. [25] Rinkinio sudėtis 7 lentelė NEW LAV-BLOT I rinkinio sudėtis [25] Etiketė Reagentai Kiekiai R1 Nitroceliuliozės strypeliai aktyvuoti ŽIV-1 viruso baltymais 18 strypelių, trijose, po ir vidine Anti-IgG kontrole. Strypeliai patalpinti į 6 griovelius vienkartinius griovelius. suskirstytose, plokštelėse. R2 Plovimo buferis/koncentruotas 5X 1 buteliukas TRIS NaCl tirpalas, Ph 7.4 ± 2.0, 25 % pieno, 2.5 % (100 ml) TWEEN 20 ir 0.5 % chloroformo. R3 Neigiama kontrolė 1 buteliukas Žmogaus kraujo serumas neigiamas prieš ŽIV-1 ir ŽIV-2 (0.2 ml) antikūnus, <0.1 % natrio azido konservantas. R4 Teigiama kontrolė 1 buteliukas Žmogaus kraujo serumas teigiamas prieš ŽIV-1 antikūnus, (0.2 ml) inaktyvuotas karščiu, <0.1 % natrio azido konservantas. R5 Konjugatas 1 buteliukas Ožkos Anti žmogaus IgG antikūnai, sujungti su šarmine (40 ml) fosfataze TRIS/NaCl buferiniame tirpale su fetaliniu veršiuko serumu. 42
43 Etiketė Reagentai R6 Spalva ryškinantis tirpalas 5-bromo-4-chloro-3-indonyl fosfatas (BCIP) ir NitroBlue Tetrazoliu (NBT) spalvą ryškinančiame buferyje. Kiekiai 1 buteliukas (40 ml) Reikalingos medžiagos, nepateiktos rinkinyje 1. Distiliuotas arba dejonizuotas vanduo; µl, 250 µl, 500µl talpos graduotų cilindrų; 3. Graduotos 2 ml pipetės; 4. Automatinės reguliuojamos arba pusiau automatinės fiksuotos pipetės, leidžiančios išmatuoti ir lašinti 20 µl kiekį; 5. Vienkartinės pirštinės; 6. Vakuuminė pompa skysčiams su atliekų butelių; 7. Natrio hipochloritas (baliklio); 8. Skystį absorbuojantis popierius; 9. Pincetas; 10. 1, 2 ar 3 dimensijų kratytuvas; 11. Biopavojaus konteineris; 12. Apsauginiai akiniai. [25] Reagentų paruošimas tyrimui R1, R3, R4, R5 ir R6 reagentai yra paruošti naudoti. R2 reagento paruošimas: išmaišomas plovimo buferio/koncentruoto 5X buteliukas ir skiedžiamas su distiliuotu vandeniu santykiu 1:5 (pvz. 30 ml plovimo buferio ir 120 ml distiliuoto vandens) bei sumaišoma. [25] Reagentų laikymo sąlygos Reagentų rinkinys laikomas +2 8 C temperatūroje. Atidarius, visi rinkinio reagentai gali būti laikomi iki galiojimo pabaigos, kuri yra nurodyta ant pakuotės. Praskiestas skiedimo buferis/diluentas (R2) stabilus 1 mėnesį laikant +2 8 C temperatūroje. [25] 43
44 2.3.5 Įspėjimai Tyrimo rezultatai bus patikimi tik laikantis Geros laboratorinės praktikos taisyklių; Kruopščiai paruošti reagentus, neužteršti jų; Naudoti tik kruopščiai išplautus ir dejonizuotu vandeniu išskalautus stiklinius indus. Rekomenduojama naudoti vienkartines priemones; Nenaudoti tų pačių priemonių konjugato ir ryškalo tirpalo paskirstymui; Patikrinti, ar pipetės ir kita įranga veikia tinkamai; Negalima keisti tyrimo procedūros; Kontrolinis serumas turi būti tiriamas paraleliai su mėginiu kiekvienos analizės metu; Negalima leisti tyrimo juostelėms džiūti daugiau nei 10 min. iki tyrimo pradžios; Jei spalvą ryškinančiame tirpale yra suspenduotų dalelių reikia leisti joms nusistovėti prieš išpilstymą. [25] Mėginių paėmimas ir naudojimas Mėginiai surenkami ir naudojami kaip imunofermentiniame tyrime (37 p.) Tyrimo procedūra 1. Strypelių rehidratacija. Strypeliai dedami į specialias kameras ir užpilami rekonstituciniu buferiu; 2. Norimų patvirtinti mėginių ar kontrolinių serumų užnešimas į atitinkamas kameras ir inkubacija kambario temperatūroje naudojant kratiklį; 3. Jei tiriamame mėginyje yra antikūnų prieš ŽIV-1, tuomet jie prisijungia prie identiškų viruso baltymų, esančių ant strypelio; 4. Plovimas. Kiekvieną strypelį reikia plauti po du kartus naudojant rekonstitucinį buferį. Po plovimo buferis pašalinamas; 5. Po plovimo į kameras užnešama konjugato ir inkubuojama kambario temperatūroje ant kratyklės. Konjugatas prisijungia prie ŽIV-1 antikūnų, fiksuotų ant kietosios fazės; 6. Plovimo metu pašalinamas konjugato perteklius; 44
45 7. Į kameras užnešamas spalvą ryškinantis tirpalas ir inkubuojama kambario temperatūroje ant kratyklės. Šiame etape jau galima stebėti ant nitroceliuliozės strypelio susidariusių kompleksų fermentų aktyvumą; 8. Reakcija stabdoma pašalinus iš kamerų reagentų likučius ir plaunant strypelius 3 kartus distiliuotu vandeniu; 9. Strypeliai džiovinami tarp 2 sugeriančio popieriaus lapų kambario temperatūroje. [25] Vidinė anti-igg kontrolė turi būti ryškios spalvos, tai leidžia užtikrinti, jog reakcijos eigoje mėginių ir reagentų sąveika vyko pagal procedūros protokolą. Kontrolinės juostelės nebuvimas ar silpnai intensyvi jos spalva parodo, jog nebuvo laikytasi testo procedūrų ir/ar klaidingai paskirstyti mėginiai ar reagentai. [25] Susidarę anti-živ-1 ir viruso baltymų kompleksai, paveikti konjugato ir spalvą ryškinančio tirpalo, tyrimo pabaigoje išryškėja spalvotų juostelių pavidalu (mėlynos-violetinės). Juostelių išsidėstymas ant nitroceliuliozinio strypelio leidžia identifikuoti viruso baltymus pagal jų molekulinę masę. [25] 8 lentelė 11 pav. NEW LAV-BLOT I testo strypeliai [25] ŽIV baltymai ir jų paskirtis [25] Pavadinimas Genomas Baltymo paskirtis GP 160 ENV GP 110/120 ir GP 41 glikoproteinų pirmtakas GP 110/120 ENV Apvalkalo glikoproteinas P 68/66 POL Atvirkštinė transkriptazė P 55 GAG Šerdinio baltymo pirmtakas P 52/51 POL Atvirkštinė transkriptazė GP 41 ENV Transmembraninis glikoproteinas P 40 GAG Šerdinio baltymo pirmtakas P 34/31 POL Endonukleazė P 24/25 GAG Šerdinis baltymas P 18/17 GAG Šerdinis baltymas 45
46 2.3.8 Tyrimo rezultatų įvertinimas NEW LAV-BLOT I testo rezultatų interpretavimas [25] Rezultatų interpretacija Pagal pasaulio sveikatos organizacijos (PSO) kriterijus Pagal retrovirusų serologijos standartizacijos konsorciumo kriterijus Teigiamas 2 ENV ± GAG ± POL 1 ENV + (1 GAG ar 1 POL) Neapibrėžtas 1 ENV ± GAG ± POL GAG + POL GAG POL GAG + POL GAG POL ENV Neigiamas Nėra juostelių Neklasifikuotos juostelės Nėra juostelių Neklasifikuotos juostelės 9 lentelė Pastaba. Neapibrėžiamus rezultatus gali įtakoti: Serokonversija, ŽIV-2 infekcija, kryžminės reakcijos su kitais retrovirusais; Užteršimas su teigiamu kraujo serumu gali sukelti teigiamą arba neapibrėžiamą rezultatą Tyrimo apribojimai 1) ŽIV-1 (M ir O grupės) ir ŽIV-2 virusų kintamumas gali iššaukti klaidingai neigiamų rezultatų susidarymą. 2) Teigiamas rezultatas, gautas atliekant atrankinius testus, tačiau nereaktyvus atliekant patvirtinamuosius testus, gali simbolizuoti pirmą ŽIV infekcijos stadiją. Taigi, neigiamas rezultatas rodo, kad tiriamajame kraujo serume nėra ŽIV-1 antikūnų, aptinkamų atliekant NEW LAV-BLOT I tyrimą. Toks rezultatas neatmeta ŽIV-1/2 ankstyvos infekcijos galimybės ir turi būti kartojamas po kurio laiko; 3) Mėginys patvirtintas atliekant NEW LAV-BLOT I tyrimą pagal retrovirusų serologijos standartizacijos konsorciumo kriterijus, kai gaunama tik viena reaktyvi ENV juostelė, neatmeta ŽIV-2 infekcijos galimybės; 46
47 4) Neapibrėžtas tyrimo rezultatas neatmeta serokonversijos, ŽIV-2 infekcijos ar kryžminės reakcijos su kitais retrovirusais galimybės; 5) Netipiniai rezultatai, kai silpnai sureaguoja viruso apvalkalo baltymai (gp120/gp160), o reakcijos su GAG ir POL baltymais aiškios, rodo ŽIV-2 arba ŽIV-1 O grupės infekcijos galimybę ir reikalauja papildomų tyrimų. [25] 47
48 3. TIRIAMOJI DALIS 3.1 Tiriamųjų imtis Vadovaujantis K. Kardeliu (2002), mokslinio tyrimo tikslas yra gauti naujos informacijos apie nagrinėjamus procesus ir reiškinius, kad juos galėtume valdyti, prognozuoti ir praktiškai pritaikyti. [26] Tyrime dalyvavo 2252 pacientai, kuriems imunochromatografiniu tyrimo metodu buvo atlikti ŽIV tyrimai nuo iki Infekcinių ligų ir tuberkuliozės ligoninės Žvėryno stacionare nuo 2013 m. sausio 1 d. buvo vykdoma sustiprinta ŽIV testavimo greitaisiais testais programa, kurios metu atrankiniai ŽIV tyrimai buvo atlikti visiems hospitalizuotiems m. amžiaus pacientams, t.p. ambulatoriškai konsultuojamiems dėl nepatikslintos kilmės karščiavimo, bėrimo, limfadenopatijos, mononukleozinio sindromo, užsitęsusio arba besikartojančio viduriavimo, bei virusinių hepatitų. Programos tikslas įvertinti infekcinėmis ligomis sergančių pacientų galimybę nešioti ŽIV. 3.2 Tyrimo metodas Tyrimui atlikti panaudojau literatūros analizės, kraujo tyrimų atlikimo, dokumentų (ŽIV tyrimų rezultatų) analizės ir statistinių duomenų apdorojimo metodus. 3.3 Tyrimo eiga ir naudojamos priemonės Tyrimą atlikau Infekcinių ligų ir tuberkuliozės ligoninės, VšĮ Vilniaus universiteto ligoninės Santariškių klinikų filialo laboratorijoje. Tyrimui atlikti naudojau kraujo mėginius, patekusius į laboratoriją nuo 2013 m. sausio 1 d., kai buvo pradėta vykdyti sustiprinta greitųjų ŽIV testų programa, kurios metu ŽIV tyrimai buvo paskiriami visiems į Infekcinių ligų ir tuberkuliozės ligoninės Žvėryno stacionarą hospitalizuotiems m. amžiaus pacientams, t. p. ambulatoriškai konsultuojamiems dėl nepatikslintos kilmės karščiavimo, bėrimo, limfadenopatijos, mononukleozinio sindromo, užsitęsusio arba besikartojančio viduriavimo, bei virusinių hepatitų. Kraujas buvo imamas į vakuuminę kraujo ėmimo sistemą, skirtą atskirti kraujo serumą nuo kraujo forminių elementų, kartu su pradiniais laboratoriniais tyrimais, gavus žodinį paciento sutikimą. ŽIV tyrimas buvo atliekami FIRST RESPONSE HIV CARD 48
49 TEST testu, gauti teigiami rezultatai buvo tvirtinami Nacionalinėje visuomenės sveikatos priežiūros laboratorijoje pakartotinai atliekant tyrimą imunofermentiniu ir Western Blot metodu. Atrinkti pacientai, kuriems nebuvo patvirtinti teigiami ŽIV rezultatai, analizuojamos jų ligos istorijos siekiant rasti ką nors bendro tarp pasikartojančių klaidingai teigiamų rezultatų. 3.4 Imunochromatografiniu tyrimo metodu atliktų ŽIV tyrimų analizė ir apibendrinimas Imunochromatografiniu tyrimo metodu ŽIV tyrimus atlikau ILTL laboratorijoje. Tyrimus atlikau visiems pacientams, dalyvavusiems sustiprintoje ŽIV greitųjų testų programoje nuo iki Metų pabaigoje atlikau ŽIV tyrimų archyvo duomenų analizę. Atrinktus duomenis sugrupavau pagal tiriamųjų lytį, amžiaus grupes, imunochromatogafiniu tyrimo metodu gautų teigiamų ir patvirtintų bei nepatvirtintų pirminių teigiamų tyrimų rezultatų skaičių, pacientų, su gautais klaidingai teigiamais rezultatais, diagnozes. 12 paveiksle pavaizduota ILTL pacientų, kuriems ŽIV tyrimai buvo atlikti imunochromatografiniu tyrimo metodu, pasiskirstymas procentais pagal lytį 2013 m. laikotarpiu. 12 pav. Pacientų, kuriems buvo atlikti ŽIV tyrimai, pasiskirstymas procentais pagal lytį Išanalizavus 2013 metų laikotarpio ŽIV tyrimų archyvo duomenis, nustatyta, jog iš 2252 pacientų, kurių 1093 sudarė vyrai ir 1159 sudarė moterys, dalyvavusių ILTL sustiprintoje greitųjų ŽIV 49
50 tyrimų programoje, tiek vyrų, tiek moterų procentinis pasiskirstymas skyrėsi labai nežymiai. Moterų, dalyvavusių tyrime, buvo tik 2 %, arba 66 atvejais, daugiau nei vyrų. 13 paveiksle pavaizduota ILTL pacientų, kuriems imunochromatografiniu tyrimo metodu buvo atliktas ŽIV tyrimas, pasiskirstymas pagal amžiaus grupes analizuojamu laikotarpiu. 13 pav. Tiriamųjų pacientų pasiskirstymas pagal amžiaus grupes Daugiausia ILTL hospitalizuotų ar ambulatoriškai konsultuotų pacientų 2013 metais sudarė metų amžiaus asmenys. Kiek mažiau 26 % - sudarė pacientai, turintys nuo 31 iki 40 metų. Tai rodo, kad infekciniams susirgimams labiausiai neatsparūs jaunesnio amžiaus žmonės, kadangi neturi imuniteto prieš įvairius infekcijų sukėlėjus. Vyresnio amžiaus pacientai, t. y. nuo 41 iki 50 metų ir nuo 51 iki 60 metų, bendrai sudaro trečdalį tiriamųjų. Jų didesnį atsparumą infekcijoms lemia per gyvenimą įgytas imunitetas. 50
51 Vyriausieji pacientai, t.y. nuo 61 iki 70 metų ir nuo 71 iki 80 metų amžiaus sudarė tik 4% visų tiriamųjų. Mažą šių amžiaus grupių skaičių lemia tai, kad į ILTL vykdomą sustiprintą greitųjų ŽIV tyrimų programą yra įtraukti tik m. amžiaus pacientai. Šie tyrimai buvo paskirti per klaidą, nesilaikant vykdomos programos nuostatų. 14 paveiksle pavaizduotas tiriamųjų pasiskirstymas pagal amžiaus grupes ir pagal lytį analizuojamu laikotarpiu. 14 pav. Tiriamųjų pasiskirstymas pagal lytį ir amžiaus grupes Nors 10-20, 41-50, metų ir vyresnio amžiaus tiriamųjų pasiskirstymas pagal lytį yra gana panašus, tačiau metų amžiaus ir metų amžiaus grupėse daugiau yra moterų nei vyrų, o metų amžiaus grupėje daugiau vyrų nei moterų. 15 paveiksle pavaizduota imunochromatografiniu tyrimo metodu atliktų ŽIV tyrimų skaičius bei gauti rezultatai. 51
52 15 pav. Imunochromatografiniu tyrimo metodu atliktų ŽIV tyrimų skaičius ir jų rezultatai Grafike pavaizduota, jog iš imunochromatografiniu tyrimo metodu atliktų 2252 ŽIV tyrimų buvo gauti 2204 neigiami rezultatai, kurie sudarė iki 98 % visų atliktų tyrimų ir tik 2 % arba 48 tyrimai buvo gauti teigiami. Imunochromatografinis tyrimas naudojamas kaip atrankinis ŽIV testas, todėl gavus teigiamą rezultatą, pagal PSO rekomendacijas, pirmiausia tas pats mėginys turi būti kartojamas didelio specifiškumo ELISA metodu. Gavus teigiamą ELISA, ŽIV infekcija galutinai patvirtinama kokybiniu Western blot metodu pagrįstu testu. Šiuos tyrimus atlieka Nacionalinė visuomenės sveikatos priežiūros laboratorija. 16 paveiksle pavaizduota NVSPL patvirtintų ir nepatvirtintų imunochromatografiniu tyrimo metodu gautų teigiamų rezultatų skaičius ir procentinė išraiška. 16 pav. NVSPL patvirtinti teigiami rezultatai 52
CTLA-4 BLOKADA PO ALOGENINĖS KKLT Skirmantė Bušeckaitė
 CTLA-4 BLOKADA PO ALOGENINĖS KKLT Skirmantė Bušeckaitė Intro Seniai žinoma, kad žmogaus imuninė sistema turi vidinį antinavikinį veikimo mechanizmą, o pagrindinis navikų progresijos mechanizmas yra galimybė
CTLA-4 BLOKADA PO ALOGENINĖS KKLT Skirmantė Bušeckaitė Intro Seniai žinoma, kad žmogaus imuninė sistema turi vidinį antinavikinį veikimo mechanizmą, o pagrindinis navikų progresijos mechanizmas yra galimybė
Microsoft PowerPoint - Presentation1
 Danutė Povilėnaitė Reumatologijos centras Vilnius 2012-12-05 Įvadas Amiloidozės tai baltymų struktūros pokyčių ligos, kai įprastas tirpus baltymas virsta nenormaliu netirpiu fibriliniu baltymu, kuris deponuojasi
Danutė Povilėnaitė Reumatologijos centras Vilnius 2012-12-05 Įvadas Amiloidozės tai baltymų struktūros pokyčių ligos, kai įprastas tirpus baltymas virsta nenormaliu netirpiu fibriliniu baltymu, kuris deponuojasi
Microsoft Word - Molekuline biologija-06.doc
 PATVIRTINTA Biochemijos krypties jungtinės komisijos posėdyje 2006 m. lapkričio 17 d. Komisijos pirmininkė prof. dr. V. Kirvelienė Biochemijos krypties 04 P (šakos P 310, P 320) doktorantūros studijų MOLEKULINĖS
PATVIRTINTA Biochemijos krypties jungtinės komisijos posėdyje 2006 m. lapkričio 17 d. Komisijos pirmininkė prof. dr. V. Kirvelienė Biochemijos krypties 04 P (šakos P 310, P 320) doktorantūros studijų MOLEKULINĖS
2010 m. vakcinomis valdomu ligu epidemiologines situacijos apzvalga Lietuvoje
 VAKCINOMIS VALDOMŲ LIGŲ EIPIDEMIOLOGINĖS SITUACIJOS APŽVALGA LIETUVOJE 2010 metai UŽKREČIAMŲJŲ LIGŲ IR AIDS CENTRAS LIETUVOS RESPUBLIKOS SVEIKATOS APSAUGOS MINISTERIJA Vilnius 2011 Parengė Imunoprofilaktikos
VAKCINOMIS VALDOMŲ LIGŲ EIPIDEMIOLOGINĖS SITUACIJOS APŽVALGA LIETUVOJE 2010 metai UŽKREČIAMŲJŲ LIGŲ IR AIDS CENTRAS LIETUVOS RESPUBLIKOS SVEIKATOS APSAUGOS MINISTERIJA Vilnius 2011 Parengė Imunoprofilaktikos
EGZAMINO PROGRAMOS MINIMALIUS REIKALAVIMUS ILIUSTRUOJANTYS PAVYZDŽIAI Egzamino programos minimalūs reikalavimai I. METODOLOGINIAI BIOLOGIJOS KLAUSIMAI
 EGZAMINO PROGRAMOS MINIMALIUS REIKALAVIMUS ILIUSTRUOJANTYS PAVYZDŽIAI Egzamino programos minimalūs reikalavimai I. METODOLOGINIAI BIOLOGIJOS KLAUSIMAI Minimalius reikalavimus iliustruojantys pavyzdžiai
EGZAMINO PROGRAMOS MINIMALIUS REIKALAVIMUS ILIUSTRUOJANTYS PAVYZDŽIAI Egzamino programos minimalūs reikalavimai I. METODOLOGINIAI BIOLOGIJOS KLAUSIMAI Minimalius reikalavimus iliustruojantys pavyzdžiai
Maisto lipidų pernaša ir jos sutrikimai. Audinių lipoproteinlipazės. Alimentinė lipemija. Akvilė Gaupšaitė Igr.
 Maisto lipidų pernaša ir jos sutrikimai. Audinių lipoproteinlipazės. Alimentinė lipemija. Akvilė Gaupšaitė Igr. Lipidai žmogaus organizme Maisto lipidai: o 1. Daugiausia trigliceridų (TAG) ~90 % o 2. Fosfolipidai;
Maisto lipidų pernaša ir jos sutrikimai. Audinių lipoproteinlipazės. Alimentinė lipemija. Akvilė Gaupšaitė Igr. Lipidai žmogaus organizme Maisto lipidai: o 1. Daugiausia trigliceridų (TAG) ~90 % o 2. Fosfolipidai;
ALYTAUS RAJONO SAVIVALDYBĖS VISUOMENĖS SVEIKATOS BIURAS ALYTAUS RAJONO MOKSLEIVIŲ SERGAMUMAS 2015 METŲ SAUSIO- BIRŽELIO MĖNESIŲ LAIKOTARPIU Parengė: A
 ALYTAUS RAJONO SAVIVALDYBĖS VISUOMENĖS SVEIKATOS BIURAS ALYTAUS RAJONO MOKSLEIVIŲ SERGAMUMAS 2015 METŲ SAUSIO- BIRŽELIO MĖNESIŲ LAIKOTARPIU Parengė: Alytaus rajono savivaldybės Visuomenės sveikatos biuro
ALYTAUS RAJONO SAVIVALDYBĖS VISUOMENĖS SVEIKATOS BIURAS ALYTAUS RAJONO MOKSLEIVIŲ SERGAMUMAS 2015 METŲ SAUSIO- BIRŽELIO MĖNESIŲ LAIKOTARPIU Parengė: Alytaus rajono savivaldybės Visuomenės sveikatos biuro
2009 m. liepa Nevyriausybinių organizacijų ir ekspertų koalicija Galiu gyventi, Didžioji g LT 01128, Vilnius, tel , faks
 2009 m. liepa Nevyriausybinių organizacijų ir ekspertų koalicija Galiu gyventi, Didžioji g. 5-303 LT 01128, Vilnius, tel. +370 5 266 1206, faks. +370 5 268 5512, el. p.: koalicija@galiugyventi.lt, www.galiugyventi.lt
2009 m. liepa Nevyriausybinių organizacijų ir ekspertų koalicija Galiu gyventi, Didžioji g. 5-303 LT 01128, Vilnius, tel. +370 5 266 1206, faks. +370 5 268 5512, el. p.: koalicija@galiugyventi.lt, www.galiugyventi.lt
Meningokokinė infekcija klinika, diagnostika (Epideminis cerebrospinalinis meningitas) Doc. E. Broslavskis VU Infekcinių, krūtinės ligų, dermatovenero
 Meningokokinė infekcija klinika, diagnostika (Epideminis cerebrospinalinis meningitas) Doc. E. Broslavskis VU Infekcinių, krūtinės ligų, dermatovenerologijos ir alergologijos klinika 2012 gegužės 9 d.,
Meningokokinė infekcija klinika, diagnostika (Epideminis cerebrospinalinis meningitas) Doc. E. Broslavskis VU Infekcinių, krūtinės ligų, dermatovenerologijos ir alergologijos klinika 2012 gegužės 9 d.,
PowerPoint Presentation
 Užkrečiamųjų ligų grėsmės: kam turi būti pasiruošusios sveikatos priežiūros įstaigos? Prof. dr. SAULIUS ČAPLINSKAS Užkrečiamųjų ligų ir AIDS centro direktorius saulius@ulac.lt www.sauliuscaplisnkas.lt
Užkrečiamųjų ligų grėsmės: kam turi būti pasiruošusios sveikatos priežiūros įstaigos? Prof. dr. SAULIUS ČAPLINSKAS Užkrečiamųjų ligų ir AIDS centro direktorius saulius@ulac.lt www.sauliuscaplisnkas.lt
Prezentacja programu PowerPoint
 TIENS KALCIS KALCIS Kalcis yra gyvybiškai svarbus cheminis elementas, kuris palaiko tinkamą žmogaus organizmo funkcionavimą KALCIO VAIDMUO ŽMOGAUS ORGANIZME Kalcis reikalingas normaliai kaulų būklei palaikyti
TIENS KALCIS KALCIS Kalcis yra gyvybiškai svarbus cheminis elementas, kuris palaiko tinkamą žmogaus organizmo funkcionavimą KALCIO VAIDMUO ŽMOGAUS ORGANIZME Kalcis reikalingas normaliai kaulų būklei palaikyti
„PowerPoint“ pateiktis
 Klaipėdos rajono savivaldybės gyventojų sveikatos būklės rodiklių tendencijos Lietuvos nepriklausomybės atkūrimo laikotarpiu ( nuo 199 m. kovo 11 d. iki 218 m. kovo 11 d.) L. Kaveckienė Sveikatos apsaugos
Klaipėdos rajono savivaldybės gyventojų sveikatos būklės rodiklių tendencijos Lietuvos nepriklausomybės atkūrimo laikotarpiu ( nuo 199 m. kovo 11 d. iki 218 m. kovo 11 d.) L. Kaveckienė Sveikatos apsaugos
[Version 7
 VETERINARINIO VAISTO APRAŠAS 1. VETERINARINIO VAISTO PAVADINIMAS STOMORGYL 20, tabletės 2. KOKYBINĖ IR KIEKYBINĖ SUDĖTIS Vienoje tabletėje yra: veikliųjų medžiagų: spiramicino metronidazolo 1 500 000 TV,
VETERINARINIO VAISTO APRAŠAS 1. VETERINARINIO VAISTO PAVADINIMAS STOMORGYL 20, tabletės 2. KOKYBINĖ IR KIEKYBINĖ SUDĖTIS Vienoje tabletėje yra: veikliųjų medžiagų: spiramicino metronidazolo 1 500 000 TV,
Lithuanian translation of Induction of labour - Information for pregnant women, their partners and families Gimdymo sužadinimas Informacija nėščiosiom
 Lithuanian translation of Induction of labour - Information for pregnant women, their partners and families Gimdymo sužadinimas Informacija nėščiosioms, jų partneriams ir šeimoms Šiame lankstinuke rasite:
Lithuanian translation of Induction of labour - Information for pregnant women, their partners and families Gimdymo sužadinimas Informacija nėščiosioms, jų partneriams ir šeimoms Šiame lankstinuke rasite:
Ar tai galėtų būti ŽIV? Ankstyva ŽIV diagnostika
 Ar tai galėtų būti ŽIV? Ankstyva ŽIV diagnostika Padėka JUSTRI tai Jungtinėje Karalystėje įsikūrusi pelno nesiekianti organizacija, teikianti informaciją užsikrėtusiems ŽIV ir dirbančiais su pacientais,
Ar tai galėtų būti ŽIV? Ankstyva ŽIV diagnostika Padėka JUSTRI tai Jungtinėje Karalystėje įsikūrusi pelno nesiekianti organizacija, teikianti informaciją užsikrėtusiems ŽIV ir dirbančiais su pacientais,
[Version 7, 08/ 2005]
![[Version 7, 08/ 2005] [Version 7, 08/ 2005]](/thumbs/101/150317338.jpg) VETERINARINIO VAISTO APRAŠAS 1. VETERINARINIO VAISTO PAVADINIMAS QUADRICAT, gyva liofilizuota ir inaktyvuota skysta vakcina 2. KOKYBINĖ IR KIEKYBINĖ SUDĖTIS Vienoje liofilizuotos vakcinos dozėje yra: gyvų
VETERINARINIO VAISTO APRAŠAS 1. VETERINARINIO VAISTO PAVADINIMAS QUADRICAT, gyva liofilizuota ir inaktyvuota skysta vakcina 2. KOKYBINĖ IR KIEKYBINĖ SUDĖTIS Vienoje liofilizuotos vakcinos dozėje yra: gyvų
HC
 Hemoraginio cistito sukelto BK viruso po alogeninės kaulų čiulpų transplantacijos gydymas Roberta Petrauskaitė Aktualumas Daugiau kaip 80% suaugusiųjų - nustatoma serologiškai teigiamas BK virusas Latentinis
Hemoraginio cistito sukelto BK viruso po alogeninės kaulų čiulpų transplantacijos gydymas Roberta Petrauskaitė Aktualumas Daugiau kaip 80% suaugusiųjų - nustatoma serologiškai teigiamas BK virusas Latentinis
Microsoft PowerPoint - Ernesto_epidemiolog_indik-UNODC
 Narkotinių ir psichotropinių medžiag iagų vartojimo ir narkomanijos paplitimo nustatymas, informacinių sistemų plėtra Pranešėjas: ERNESTAS JASAITIS Data: 2008 m. gegužės 30 d. NACIONALINĖS NARKOTIKŲ KONTROLĖS
Narkotinių ir psichotropinių medžiag iagų vartojimo ir narkomanijos paplitimo nustatymas, informacinių sistemų plėtra Pranešėjas: ERNESTAS JASAITIS Data: 2008 m. gegužės 30 d. NACIONALINĖS NARKOTIKŲ KONTROLĖS
PATVIRTINTA Pasvalio rajono savivaldybės tarybos 2016 m. gruodžio 21 d. sprendimu Nr. T1-242 Pasvalio rajono savivaldybės Visuomenės sveikatos biuras
 PATVIRTINTA Pasvalio rajono savivaldybės tarybos 2016 m. gruodžio 21 d. sprendimu Nr. T1-242 Pasvalio rajono savivaldybės Visuomenės sveikatos biuras Savivaldybės biudžetinė įstaiga Vytauto Didžiojo a.
PATVIRTINTA Pasvalio rajono savivaldybės tarybos 2016 m. gruodžio 21 d. sprendimu Nr. T1-242 Pasvalio rajono savivaldybės Visuomenės sveikatos biuras Savivaldybės biudžetinė įstaiga Vytauto Didžiojo a.
INFORMACIJA APIE UŽKREČIAMŲJŲ LIGŲ SUKĖLĖJUS, UŽREGISTRUOTUS UŽKREČIAMŲJŲ LIGŲ IR JŲ SUKĖLĖJŲ VALSTYBĖS INFORMACINĖJE SISTEMOJE 2018 M m. gauti
 INFORMACIJA APIE UŽKREČIAMŲJŲ LIGŲ SUKĖLĖJUS, UŽREGISTRUOTUS UŽKREČIAMŲJŲ LIGŲ IR JŲ SUKĖLĖJŲ VALSTYBĖS INFORMACINĖJE SISTEMOJE 2018 M. 2018 m. gauti 6 349 Pranešimai apie užkrečiamųjų ligų sukėlėją (apskaitos
INFORMACIJA APIE UŽKREČIAMŲJŲ LIGŲ SUKĖLĖJUS, UŽREGISTRUOTUS UŽKREČIAMŲJŲ LIGŲ IR JŲ SUKĖLĖJŲ VALSTYBĖS INFORMACINĖJE SISTEMOJE 2018 M. 2018 m. gauti 6 349 Pranešimai apie užkrečiamųjų ligų sukėlėją (apskaitos
Kiekvienos įstaigos klaidingų atvejų skaičius (procentas) pagal kiekvieną specialųjį rodiklį
 2016 M. KLINIKINIO KODAVIMO STEBĖSENOS REZULTATŲ VERTINIMO ATASKAITOS priedas Kiekvienos įstaigos (procentas) pagal kiekvieną specialųjį rodiklį Respublikos lygmens ligoninė VšĮ Klaipėdos Jūrininkų ligoninė
2016 M. KLINIKINIO KODAVIMO STEBĖSENOS REZULTATŲ VERTINIMO ATASKAITOS priedas Kiekvienos įstaigos (procentas) pagal kiekvieną specialųjį rodiklį Respublikos lygmens ligoninė VšĮ Klaipėdos Jūrininkų ligoninė
VETERINARINIO VAISTO APRAŠAS 1. VETERINARINIO VAISTO PAVADINIMAS CANIGEN DHPPi/L liofilizatas ir suspensija injekcinei suspensijai ruošti šunims 2. KO
 VETERINARINIO VAISTO APRAŠAS 1. VETERINARINIO VAISTO PAVADINIMAS CANIGEN DHPPi/L liofilizatas ir suspensija injekcinei suspensijai ruošti šunims 2. KOKYBINĖ IR KIEKYBINĖ SUDĖTIS Vienoje 1 ml dozėje yra:
VETERINARINIO VAISTO APRAŠAS 1. VETERINARINIO VAISTO PAVADINIMAS CANIGEN DHPPi/L liofilizatas ir suspensija injekcinei suspensijai ruošti šunims 2. KOKYBINĖ IR KIEKYBINĖ SUDĖTIS Vienoje 1 ml dozėje yra:
VETERINARINIO VAISTO APRAŠAS
 VETERINARINIO VAISTO APRAŠAS 1. VETERINARINIO VAISTO PAVADINIMAS Colvasone 2 mg/ml, injekcinis tirpalas 2. KOKYBINĖ IR KIEKYBINĖ SUDĖTIS 1 ml yra: veikliosios medžiagos: deksametazono (natrio fosfato)
VETERINARINIO VAISTO APRAŠAS 1. VETERINARINIO VAISTO PAVADINIMAS Colvasone 2 mg/ml, injekcinis tirpalas 2. KOKYBINĖ IR KIEKYBINĖ SUDĖTIS 1 ml yra: veikliosios medžiagos: deksametazono (natrio fosfato)
Slide 1
 Ar kanabinoidų preparatai pasižymi priešvėžiniu poveikiu: įrodymais pagrįstas vertinimas Kęstutis Sužiedėlis Nacionalinis vėžio institutas Vilniaus universitetas 2019-04-01 Kababinoidų klasifikacija; Pranešimo
Ar kanabinoidų preparatai pasižymi priešvėžiniu poveikiu: įrodymais pagrįstas vertinimas Kęstutis Sužiedėlis Nacionalinis vėžio institutas Vilniaus universitetas 2019-04-01 Kababinoidų klasifikacija; Pranešimo
NAUJOVĖ Celiuliazė Beta gliukozidazė Individuali produkto koncepcija mažesniam klampumui ir geresniam substrato panaudojimui pasiekti Kitos gliukanazė
 NAUJOVĖ Celiuliazė Beta gliukozidazė Individuali produkto koncepcija mažesniam klampumui ir geresniam substrato panaudojimui pasiekti Kitos gliukanazės Ksilanazės Beta-ksilozidazė Arabinofuranozidazė Beta-galaktozidazė
NAUJOVĖ Celiuliazė Beta gliukozidazė Individuali produkto koncepcija mažesniam klampumui ir geresniam substrato panaudojimui pasiekti Kitos gliukanazės Ksilanazės Beta-ksilozidazė Arabinofuranozidazė Beta-galaktozidazė
VILNIAUS UNIVERSITETO ONKOLOGIJOS INSTITUTO VĖŽIO KONTROLĖS IR PROFILAKTIKOS CENTRAS VĖŽIO REGISTRAS Vėžys Lietuvoje 2010 metais ISSN
 VILNIAUS UNIVERSITETO ONKOLOGIJOS INSTITUTO VĖŽIO KONTROLĖS IR PROFILAKTIKOS CENTRAS VĖŽIO REGISTRAS Vėžys Lietuvoje 2010 metais ISSN 2029-6274 ISSN 2029-6274 Informacinį leidinį sudarė: Giedrė Smailytė
VILNIAUS UNIVERSITETO ONKOLOGIJOS INSTITUTO VĖŽIO KONTROLĖS IR PROFILAKTIKOS CENTRAS VĖŽIO REGISTRAS Vėžys Lietuvoje 2010 metais ISSN 2029-6274 ISSN 2029-6274 Informacinį leidinį sudarė: Giedrė Smailytė
HOT-G II
 Heparino indukuotos trombocitopenijos (HIT) diagnostikos ir gydymo algoritmas Įvertinkite klinikinę HIT tikimybę, naudojantis 4T skale Atlikite antipf4/ heparino antikūnų titro tyrimą 1:4 ir, jei pastarasis
Heparino indukuotos trombocitopenijos (HIT) diagnostikos ir gydymo algoritmas Įvertinkite klinikinę HIT tikimybę, naudojantis 4T skale Atlikite antipf4/ heparino antikūnų titro tyrimą 1:4 ir, jei pastarasis
PATVIRTINTA Pasvalio rajono savivaldybės tarybos 2017 m. gruodžio 20 d. sprendimu Nr. T1-273 Pasvalio rajono savivaldybės Visuomenės sveikatos biuras
 PATVIRTINTA Pasvalio rajono savivaldybės tarybos 2017 m. gruodžio 20 d. sprendimu Nr. T1-273 Pasvalio rajono savivaldybės Visuomenės sveikatos biuras Savivaldybės biudžetinė įstaiga Vytauto Didžiojo a.
PATVIRTINTA Pasvalio rajono savivaldybės tarybos 2017 m. gruodžio 20 d. sprendimu Nr. T1-273 Pasvalio rajono savivaldybės Visuomenės sveikatos biuras Savivaldybės biudžetinė įstaiga Vytauto Didžiojo a.
k
 KLINIKINIO KODAVIMO BIULETENIS 2016 m. balandis, Nr. 14. Šiame biuletenyje toliau aprašomi stacionare teikiamų aktyviojo gydymo ir transplantacijos paslaugų klinikinio kodavimo kokybės stebėsenos rodikliai.
KLINIKINIO KODAVIMO BIULETENIS 2016 m. balandis, Nr. 14. Šiame biuletenyje toliau aprašomi stacionare teikiamų aktyviojo gydymo ir transplantacijos paslaugų klinikinio kodavimo kokybės stebėsenos rodikliai.
PULMONOLOGIJOS NAUJIENOS 2016 / Nr ŽIDINIŲ PLAUČIUOSE STEBĖJIMO PRINCIPAI Giedrė Cincilevičiūtė VšĮ Vilniaus universiteto ligoninės Santariškių
 PULMONOLOGIJOS NAUJIENOS 2016 / Nr. 5 66 ŽIDINIŲ PLAUČIUOSE STEBĖJIMO PRINCIPAI Giedrė Cincilevičiūtė VšĮ Vilniaus universiteto ligoninės Santariškių klinikų Pulmonologijos ir alergologijos centras Nėra
PULMONOLOGIJOS NAUJIENOS 2016 / Nr. 5 66 ŽIDINIŲ PLAUČIUOSE STEBĖJIMO PRINCIPAI Giedrė Cincilevičiūtė VšĮ Vilniaus universiteto ligoninės Santariškių klinikų Pulmonologijos ir alergologijos centras Nėra
2018
 2018 NARKOTINIŲ MEDŽIAGŲ TYRIMO KLAIPĖDOS RAJONO VAIKŲ UGDYMO ĮSTAIGŲ IR ATVIRŲ JAUNIMO ERDVIŲ APLINKOSE REZULTATAI ĮVADAS Klaipėdos rajono savivaldybės tarybos patvirtintoje, Klaipėdos rajono savivaldybės
2018 NARKOTINIŲ MEDŽIAGŲ TYRIMO KLAIPĖDOS RAJONO VAIKŲ UGDYMO ĮSTAIGŲ IR ATVIRŲ JAUNIMO ERDVIŲ APLINKOSE REZULTATAI ĮVADAS Klaipėdos rajono savivaldybės tarybos patvirtintoje, Klaipėdos rajono savivaldybės
Ginčo byla Nr LIETUVOS BANKO PRIEŽIŪROS TARNYBOS FINANSINIŲ PASLAUGŲ IR RINKŲ PRIEŽIŪROS DEPARTAMENTO DIREKTORIUS SPRENDIMAS DĖL N. J. IR
 Ginčo byla Nr. 2016-00757 LIETUVOS BANKO PRIEŽIŪROS TARNYBOS FINANSINIŲ PASLAUGŲ IR RINKŲ PRIEŽIŪROS DEPARTAMENTO DIREKTORIUS SPRENDIMAS DĖL N. J. IR UAB PZU LIETUVA GYVYBĖS DRAUDIMAS GINČO NAGRINĖJIMO
Ginčo byla Nr. 2016-00757 LIETUVOS BANKO PRIEŽIŪROS TARNYBOS FINANSINIŲ PASLAUGŲ IR RINKŲ PRIEŽIŪROS DEPARTAMENTO DIREKTORIUS SPRENDIMAS DĖL N. J. IR UAB PZU LIETUVA GYVYBĖS DRAUDIMAS GINČO NAGRINĖJIMO
Senebactum PIL_Kaunas
 Pakuotės lapelis: informacija vartotojui Senebactum 100 mg/ml odos tirpalas Joduotas povidonas Atidžiai perskaitykite visą šį lapelį, prieš pradėdami vartoti šį vaistą, nes jame pateikiama Jums svarbi
Pakuotės lapelis: informacija vartotojui Senebactum 100 mg/ml odos tirpalas Joduotas povidonas Atidžiai perskaitykite visą šį lapelį, prieš pradėdami vartoti šį vaistą, nes jame pateikiama Jums svarbi
LIETUVOS SVEIKATOS MOKSLŲ UNIVERSITETAS MEDICINOS AKADEMIJA MEDICINOS FAKULTETAS LABORATORINĖS MEDICINOS BIOLOGIJA ANTROS PAKOPOS STUDIJOS Ieva Rečiūn
 LIETUVOS SVEIKATOS MOKSLŲ UNIVERSITETAS MEDICINOS AKADEMIJA MEDICINOS FAKULTETAS LABORATORINĖS MEDICINOS BIOLOGIJA ANTROS PAKOPOS STUDIJOS Ieva Rečiūnaitė ANTIKŪNŲ PRIEŠ HLA VERTINIMAS INKSTŲ RECIPIENTAMS
LIETUVOS SVEIKATOS MOKSLŲ UNIVERSITETAS MEDICINOS AKADEMIJA MEDICINOS FAKULTETAS LABORATORINĖS MEDICINOS BIOLOGIJA ANTROS PAKOPOS STUDIJOS Ieva Rečiūnaitė ANTIKŪNŲ PRIEŠ HLA VERTINIMAS INKSTŲ RECIPIENTAMS
VAIKŲ, VARTOJANČIŲ NARKOTINES IR PSICHOTROPINES MEDŽIAGAS VARTOJIMO NUSTATYMO ORGANIZAVIMAS Atmintinė ugdymo įstaigų darbuotojams ir jose dirbantiems
 VAIKŲ, VARTOJANČIŲ NARKOTINES IR PSICHOTROPINES MEDŽIAGAS VARTOJIMO NUSTATYMO ORGANIZAVIMAS Atmintinė ugdymo įstaigų darbuotojams ir jose dirbantiems visuomenės sveikatos specialistams Vilnius, 2011 Atpažinti
VAIKŲ, VARTOJANČIŲ NARKOTINES IR PSICHOTROPINES MEDŽIAGAS VARTOJIMO NUSTATYMO ORGANIZAVIMAS Atmintinė ugdymo įstaigų darbuotojams ir jose dirbantiems visuomenės sveikatos specialistams Vilnius, 2011 Atpažinti
Prezentacja programu PowerPoint
 TIENS DiCHO II kartos prietaisas vaisiams ir daržovėms valyti (ozonatorius) PROBLEMOS, KURIAS SUKELIA APLINKOS TARŠA PARAZITAI MIKROORGANIZMAI BAKTERIJOS Švieži vaisiai ir daržovės yra spalvingi ir skanūs,
TIENS DiCHO II kartos prietaisas vaisiams ir daržovėms valyti (ozonatorius) PROBLEMOS, KURIAS SUKELIA APLINKOS TARŠA PARAZITAI MIKROORGANIZMAI BAKTERIJOS Švieži vaisiai ir daržovės yra spalvingi ir skanūs,
JONIŠKIO RAJONO SAVIVALDYBĖS VISUOMENĖS SVEIKATOS BIURAS Savivaldybės biudžetinė įstaiga, Vilniaus g. 6, LT Joniškis, tel. (8 426) , faks.
 JONIŠKIO RAJONO SAVIVALDYBĖS VISUOMENĖS SVEIKATOS BIURAS Savivaldybės biudžetinė įstaiga, Vilniaus g. 6, LT-84147 Joniškis, tel. (8 426) 605 37, faks. (8 426) 605 36, el. p. joniskis.sveikata@gmail.com.
JONIŠKIO RAJONO SAVIVALDYBĖS VISUOMENĖS SVEIKATOS BIURAS Savivaldybės biudžetinė įstaiga, Vilniaus g. 6, LT-84147 Joniškis, tel. (8 426) 605 37, faks. (8 426) 605 36, el. p. joniskis.sveikata@gmail.com.
Microsoft Word Visuomenes sveikatos bukle Vilniaus rajone_galutine
 VISUOMENĖS SVEIKATOS BŪKLĖ VILNIAUS RAJONE 2014 M. VILNIUS 2015 M. TURINYS 1. ĮVADAS... 3 2. BENDROJI DALIS... 4 2.1. PAGRINDINIŲ STEBĖSENOS RODIKLIŲ SAVIVALDYBĖJE ANALIZĖ IR INTERPRETAVIMAS ( ŠVIESOFORAS
VISUOMENĖS SVEIKATOS BŪKLĖ VILNIAUS RAJONE 2014 M. VILNIUS 2015 M. TURINYS 1. ĮVADAS... 3 2. BENDROJI DALIS... 4 2.1. PAGRINDINIŲ STEBĖSENOS RODIKLIŲ SAVIVALDYBĖJE ANALIZĖ IR INTERPRETAVIMAS ( ŠVIESOFORAS
Microsoft Word - Techninis biuletenis.doc
 Techninis biuletenis CE ženklinimas: nuo 2013 m. liepos 1 d. Nauji reikalavimai Naujos atsakomybės Tas pats CE ženklinimas Mes susiduriame su didžiausiu dešimtmečio pokyčiu, kai statybos produktai yra
Techninis biuletenis CE ženklinimas: nuo 2013 m. liepos 1 d. Nauji reikalavimai Naujos atsakomybės Tas pats CE ženklinimas Mes susiduriame su didžiausiu dešimtmečio pokyčiu, kai statybos produktai yra
CPO veiklos rezultatų ir finansinės naudos VALSTYBEI vertinimo ATASKAITA
 2010 Karolis Šerpytis CPO VEIKLOS REZULTATŲ IR FINANSINĖS NAUDOS VALSTYBEI VERTINIMO ATASKAITA Centrinė perkančioji organizacija 1 TURINYS Santrauka... 2 1. CPO veiklos rezultatų vertinimas... 3 1.1. Pirkimų
2010 Karolis Šerpytis CPO VEIKLOS REZULTATŲ IR FINANSINĖS NAUDOS VALSTYBEI VERTINIMO ATASKAITA Centrinė perkančioji organizacija 1 TURINYS Santrauka... 2 1. CPO veiklos rezultatų vertinimas... 3 1.1. Pirkimų
PATVIRTINTA Valstybinės kainų ir energetikos kontrolės komisijos pirmininko 2017 m. d. įsakymu Nr. O1- VALSTYBINĖS KAINŲ IR ENERGETIKOS KONTROLĖS KOMI
 PATVIRTINTA Valstybinės kainų ir energetikos kontrolės komisijos pirmininko 2017 m. d. įsakymu Nr. O1- VALSTYBINĖS KAINŲ IR ENERGETIKOS KONTROLĖS KOMISIJOS ELEKTROS ENERGIJOS KAINŲ PALYGINIMO INFORMACINĖS
PATVIRTINTA Valstybinės kainų ir energetikos kontrolės komisijos pirmininko 2017 m. d. įsakymu Nr. O1- VALSTYBINĖS KAINŲ IR ENERGETIKOS KONTROLĖS KOMISIJOS ELEKTROS ENERGIJOS KAINŲ PALYGINIMO INFORMACINĖS
AKMENĖS RAJONO BENDROJO LAVINIMO MOKYKLŲ MOKINIŲ PROFILAKTINIŲ SVEIKATOS PATIKRINIMŲ DUOMENŲ ANALIZĖ 2016 M. Parengė: Akmenės rajono savivaldybės visu
 AKMENĖS RAJONO BENDROJO LAVINIMO MOKYKLŲ MOKINIŲ PROFILAKTINIŲ SVEIKATOS PATIKRINIMŲ DUOMENŲ ANALIZĖ 2016 M. Parengė: Akmenės rajono savivaldybės visuomenės sveikatos biuro visuomenės sveikatos stebėsenos
AKMENĖS RAJONO BENDROJO LAVINIMO MOKYKLŲ MOKINIŲ PROFILAKTINIŲ SVEIKATOS PATIKRINIMŲ DUOMENŲ ANALIZĖ 2016 M. Parengė: Akmenės rajono savivaldybės visuomenės sveikatos biuro visuomenės sveikatos stebėsenos
INFORMACINIS PRANEŠIMAS 2018 m. gegužės 30 d., Vilnius ALKOHOLIO IR TABAKO VARTOJIMAS IR PADARINIAI 2017 M m. vienam 15 metų ir vyresniam šalies
 INFORMACINIS PRANEŠIMAS 2018 m. gegužės 30 d., Vilnius ALKOHOLIO IR TABAKO VARTOJIMAS IR PADARINIAI 2017 M. 2017 m. vienam 15 metų ir vyresniam šalies gyventojui teko 12,3 litro suvartoto absoliutaus (100
INFORMACINIS PRANEŠIMAS 2018 m. gegužės 30 d., Vilnius ALKOHOLIO IR TABAKO VARTOJIMAS IR PADARINIAI 2017 M. 2017 m. vienam 15 metų ir vyresniam šalies gyventojui teko 12,3 litro suvartoto absoliutaus (100
Microsoft Word - Utenos_raj_bio_2018_7-8kl..docx
 Utenos rajono mokinių biologijos olimpiada 2018 m. balandžio 19 d. UŽDUOTYS 7-8 klasei Mokinio Vardas, Pavardė... Klasė... Mokyklos pavadinimas... Mokytojo Vardas, Pavardė... Užduotis sudaro A, B ir C
Utenos rajono mokinių biologijos olimpiada 2018 m. balandžio 19 d. UŽDUOTYS 7-8 klasei Mokinio Vardas, Pavardė... Klasė... Mokyklos pavadinimas... Mokytojo Vardas, Pavardė... Užduotis sudaro A, B ir C
Dažniausios kvėpavimo takų infekcijos
 Vytautas Kasiulevičius VU Medicinos fakultetas Vidaus ligų, šeimos medicinos ir onkologijos klinika Rinoviruso inkubacinis periodas trunka 8 12 valandų. Simptomai pasireiškia maždaug 10 12 infekcijos
Vytautas Kasiulevičius VU Medicinos fakultetas Vidaus ligų, šeimos medicinos ir onkologijos klinika Rinoviruso inkubacinis periodas trunka 8 12 valandų. Simptomai pasireiškia maždaug 10 12 infekcijos
SVEIKATOS APSAUGOS MINISTERIJOS 2018 M. EKSTREMALIŲJŲ SITUACIJŲ PREVENCIJOS PRIEMONIŲ VYKDYMAS Sveikatos apsaugos ministerijos (toliau SAM)
 SVEIKATOS APSAUGOS MINISTERIJOS 2018 M. EKSTREMALIŲJŲ SITUACIJŲ PREVENCIJOS PRIEMONIŲ VYKDYMAS Sveikatos apsaugos ministerijos (toliau SAM) 2018 2020 metų ekstremaliųjų situacijų prevencijos priemonių
SVEIKATOS APSAUGOS MINISTERIJOS 2018 M. EKSTREMALIŲJŲ SITUACIJŲ PREVENCIJOS PRIEMONIŲ VYKDYMAS Sveikatos apsaugos ministerijos (toliau SAM) 2018 2020 metų ekstremaliųjų situacijų prevencijos priemonių
HOT-G II
 Hodžkino limfomos (HD) Klasifikatoriai Hodžkino limfomų klasifikatorius Nodulinė dominuojančių limfocitų Hodgkin limfoma WHO: 96593, TLK-10: C81.0 Klasikinė Hodgkin limfoma WHO: 96503, TLK-10: C81.9 Nodulinės
Hodžkino limfomos (HD) Klasifikatoriai Hodžkino limfomų klasifikatorius Nodulinė dominuojančių limfocitų Hodgkin limfoma WHO: 96593, TLK-10: C81.0 Klasikinė Hodgkin limfoma WHO: 96503, TLK-10: C81.9 Nodulinės
VETERINARINIO VAISTO APRAŠAS 1. VETERINARINIO VAISTO PAVADINIMAS FLORKEM 300 mg/ml injekcinis tirpalas galvijams ir kiaulėms 2. KOKYBINĖ IR KIEKYBINĖ
 VETERINARINIO VAISTO APRAŠAS 1. VETERINARINIO VAISTO PAVADINIMAS FLORKEM 300 mg/ml injekcinis tirpalas galvijams ir kiaulėms 2. KOKYBINĖ IR KIEKYBINĖ SUDĖTIS Kiekviename ml yra: veikliosios medžiagos:
VETERINARINIO VAISTO APRAŠAS 1. VETERINARINIO VAISTO PAVADINIMAS FLORKEM 300 mg/ml injekcinis tirpalas galvijams ir kiaulėms 2. KOKYBINĖ IR KIEKYBINĖ SUDĖTIS Kiekviename ml yra: veikliosios medžiagos:
DANTŲ ĖDUONIS IR PERIODONTO LIGOS Jau daugiau nei 200 metų ColgatePalmolive yra pasaulinis burnos priežiūros lyderis, siekiantis gerinti burnos sveika
 DANTŲ ĖDUONIS IR PERIODONTO LIGOS Jau daugiau nei 200 metų ColgatePalmolive yra pasaulinis burnos priežiūros lyderis, siekiantis gerinti burnos sveikatą visame pasaulyje. Įmonė gamina pastas ir rankinius
DANTŲ ĖDUONIS IR PERIODONTO LIGOS Jau daugiau nei 200 metų ColgatePalmolive yra pasaulinis burnos priežiūros lyderis, siekiantis gerinti burnos sveikatą visame pasaulyje. Įmonė gamina pastas ir rankinius
PRITARTA Alytaus miesto savivaldybės tarybos 2011 m. d. sprendimu Nr. ALYTAUS MIESTO SAVIVALDYBĖS VISUOMENĖS SVEIKATOS STEBĖSENOS METŲ PROGR
 PRITARTA Alytaus miesto savivaldybės tarybos 2011 m. d. sprendimu Nr. ALYTAUS MIESTO SAVIVALDYBĖS VISUOMENĖS SVEIKATOS STEBĖSENOS 2009 2011 METŲ PROGRAMOS 2010 METŲ ATASKAITA I. ĮVADAS Alytaus miesto savivaldybės
PRITARTA Alytaus miesto savivaldybės tarybos 2011 m. d. sprendimu Nr. ALYTAUS MIESTO SAVIVALDYBĖS VISUOMENĖS SVEIKATOS STEBĖSENOS 2009 2011 METŲ PROGRAMOS 2010 METŲ ATASKAITA I. ĮVADAS Alytaus miesto savivaldybės
Projektas
 APSKRITIES ANTIMIKROBINIO ATSPARUMO VALDYMO GRUPĖS VEIKLOS ATASKAITA Apskrities valdymo grupė: KAUNO APSKRITIS Laikotarpis, už kurį teikiama ataskaita: 208 metai Ataskaitą parengė: Kauno departamento Užkrečiamųjų
APSKRITIES ANTIMIKROBINIO ATSPARUMO VALDYMO GRUPĖS VEIKLOS ATASKAITA Apskrities valdymo grupė: KAUNO APSKRITIS Laikotarpis, už kurį teikiama ataskaita: 208 metai Ataskaitą parengė: Kauno departamento Užkrečiamųjų
65 m. amžiaus ir vyresnių asmenų sveikatos netolygumai Lietuvoje
 65 m. amžiaus ir vyresnių asmenų sveikatos netolygumai Lietuvoje Projekto vadovė: dr. Laura Nedzinskienė Atsakinga vykdytoja: Vaida Aguonytė, Jolanta Valentienė Tyrimo dalyvės: dr. Aušra Beržanskytė, Eimantė
65 m. amžiaus ir vyresnių asmenų sveikatos netolygumai Lietuvoje Projekto vadovė: dr. Laura Nedzinskienė Atsakinga vykdytoja: Vaida Aguonytė, Jolanta Valentienė Tyrimo dalyvės: dr. Aušra Beržanskytė, Eimantė
Microsoft PowerPoint - HI diskusijai2010_03_05 [Compatibility Mode]
![Microsoft PowerPoint - HI diskusijai2010_03_05 [Compatibility Mode] Microsoft PowerPoint - HI diskusijai2010_03_05 [Compatibility Mode]](/thumbs/88/116343227.jpg) Vaikų sveikatos stebėsenos vykdymas ir perspektyvos savivaldybėse Neringa Tarvydienė Klaipėdos rajono savivaldybės visuomenės sveikatos biuro direktorė 1 2010-03-05, Vilnius Vaikų sveikatos stebėsenos
Vaikų sveikatos stebėsenos vykdymas ir perspektyvos savivaldybėse Neringa Tarvydienė Klaipėdos rajono savivaldybės visuomenės sveikatos biuro direktorė 1 2010-03-05, Vilnius Vaikų sveikatos stebėsenos
EUROPOS KOMISIJA Briuselis, C(2017) 4679 final KOMISIJOS ĮGYVENDINIMO SPRENDIMAS (ES) / dėl bendros sistemos techninių standa
 EUROPOS KOMISIJA Briuselis, 2017 07 11 C(2017) 4679 final KOMISIJOS ĮGYVENDINIMO SPRENDIMAS (ES) /... 2017 07 11 dėl bendros sistemos techninių standartų ir formatų, kad EURES portale būtų galima susieti
EUROPOS KOMISIJA Briuselis, 2017 07 11 C(2017) 4679 final KOMISIJOS ĮGYVENDINIMO SPRENDIMAS (ES) /... 2017 07 11 dėl bendros sistemos techninių standartų ir formatų, kad EURES portale būtų galima susieti
Ibuprofen Art 31 CMDh agreement Annexes
 II priedas Mokslinės išvados ir pagrindas keisti rinkodaros leidimų sąlygas 355 Mokslinės išvados ir pagrindas keisti rinkodaros leidimų sąlygas Ibuprofenas yra nesteroidinis vaistas nuo uždegimo (NVNU),
II priedas Mokslinės išvados ir pagrindas keisti rinkodaros leidimų sąlygas 355 Mokslinės išvados ir pagrindas keisti rinkodaros leidimų sąlygas Ibuprofenas yra nesteroidinis vaistas nuo uždegimo (NVNU),
DANTŲ ĖDUONIS IR PERIODONTO LIGOS Rekomendacijos bendrosios sveikatos priežiūros specialistams Svarbiausios EFP ir ORCA organizuotos 2016 m. Perio dar
 DANTŲ ĖDUONIS IR PERIODONTO LIGOS Rekomendacijos bendrosios sveikatos priežiūros specialistams Svarbiausios EFP ir ORCA organizuotos 2016 m. Perio darbo grupės žinutės apie dantų ėduonies ir periodonto
DANTŲ ĖDUONIS IR PERIODONTO LIGOS Rekomendacijos bendrosios sveikatos priežiūros specialistams Svarbiausios EFP ir ORCA organizuotos 2016 m. Perio darbo grupės žinutės apie dantų ėduonies ir periodonto
Vorikonazolio koncentracijos stebėsena Roberta Petrauskaitė
 Vorikonazolio koncentracijos stebėsena Roberta Petrauskaitė Planas Ê Vaisto charakteristika Ê Vorikonazolio (VRC) terapinės dozės monitoravimo (TDM) multicentrinis tyrimas, nutrauktas anksčiau nei planuota
Vorikonazolio koncentracijos stebėsena Roberta Petrauskaitė Planas Ê Vaisto charakteristika Ê Vorikonazolio (VRC) terapinės dozės monitoravimo (TDM) multicentrinis tyrimas, nutrauktas anksčiau nei planuota
SIŪLOMO ĮRAŠYTI Į KOMPENSAVIMO SĄRAŠUS VAISTINIO PREPARATO FARMAKOEKONOMINĖS VERTĖS NUSTATYMO PROTOKOLAS (data) Vertinimas pirminis patiksl
 SIŪLOMO ĮRAŠYTI Į KOMPENSAVIMO SĄRAŠUS VAISTINIO PREPARATO FARMAKOEKONOMINĖS VERTĖS NUSTATYMO PROTOKOLAS 2017-11-27 (data) Vertinimas pirminis patikslintas Vilnius (sudarymo vieta) Paskutinio vertinimo
SIŪLOMO ĮRAŠYTI Į KOMPENSAVIMO SĄRAŠUS VAISTINIO PREPARATO FARMAKOEKONOMINĖS VERTĖS NUSTATYMO PROTOKOLAS 2017-11-27 (data) Vertinimas pirminis patikslintas Vilnius (sudarymo vieta) Paskutinio vertinimo
Présentation PowerPoint
 Imigracija ir Darbo migracija ES ir Lietuvoje Audra Sipavičienė TMO, EMN Migracijos svarba pasaulyje 2,9% 2,8% 2,8% 2,9% 3,2% 3,3% 3,4% 3,5% Iš kurių 75+ milijonai arba maždaug 1/3 yra Europoje 153 mln
Imigracija ir Darbo migracija ES ir Lietuvoje Audra Sipavičienė TMO, EMN Migracijos svarba pasaulyje 2,9% 2,8% 2,8% 2,9% 3,2% 3,3% 3,4% 3,5% Iš kurių 75+ milijonai arba maždaug 1/3 yra Europoje 153 mln
STEPS projektas ir jo aktualumas Lietuvoje
 STEPS projektas ir jo aktualumas Dr. Rima Vaitkienė Sveikatos apsaugos ministerijos ES reikalų ir tarptautinių ryšių skyriaus vedėjo pavaduotoja STEPS projektas STEPS: angl. Strengthening Engagement in
STEPS projektas ir jo aktualumas Dr. Rima Vaitkienė Sveikatos apsaugos ministerijos ES reikalų ir tarptautinių ryšių skyriaus vedėjo pavaduotoja STEPS projektas STEPS: angl. Strengthening Engagement in
Dalyvavusių skaičius (pagal tyrimo metus)
 INTERVENCIJOS, SIEKIANT MAŽINTI PSICHOAKTYVIŲ MEDŽIAGŲ VARTOJIMĄ TARP JAUNIMO Klaipėda, 2015 TEMOS AKTUALUMAS Nesaikingas tabako, alkoholio ir kitų psichoaktyvių medžiagų vartojimas kelia didelį susirūpinimą
INTERVENCIJOS, SIEKIANT MAŽINTI PSICHOAKTYVIŲ MEDŽIAGŲ VARTOJIMĄ TARP JAUNIMO Klaipėda, 2015 TEMOS AKTUALUMAS Nesaikingas tabako, alkoholio ir kitų psichoaktyvių medžiagų vartojimas kelia didelį susirūpinimą
TURTO VALDYMO IR ŪKIO DEPARTAMENTAS PRIE LIETUVOS RESPUBLIKOS VIDAUS REIKALŲ MINISTERIJOS PERSONALO FORMAVIMO, VALDYMO IR ADMINISTRAVIMO VEIKLOS SRITI
 TURTO VALDYMO IR ŪKIO DEPARTAMENTAS PRIE LIETUVOS RESPUBLIKOS VIDAUS REIKALŲ MINISTERIJOS PERSONALO FORMAVIMO, VALDYMO IR ADMINISTRAVIMO VEIKLOS SRITIES VERTINIMO APRAŠYMAS 2018 m. rugsėjo 25 d. Turto
TURTO VALDYMO IR ŪKIO DEPARTAMENTAS PRIE LIETUVOS RESPUBLIKOS VIDAUS REIKALŲ MINISTERIJOS PERSONALO FORMAVIMO, VALDYMO IR ADMINISTRAVIMO VEIKLOS SRITIES VERTINIMO APRAŠYMAS 2018 m. rugsėjo 25 d. Turto
Alkoholis, jo poveikis paauglio organizmui ir elgesiui, vartojimo priežastys ir pasekmės Justinos Jurkšaitės (I e) nuotr.
 Alkoholis, jo poveikis paauglio organizmui ir elgesiui, vartojimo priežastys ir pasekmės Justinos Jurkšaitės (I e) nuotr. Paauglystė svarbus gyvenimo laikotarpis, kuris tęsiasi nuo fizinio lytinio brendimo
Alkoholis, jo poveikis paauglio organizmui ir elgesiui, vartojimo priežastys ir pasekmės Justinos Jurkšaitės (I e) nuotr. Paauglystė svarbus gyvenimo laikotarpis, kuris tęsiasi nuo fizinio lytinio brendimo
PATVIRTINTA Lietuvos banko valdybos 2015 m. sausio 29 d. nutarimu Nr (Lietuvos banko valdybos 2018 m. spalio 30 d. nutarimo Nr redakcij
 PATVIRTINTA Lietuvos banko valdybos 2015 m. sausio 29 d. nutarimu Nr. 03-10 (Lietuvos banko valdybos 2018 m. spalio 30 d. nutarimo Nr. 03-202 redakcija) PRIĖMIMO Į TARNYBĄ LIETUVOS BANKE TVARKOS APRAŠAS
PATVIRTINTA Lietuvos banko valdybos 2015 m. sausio 29 d. nutarimu Nr. 03-10 (Lietuvos banko valdybos 2018 m. spalio 30 d. nutarimo Nr. 03-202 redakcija) PRIĖMIMO Į TARNYBĄ LIETUVOS BANKE TVARKOS APRAŠAS
Antros kartos TKI lūkesčiai ir STOP tyrimai
 Antros kartos TKI lūkesčiai ir STOP tyrimai: LML taps išgydoma? Neringa Gailiūtė 2012.07.21 LML išgydoma? Pacientui: viltis, kad galima išgyti nėra šalutinio vaistų poveikio Visuomenei: gydymo kaina Pasveikimas
Antros kartos TKI lūkesčiai ir STOP tyrimai: LML taps išgydoma? Neringa Gailiūtė 2012.07.21 LML išgydoma? Pacientui: viltis, kad galima išgyti nėra šalutinio vaistų poveikio Visuomenei: gydymo kaina Pasveikimas
Microsoft Word - METODINES_raupu.doc
 TERITORIJOS APSAUGOS NUO RAUPŲ ĮVEŽIMO IR IŠPLITIMO TIPINöS TVARKOS APRAŠAS (metodin s rekomendacijos) BENDROSIOS NUOSTATOS 1. Teritorijos apsaugos nuo raupų įvežimo ir išplitimo tipin s tvarkos aprašas
TERITORIJOS APSAUGOS NUO RAUPŲ ĮVEŽIMO IR IŠPLITIMO TIPINöS TVARKOS APRAŠAS (metodin s rekomendacijos) BENDROSIOS NUOSTATOS 1. Teritorijos apsaugos nuo raupų įvežimo ir išplitimo tipin s tvarkos aprašas
PowerPoint Presentation
 KAIP FORMUOJAMASIS VERTINIMAS PADEDA SIEKTI INDIVIDUALIOS PAŽANGOS: REFLEKSIJA KOKYBĖS SIEKIANČIŲ MOKYKLŲ KLUBO KONFERENCIJA MOKINIŲ UGDYMO(SI) PASIEKIMAI. SAMPRATA IR SKATINIMO GALIMYBĖS Doc. dr. Viktorija
KAIP FORMUOJAMASIS VERTINIMAS PADEDA SIEKTI INDIVIDUALIOS PAŽANGOS: REFLEKSIJA KOKYBĖS SIEKIANČIŲ MOKYKLŲ KLUBO KONFERENCIJA MOKINIŲ UGDYMO(SI) PASIEKIMAI. SAMPRATA IR SKATINIMO GALIMYBĖS Doc. dr. Viktorija
Sausio mėnesio rinkos apžvalga metai elektros energijos rinkoje pasižymėjo kainų kritimu: Elektros perdavimo jungčių pajėgumas ir efek
 Sausio mėnesio rinkos apžvalga 2015 02 24 2015 metai elektros energijos rinkoje pasižymėjo kainų kritimu: Elektros perdavimo jungčių pajėgumas ir efektyvus Rygos šiluminių elektrinių veikimas sausį Nord
Sausio mėnesio rinkos apžvalga 2015 02 24 2015 metai elektros energijos rinkoje pasižymėjo kainų kritimu: Elektros perdavimo jungčių pajėgumas ir efektyvus Rygos šiluminių elektrinių veikimas sausį Nord
LIETUVOS RESPUBLIKOS SVEIKATOS APSAUGOS MINISTRO
 Forma patvirtinta Lietuvos Respublikos sveikatos apsaugos ministro 2002 m. balandžio 5 d. įsakymu Nr. 159 (Lietuvos Respublikos sveikatos apsaugos ministro 2015 m. kovo 27 d įsakymo Nr. V-445 redakcija)
Forma patvirtinta Lietuvos Respublikos sveikatos apsaugos ministro 2002 m. balandžio 5 d. įsakymu Nr. 159 (Lietuvos Respublikos sveikatos apsaugos ministro 2015 m. kovo 27 d įsakymo Nr. V-445 redakcija)
Norovirusinė infekcija, naujienos Roberta Petrauskaitė
 Norovirusinė infekcija, naujienos Roberta Petrauskaitė Noro viruso sukeltas gastroenteritas (susijęs su Norvalko (Norwalk) virusu) Viena iš pagrindinių infekcinių viduriavimų priežasčių, plintanti per
Norovirusinė infekcija, naujienos Roberta Petrauskaitė Noro viruso sukeltas gastroenteritas (susijęs su Norvalko (Norwalk) virusu) Viena iš pagrindinių infekcinių viduriavimų priežasčių, plintanti per
Viešoji konsultacija dėl dezinformacijos apie Lietuvą sklaidos mažinimo užsienyje 2019 m. kovo mėn., Vilnius KONTEKSTAS KONSULTACIJOS TIKSLAS VIEŠOSIO
 Viešoji konsultacija dėl dezinformacijos apie Lietuvą sklaidos mažinimo užsienyje 2019 m. kovo mėn., Vilnius KONTEKSTAS TIKSLAS VIEŠOSIOS POLITIKOS PRIORITETAS Lietuvai priešiškos šalys jau ilgą laiką
Viešoji konsultacija dėl dezinformacijos apie Lietuvą sklaidos mažinimo užsienyje 2019 m. kovo mėn., Vilnius KONTEKSTAS TIKSLAS VIEŠOSIOS POLITIKOS PRIORITETAS Lietuvai priešiškos šalys jau ilgą laiką
Co-funded by the Health Programme of the European Union Švirkščiamuosius narkotikus vartojančių asmenų TUBERKULIOZĖS prevencijos REKOMENDACIJOS, skirt
 Co-funded by the Health Programme of the European Union Švirkščiamuosius narkotikus vartojančių asmenų TUBERKULIOZĖS prevencijos REKOMENDACIJOS, skirtos bendruomeninėms organizacijoms Švirkščiamuosius
Co-funded by the Health Programme of the European Union Švirkščiamuosius narkotikus vartojančių asmenų TUBERKULIOZĖS prevencijos REKOMENDACIJOS, skirtos bendruomeninėms organizacijoms Švirkščiamuosius
TURINYS
 Finansuojama iš Europos socialinio fondo. Projekto vykdytojas: Lietuvos vaikų pulmonologų draugija LIETUVOS VAIKŲ PULMONOLOGŲ DRAUGIJA VILNIAUS UNIVERSITETAS LIETUVOS SVEIKATOS MOKSLŲ UNIVERSITETAS LIETUVOS
Finansuojama iš Europos socialinio fondo. Projekto vykdytojas: Lietuvos vaikų pulmonologų draugija LIETUVOS VAIKŲ PULMONOLOGŲ DRAUGIJA VILNIAUS UNIVERSITETAS LIETUVOS SVEIKATOS MOKSLŲ UNIVERSITETAS LIETUVOS
[Version 7
 VETERINARINIO VAISTO APRAŠAS 1. VETERINARINIO VAISTO PAVADINIMAS POULVAC MAREK CVI, šaldyta suspensija (skirta naudoti su Poulvac Marek Diluent skiedikliu) 2. KOKYBINĖ IR KIEKYBINĖ SUDĖTIS Vienoje 0,2
VETERINARINIO VAISTO APRAŠAS 1. VETERINARINIO VAISTO PAVADINIMAS POULVAC MAREK CVI, šaldyta suspensija (skirta naudoti su Poulvac Marek Diluent skiedikliu) 2. KOKYBINĖ IR KIEKYBINĖ SUDĖTIS Vienoje 0,2
PATVIRTINTA Šiaulių rajono savivaldybės tarybos 2017 m. vasario d. sprendimu Nr. T- ŠIAULIŲ RAJONO SAVIVALDYBĖS VISUOMENĖS SVEIKATOS BIURO DIREKTORIAU
 PATVIRTINTA Šiaulių rajono savivaldybės tarybos 2017 m. vasario d. sprendimu Nr. T- ŠIAULIŲ RAJONO SAVIVALDYBĖS VISUOMENĖS SVEIKATOS BIURO DIREKTORIAUS 2016 M. ATASKAITA Ataskaitą parengė Edvinas Pečiukėnas
PATVIRTINTA Šiaulių rajono savivaldybės tarybos 2017 m. vasario d. sprendimu Nr. T- ŠIAULIŲ RAJONO SAVIVALDYBĖS VISUOMENĖS SVEIKATOS BIURO DIREKTORIAUS 2016 M. ATASKAITA Ataskaitą parengė Edvinas Pečiukėnas
Individualus projektas Programa TE-PM, TE-PS, TE-SL, TEstream 4, TEstream 6, TEstream 8, TEstreamOBD 4, TEstreamOBD 6, TEstreamOBD 8 sistemų naudotoja
 Individualus projektas Programa TE-PM, TE-PS, TE-SL, TEstream 4, TEstream 6, TEstream 8, TEstreamOBD 4, TEstreamOBD 6, TEstreamOBD 8 sistemų naudotojams Alternatyvus valdymo pultas telefone ViPGaS programos
Individualus projektas Programa TE-PM, TE-PS, TE-SL, TEstream 4, TEstream 6, TEstream 8, TEstreamOBD 4, TEstreamOBD 6, TEstreamOBD 8 sistemų naudotojams Alternatyvus valdymo pultas telefone ViPGaS programos
Microsoft Word - Document1
 PAKUOTĖS LAPELIS: INFORMACIJA VARTOTOJUI Betadine 100 mg/ml odos tirpalas Joduotas povidonas Atidžiai perskaitykite visą šį lapelį, nes jame pateikiama Jums svarbi informacija. Betadine galima įsigyti
PAKUOTĖS LAPELIS: INFORMACIJA VARTOTOJUI Betadine 100 mg/ml odos tirpalas Joduotas povidonas Atidžiai perskaitykite visą šį lapelį, nes jame pateikiama Jums svarbi informacija. Betadine galima įsigyti
Užduotys 12 klasei 2017 m. geografijos olimpiada Dalyvio kodas Surinkti taškai
 Užduotys 12 klasei 2017 m. geografijos olimpiada Dalyvio kodas Surinkti taškai 1. Kurios tautos gyvenamoji teritorija parodyta žemėlapyje? A berberų B fulbių C hausų D tuaregų 3. Ką vaizduoja šis neįprastu
Užduotys 12 klasei 2017 m. geografijos olimpiada Dalyvio kodas Surinkti taškai 1. Kurios tautos gyvenamoji teritorija parodyta žemėlapyje? A berberų B fulbių C hausų D tuaregų 3. Ką vaizduoja šis neįprastu
red-BK_moduliai_ _Po redaktores
 P R O J E K T A S VP1-2.2-ŠMM-04-V-01-001 MOKYMOSI KRYPTIES PASIRINKIMO GALIMYBIŲ DIDINIMAS 14-19 METŲ MOKINIAMS, II ETAPAS: GILESNIS MOKYMOSI DIFERENCIJAVIMAS IR INDIVIDUALIZAVIMAS, SIEKIANT UGDYMO KOKYBĖS,
P R O J E K T A S VP1-2.2-ŠMM-04-V-01-001 MOKYMOSI KRYPTIES PASIRINKIMO GALIMYBIŲ DIDINIMAS 14-19 METŲ MOKINIAMS, II ETAPAS: GILESNIS MOKYMOSI DIFERENCIJAVIMAS IR INDIVIDUALIZAVIMAS, SIEKIANT UGDYMO KOKYBĖS,
Microsoft Word - pavadinimas _2_.doc
 UŽKREČIAMŲJŲ LIGŲ PROFILAKTIKOS IR KONTROLöS CENTRAS VILNIAUS UNIVERSITETO MEDICINOS FAKULTETO INFEKCINIŲ LIGŲ DERMATOVENEROLOGIJOS IR MIKROBIOLOGIJOS KLINIKA TERITORIJOS APSAUGOS NUO RAUPŲ ĮVEŽIMO IR
UŽKREČIAMŲJŲ LIGŲ PROFILAKTIKOS IR KONTROLöS CENTRAS VILNIAUS UNIVERSITETO MEDICINOS FAKULTETO INFEKCINIŲ LIGŲ DERMATOVENEROLOGIJOS IR MIKROBIOLOGIJOS KLINIKA TERITORIJOS APSAUGOS NUO RAUPŲ ĮVEŽIMO IR
Microsoft Word - Porcilis PRRS
 I PRIEDAS VETERINARINIO VAISTO APRAŠAS 1 1. VETERINARINIO VAISTO PAVADINIMAS Porcilis PRRS liofilizatas ir skiediklis injekcinei suspensijai kiaulėms 2. KOKYBINĖ IR KIEKYBINĖ SUDĖTIS Vienoje 2 ml (švirkšti
I PRIEDAS VETERINARINIO VAISTO APRAŠAS 1 1. VETERINARINIO VAISTO PAVADINIMAS Porcilis PRRS liofilizatas ir skiediklis injekcinei suspensijai kiaulėms 2. KOKYBINĖ IR KIEKYBINĖ SUDĖTIS Vienoje 2 ml (švirkšti
VILNIUS, 2017
 VILNIUS, 2017 Higienos instituto Sveikatos informacijos centras Didžioji g. 22, LT 01128 Vilnius Tel. (8 5) 277 3302 Faksas (8 5) 262 4663 www.hi.lt Leidinį parengė: Žilvinė Našlėnė, zilvine.naslene@hi.lt
VILNIUS, 2017 Higienos instituto Sveikatos informacijos centras Didžioji g. 22, LT 01128 Vilnius Tel. (8 5) 277 3302 Faksas (8 5) 262 4663 www.hi.lt Leidinį parengė: Žilvinė Našlėnė, zilvine.naslene@hi.lt
HIGIENOS INSTITUTAS HOSPITALINIŲ INFEKCIJŲ VALDYMO SVEIKATOS PRIEŽIŪROS ĮSTAIGOSE M. PROGRAMA HOSPITALINIŲ INFEKCIJŲ EPIDEMIOLOGINĖ PRIEŽIŪR
 HIGIENOS INSTITUTAS HOSPITALINIŲ INFEKCIJŲ VALDYMO SVEIKATOS PRIEŽIŪROS ĮSTAIGOSE 2007 2011 M. PROGRAMA HOSPITALINIŲ INFEKCIJŲ EPIDEMIOLOGINĖ PRIEŽIŪRA REANIMACIJOS - INTENSYVIOS TERAPIJOS SKYRIUOSE 2008
HIGIENOS INSTITUTAS HOSPITALINIŲ INFEKCIJŲ VALDYMO SVEIKATOS PRIEŽIŪROS ĮSTAIGOSE 2007 2011 M. PROGRAMA HOSPITALINIŲ INFEKCIJŲ EPIDEMIOLOGINĖ PRIEŽIŪRA REANIMACIJOS - INTENSYVIOS TERAPIJOS SKYRIUOSE 2008
PATVIRTINTA Mykolo Romerio universiteto Rektoriaus 2014 m. birželio 2 d. įsakymu Nr.1I-291 MYKOLO ROMERIO UNIVERSITETO LAIKINOSIOS STUDIJŲ REZULTATŲ Į
 PATVIRTINTA Mykolo Romerio universiteto Rektoriaus 2014 m. birželio 2 d. įsakymu Nr.1I-291 MYKOLO ROMERIO UNIVERSITETO LAIKINOSIOS STUDIJŲ REZULTATŲ ĮVERTINIMO PATIKROS TVARKA I. BENDROSIOS NUOSTATOS 1.
PATVIRTINTA Mykolo Romerio universiteto Rektoriaus 2014 m. birželio 2 d. įsakymu Nr.1I-291 MYKOLO ROMERIO UNIVERSITETO LAIKINOSIOS STUDIJŲ REZULTATŲ ĮVERTINIMO PATIKROS TVARKA I. BENDROSIOS NUOSTATOS 1.
RR-GSM_IM_LT_110125
 Retransliatorius RR-GSM Įrengimo instrukcija Draugystės g. 17, LT-51229 Kaunas El. p.: info@trikdis.lt www.trikdis.lt Retransliatorius RR-GSM perduoda priimtus pranešimus į centralizuoto stebėjimo pultą
Retransliatorius RR-GSM Įrengimo instrukcija Draugystės g. 17, LT-51229 Kaunas El. p.: info@trikdis.lt www.trikdis.lt Retransliatorius RR-GSM perduoda priimtus pranešimus į centralizuoto stebėjimo pultą
VILNIAUS APSKRITIES TARPINSTITUCINĖS ANTIMIKROBINIO ATSPARUMO VALDYMO GRUPĖS 2018 M. VEIKLOS ATASKAITA Nr. ( E) 2- Vilnius Priemon
 VILNIAUS APSKRITIES TARPINSTITUCINĖS ANTIMIKROBINIO ATSPARUMO VALDYMO GRUPĖS 2018 M. VEIKLOS ATASKAITA 2019-02- Nr. (10-13 16.1.1E) 2- Vilnius Priemonės įvykdymo data Priemonės pobūdis ir pavadinimas Priemonės
VILNIAUS APSKRITIES TARPINSTITUCINĖS ANTIMIKROBINIO ATSPARUMO VALDYMO GRUPĖS 2018 M. VEIKLOS ATASKAITA 2019-02- Nr. (10-13 16.1.1E) 2- Vilnius Priemonės įvykdymo data Priemonės pobūdis ir pavadinimas Priemonės
Privalomai pasirenkamas istorijos modulis istorija aplink mus I dalis _suredaguotas_
 P R O J E K T A S VP1-2.2-ŠMM-04-V-01-001 MOKYMOSI KRYPTIES PASIRINKIMO GALIMYBIŲ DIDINIMAS 14-19 METŲ MOKINIAMS, II ETAPAS: GILESNIS MOKYMOSI DIFERENCIJAVIMAS IR INDIVIDUALIZAVIMAS, SIEKIANT UGDYMO KOKYBĖS,
P R O J E K T A S VP1-2.2-ŠMM-04-V-01-001 MOKYMOSI KRYPTIES PASIRINKIMO GALIMYBIŲ DIDINIMAS 14-19 METŲ MOKINIAMS, II ETAPAS: GILESNIS MOKYMOSI DIFERENCIJAVIMAS IR INDIVIDUALIZAVIMAS, SIEKIANT UGDYMO KOKYBĖS,
PATVIRTINTA VšĮ Alytaus miesto socialinių paslaugų centro direktoriaus 2017 m. lapkričio 6 d. įsakymu Nr. V-88 VŠĮ ALYTAUS MIESTO SOCIALINIŲ PASLAUGŲ
 PATVIRTINTA VšĮ Alytaus miesto socialinių paslaugų centro direktoriaus 2017 m. lapkričio 6 d. įsakymu Nr. V-88 VŠĮ ALYTAUS MIESTO SOCIALINIŲ PASLAUGŲ CENTRO LYGIŲ GALIMYBIŲ POLITIKA IR JOS ĮGYVENDINIMO
PATVIRTINTA VšĮ Alytaus miesto socialinių paslaugų centro direktoriaus 2017 m. lapkričio 6 d. įsakymu Nr. V-88 VŠĮ ALYTAUS MIESTO SOCIALINIŲ PASLAUGŲ CENTRO LYGIŲ GALIMYBIŲ POLITIKA IR JOS ĮGYVENDINIMO
Kai kurie gyvūnai tokie primityvūs, kad jiems kraujotakos nereikia. Pvz., hidros kūno sandara tokia, kad visas ląsteles skalauja vanduo gaunamas O 2,
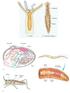 Kai kurie gyvūnai tokie primityvūs, kad jiems kraujotakos nereikia. Pvz., hidros kūno sandara tokia, kad visas ląsteles skalauja vanduo gaunamas O 2, visos jos turi priėjimą prie virškinamosios ertmės,
Kai kurie gyvūnai tokie primityvūs, kad jiems kraujotakos nereikia. Pvz., hidros kūno sandara tokia, kad visas ląsteles skalauja vanduo gaunamas O 2, visos jos turi priėjimą prie virškinamosios ertmės,
2016 M. KLINIKINIO KODAVIMO STEBĖSENOS REZULTATŲ VERTINIMO ATASKAITA
 VALSTYBINĖ LIGONIŲ KASA PRIE SVEIKATOS APSAUGOS MINISTERIJOS 2016 M. KLINIKINIO KODAVIMO STEBĖSENOS REZULTATŲ VERTINIMO ATASKAITA 2017 m. kovo 27 d. Nr. 7K-427 Vilnius Turinys 1. Įvadas... 1 2. Bendrųjų
VALSTYBINĖ LIGONIŲ KASA PRIE SVEIKATOS APSAUGOS MINISTERIJOS 2016 M. KLINIKINIO KODAVIMO STEBĖSENOS REZULTATŲ VERTINIMO ATASKAITA 2017 m. kovo 27 d. Nr. 7K-427 Vilnius Turinys 1. Įvadas... 1 2. Bendrųjų
MAITINKIS SVEIKAI, SUMAŽINK GRĖSMĘ SUSIRGTI VĖŽIU
 MAITINKIS SVEIKAI, SUMAŽINK GRĖSMĘ SUSIRGTI VĖŽIU Mūsų mityba gali padidinti vėžio išsivystymo grėsmę. Patikimų mokslinių įrodymų duomenimis apie 30 proc. vėžio atvejų išsivysčiusiose šalyse ir 20 proc.
MAITINKIS SVEIKAI, SUMAŽINK GRĖSMĘ SUSIRGTI VĖŽIU Mūsų mityba gali padidinti vėžio išsivystymo grėsmę. Patikimų mokslinių įrodymų duomenimis apie 30 proc. vėžio atvejų išsivysčiusiose šalyse ir 20 proc.
Rotarix, INN-Rotavirus vaccine, live
 I PRIEDAS PREPARATO CHARAKTERISTIKŲ SANTRAUKA 1 1. VAISTINIO PREPARATO PAVADINIMAS Rotarix milteliai ir tirpiklis geriamajai suspensijai Vakcina nuo rotaviruso (gyvoji) 2. KOKYBINĖ IR KIEKYBINĖ SUDĖTIS
I PRIEDAS PREPARATO CHARAKTERISTIKŲ SANTRAUKA 1 1. VAISTINIO PREPARATO PAVADINIMAS Rotarix milteliai ir tirpiklis geriamajai suspensijai Vakcina nuo rotaviruso (gyvoji) 2. KOKYBINĖ IR KIEKYBINĖ SUDĖTIS
SANTE/11059/2016-EN Rev. 2
 Europos Sąjungos Taryba Briuselis, 2017 m. rugpjūčio 17 d. (OR. en) 11651/17 AGRILEG 150 DENLEG 63 PRIDEDAMAS PRANEŠIMAS nuo: Europos Komisijos gavimo data: 2017 m. rugpjūčio 24 d. kam: Komisijos dok.
Europos Sąjungos Taryba Briuselis, 2017 m. rugpjūčio 17 d. (OR. en) 11651/17 AGRILEG 150 DENLEG 63 PRIDEDAMAS PRANEŠIMAS nuo: Europos Komisijos gavimo data: 2017 m. rugpjūčio 24 d. kam: Komisijos dok.
TVIEŠOSIOS
 VIEŠOJI ĮSTAIGA PRIENŲ LIGONINĖ 2015 M. VEIKLOS ATASKAITA VšĮ Prienų ligoninės direktorė Jūratė Milaknienė PRIENAI 2016 LIGONINĖS MISIJA Teikti prieinamas, mokslu ir pažangiausiomis technologijomis pagrįstas,
VIEŠOJI ĮSTAIGA PRIENŲ LIGONINĖ 2015 M. VEIKLOS ATASKAITA VšĮ Prienų ligoninės direktorė Jūratė Milaknienė PRIENAI 2016 LIGONINĖS MISIJA Teikti prieinamas, mokslu ir pažangiausiomis technologijomis pagrįstas,
PSICHOLOGINĖS TRAUMOS IR SAVIŽUDYBĖS SOCIOKULTŪRINIŲ POKYČIŲ KONTEKSTE
 GYVENIMAS PO LŪŽIO Danutė Gailienė Vilniaus universitetas ISTORINIAI LŪŽIAI 1. 1940 m. Lietuva prarado nepriklausomybę 2. 1990 m. Lietuva atkūrė nepriklausomybę 3. Istoriniai lūžiai sukėlė kultūrines traumas
GYVENIMAS PO LŪŽIO Danutė Gailienė Vilniaus universitetas ISTORINIAI LŪŽIAI 1. 1940 m. Lietuva prarado nepriklausomybę 2. 1990 m. Lietuva atkūrė nepriklausomybę 3. Istoriniai lūžiai sukėlė kultūrines traumas
Pasiutligës prevencija Lietuvoje
 PNEUMOKOKINöS PNEUMONIJOS KLINIKOS, DIAGNOSTIKOS, GYDYMO, PROGNOZöS IR PROFILAKTIKOS METODINöS REKOMENDACIJOS I. BENDROSIOS NUOSTATOS 1. Pneumokokin infekcija grup ligų, kurias sukelia pneumonijos streptokokas
PNEUMOKOKINöS PNEUMONIJOS KLINIKOS, DIAGNOSTIKOS, GYDYMO, PROGNOZöS IR PROFILAKTIKOS METODINöS REKOMENDACIJOS I. BENDROSIOS NUOSTATOS 1. Pneumokokin infekcija grup ligų, kurias sukelia pneumonijos streptokokas
Palaikomojo gydymo opioidų antagonistu revia tikslai
 PRIKLAUSOMYBĖS NUO OPIOIDŲ GYDYMO METADONU METODIKA Projektas 2009.02.25 I. BENDRA DALIS 1. Ligos pavadinimas ir TLK-10 kodas pagal Tarptautinę statistinę ligų ir sveikatos problemų klasifikaciją 1.1.
PRIKLAUSOMYBĖS NUO OPIOIDŲ GYDYMO METADONU METODIKA Projektas 2009.02.25 I. BENDRA DALIS 1. Ligos pavadinimas ir TLK-10 kodas pagal Tarptautinę statistinę ligų ir sveikatos problemų klasifikaciją 1.1.
PowerPoint Presentation
 IBM-Lietuvos tyrimų centras bendras projektas Lietuvos mokslo ir žinių visuomenei Tomas Deržanauskas UAB Lietuvos tyrimų centras 2011 m. spalio 18d. Vilnius IBM tarp pasaulinių inovatorių lyderių IBM jungia
IBM-Lietuvos tyrimų centras bendras projektas Lietuvos mokslo ir žinių visuomenei Tomas Deržanauskas UAB Lietuvos tyrimų centras 2011 m. spalio 18d. Vilnius IBM tarp pasaulinių inovatorių lyderių IBM jungia
Microsoft Word - RVI profilaktikos rekomendacijos_2012_01_20
 UŽKREČIAMŲJŲ LIGŲ IR AIDS CENTRAS ROTAVIRUSINöS INFEKCIJOS PROFILAKTIKA IKIMOKYKLINIO UGDYMO ĮSTAIGOSE METODINöS REKOMENDACIJOS Vilnius 2011 2 Rotavirusin s infekcijos profilaktikos ikimokyklinio ugdymo
UŽKREČIAMŲJŲ LIGŲ IR AIDS CENTRAS ROTAVIRUSINöS INFEKCIJOS PROFILAKTIKA IKIMOKYKLINIO UGDYMO ĮSTAIGOSE METODINöS REKOMENDACIJOS Vilnius 2011 2 Rotavirusin s infekcijos profilaktikos ikimokyklinio ugdymo
